Nová metoda endovaskulární výplně výdutě aorty abdominální (endovascular aneurysm sealing − EVAS)
A novel method of endovascular aneurysm sealing (EVAS) in patients with abdominal aortic aneurysm
Introduction:
Endovascular stent graft therapy of abdominal aortic aneurysms is sometimes complicated due to unusual anatomy of the aorta and adjacent arterial regions, an irregular or short proximal neck, numerous patent branches originating from the aneurysm, or tortuous iliac arteries. Endovascular aneurysm sealing is a new method designed to overcome certain limitations of current stent grafts.
Method:
At the Department of Vascular Surgery of Na Homolce Hospital, we implanted 51 stent grafts in the subrenal aorta and iliac arteries. Most of them were regular bifurcated stent grafts. Two patients were treated with the new Nellix stent graft, in one case due to a short subrenal neck of only 13 mm, and due to a considerably conical neck in the second case.
Results:
The post-operative course was uneventful in both patients and they were discharged on the 5th postoperative day. CT angiography after six weeks proved that the stent graft had sealed well. The polymer filled the aortic lumen completely.
Conclusion:
This new method of endovascular aneurysm sealing (EVAS) of abdominal aortic aneurysm makes it possible to treat patients whose anatomy would normally require technically complex and more expensive endovascular methods. We aim to follow long-term results of the method in larger patient cohorts.
Key words:
abdominal aortic aneurysm − stent grafts − endoleak
Authors:
P. Šedivý 1; H. Přindišová 2; K. El Samman 1
Authors‘ workplace:
Oddělení cévní chirurgie, Nemocnice Na Homolce, Praha, primář: prof. MUDr. P. Štádler, Ph. D.
1; Oddělení radiodiagnostiky, Nemocnice Na Homolce, Praha, primář: prof. MUDr. J. Vymazal, DrSc.
2
Published in:
Rozhl. Chir., 2015, roč. 94, č. 6, s. 238-241.
Category:
Original articles
Overview
Úvod:
Léčení výdutě aorty abdominální pomocí endovaskulární implantace stentgraftu je někdy komplikované nebo nemožné z důvodu nevhodné anatomické konfigurace výdutě a přilehlých úseků aorty. Příčinou obtíží bývá nevhodný proximální krček, průchodné větve ústící do vaku výdutě nebo výrazně vinuté přístupové pánevní tepny. Metoda endovaskulární výplně aortální výdutě je nový pracovní postup, jehož cílem je překonat některé nedostatky současných stentgraftů.
Metoda:
V roce 2014 jsme na Oddělení cévní chirurgie Nemocnice Na Homolce zavedli 51 stentgraftů do subrenální aorty a pánevních tepen. Většinou se jednalo o bifurkační stentgrafty klasické konstrukce. U dvou nemocných jsme použili nový stentgraft Nellix, v jednom případě pro krátký subrenální krček 13 mm, ve druhém pro výrazně kónický tvar krčku.
Výsledky:
Pooperační průběh byl u obou pacientů bez rušivých příhod a byli propuštěni do ambulantní péče 5. pooperační den. Kontrolní CT angiografie po šesti týdnech prokázala dobré těsnění SG a polymerem kompletně vyplněný vak výdutě.
Závěr:
Nová metoda endovaskulární výplně výdutě aorty abdominální (endovascular aneurysm sealing – EVAS) umožní léčit pacienty, u kterých by anatomická situace vedla k technicky obtížným a finančně náročným endovaskulárním postupům. Její dlouhodobé výsledky bude možné sledovat teprve na větších souborech pacientů.
Klíčová slova:
aneuryzma aorty abdominální – stentgraft − endoleak
Úvod
Endovaskulární léčba výdutě abdominální aorty pomocí implantace stentgraftu (EVAR) se během více než dvaceti let od svého vzniku stala ve vaskulárních centrech všeobecně dostupnou, vyvinuly se specializované pomůcky a postupy k řešení složitějších anatomických situací, k perkutánnímu zavádění a k ošetření větví nebo krátkých krčků.
Přesto jsou situace, které EVAR komplikují nebo znemožňují z důvodu nevhodné anatomické konfigurace výdutě a přilehlých úseků aorty. Jedná se hlavně o tyto tři skupiny problémů: nevhodný proximální krček, průchodné větve ústící do vaku výdutě a výrazně vinuté přístupové pánevní tepny [1]. Proximální krček angulovaný nebo kónický, krátký nebo ve tvaru přesýpacích hodin, znemožňuje bezpečné kotvení klasických stentgraftů (SG), které ke spolehlivému utěsnění a zabránění proximálnímu endoleaku (EL) I. typu potřebují délku zdravého úseku aorty subrenálně alespoň 15−20 mm. V případě kratších krčků je možné použít stentgraft s fenestrovanou nebo větvenou proximální částí, která umožní přítok krve do větví viscerálního segmentu. U těchto typů SG se ve vyšším počtu (až ve 30 %) objevuje EL nebo dochází k uzávěrům a zalamování bočních větví [2].
Pro riziko vzniku endoleaku je nutné pacienty v pravidelných intervalech sledovat CT angiografií nebo sonograficky [3]. Endoleak I. typu je v současné době při znalosti technického omezení metody výjimečný. Typ II se vyskytuje ve frekvenci 15−30 %, ale obvykle nevadí, protože nedochází k přenosu většího tlaku do vaku, a ten se buď zmenšuje, nebo alespoň neroste [4,5]. Pokud se endoleak udrží, může dojít ke zvětšování vaku, uvolnění a migraci SG z krčku nebo k pozdní ruptuře vaku. Riziko potřeby reintervencí a rehospitalizací vyžaduje celoživotní sledování, které je spojeno s dodatečnými náklady. Podle posledních studií potřebuje sekundární intervenci každý 8. pacient s implantovaným SG, přičemž 66 % z těchto reintervencí je kvůli endoleaku [6,7].
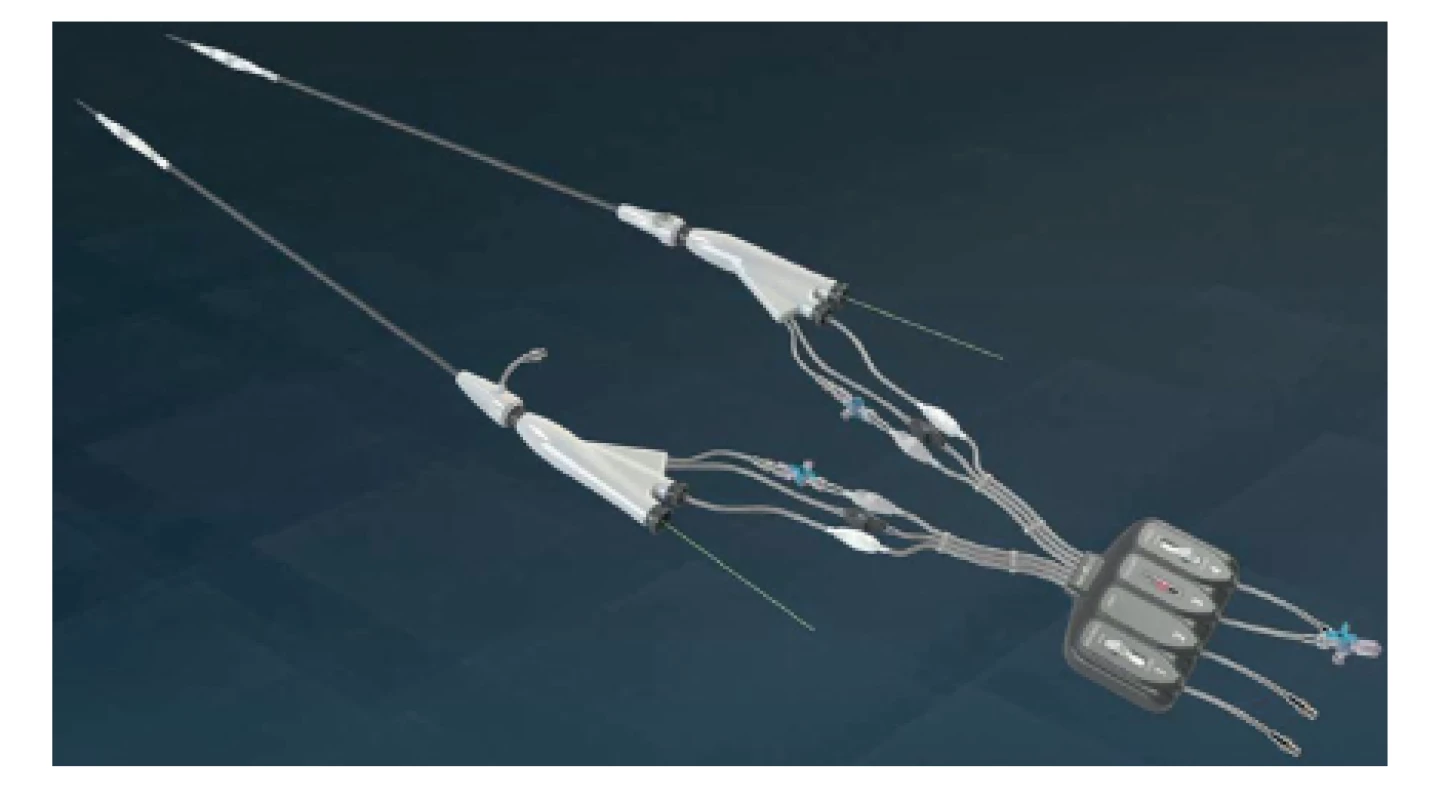
EVAS je nová technologie, jejímž cílem je vyplnit celý vak aortální výdutě [8]. Pod obchodním jménem Nellix system (Endologix Inc., CA, USA) je od roku 2014 certifikována pro použití v České republice. Systém oproti všem předchozím typům SG není modulární, sestává ze dvou tubulárních balon-expandibilních PTFE krytých stentgraftů o průměru 10 mm, na jejichž povrchu jsou připevněny tenkostěnné polyuretanové vaky o průměru 60 mm. Endovaky jsou během výkonu současně naplněny hydrogelem polyetylenglykolem, jehož dvě složky po smíchání při tělesné teplotě během 10 minut polymerizují prostorovou 3D vazbou. Po polymerizaci zůstává obsah dlouhodobě bez pozitivních i negativních změn objemu. Polymer obsahuje 1 % kontrastní látky, takže endovaky jsou na následné CT angiografii kontrastní. Vaky naplněné polymerem kompletně vyplní vak výdutě, překryjí odstupy a. mesenterica inferior i všech lumbálních tepen a také utěsní proximální krček v subrenální oblasti a distální konce SG v obou společných pánevních tepnách. Kontrast se v průběhu několika týdnů po implantaci nahromadí na vnitřním obvodu obou endovaků, jejichž obvodová kontura se tím pro rentgenové paprsky zvýrazní.
Anatomické indikace systému Nellix jsou vyjmenovány v Tab. 1. Metoda má určitá omezení: průtočné lumen výdutě může být maximálně 60 mm, protože každý z endovaků má průměr 60 mm, ale musí vyplnit celý vnitřní objem výdutě včetně různých tvarových nepravidelností. Standardní průměr stentgraftu je 10 mm, takže minimální přípustná šířka distálního aortálního krčku je 18 mm (o 2 milimetry méně než dvojnásobek průměru), což je podstatná výhoda proti stentgraftům nejběžnějších výrobců, jejichž raménka jsou obvyklé šíře od 13 do 16 mm. Toto omezení klasických SG nutí lékaře plánovat složitá řešení se změnami průměrů ramének nebo použít aorto-unilický stentgraft a provést femoro-femorální cross-over bypass, což je řešení, které přináší nevýhody hemodynamické a rovněž vyšší riziko infekce cévní protézy umístěné do třísel pacienta. Stentgraft Nellix je dostupný v délkách 100−180 mm, je možné kombinovat různé délky.

METODA
V našem centru je většina implantací SG prováděna plánovaně u asymptomatických i symptomatických pacientů se zvýšeným nebo vysokým rizikem (GAS skóre >90 nebo NYHA klasifikace III−IV). V roce 2014 jsme na Oddělení cévní chirurgie Nemocnice Na Homolce zavedli 51 stentgraftů do subrenální aorty a pánevních tepen. U dvou z těchto nemocných jsme použili stentgraft Nellix, u jednoho pro krátký subrenální krček 13 mm, u druhého pro výrazně kónický tvar krčku. Stentgrafty byly zavedeny v celkové anestezii cestou chirurgicky exponovaných společných femorálních tepen a po standardních rigidních vodičích. Endovaky byly naplněny polymerem za kontroly tlaku a objemu přes speciální konzoli a tlakový monitor (Obr. 1). Implantace systému Nellix od zavedení katétrů do finální angiografie trvala u prvního pacienta 75 minut, u druhého pacienta 45 minut. Doby fluoroskopie byly 8,9 a 8,0 minuty.
VÝSLEDKY
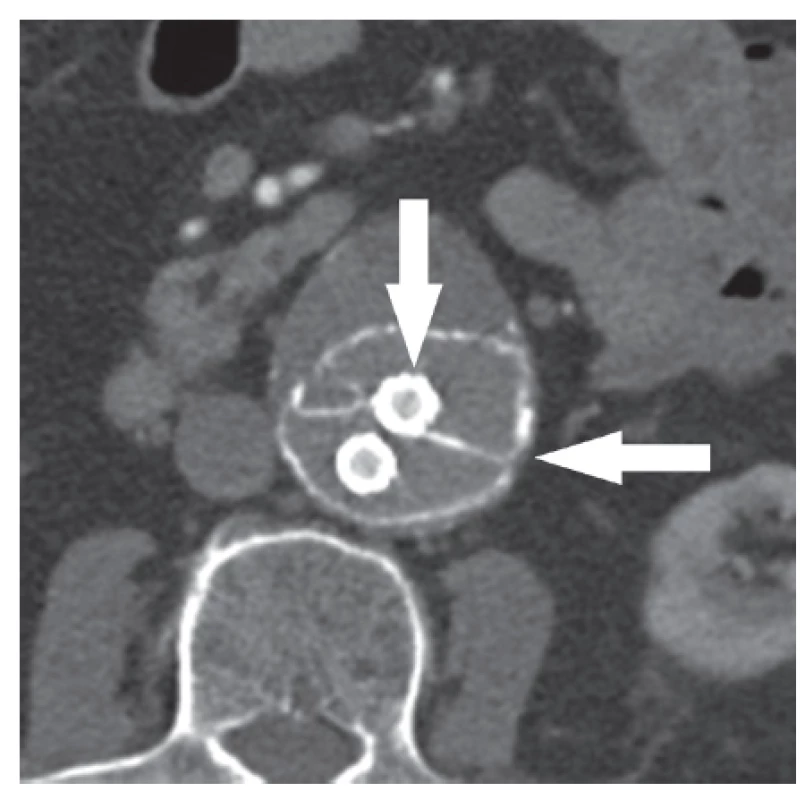
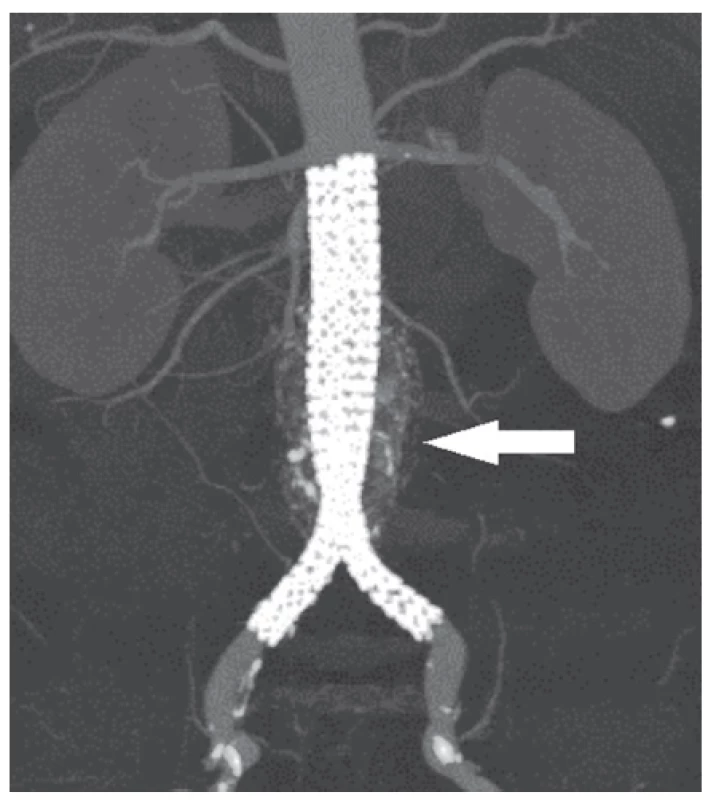
Pooperační průběh u obou pacientů byl bez rušivých příhod a byli propuštěni do ambulantní péče 5. pooperační den. Kontrolní CT angiografie po šesti týdnech ukazuje dobré těsnění SG a polymerem kompletně vyplněný vak výdutě (Obr. 2, 3). Je patrná zesílená kontura endovaků způsobená migrací kontrastní látky k jejich povrchu.
DISKUZE
Jedním ze základních cílů EVAS je vyloučit to, co je největší limitací klasického stentgraftu. Po implantaci standardních stentgraftů dochází k endoleakům pěti typů, z nich nejčastější je typ II způsobený zpětným tokem větví ústících do vaku výdutě. Riziko EL II. typu se významně zvyšuje, je-li průchodná a. mesenterica inferior a větší počet lumbálních tepen. Další typy EL jsou způsobeny netěsností v proximálním nebo distálním krčku, vzájemnou netěsností jednotlivých komponent nebo porušením protetického krytí. Celkový výskyt všech endoleaků u EVAR se odhaduje na 15−30 % [6,7,9]. Protože endovaky vytvoří kompletní odlitek průtočného lumen vaku výdutě, je všem typům EL principiálně zabráněno. Počet EL v iniciální londýnské studii implantace systému Nellix byl 0,7 %.
Další indikací jsou velmi tortuózní nebo zalomené pánevní tepny, které stentgraft a náplň vaku polymerem narovná. V této situaci je nutné zabránit, aby se zalomení tepen pouze neposunulo dále distálně. Dalším rizikovým faktorem EVAR je krátká délka společných pánevních tepen pod 2 cm, která je pro kotvení klasických SG nedostatečná, ale pro EVAS je právě jednou z indikací. Krátké společné pánevní tepny jsou typické pro asijskou populaci a v našem regionu se vyskytují zřídka.
K plánování výkonu je vhodný 3D plánovací software, který vypočítá centrální délku aortoilického úseku od renálních tepen po bifurkaci a odhadne objem polymerové náplně. Také přesně navrhne potřebné délky obou ramének stentgraftu Nellix (100−180 mm), přičemž délka pro každou stranu může být individuální.
Podle statistiky londýnské nemocnice St. Thomas, která má největší zkušenosti s implantací SG Nellix, je tento systém aplikovatelný u 73 % pacientů, jimž byl implantován SG jiných výrobců, a u 50 % pacientů, kteří byli operováni otevřeně [8]. Většina implantací byla dosud provedena na Novém Zélandu a v Evropě, kde výrobce získal CE značku v únoru 2013. Na českém trhu je výrobek registrován od roku 2014.
Výhledově bude možné systém Nellix použít mimo dosud schválené instrukce pro používání k léčení paraanastomotických výdutí nebo k různým sekundárním intervencím po otevřených operacích. EVAS je možné použít k proximálním extenzím, k léčbě krvácejících AAA a v kombinaci s chimney/snorkel grafty k léčbě juxtarenálních výdutí [10,11,12].
ZÁVĚR
Nová metoda EVAS umožní léčit pacienty, u kterých anatomická situace vedla k technicky obtížným a finančně náročným endovaskulárním postupům. Její dlouhodobé výsledky bude možné sledovat teprve na větších souborech pacientů.
Podpořeno MZ ČR – RVO (Nemocnice Na Homolce – NNH, 00023884), PVI7501IPMZ
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
MUDr. Petr Šedivý, Ph.D.
Oddělení cévní chirurgie Nemocnice Na Homolce
Roentgenova 2
150 00 Praha 5
e-mail: petr.sedivy@homolka.cz
Sources
1. Becquemin J, Pillet J, Lescallie F, et al. ACE trialists. A randomized controlled trial of endovascular aneurysm repair versus open surgery for abdominal aortic aneurysms in low - to moderate - risk patients. J Vasc Surg 2011;53 : 1167−73.
2. Blair R, Collins A, Harkin D. Complex EVAR for abdominal aorto-iliac aneurysms (AAIA) is associated with high rate of endoleak and less aortic sac shrinkage compared to conventional EVAR for AAA. Ir J Med Sci 2014; ahead of print.
3. Wain R, Marin M, Ohki T, et al. Endoleaks after endovascular graft treatment of aortic aneurysms: classification, risk factors and outcome. J Vasc Surg 1998;27 : 69−78.
4. Cieri E, De Rango P, Isernia G, et al. Type II endoleak is an enigmatic and unpredictable marker of worse outcome after endovascular aneurysm repair. J Vasc Surg 2014;59 : 930−7.
5. Ward T, Cohen S, Patel R, et al. Anatomic risk factors for type-2 endoleak following EVAR: a retrospective review of preoperative CT angiography in 326 patients. Cardiovasc Intervent Radiol 2014;37 : 324−8.
6. Al-Jubbouri M, Comerota A, Thakur S, et al. Reintervention after EVAR and open surgical repair of AAA: a 15-year experience. Ann Surg 2013;258 : 652−8.
7. Verzini F, Isernia G, De Rango P, et al. Abdominal aortic endografting beyond the trials: a 15-year single-center experience comparing newer to older generation stent-grafts. J Endovasc Ther 2014;21 : 439−47.
8. Karthikesalingam A, Cobb R, Khoury A, et al. The morphological applicability of a novel endovacular sealing (EVAS) system (Nellix) in a patient with abdominal aortic aneurysms. Eur J Vas Endovasc Surg 2013;46 : 440−5.
9. Löwenthal D, Herzog L, Rogits B, et al. Identification of predictive CT angiographic factors in the development of high-risk type 2 endoleaks after endovascular aneurysm repair in patients with infrarenal aortic aneurysms. Rofo 2015;187 : 49−55.
10. Boeckler D, Reijnen M, Krievins D, et al. Nellix for post-EVAR complications and to treat challenging infrarenal necks. J Cardiovasc Surg 2014;55 : 601−12.
11. Dijkstra M, Lardenoye J, van Oostayen J, et al. Endovascular aneurysm sealing for juxtarenal aneurysm using the Nellix device and chimney covered stents. J Endovasc Ther 2014; 21 : 541−7.
12. Malkawi A, de Bruin J, Loftus I, et al. Treatment of a juxtarenal aneurysm with the Nellix Endovascular aneurysm sealing system and chimney stent. J Endovasc Ther 2014;21 : 538−40.
Labels
Surgery Orthopaedics Trauma surgeryArticle was published in
Perspectives in Surgery

2015 Issue 6
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
- Metamizole vs. Tramadol in Postoperative Analgesia
- Safety and Tolerance of Metamizole in Postoperative Analgesia in Children
-
All articles in this issue
- Individualizovaná medicína
- Operace v těhotenství pro náhlé příhody břišní z pohledu chirurga
- Současné standardy v péči o pacienty s břišní sepsí
- Nová metoda endovaskulární výplně výdutě aorty abdominální (endovascular aneurysm sealing − EVAS)
- Ganglioneurom, raritní příčina nádoru měkkých tkání krku v dospělosti
- Synchronní nádorové duplicity pankreatu a žaludku/ledviny a jejich léčba
- Krvácení z pseudoaneuryzmatu a. hepatica po pankreatoduodenektomii řešené implantací stentgraftu
- Polymorfismy NOD2/CARD15 genu a riziko reoperací u Crohnovy nemoci
- Perspectives in Surgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Operace v těhotenství pro náhlé příhody břišní z pohledu chirurga
- Současné standardy v péči o pacienty s břišní sepsí
- Ganglioneurom, raritní příčina nádoru měkkých tkání krku v dospělosti
- Nová metoda endovaskulární výplně výdutě aorty abdominální (endovascular aneurysm sealing − EVAS)
