-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Abstrakta satelitních sympozií
Vyšlo v časopise: Čes. Revmatol., 24, 2016, No. 3, p. 126-131.
Kategória: Abstrakta
BIOLOGICKÁ LIEČBA A TEHOTENSTVO – NOVÉ POZNATKY
Mičeková D
Národný ústav reumatických chorôb, Piešťany
Zavedenie biologickej liečby do liečby zápalových reumatických chorôb prinieslo veľký pokrok a zmenu kvality života týchto pacientov. Vzhľadom tomu čoraz viac pacientok, hlavne s reumatoidnou artritídou, uvažuje o tehotenstve a plánuje rodičovstvo. Liečba počas tehotenstva musí zohľadniť pomer nutnosti kontroly zápalového reumatického ochorenia a potenciálneho rizika liečby pre fetus. Postoj k aplikácii liekov, a hlavne biologických liekov, pred počatím, v priebehu tehotenstva a v období laktácie sa postupne mení. Údaje zo súborov tehotných pacientok z klinických štúdií, registrov, kazuistikých zdelení menia náš pohľad na bezpečnosť predovšetkým z hľadiska teratogenicity. Veľkým prínosom sú tiež informácie o aplikácii biologických liekov u pacientok v gastroenterológii, kde pomer rizika liečby k benefitu liečby vyžaduje mnohokrát aplikáciu biologických liečiv počas veľkej časti tehotenstva. Jednotlivé reumatologické spoločnosti vydávajú svoje odporúčania k tejto problematike. V januári 2016 vyšlo napríklad odporúčanie Britskej reumatologickej spoločnosti týkajúce sa predpisu chorobu modifikujúcich liekov a kortikosteroidov v tehotenstve a laktácii. Najnovšie bolo publikované i stanovisko EULAru k použitiu antireumatík pred tehotenstvom, počas tehotenstva a v období laktácie. Základným pravidlom má byť oboznámenie každého pacienta v reprodukčnom období s rizikami a hlavne nutnosťou plánovania tehotenstva. Liečba pacientov pred a počas tehotenstva a laktácie má potlačiť aktivitu ochorenia matky a zohľadniť vplyv liekov na dieťa. Rozhodnutie o liečbe by malo byť založené súhlase a spolupráci medzi reumatológmi, internistami, gynekológmi ako i samotnou pacientkou. Kompatilibita s tehotenstvom bola potvrdená pri antimalarikách, sulfasalazíne, azathioprine, cyklosporíne, takrolime, kolchicíne, intravenóznych imunoglobulínoch a glukortikoidoch. Naopak liečbu methotrexátom, mycophenalat mofetilom a cyclophophamidom je potrebné prerušiť pred koncepciou z pohľadu možnej teratogenicity. Pri niektorých liekoch , akými sú napríklad leflunomid, tofacitinib, abatacept, rituximab, belimumab, tocilizumab, ustekinumab a anakinra, nie je dostatok informácii o ich fetálnej bezpečnosti a preto je tiež odporúčané túto liečbu ukončiť. Najviac údajov a najlepšie informácie sú o použití biologických liekov s anti TNF účinkom. Osobitne hlavne certolizumab má vzhľadom na svoju štruktúru najlepšie predpoklady byť v určitých nutných prípadoch aplikovaný počas celého tehotenstva. Certolizumab, ako pegylovaná Fab verzie TNF neobsahuje Fc časť IgG a vykazuje minimálny transplacentárny prenos. V odporúčaniach britskej reumatologickej spoločnosti je certolizumab ako jediný anti TNF vhodný v prípade potreby počas celého tehotenstva, včítane posledného trimestra.
DOPORUČENÍ EULAR PRO LÉČBU REVMATOIDNÍ ARTRITIDY – ROZDÍLY DOPORUČENÍ 2013 A 2016
Pavelka K
Revmatologický ústav, Praha
EULAR prezentoval v Londýně svoje Doporučení pro léčbu revmatoidní artritidy 2016. Jedná se o update Doporučení z roku 2013 a změny byly provedeny pouze tam, kde byla získána nová evidence o účinnosti. Metodologie byla stejná, jako u všech Doporučení EULAR, tzn.: provedení obsahové literární rešerše, ve snaze k získání evidence, steering committee sestávající se z 50 členů (Evropa, Asie, Austrálie – lékaři, epidemiologové, pacienti), návrh jednotlivých Doporučení a jejich finalizace Delphskou technikou. Nových Doporučení je 12 a zde je uveden text.
Léčba syntetickými DMARDs by měla být zahájena okamžitě, jakmile je stanovena diagnóza revmatoidní artritidy.
Léčba by měla být prováděna tak, aby bylo dosaženo cíle trvalé remise nebo nízké aktivity u každého pacienta.
Monitorování by mělo být časté u aktivní nemoci (1–3 měsíce), jestliže zde není zlepšení po 3 měsících od začátku léčby nebo není docíleno cíle po 6 měsících, terapie by měla být adjustována.
Methotrexát by měl být součástí první linie léčby u pacientů s aktivní RA.
V případě kontraindikací methotrexátu (nebo časné intolerance) tato další DMARDs by měla být zvážena jako postup (1.) volby (leflunomid, sulfasalazin).
Krátká aplikace glukokortikoidů by měla být zvážena, když se začíná nebo mění léčba csDMARDs při různých režimech léčby a způsobech podání, ale měla by být vysazena tak rychle, jak je klinicky možné.
Jestliže není dosaženo cíle prvním csDMARDs a při nepřítomnosti špatných prognostických faktorů, ostatní csDMARDs by měla být zvážena.
Jestliže není dosaženo cíle prvním csDMARDs a špatné prognostické faktory jsou přítomny, přidání biologického DMARDs nebo tsDMARDs by mělo být zváženo. Současná praxe je začít bDMARD.
Jestliže selhala léčba bDMARD a tsDMARD, léčba jinými bDMARD nebo tsDMARD by měla být zvážena. Jestliže selhala léčba TNF inhibitorem, pacienti mohou dostat další TNF inhibitor nebo léky s jiným mechanismem léčby.
Jestliže selhala léčba bDMARD a tsDMARD, léčba jinými bDMARD nebo tsDMARD by měla být zvážena. Jestliže selhala léčba TNF inhibitorem, pacienti mohou dostat další TNF inhibitor nebo léky s jiným mechanismem léčby.
Jestliže je pacient v trvalé remisi po snížení glukokortikoidů je možné uvažovat o snížení dávek bDMARD, zvláště pokud je terapeutický režim kombinován s csDMARD.
Jestliže je pacient v trvalé remisi, snížení dávek csDMARD by mělo být zváženo.
PŘEDNÍ UVEITIDA U SPONDYLARTRITID A JEJÍ MOŽNOSTI LÉČBY
Heissigerová J1, Mazná M1, 2, Říhová E1
1Oční klinika, 1. lékařská fakulta, Univerzita Karlova v Praze a Všeobecná fakultní nemocnice v Praze, 2Oční klinika JL
Úvod: Uveitidy jsou souborem různorodých onemocnění, která zahrnují jak oční projevy zánětu u systémových onemocnění, tak i oční postižení izolované. Uveitida u spondylartritidy (SpA) je většinou akutní, menší podíl pacientů trpí chronickou formou tohoto onemocnění, která vyžaduje systémovou imunomodulační terapii.
Metody: Retrospektivní analýza databáze pacientů Centra pro diagnostiku a léčbu uveitid Oční kliniky VFN a 1. LF UK v Praze v letech 2003–2016.
Výsledky: Od roku 2003 do 2016 vyšetřeno více než 2500 pacientů s uveitidou. U 550 (22 %) z nich byla prokázána souvislost nitroočního zánětu s antigenem HLA-B27, u 150 pacientů (6 %) byla diagnostikována SpA. U SpA je nejčastějším projevem uveitida přední, vyžadující většinou lokální léčbu. Zrak ohrožující komplikace, z nich nejčastěji cystoidní makulární edém, často recidivující či chronické zrak ohrožující formy zánětu jsou podkladem pro systémovou terapii, kterou jsou kortikoidy, biologická léčba, zejména inhibitory tumor nekrotizujícího faktoru alfa (např. infliximab, adalimumab, golimumab, certilizumab) aj.
Závěr: Revmatická onemocnění mohou vést k rozvoji nitroočního zánětu. V našem Centru pro diagnostiku a léčbu uveitid je uveitida asociovaná s SpA za posledních 13 let nejčastější uveitidou spojenou se systémovým neinfekčním onemocněním. Systémová imunointervenční léčba uveitidy se nerozlišuje podle toho, zda jde o systémové onemocnění nebo o oční projevy samotné, rozhodujícím kritériem je zrak ohrožující průběh zánětu. Pro účinnou léčbu pacientů, u kterých systémové onemocnění vede k postižení či ohrožení zraku, je naprosto nezbytná fungující mezioborová spolupráce.
VÝSKYT KOMORBIDIT U SPA, JEJICH SKRÍNINK A PREVENCE
Pavelka K
Revmatologický ústav, Praha
Spondyloartritidy (SpA) tvoří skupinu zánětlivých revmatických onemocnění, které postihují páteř a periferní pohybové struktury. Typický je také výskyt extraartikulárních manifestací, jako jsou akutní přední uveitida, idiopatický střevní zánět nebo psoriáza. Jako komorbidity u SpA se považují kardiovaskulární onemocnění, onemocnění ledvin, malignity, osteoporóza a deprese. Byla provedena mezinárodní studie komorbidit nazvaná ASAS COMOSPA, která ukázala vysokou prevalenci těchto komorbidit a nedostatečné procento pacientů, kteří jsou optimálně monitorováni. Obsahem přednášky je EULAR Doporučení pro hlášení a prevenci komorbidit. Zvláštní důraz je kladen na prevenci aterosklerotických onemocnění u ankylozující spondylitidy (AS). Některé novější studie prokázaly snížení kardiovaskulárního rizika u AS při léčbě anti TNF. Další významnou komorbiditou u SpA jsou osteoporotické fraktury, které jsou v klinické praxi diagnostikovány pouze v jedné čtvrtině. Nově náhle vzniklá bolest v zádech, která nekoreluje s aktivitou nemoci, by měla být vyšetřena s podezřením na frakturu. Další komorbidity jsou deprese, které jsou především výrazné u psoriatické artritidy. Byly vypracovány dotazníky, které jsou klinicky proveditelné i v běžné praxi revmatologa.
BIOLOGICKÁ LÉČBA REVMATOIDNÍ ARTRITIDY UMOŽŇUJE SNÍŽENÍ DÁVKY GLUKOKORTIKOIDŮ
Pavelka K
Revmatologický ústav, Praha
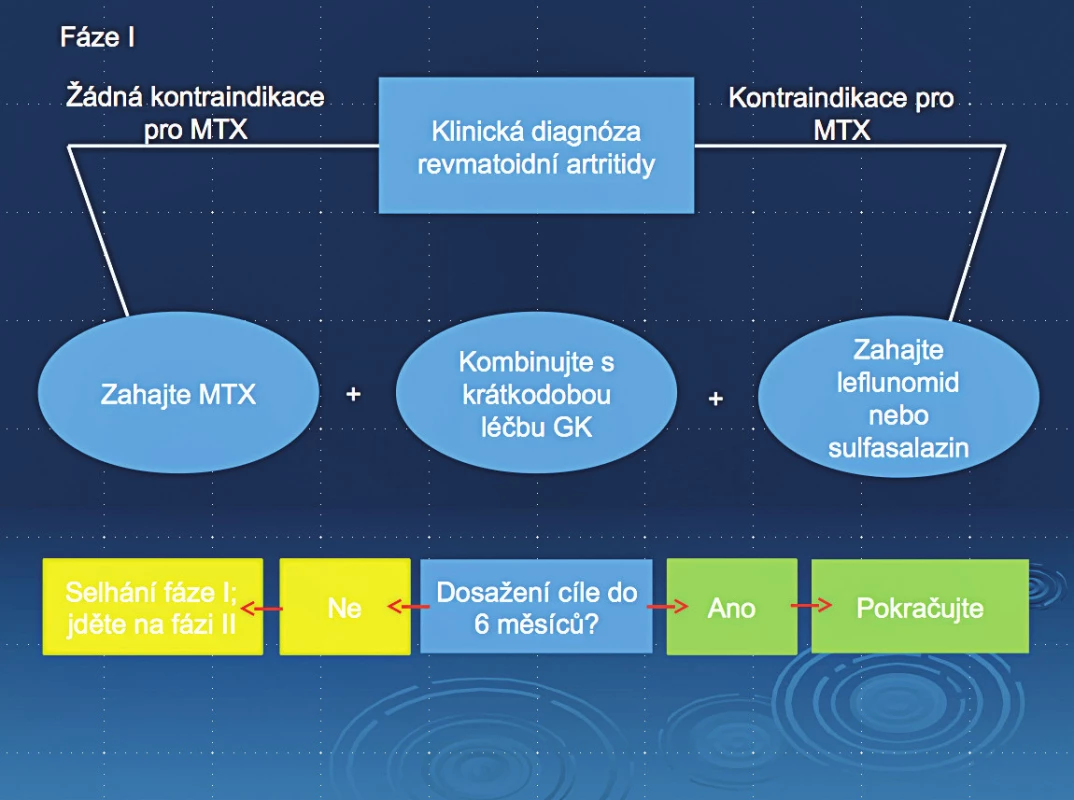
Glukokortikoidy (GK) jsou dle nových Doporučení EULAR součástí první léčebné linie v léčbě aktivní revmatoidní artritidy v kombinaci s methotrexátem. Doporučují se nižší, ale i střední dávky, přičemž ale doba aplikace by měla být optimálně do 6 měsíců nebo by měla být detrakce prováděna, jak je klinicky možná. GK však mají celou řadu nežádoucích účinku, jednak muskuloskeletálních, metabolických a dalších. Velmi významné je zvýšení kardiovaskulárního rizika (RR 1,47), dále pak zvýšené riziko závažných infekcí, vznik glaukomu, kožní atrofie a osteoporózy. Vznik osteoporózy (GIOP) je závislý na denní i kumulativní dávce. Dle novějších Doporučení EULAR (1) v dávkách 5 mg a menších převyšuje benefit GK jejich riziko, v dávkách nad 10 mg je naopak vyšší riziko. V intervalu 5–10 mg denně je riziko individuální. Jedním z cílů biologické léčby je kromě potlačení aktivity a zastavení strukturální progrese i snížení dávky podávaných GK.
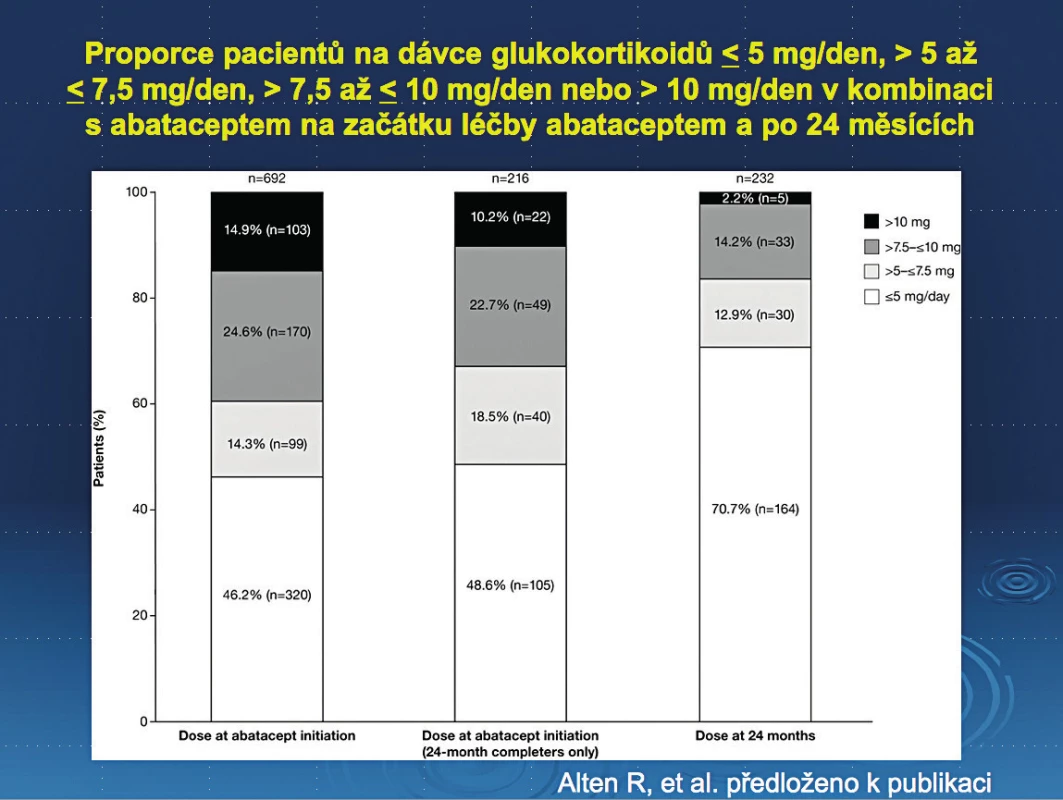
Studie ACTION byla dlouhodobá, observační studie s aplikací abataceptu i.v. u nemocných s aktivní revmatoidní artritidou. Studie prokázala výbornou účinnost abataceptu ve všech primárních i sekundárních kritériích. Bylo také prokázáno možné snížení nutné dávky GK. Zatímco na začátku léčby měl nízké dávky (méně než 5 mg) 46,2 % na konci léčby to již bylo 70,7 %. Počet pacientů na vysoké dávce byl naopak na začátku 15 % a na konci léčby klesl na 2 %. Studie tedy prokázala jednoznačně tzv. kortikoid šetřící efekt biologické léčby abataceptem (obrázek 1, 2).
PROBLEMATIKA DÁVKOVÁNÍ METHOTREXÁTU V MONOTERAPII A PŘI KOMBINAČNÍ LÉČBĚ
Moravcová R
Revmatologický ústav Praha
Methotrexát (MTX) podávaný samostatně nebo v kombinaci s jinými konvenčními chorobu modifikujícími léky (csDMARDs) je stále doporučován Evropskou ligou proti revmatismu (EULAR) a Americkou revmatologickou společností (ACR) jako lék první volby v terapii revmatoidní artritidy (RA). Snižuje aktivitu onemocnění a zpomaluje strukturální poškození kloubů. U pacientů s nedostatečnou účinností csDMARDs s přetrvávající vysokou aktivitou onemocnění a při přítomnosti rizikových faktorů majících negativní vliv na jeho průběh, jako je pozitivita protilátek proti citrulinovaným peptidům (anti-CCP) a revmatoidních faktorů (RF) a při erozivním průběhu nemoci, je doporučeno včasné zahájení biologické terapie k zabránění kloubního poškození a zhoršování funkční schopnosti pacienta. Doporučená iniciální dávka MTX je 10–15 mg týdně s její eskalací o 5 mg každé 2–4 týdny do dávky 20–30 mg týdně. Při nedostatečné účinnosti je vhodné přejít na parenterální aplikaci MTX, která ve srovnání s perorálním nabízí rychlejší nástup účinku při vyšší biologické dostupnosti, nižším výskytu nežádoucích účinků na gastrointestinální trakt a možnosti podávání vyšších dávek MTX dle individuální potřeby. Nyní je preferováno s.c. podání, které je pro pacienta výhodnější, méně bolestivé a jednodušší při samoaplikaci. Pokud není MTX v monoterapii dostatečně účinný, je kotevním lékem pro kombinace s jinými csDMARDs nebo s biologickými přípravky, které prokazují vyšší účinnost než samotný MTX, ale i než monoterapie biologickými přípravky. V poslední době byly prováděny celé řady klinických hodnocení, které porovnávaly účinnost MTX v kombinaci s protilátkami proti tumor nekrotizujícímu faktoru alfa (TNF-a inhibitory), ale i biologickými léky s jiným mechanismem účinku, ale až dosud nebyla provedena žádná studie, která by porovnávala účinnost a bezpečnost různých dávek MTX v kombinaci s TNF-a inhibitorem. První takovou prací je studie CONCERTO, která hodnotí různé dávky MTX v kombinaci s adalimumabem. Byl prokázán statisticky významný trend s rostoucí dávkou MTX u pacientů, kteří dosáhli nízké aktivity nebo remise onemocnění. Nebyl zde ale prokázán statisticky významný rozdíl v účinnosti MTX a sérových hladinách adalimumabu u dávek 10 a 20 mg týdně.
Je tedy předpoklad, že při rozhodování lékaře o dávce MTX v kombinaci s bDMARDs bude možné zvolit dávku nižší, čímž se sníží výskyt NÚ či intolerance MTX. Zda tomu tak bude i v kombinaci s ostatními bDMARDs, prokáží až další stude, které bude potřeba provést.
DESETILETÁ ÚČINNOST ADALIMUMABU V LÉČBĚ REVMATOIDNÍ ARTRITIDY
Pavelka K
Revmatologický ústav, Praha
Revmatoidní artritida (RA) je chronické a někdy i celoživotní onemocnění. Většina randomizovaných, kontrolovaných studií (RCT) je krátkodobá, a proto jsou důležitá jako doplňující data i z dlouhodobých extenzí a registrů biologické léčby.
Do studie (DEO20) byli zařazeni pacienti, kteří se původně zúčastnili v jedné ze 4 registračních studií s adalimumabem fáze 3 klinického zkoušení. Tyto studie byla prováděna zhruba před 10–12 lety, čemuž odpovídá i relativně vysoká aktivita na začátku studie (DAS 28 5,7), která se již v novějších studiích podstatně snížila. Do 4 jmenovaných studií bylo původně zařazeno 846 pacientů, z nichž desetiletou léčbu dokončilo 286 (33,7 %) pacientů. Přežívání na léčbě, někdy také charakterizované jako adherence k léčbě, je složený ukazatel, který v sobě obsahuje jak faktory účinnosti, ale i bezpečnosti, někdy však bohužel i nemedicínské faktory (např. úhrady pojišťoven), ale všeobecně je tento ukazatel ceněný jako komplexní ukazatel efektivnosti léčby daným preparátem. Zpravidla přežívání na léčbě klesá nejvíce v prvních 6–12 měsících a pak již pozvolněji přibližně o 10 % ročně. Přežívání na léčbě jedné třetiny pacientů na léčbě ADA je proto nutné hodnotit jako velmi dobré. Důvody pro ukončení léčby ADA byly nejčastěji nežádoucí účinky (23 %), nedostatek účinnosti pak pouze ve 12 %, což je překvapivé.
Co se týče hodnocení účinnosti u pacientů, kteří ukončili 10 let, byly výsledky vynikající, když hodnoty ACR 20, 50, 70 byly 78,6 %, 55,5 %, resp. 32,8 %. Toto je však dáno metodikou studie, kdy pacienti, kteří nedokončili studii, nebyli do statistického hodnocení uvedeni. Podobné je možné říci i o dosažení remise DAS 28 CRP v 57,2 % případů.
Jedním z největších problémů v dlouhodobém průběhu RA je zhoršování funkce, jinak řečeno vzniku disability, která vede k invaliditě. Je pozoruhodným výsledkem této studie, že prokázala, že v průběhu 10 let mělo více než 40 % pacientů normální funkci a více než jedna třetina pacientů měla současně normální funkci a stav nízké aktivity.
Byly také vyhodnocovány faktory, které na začátku léčby předurčovaly dosažení remise, z nichž jediným faktorem, který predikoval remisi, bylo kratší trvání onemocnění než 2 roky na začátku léčby. Je to další nepřímý důkaz o tom, že je vhodné zahájit anti TNF léčbu časně v průběhu onemocnění. Pozitivita revmatoidních faktorů neměla na přežívání na léčbě vliv, a anti CCP protilátky nebyly vyhodnocovány.
Ještě větší význam než určení účinnosti léčby mají dlouhodobé extenze a observační a kohortové studie pro získání bezpečnostních dat. Výskyt závažných infekcí byl 3,1/100 paciento/roků, což je méně než v randomizovaných studiích, ale co je obvyklé v observačních studiích a registrech. Bylo zaznamenáno několik oportunních infekcí, ale pouze 2 pacienti s tuberkulózou, což svědčí o efektivitě skrínovacího procesu k vyloučení latentní tuberkulózy.
Druhou sledovanou závažnou nežádoucí příhodou je výskyt malignit. V této studii nebyl zaznamenán zvýšený výskyt malignit celkově. Byl však zaznamenán vyšší výskyt melanomových a ne-melanomových kožních nádorů, což odpovídá zkušenostem z několika především severských registrů.
Výskyt infarktů myokardu, srdečního selhání a cerebrovaskulárních příhod byl ve studii relativně nízký. Některé metaanalýzy z poslední doby ukazují, že snížení celkové zánětlivé aktivity (a zvláště CRP) po aplikaci MTX či anti TNF může vést k podstatnému snížení výskytu kardiovaskulárních příhod, a naopak aplikace glukokortikoidů může toto riziko zvyšovat.
Závěrem lze ale říci, že jde o unikátní studii s takto dlouhým sledováním pacientů na anti TNF léčbě, která přinesla řadu příznivých zpráv především v oblasti závažných nežádoucích účinků. Z činnostních dat je nutné vyzdvihnout především zjištění lepší účinnosti adalimumabu a adherence k léčně u pacientů s kratším trváním nemoci než 2 roky. Dlouhodobé snížení aktivity RA při léčbě adalimumabem také vede k zachování funkce a tím i kvality života nemocných.
NOVÁ DOPORUČENÍ EULAR PRO LÉČBU PSORIATICKÉ ARTRITIDY
Pavelka K.
Revmatologický ústav, Praha
Podle metodologie EULAR byla vypracována Doporučení EULAR pro léčbu psoriatické artritidy (PsA), která se člení na tzv. nadřazené principy a dále na 10 Doporučení. Nutné je zdůraznit, že se jedná o Doporučení, nikoliv o návody. Text deseti Doporučení je následující:
Léčba by měla být cílena na dosažení cíle, kterým je remise nebo alternativně stav minimální / nízké aktivity. Tohoto je docíleno pravidelným monitorováním, vhodnou adjustací (úpravou) léčby.
U pacientů s psoriatickou artritidou mohou být použita nesteroidní antirevmatika k úlevě od muskuloskeletálních příznaků a symptomů.
U pacientů s periferní artritidou, zvláště s mnoha oteklými klouby, strukturální destrukcí a v přítomnosti zánětu, vysokého ESR/CRP a/nebo klinicky relevantních, mimokloubních manifestací, by mělo být zvážené použití csDMARDs v časném stadiu, přičemž methotrexát je preferovaným lékem u pacientů s významnějším kožním postižením.
Lokální injekce glukokortikoidů by měly být zváženy jako podpůrná léčba PsA; systémové glukokortikoidy by měly být použity s opatrností v nejnižší účinné dávce.
U pacientů s periferní artritidou a s nedostatečnou odpovědí na alespoň jeden csDMARD, léčba s bDMARD, obvykle s TNF inhibitorem by měla být zvážena.
U pacientů s periferní artritidou a nedostatečnou odpovědí na alespoň jedno csDMARD, u kterých je použití TNF inhibitoru nevhodné, by měla být zvážena léčba bDMARD cílená na IL12/23 nebo IL17.
U pacientů s periferní artritidou a nedostatečnou odpovědí na alespoň jedno csDMARD, u kterých je bDMARD nevhodné, může být zvážena léčba cíleným syntetickým DMARD, jako je inhibitor PDE4.
U pacientů s aktivní entezitidou a/nebo daktilitidu a nedostatečnou odpovědí na NSA nebo lokální injekce glukokortikoidů by měla být zvážena léčba biologickými DMARD, kterým podle současné praxe je TNF inhibitor.
U pacientů s převážně axiálním onemocněním, které je aktivní a má nedostatečnou odpověď na NSA, by měla být zvážena terapie biologickými DMARD, kterými podle současné praxe je TNF inhibitor.
U pacientů, kteří neodpovídají adekvátně na bDMARD, by měl být zvážen switching na jiný bDMARD, včetně switchování na jiný anti TNF inhibitor.
VISKOSUPLEMENTACE V LÉČBĚ OSTEOARTRÓZY
Pavelka K
Revmatologický ústav, Praha
Přednáška podporována firmou Stada
Intraartikulární aplikace hyaluronové kyseliny (HK) byla zavedena do léčby osteoartrózy (OA) před 50 lety a podle tehdejších představ o mechanismu účinku byla nazvána viskosuplementací. Kromě tohoto bariérového efektu však dochází k vazbě na receptory CD44 a četným farmakologickým účinkům, které lze shrnout jako protizánětlivé, analgetické, antikatabolické a proanabolické. Existuje velké množství preparátů HK, které se podle původu dělí jednak na extraktivní (většinou z kohoutích hřebínků) a biotechnologické, podle velikosti molekuly pak na velikost menší a střední a molekulu velkou. Zatím nebylo přesně definováno, jaká je optimální velikost molekuly HK z hlediska účinku a bezpečnosti.
Byla provedena řada klinických studií a též 15 významných metaanalýz a přehledných prací. Většina metaanalýz je pozitivních, ale byly publikovány i studie negativní. Dle nejnovější studie Coopera a spol. měla maximální efekt aplikace HK za 8 týdnů (ES = 0,46 95 % CI, 0,28–0,65) a efekt byl stále prokazatelný v týdnu 24 (ES = 0,21 95 % CI, 0,10–0,31). Byla provedena i velká observační studie ze spojených států, která obsahovala databázi 79 milionů pacientů a 182 000 pacientů po totální náhradě kolenního kloubu. V této studii docházelo ke zpoždění nutnosti aplikace totální náhrady o 3 roky (obr. 1). Dle posledních Doporučení ESCEO (1) je HK indikována u pacientů s bolestivou gonartrózou kolenního kloubu v druhém kroku, když selhává základní léčba režimovými opatřeními, analgetiky a nesteroidními antirevmatiky. Metaanalýzy studií také prokazují relativní bezpečnost i.a. aplikace HK a přetrvávající příznivý poměr účinnost / bezpečnost.
LIŠÍ SE FEBUXOSTAT OD ALLOPURINOLU V LÉČBĚ HYPERURIKÉMIE?
Pavelka K
Revmatologický ústav, Praha
Přednáška podporovaná firmou Berlin-Chemie
Dna je zánětlivé, krystaly indukované onemocnění, které postihuje až 1 % populace. Základem léčby dny je dlouhodobá normalizaci hladiny kyseliny močové v séru. Toho se docílí kombinací nefarmakologických postupů (režimová opatření, abstinence, redukce hmotnosti) a podáním léků, které snižují hladiny kyseliny močové. Dle nových Doporučení EULAR je cílovou hodnotou pro pacienty s dnavou artritidou 360 μmol/l. Indikovaní k léčbě hyperurikémie jsou pacienti s častými atakami akutního zánětu, chronickou tofózní dnou, destrukcemi kloubů a urolitiázou.
Medikamentózně se dají použít urikosurika (tč. není žádné k dispozici) a inhibitory xanthinoxidázy, tzn. allopurinol a febuxostat. Febuxostat je nepurinový, selektivní inhibitor xanthinoxidázy, který je metabolizován a vylučován játry a proto není nutná adjustace dávky u renální insuficience. Nemá také žádné jiný vliv na enzymy purinového a pyrimidinového metabolismu.
Ve studii FACT byl srovnáván febuxostat s allopurinolem a cílové hodnoty po febuxostatu (80 mg denně) bylo docíleno u 53 % pacientů, zatímco po allopurinolu (300 mg denně) u 21 % pacientů. Febuxostat byl účinný i u pacientů s poškozením ledvin. V dlouhodobé studii EXCEL, při dlouhodobém poklesu kyseliny močové po febuxostatu docházelo ke zlepšení progrese onemocnění ledvin.
Febuxostat je indikován u pacientů, u nichž je allopurinol kontraindikován nebo není tolerován, dále u pacientů, u kterých nebylo po allopurinolu dosaženo cílové hodnoty. Zdá se být výhodnější u pacientů s částečnou ledvinnou nedostatečností. Snížení hladiny kyseliny močové také může snižovat kardiovaskulární riziko.
Štítky
Dermatológia Detská reumatológia Reumatológia
Článok vyšiel v časopiseČeská revmatologie
Najčítanejšie tento týždeň
2016 Číslo 3- První zkušenosti s léčbou psoriázy bimekizumabem v české reálné praxi – kazuistika z FNUSA
- Na český trh přichází biosimilar adalimumabu s prokázanou terapeutickou ekvivalencí
- Nehoňte nemocné s mMCC od čerta k ďáblu!
-
Všetky články tohto čísla
- Abstrakta satelitních sympozií
- Abstrakta sekce nelékařských zdravotnických pracovníků
- C-reaktivní protein: biomarker sekundární osteoporózy a zlomenin při chronických zánětlivých onemocněních
- Účinnost první a následné linie léčby adalimumabem u revmatoidní artritidy: analýza dat Českého národního registru ATTRA
- 60. výroční sjezd českých a slovenských revmatologů
- Česká revmatologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- C-reaktivní protein: biomarker sekundární osteoporózy a zlomenin při chronických zánětlivých onemocněních
- 60. výroční sjezd českých a slovenských revmatologů
- Účinnost první a následné linie léčby adalimumabem u revmatoidní artritidy: analýza dat Českého národního registru ATTRA
- Abstrakta sekce nelékařských zdravotnických pracovníků
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy