-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Alkalimetrické titrácie solí organických zásad v liekopise
Alkalimetric titrations of salts of organic bases in the Pharmacopoeia
Modified methods – alkalimetry in ethanol 70% with a defined small volume of hydrochloric acid 0.01 mol/l added to the solution of the sample before the titration and alkalimetry in ethanol 70% or ethanol 96% alone with potentiometric end-point detection for the assay of halide salts of 11 organic N-bases has been investigated. The results were compared to those obtained by the method of the European Pharmacopoeia 7th Ed. (Ph. Eur. 7th Ed.). The Ph. Eur. 7th Ed. use for 8 investigated substances alkalimetry in alcohol 96 % with a defined small volume of hydrochloric acid 0.01 mol/l (5 ml) with potentiometric end-point detection: Cinchocaine hydrochloride, Codeine hydrochloride dihydrate, Ethylmorphine hydrochloride, Lidocaine hydrochloride, Papaverine hydrochloride, Pilocarpine hydrochloride, Quinine hydrochloride, Tetracaine hydrochloride. Our results revealed that the Ph. Eur. 7th Ed. method did not work for 5 drugs from this group: Cinchocaine hydrochloride, Ethylmorphine hydrochloride, Papaverine hydrochloride, Pilocarpine hydrochloride and Tetracaine hydrochloride. In the group of investigated substances we included also drugs with the character of weak organic bases for which Ph. Eur. 7th Ed. prescribed different methods for their assay: Thiamine hydrochloride and Pyridoxine hydrochloride – acidimetric titration in non-aqueous solvents with perchloric acid and Procaine hydrochloride – determination of primary aromatic amino-nitrogen (Ph. Eur. 7th Ed., chapter 2.5.8).
Keywords:
weak organic bases • alkalimetry • potentiometric end-point detection • assay
Autoři: Želmíra Bezáková; Mária Stankovičová
Působiště autorů: Bratislava, Slovenská republika ; Katedra farmaceutickej chémie FaF UK
Vyšlo v časopise: Čes. slov. Farm., 2013; 62, 264-269
Kategorie: Původní práce
Souhrn
Boli vypracované modifikované postupy stanovenia obsahu vybratých solí dusík obsahujúcich organických zásad alkalimetrickou titráciou v prostredí etanolu 70 % a kyseliny chlorovodíkovej 0,01 mol/l, v prostredí samotného etanolu 70 %, resp. etanolu 96 % s potenciometrickou indikáciou konca titrácie. Výsledky stanovenia obsahu vybratých substancií liečiv porovnávame s výsledkami stanovenia obsahu týchto liečiv v Ph. Eur. 7 Ed. V skupine 11 nami analyzovaných liečiv predpisuje Ph. Eur. 7th Ed. uvedenú alkalimetrickú titráciu pre 8 liečiv: Cinchocaine hydrochloride, Codeine hydrochloride dihydrate, Ethylmorphine hydrochloride, Lidocaine hydrochloride, Papaverine hydrochloride, Pilocarpine hydrochloride, Quinine hydrochloride, Tetracaine hydrochloride. Pri 5 liečivách z tejto skupiny: Cinchocaine hydrochloride, Ethylmorphine hydrochloride, Papaverine hydrochloride, Pilocarpine hydrochloride a Tetracaine hydrochloride metóda neposkytuje výsledky zhodné s deklarovaným obsahom liečiv v príslušných liekopisných článkoch. Do súboru 11 analyzovaných liečiv sme zaradili aj liečivá charakteru slabých organických zásad, pre ktoré liekopis predpisuje iné postupy stanovenia obsahu: pre Thiamine hydrochloride a Pyridoxine hydrochloride je v liekopise predpísaná acidimetrická titrácia odmerným roztokom kyseliny chloristej v nevodnom prostredí a pre liečivo Procaine hydrochloride je to nitritometria, t.j. stanovenie dusíka v primárnych aromatických amínoch.
Kľúčové slová:
slabé organické zásady, alkalimetria, potenciometrická titrácia, stanovenie obsahuÚvod
Jedným z najdôležitejších kritérií hodnotenia akosti liečiva popri skúškach totožnosti a skúškach na čistotu je stanovenie obsahu liečiva, ktoré charakterizuje jeho terapeutickú hodnotu a súčasne upozorňuje na prítomnosť nečistôt, vrátane rozkladných produktov. Pri stanovení obsahu liečiv predpisuje a používa Ph. Eur. 7th Ed.1) prakticky všetky metódy klasickej kvantitatívnej analytickej chémie, fyzikálne, fyzikálnochemické, biologické a mikrobiologické metódy.
Do skupiny metód odmernej analýzy, ktoré používa Ph. Eur. 7th Ed.1) pri stanovení obsahu liečiv, patria aj acidobázické titrácie. Acidobázické titrácie látok zásaditého a kyslého charakteru vo vodnom prostredí, prípadne v zmesiach vody s vhodným organickým rozpúšťadlom s vizuálnou indikáciou konca titrácie sa dajú vykonať v prípadoch, keď hodnoty ich disociačných konštánt sú väčšie ako 10–6. Slabšie kyseliny a zásady, prípadne kyslé a zásadité soli možno úspešne titrovať za potenciometrickej indikácie konca titrácie. Liečivá zaradené do liekopisu sú často kyselinami a zásadami podstatne slabšími (pKa = 8–13), len ojedinele sa dajú titrovať vo vodnom prostredí v dôsledku nízkej disociácie alebo rozpustnosti. Na stanovenie obsahu týchto liečiv predpisujú liekopisy acidobázické titrácie v nevodných organických rozpúšťadlách, ktoré majú svoje trvalé miesto v skupine odmerných metód vo farmaceutickej analytike, pričom acidimetria je v liekopisoch a v praxi niekoľkonásobne početnejšia. Začiatky acidobázických titrácií v nevodnom prostredí siahajú do roku 1953. V 60. až 70. rokoch 20. storočia bola metóda zaradená do všetkých moderných liekopisov. Teórie acidobázických titrácií v nevodných prostrediach vychádzajú z Brönstedovej a Löwryho protónovej teórie kyselín a zásad. O vývoji, teoretických základoch, zdokonaľovaní metódy a jej rozširovaní v praxi informujú mnohé práce v odborných časopisoch a monografiách2–5). Pri titráciách v nevodnom prostredí sa používajú bezvodé organické rozpúšťadlá s vhodnými vlastnosťami6, 7). Mnohé z používaných rozpúšťadiel sú však škodlivé a toxické, preto je na mieste snaha odborníkov nahradiť titrácie v nevodnom prostredí pre stanovenie solí alkaloidov a ďalších dusík obsahujúcich organických zásad metódami, ktoré využívajú reagencie pripravené vo vodnom prostredí, reagencie menej toxické, chrániace životné prostredie. Už Ph. Eur., 3rd. Ed.8) predpisoval pre stanovenie obsahu niektorých halogenidov organických zásad alkalimetrickú titráciu odmerným roztokom hydroxidu sodného v prostredí etanolu 96 % alebo v prostredí zmesi etanolu 96 % a vody s prídavkom definovaného malého množstva kyseliny chlorovodíkovej s potenciometrickou indikáciou konca titrácie namiesto acidimetrie v nevodnom prostredí. Pri tomto postupe obsah soli organickej zásady zodpovedá objemu odmerného roztoku hydroxidu sodného 0,1 mol/l medzi dvoma bodmi inflexie pri potenciometrickej titrácii. V ďalšom vydaní Ph. Eur. 4th Ed.9) sa tento pracovný postup uplatnil pri 75 liečivách, čo predstavovalo asi 50 % solí organických zásad zaradených v uvedenom liekopise. Použitie alkalimetrickej titrácie pre stanovenie obsahu solí alkaloidov v organickej fáze (organické rozpúšťadlo, najčastejšie chloroform, bolo súčasťou titračného prostredia) predpisoval už nemecký liekopis10), uprednostnená bola vizuálna indikácia konca titrácie. Metóda alkalimetrickej titrácie v Ph. Eur. 4th Ed.9) sa od metódy uvedenej v nemeckom liekopise10) líšila v troch aspektoch: 1. ako titračné prostredie bola predpísaná zmes etanolu 96 % a vody; 2. potenciometrická indikácia koncového bodu titrácie a 3. súčasťou titračného prostredia bol prídavok presne definovaného malého objemu kyseliny chlorovodíkovej pred začiatkom titrácie. O teoretickej a praktickej potrebe pridať do titračného prostredia presne známe malé množstvo kyseliny chlorovodíkovej sa viedli diskusie11).
Pokusná časť
Liečivá Cinchocaine hydrochloride, Codeine hydrochloride dihydrate, Ethylmorphine hydrochloride, Lidocaine hydrochloride, Papaverine hydrochloride, Pilocarpine hydrochloride, Procaine hydrochloride, Pyridoxine hydrochloride, Quinine hydrochloride, Tetracaine hydrochloride, Thiamine hydrochloride boli liekopisnej kvality.
Rozpúšťadlá, reagencie, odmerné roztoky, roztoky indikátorov sa pripravili podľa Ph. Eur., 7th Ed.1).
Vážilo sa na analytických váhach typ WA-32, pri potenciometrických titráciách sa použil Precision digital pH meter OP – 208/1, Radelkis, Maďarsko s dvojicou elektród sklenená a kalomelová pre acidimetrické titrácie v nevodnom prostredí a pre alkalimetrické titrácie v zmesi etanolu 96 % a kyseliny chlorovodíkovej 0,01 mol, platinová a grafitová elektróda sa použila pre nitritometrické stanovenie primárnych aromatických amínov, automatické byrety 10,00 ml a 25,00 ml. Ostatné laboratórne sklo: kadičky, odmerné valce, navažovačky, pipety boli triedy kvality A.
Pracovný postup stanovenia obsahu analyzovaných liečiv podľa Ph. Eur. 7th Ed.1)
Predpísaný návažok liečiva sa rozpustí v zmesi kyseliny chlorovodíkovej 0,01 mol/l VS a etanolu 96 %. Roztok sa titruje odmerným roztokom hydroxidu sodného 0,1 mol/l VS za potenciometrickej indikácie ekvivalenčného bodu do druhého inflexu. Odčíta sa spotreba medzi dvoma bodmi inflexie (Cinchocaine hydrochloride, Codeine hydrochloride dihydrate, Ethylmorphine hydrochloride, Lidocaine hydrochloride, Papaverine hydrochloride, Pilocarpine hydrochloride, Quinine hydrochloride, Tetracaine hydrochloride). Liečivá Pyridoxine hydrochloride a Thiamine hydrochloride sa titrujú acidimetricky v nevodnom prostredí (bezvodá kyselina mravčia a anhydrid kyseliny octovej) odmerným roztokom kyseliny chloristej 0,1 mol/l VS za potenciometrickej indikácie ekvivalenčného bodu, vykoná sa slepá skúška. Pre stanovenie obsahu liečiva Procaine hydrochloride predpisuje Ph. Eur. 7th Ed.1) stanovenie dusíka v primárnych aromatických amínoch (kap. 2.5.8).
Alternatívny pracovný postup stanovenia obsahu analyzovaných liečiv I
Návažok liečiva (Pilocarpine hydrochloride 0,200 g, Procaine hydrochloride a Tetracaine hydrochloride 0,250 g) sa rozpustí v zmesi 5 ml kyseliny chlorovodíkovej 0,01 mol/l a 50 ml etanolu 70 % R a titruje sa odmerným roztokom hydroxidu sodného 0,1 mol/l VS za potenciometrickej indikácie ekvivalenčného bodu do druhého inflexu. Odčíta sa spotreba medzi dvoma bodmi inflexie.
Alternatívny pracovný postup stanovenia obsahu analyzovaných liečiv II
Návažok liečiva (Cinchocaine hydrochloride a Ethylmorphine hydrochloride 0,300 g, Pilocarpine hydrochloride 0,200 g, Procaine hydrochloride a Tetracaine hydrochloride 0,250 g, Pyridoxine hydrochloride 0,150 g,) sa rozpustí v 50 ml etanolu 70 % R (Ethylmorphine hydrochloride 30 ml etanolu 70 % R a Cinchocaine hydrochloride v 50 ml etanolu 96 % R) a titruje sa odmerným roztokom hydroxidu sodného 0,1 mol/l VS za potenciometrickej indikácie ekvivalenčného bodu do prvého inflexu.
Výsledky a diskusia
Ph. Eur. 7th Ed.1) predpisuje pre veľkú skupinu liečiv typu halogenidov organických zásad alkalimetrickú tiráciu odmerným roztokom hydroxidu sodného 0,1 mol/l VS v prostredí kyseliny chlorovodíkovej (0,01 mol/l) a etanolu 96 % za potenciometrickej indikácie konca titrácie s použitím sklenenej a nasýtenej kalomelovej elektródy. Zo skupiny 11 nami analyzovaných liečiv je tento postup uvedený pri liečivách: Cinchocaine hydrochloride, Codeine hydrochloride dihydrate, Ethylmorphine hydrochloride, Lidocaine hydrochloride, Papaverine hydrochloride, Pilocarpine hydrochloride, Quinine hydrochloride, Tetracaine hydrochloride. Prítomnosť kyseliny chlorovodíkovej v etanole 96 % môže spôsobovať systematické chyby pri stanovení obsahu, ktoré je možné eliminovať slepým pokusom. Aby sa slepý pokus nemusel realizovať, do etanolu 96 % ako titračného prostredia sa pridáva malé, presne definované množstvo silnej kyseliny chlorovodíkovej 0,01 mol/l. Potenciometrická titračná krivka má pri týchto titráciách dva inflexy: prvý inflex odpovedá neutralizácii pridanej kyseliny chlorovodíkovej, druhý inflex odpovedá deprotonizovanému liečivu. Pre výpočet obsahu liečiva sa použije spotreba odmerného roztoku hydroxidu sodného 0,1 mol/l VS medzi dvoma bodmi inflexie. Okrem eliminácie systematických chýb umožňuje tento postup overiť („validovať“) koncentráciu odmerného roztoku hydroxidu sodného 0,1 mol/l VS, čím sa stanovenia obsahu liečiv charakteru slabých protonizovaných kyselín stávajú precíznejšími12, 13). Postup predstavuje modifikáciu titrácií v dvojfázovom prostredí, kde sa zásada uvoľnená zo soli v priebehu titrácie kvantitatívne extrahuje do organického rozpúšťadla nemiešateľného s vodou; ako organické rozpúšťadlá sa najčastejšie používali chloroform, dichlórmetán a pod.14).
V našej práci sme použili postup alkalimetrickej titrácie podľa Ph. Eur. 7th Ed.1) pri stanovení obsahu substancií liečiv uvedených v experimentálnej časti práce. Metódu sme aplikovali ako alternatívnu metódu aj pre stanovenie obsahu liečiv Thiamine hydrochloride, Pyridoxine hydrochloride, Procaine hydrochloride v snahe unifikovať pracovné postupy stanovenia obsahu liečiv charakteru solí organických zásad.
Postup alkalimetrickej titrácie pri stanovení obsahu podľa Ph. Eur. 7th Ed.1) neposkytoval pri stanovení obsahu všetkých analyzovaných liečiv výsledky deklarované v odpovedajúcom liekopisnom článku. Pri liečivách: Codeine hydrochloride dihydrate, Lidocaine hydrochloride a Quinine hydrochloride poskytoval liekopisný pracovný postup pri stanovení ich obsahu výsledky zhodné s deklarovaným obsahom týchto liečiv v liekopisných článkoch. Na základe našich skúseností môžeme konštatovať, že liekopisný postup pre stanovenie obsahu liečiv: Cinchocaine hydrochloride, Ethylmorphine hydrochloride, Papaverine hydrochloride, Pilocarpine hydrochloride a Tetracaine hydrochloride nie je vhodný. Pri potenciometrickej titrácii týchto liečiv sme na potenciometrických titračných krivkách nezaznamenali prvý inflexný bod (obr. 1) napriek tomu, že do titračného prostredia sa pridalo 5 ml kyseliny chlorovodíkovej 0,01 mol/l VS, alebo bol prvý inflexný bod ťažko rozpoznateľný, čo sťažovalo vyhodnotenie stanovenia obsahu liečiv. Predpokladáme, že príčinou absencie prvého inflexného bodu na potenciometrických titračných krivkách je príliš slabá bázicita týchto liečiv, hodnoty ich disociačných konštánt sú blízke hodnote 7 (etylmorfín = 7,88, papaverín = 6,38, pilokarpín = 1, 63 a 7,08, tetrakaín = 8,39)15, 16). Ak majú byť na potenciometrickej titračnej krivke dva od seba dobre oddelené inflexné body, rozdiel hodnôt Δ pKa musí byť najmenej 4, čo sa vzťahuje na vodné prostredie. Alkalimetrické titrácie však v tomto prípade prebiehajú v prostredí voda – etanol 96 %; relatívna permitivita tohto prostredia je nižšia ako relatívna permitivita vody, čo ovplyvňuje do určitej miery ionizačné pomery. Rozsah ionizácie liečiv je znížený a v dôsledku toho je ich bázicita nižšia a ich hodnoty pKa v zmesi vody a etanolu 96 % sú tiež o niečo nižšie ako hodnoty pKa týchto liečiv vo vode. Túto skutočnosť potvrdili autori14) v svojej práci, keď stanovovali hodnoty pKa papaverínu a pilokarpínu v zmesi etanol – voda a obsah etanolu 96 % v titračnom prostredí sa pohyboval od 30 % do 60 %. So stúpajúcim podielom etanolu 96 % bázicita obidvoch liečiv klesala, hodnoty pKa obidvoch liečiv tak isto klesali. Pri liečive Tetracaine hydrochloride na potenciometrickej titračnej krivke boli dva výrazné inflexné body, ale obsah liečiva sa pohyboval vysoko nad obsahom deklarovaným v liekopisnom článku (tab. 1).
Obr. 1. Priebeh potenciometrickej titrácie liečiva Pilocarpine hydrochloride v prostredí etanolu 96 % (50,00 ml) a HCl 0,01 mol/l (5,00 ml) 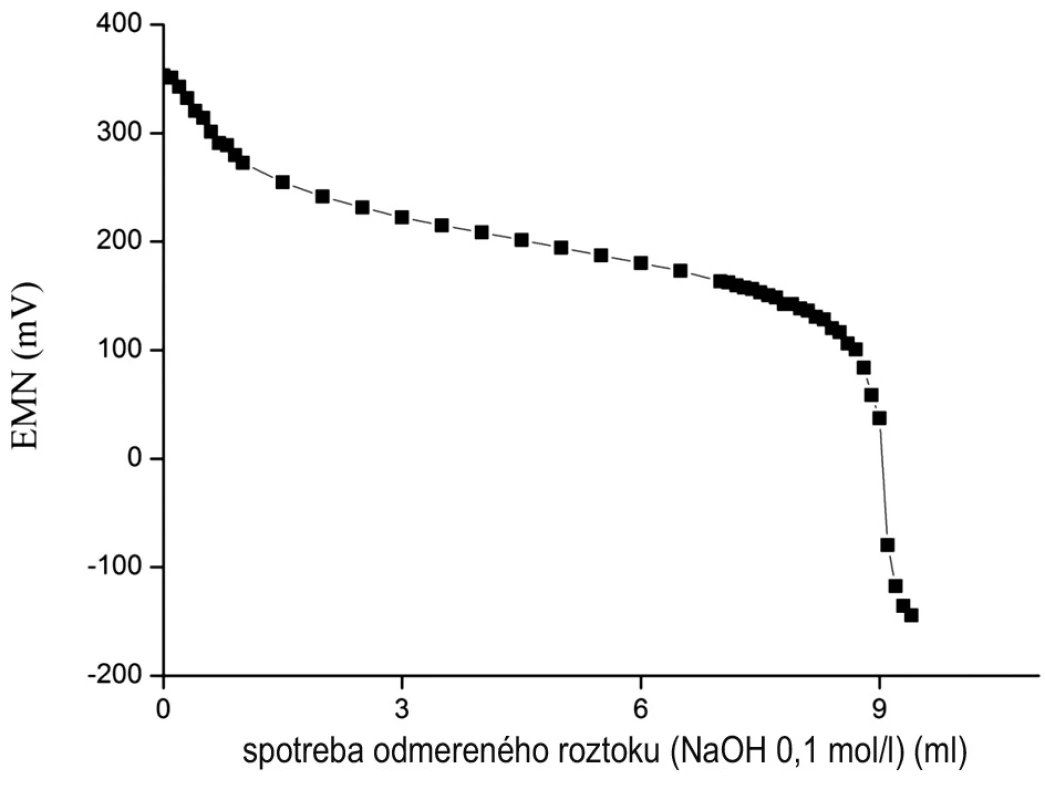
Tab. 1. Stanovenie obsahu analyzovaných liečiv podľa Ph. Eur., 7th Ed. 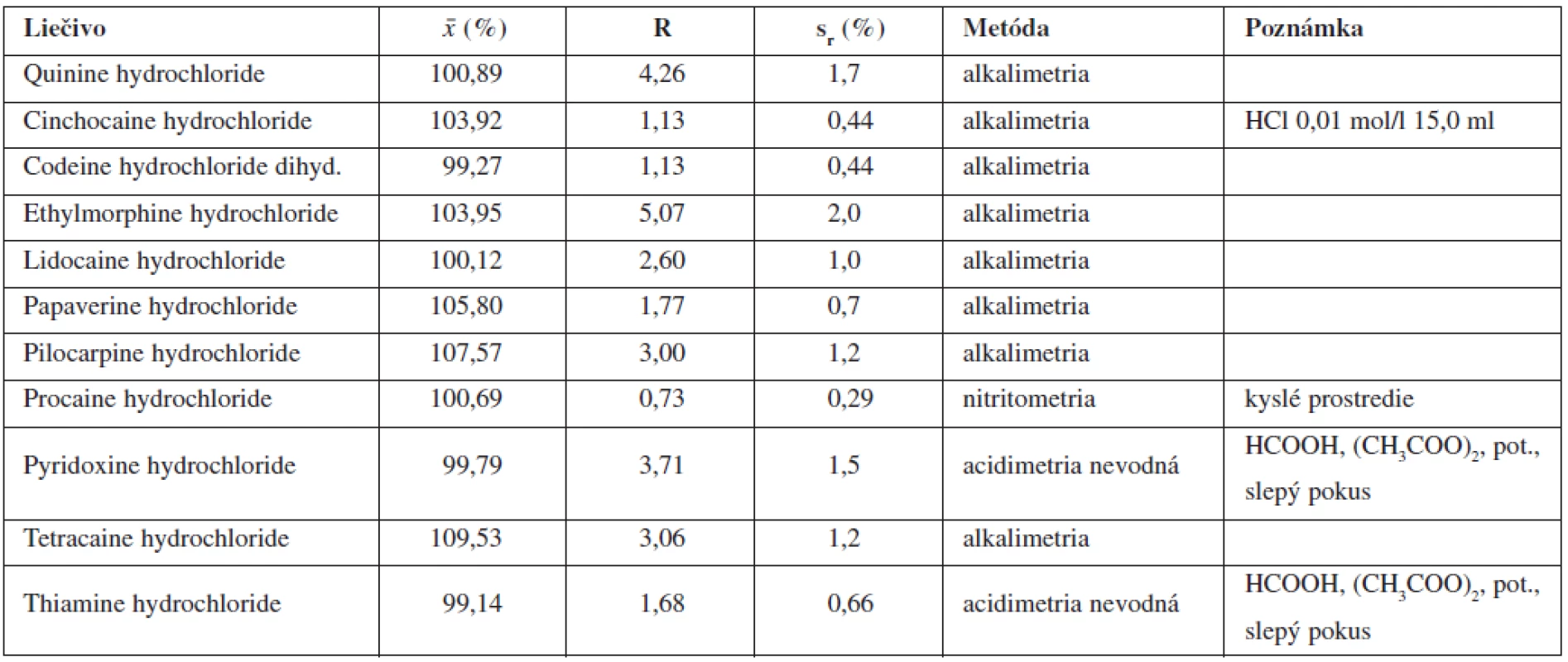
pot. – potenciometrická titrácia Na základe skutočnosti, že sme pri 5 liečivách nedosiahli pri použití postupu podľa Ph. Eur. 7th Ed.1) zhodné výsledky stanovenia ich obsahu s obsahom deklarovaným v odpovedajúcom liekopisnom článku, pristúpili sme pri alkalimetrickej titrácii s potenciometrickou indikáciou konca titrácie k modifikácii titračného prostredia. Menili sme koncentráciu etanolu a titrácie sme uskutočnili v prostredí samotného etanolu 96 % alebo etanolu 70 % bez prídavku, alebo s presne definovaným prídavkom kyseliny chlorovodíkovej 0,01 mol/l.
Uvedené zmeny sme aplikovali pri stanovení obsahu liečiva Cinchocaine hydrochloride, u ktorého metóda podľa Ph. Eur. 7th Ed.1) poskytovala výsledky vyššie ako je limit v liekopisnom článku (tab. 1). Ako vhodným titračným prostredím pre toto liečivo bol samotný etanol 96 % bez prídavku kyseliny chlorovodíkovej 0,01 mol/l, potenciometrická titračná krivka vykazovala jeden výrazný inflexný bod (obr. 2). Zistený obsah liečiva (tab. 2) odpovedal obsahu deklarovanému v liekopisnom článku (98,5 % až 101,0 %). Ďalej sme pre liečivo Cinchocaine hydrochloride použili ako titračné prostredie aj prostredie etanolu 70 % (jeden inflexný bod) a prostredie etanolu 70 % s prídavkom kyseliny chlorovodíkovej 0,01 mol/l (5,0 ml, titrovalo sa do druhého inflexu). Pri týchto titráciách boli výsledky stanovenia obsahu liečiva vyššie ako jeho deklarovaný obsah v liekopisnom článku asi o 4,0 %, uvedené titračné prostredie bolo pre stanovenie obsahu liečiva nevhodné.
Obr. 2. Priebeh potenciometrickej titrácie liečiva Cinchocaine hydrochloride v prostredí etanolu 96 % (50,00 ml) 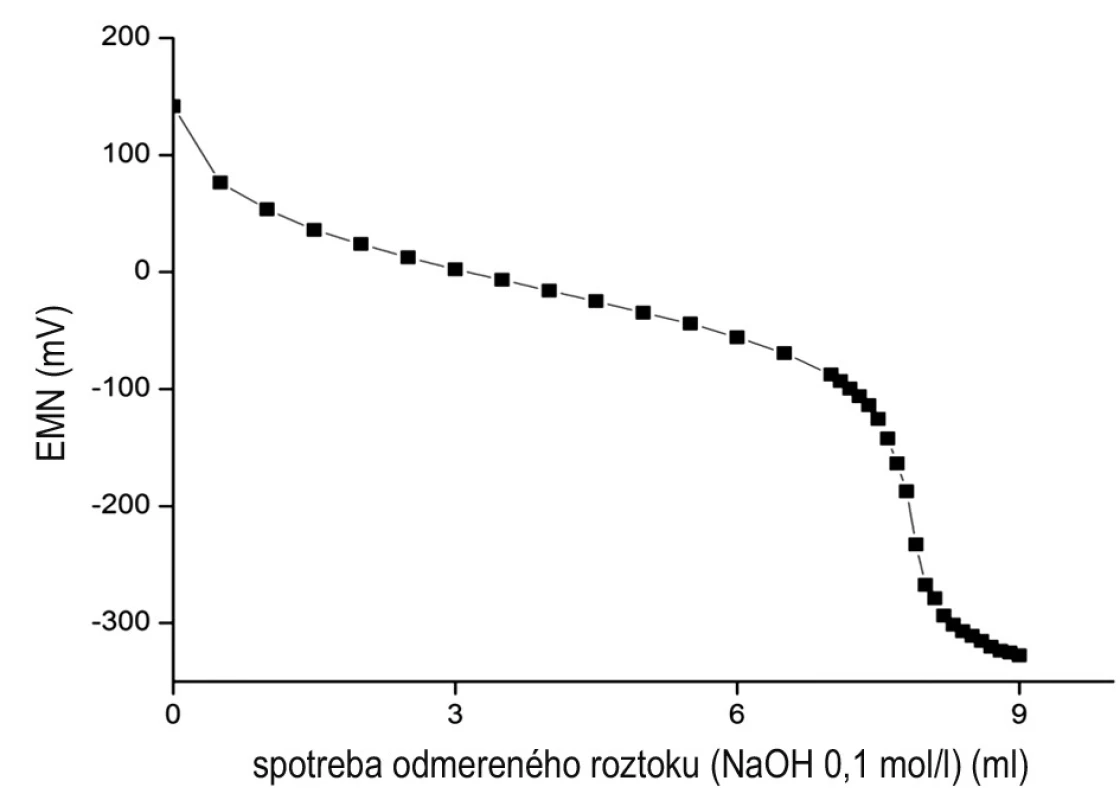
Tab. 2. Stanovenie obsahu analyzovaných liečiv alternatívnymi postupmi I a II 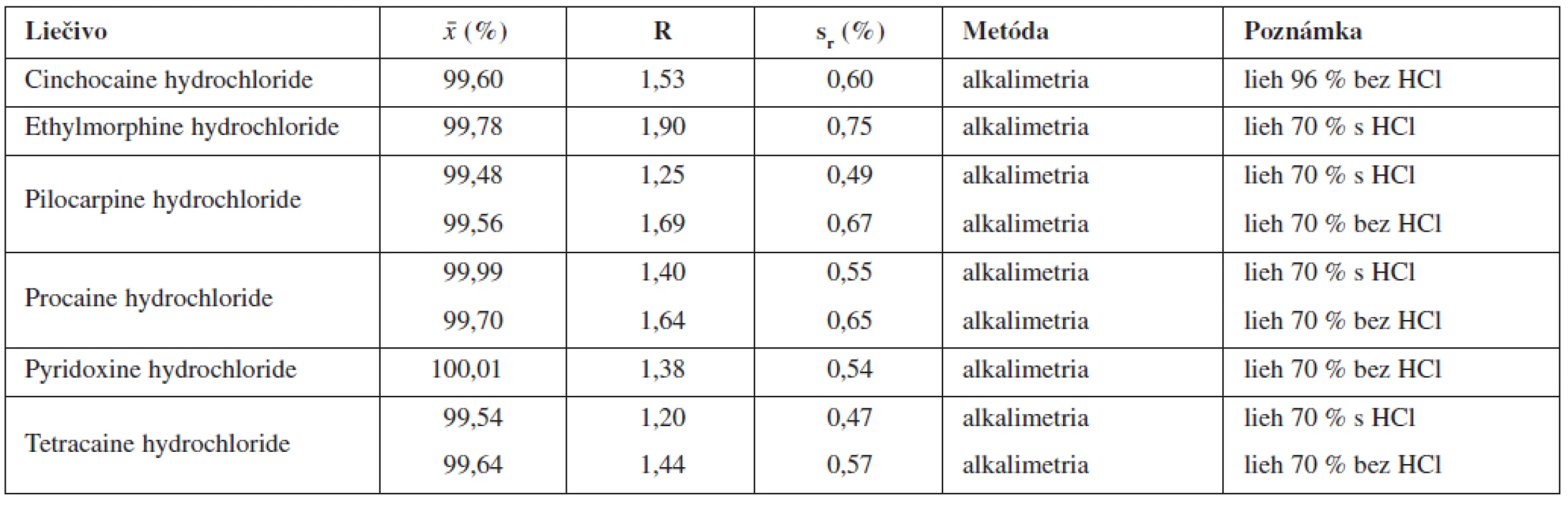
Rovnako sme postupovali aj pri stanovení obsahu ďalších liečiv, pri ktorých sme nedosiahli pri použití postupu podľa Ph. Eur. 7th Ed.1) výsledky zhodné s obsahom deklarovaným v odpovedajúcom liekopisnom článku. Zistili sme, že pre liečivo Ethylmorphine hydrochloride je vhodným titračným prostredím etanol 70 % (30,0 ml) s prídavkom kyseliny chlorovodíkovej 0,01 mol/l (5,0 ml). Potenciometrická titračná krivka mala dva výrazné inflexné body, prvý inflexný bod bol výraznejší (obr. 3). Všetkých 6 výsledkov paralelných stanovení obsahu liečiva bolo v deklarovanom rozpätí uvedenom v liekopisnom článku (99,0 % až 101,0 %) (tab. 2). Pri tomto liečive sa ukázal byť dôležitý pomer etanolu 70 % a kyseliny chlorovodíkovej 0,01 mol/l. Keď sme pri alkalimetrickej titrácii použili etanol 70 % v množstve 50,0 ml s prídavkom kyseliny chlorovodíkovej 0,01 mol/l (5,0 ml), resp. samotný etanol 70 % v množstve 50,0 ml, výsledky stanovenia obsahu etylmorfíniumchloridu sa pohybovali pod 90,0 %, titračné prostredie sa ukázalo byť nevhodné. Pre stanovenie obsahu ďalších dvoch liečiv – Pilocarpine hydrochloride a Tetracaine hydrochloride je pri alkalimetrickej titrácii odmerným roztokom hydroxidu sodného 0,1 mol/l s potenciometrickou indikáciou konca titrácie vhodným titračným prostredím: a) etanol 70 % samotný (50,0 ml), potenciometrická titračná krivka vykazuje jeden inflexný bod; b) etanol 70 % (50,0 ml) s prídavkom kyseliny chlorovodíkovej 0,01 mol/l (5,0 ml), titruje sa do druhého inflexu. Pri tomto postupe je prvý inflexný bod pri pilokarpíniumchloride menší, ale dobre rozpoznateľný. Výsledky 6 paralelných stanovení obsahu obidvoch liečiv sa pohybovali v deklarovanom rozpätí 99,0 % až 101,0 % (tab. 2).
Obr. 3. Priebeh potenciometrickej titrácie liečiva Ethylmorphine hydrochloride v prostredí etanolu 70 % (30,00 ml) a HCl 0,01 mol/l (5,00 ml) 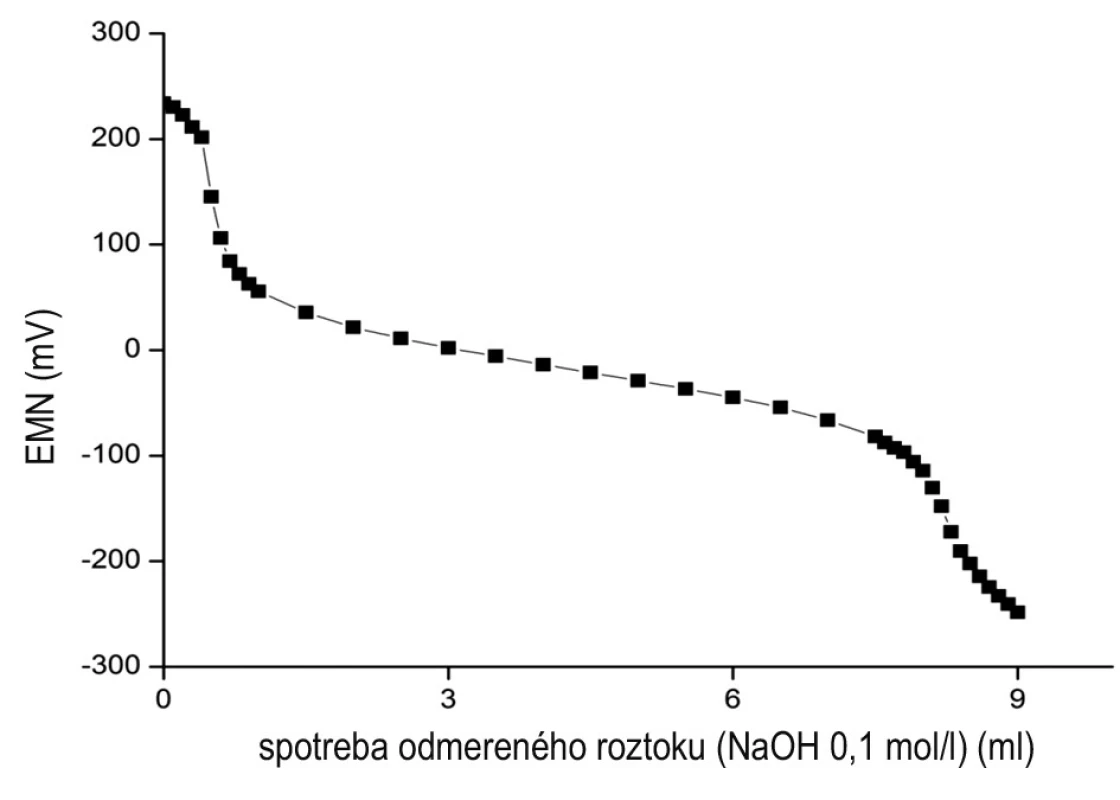
Pri stanovení obsahu liečiva Papaverine hydrochloride podľa Ph. Eur. 7th Ed.1) sa naše výsledky (tab. 1) pohybovali vysoko nad obsah deklarovaný v liekopisnom článku (99,0–101,0 %), pričom na potenciometrickej titračnej krivke chýbal prvý inflexný bod. Rovnako vysoké výsledky stanovenia obsahu liečiva boli aj pri jeho potenciometrickej titrácii v samotnom etanole 96 % (108,20 %). Pri potenciometrickej titrácii liečiva v prostredí etanolu 70 % s prídavkom kyseliny chlorovodíkovej 0,01 mol/l (5,0 ml a 15,0 ml) prvý inflexný bod na potenciometrickej titračnej krivke chýbal. Obsah liečiva sa pri obidvoch alternatívnych postupoch (rôzne množstvo kyseliny chlorovodíkovej 0,01 mol/l) pohyboval vysoko nad limit povolený liekopisom (109,27 %, 108,56 %). Pri titrácii papaveríniumchloridu v prostredí samotného etanolu 70 % sa titrovalo do prvého inflexu, obsah liečiva bol približne o 3 % nad hranicou jeho deklarovaného obsahu v liekopisnom článku (103,19 %). Zmena koncentrácie kyseliny chlorovodíkovej, ktorá sa pridávala do titračného prostredia (použili sme koncentráciu 0,1 mol/l v množstve 5 ml) nepriniesla pozitívny efekt. Riešeniu tohto problému sa budeme venovať v ďalšej našej práci. Acidimetrická titrácia liečiva v nevodnom prostredí podľa17) poskytuje spoľahlivé výsledky (6 paralelných stanovení, priemer = 99, 42 %).
Obsah lokálneho anestetika Procaine hydrochloride sa podľa Ph. Eur. 7th Ed.1) stanovuje nitritometricky, metóda poskytuje spoľahlivé výsledky. Pri alkalimetrickej titrácii liečiva s potenciometrickou indikáciou konca titrácie v prostredí etanolu 96 % s prídavkom kyseliny chlorovodíkovej 0,01 mol/l (5 ml) sme dosiahli výsledky (116,15 %), ktoré sa pohybovali vysoko nad deklarovaný obsah liečiva v liekopisnom článku (99,0–101,0 %); na titračnej krivke boli dva výrazné inflexné body. Po zmene tiračného prostredia: etanol 70 % s prídavkom kyseliny chlorovodíkovej 0,01 mol/l (5,0 ml), resp. etanol 70 % samotný boli výsledky alkalimetrickej titrácie prokaíniumchloridu s potenciometrickou indikáciou konca titrácie v zhode s deklarovaným obsahom látky (tab. 2). Potenciometrická titračná krivka v prvom prípade vykazovala dva inflexné body, v druhom prípade sa titrovalo do prvého inflexu.
V Ph. Eur. 3rd Ed.8) bola v snahe o unifikáciu postupov stanovenia obsahu liečiv charakteru organických zásad aj pre liečivá Thiamine hydrochloride a Pyridoxine hydrochloride navrhnutá metóda alkalimetrickej titrácie s potenciometrickou indikáciou konca titrácie. Uvedený postup neposkytoval výsledky v zhode s deklarovaným obsahom týchto liečiv v príslušných liekopisných článkoch, preto sa Ph. Eur. vrátil v Supplemente 4.218) pre tiamíniumchlorid a v Supplemente 4.319) pre pyridoxíniumchlorid pri stanovení obsahu k acidimetrickej titrácii v nevodnom prostredí, ktorá poskytuje dobré výsledky (tab. 1). Pre tiamíniumchlorid je alkalimetrická titrácia nevhodná, o liečive je známe, že sa ľahko rozkladá v alkalickom prostredí, preto zmeny EMN v oblasti bodu ekvivalencie nezodpovedajú skutočnosti (tzv. nepravá odozva potenciálu).
Stanovením obsahu pyridoxíniumchloridu podľa Ph. Eur. 4th. Ed.1) sa podrobne zaoberajú aj práce12, 13). Aj v tomto prípade ide o simultánnu alkalimetrickú titráciu dvoch rôzne silných kyselín s potenciometrickou indikáciou bodu ekvivalencie; titračná krivka by mala mať dva inflexy. Kyselina chlorovodíková je silná kyselina, prakticky kvantitatívne disociuje vo vode na H3O+ ióny (pKa = 0), pyridoxíniumchlorid je slabá protonizovaná báza s hodnotou pKa = 4,84. Rozdiel v hodnotách pKa týchto dvoch kyselín je podľa12) dostatočne veľký, aby titrácia bola úspešná. Za podmienok9) je koncentrácia liečiva v titračnom prostredí (13,265 mmol.l–1) asi 14-krát väčšia ako koncentrácia kyseliny chlorovodíkovej (0,909 mmol.l–1), čo spôsobuje, že pri titrácii liečiva za uvedených podmienok je inflexný bod pre kyselinu chlorovodíkovú sporný a stanovenie obsahu pyridoxíniumchloridu neposkytuje správne a presné výsledky, čo potvrdili nielen naše experimenty (prvý inflexný bod ťažko identifikovateľný, druhý inflexný bod výrazný, obsah liečiva 3–4 % nad deklarovaný obsah v liekopisnom článku), ale aj simulovaná titrácia zmesi kyseliny chlorovodíkovej (0,05 mmol) a pyridoxíniumchloridu (0,73 mmol) v titračnom prostredí s autoprotolytickou konštantou pKauto = 16, ktorá je opísaná v práci12). Autori13) pri alkalimetrickej potenciometrickej titrácii pyridoxíniumchloridu vychádzajú zo skutočnosti, že látka má v molekule dve kyslé funkčné skupiny: pyridíniový katión (pKa1 = 4,84) a fenolovú -OH skupinu (pKa2 = 9,04). Rozdiel termodynamických (makroskopických) konštánt acidity týchto funkčných skupín je dostatočne veľký a umožňuje alkalimetrickú titráciu v titračnom prostredí, ktorého autoprotolytická konštanta < 10–14. Alkalimetrická titrácia pyridoxíniumchloridu s potenciometrickou indikáciou konca titrácie prebieha v prostredí zmesi vody (5 ml) a etanolu 96 % (50 ml); autori tak upustili od prídavku presne definovaného množstva kyseliny chlorovodíkovej 0,01 mol.l–1. Návažok pyridoxíniumchloridu (75,0 mg) pre stanovenie obsahu sa zvolil tak, aby spotreba odmerného roztoku hydroxidu sodného 0,1 mol.l–1 nebola vyššia ako 9 ml.
Naše výsledky ukázali, že obsah liečiva Pyridoxine hydrochloride stanovený alkalimetrickou titráciou v prostredí etanolu 70 % s prídavkom kyseliny chlorovodíkovej 0,01 mol/l (5 ml) bol nad hranicou deklarovaného obsahu. Prikláňame sa k názoru13), že použitie presne definovaného prídavku kyseliny chlorovodíkovej 0,01 mol.l–1 ovplyvňuje vyhodnotenie objemu odmerného roztoku hydroxidu sodného, ktorý sa spotrebuje do prvého inflexu pri titrácii. Spotreba odmerného roztoku hydroxidu sodného do prvého inflexu zodpovedá báze pyridoxíniumchloridu a množstvu silnej kyseliny chlorovodíkovej prítomnej v titračnom prostredí; mala by byť menšia ako spotreba odmerného roztoku hydroxidu sodného do druhého inflexu.
Etanol 70 % samotný sa ukázal byť vhodným titračným prostredím pre stanovenie obsahu pyridoxíniumchloridu, titrovalo sa do prvého inflexu. Výsledky 6 paralelných stanovení obsahu tohto liečiva sa pohybovali v rozpätí 99,0–100,3 %.
So všetkými študovanými liečivami sme vykonali vždy 6 paralelných stanovení, výsledky v tabuľkách 1 a 2 predstavujú priemernú hodnotu stanovenia obsahu.
Relatívnu smerodajnú odchýlku sme vypočítali z rozpätia. Na základe našich výsledkov a skúseností môžeme konštatovať, že úspešná realizácia stanovenia obsahu študovaných liečiv modifikovanou alkalimetrickou titráciou závisí od viacerých faktorov: návažku liečiva, rovnakých prídavkov odmerného roztoku v priebehu titrácie a aj od spôsobu vyhodnotenia titrácií v bode ekvivalencie. Z vyššie uvedených postupov žiaden nie je vhodný pre stanovenie obsahu papaveríniumchloridu a tiamíniumchloridu. Acidimetrická titrácia týchto dvoch liečiv v nevodnom prostredí poskytuje presné a reprodukovateľné výsledky.
Záver
Výsledky stanovenia obsahu vybraných liečiv charakteru solí slabých organických zásad metódou alkalimetrickej titrácie odmerným roztokom hydroxidu sodného 0,1 mol.l–1 v prostredí zmesi etanolu 96 % a kyseliny chlorovodíkovej 0,01 mol.l–1 s potenciometrickou indikáciou konca titrácie podľa Ph. Eur. 7th Ed. v našej práci potvrdili, že metóda poskytuje reprodukovateľné výsledky, ale má určité obmedzenia. V svojej súčasnej podobe nie je vhodná pre stanovenie obsahu liečiv charakteru slabých zásad, ktorých disociačná konštanta pKa > 7. Pre stanovenie obsahu liečiv tohto typu sme použili modifikovanú alkalimetrickú titráciu, ako titračné prostredie sme použili etanol 96 % samotný, etanol 70 % samotný, alebo etanol 70 % s prídavkom presne definovaného objemu kyseliny chlorovodíkovej 0,01 mol.l–1 (tab. 2).
Stret záujmov: žiadny.
Došlo 2. októbra 2013
Prijato 11. novembra 2013
doc. RNDr. Želmíra Bezáková, CSc. (∗) • M. Stankovičová
Katedra farmaceutickej chémie FaF UK
Odbojárov 10, 832 32 Bratislava, Slovenská republika
e-mail: bezakovaz@fpharm.uniba.sk
Zdroje
1. European Pharmacopoeia, 7th Ed. Strasbourg: Cedex, Council of Europe 2010.
2. Gyenes I. Titrationen in nichtwässrigen Medien, 3. Aufl., Stuttgart: F. Enke Verlag 1970; 701.
3. Šafařík L., Kašová M. Die nichtwässrige Protometrie als Arzneibuchmethode zur Gehaltsbestimmung von Arzneistoffen. Pharmazie 1984; 39, 843.
4. Fritz J. S. Acid-base Titration in Nonaqueous Solutions Boston: Allyn and Bacon Inc. 1973; 142.
5. Šafařík L., Stránský Z. Odměrná analýza v organických rozpouštědlech. Praha: SNTL 1982; 399 s.
6. Bezáková Ž., Bachratá M., Blešová M., Šubert J. Acidobázické titrácie v nevodnom prostredí vo farmaceutickej analytike II. Acidimetria 1. Českoslov. Farm. 1993; 42, 7–27.
7. Bezáková Ž., Šubert J. Acidobázické titrácie v nevodnom prostredí vo farmaceutickej analytike II. Acidimetria 2. Čes. a slov. Farm. 1994; 43, 43–63.
8. European Pharmacopoeia, 3rd Ed. Strasbourg: Cedex, Council of Europe 1997.
9. European Pharmacopoeia, 4th Ed. Strasbourg: Cedex, Council of Europe 2002.
10. Deutsches Arzneibuch, 7th Ed. Stuttgart: Deutscher Apotheker-Verlag 1968.
11. Bye R. Theoretical and practical considerations of the newer methods of the European Pharmacopoeia for the assay of halide salts of organic bases. Sci. Pharm. 2002; 70, 129.
12. Pohl B. Pyridoxin-HCl. In: Bracher F., Heisig P., Langguth P., Mutschler E., Rücker G., Scriba G., Stahl-Biskup E (ed.) Kommentar zum Europäischen Arzneibuch. Stuttgart: Wissenschaftliche Verlagsgesellschaft 2002.
13. Kos N., Surmann J. P. Die Gehaltsbestimmung von Pyridoxinhydrochlorid (Vitamin B6) nach Ph. Eur. 4. Ausgabe, Grundwerk 2002. Pharmazie 2006; 61, 414–416.
14. Connors K. A. A textbook of Pharmaceutical Analysis. J. Wiley & Sons, 1967; 614.
15. Newton D. W., Kluza Ronald B. pKa value of medicinal compounds in pharmacy practice. Drug Intelligence and Clinical Pharmacy 1978; 12, 546–554.
16. Takács-Novák K., Völgyi G. Alkalimetry in alkohol-water mixtures with potentiometric end-point detection. Critical remarks on a newer method of European Pharmacopoeia. Anal. Chim. Acta. 2004; 507, 275–280.
17. Československý lékopis, 4. vyd., 2. Svazek. Praha: Avicenum-Zdravotnické nakladatelství, n.p. 1987, 697–698.
18. European Pharmacopoeia, 4th Ed., Supplement 4.2. Strasbourg: Cedex, Council of Europe 2002.
19. European Pharmacopoeia, 4th Ed., Supplement 4.3. Strasbourg: Cedex, Council of Europe 2002.
Štítky
Farmácia Farmakológia
Článek Nové knihyČlánek Rejstříky
Článok vyšiel v časopiseČeská a slovenská farmacie

2013 Číslo 6-
Všetky články tohto čísla
- Fyziologické faktory ovlivňující osud léčiva v gastrointestinálním traktu
- Cationic Eudragit® Polymers as Excipients for Microparticles Prepared by Solvent Evaporation Method
- Nové knihy
- Vplyv kvartérnej amóniovej soli na liberáciu liečiva s antiseptickým účinkom
- Sledování vzniku hydrátů diklofenaku sodné soli a jejich vlivu na disoluci léčiva z připravených tablet
- K životnímu jubileu doc. RNDr. PhMr. Milana Čeladníka, CSc.
- Alkalimetrické titrácie solí organických zásad v liekopise
- Stanovenie vareniklínu v lieku Champix® dvojdimenzionálnou kapilárnou elektroforézou v spojení s UV detekciou
- Pohľad na poskytovanie starostlivosti v oblasti liekov na Slovensku – lekárnik a pacient
- A chapter from the history of the pharmacy of the Brothers of Mercy in Spišské Podhradí in the 19th and 20th centuries
- 42. sympozium klinické farmacie
- Padesát let seminářů a sympozií z dějin farmacie
- Rejstříky
- Česká a slovenská farmacie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Pohľad na poskytovanie starostlivosti v oblasti liekov na Slovensku – lekárnik a pacient
- Alkalimetrické titrácie solí organických zásad v liekopise
- Vplyv kvartérnej amóniovej soli na liberáciu liečiva s antiseptickým účinkom
- Fyziologické faktory ovlivňující osud léčiva v gastrointestinálním traktu
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



