-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Operační léčba poranění plexus brachialis
Surgical Treatment of Brachial Plexus Injury
Brachial plexus injury has been attracting increasing attention in recent times, partly because of an increasing incidence arising out of higher survival rates for patients after polytrauma and also due to higher success rates for surgical treatment. Obstetric brachial plexus palsy has recently become the focus of interest for a number of articles. Many injured elements of the brachial plexus are reconstructed by a donor nerve transferred onto the recipient nerve, i.e. by neurotization. This method leads to better outcomes than suture of the injured nerve in the proximal part of the plexus, the main advantage of which is the opportunity to place the suture as close to the muscle as possible. There are two newer methods – Oberlin´s technique and end-to-side anastomosis. It remains unclear as to which donor nerve is better to use for neurotization in specific recipients due to a lack of large, randomized clinical trials. Generally, neurotization using the intraplexal nerve as a donor of motor nerve fibres is more successful than neurotization using the extraplexal nerve.
Key words:
brachial plexus injury – neurotization – Oberlin´s technique – end-to-side anastomosis – nerve suture – obstetric brachial plexus palsy
Autoři: P. Haninec; R. Kaiser
Působiště autorů: Neurochirurgická klinika 3. LF UK a FN Královské Vinohrady, Praha
Vyšlo v časopise: Cesk Slov Neurol N 2011; 74/107(6): 619-630
Kategorie: Minimonografie
Souhrn
Poranění pažní pleteně je velmi těžký úraz. V posledních letech nabývá na významu jak pro jeho vzrůstající incidenci (vyšší přežívání pacientů po polytraumatech), tak pro větší úspěchy s operační léčbou. Navíc se dostává do popředí i v minulosti opomíjená problematika perinatálních poranění. Velká část poraněných elementů plexus brachialis je řešena přenesením dárcovského nervu na příslušného příjemce, tzv. neurotizací. V poslední době se ukazuje, že může mít dokonce lepší výsledky než sutura přerušeného nervu v proximální části pleteně. Hlavní předností neurotizace je možnost sutury co nejblíže cílovému svalu. Novějšími metodami jsou Oberlinova technika a end-to-side anastomóza. Kvůli chybění větších randomizovaných studií zůstává nadále ne úplně jasné, který dárce je lépe využitelný pro daného příjemce. Obecně však platí, že neurotizace s využitím intraplexálních nervů jako dárců motorických vláken je lepší než neurotizace pomocí extraplexálních zdrojů.
Klíčová slova:
poranění pažní pleteně – neurotizace – Oberlinova technika – end-to-side anastomóza – sutura nervu – perinatální poranění plexus brachialisÚvod
Poranění pažní pleteně (PPP) je jedním z nejtěžších a nejvíce mutilujících úrazů. Díky pokrokům v chirurgických technikách lze úspěšného výkonu s částečným návratem funkce dosáhnout ve zhruba 60–80 % [1–3]. Ty nejsložitější případy však zůstávají těžko řešitelné a i při návratu motorické funkce nelze končetinu vrátit do původního stavu [4–6]. Postihuje typicky mladé muže v produktivním věku, má tedy závažný socio-ekonomický dopad [7,8]. Až 80 % pacientů navíc trpí bolestmi postižené končetiny [9]. Zájem o tuto problematiku nastal až koncem 70. let minulého století, kdy Millesi [10] a záhy nato Narakas [11] poprvé popsali funkční výsledky s využitím mikrochirurgických technik. Do té doby byla tato zranění považována za neřešitelná [12,13]. O další rozvoj se zasloužili Kline a Judice, kteří začali používat peroperační elektromyografické vyšetření [14].
S rozvojem operací u dospělých pacientů se později staly předmětem zájmu i perinatální PPP [15]. Ty jsou, co se týče diagnostiky i operačního řešení, mnohem komplikovanější. Jejich řešení však přináší také velmi dobré výsledky [16,17]. I přes tyto úspěchy, které jsou známy již více než 20 let, však stále zůstává velká část těchto zranění novorozenců neřešena zejména pro stále neuzavřená indikační kritéria.
Mechanizmus poranění a incidence
V případě avulzí a trakčních poranění je patofyziologickým mechanizmem poranění prudký náraz na oblast ramene (méně často tah za končetinu) s jeho rychlým odtažením od krku způsobený nejčastěji pádem z motocyklu či při zimních sportech [5,18,19]. Poranění plexus brachialis (PB) se vyskytuje asi u 5 % polytraumat po motocyklové nehodě, resp. v 3–4,8 % po pádu na lyžích či snowboardu [7]. U malých dětí je nejčastější příčinou traumatického PPP autonehoda, následuje sražení chodce autem [20]. Naprostá většina lézí jsou zavřená poranění, z nichž až 2/3 případů vyžadují operační léčbu [21]. Převládají kompletní léze, následované postižením pouze horních kořenů [17]. Celkový počet těchto diagnóz narůstá s lepšícími se resuscitačními technikami umožňujícími přežití většího množství pacientů po polytraumatech [4]. Lacerační (bodné rány) či střelná poranění jsou méně častá, tvoří maximálně pětinu všech operačně řešených případů [2]. Obecně mají lepší výsledky mladší pacienti [5].
Incidence perinatálního PPP je 1–2/1 000 živě narozených dětí [4,16,20,22,23]. Hlavními rizikovými faktory jsou velký plod (nad 4 000 g) a poloha koncem pánevním. Dalšími faktory mohou být obezita matky, použití porodních kleští a prolongovaný porod, naopak porod císařským řezem se zdá být protektivní [4,24]. Obecně vzniká postižení tahem za kořeny v průběhu porodu ramene při inklinaci hlavy na druhou stranu [25]. Předpokládá se, že část těchto zranění však vzniká již intrauterinně nebo samotným mechanizmem porodu, nikoli traumatickým postižením za porodu [26]. Proto se doporučuje používat obecnější termín „perinatální“ PPP spíše než „porodní“.
Diagnóza
Klinické vyšetření
- Syndrom horního PPP – obrna Erb-Duchennova (C5–6 ± C7) – postižení abdukce a zevní rotace ramene (m. supraspinatus, infraspinatus, teres minor, deltoideus), flexe v lokti (m. biceps brachii a brachialis) a supinace předloktí (m. biceps a supinator, obr. 1). Svalová síla se hodnotí pomocí svalového testu [27], resp. britského ekvivalentu Medical Research Council muscle grade score (MRC) [21].
Obr. 1. Addukce, vnitřní rotace, extenze a pronace levé horní končetiny při perinatální Erbově obrně. 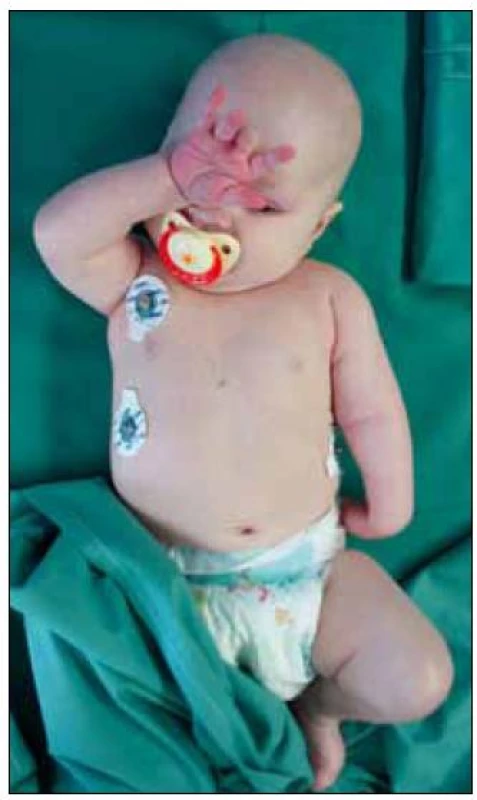
- Syndrom dolního PPP – obrna Déjerine-Klumpkeové (C8–Th1 ± C7) – postižení hybnosti ruky a předloktí v inervační zóně n. ulnaris a medianus – flexe zápěstí a prstů, dukce zápěstí a prstů, pronace předloktí.
- Kompletní léze PB (C5–Th1) – plegie celé končetiny a anestezie všech dermatomů vyjma vnitřní strany paže (z Th2).
- Obrna n. phrenicus (C3–5) – pokud je rozdíl v depresi poloviny bránice menší než dva mezižeberní prostory při porovnání expiračního a inspiračního RTG snímku,může odpovídat avulzi C4, ale také C5 [13].
- Tinelův příznak – lehký poklep na supraklavikulární oblast působící parestezie laterální plochy paže a event. i předloktí (C5) nebo ruky (C6) odpovídá až v 84 % ruptuře C5, pro diagnostiku avulze C6 má nízkou vypovídací hodnotu, u ostatních kořenů vyvolat nelze.
- Hornerův příznak – mióza, ptóza a enoftalmus vzniklé ztrátou sympatické inervace vycházející z C7, až v 90 % odpovídá avulzi jednoho nebo obou kořenů C8–Th1. Enoftalmus je většinou obtížně zjistitelný, ptóza časem odezní (díky hyperfunkci m. levator palpebrae superioris), mióza je však trvalá (obr. 2) [13].
Obr. 2. Hornerův syndrom vpravo – zjevná ptóza víčka a mióza. 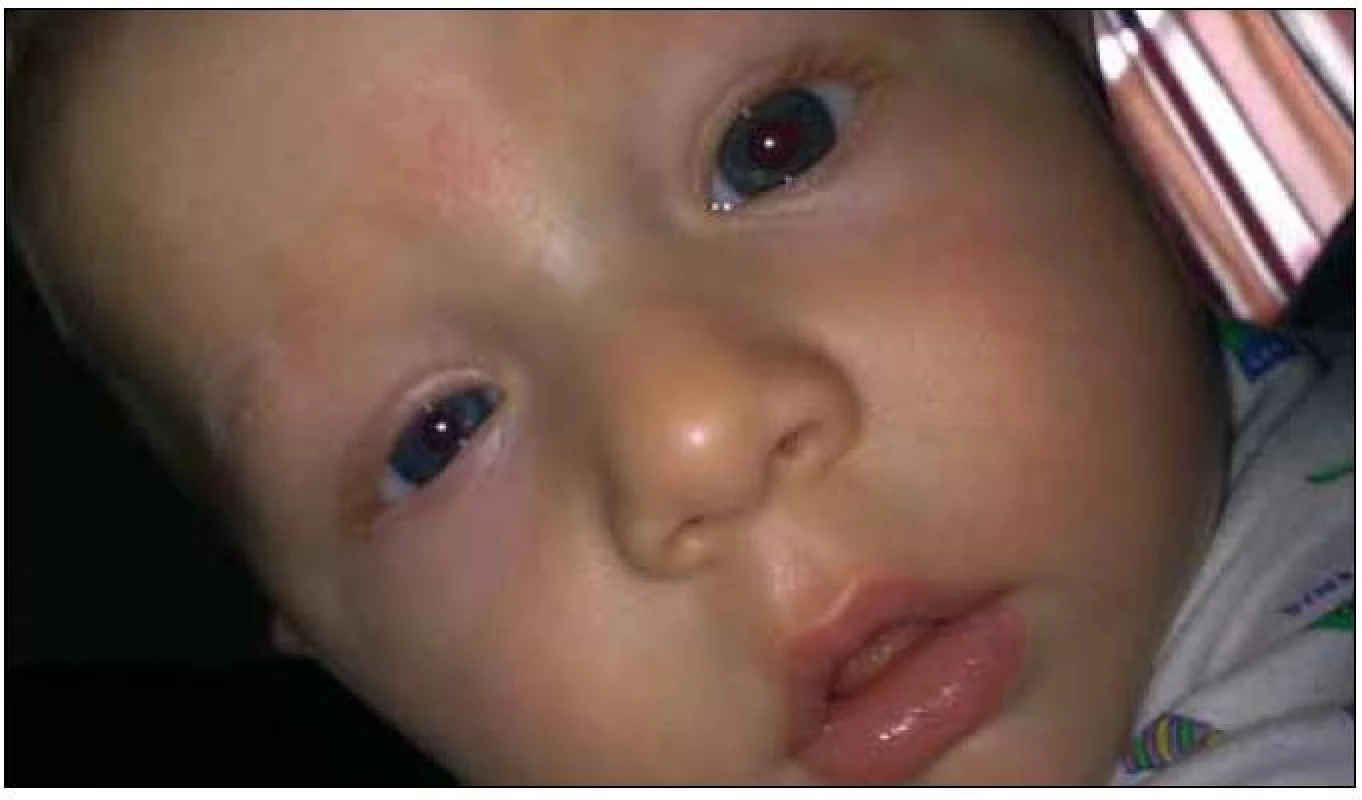
- Bolest ruky – trvalé nebo ojedinělé iritace akra charakteru řezání či pálení, obecně se uznává, že až v 90 % odpovídají avulzi některého z dolních kořenů. Bolest nevzniká v čase úrazu, ale typicky až po několika dnech [13]. Iritace v prvních fázích odeznívají s běžnými analgetiky. Jestliže bolest progreduje, je přítomna centrální komponenta (deaferentační bolest). Jedinou kauzální léčbou je v těchto situacích DREZ (Dorsal Root Entry Zone) termokoagulace [13,25,28–31].
Elektrofyziologické vyšetření
Základní metodou v diagnostice je jehlová EMG. Vyšetřují se jak postižené svaly, tak i svaly, jejichž nervy jsou zvažovány k odběru pro neurotizaci (např. m. pectoralis major, m. latissimus dorsi apod). V další linii stojí vyšetření senzitivního nervového akčního potenciálu (SNAP) ve formě neurogramů n. medianus a n. ulnaris ze stimulace I.–V. prstu obou rukou. Přítomný SNAP prokazuje zachovalý kontakt periferního nervu s mateřským neuronem ve spinálním gangliu – prokazuje tedy žádnou nebo supraganglionární lézi. Naopak jeho nevýbavnost ukazuje na přerušení nervu pod spinálním gangliem, jedná se tedy o lézi infraganglionární. Nevylučuje však současnou lézi supraganglionární. Peroperační elektromyografické vyšetření je popsáno v odstavcích o chirurgické léčbě.
Zobrazovací vyšetření
Průkaz vytržení kořene z míchy je kruciální pro management poranění. Prvním používaným vyšetřením byla prostá perimyelografie, v éře CT vyšetření získala vedoucí úlohu CT-perimyelografie (CT-PMG). Ačkoli má MR vyšetření obecně dominantní roli v diagnostice měkkotkáňových lézí, její výhodnost v případě avulze však zdaleka není tak jednoznačná. Senzitivita CT-PMG může při dobře provedeném vyšetření dosahovat až 95 % a specifita až 98 % (obr. 3). Obecně se soudí, že durální pseudocysty jsou známkou avulze. Neplatí to však absolutně. I při nálezu pseudocysty lze u některých pacientů sledovat na CT-PMG probíhající filla radicularia. Běžné metody používané v rámci MR vyšetření byly zklamáním, vypovídací hodnota činila asi 52 % [32].
Obr. 3. CT-PMG – šipka ukazuje na chybějící kořeny C6 a laterální deviaci durálního vaku vpravo, vlevo zřetelně viditelný přední i zadní kořen. 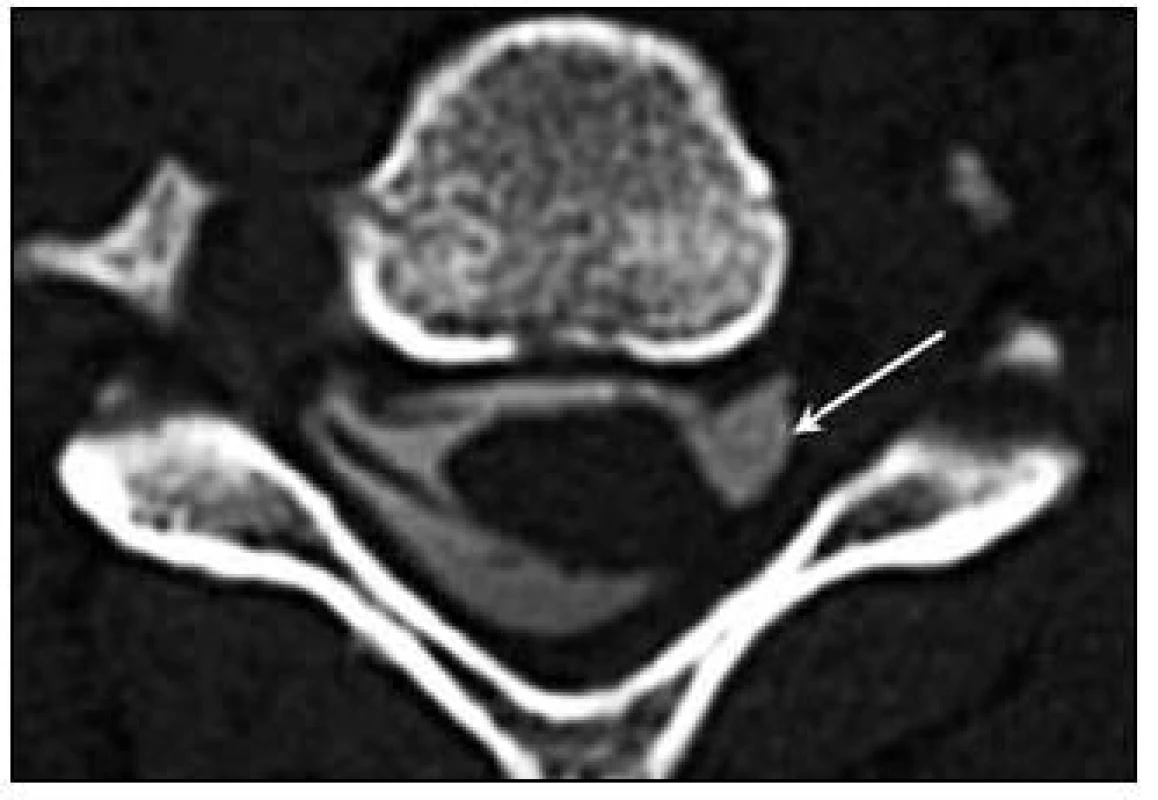
Léčba
Načasování rekonstrukčního výkonu
Otevřená poranění
Načasování operačního výkonu se i zde řídí obecnými postupy při poranění periferních nervů. Akutní výkon je prováděn pouze při otevřeném ostrém poranění (bodné či řezné rány) s revizí rány, zástavou případného krvácení a rekonstrukcí přerušených částí PB. Zpoždění v případě ostrých poranění nervů obecně vedou k retrakci obou pahýlů a zbytečné potřebě štěpování s horšími výsledky. Pokud nejsou známky tepenného krvácení a v ráně nejsou přítomna cizí tělesa, lze revizi provést do 72 hodin, kdy je ještě stimulovatelný distální úsek nervu. Otevřené tržné či střelné rány (silně znečištěná či ztrátová poranění) jsou akutně ošetřeny pouze základně (vyčištění rány, zástava krvácení či rekonstrukce velkých cév, označení konců nervových elementů či jejich hrubé přiblížení k zabránění retrakce). Revize je prováděna za cca tři týdny, kdy jsou již zjevně patrné výsledky trakčního poranění. Elementy jsou seřezány až do zdravě vyhlížející fascikulární struktury a poté jsou propojeny štěpy. Pokud toto není možné, přistoupí se k neurotizaci. Tvorba jizvy však činí revizi velmi nesnadnou [19,23].
Zavřená poranění
Zcela jiný je ale postup u zavřených poranění – vzhledem k časté neurapraxii, kdy se stav upraví, je operováno pouze 50–60 % pacientů. První EMG vyšetření má smysl při zjevné poruše hybnosti až po třech týdnech od úrazu, kdy odezní případná neurapraxie. Vypovídací hodnotu má však až vyšetření provedené tři měsíce po úrazu, které potvrdí víceméně definitivní stav. Dříve nemá smysl, podobně jako u jiných zavřených poranění končetinových nervů, operaci provádět. Do té doby je nutná co nejintenzivnější rehabilitace a elektrostimulace denervovaných svalů [3,23,33]. V případě nálezu regenerace ve všech hlavních svalech není operace indikována a pacient je nadále dispenzarizován. Pokud je u některého ze zvažovaných dárcovských nervů zjištěn v této době regenerační akční potenciál, lze měsíc počkat k jeho případné úpravě. Pro reinervaci lze použít i dárcovské nervy, u kterých byl v korespondujících svalech nalezen částečný denervační syndrom. Nebyla zjištěna statisticky signifikantní závislost mezi poškozením dárcovského nervu a výsledkem reinervace [3]. Pro rozlišení pre - a postganglionární léze se EMG doplňuje o vyšetření SNAP, kdy jeho výbavnost ukazuje na avulzi (preganglionární léze), nevýbavnost naopak na rupturu za spinálním gangliem [34]. Po první návštěvě je navíc naplánováno CT-PMG vyšetření k průkazu avulze krčních kořenů. Toto je ideální scénář, bohužel se stále setkáváme s případy, kdy se pacienti dostaví se značným zpožděním, někdy i více než rok po úrazu. Jak z experimentálních, tak i klinických studií však jasně vyplývá, že operace prováděné mezi třetím a šestým měsícem po úrazu mají nejlepší výsledky [2,3,7,12,19,35–37]. Po osmém měsíci je šance na zdárný výsledek velmi malá, takový výkon lze obhájit jen u mladého člověka [7].
Perinatální poranění
80–90 % případů postihuje pouze horní kmen a upraví se spontánně, resp. konzervativní léčbou. Zbylých 10–20 % je postiženo neurotmezí s vytvořením neuromu v kontinuitě nebo avulzí a zaslouží si mikrochirurgickou revizi [4,24]. Avšak i u těch nálezů, které se na první pohled spontánně upraví, je až ve 20–30 % přítomno reziduální postižení, nejčastěji opožděná či snížená reinervace extenzorů a zevních rotátorů paže vedoucí k deformitám končetiny během růstu [4,22]. Na základě dostupných studií lze udělat pouze dva jednoznačné závěry: kompletní léze s Hornerovým syndromem jsou jednoznačně indikovány k mikrochirurgické revizi, naopak pro děti s lehkým poraněním, které se upraví do jednoho měsíce, je lepší konzervativní léčba [20,24,38–40]. Indikační kritéria v případě Erbovy obrny jsou však stále kontroverzní. Jako nejpřijatelnější se zdá být doporučení Chuanga et al, kteří indikují k časné revizi do tří měsíců děti s obrnou ruky. Při trvající poruše pouze proximálního svalstva lze operaci provést v šesti měsících [41,42].
Jiná situace je v případě kompletního PPP. V 90. letech došlo ke změně strategie, která byla do té doby stejná jako u dospělých pacientů, tj. obnova abdukce ramene a flexe lokte. V současné době je hlavní důraz kladen na obnovu inervace ruky. Senzitivita ruky totiž zabraňuje rozvoji končetinového neglect syndromu a sebemutilace. Obnova proximální hybnosti totiž sama o sobě nevede k zapojení končetiny do bimanuální činnosti [16]. Flexe lokte je tak na druhém místě, teprve na třetím místě je snaha o obnovu abdukce ramene [43]. V případě indikace k revizi je nutno počítat s obětováním případné částečně obnovené hybnosti ramene a lokte k rekonstrukci PB jako celku [20]. V našem souboru jsme z jednoho či několika zachovalých kořenů (zejména horních) opakovaně funkčně reinervovali celou pažní pleteň (obr. 4).
Obr. 4. 1 – Rekonstrukce fasciculus lateralis a částečně i posterior navazujících na C5–6 z kořene C4 (bez štěpu, kořen přeťat pod odstupem n. phrenicus. 1, 2 – fasc. medialis a zbytku fasc. posterior navazujících na kořeny C6–Th1 pomocí čtyř štěpů (2,5 cm) z kořene C5. Klinický výsledek obr. 12. 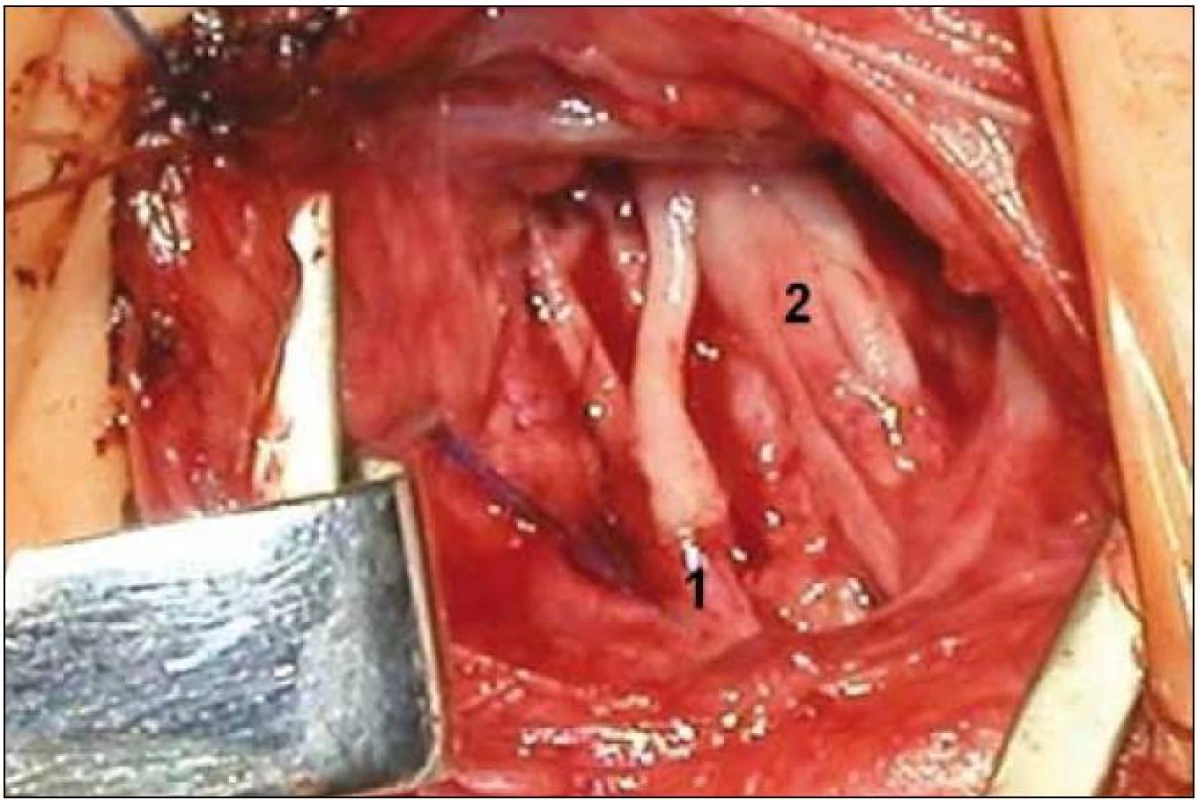
Indikační kritéria a načasování operace shrnuje tab. 1.
Tab. 1. Načasování operačního řešení u jednotlivých typů poranění plexus brachialis. Primární ošetření – sutura měkkých tkání, případně akutní cévní nebo ortopedický výkon. 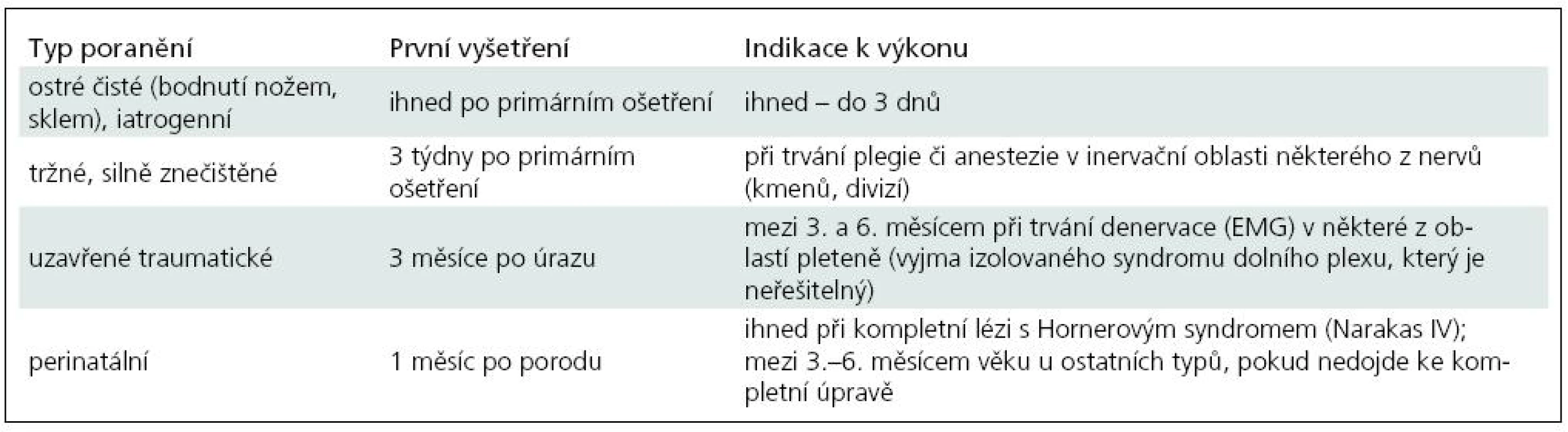
Rekonstrukční metody
Přímá sutura a rekonstrukce pomocí štěpů
Zatímco preganglionární lézi lze řešit pouze neurotizací, v případě ruptury elementů PB je situace složitější. První fází supraklavikulární revize je explorace všech částí PB včetně foraminální úrovně. Po exoneurolýze nervových struktur je provedena motorická evokovaná stimulace k průkazu míry zachovalé inervace ve všech kořenech – kontrakce svalů se sledují přímo, případně je provedena jehlová elektromyografie. Dále je prováděno vyšetření NAP: při dobře výbavných rychlých kondukčních časech bez distální odpovědi se jedná o preganglionární lézi, kterou nelze z tohoto přístupu rekonstruovat. Menší, pomalejší odpověď představuje průchodnost, zachovanou vodivost; neurolýza je tedy adekvátní léčebný postup. Při žádné odpovědi se může jednat o postganglionární (přímo rekonstruovatelnou) nebo kombinovanou pre-postganglionární lézi. Obecně je v těchto případech možno vytnout neurom v kontinuitě se salámovým seřezáváním konců nervů do zdravé tkáně s viditelnými fascikly a následný defekt vyplnit štěpem [2,3,12,17,23,44]. Při nálezu přerušených částí (kořeny, kmeny) je po obnažení konců až do zdravé tkáně provedena buď přímá sutura, většinou je však třeba vlivem retrakce obou konců přistoupit k rekonstrukci pomocí štěpů. Nejčastěji se využívá n. suralis (obr. 5), denervovaný n. cutaneus antebrachii medialis, případně lze u jisté avulze dolních kořenů využít vaskularizovaný denervovaný n. ulnaris (obr. 6) [36]. V případě velmi dlouhých poranění není možné PB rekonstruovat kvůli nedostatku dárců pro přemostění defektu. Vzhledem k velkému množství možností, které mohou při úrazu nastat, nelze stanovit jednotný návod, jak postupovat. Zásadní při propojování proximální části PB s jednotlivými funkčně důležitými příjemci je nalezení přesného místa, ze kterého vyrůstají axony pro daný sval. Žádná podobná studie však nebyla provedena. Pokud je štěp proximálně našit na oblast pro jiný nerv, jedná se v podstatě opět o neurotizaci, která však zbytečně ztrácí svůj potenciál pro přílišnou vzdálenost od cílového svalu. Při našití na oblast senzorických vláken ztrácí sutura zcela smysl [45]. Ke konstituci senzorických a motorických fasciklů dochází až na úrovni nervů. To ztěžuje výsledek štěpování na úrovni PB pro větší pravděpodobnost chybné reinervace [13]. Někteří autoři doporučují lézi PB překlenout štěpem vždy mezi proximálním pahýlem a jednotlivými nervy [46]. Obecně mají supraklavikulární poranění horší prognózu než infraklavikulární [7].
Obr. 5. Rekonstrukce kořenů C5 a C6 šesti 3,5 cm dlouhými štěpy z n. suralis. 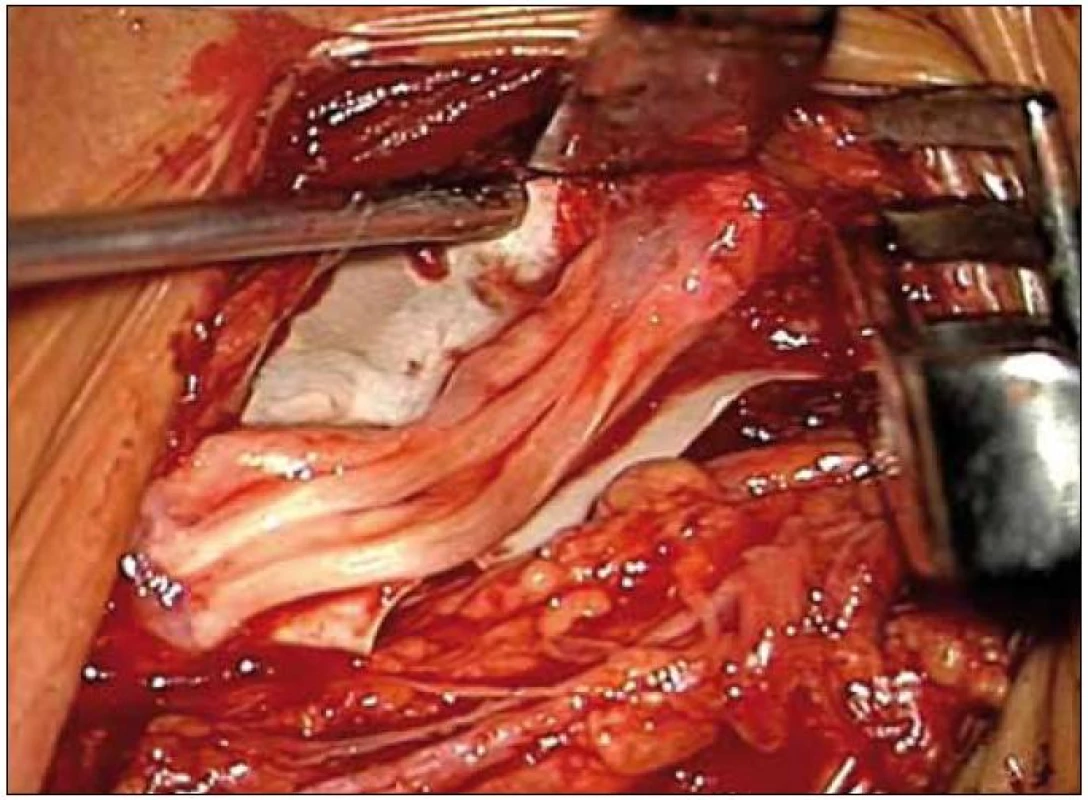
Obr. 6. Sutura n. musculocutaneus (MC) na kořen C5 pomocí vaskularizovaného štěpu z n. ulnaris (U) při avulzi dolních kořenů. A – n. ulnaris s cévní stopkou (1), B – stav po sutuře štěpu na n. musculocutaneus (MC) (2), M – n. medianus. 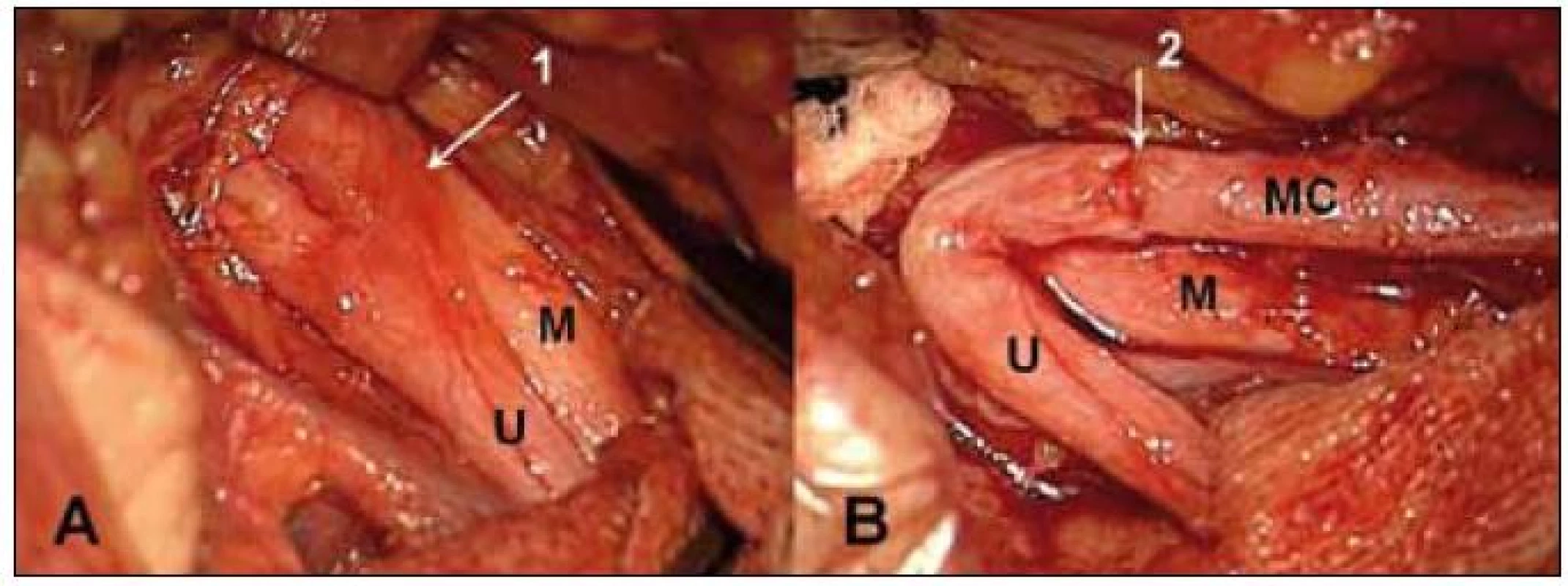
Neurotizace
Neurotizace (tzv. zkřížená rekonstrukce) je metoda využívající jako zdroj axonů intaktní nerv (tzv. dárce, funkčně méně významný) v případech, kdy je původní zdroj nedostupný (avulze kořenů nebo težké ztrátové poranění proximálního pahýlu). Provádí se většinou z infraklavikulárního přístupu. Výjimkou je neurotizace n. suprascapularis pomocí n. XI, která se provádí z přístupu nad klíční kostí. Dárce je přerušen a jeho proximální pahýl našit na distální pahýl rekonstruovaného nervu (tzv. příjemce). První zmínka pochází od Harrise a Lowa z roku 1903. Ti se pokusili napojit přerušený kořen C5 na intaktní C6 [47]. První extraplexální výkon popsal Tuttle v roce 1913. Ten vyzkoušel reinervaci horního kmene plexus brachialis pomocí plexus cervicalis [48]. Hlavní výhoda je možnost co nejdistálnější sutury se zkrácením regenerační doby, což je umocněno nepotřebností štěpu. I přes nutnost reorganizace motorické kůry s sebou tento postup přináší velmi dobré výsledky [3,13,35,49]. K neurotizaci lze využít intraplexální (z vlastního PB, obr. 7) a extraplexální nervy (mimo PB), ztráta funkce určitého svalu z obětování jeho nervu musí být vždy převážena očekávaným výsledkem. Úspěšnost při využití nervů z vlastního PB je obecně větší – jednak mají vyšší počet motorických axonů, jednak je jednodušší proces reorganizace mozkové kůry [3,4,36].
Obr. 7. Neurotizace n. musculocutaneus třemi větvemi nn. pectorales. 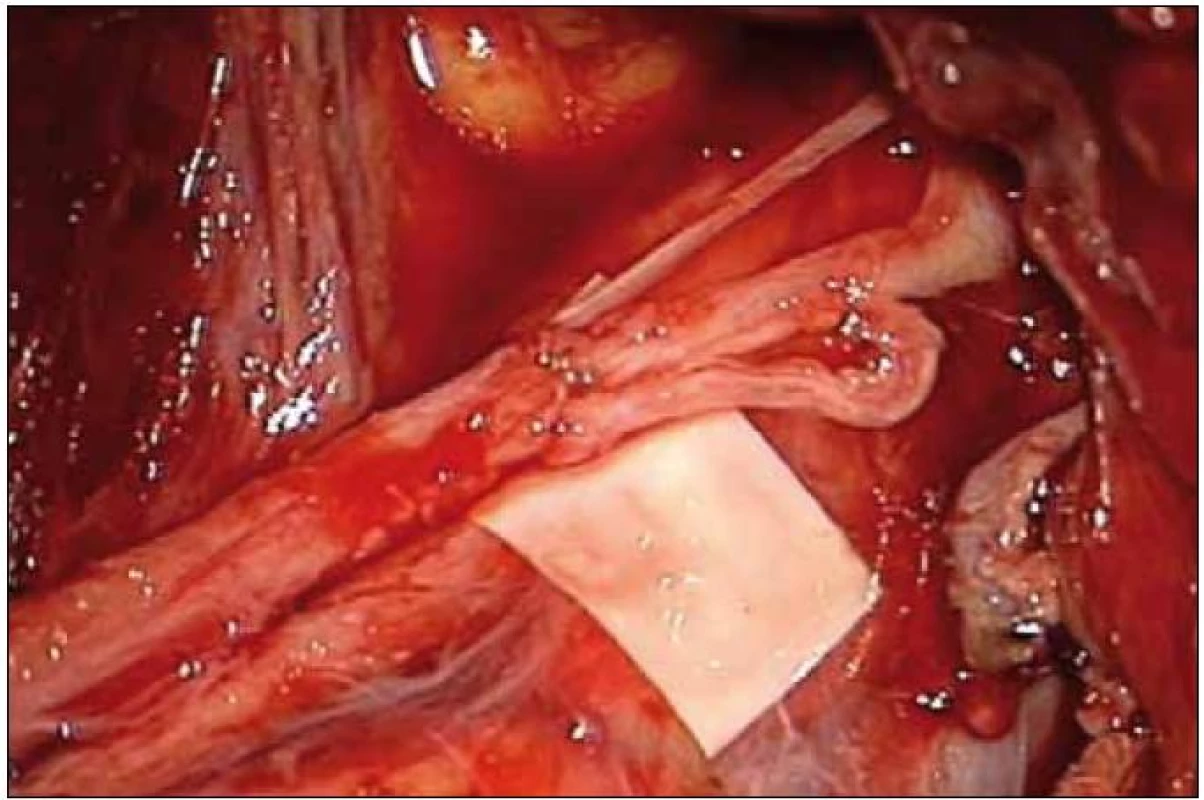
Intraplexální dárci
- Nervi pectorales – medialis (C8–Th1) a lateralis (C5–7), někdy je místo dvou větví přítomna tzv. pektorální pleteň. Někteří autoři jejich použití odmítají pro možnost ztráty addukce, která je u paretické končetiny o to důležitější – přidržení předmětu v podpaží. Tento výpadek se projeví zvláště tehdy, je-li poškozený nebo využitý n. thoracodorsalis [50]. Odběr n. pectoralis medialis, resp. dvou až tří konečných větví v případě přítomnosti pleteně, je tedy možný zejména u čistého syndromu horního plexu, kdy zůstává laterální část intaktní [36].
- N. dorsalis scapulae (C5, částečně C4 a C6) – inervuje mm. rhomboidei a částečně i levator scapulae. Výsledky nejsou příliš dobré [51].
- N. thoracodorsalis (C6–8) – používá se zejména k rekonstrukci n. axillaris. Výsledky jsou velmi dobré i přes možné riziko vývoje nestabilní lopatky [3,52,53].
- N. thoracicus longus (C5–7) – k neurotizaci lze použít jeho horní větev [13], výjimečně i celý nerv, zde však hrozí riziko nestabilní lopatky s nemožností rozsáhlejší abdukce paže, i když n. axillaris zdárně reinervoval.
- Větve n. radialis pro m. triceps (C5––Th1) – bylo popsáno využití každé z větví pro obnovu n. axillaris, nejčastěji je se uvádí použití větve pro dlouhou hlavu [36,45].
Extraplexální dárci
- Nervi intercostales – současný konsenzus je použití tří nervů. Největší počet motorických axonů obsahují III.–IV. nerv [19]. Ventilační potíže nebyly po odběru zaznamenány (pokud není současně odebírán i n. phrenicus). Kontraindikací je sériová stejnostranná fraktura žeber. Komplikací mohou být svalové synkinézy při respiraci [4,12,36]. Ty však většinou mizí zhruba dva roky po operaci, objevit se ale mohou během kašle a kýchnutí [19].
- Ramus externus nervi accessorii (n. XI) – při svém průběhu vydává 2–3 větve pro trapézový sval a poté běží jako konečná větev inervující dolní část svalu. Odebírá se tedy tato jeho zevní větev, a m. trapezius tak není po odběru denervován. V současné době většina chirurgů uznává jeho dominantní roli při neurotizaci n. suprascapularis [19,36,45,51,52].
- Kontralaterální kořen C7 – kořen je pomocí volného či vaskularizovaného štěpu prodloužen na poraněnou stranu a využit k rekonstrukci dolních elementů PB. Odběr je založen na faktu, že všechny svaly inervované z C7 mají další inervaci i z C6 a C8. Technika je racionálně použitelná pro svoji komplikovanost pouze u kompletního PPP s nedostatkem dárců, v dnešní době zůstává spíše v pozadí, i když může mít dobré výsledky [13].
- Plexus cervicalis – využívá se napojení na C5(6), výsledky však nejsou povzbudivé, snad pro velmi variabilní, ale obecně nízký počet motorických axonů (vyjma n. phrenicus). Rizikem je vývoj nestabilní lopatky, zejména při současném odběru n. XI [12,51]. V našem souboru byla tato technika úspěšná v 50 % [3]. Většina autorů tuto metodu v současné době nevyužívá [19,36]. Ramus ventralis C4 je však velmi dobře využitelný u perinatálních PPP k rekonstrukci jiných kořenů.
- N. phrenicus (C4, částečně C3 a C5) – opakovaně byla prokázána bezpečnost jeho odběru. Po jeho přerušení se sice většinou vyvine hemidiafragmatická plegie [54], ta však nepůsobí respirační obtíže a funkce se normalizují za 6–24 měsíců (výjimkou jsou staří pacienti, pacienti s plicním onemocněním a kuřáci či současný odběr mezižeberních nervů). Před odběrem však musí být vždy stav bránice a respirační funkce vyšetřeny, při jejich postižení je jeho použití jednoznačně kontraindikováno, stejně jako odběr u dětí (poporodní hemiparalýza bránice vede k častějším a těžším plicním infekcím) a současný odběr mezižeberních nervů [19].
- N. hypoglossus (n. XII) – výsledky při neurotizaci jsou špatné, ke kontrakci je navíc nutný pohyb jazyka, a i když dojde k reorganizaci kůry, přetrvávají synkinézy při žvýkání [19,54,55]. Technika byla v této indikaci víceméně opuštěna.
Oberlinova technika
Roku 1994 Oberlin et al popsali metodu distální neurotizace, kdy provedli transfer motorického fasciklu n. ulnaris pro m. flexor carpi ulnaris na n. musculocutaneus. Technika vzbudila ohlas pro své excelentní výsledky, protože u všech čtyř operovaných pacientů došlo k obnovení flexe v lokti za méně než šest měsíců [18], což lze vysvětlit velmi distální suturou (obr. 8). V roce 2001 využili Songcharoen et al obdobný postup u n. medianus se získáním fasciklu pro m. pronator teres a m. flexor carpi radialis, ačkoli panovala obava, že výsledky budou horší díky narušení části vláken n. medianus při poranění horní úrovně PB [56]. To se však nepotvrdilo a výsledky se zdají být obdobné [46,57]. Technicky je operace navíc jednodušší (n. medianus je tlustší a je blíže cíli) a je zde umožněn bezpečnější odběr dvou motorických fasciklů, což může zlepšit výsledek výkonu [46]. Oberlinova technika je využitelná při poranění horních kořenů, ale pouze při intaktním dárcovském nervu (normální hybnost ruky). Fascikl je po otevření epineuria daného nervu v horní třetině paže vyhledán elektrickou stimulací (0,3–0,5 mA), přičemž se sleduje kontrakce sledovaného svalu. Fascikl je následně přeťat a jeho proximální pahýl uvolněn v délce několika cm. Pro využití přednosti distální sutury je poté tento pahýl našit perineurální technikou na větev pro m. biceps brachii před jejím vstupem do svalu, nikoli na kmen n. musculocutaneus. Jako komplikace výkonu byly popsány dočasné poruchy citlivosti a výjimečně i motorické postižení v inervační zóně nervu. V našem souboru 14 pacientů jsme poruchu hybnosti nezaznamenali. Oberlinovu techniku jsme u 12 pacientů využili k reinervaci n. axillaris. Celková úspěšnost byla téměř 78 %. Pro reinervaci n. axillaris jsme tuto techniku aplikovali poprvé. Je tedy patrné, že Oberlinova technika může být úspěšně použita i pro reinervaci tohoto nervu.
Obr. 8. Oberlinova technika – napojení fasciklu z n. ulnaris (1) na n. axillaris (2). 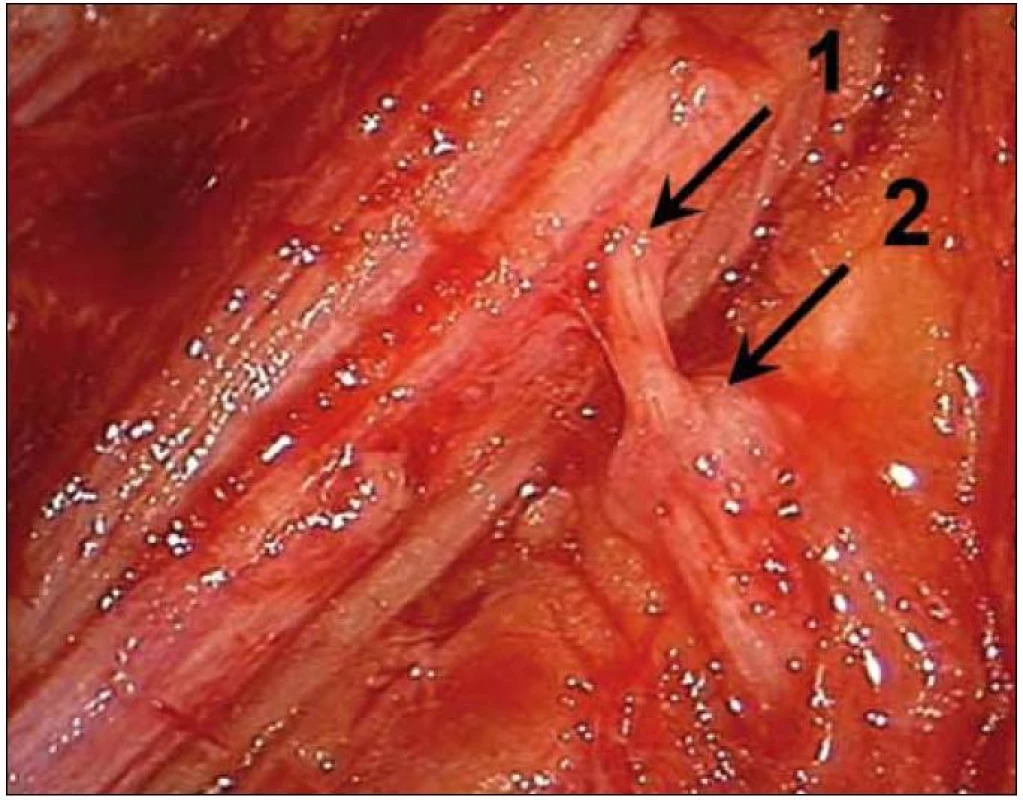
End-to-side anastomóza
Poprvé ji popsali Kennedy et al v roce 1901 jako pokus o reinervaci poraněného n. facialis z n. XII [58]. Vzhledem ke špatným výsledkům byla ETS metoda na téměř 90 let zapomenuta, až roku 1992 Viterbo et al dosáhli dobrých výsledků na zvířecích modelech [59]. Principem techniky je napojení distálního pahýlu poškozeného nervu ke straně intaktního dárcovského nervu v případě end-to-side (obr. 9). Využívá se v situaci, kdy je nedostatek dárců pro klasickou neurotizaci. Na buněčné úrovni je úspěšnost založena na poznatku, že kromě terminálního větvení jsou axony schopny dělení i ve svém průběhu – kolaterální větvení (collateral sprouting) [35,60].
Obr. 9. End-to-side anastomóza – laterální sutura n. axillaris (v pinzetě) na n. ulnaris (šipka). 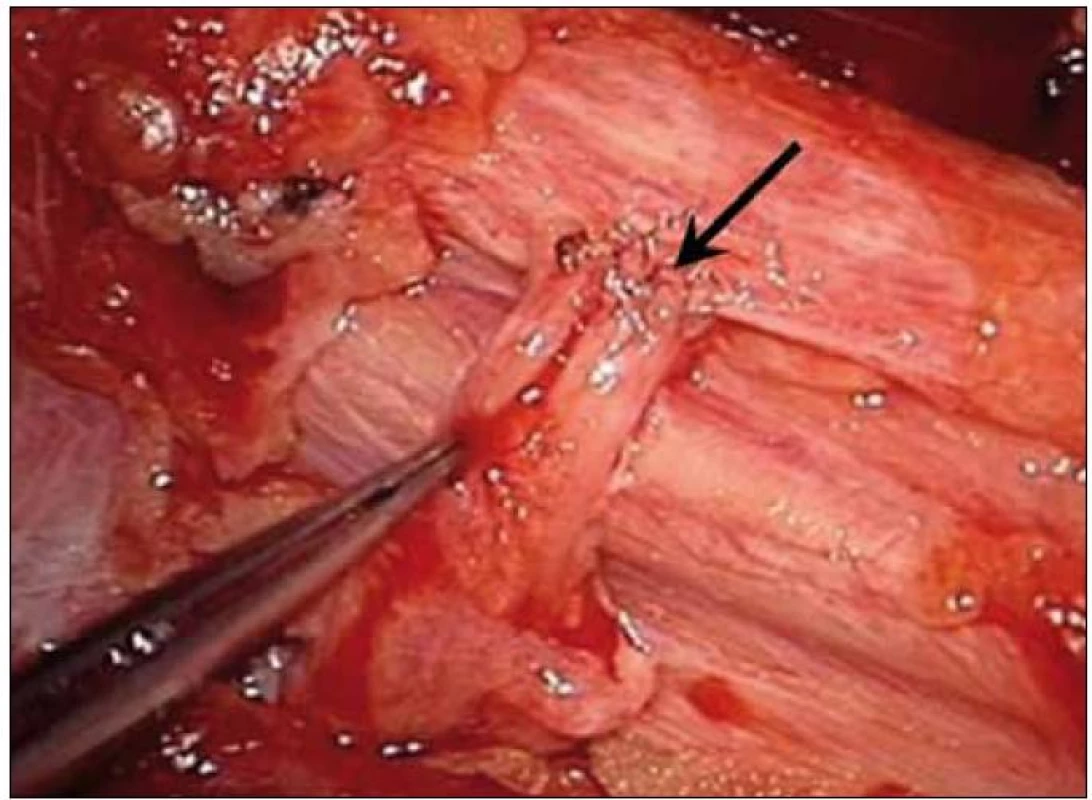
Většina literárních údajů o využití ETS v klinické praxi jsou soubory několika pacientů nebo kazuistiky [61–64]. V souhrnné publikaci hodnotící úspěšnost všech používaných metod při řešení PPP u pacientů z našeho pracoviště bylo publikováno použití ETS anastomózy pro reinervaci poraněné pažní pleteně [3]. Celková úspěšnost dosahuje 43,5 %, což reálně odpovídá obecnému pohledu na tuto techniku [63].
V experimentálním modelu byla svalová síla dosažena pomocí ETS spojení 60–70 % ve srovnání s druhou, zdravou stranou [65] a 70 % ve srovnání s end--to-end spojením [66]. V klinické praxi je k úspěšné reinervaci u proximálních poranění nutné vytvoření perineurálního okna (Haninec et al, připraveno k publikaci) [60,61,63,67–69]. Provedení epi - nebo perineurálního okna nevede k funkčnímu deficitu v inervační oblasti dárcovského nervu [61,67,70–72].
Alternativní metody
- Replantace vytržených kořenů do míchy – ačkoli bylo provedeno několik víceméně úspěšných studií, metoda není uznána jako alternativa tradičních technik. K reinervaci může dojít, stav má však jednu zásadní nevýhodu: nikdy nedojde k vytvoření specifických drah k určitému svalu. Axonální struktura v periferii je značně neuspořádaná, což má za následek vzájemnou reinervaci nejen různých svalů, ale hlavně agonistů a antagonistů. To v klinickém obraze vede k synkinézám [73,74].
- Využití volných svalových laloků a šlachových transferů – volný svalový lalok lze použít v případě starých neurotraumat či při neúspěchu předchozí rekonstrukce nervů. Nový sval v podstatě nahradí sekundárně změněný sval původní a je třeba jej neurotizovat podle obecných pravidel. Jako nejlepší se jeví m. gracilis – je snadno dosažitelný, dostatečně dlouhý a má proximálně lokalizovaný neurovaskulární pedikl. Nejčastěji se využívá k obnově flexe lokte [75,76].
Šlachové a svalové transfery: pro obnovení flexe prstů je možno použít transfer m. brachialis k našití na flexory předloktí, pro obnovu extenze prstů buď stejný sval nebo m. pronator teres našitý na extenzory [8,13], nejčastěji se však provádí transfer šlachy m. flexor carpi ulnaris na šlachy extenzorů [77]. K obnovení zevní rotace paže slouží L’Episcopův transfer společné šlachy m. latissimus dorsi a teres major z crista tuberculi minoris na crista tuberculi majoris. Steindlerova metoda se využívá k navrácení flexe lokte u pacientů se zachovalou akrální hybností – oddělený zevní epikondyl humeru s úponem flexorů předloktí je fixován na hranici dolní a střední třetiny humeru [8]. Stejnou funkci může obnovit i přenos úponové šlachy caput longum m. triceps brachii [8,78] či přenos stopkatého m. latissimus dorsi na m. biceps [79].
Cíle operace
V případě horních a kompletních PPP jsou flexe v lokti a abdukce ramene nejdůležitějšími pohyby horní končetiny pro její alespoň částečné využití. U kompletních PPP je tedy obnova těchto pohybů na prvním místě, resp. největší důraz je kladen na obnovení n. musculocutaneus [2,4,17,57]. Pro většinu všedních aktivit je dostatečná plná flexe lokte, abdukce ramene do 90° a zevní rotace paže do 110° [13].
Abdukce ramene je komplikovaný pohyb sestávající ze tří fází – za prvních 30–45° je zodpovědný samotný m. supraspinatus, dalších 45° provádí samotný m. deltoideus. Pohyb nad 90° je vykonáván společnou aktivitou m. deltoideus a m. serratus anterior, který umožňuje anterolaterální rotaci lopatky kolem hrudníku [45]. Při nedostatku dárců je jako první nutno vždy rekonstruovat n. suprascapularis – m. supraspinatus nejenže abdukci iniciuje, ale u některých pacientů vytvoří i bez funkčního deltového svalu dostatečně silný pohyb, který je dobře využitelný pro běžnou funkci končetiny [12,19,26,36]. Nejlepších výsledků je však samozřejmě dosaženo při rekonstrukci obou nervů [51].
U perinatálních PPP je, jak už bylo uvedeno, situace stejná pouze u horního typu poranění pažní pleteně. V případě kompletních PPP je na prvním místě snaha o obnovení hybnosti ruky. Flexe lokte je tak na druhém místě, teprve na třetím místě je snaha o obnovu abdukce ramene. Na rozdíl od PPP dospělých pacientů je tedy aktivně přistupováno i k izolované obrně dolního typu s rekonstrukcí dolních elementů PB [43].
Obnova flexe v lokti – n. musculocutaneus (m. biceps brachii a m. brachialis)
Úspěšná reinervace může být dosažena v případě využití mezižeberních nervů v 44–70 % [2–4,50,80–82], n. XI v 50–88 % (i přes nutnost využití štěpu), n. phrenicus v 66–100 % [4,19,36], n. pectoralis medialis v 84–91 % [2,3,36,52]. Většina autorů preferuje použití mezižeberních nervů, ačkoliv pektorální nervy mají výrazně lepší výsledky. Byla také prokázána větší úspěšnost při použití n. XI, ten je však rezervován pro obnovu n. suprascapularis [3,36]. Při využití Oberlinovy techniky je návrat funkce očekávatelný v 90–100 % případů (z n. ulnaris, obr. 10), resp. u 64–80 % pacientů při využití n. medianus. Podmínkou je však zachování funkce dolního PB [19,36,50,83]. Zlepšení výsledků lze dosáhnout využitím axonů regenerovaných do n. cutaneus antebrachii lateralis buď jeho zanořením do m. biceps, nebo napojením na větev pro m. brachialis [19].
Obr. 10. Pacient 14 měsíců po rekonstrukci n. musculocutaneus Oberlinovou technikou z n. ulnaris vpravo. 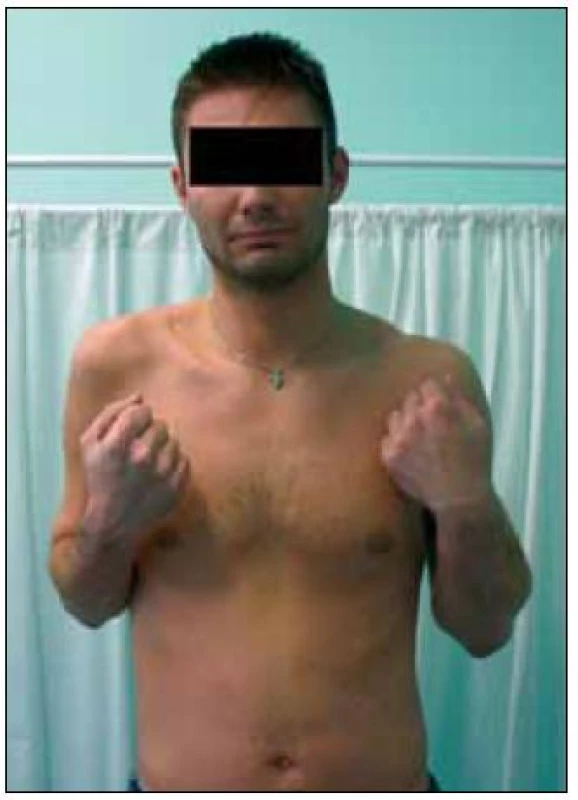
Obnova abdukce v rameni – n. suprascapularis (m. supraspinatus)
Panuje jednotný názor, že nejlepší volbou pro neurotizaci je blízký n. XI, při jehož použití je funkční reinervace dosaženo v 79–95 % (platí pro m. supraspinatus, reinervace m. infraspinatus je oslabena pravděpodobně pro delší vzdálenost cíle a dosahuje asi 50 %) [2,19,45,52]. Při použití n. phrenicus lze úspěch očekávat až v 75 % bez potřeby štěpu [19].
Obnova abdukce v rameni nad 30° – n. axillaris (m. deltoideus)
Dobrý funkční výsledek může být dosažen v případě použití n. XI v 60 %, n. phrenicus v 66 % [21], mezižeberních nervů v 33–67 % [3,51,82], n. thoracodorsalis v 36–93 % (obr. 11) [3,52,53], n. thoracicus longus v 64 % [3] či kontralaterálního kořene C7 až v 52 % [83]. V poslední době se využívá neurotizace pomocí některé z větví n. radialis pro m. triceps [19,36]. V našem souboru máme dobré zkušenosti i s Oberlinovou technikou, pomocí níž se abdukce obnovila u 78 % pacientů, end-to-side anastomóza měla efekt nižší – 48 % (publikace v přípravě).
Obr. 11. Pacient 30 měsíců po neurotizaci n. axillaris z n. thoracodorsalis a n. musculocutaneus z nn. pectorales vlevo. 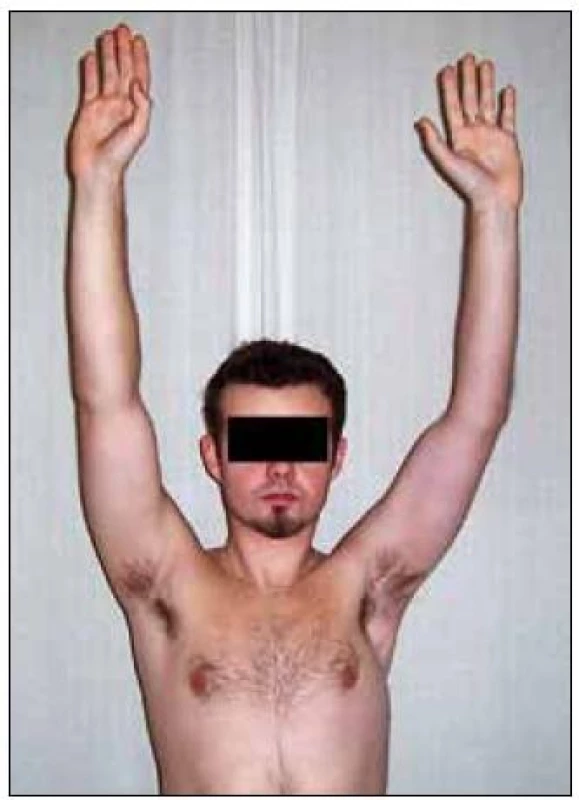
Obnova extenze paže a předloktí – n. radialis
Obrna n. radialis vzniklá v rámci PPP je většinou neřešitelná kvůli velmi dlouhé reinervační dráze (vyjma m. triceps, který však standardně není neurotizován pro jeho relativně malou důležitost v případě těžkých PPP – končetina totiž do extenze „padá“ spontánně) [3]. Stav je tedy většinou řešen sekundárně pomocí šlachových transpozicí.
Doporučené návody na řešení jednotlivých stavů
Snad pro velkou rozmanitost této problematiky, kdy se těžko hledají dva naprosto srovnatelní pacienti [8], nebyla do dnešní doby provedena žádná randomizovaná studie, která by srovnávala byť jen dvě různé metody používané v rámci rekonstrukce PB. I když jsou veškeré dostupné práce pouhými retrospektivními studiemi, resp. soubory kazuistik, lze na jejich základě alespoň u některých poranění odvodit nějaké návody, jak postupovat [84].
Poranění C5–6
Pokud není možná rekonstrukce kořenů (avulze), potom se jako metoda volby jeví neurotizace n. suprascapularis pomocí n. XI, n. axillaris pomocí n. thoracodorsalis [3], Oberlinovou technikou (naše nepublikovaná data) nebo větví pro dlouhou hlavu m. triceps (zatím neverifikováno dlouhodobými výsledky na větších souborech) [19] a pro obnovení flexe v lokti Oberlinova technika z n. ulnaris či medianus [13,36] nebo neurotizace n. musculocutaneus z n. pectoralis medialis [3,85]. Obecně mají lepší výsledky intraplexální dárci než zdroje mimo PB [3].
Poranění C5–7
Postup je stejný jako u předchozího typu, pokud je však n. radialis postižen (m. triceps je slabý), k neurotizaci n. axillaris je použit jiný dárce [13]. Postižený n. radialis na předloktí lze neurotizovat větvemi z n. medianus a ulnaris. Může být využita také transpozice m. flexor carpi ulnaris na m. extensor digitorum.
Poranění C8–Th1
Tento typ léze má při použití tradičních technik (sutura při lézi distálních elementů PB, neurotizace při avulzi) velmi špatnou prognózu [2,3]. Při zachování n. radialis lze využít transfer jeho větví (pro m. triceps a m. supinator). Pokud není dostupný, pak lze provést sekundární zákroky – svalové či šlachové transpozice [13].
Kompletní léze C5–Th1
Opět lze využít neurotizace n. suprascapularis pomocí n. XI, dále ramus ventralis C4, resp. mezižeberní nervy. Vždy je však nutné s jistotou potvrdit avulzi C5–6, které lze v případě jejich častější ruptury rekonstruovat [36]. Bertelli et al udávají jako dobrý výsledek 30° externí rotaci, 40° abdukci a zachovalou addukci paže a 45° flexi v lokti. Až u 80 % kompletních lézí bývá zachován některý z kořenů, nejčastěji C5. Ten tedy může být prodloužen štěpem na laterální svazek (flexe v lokti) a zbylé nervy neurotizovány pomocí n. XI a mezižeberních nervů [13].
Pooperační období
Končetina je imobilizována na šátku po dobu tří týdnů, poté je nutná intenzivní každodenní rehabilitace a elektrostimulace denervovaných svalů [3,12]. Nervová poranění, zvláště proximální, mají zásadní nevýhodu v tom, že se první výsledky začínají objevovat po relativně dlouhé době (kolem jednoho roku). Výsledný efekt je založen na compliance pacienta a jeho silné vůli dlouhodobě dodržovat léčebný režim, což nelze jistě očekávat u všech [8]. Tato spolupráce není zjistitelná (ani neznáme žádnou publikaci na toto téma), což zkresluje celkové výsledky každého souboru. Pacienti jsou zváni na pravidelné EMG kontroly v půlročních intervalech do dvou let od výkonu, při očekávatelné změně i déle.
U perinatálních PPP lze první známky návratu motorické funkce vidět v deltovém svalu a m. biceps nejdříve po devíti měsících, ve flexorech a extenzorech zápěstí mezi 12. a 18. měsícem a v intrinsických svalech koncem druhého roku. Proces reinervace a reorganizace mozkové kůry může trvat několik let, finální výsledky se dají u hybnosti ruky očekávat mezi čtvrtým a osmým rokem věku (obr. 12) [27,84].
Obr. 12. Dítě 49 měsíců po operaci – dobrá svalová síla ve všech segmentech vyjma extenze zápěstí (před plánovanou transpozicí šlachy m. flexor carpi ulnaris na m. extensor digitorum). Výkon proveden ve 3 měsících věku – plegie pravé horní končetiny, na CT-PMG avulze kořene C6–Th1, viz obr. 4. 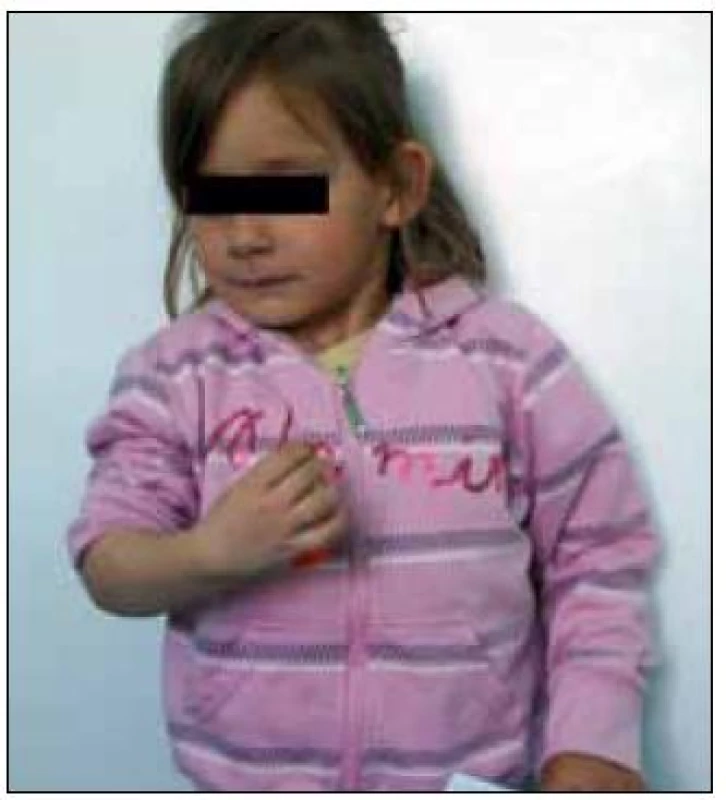
K sekundárním výkonům se přistupuje až po čtvrtém roce věku, kdy lze považovat reinervaci za definitivní a navíc je již dítě schopno plně spolupracovat během rehabilitace. Nejčastěji se provádí rotační osteotomie a šlachové transfery k obnově extenze zápěstí [4,18].
Závěr
Operační léčba PPP má v dnešní době velmi dobré výsledky v obnově pohybu v rameni a lokti u dospělých pacientů a kompletní hybnosti u dětí. Ty jsou tím lepší, čím dříve je správně indikovaná operace provedena. U zavřených poranění to je rozmezí 3–6 měsíců po úrazu. To platí i pro perinatální poranění, kdy je potřeba (pokud paréza trvá) první vyšetření provést již na konci prvního měsíce věku. Diagnosticky se používá EMG a CT-PMG, ačkoli je jen otázkou času, kdy převezme hlavní roli MR. Celá problematika čeká na další výzkum.
Poděkování
Práce vznikla za podpory grantů IGA NS 10496-3/2009 a MSM 0021620816.
prof. MUDr. Pavel Haninec, CSc.
Neurochirurgická klinika
3. LF UK a FN Královské Vinohrady
Šrobárova 50
100 34 Praha 10
e-mail: haninec@fnkv.cz
Přijato k recenzi: 1. 8. 2011
Přijato do tisku: 4. 10. 2011
Recenzenti
prof. MUDr. Lubor Stejskal, DrSc.
prof. RNDr. Petr Dubový, CSc.
MUDr. Dušan Urgošík, Ph.D.MUDr. Pavel Haninec, CSc. (1958)
Profesor Pavel Haninec se narodil 29. 3. 1958 v Praze. Promoval na Fakultě všeobecného lékařství UK v Praze v roce 1983 s vyznamenáním. Po promoci v roce 1983 pracoval až do roku 1989 jako odborný asistent v Anatomickém ústavu FVL UK Praha. V letech 1987–1989 (paralelně) jako sekundář I. chirurgické kliniky FVL UK v Praze. V roce 1989 složil atestaci 1. stupně z chirurgie a zároveň obhájil kandidátskou práci na téma Vývojová anatomie obalů periferních nervů a míchy. Od roku 1989 působil na Neurochirurgické klinice 1. LF UK a ÚVN Praha. V letech 1991 a 1992 pracoval jako asistent prof. Frerebeaua (Neurochirurgická klinika LF Univerzity Montpellier, Francie – roční pobyt). Absolvoval řadu stáží na prestižních zahraničních univerzitách (např. Toronto – Kanada, Pittsburgh – USA, Adelaide, Sydney – Austrálie). V roce 1996 obhájil na 1. LF UK habilitační práci a v roce 1997 byl jmenován docentem chirurgie. Od roku 1988 je přednostou Neurochirurgické kliniky 3. LF UK a FN Královské Vinohrady. V roce 2002 byl jmenován profesorem chirurgie na UK v Praze. Publikoval celkem 64 původních prací, z toho 35 v časopisech s impact faktorem. Podílel se celkem na 13 monografiích. Jeho současný citační ohlas je 223 bez autocitací, dle „science citation index“, H index 10. Na zahraničních sjezdech odpřednášel více než 100 sdělení. Je řešitelem či spoluřešitelem mnoha výzkumných grantů. Jeho práce opakovaně obdržely významná ocenění ČLS JEP a České neurochirurgické společnosti. Profesor Haninec byl v letech 2003–2010 proděkanem 3. LF UK, byl také členem revizní komise výboru České neurochirurgické společnosti, je členem akreditační komise MZ ČR pro obor neurochirurgie, členem zkušební komise pro atestační zkoušky v oboru, členem oborové rady Neurověd, UK, členem redakčních rad Acta Universitatis Carolinae, Acta Orthopediceae et Chirurgieae, členem vědecké rady 3. LF UK v P raze. Byl členem i předsedou oborů grantových rad České republiky a UK v Praze. Odborným zájmem profesora Hanince je neurochirurgie v celém rozsahu včetně cévní neurochirurgie a neuroonkologie, výzkumným zájmem je stavba regenerace periferního nervového systému. Mezi jeho priority patří např. původ obalů periferních nervů a obalů svalového vřeténka, vymezení nespecifické cholinesterézy jako adhezivní molekuly při vývoji a regeneraci periferních nervů, kvantifikace a postavení end-to-side anastomózy periferních nervů v rekonstrukci pažní pleteně a také zavedení nových technik v operační léčbě pažní pleteně včetně protibolestivých operací na úrovni míchy.
Zdroje
1. Songcharoen P. Brachial plexus injury in Thailand: a report of 520 cases. Microsurgery 1995; 16(1): 35–39.
2. Kim DH, Cho YJ, Tiel RL, Kline DG. Outcomes of surgery in 1019 brachial plexus lesions treated at Louisiana State University Health Sciences Center. J Neurosurg 2003; 98(5): 1005–1016.
3. Haninec P, Sámal F, Tomás R, Houstava L, Dubový P. Direct repair (nerve grafting), neurotization, and end--to-side neurorrhaphy in the treatment of brachial plexus injury. J Neurosurg 2007; 106(3): 391–399.
4. Vekris MD, Beris AE, Johnson EO, Korobilias AV, Pafilas D, Vekris AD et al. Musculocutaneous neurotization to restore elbow flexion in brachial plexus paralysis. Microsurgery 2006; 26(4): 325–329.
5. Lanaras TI, Schaller HE, Sinis N. Brachial plexus lesions: 10 years of experience in a center for microsurgery in Germany. Microsurgery 2009; 29(2): 87–94.
6. Jiang S, Li ZY, Hua XY, Xu WD, Xu JG, Gu YD. Reorganization in motor cortex after brachial plexus avulsion injury and repair with the contralateral C7 root transfer in rats. Microsurgery 2010; 30(4): 314–320.
7. Ahmed-Labib M, Golan JD, Jacques L. Functional outcome of brachial plexus reconstruction after trauma. Neurosurgery 2007; 61(5): 1016–1022.
8. Krishnan KG, Martin KD, Schackert G. Traumatic lesions of the brachial plexus: an analysis of outcomes in primary brachial plexus reconstruction and secondary functional arm reanimation. Neurosurgery 2008; 62(4): 873–885.
9. Bertelli JA, Ghizoni MF, Loure Iro Chaves DP. Sensory disturbances and pain complaints after brachial plexus root injury: A prospective study involving 150 adult patients. Microsurgery 2011; 31(2): 93–97.
10. Millesi H. Surgical management of brachial plexus injuries. J Hand Surg (Am) 1977; 2(5): 367–378.
11. Narakas A. Surgical treatment of traction injuries of the brachial plexus. Clin Orthop 1978; 133 : 71–90.
12. Kandenwein JA, Kretschmer T, Engelhardt M, Richter HP, Antoniadis G. Surgical interventions for traumatic lesions of the brachial plexus: a retrospective study of 134 cases. J Neurosurg 2005; 103(4): 614–621.
13. Bertelli JA, Ghizoni MF. Concepts of nerve regeneration and repair applied to brachial plexus reconstruction. Microsurgery 2006 a; 26(4): 230–244.
14. Kline DG, Judice DJ. Operative management of selected brachial plexus lesions. J Neurosurg 1983; 58(5): 631–649.
15. Narakas A. Obstetrical brachial plexus injuries. In: Lamb D (ed). The Paralyzed Hand. Edinburgh: Churchill Livingstone 1987 : 116–135.
16. Maillet M, Romana C. Complete obstetric brachial plexus palsy: surgical improvement to recover a functional hand. J Child Orthop 2009; 3(2): 101–118.
17. Samii M, Carvalho GA, Nikkhah G, Penkert G. Surgical reconstruction of the musculocutaneous nerve in traumatic brachial plexus injuries. J Neurosurg 1997; 87(6): 881–886.
18. Oberlin C, Beal D, Leechavengvongs S, Salon A, Dauge MC, Sarcy JJ. Nerve transfer to biceps muscle using a part of ulnar nerve for C5–C6 avulsion of the brachial plexus: anatomical study and report of four cases. J Hand Surg Am 1994; 19(2): 232–237.
19. Songcharoen P. Management of brachial plexus injury in adults. Scand J Surg 2008; 97(4): 317–323.
20. Gilbert A, Pivato G, Kheiralla T. Long-term results of primary repair of brachial plexus lesions in children. Microsurgery 2006; 26(4): 334–342.
21. Sunderland S. Nerves and nerve injuries. Edinburgh: Churchill Livingstone 1972.
22. Pondaag W, de Boer R, van Wijlen-Hempel MS, Hofstede-Buitenhuis SM, Malessy MJ. External rotation as a result of suprascapular nerve neurotization in obstetric brachial plexus lesions. Neurosurgery 2005; 57(3): 530–537.
23. Russell SM, Kline DG. Complication avoidance in peripheral nerve surgery: preoperative evaluation of nerve injuries and brachial plexus exploration – part 1. Neurosurgery 2006; 59 (4 Suppl 2): ONS441–ONS447.
24. Chen L, Gu YD, Wang H. Microsurgical reconstruction of obstetric brachial plexus palsy. Microsurgery 2008; 28(2): 108–112.
25. Tomáš R, Stejskal L, Haninec P, Houšťava L. Intraoperative monitoring and dorsal column pathway determination in DREZ thermocoagulation. Bolest 2001; 4(1): 34–38.
26. Macko J. Perinatální paréza brachiálního plexu. Cesk Gynekol 2010; 75(4): 279–283.
27. Janda V. Funkční svalový test. Praha: Grada, Avicenum 1996.
28. Haninec P, Houšťava L, Tomáš R, Stejskal L. DREZ thermocoagulation. Bolest 2001; 4(1): 28–32.
29. Haninec P, Tomáš R, Sereghy T, Houšťava L. DREZ thermocoagulation in treatment of deafferentation pain. Bolest 2002; 5(3): 177–180.
30. Tomás R, Haninec P. Dorsal root entry zone (DREZ) localization using direct spinal cord stimulation can improve results of the DREZ termocoagulation procedure for intractable pain relief. Pain 2005; 116(1–2): 159–163.
31. Bonilla G, Di Masi G, Battaglia D, Otero JM, Socolovsky M. Pain and brachial plexus lesions: evaluation of initial outcomes after reconstructive microsurgery and validation of a new pain severity scale. Acta Neurochir (Wien) 2011; 153(1): 171–176.
32. Bertelli JA, Ghizoni MF. Use of clinical signs and computed tomography myelography findings in detecting and excluding nerve root avulsion in complete brachial plexus palsy. J Neurosurg 2006; 105(6): 835–842.
33. Kaiser R, Houšťava L, Mencl L, Brzezny R, Haninec P. Operační léčba poranění peroneálního nervu. Cesk Slov Neurol N 2011; 74/107(2): 187–190.
34. Belzberg AJ, Dorsi MJ, Storm PB, Moriarity JL. Surgical repair of brachial plexus injury: a multinational survey of experienced peripheral nerve surgeons. J Neurosurg 2004; 101(3): 365–376.
35. Brown JM, Shah MN, Mackinnon SE. Distal nerve transfers: a biology-based rationale. Neurosurg Focus 2009; 26(2): E12.
36. Midha R. Nerve transfers for severe brachial plexus injuries: a review. Neurosurg Focus 2004; 16(5): E5.
37. Stejskal L, Haninec P. Indications for surgical reconstruction of the brachial plexus. electrodiagnostic. results of reconstructions. Cesk Slov Neurol N 1997; 60/93(3): 126–133.
38. Marcus JR, Clarke HM. Management of obstetrical brachial plexus palsy evaluation, prognosis, and primary surgical treatment. Clin Plast Surg 2003; 30(2): 289–306.
39. Birch R, Ahad N, Kono H, Smith S. Repair of obstetric brachial plexus palsy – Results in 100 children. J Bone Joint Surg (Br) 2005; 87(8): 1089–1095.
40. Bain JR, Dematteo C, Gjertsen D, Hollenberg RD. Navigating the gray zone: a guideline for surgical decision making in obstetrical brachial plexus injuries. J Neurosurg Pediatr 2009; 3(3): 173–180.
41. Chuang DC, Mardini S, Ma HS. Surgical strategy for infant obstetrical brachial plexus palsy: Experiences at Chang Gung Memorial Hospital. Plast Reconstr Surg 2005; 116(1): 132–142.
42. Haninec P, Kaiser R, Brzezny R, Mencl L. Chirurgická léčba porodní parézy brachiálního plexu. Neonatol Listy 2011; 17(1): 3–8.
43. Pondaag W, Malessy MJ. Recovery of hand function following nerve grafting and transfer in obstetric brachial plexus lesions. J Neurosurg 2006; 105 (1 Suppl): 33–40.
44. Tender GC, Kline DG. Anterior supraclavicular approach to the brachial plexus. Neurosurgery 2006; 58 (4 Suppl 2): ONS360–ONS364.
45. Malessy MJ, de Ruiter GC, de Boer KS, Thomeer RT. Evaluation of suprascapular nerve neurotization after nerve graft or transfer in the treatment of brachial plexus traction lesions. J Neurosurg 2004; 101(3): 377–389.
46. Nath RK, Lyons AB, Bietz G. Physiological and clinical advantages of median nerve fascicle transfer to the musculocutaneous nerve following brachial plexus root avulsion injury. J Neurosurg 2006; 105(6): 830–834.
47. Harris W, Low VW. On the importance of accurate muscular analysis in lesions of the brachial plexus and the treatment of Erb’s palsy and infantile paralysis of the upper extremity by cross-union of nerve roots. BMJ 1903; 2 : 1035–1038.
48. Tuttle HK. Exposure of the brachial plexus with nerve transplantation. JAMA 1913; 61 : 15–17.
49. MacKinnon SE, Roque B, Tung TH. Median to radial nerve transfer for treatment of radial nerve palsy. Case report. J Neurosurg 2007; 107(3): 666–671.
50. Ferraresi S, Garozzo D, Buffatti P. Reinnervation of the biceps in C5–7 brachial plexus avulsion injuries: results after distal bypass surgery. Neurosurg Focus 2004; 16(5): E6.
51. Terzis JK, Kostas I, Soucacos PN. Restoration of shoulder function with nerve transfers in traumatic brachial plexus palsy patients. Microsurgery 2006; 26(4): 316–324.
52. Sulaiman OA, Kim DD, Burkett C, Kline DG. Nerve transfer surgery for adult brachial plexus injury: a 10--year experience at Louisiana State University. Neurosurgery 2009; 65 (4 Suppl): A55–A62.
53. Samardzic MM, Grujicic DM, Rasulic LG, Milicic BR. The use of thoracodorsal nerve in restoration of irreparable C5 and C6 spinal nerve lesions. Br J Plast Surg 2005; 58(4): 541–546.
54. Luedemann W, Hamm M, Blömer U, Samii M, Tatagiba M. Brachial plexus neurotization with donor phrenic nerves and its effect on pulmonary function. J Neurosurg 2002; 96(3): 523–526.
55. Malessy MJA, Hoffman CFE, Thomeer RTWM. Initial report on the limited value of hypoglossal nerve transfer to treat brachial plexus avulsions. J Neurosurg 1999; 91 : 601–604.
56. Songcharoen P, Mahaisavariya B, Wongtrakul S, Lamsam C. Ipsilateral median nerve´s fascicle transfer for restoration of elbow flexion in root avulsion brachial plexus injury. J Thai Orthop Surg 2001; 26(2): 93–95.
57. Sungpet A, Suphachatwong C, Kawinwonggowit V. One-fascicle median nerve transfer to biceps muscle in C5 and C6 root avulsions of brachial plexus injury. Microsurgery 2003; 23(1): 10–13.
58. Kennedy R. On the resoration of co-ordinated movements after nerve crossing, with interchange of fiction of the cerebral cortical centres. Philos Trans R Soc London 1901; 194B: 127–164.
59. Viterbo F, Trinidade JC, HoshinoK, Mazzoni A. Latero-terminal neurorrhaphy without removal of the epineural sheath: experimantal study in rats. Sao Paulo Med J 1992; 110(6): 267–275.
60. Geuna S, Papalia I, Tos P. End-to-side (terminolateral) nerve regeneration: a challenge for neuroscientists coming from an intriguing nerve repair concept. Brain Res Rev 2006; 52(2): 381–388.
61. Schmidhammer R, Nógrádi A, Szabó A, Redl H, Hausner T, van der Nest DG et al. Synergistic motor nerve fiber transfer between different nerves through the use of end-to-side coaptation. Exp Neurol 2009; 217(2): 388–394.
62. Oğün TC, Ozdemir M, Senaran H, Ustün ME. End-to-side neurorrhaphy as a salvage procedure for irreparable nerve injuries. Technical note. J Neurosurg 2003; 99(1): 180–185.
63. Beris A, Lykissas M, Korompilias A, Mitsionis G. End-to-side nerve repair in peripheral nerve injury. J Neurotrauma 2007; 24(5): 909–916.
64. Mennen U. End-to-side nerve suture in clinical practice. Hand Surg 2003; 8(1): 33–42.
65. Lutz BS, Chuang DC, Hsu JC, Ma SF, Wei FC. Selection of donor nerves – an important factor in end-to-side neurorrhaphy. Br J Plast Surg 2000; 53(2): 149–154.
66. Sámal F, Haninec P, Raska O, Dubový P. Quantitative assessment of the ability of collateral sprouting of the motor and primary sensory neurons after the end-to-side neurorrhaphy of the rat musculocutaneous nerve with the ulnar nerve. Ann Anat 2006; 188(4): 337–344.
67. Hayashi A, Pannucci C, Moradzadeh A, Kawamura D, Magill C, Hunter DA et al. Axotomy or compression is required for axonal sprouting following end-to-side neurorrhaphy. Exp Neurol 2008; 211(2): 539–550.
68. Kelly EJ, Jacoby C, Terenghi G, Mennen U, Ljungberg C, Wiberg M. End-to-side nerve coaptation: a qualitative and quantitative assessment in the primate. J Plast Reconstr Aesthet Surg 2007; 60(1): 1–12.
69. Rovak JM, Cederna PS, Kuzon VW jr. Terminolateral neurorrhaphy: a review of the literature. J Reconstr Microsurg 2001; 17(8): 615–624.
70. Haastert K, Joswig H, Jäschke K, Samii M, Grothe C. Nerve repair by end-to-side nerve coaptation: Histologic and morphometric evaluation of axonal origin in a rat sciatic nerve model. Neurosurgery 2010; 66(3): 567–576.
71. Kim JK, Chung MS, Baek GH. The origin of regenerating axons after end-to-side neurorrhaphy without donor nerve injury. J Plast Reconstr Aesthet Surg 2011; 64(2): 255–260.
72. Walker JC, Brenner MJ, Mackinnon SE, Winograd JM, Hunter DA. Effect of perineurial window size on nerve regeneration, blood-nerve barrier integrity, and functional recovery. J Neurotrauma 2004; 21(2): 217–227.
73. Carlstedt T, Anand P, Hallin R, Misra PV, Norén G, Seferlis T. Spinal nerve root repair and reimplantation of avulsed ventral roots into the spinal cord after brachial plexus injury. J Neurosurg 2000; 93 (2 Suppl): 237–247.
74. Amr SM, Essam AM, Abdel-Meguid AM, Kholeif AM, Moharram AN, El-Sadek RE. Direct cord implantation in brachial plexus avulsions: revised technique using a single stage combined anterior (first) posterior (second) approach and end-to-side side-to-side grafting neurorrhaphy. J Brachial Plex Peripher Nerve Inj 2009; 4 : 8.
75. Doi K, Sakai K, Kuwata N et al. Double free-muscle transfer to restore prehension following complete brachial plexus avulsion. J Hand Surg Am 1995; 20(3): 408–414.
76. Barrie KA, Steinmann SP, Shin AY, Spinner RJ, Bishop AT. Gracilis free muscle transfer for restoration of function after complete brachial plexus avulsion. Neurosurg Focus 2004; 16(5): E8.
77. Haninec P, Dubový P, Sámal F. Reconstruction of elbow flexion, wrist and finger extension by transposition of pedicled latissimus dorsi muscle and flexor carpi ulnaris muscle. Acta Chir Plast 2001; 43(3): 80–85.
78. Haninec P, Szeder V. Reconstruction of elbow flexion by transposition of pedicled long head of triceps brachii muscle. Acta Chir Plast 1999; 41(3): 82–86.
79. Haninec P, Smrčka V. Reconstruction of paralysed biceps brachii muscle by transposition of pedicled latissimus dorsi muscle: Report of two cases. Acta Chir Plast 1998; 40(2): 41–44.
80. Haninec P, Dubový P, Houšťava L, Stejskal L. Reconstructive operations of brachial plexus injury and the experimental model of their management. 11th International Congress of Neurological Surgery. Amsterdam, The Netherlands. 1997.
81. Haninec P, Dubový P, Houšťava L, Stejskal L. Surgical management of brachial plexus injuries and the experimental reinnervation of the biceps brachii muscle by the spinal motor neurons through acellular nerve graft. Congress of the International Federation of Societies for Surgery of the Hand. Vancouver, Canada. 1998.
82. Moiyadi AV, Devi BI, Nair KP. Brachial plexus injuries: outcome following neurotization with intercostal nerve. J Neurosurg 2007; 107(2): 308–313.
83. Terzis JK, Kokkalis ZT. Selective contralateral c7 transfer in posttraumatic brachial plexus injuries: a report of 56 cases. Plast Reconstr Surg 2009; 123(3): 927–938.
84. El-Gammal TA, El-Sayed A, Kotb MM, Ragheb YF, Saleh WR, Elnakeeb RM et al. Total obstetric brachial plexus palsy: results and strategy of microsurgical reconstruction. Microsurgery 2010; 30(3): 169–178.
85. Zheng XY, Hou CL, Gu YD, Shi QL, Guan SB. Repair of brachial plexus lower trunk injury by transferring brachialis muscle branch of musculocutaneous nerve: anatomic feasibility and clinical trials. Chin Med J (Engl) 2008; 121(2): 99–104.
Štítky
Detská neurológia Neurochirurgia Neurológia
Článek Webové okénko
Článok vyšiel v časopiseČeská a slovenská neurologie a neurochirurgie
Najčítanejšie tento týždeň
2011 Číslo 6- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Neuromultivit v terapii neuropatií, neuritid a neuralgií u dospělých pacientů
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Důvody a průběh novelizace české verze Addenbrookského kognitivního testu (ACE-CZ)
- Operační léčba poranění plexus brachialis
- Komentář k článku autorů Haninec a Kaiser Operační léčba poranění plexus brachialis
- Použití dotazníků aktivit denního života u pacientů s Alzheimerovou nemocí
- Parkinsonské fenotypy – na cestě k nové nozologii atypických parkinsonských syndromů
- Současný pohled na patofyziologii migrény
- Motorické aspekty poruch řeči u Parkinsonovy nemoci a jejich hodnocení
- Posturální reflexy v podmínkách zrakové poruchy
- Využití traktografie začleněné do neuronavigace při operacích intraaxiálních tumorů mozku uložených v těsné blízkosti kortikospinální dráhy
- Novelizace české verze Addenbrookského kognitivního testu (ACE-CZ)
- Rozšíření terapeutického časového okna pro intravenózní trombolýzu by nemělo vést k prodloužení „door-to-needle time“ intervalu
- Miller Fisherův syndrom – čtyři vlastní pozorování a přehled současných poznatků
- Parkinsonova nemoc s fenotypem progresivní supranukleární paralýzy – kazuistika
- Kognitivní a emocionální změny pět let po SAH – kazuistika
- Amisulprid v léčbě schizofrenie
- Webové okénko
- Analýza dat v neurologii - XXX. Validita klinických testů v širším kontextu
- MUDr. Jan Pařízek osmdesátníkem
- Česká a slovenská neurologie a neurochirurgie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Miller Fisherův syndrom – čtyři vlastní pozorování a přehled současných poznatků
- Současný pohled na patofyziologii migrény
- Novelizace české verze Addenbrookského kognitivního testu (ACE-CZ)
- Operační léčba poranění plexus brachialis
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy




