-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Indikace Avastinu v oftalmologii
Indication Avastin in Ophthalmology
Bevacizumab (Avastin) is a humanized monoclonal antibody to vascular endothelial growth factor A that is approved for the treatment of metastatic colorectal cancer. Although this drug is off-label for intraocular use, it has been widely used as intravitreal therapy for lot of ocular diseases. This paper will describe the efficacy and safety of the intraocular Avastin in the treatment of ocular diseases. The results described in the article warrant further study of bevacizumab in larger, controlled, randomized trials.
Key words:
Avastin, vascular endothelial growth factor A, bevacizumab
Autori: J. Studnička
Pôsobisko autorov: Oční klinika FN a LF UK, Hradec Králové, přednosta prof. MUDr. Pavel Rozsíval, CSc., FEBO
Vyšlo v časopise: Čes. a slov. Oftal., 66, 2010, No. 5, p. 229-233
Kategória: Původní práce
Súhrn
Předneseno na Futurum ophthalmologicum 2010 dne 19. 3. 2010 v Poděbradech
Bevacizumab (Avastin) je humanizovaná monoklonální protilátka zaměřená proti vaskulárnímu endotelovému růstovému faktoru A, která je registrovaná pro léčbu metastáz kolorektálního karcinomu. Přestože je užití tohoto léku v oftalmologii off-label, je široce užíván při intravitreální aplikaci u řady očních onemocnění. V této práci je popsána účinnost a bezpečnost intraokulárního podání Avastinu v léčbě očních onemocnění. Výsledky uvedené v článku jsou motivací k dalšímu studiu bevacizumabu v rámci velkých, srovnávacích, randomizovaných studií.Klíčová slova:
Avastin, vaskulární endotelový růstový faktor A, bevacizumabÚvod
Bevacizumab (Avastin) je humanizovaná monoklonální protilátka velikosti 149 kDa zaměřená proti vaskulárnímu endotelovému růstovému faktoru A (VEGF-A). V roce 2004 byla v USA schválena Federal Drug Administration (FDA) pro léčbu metastáz kolorektálního karcinomu. V ČR je registrována k léčbě stejného onemocnění Státním ústavem pro kontrolu léčiv (SÚKL) od roku 2005. V současné době se používá v kombinaci s jinými protinádorovými přípravky také k léčbě metastazující rakoviny prsu, neresektabilního pokročilého, metastazujícího nebo rekurentního nemalobuněčného karcinomu plic a pokročilé nebo metastazující rakoviny ledvin.
Vzhledem k jeho mechanismu účinku byl také zkoušen v roce 2005 k ovlivnění choroidální neovaskularizace (CNV) při exsudativní formě věkem podmíněné makulární degenerace (VPMD). Při intravenózním podávání se v léčené skupině 18 pacientů za 6 měsíců po léčbě statisticky významně zlepšila nejlépe korigovaná zraková ostrost (NKZO) postiženého oka s poklesem centrální retinální tloušťky (CRT) na optické koherentní tomografii (OCT). Nežádoucím účinkem byla elevace systolického i diastolického krevního tlaku (29). K odstranění potenciálních nežádoucích účinků intravenózního podávání bevacizumabu bylo přikročeno k pokusu o intravitreální podání. V preklinické fázi těchto zkoušek však nebyl zjištěn výrazný efekt bevacizumabu, proto další pokusy byly prováděny pouze s fragmentem této humanizované monoklonální protilátky (Fab). Tento fragment velikosti 48 kDa, který byl pojmenován ranibizumab, se ukázal jako účinný a pro svou menší molekulu prostupný i při intravitreálním podávání k choroidální neovaskularizaci zvířat i lidí. V roce 2006 byl ranibizumab schválen FDA k léčbě exsudativní formy VPMD. Přes neúspěchy v preklinické fázi zkoušek i vzhledem k výborným výsledkům při intravenózním podávání a k nižší komerční dostupnosti ranibizumabu byl v roce 2005 vyzkoušen bevacizumab u pacienta s exsudativní VPMD, který nereagoval na léčbu pegaptanibem (36). Po aplikaci 1,0 mg bevacizumabu se během 1 týdne zcela resorboval makulární edém. Důvody pro účinek intravitreální aplikace bevacizumabu u nemocných lidí mohou být následující. Dávky používané v klinické praxi jsou 50–100násobně vyšší než dávka použitá v preklinických pokusech na zvířatech, u primátů je silnější lamina limitans interna než u lidí a edematózní sítnice je více prostupná pro větší molekulu bevacizumabu.
Od roku 2006 se výrazně zvyšuje počet pacientů léčených bevacizumabem a zvyšuje se také počet indikací u kterých je tento preparát zkoušen. Od začátku roku 2006 se tak podle American Society of Retina Specialists stává Avastin jedním z léků první linie v léčbě vlhké formy VPMD a v roce 2007 tvoří bevacizumab více než 50 % veškeré anti VEGF léčby v USA. Od roku 2005 je publikováno mnoho prací se stále zvyšujícím se počtem indikací, u kterých se ukazuje efektivní účinek bevacizumabu. Od roku 2008 probíhá v USA srovnávací studie CATT (Comparison of Age related macular degeneration Treatments Trial), která porovnává účinnost a bezpečnost bevacizumabu oproti ranibizumabu v ovlivnění vlhké formy VPMD. Tato studie je zadána Národním institutem zdraví (NIH) a je plánována na čtyři roky. K 1. 8. 2008 bylo podle databáze Národní lékařské knihovny Národního institutu zdraví v USA publikováno použití Avastinu u 51 očního onemocnění (17). Použití Avastinu v očních indikacích v České republice se opírá o zákon č. 378/2007 Sb. – Zákon o léčivech. Podle § 8 odst. 4 tohoto zákona může ošetřující lékař použít registrovaný léčivý přípravek způsobem, který není v souladu se souhrnem údajů o přípravku, pokud není standardní léčivý přípravek distribuován nebo není v oběhu léčivý přípravek potřebných terapeutických vlastností. Tento způsob použití však musí být dostatečně odůvodněn vědeckými poznatky.
Indikace Avastinu v oftalmologii
Indikace použití Avastinu lze rozdělit do několika skupin podle primárního cíleného účinku. První skupinu tvoří onemocnění, při kterých ovlivňujeme CNV, druhou skupinu tvoří onemocnění, při kterých působíme na retinální neovaskularizace, třetí skupinu tvoří onemocnění, které se vyznačují především makulárním edémem, čtvrtou skupinu lze vyhradit pro ovlivnění nitroočního tlaku a do páté skupiny jsou zařazena zbývající oční onemocnění, u kterých byla aplikace Avastinu vyzkoušena.
Oční onemocnění, která mohou být komplikována CNV a u kterých byla s efektem vyzkoušena léčba Avastinem jsou uvedena v následující tabulce (tab. 1) (17). V léčbě exsudativní VPMD byl Avastin poprvé použit u pacientů, kteří nereagovali na pegaptanib (Macugen) nebo fotodynamickou léčbu s Visudynem (PDT). Avery a kol. prezentovali výsledky použití měsíční intravitreální aplikace Avastinu 1,25 mg u 81 očí, z nichž mělo 78 % předchozí léčbu pegaptanibem nebo PDT. Po dvou měsících zjistili v 50 % ústup subretinální tekutiny prokazatelný na OCT, NKZO se zlepšila z 20/200 na 20/125 (8). Spaide a kol. publikovali použití Avastinu 1,25 mg u 266 očí, z nichž bylo 70 % po předchozí léčbě. Po 3 měsících zjistili pokles CRT na OCT z 340 na 213 μm, NKZO se zlepšila z 20/184 na 20/109 a celkem 38,3 % očí bylo zlepšeno o ≥ 2 řádků ETDRS optotypů (41). Wu a kol. srovnávali použití dvou různých dávek bevacizumabu. Při použití dávky 1,25 mg zjistili za rok zlepšení NKZO o 3 a více řádků ETDRS optotypů u 46 %, srovnatelně při dávce 2,5 mg u 44 % očí. Ztrátu 3 a více řádků optotypů dokumentoval u 20 % očí při použití dávky 1,25 mg, srovnatelně u 16 % očí při dávce 2,5 mg. U obou dávek se signifikantně zmenšila CRT. Počet průměrně aplikovaných injekcí byl nevýznamně vyšší u dávky 1,25 mg (3,8 injekcí x 3,2 injekcí) (47). Arevalo a kol. letos prezentovali v rámci stejné studie dvouleté výsledky u celkem 207 očí 180 pacientů. V první skupině 124 očí bylo potvrzeno zlepšení NKZO z průměrné hodnoty 20/235 na 20/172 a pokles CRT z 308,4 μm na 249,3 μm s průměrným počtem 5,1 injekce. Hodnoty v druhé skupině 83 očí byly podobné (4). Doležalová a kol. prezentovali dlouhodobé výsledky léčby Avastinem na souboru 71 očí 71 pacientů. Při průměrné sledovací době 18,5 měsíců zjistili zlepšení NKZO o více než 3 řádky optotypů u 11,3 % očí a ztrátu více než 15 písmen optotypů u 7 % očí. Stabilizaci NKZO tak dosáhlo celkem 93 % pacientů při průměrném počtu 3,52 injekce (12). Schéma terapie vlhké formy věkem podmíněné makulární degenerace Avastinem není jednoznačně stanovené. Pro chemickou podobnost a stejnou vazbu na receptory je často používáno léčebné schéma Lucentisu založené na úvodní fázi tří injekcí v měsíčních intervalech a následné udržovací fázi dalších injekcí podle aktuálního nálezu a stanovených kriterií. S cílem zmenšení počtu aplikovaných injekcí jsou zkoušeny kombinované postupy léčby. Kaiser a kol. prezentovali souhrnné výsledky 45 vitreoretinálních center v USA, která prováděla kombinovanou léčbu PDT a Avastinu. Celkem bylo do souboru zařazeno 1196 pacientů, z nichž 1073 mělo sledovací dobu 6 měsíců a delší. Z těchto probandů mělo 56,3 % léčbou neovlivněnou CNV. Všichni pacienti podstoupili úvodní PDT a injekci Avastinu v rozmezí 14 dnů. Během sledovací doby 15 měsíců podstoupili průměrně dalších 0,6 PDT a 2 injekce Avastinu. Za 12 měsíců od zahájení léčby se NKZO stabilizovala nebo zlepšila u 82 % očí, z toho u 36 % očí se zlepšila o 3 a více řádků optotypů a u 17 % očí se zlepšila o 6 a více řádků optotypů (25). Augustine a kol. upřednostňují použití trojité léčby – PDT v redukované dávce 42 J/cm + dexamethasone 800 μg + Avastin 1,5 mg k dosažení komplexního ovlivnění CNV. V souboru 104 očí zjistili ve sledovací době 10 měsíců zisk ≥ 3 řádky optotypů u 39,4 % očí a ztrátu ≥ 3 řádky optotypů pouze u 3,8 % očí. Pouze u 17,3 % očí bylo nutno aplikovat v průměrném období 15 týdnů druhou injekci Avastinu (6). Vzhledem k těmto výsledkům lze říci, že přestože standardem pro léčbu exsudativní formy VPMD je aplikace Lucentisu, Macugenu, PDT s Visudynem a ve vymezených indikacích termální fotokoagulace CNV, v případě, kdy nelze standardní léčbu použít, je aplikace Avastinu oprávněná.
Tab. 1. Oční onemocnění komplikované choroidální neovaskularizací 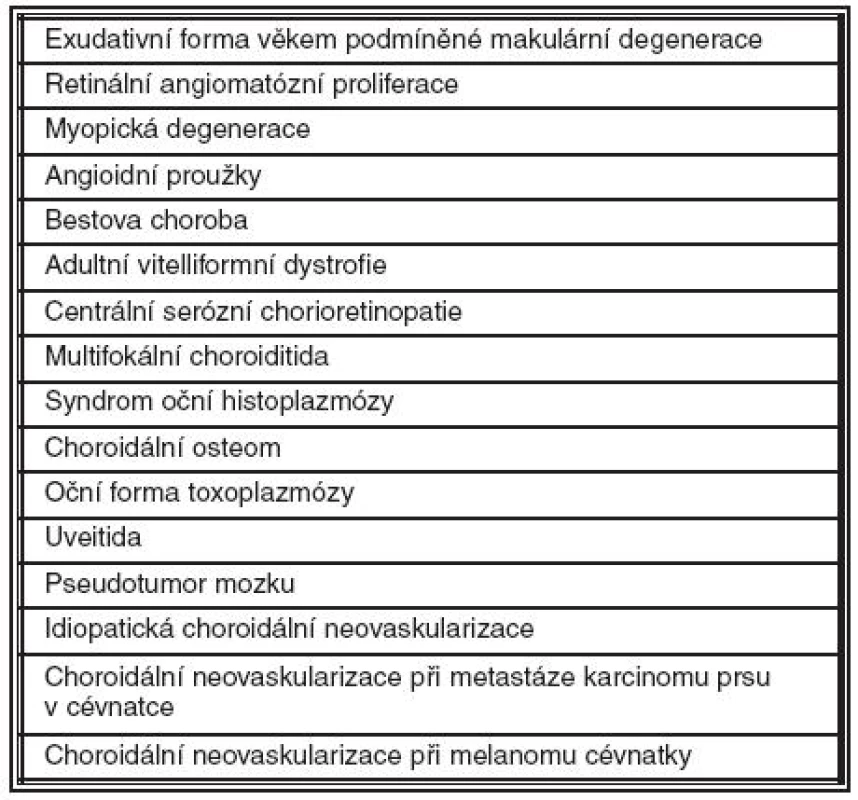
Účinek bevacizumabu byl zjištěn i u jiných očních onemocnění, která mohou mít ve svém klinickém obrazu CNV. Gharbiya a kol. dokumentovali účinek léčby Avastinem 1,25 mg u agresivní formy VPMD retinální angiomatózní proliferace. Při roční léčbě zjistili zlepšení NKZO o ≥ 3 řádky optotypů u 17,7 % očí, stabilizaci NKZO pozoroval v 82,4 % (15). Chan a kol. publikovali výsledky léčby Avastinem 1,25 mg 22 očí s myopickou degenerací komplikovanou CNV. Za 6 měsíců léčby zjistili zlepšení o ≥ 2 řádky optotypů u 68 % očí při dávkovacím schématu třikrát aplikace po měsíci, poté další 3 aplikace při prokázaném perzistujícím prosakování, což bylo potřebné u 10 % očí (19). Řada menších studií potvrdila i účinek léčby bevacizumabem u angioidních proužků komplikovaných přítomnou CNV (30, 31, 37, 44).
Druhou skupinou onemocnění indikovaných k léčbě Avastinem jsou choroby sítnice, které se projevují přítomností retinálních neovaskularizací. Mezi ně se řadí proliferativní diabetická retinopatie, retinopatie předčasně narozených dětí (ROP), Coatsova choroba, Ealsova choroba a retinopatie při srpkovité anémii.
V případě proliferativní diabetické retinopatie zůstává standardním ošetřením laserová panretinální fotokoagulace. Pokud se onemocnění rozvíjí přes laserové ošetření nebo nelze toto ošetření provést například pro neprůhledná optická média, je aplikace Avastinu oprávněná. Regrese neovaskularizací sítnice, terče zrakového nervu i duhovky po injekci bevacizumabu je velice rychlá (1–3 týdny po injekci) a byla doložena řadou autorů (7, 9, 22).
Schmidinger a kol. publikovali výsledky intravitreální aplikace Avastinu 1 mg u perzistujících neovaskularizací po kompletní laserové panretinální fotokoagulaci. První týden po léčbě bevacizumabem zjistili regresi perzistujících retinálních neovaskualizací v 73 %, během 6 měsíců se však neovaskularizace znovu objevily v 36 %. Těchto výsledků bylo dosaženo při průměrném počtu dvou injekcí bevacizumabu za 6 měsíců, druhá injekce byla aplikována průměrně ve třetím měsíci léčby (38). Tyto výsledky dokládají úspěšnost léčby Avastinem a zároveň nutnost pravidelného sledování při léčbě tímto přípravkem. V případě proliferativní diabetické retinopatie komplikované intravitreálním krvácením nebo preretinální vazivovou membránou lze aplikovat Avastin 2–7 dní před plánovanou pars plana vitrektomií (PPV). Cílem je indukovat cévní regresi před operací a redukovat tak peroperační krvácení a usnadnit odloučení fibroproliferativní membrány.
Vzhledem k tomu, že přes časně provedenou standardní terapii je stále velká skupina dětí s ROP s trvale sníženou zrakovou ostrostí, je i u těchto nemocných zkoušena léčba bevacizumabem. Palmer a kol. uvádějí, že 31 % nedonošených dětí s ROP stadia 3 v zóně I má navzdory časně provedené kryoterapii neuspokojivé vidění (33). Mintz-Hittner a Kuffel prezentovali výsledky ošetření 22 očí 11 dětí s ROP stadia 3 v zóně I nebo II, kterým byla aplikována jedna injekce Avastinu 0,625 mg v průměrném 11. týdnu života. Ve všech případech pozorovali regresi retinálních neovaskularizací bez komplikací (28). Honda a kol. však upozornili na riziko akutní kontrakce proliferativní membrány se vznikem nepříznivé trakční amoce po injekci bevacizumabu u dětí s ROP (18). Vzhledem k těmto výsledkům lze stanovit, že standardní léčbou ROP stále zůstává fotokoagulace nebo kryoterapie nemocné sítnice. Pokud však dochází k selhání léčby a progresi nálezu lze považovat použití Avastinu za odůvodněné. Otázkou zůstává potenciální dlouhodobý oční nebo systémový vedlejší efekt. Úspěšné použití bevacizumabu u dalších nemocí sítnice, které se projevují retinálními neovaskularizacemi (Coatsova choroba, Ealsova choroba, oční ischemický syndrom) bylo doloženo jednotlivými kazuistikami (3, 13, 20, 27).
Další možností léčby Avastinem je využití jeho vlivu na ovlivnění makulárního edému. Do této skupiny patří především diabetický makulární edém (DME) a makulární edém při žilní okluzi.
Standardní léčbou DME je laserová fotokoagulace. Podle Early Treatment Diabetic Retinopathy Study (ETDRS) vedla laserová léčba DME během 3 let k zisku 3 a více řádků optotypů u 3 % očí, ke ztrátě 3 a více řádků u 12 % očí. Hlavním výsledkem laserové léčby DME je stabilizace NKZO, což potvrdila i ETDRS. Současné alternativní možnosti léčby, mezi které patří i léčba Avastinem, se snaží dosáhnout zlepšení NKZO u pacientů s DME. O intravitreální aplikaci bevacizumabu u DME již bylo četně publikováno (1, 14, 32). Arevalo a kol. porovnávali ve skupině 139 očí s DME dvě dávky Avastinu: 1,25 mg x 2,5 mg. Za 2 roky léčby pozoroval porovnatelné zlepšení NKZO. Avastin 1,25 mg: NKZO z 20/150 při vstupu do studie byla zlepšena na průměrně 20/75 při konečném vyhodnocení. Avastin 2,5 mg: NKZO při vstupním vyšetření 20/168 byla zlepšena na 20/114 za 2 roky. Průměrně bylo v obou skupinách aplikováno 5,8 injekce/oko/2 roky (5). Soheilian a kol. srovnávali léčbu Avastinem 1,25 mg s kombinovanou léčbou Avastin 1,25 mg + Triamcinolon 2 mg intravitreálně. Jako kontrolní skupina jim sloužili pacienti s laserovou koagulací makuly. V souboru zahrnujícím celkem 150 očí po 36 týdnech léčby zjistili zlepšení NKZO o > 2 řádky optotypů u 37 % očí léčených pouze Avastinem, u 25 % léčených kombinací a u 14,8 % očí léčených laserovou koagulací. Pouze jednu injekci Avastinu potřebovalo k dosažení těchto výsledků 72 % očí (40).
Standardní léčba makulárního edému při kmenové okluzi centrální sítnicové žíly zatím není v ČR jednoznačně definována. Studie Central Vein Occlusion Study (CVOS) prokázala na fluorescenční angiografii, že laserová léčba signifikantně redukuje makulární edém, neprokázala však signifikantní zlepšení NKZO. V roce 2009 byla v USA schválena léčba intravitreálním implantátem dlouhodobě uvolňujícím 700 μg dexamethasone (Ozurdex). Výsledky randomizované, placebem kontrolované studie ukázaly, že až 30 % nemocných získalo 3 a více řádků ETDRS optotypů při této léčbě. Priglinger a kol. publikovali výsledky léčby Avastinu 1,25 mg u 46 očí s makulárním edémem při kmenové okluzi centrální retinální žíly. Při průměrném počtu 3 injekcí/oko zjistili zlepšení NKZO za 6 měsíců z 20/250 na 20/80 (34). Algvere a kol. prezentovali podobně úspěšné výsledky na souboru 13 očí. Při aplikaci Avastinu 1,25 mg každých 6 týdnů po dobu 6 měsíců prokázal průměrné zlepšení NKZO o 24 písmen ETDRS optotypů a pokles CRT na OCT z 596 na 288 μm (2). Dlouhodobé výsledky letos publikovali Wu a kol. V souboru 86 očí srovnávali účinek 1,25 mg a 2,5 mg Avastinu. Ve skupině 44 očí léčených injekcemi 1,25 mg Avastinu se během dvou let zlepšila NKZO o 3 a více řádků ETDRS optotypů u 56,8 % očí, ztráta 3 a více řádků optotypů byla u 13,6 % očí. Průměrná CRT se zmenšila z 635 μm na 264 μm při průměrném počtu 7,2 injekcí/oko. Ve skupině 42 očí léčených injekcemi 2,5 mg Avastinu se NKZO zlepšila u 57,1 % očí a ztráta 3 a více řádků optotypů byla zaznamenána u 16,7 % očí. CRT se zmenšila z 528 μm na 293 μm při průměrném počtu 8,1 injekce/oko (46).
Standardní léčbou makulárního edému u větvové okluze centrální sítnicové žíly je v ČR zatím pouze mřížková laserová koagulace sítnice. Studie Branch Retinal Vein Occlusion Study (BVOS) její účinnost prokázala. Zlepšení NKZO ≥ 2 řádky optotypů bylo pozorováno během 3 let v 65 % léčených očí oproti 37 % neléčených očí. Od roku 2009 je v USA také u tohoto onemocnění registrován Ozurdex, a to na základě výsledků klinické studie, která u nemocných prokázala v 30 % zlepšení o 3 a více řádků ETDRS optotypů. Lepší výsledky prezentovali Wu a kol. jako výsledek Pan-American Collaborative Retina Study Group u 63 očí léčených Avastinem. Při porovnání dvou dávek 1,25 mg x 2,5 mg mělo za 2 roky zlepšení ≥ 3 řádky optotypů 68 % x 72 % při průměrném počtu 3,6 x 4,3 injekcí (45). Na základě nejen těchto výsledků lze konstatovat, že užití Avastinu je v ČR zdůvodněno v případě, kdy selže laserová léčba makulárního otoku u větvové okluze centrální sítnicové žíly nebo tuto léčbu nelze provést. V případě kmenové okluze centrální sítnicové žíly lze Avastin užít jako jednu z terapeutických možností.
Čtvrtou skupinou očních onemocnění, při kterých se zkouší účinnost Avastinu, jsou glaukomy. V léčbě sekundárního – neovaskulárního glaukomu se využívá antiproliferativního efektu bevacizumabu. Sivak-Callcot a kol. publikovali v souhrnné práci 42–82% úspěšnost retinální fotokoagulace a kryoterapie v efektivním snížení tlaku u neovaskulárního glaukomu. Ve většině případů byla nutná doprovodná léčba lokálními nebo celkovými antiglaukomatiky, někdy v kombinaci s chirurgickým zákrokem (39). Práce různých autorů (16, 21, 24) dokumentují snížení nitroočního tlaku po aplikaci bevacizumabu intravitreálně. Vasudev a kol. porovnávali terapii 27 pacientů s neovaskulárním glaukomem. Skupina s kombinovanou léčbou jedné injekce 1,25 mg bevacizumabu a panretinální fotokoagulací měla roční pokles nitroočního tlaku z 32,3 mmHg na 19,2 mmHg, kdežto skupina, kterou léčili pouze panretinální fotokoagulací, měla pokles z 31,8 mmHg na 26,2 mmHg za rok (42). Lze tedy stanovit, že užití Avastinu je zdůvodnitelné jako doplněk panretinální fotokoagulace nebo kryoterapie nebo v případě, kdy tuto standardní léčbu nelze provést nebo není zcela účinná.
Další indikací Avastinu je zabránění selhání funkce filtračního polštáře, což je docíleno antivaskularizačním účinkem bevacizumabu, který brání vaskularizaci, migraci fibroblastů a jizvení filtračního puchýře. Několik autorů (10, 23, 26) publikovalo úspěšnou intravitreální aplikaci bevacizumabu při prováděné trabekulektomii.
Do poslední skupiny lze zařadit všechna ostatní oční onemocnění, při kterých byl prokázán účinek bevacizumabu. Léčba těchto onemocnění byla většinou doložena pouze jednotlivými kazuistikami a obecně lze tedy říci, že použití Avastinu v těchto případech je možné, pokud selže nebo není dostupná standardní léčba těchto onemocnění. Jednotlivé indikace jsou uvedeny v tabulce (tab. 2) (17). Zvláštní indikací jsou neovaskularizace rohovky, při kterých je bevacizumab používán jako roztok ve formě kapek (11).
Tab. 2. Ostatní oční onemocnění léčené Avastinem 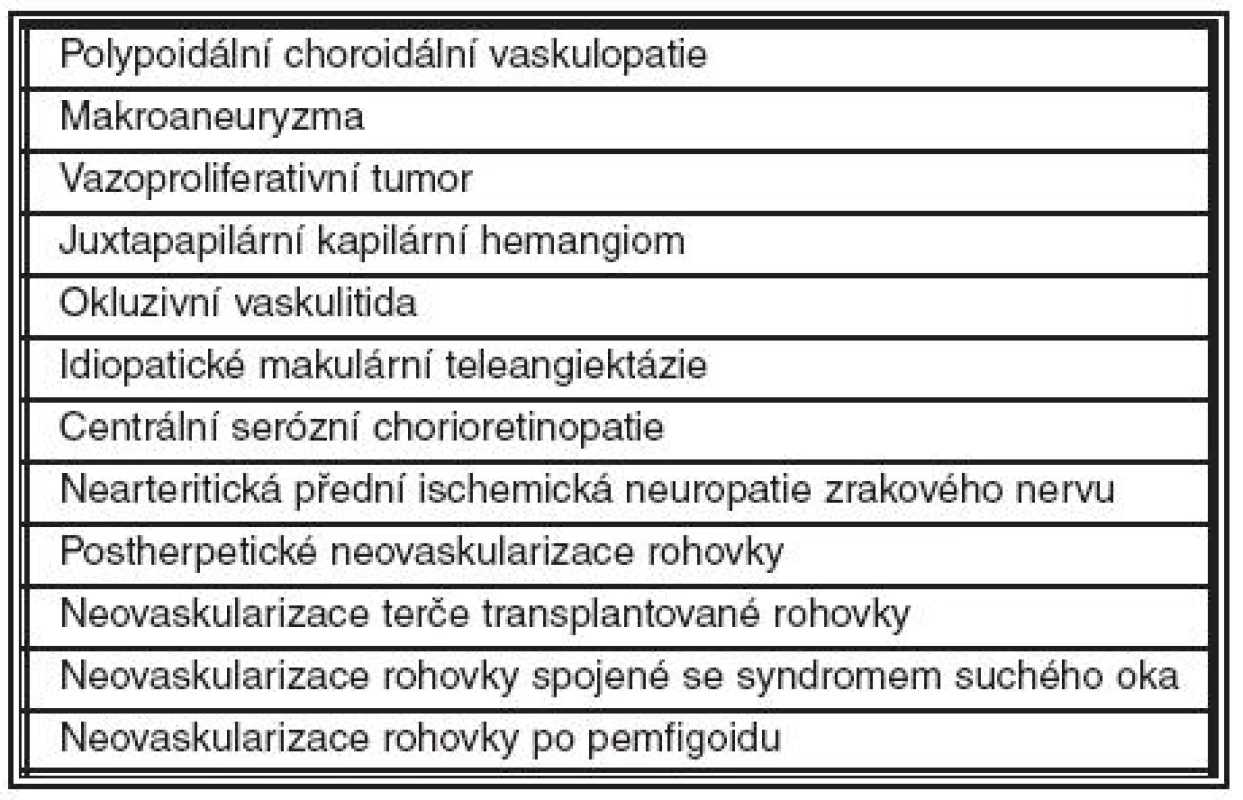
Bezpečnost použití Avastinu musí být ještě potvrzena randomizovanými srovnávacími studiemi. Současné práce ukazují mírně vyšší riziko ruptury retinálního pigmentového epitelu (RPE) u vlhké formy VPMD s okultní CNV a velkou ablací RPE (35, 43), další nežádoucí účinky jsou srovnatelné s ostatními anti VEGF preparáty, jak dokázalo zhodnocení ročních výsledků 1173 pacientů jihoamerické studie Pan – American Collaborative Retina Study Group (tab. 3) (48).
Tab. 3. Nežádoucí účinky Avastinu – výsledky Pan – American Collaborative Retina Study Group 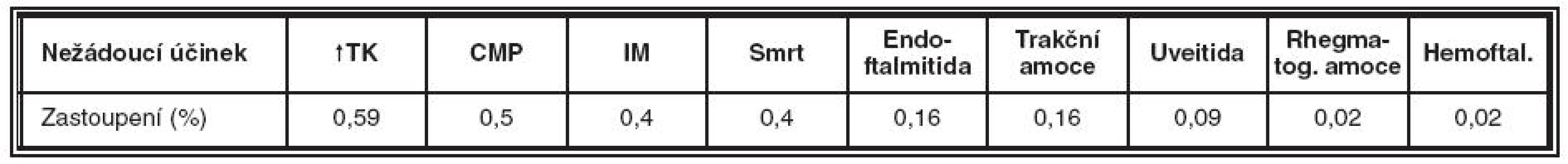
Závěr
Při přípravě bevacizumabu k intraokulární aplikaci je třeba dodržovat maximální míru bezpečnosti s důrazem na sterilitu připraveného léku. Účinnost a bezpečnost léčby je dokumentována řadou menších i větších studií a kazuistik u různých očních onemocnění. Protože Avastin zatím není celosvětově zdravotními národními autoritami schválen a registrován k očnímu užití, lze ho používat pouze způsobem off-label. V České republice lze takto používat lék v případě, že není známa standardní léčba potřebných terapeutických vlastností, nebo ji nelze použít a zároveň jsou pro vlastní užití vědecké předpoklady. Přestože je použití Avastinu dosud ještě ne zcela standardní léčbou, je stále více používán pro jeho vysokou efektivnost, malou míru nežádoucích účinků a nízkou cenu. Pokud výsledky současně probíhajících randomizovaných srovnávacích studií nebudou v přímém rozporu s dosud publikovanými výsledky, bude jistě Avastin již brzy zařazen mezi standardní oční léky.
Do redakce doručeno dne 21. 4. 2010
Do tisku přijato dne 15. 10. 2010MUDr. Jan Studnička, Ph.D.
Oční klinika FN a LF UK
Sokolská 581
500 05 Hradec Králové
e-mail: studnicka@fnhk.cz
Zdroje
1. Ahmadieh, H., Ramezani, A., Shoeibi, N. et al.: Intravitreal bevacizumab with or without triamcinolone for refractory diabetic macular edema: a placebo-controlled, randomized clinical trial. Graefes Arch Clin Exp Ophthalmol, 246(4), 2008, 483–9.
2. Algvere, P.V., von Wendt, G., Gudmundsson, J. et al.: Visual improvement in central retinal vein occlusion (CRVO) following intravitreal injections of bevacizumab (Avastin). Acta Ophthalmol, v tisku.
3. Anselem, L., Montero, J., Diaz-Llopis, M. et al.: Intravitreal bevacizumab (Avastin) injection in ocular ischemic syndrome. Am J Ophthalmol., 144(1), 2007, 122–4.
4. Arevalo, J.F., Sanchez, J.G., Wu, L. et al.: Intravitreal Bevacizumab for Subfoveal Choroidal Neovascularization in Age-Related Macular Degeneration at Twenty-four Months: The Pan-American Collaborative Retina Study Group. Ophthalmology, 2010.
5. Arevalo, J.F., Sanchez, J.G., Wu, L. et al.: Primary intravitreal bevacizumab for diffuse diabetic macular edema: the Pan-American Collaborative Retina Study Group at 24 months.Ophthalmology, 116(8), 2009, 1488–97.
6. Augustine, A.J., Puls, S., Offermann, I.: Triple therapy for choroidal neovascularization due to age-related macular degeneration: verteporfin PDT, bevacizumab, and dexamethasone. Retina, 27(2), 2007, 133–40.
7. Avery, R.L.: Regression of retinal and iris neovascularization after intravitreal bevacizumab (Avastin) treatment. Retina, 26(3), 2006, 352–4.
8. Avery, R.L., Pieramici, D.J., Rabena, M.D. et al.: Intravitreal bevacizumab (Avastin) for neovascular age-related macular degeneration. Ophthalmology, 113, 2006, 363–372.
9. Bakri, S.J., Donaldson, M.J., Link, T.P.: Rapid regression of disc neovascularization in a patient with proliferative diabetic retinopathy following adjunctive intravitreal bevacizumab. Eye, 20(12), 2006, 1474–5.
10. Cornish, K.S., Ramamurthi, S., Saidkasimova, S. et al.: Intravitreal bevacizumab and augmented trabeculectomy for neovascular glaucoma in young diabetic patients. Eye, 23(4), 2009, 979–81.
11. Dastjerdi, M.H., Al-Arfaj, K.M., Nallasamy, N. et al.: Topical bevacizumab in the treatment of corneal neovascularization: results of a prospective, open-label, noncomparative study. Arch Ophthalmol, 127(4), 2009, 381–9.
12. Doležalová, J., Karel, I., Hallová, H.: Naše dvouleté zkušenosti s léčbou vlhké formy věkem podmíněné makulární degenerace bevacizumabem (Avastin). Čes. a Slov. Oftal., 66 (1), 2010, 10–14.
13. Entezari, M., Ramezani, A., Safavizadeh, L. et al.: Resolution of macular edema in Coats disease. Indian J Ophthalmol., 58(1), 2010, 80–2.
14. Fang, X., Sakaguchi, H., Gomi, F. et al.: Efficacy and safety of one intravitreal injection of bevacizumab in diabetic macular oedema. Acta Ophthalmol, 86(7), 2008, 800–5.
15. Gharbiya, M., Allievi, F., Recupero, V. et al.: Intravitreal bevacizumab as primary treatment for retinal angiomatous proliferation: twelve-month results. Retina, 29(6), 2009, 740–9.
16. Grisanti, S., Biester, S, Peters, S. et al.: Intravitreal bevacizumab (avastin) in the treatment of neovascular glaucoma. Am J Ophthalmol, 142, 2006, 158–60.
17. Gunther, J.B., Altaweel M.M.: Bevacizumab for the treatment of ocular disease. Surv Ophthalmol, 54(3), 2009, 372–400.
18. Honda, S., Hirabayashi, H., Tsukahara, Y. et al.: Acute contraction of the proliferative membrane after an intravitreal injection of bevacizumab for advanced retinopathy of prematurity. Graefes Arch Clin Exp Ophthalmol, 246(7), 2008, 1061–3.
19. Chan, W.M., Lai, T.Y., Liu, D.T. et al.: Intravitreal bevacizumab (Avastin) for myopic choroidal neovascularization: six month results of a prospective pilot study. Ophthalmology, 114(12), 2007, 2190–6.
20. Chanana, B., Azad, R.V., Patwardhan, S. et al.: Role of intravitreal bevacizumab in the management of Eales disease. Int Ophthalmol, 30(1), 2010, 57–61.
21. Iliev, M.E., Domig, D., Wolf-Schnurrbursch, U. et al.: Intravitreal bevacizumab (Avastin) in the treatment of neovascular glaucoma. Am J Ophthalmol, 142(6), 2006, 1054–6.
22. Isaacs, T.W., Barry, C.: Rapid resolution of severe disc new vessels in proliferative diabetic retinopathy following a single intravitreal injection of bevacizumab (Avastin). Clin Experiment Ophthalmol, 34(8), 2006, 802–3.
23. Jonas, J.B., Spandau, U.H., Schlichtenbrede, F.: Intravitreal bevacizumab for filtering surgery. Ophthalmic Res, 39(2), 2007, 121–2.
24. Kahook, M.Y., Schuman, J.S., Noecker, R.J.: Intravitreal bevacizumab in a patient with neovascular glaucoma. Ophthalmic Surg Lasers Imaging, 37(2), 2006, 144–6.
25. Kaiser, P.K., Boyer, D.S., Garcia, R. et al.: Verteporfin photodynamic therapy combined with intravitreal bevacizumab for neovascular age-related macular degeneration. Ophthalmology, 116(4), 2009, 747–59.
26. Kitnarong, N., Chindasub, P., Metheetrairut, A.: Surgical outcome of intravitreal bevacizumab and filtration surgery in neovascular glaucoma. Adv Ther. 25(5), 2008, 438–43.
27. Lin, C.J., Hwang, J.F., Chen, Y.T. et al.: The effect of intravitreal bevacizumab in the treatment of Coats disease in children. Retina, 30(4), 2010, 617–22.
28. Mintz-Hittner, H.A., Kuffel, R.R. Jr.: Intravitreal injection of bevacizumab (avastin) for treatment of stage 3 retinopathy of prematurity in zone I or posterior zone II. Retina, 28(6), 2008, 831–8.
29. Moshfeghi, A.A., Rosenfeld, P.J., Puliafito, C.A. et al.: Systemic bevacizumab (Avastin) therapy for neovascular age-related macular degeneration: twenty-four-week results of an uncontrolled open-label clinical study. Ophthalmology, 113(11), 2006, 1–12.
30. Myung, J.S., Bhatnagar, P., Spaide, R.F. et al.: Long-term outcomes of intravitreal antivascular endothelial growth factor therapy for the management of choroidal neovascularisation in pseudoxanthoma elasticum. Retina, 30(5), 2010, 748–55.
31. Neri, P., Salvolini, S., Mariotti, C. et al.: Long-term control of choroidal neovascularisation secondary to angioid streaks treated with intravitreal bevacizumab (Avastin). Br. J. Ophthalmol.93(2), 2009, 155–8.
32. Ornek, K., Ornek, N.: Intravitreal bevacizumab treatment for refraktory diabetic macular oedema. J Ocul Pharmacol Ther, 24(4), 2008, 403–7.
33. Palmer, E.A, Hardy, R.J., Dobson, V. et al.: 15-year outcomes following threshold retinopathy of prematurity: final results from Multicenter Trial of Cryotherapy for Retinopathy of Prematurity. Arch Ophthalmol, 123, 2005, 311–18.
34. Priglinger, S.G., Wolf, A.H., Kreutzer, T.C. et al.: Intravitreal bevacizumab injections for treatment of central retinal vein occlusion: six month results of a prospective trial. Retina, 27(8), 2007, 1004–12.
35. Ronan, S.M., Yoganathan, P., Chien, F.Y. et al.: Retinal pigment epithelium tears after intravitreal injection of bevacizumab (avastin) for neovascular age-related macular degeneration. Retina, 27(5), 2007, 535–40.
36. Rosenfeld, P.J., Moshfeghi, A.A., Puliafito, C.A.: Optical coherence tomography findings after an intravitreal injection of bevacizumab (avastin) for neovascular age-related macular degeneration. Ophthalmic Surg Lasers Imaging, 36(4), 2005, 331–5.
37. Sawa, M., Gomi, F., Tsujikawa, M. et al.: Long-term results of intravitreal bevacizumab injection for choroidal neovascularisation secondary to angioid streaks. Am J Ophthalmol, 148(4), 2009, 584–590.
38. Schmidinger, G., Maar, N., Bolz, M. et al.: Repeated intravitreal bevacizumab (Avastin(R)) treatment of persistent new vessels in proliferative diabetic retinopathy after complete panretinal photocoagulation. Acta Ophthalmol, v tisku.
39. Sivak-Callcott, J.A., O’Day, D.M., Gass, D.M. et al.: Evidence-based recommendations for the diagnosis and treatment of neovascular glaucoma. Ophthalmology, 108, 2001, 1767–76.
40. Soheilian, M., Ramezani, A., Obudi, A. et al.: Randomized trial of intravitreal bevacizumab alone or combined with triamcinolone versus macular photocoagulation in diabetic macular edema. Ophthalmology, 116(6), 2009, 1142–50.
41. Spaide, R.F., Laud., K., Fine, J.F.F. et al.: Intravitreal bevacizumab treatment of choroidal neovascularization secondary to age-related macular degeneration. Retina, 26, 2006, 383–90.
42. Vasudev, D., Blair, M.P., Galasso, J. et al.: Intravitreal bevacizumab for neovascular glaucoma.J Ocul Pharmacol Ther, 25(5), 2009, 453–8.
43. Weinberger, A.W., Thiel, M., Mohammadi, B. et al.: Retinal pigment epithelium tears after intravitreal bevacizumab in pigment epithelium detachment. Am J Ophthalmol, 144(2), 2007, 294–6.
44. Wiegand, T.W., Rogers, A.H., McCabe, F. et al.: Intravitreal bevacizumab (Avastin) treatment of choroidal neovascularisation in patients with angioid streaks. Br. J. Ophthalmol., 93(1), 2009, 47–51.
45. Wu, L., Arevalo, J.F., Berrocal, M.H. et al.: Comparison of two doses of intravitreal bevacizumab as primary treatment for macular edema secondary to branch retinal vein occlusions: results of the Pan American Collaborative Retina Study Group at 24 months. Retina, 29(10), 2009, 1396–403.
46. Wu, L., Arevalo, J.F., Berrocal, M.H. et al.: Comparison of two doses of intravitreal bevacizumab as primary treatment for macular edema secondary to central retinal vein occlusions: results of the pan American collaborative retina study group at 24 months.Retina, 30(7), 2010, 1002–11.
47. Wu, L., Arevalo, J.F., Maia, M. et al.: Comparing outcomes in patients with subfoveal choroidal neovascularization secondary to age-related macular degeneration treated with two different doses of primary intravitreal bevacizumab: results of the Pan-American Collaborative Retina Study Group (PACORES) at the 12-month follow-up. Jpn J Ophthalmol, 53(2), 2009, 125–30.
48. Wu, L., Martinez-Castellanos, M.A., Quiroz-Mercado, H. et al.: Twelve-month safety of intravitreal injections of bevacizumab (Avastin): results of the Pan-American Collaborative Retina Study Group (PACORES). Graefes Arch Clin Exp Ophthalmol, 246(1), 2008, 81–7.
Štítky
Oftalmológia
Článek Ako zvládnuť úzku zrenicu?
Článok vyšiel v časopiseČeská a slovenská oftalmologie
Najčítanejšie tento týždeň
2010 Číslo 5- Dlouhodobé výsledky lokální léčby cyklosporinem A u těžkého syndromu suchého oka s 10letou dobou sledování
- Cyklosporin A v léčbě suchého oka − systematický přehled a metaanalýza
- Účinnost a bezpečnost 0,1% kationtové emulze cyklosporinu A v léčbě těžkého syndromu suchého oka − multicentrická randomizovaná studie
- Pomocné látky v roztoku latanoprostu bez konzervačních látek vyvolávají zánětlivou odpověď a cytotoxicitu u imortalizovaných lidských HCE-2 epitelových buněk rohovky
- Konzervační látka polyquaternium-1 zvyšuje cytotoxicitu a zánět spojený s NF-kappaB u epitelových buněk lidské rohovky
-
Všetky články tohto čísla
- Diabetická retinopatie – rizikové faktory, prevence a terapie
- Selektivní laserová trabekuloplastika v léčbě glaukomu – výsledky v tříletém sledování
- Vplyv sférických a asférických umelých vnútroočných šošoviek na kvalitu centrálnej ostrosti zraku a kontrastnej citlivosti
- Subjektivní zrakové vnímání po laserové operaci myopie provedené na dvou typech laserů
- Ako zvládnuť úzku zrenicu?
- Zrakové evokované potenciály v manažmente amblyopie u detí
- Indikace Avastinu v oftalmologii
- Primář MUDr. Karel Vrba zemřel
- Česká a slovenská oftalmologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Indikace Avastinu v oftalmologii
- Diabetická retinopatie – rizikové faktory, prevence a terapie
- Subjektivní zrakové vnímání po laserové operaci myopie provedené na dvou typech laserů
- Selektivní laserová trabekuloplastika v léčbě glaukomu – výsledky v tříletém sledování
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



