-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Léčba diabetického makulárního edému mikropulsním laserem – první zkušenosti
Treating Diabetic Macular Edema by a Micropulse Laser – First Findings
Introduction:
Diabetic macular edema (DME) is the most common cause of a visus dicrease in patients suffering type 2 diabetes. DME originates in abnormal macula capillars permeability. This study presents the findings of observing patients with DME after by micropulse laser therapy with the wavelength of 577 nm.Methods:
The study covers 23 eyes of 15 patients with focal or difuse DME. In all patients we performed a 577 nm micropulse laser therapy of the macula, proceeding by a technique of placing spots next to each other in the shape of EDTRS optotype letters. In average we performed 3 treatments per eye.Results:
Best-corrected visual acuity (BCVA) was 61,8 of a letter at the beginning, 62,5 of a letter after 3 months, 59,5 of a letter after 6 months, 57,6 of a letter after 9 months and 59,2 of a letter after 12 months. The average difference between BVAC at the beginning and after a year was -2.7 of a letter. A T-test does shows statistically insignificant difference.
The average central retinal thickness (CRT) was 380,4 µm at the beginning, 368,1 µm after 3 months, 327,5 µm after 6 months, 329,2 µm after 9 months and 301,0 µm after 12 months. The difference between the average CRT at the beginning and after 12 months was -79,5 µm. A T-test shows statistically significant difference.Discussion:
Our studied group reported visus improvement or stabilization in 61% of eyes and decrease or stabilization of DME in 83% of eyes. Without treatment a deterioration would occur due to the progressive nature of the disorder. Taking into account these results and relevant literature we resolved to change our treatment methods in favour of placing laser spots as close as possible. An evaluative study of this method will follow.Conclusion:
In the studied group the average CRT improved and the average BCVA remained virtually equal. Treating DME by means of a micropulse laser has proven to be an effective method. It does not leave scars on retina and thus prevents creating scotoms. If the edema is higher or a resistent cyst occurs in the macula, it is recommended to combine laser and anti-VEGF therapies. In case of insufficient effects of a laser therapy there is a possibility of combining it with an anti-VEGF treatment.Key words:
diabetic macular edema, laser treatment, micropulse laser
Autoři: M. Závorková; L. Procházková
Působiště autorů: Oční klinika UJEP, Krajská zdravotní a. s., Masarykova nemocnice Ústí nad Labem primářka MUDr. Ivana Liehneová Ph. D.
Vyšlo v časopise: Čes. a slov. Oftal., 71, 2015, No. 5, p. 223-228
Kategorie: Původní práce
Souhrn
Úvod:
Diabetický makulární edém (DME) je nejčastějším důvodem poklesu vízu u diabetiků 2. typu. Příčinou DME je abnormální permeabilita kapilár makuly. Cíl: Autorky prezentují výsledky sledování pacientů s DME po léčbě mikropulsním laserem s vlnovou délkou 577 nm.Metodika:
Do souboru bylo zařazeno celkem 23 očí 15 pacientů s fokálním nebo difúzním DME. U všech pacientů bylo provedeno ošetření makuly mikropulsním laserem 577 nm, byla použita technika kladení stop vedle sebe jako písmena ETDRS optotypů, průměrně proběhlo 2,5 sezení léčby.Výsledky:
Nejlépe korigovaná zraková ostrost (NKZO) byla na počátku sledování 61,8 písmene ETDRS, po 3 měsících 62,5 písmene, po 6 měsících 59,5 písmene, po 9 měsících 57,6 písmene, po 12 měsících 59,2 písmene. Rozdíl mezi průměrnou NKZO počáteční a po roce byl -2,7 písmene. Rozdíl není podle t-testu statisticky významný. Centrální tloušťka sítnice (CRT) byla na počátku sledování průměrně 380,4 µm, po 3 měsících 368,1 µm, po 6 měsících 327,5 µm, po 9 měsících 329,2 µm, po 12 měsících 301 µm. Rozdíl mezi průměrnou CRT počáteční a po 12 měsících byl -79,5 µm. Rozdíl podle t-testu je statisticky významný na 1% hladině významnosti.Diskuse:
V našem souboru došlo ke snížení nebo stabilizaci DME u 83 % očí a ke zlepšení nebo stabilizaci vízu u 61 % očí. Vzhledem k progresívní povaze onemocnění by bez léčby došlo k jeho zhoršení. Na základě tohoto sledování a v souladu s literaturou jsme v současné době změnily léčebný postup, používáme techniku kladení laserových stop těsně vedle sebe. Nová pozorování budeme prezentovat.Závěr:
V našem souboru došlo ke zlepšení průměrné CRT a průměrná NKZO zůstala prakticky stejná. Léčba DME mikropulsním laserem se jeví jako účinná metoda, jejíž hlavní výhodou je, že nedochází k tvorbě jizev na sítnici a tím možné tvorbě skotomů. Při nedostatečném efektu léčby laserem máme možnost kombinace s anti-VEGF léčbou.Klíčová slova:
diabetický makulární edém, laserová léčba, mikropulsní laserÚvod
Diabetická retinopatie (DR) a diabetický makulární edém (DME) jsou závažné komplikace diabetu (DM). DME je nejčastějším projevem DR, který způsobuje pokles vízu. DME je zároveň nejčastější příčinou poklesu centrální zrakové ostrosti v populaci do 50 let v rozvinutých zemích. Jedná se tedy o závažný společenský a ekonomický problém.
Cílem práce byla prezentace výsledků sledování pacientů s DME po léčbě mikropulsním laserem s vlnovou délkou 577 nm.
Epidemiologie: Celosvětově existuje velké množství studií zabývajících se epidemiologií DR, DME a klinicky signifikantního DME (KSME). KSME je definován jako DME, který bezprostředně ohrožuje foveu a centrální zrakovou ostrost [13]. Prevalence DME a KSME je závislá na typu DM, délce jeho trvání, věku pacienta a etnické skupině [20]. Prevalence edému narůstá nejen s délkou onemocnění, ale i s vyšší hladinou glykovaného hemoglobinu a proteinurií [16]. Klinicky signifikantní DME postihuje 6 až 10 % pacientů s DM [4]. Dle Českého statistického úřadu bylo v roce 2012 v ČR evidováno celkem 841 227 diabetiků (442 388 žen a 398 839 mužů), což tvořilo 8 % populace [22]. Výskyt DME není v ČR statisticky sledován, ale je prováděn aktivní screening DR a DME [5,6]. Za předpokladu 6–10% prevalence KSME u pacientů s DM je možno předpokládat, že počet pacientů, kteří během života prodělají KSME, bude v ČR mezi 50 a 84 tisíci (0,5 % až 0,6 % obyvatelstva).
Patofyziologie: Příčinou DME je abnormální permeabilita kapilár makuly. Závažnost vaskulární patologie je významně ovlivněna genetickou dispozicí jedince a je modifikována dalšími metabolickými (hyperglykémie, dyslipidémie a inzulinová rezistence) a hemodynamickými faktory (hypertenze) [12]. Za oční rizikový faktor je považována operace katarakty. Naopak protektivní účinek je přisuzován chorioretinálním jizvám, amblyopii a pravděpodobně i vysoké myopii. Ochranným mechanismem je zřejmě ztráta gangliových buněk a tím snížená metabolická aktivita sítnice, stejně jako hemomodulační změny při chorioretinálním pnutí cév, což je jeden z principů laserové léčby DR [17].
Léčba: Současné možnosti léčby DME jsou vedle laserové terapie také intravitreální aplikace blokátorů vaskulárního růstového faktoru (VEGF) či kortikosteroidů nebo provedení pars plana vitrektomie (PPV) [18]. V ČR je v tuto chvíli schválena léčba laserem, PPV a léčba anti-VEGF preparátem ranibizumabem a afliberceptem. Laserová léčba DME může být provedena klasickou metodou fokální fotokoagulace u fokálního edému nebo mřížkovou fotokoagulací u difúzního DME [7]. Další možností léčby je moderní mikropulsní fotokoagulace. Early Treatment Diabetic Retinopathy Study (ETDRS) ukázala u pacientů po fokální fotokoagulaci pro DME 50% redukci nebezpečí vzniku středně závažného poklesu vízu, zlepšení o více než 15 písmen však lze očekávat zhruba u 3 % pacientů po 3 letech sledování [13,14]. Efekt fokální fotokoagulace může být z části díky okluzi prosakujících mikroaneurysmat, přesný mechanismus redukce edému po fotokoagulaci je však neznámý [15].
Princip mikropulsní laserové léčby DME: Puls laseru není kontinuální, ale je rozdělen do 100 mikropulsů, přičemž délka „on“ a „off“ režimu je volitelná. Při volbě „5 % duty cycle“ bude celková délka expozice 10ms z celkové délky pulsu 200 ms. Tím nedochází k termickému poškození sítnice a netvoří se klinicky detekovatelná jizva – biomikroskopicky, autofluorescencí, fluorescenční angiografií nebo optickou koherenční tomografií (OCT). Princip tzv. pravé subtreshold fotokoagulace znamená, že jizva není detekovatelná žádnou metodou v době léčby ani v budoucnu [9]. V laboratorních zkouškách na myších bylo prokázáno, že při použití 5 % duty cyklu laseru 810 nebo 532 nm bylo obtížné histologicky rozeznat jakákoli narušení sítnice nebo poškození retinálního pigmentového epitelu (RPE) v oblasti stopy laseru [21].
Soubor
Do souboru byli zařazeni pacienti, u kterých byla započata léčba pro DME za použití mikropulsního módu laseru na našem oddělení od února roku 2012 do října 2013. Sledovací doba byla 12 měsíců.
Charakteristika souboru
Do souboru bylo zařazeno celkem 23 očí 15 pacientů (12 mužů a 3 žen). U 7 pacientů bylo sledováno jen jedno oko (na druhém oku jednoho pacienta byl stav po pars plana vitrektomii a peelingu MLI, u dalšího pacienta byl stav po centrální venózní okluzi, u jednoho pacienta byl stav po větvové venózní okluzi a další 4 pacienti měli DME jen na jednom oku). Do souboru nebyli zařazeni pacienti, u kterých byla možná terapie anti-VEGF preparáty nebo na tuto léčbu v průběhu sledování přestoupili. Průměrný věk pacientů byl 67,7 roku (směrodatná odchylka (SD) 10,1 roku, medián 68 let). Dva pacienti byli léčeni pro DM 1. typu, 13 pacientů pro DM 2. typu. Trvání DM bylo od 2 do 31 let, průměrně 18,8 roku, SD 8,2 roku, medián 20 let. Celkem 7 pacientů bylo léčeno perorálními antidiabetiky, 5 pacientů inzulínem a 3 pacienti kombinací perorálních antidiabetik a inzulínu. V osobní anamnéze mělo 11 pacientů léčbou kompenzovanou arteriální hypertenzi, 3 pacienti stav po infarktu myokardu a 1 pacient stav po proběhlé cévní mozkové příhodě. Glykovaný hemoglobin (HbA₁C) byl na začátku sledování průměrně 68,1 mmol/mol, SD 17,2 mmol/mol, medián 66 mmol/mol (min. 45, max. 115 mmol/mol). Po 6 měsících byl HbA₁C průměrně 65,5 mmol/mol, SD 16,4 mmol/mol, medián 65 mmol/mol (min. 40, max. 108 mmol/mol). Na konci sledování byl HbA₁C průměrně 66,3 mmol/mol, SD 13,7 mmol/mol, medián 63 mmol/mol (min. 50, max. 95 mmol/mol). Na začátku i na konci sledování mělo 6 pacientů HbA₁C ≤ 60 mmol/mol.
U 9 očí byla diagnostikována středně pokročilá neproliferativní DR (NPDR II), u 13 očí těžká neproliferativní DR (NPDR III) a na jednom oku počínající proliferativní DR (PDR I). Před započetím mikropulsní léčby makuly byla u 9 očí s NPDR II provedena fokální fotokoagulace (FK) sítnice mimo makulu a u 14 ostatních očí fotokoagulace panretinální (PRFK). PRFK byla ukončena vždy déle než 3 měsíce před započetím mikropulsní léčby. Fokální FK střední periferie sítnice byla provedena také před mikropulsní FK, v případě potřeby byla doplňována. Celková doba od první fotokoagulace sítnice do začátku léčby DME mikropulsním laserem byla v intervalu od 3 měsíců až do 11 let, průměrně 4,1 roku, SD 3,6 roku, medián 3 roky. Trvání makulopatie bylo od 1 měsíce až po 10 let, průměrně 2,2 roku (SD 2,4 roku, medián 1,3 roku). U 8 očí byl popisován fokální DME a u 15 očí difúzní DME (tab. 1). Před započetím mikropulsní FK byla provedena fokální FK makuly u 15 očí. Fokální FK byla vždy provedena minimálně 3 měsíce před mikropulsní FK. Průměrně byla fokální FK makuly provedena 10,8 měsíců před mikropulsní FK (SD 6,7 měsíce a medián 11 měsíců).
Tab. 1. Charakteristika souboru 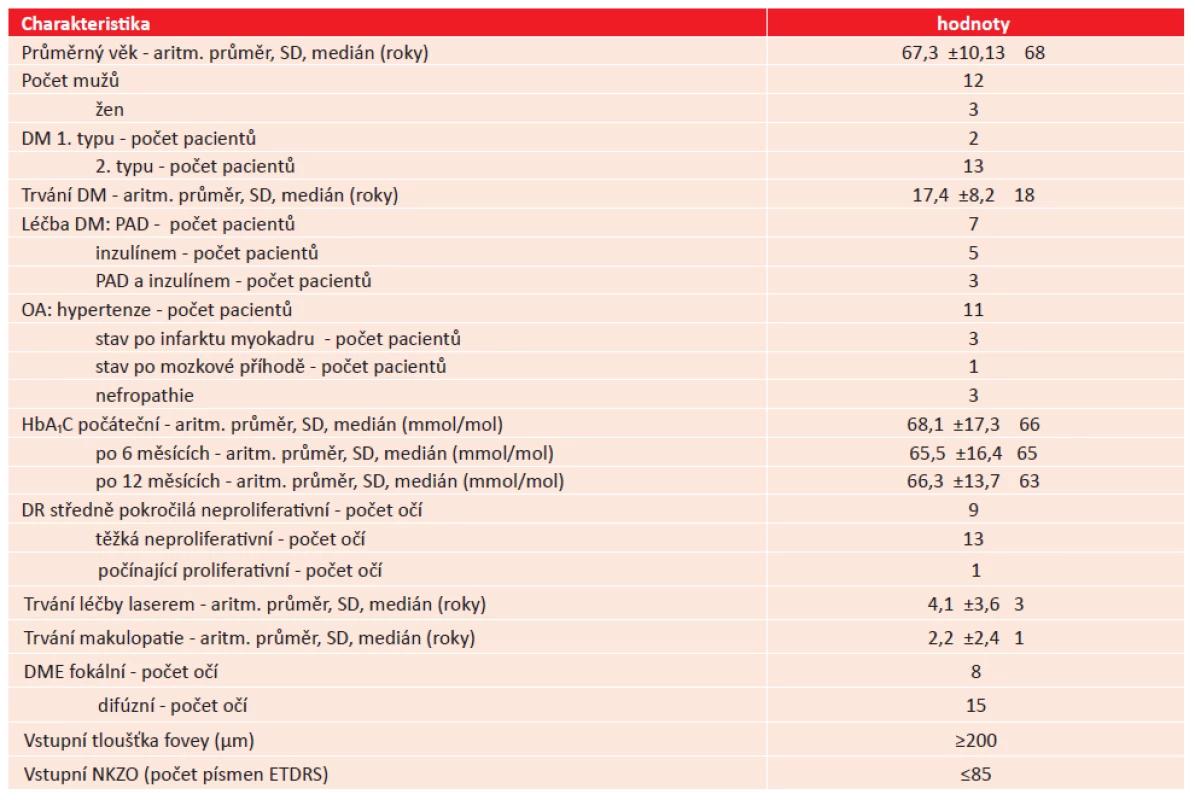
Metodika
U všech pacientů byla provedena fotokoagulace makuly žlutým diodovým laserem o vlnové délce 577 nm značky IQ 577™ IRIDEX. Byl použit mikropulsní 5% duty cycle mód laserového paprsku. To znamená, že při celkové expozici 200 ms byla účinná dávka laseru rozdělena do 100 mikropulsů, jejichž souhrnná délka je 5% tedy 10 ms. Každý mikropuls trval 2,0 ms, z tohoto času byl laser zapnut 0,1 ms a 1,9 ms vypnut. Dozování energie bylo prováděno v oblasti nazálně od papily kontinuálním módem laseru, byla použita stopa o průměru 100 µm, čas 100 ms a energie nejprve 50 mW. Postupně byla energie zvyšována až do úrovně, kdy na sítnici zůstala viditelná stopa. Potom byl nastaven mikropulsní mód 5% duty cycle, expozice 200 ms a energie 2-3krát větší než energie naměřená při dozování. Stopy byly kladeny vedle sebe jako písmena ETDRS, tzn. mezera mezi stopami stejně velká jako laserová stopa. Stopy nejsou na sítnici viditelné, orientace je možná jen podle paměti. Mikropulsní fotokoagulace byla prováděna vždy podle aktuálního stavu makuly, a proto při zlepšení nálezu nebyla prováděna při každé kontrole.
Vízus byl měřen s nejlepší korekcí na ETDRS optotypech a ve výsledcích je uváděn v písmenech ETDRS optotypů (dále jen písmena) jako nejlépe korigovaná zraková ostrost (NKZO).
Tloušťka sítnice byla měřena na OCT od začátku studie na přístroji Zeiss Stratus a od února 2014 na přístroji Spectralis. V obou případech bylo měření nastaveno na vzdálenost mezi membránou limitans interna a Bruchovou membránou. Interval sledování byl 3 měsíce.
Výsledky
CRT byla na počátku sledování průměrně 380,4 µm (SD 146,0 µm, medián 380 µm). Po 3 měsících byla CRT průměrně 368,1 µm (SD 141,6 µm, medián 320 µm). Po 6 měsících byla CRT průměrně 327,5 µm (SD 105,6 µm, medián 323 µm). Po 9 měsících byla CRT průměrně 329,2 µm (SD 113,2 µm, medián 317 µm). Po 12 měsících byla CRT průměrně 301 µm (SD 110,6 µm, medián 288 µm). Rozdíl mezi průměrnou CRT počáteční a po 12 měsících byl -79,5 µm. Rozdíl je podle t-testu statisticky významný na 1% hladině významnosti (tab. 2, graf 1).
Tab. 2. Tloušťka fovey udávaná v μm během ročního sledování 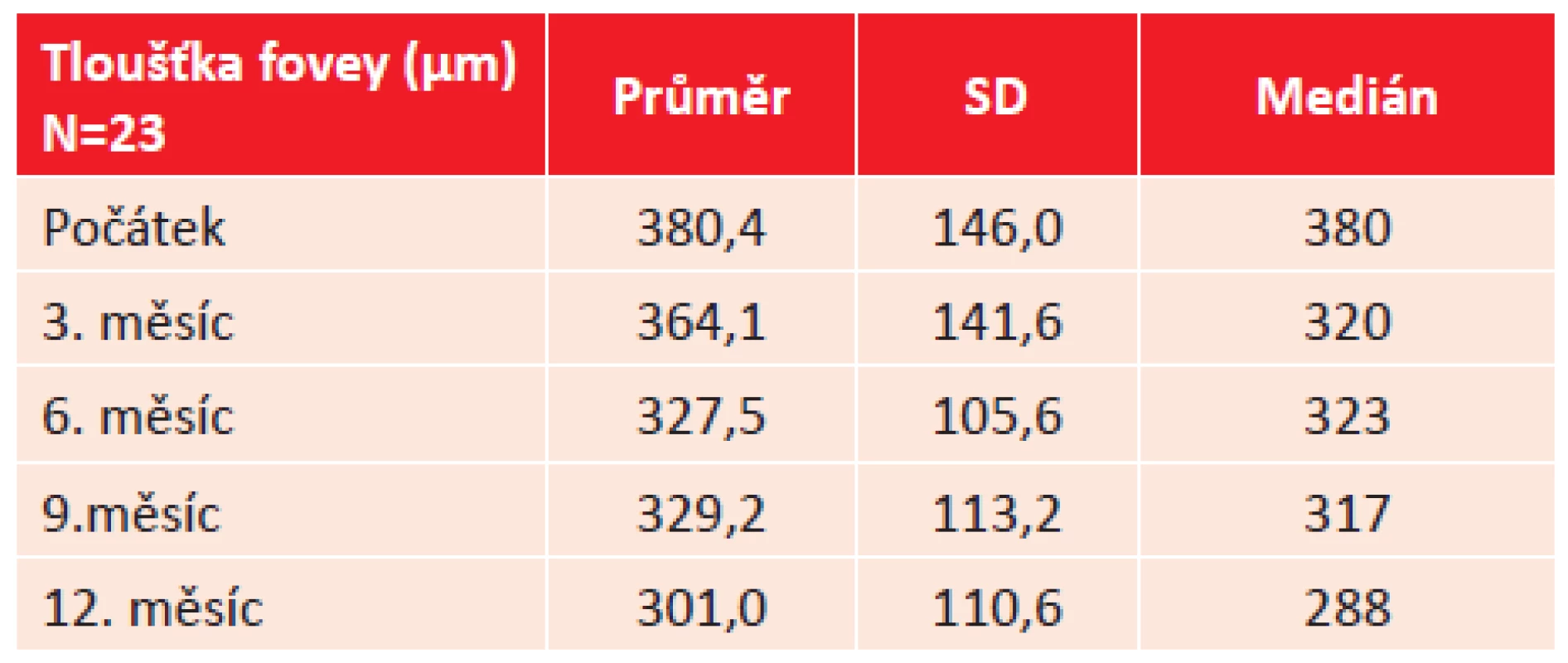
Graf 1. Tloušťka fovey udávaná v μm během ročního sledování. 
Celkem u 13 očí (57 %) došlo v průběhu sledování ke snížení CRT o více než 30 µm. U 6 očí (26 %) byl rozdíl mezi prvním a posledním měřením menší nebo roven ± 30 µm a u 4 očí (17 %) došlo ke zhoršení o více než 30 µm.
NKZO byla na počátku sledování 61,8 písmene (SD 14,2 a medián 60 písmen). Po 3 měsících 62,2 písmene (SD 14,4 a medián 65 písmen). Po 6 měsících 59,5 písmene (SD 13,6 a medián 60 písmen). Po 9 měsících 57,6 písmene (SD 12,8 a medián 58 písmen). Po 12 měsících 59,2 písmene (SD 14,2 a medián 60 písmen). Průměrný rozdíl mezi počáteční NKZO a po 12 měsících byl -2,7 písmene. Rozdíl podle t-testu není statisticky významný (tab. 3, graf 2).
Tab. 3. NKZO udávaná v počtech písmen ETDRS optotypů během ročního sledování 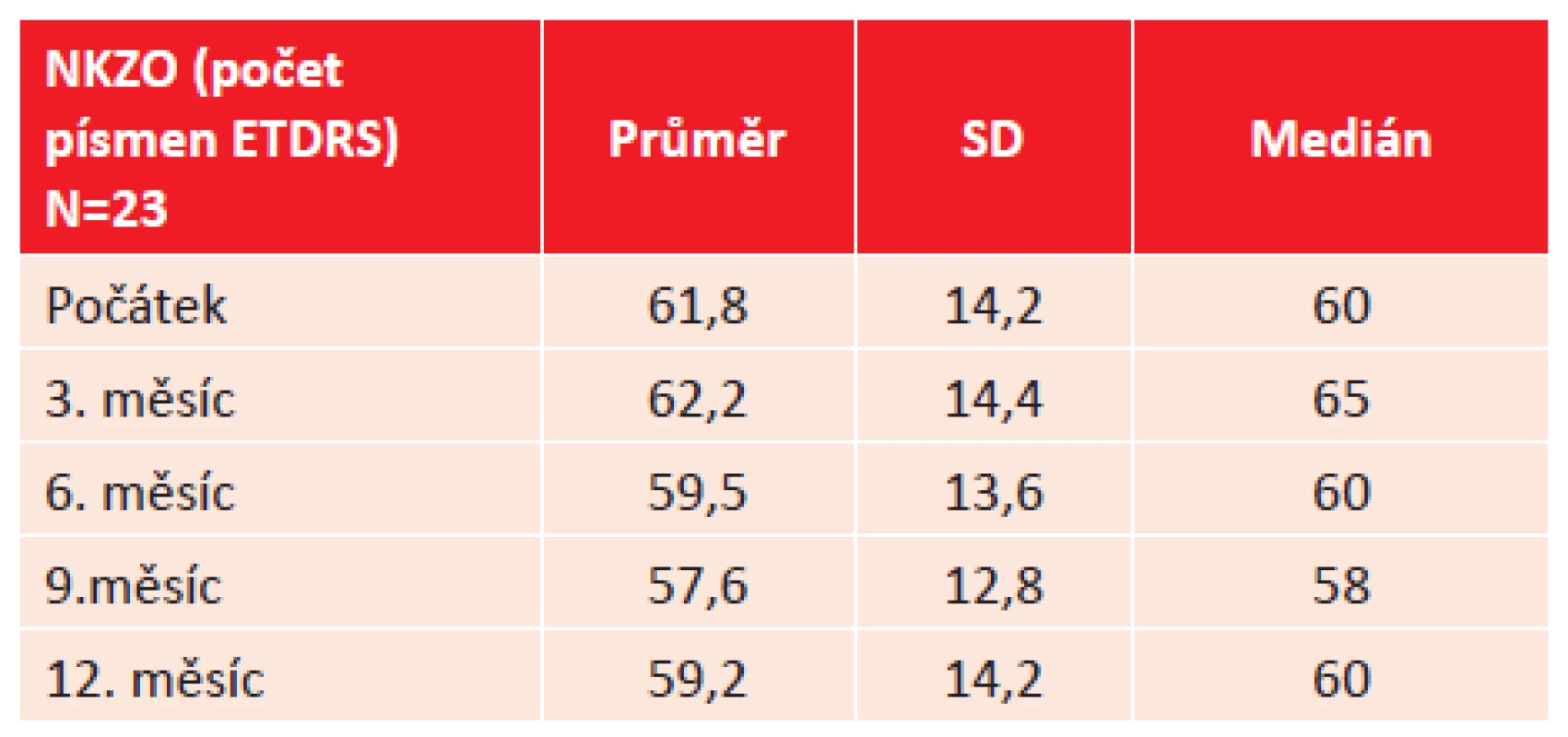
Graf 2. NKZO udávaná v počtech písmen ETDRS optotypů během ročního sledování. 
Celkem u 5 očí (22 %) došlo v průběhu sledování ke zlepšení NKZO minimálně o 5 písmen. U 9 očí (39 %) zůstala NKZO nezměněna a u 9 očí (39 %) došlo ke zhoršení o více než 5 písmen (obrázek 1). U dvou očí došlo ke zhoršení o 15 a více písmen ETDRS, konkrétně 1x o 15 písmen a 1x o 16 písmen.
Obr. 1. Příklad OCT: snížení CRT po roce o 214 μm, ale došlo ke zhoršení vízu o 5 písmen. 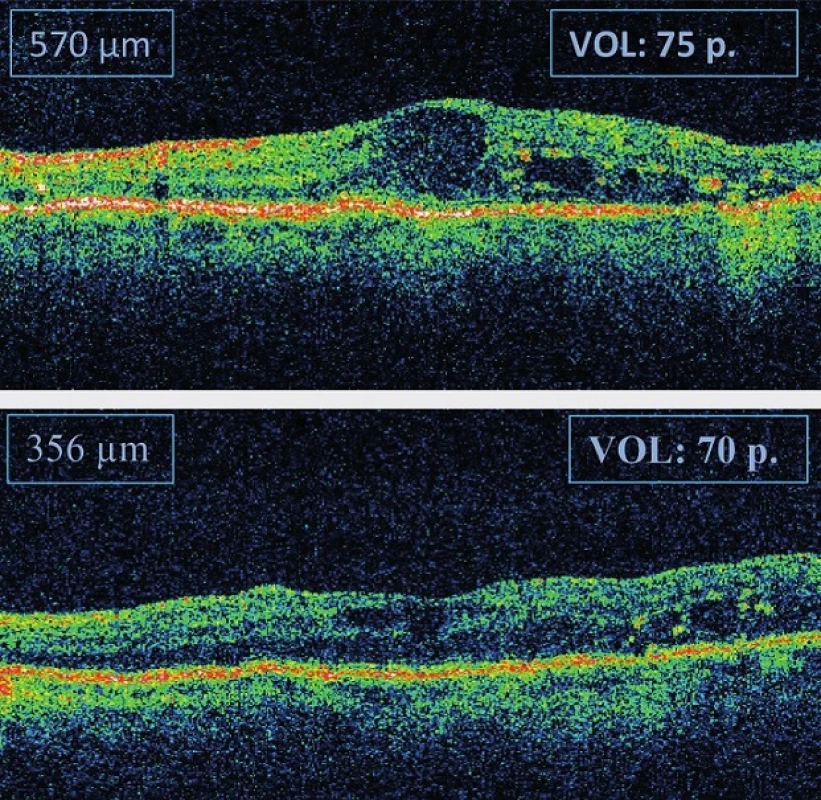
Průměrný počet sezení fotokoagulací byl 3,0 (SD 0,8 a medián 3 sezení). Jedenkrát byla fotokoagulace makuly provedena u 1 oka (4 %), dvakrát u 5 očí (22 %), třikrát u 10 očí (44 %) a čtyřikrát u 7 očí (30 %). Průměrný počet bodů byl 929,4 (SD 504,5 a medián 882,5). Průměrná energie použitá k fotokoagulaci byla 307,9 mW (SD 95,7 mW a medián 300 mW).
Diskuse
Naše klinické výsledky můžeme porovnat s výsledky klinických studií, kde byla použita klasická metoda mřížkové fotokoagulace. Ve studii RESTORE byla jedna skupina pacientů léčena monoterapií laserem (injekce ranibizumabu byla předstírána), po 12 měsících byla NKZO zlepšena o 0,9 písmene a CRT snížena o 61,3 µm. Vstupním kritériem byla NKZO v rozmezí 39 až 78 písmen ETDRS a DME snižující vízus [11]. Stejné rameno tzn. předstírání injekce ranibizumabu a aktivní léčba laserem bylo i ve studii DRCR.net. Zde po 12 měsících došlo ke zlepšení NKZO průměrně o 3 písmena a snížení CRT o 102 µm. Vstupními kritérii byly NKZO mezi 24 a 78 písmeny a DME zahrnující foveu [2].
Z literatury o léčbě DME mikropulsním laserem lze provést srovnání s prací z univerzity v Římě a Padově, která prezentuje výsledky léčby DME mikropulsním laserem 810 nm. V ročním sledování došlo ke zlepšení NKZO o 1 písmeno (0,02 logMAR) a snížení CRT o 46,6 µm. Vstupním kritériem byly NKZO minimálně 35 písmen a CTR větší nebo rovna 250 µm [19]. Další práce z univerzity v Sao Paulu srovnávala mikropulsní léčbu s normální a vysokou hustotou stop za použití laseru 810 nm. Vstupními kritérii byly NKZO mezi 20/40 a 20/400 a CRT mezi 250 a 500 µm. Lepších výsledků dosáhlo rameno léčené s vysokou hustotou stop (těsně vedle sebe), po jednom roce dosáhli zlepšení NKZO o 12,5 písmene a snížení CRT o 154 µm, oproti tomu v rameni s normální hustotou bodů došlo ke zhoršení NKZO o 1,5 písmene a CTR se snížila o 32 µm [8]. Pro srovnatelnost jsou všechny výsledky NKZO převedeny na písmena ETDRS [1].
Do naší práce jsme zařadily i pacienty s fokálním DME s NKZO 85 písmen a CRT nižší než 250 µm. Ve srovnání s výše zmíněnými studiemi dosahujeme horších průměrných výsledků NKZO, kdy po roce došlo ke snížení NKZO o 2,7 písmene ETDRS. Snížení CRT o 79,5 µm je s některými studiemi srovnatelné. Subanalýzou pacientů s CRT 250 µm a vyšší dostaneme skupinu 17 očí 13 pacientů. Průměrná NKZO na začátku sledování byla 60,1 písmene a po roce 59,3 písmene, rozdíl byl zhoršení NKZO o 0,8 písmene. Průměrná CRT na začátku byla 438,1 µm a po roce 334,3 µm, došlo ke zlepšení CRT o 103,8 µm (tab. 4).
Tab. 4. Srovnání výsledků studií a publikovaných prací o laserové léčbě DME s našimi výsledky 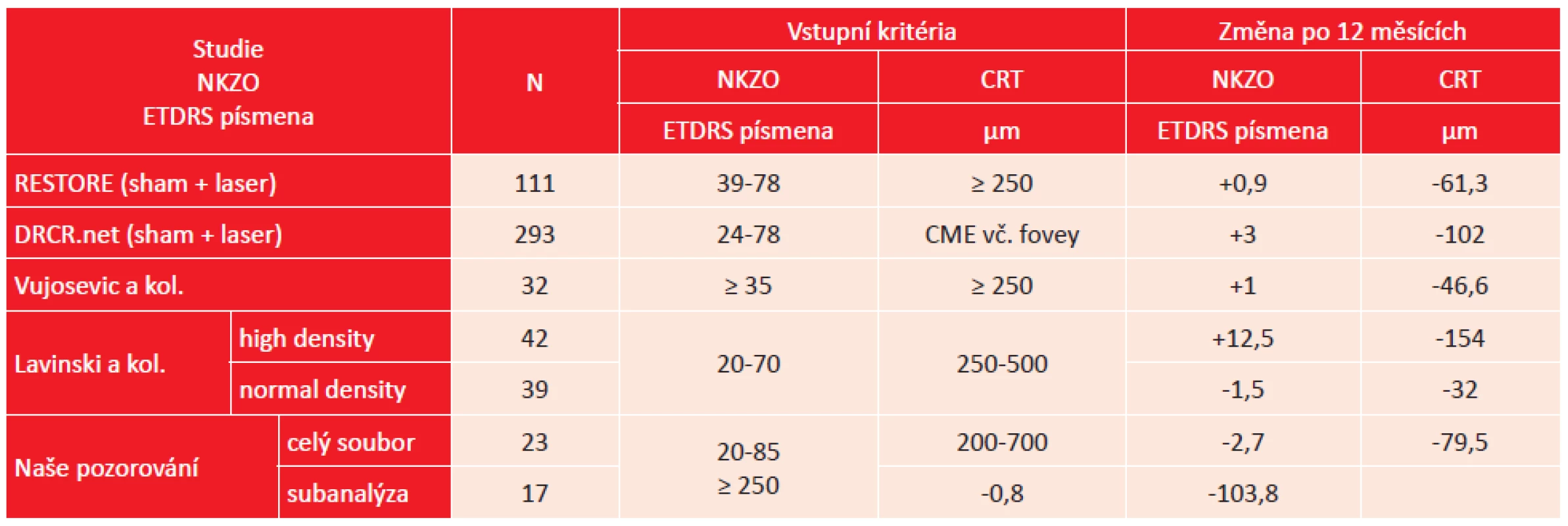
Dle doporučení výrobce laseru je použití mikropulsní laserové terapie DME účinné zvláště u pacientů s mírným DME s dobrým vízem a otokem okolo fovey, kteří nejsou kandidáty pro anti-VEGF injekci nebo u pacientů, kde anti-VEGF léčba selhává [3]. V našem souboru je zařazeno 6 očí 5 pacientů s edémem 500 µm a více. Tloušťka fovey byla na počátku průměrně 573,3 µm po 12 měsících 369,2 µm, došlo tedy ke zlepšení o 204,2 µm. NKZO byla na počátku 55,8 písmene a po 12 měsících 53,3 písmene, rozdíl byl -2,5 písmene ETDRS. Zlepšení CRT nastalo u všech 6 očí, ke zlepšení NKZO však došlo jen u 1 oka, 2 očí zůstaly stabilní a u 3 očí došlo ke zhoršení NKZO. Pozorování u tak malého souboru není statisticky významné, ale naznačuje možnost využití mikropulsní léčby i u těžších forem DME.
V současné době je v ČR schválená a hrazená zdravotní pojišťovnou léčba DME anti-VEGF preparátem ranibizumabem, která má podle mezinárodních klinických studií vyšší účinnost než léčba laserem [2,11]. Důvodem pro nezařazení pacientů z našeho souboru do léčby ranibizumabem byla u 6 pacientů skutečnost, že v roce 2012 ještě nebyl ranibizumab hrazen zdravotní pojišťovnou, u dalších 11 nebyla splněna indikační kritéria úhrady na začátku léčby mikropulsním laserem, ani v průběhu sledování. Hlavním nesplněným kritériem bylo u 3 pacientů překročení 12 měsíců trvání DME při zařazení do souboru, u 4 pacientů byl HbA₁C vyšší než 60 mmol/mol, u 3 pacientů byla centrální tloušťka fovey nižší než 300 µm a u jednoho pacienta vízus lepší než 6/12 na Snellenových optotypech (což odpovídá 4/8 na ETDRS optotypech). Od listopadu 2014 jsou kritéria úhrady ranibizumabu pro DME změněna (HbA₁C může být do 70 mmol/mol a délka DME do 24 měsíců), naše pozorování bylo ukončeno před tímto datem. Další anti-VEGF preparátem schváleným pro léčbu DME v ČR je aflibercept, který v současnosti nemá stanovenou úhradu zdravotní pojišťovnou pro léčbu DME. Pro žádného z našich pacientů nebyla léčba ranibizumabem nebo afliberceptem v režimu samoplátce finančně dostupná.
V našem souboru došlo ke snížení nebo stabilizaci DME u 83 % očí, ale ke zlepšení nebo stabilizaci vízu u 61 % očí. Pokračující zhoršování vízu u některých pacientů, navzdory zlepšení tloušťky fovey, připisujeme postupující diabetické neuropatii.
Na základě tohoto sledování a v souladu s nejnovějším doporučením [10] jsme v současné době změnily léčebný postup, používáme techniku kladení laserových stop těsně vedle sebe. Nová pozorování budeme prezentovat.
Závěr
Léčba DME mikropulsním laserem se jeví jako účinná metoda, jejíž hlavní výhodou je, že nedochází k tvorbě jizev na sítnici a tím možné tvorbě skotomů. Vhodné je její použití u dvou skupin pacientů. První skupinou jsou pacienti s nově zjištěným DME. Při nedostatečném efektu laserové léčby je potom u těchto pacientů možno použít léčbu anti-VEGF preparáty, neboť anti-VEGF léčba je dle indikačních kritérií možná až po selhání laserové léčby. Druhou skupinu tvoří pacienti, u kterých není léčba anti-VEGF preparáty možná nebo selhává, u kterých zároveň není přítomnost adhezivních membrán, a proto není indikováno operační řešení DME.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmu a není podpořeno žádnou farmaceutickou firmou.
Do redakce doručeno dne 11. 12. 2014
Do tisku přijato dne 25. 9. 2015
MUDr. Martina Zázvorková
Oční klinika UJEP, Krajská zdravotní, a.s.
Masarykova nemocnice
Sociální péče 3316/12A
401 13 Ústí nad Labem
e-mail: martina.zavorkova@kzcr.eu
Zdroje
1. Beck, RW., Moke, PS., Turpin, AH. at al.: A computerized method of visual acuity testing: adaptation of the early treatment of diabetic retinopathy study testing protocol. Am J Ophthalmol, 135; 2003, 2 : 194–205.
2. Elman, MJ., Aiello, LP., Beck, RW.: Randomized trial evaluating ranibizumab plus prompt or deferred laser or triamcinolone plus prompt laser for diabetic macular edema. Ophthalmology, 117; 2010 : 1064 –1077.
3. Feistmann, JA., Rosenthal, JL.: Making the Jump to MicroPulse Laser Therapy for Treating the Macula, An effective first-line therapy or adjunct to current treatments. MicroPulse safely treats areas of the retina including the fovea.Iridex [online] Dostupné na WWW:
http://www.iridex.com/Portals/0/pdf/Rosenthal_Feistmann_webinar_writeup.pdf4. Chen, E., Looman, M., Laouri, M. et al.: Burden of illness of diabetic macular edema: literature review. Curr Med Res Opin, 26; 2010, 7 : 1587–97.
5. Kalvodová, B.: Screening diabetické retinopatie v ČR – guideline. Čes a Slov Oftal, 58; 2002 : 3–10.
6. Kalvodová, B., Oudová, P.: Screening diabetické makulopatie. Čes a Slov Oftal, 58; 2002 : 11–15.
7. Kalvodová, B., Pelikánová, T. et al.: Doporučené postupy pro diagnostiku a léčbu diabetické retinopatie. Čes a Slov Oftal, 68; 2012 : 236–241.
8. Lavinsky, D., Cardillo, JA., Mělo, LA. Jr. et al.: Randomized clinical trial evaluating mETDRS versus normal or high-density micropulse photocoagulation for diabetic macular edema. Invest Ophthalmol Vis Sci, 52; 2011, 7 : 4314–23.
9. Luttrull, JK., Dorin, G.: Subtreshold Diode Micropulse Laser Photocoagulation (SMD) as Invisible Retinal Phototherapy for Diabetic Macular Edema: A Review, Current Diabetes Reviews, 2012; 8 : 274–284.
10. Mansour, S., Gossage, D.: Tissue-sparing MicroPulse 577 nm Laser Therapy: The “Aha” Moment from the Ultimate Skeptic. Supplement to Retina today, 2012, 6/7 : 4–6.
11. Mitchell P., Bandello F., Schmidt-Erfurth U.: The RESTORE study: ranibizumab monotherapy or combined with laser versus laser monotherapy for diabetic macular edema. Ophthalmology, 2011; 118 : 615–625.
12. Pelikánová, T.: Patogeneze Diabetické retinopatie. Vnitř Lék, 53; 2007, 5 : 498–505.
13. Photocoagulation for diabetic macular edema: Early Treatment Diabetic Retinopathy Study report number 1. Early Treatment Diabetic Retinopathy Study research group. Arch Ophthalmol, 103; 1985 : 1796–1806.
14. Early photocoagulation for diabetic retinopathy. ETDRS report number 9. Early Treatment Diabetic Retinopathy Study Research Group. Ophthalmology, 98; 1991, 5 Suppl: 766–85.
15. Shamsi, HN., Masaud, JS., Ghazi NG.: Diabetic macular edema: New promising therapies. World J Diabetes, 4; 2013, 6 : 324–38.
16. Sosna, T., Švancarová, R., Netuková, M. et al.: Současný pohled na diabetický makulární edém. Čes a Slov Oftal, 68; 2012 : 91–97.
17. Sosna, T., Švancarová, R., Netuková, M.: Diabetická retinopatie – rizikové faktory, prevence a terapie. Čes a Slov Oftal, 66; 2010 : 195–203.
18. Studnička, J.: Diabetický makulární edém – nové možnosti léčby. Čes a Slov Oftal, 68; 2012 : 61–63.
19. Vujosevic, S., Bottega, E., Casciano, M. et al.: Microperimetry and fundus autofluorescence in diabetic macular edema: subthreshold micropulse diode laser versus modified early treatment diabetic retinopathy study laser photocoagulation. Retina, 30; 2010 6 : 908–16.
20. Williams, R. Airey, M. Baxter, H.: Epidemiology of diabetic retinopathy and macular oedema: a systematic review, Eye [online]. 2004, č.18. [cit. 2 July 2004] Dostupné na WWW: <http://www.nature.com/eye/journal/v18/n10/full/6701476a.html#abs>
21. Yu, AK., Merrill, KD., Truong, SN. et al.: The comparative histologic effects of subthreshold 532 - and 810-nm diode micropulse laser on the retina. Invest Ophthalmol Vis Sci, 54; 2013, 3 : 2216–24.
22. Zvolský, M.: Činnost oboru diabetologie, péče o diabetiky v roce 2012, ÚZIS ČR [online]. 2013 č.24 [cit. 9. července 2013] Dostupné na WWW: www.uzis.cz/rychle-informace/cinnost-oboru-diabetologie-pece-diabetiky-roce-2012
Štítky
Oftalmológia
Článek Oční myiáza
Článok vyšiel v časopiseČeská a slovenská oftalmologie
Najčítanejšie tento týždeň
2015 Číslo 5- Dlouhodobé výsledky lokální léčby cyklosporinem A u těžkého syndromu suchého oka s 10letou dobou sledování
- Cyklosporin A v léčbě suchého oka − systematický přehled a metaanalýza
- Účinnost a bezpečnost 0,1% kationtové emulze cyklosporinu A v léčbě těžkého syndromu suchého oka − multicentrická randomizovaná studie
- Pomocné látky v roztoku latanoprostu bez konzervačních látek vyvolávají zánětlivou odpověď a cytotoxicitu u imortalizovaných lidských HCE-2 epitelových buněk rohovky
- Konzervační látka polyquaternium-1 zvyšuje cytotoxicitu a zánět spojený s NF-kappaB u epitelových buněk lidské rohovky
-
Všetky články tohto čísla
- Léčba diabetického makulárního edému mikropulsním laserem – první zkušenosti
- Výsledky léčby diabetického makulárního edému laserovým systémem PASCAL
- Prevalencia DIAbetickej RETinopatie a význam genetických faktorov v rozvoji diabetickej retinopatie u pacientov s diabetes mellitus typu 1. a 2. na Slovensku (DIARET SK). Prehľad aktuálnych poznatkov a postavenie epidemiologickej štúdie DIARET SK
- Aflibercept v léčbě diabetického makulárního edému
- Možnosti chirurgické léčby diplopie u pacientů s endokrinní orbitopatií
- Solární makulopatie po sledování částečného zatmění slunce
- Oční myiáza
- Česká a slovenská oftalmologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Oční myiáza
- Možnosti chirurgické léčby diplopie u pacientů s endokrinní orbitopatií
- Solární makulopatie po sledování částečného zatmění slunce
- Léčba diabetického makulárního edému mikropulsním laserem – první zkušenosti
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



