-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Invazivní metody při léčbě žilní insuficience
Invasive Therapy for Chronic Venous Insuficiency
Venous diseases and their complications are highly prevalent in the adult population (40–50%), with the prevalence of chronic venous insufficiency (CVI) being 5–30%. The authors present current knowledge about vasculogenesis and genetic factors playing a role in the pathogenesis of chronic venous insufficiency, anatomy and pathophysiology of the lower limb circulation, treatment with emphasis on modern minimally invasive outpatient methods including endovenous laser ablation, radiofrequency ablation, mechanochemical ablation, use of cyanoacrylate adhesive and ultrasonically controlled sclerosis foaming.
Keywords:
chronic venous insuficiency – varices – mini-invasive methods
Autori: A. Havlínová
Pôsobisko autorov: Dermatovenerologická klinika 1. LF UK a VFN, přednosta prof. MUDr. Jiří Štork, CSc.
Vyšlo v časopise: Čes-slov Derm, 94, 2019, No. 1, p. 7-17
Kategória: Souborné referáty (doškolování lékařů)
Súhrn
Žilní onemocnění a jejich případné komplikace představují stavy postihující 40–50 % dospělé populace, 5–30 % trpí chronickou žilní nedostatečností. Autoři předkládají současné poznatky o vaskulogenezi a genetických faktorech uplatňujících se při vzniku chronické žilní nedostatečnosti, anatomii a patofyziologii žilního oběhu dolních končetin, léčbě s důrazem na moderní minimálně invazivní ambulantní metody zahrnující endovenózní laserovou ablaci, radiofrekvenční ablaci, mechanochemickou ablaci, použití cyanoakrylátového lepidla a ultrazvukem kontrolovanou sklerotizaci pěnou.
Klíčová slova:
chronická žilní insuficience – varixy – miniinvazivní metody
ÚVOD
Chronická žilní insuficience (CVI, chronická žilní nedostatečnost) postihuje různými formami v průběhu života 40–50 % populace. Incidence pokročilé formy se závažnými komplikacemi se uvádí až 6%. Onemocnění se může komplikovat varikoflebitidou a krvácením z varixů, což opět prodlužuje léčbu nemocného. Oproti tomu CVI i s výraznějšími varikozitami bez komplikací postihuje až 20–25 % [25, 43, 53].
Žilní nedostatečnost může být buď primární, nebo sekundární čili posttrombotická. Z patofyziologického hlediska rozdělujeme varixy na kongenitální (např. syndrom Klippel Trenaunay, Parkes-Weberův syndrom), primární (idiopatické), kde se uplatňuje geneticky podmíněná méněcennost žilní stěny a nedomykavost žilních chlopní, progesteron způsobující žilní dilataci. Sekundární varixy jsou následkem hluboké žilní trombózy (HŽT). Vzniká tak posttrombotický syndrom, kde je pak kladen hlavní důraz na antikoagulační léčbu jako prevenci rekurencí.
EMBRYOLOGIE A GENETIKA
Vaskulogeneze, což je vznik cév de novo z krevních ostrůvků, počíná ve 3. týdnu vývoje extraembryonálně v primárním mezodermu, kdy se ve stěně žloutkového váčku, zárodečného stvolu a choria zakládají krevní ostrůvky z angioblastů. Z intraembryonálního mezenchymu se pak formují krevní ostrůvky embryonálních cév. Krevní ostrůvky luminizují, na povrchu vzniká endotel cévních trubic, uvnitř cirkulující erytroblasty. Následuje fáze angiogeneze, což je další tvorba cévního řečiště pučením z již založených cév [36].
Genetika u primárních varixů je do současnosti ne zcela jasná, ale nepopíratelně její roli potvrzují studie postižení homozygotních dvojčat. Studiem různých kohort pacientů byly navrhovány dokonce různé způsoby dědičnosti. Nejběžněji bývala uváděna autozomálně recesivní dědičná vazba, mnohem vzácněji byly rysy dědičnosti slučitelné s dominantním chováním alely. Studiem postižení rodin dokladovatelným ve více generacích se ale zdá, že ve skutečnosti neexistuje jednoznačný důkaz pro vazbu gonozomálního typu. Při neúplné penetranci a expresivitě pak nadále převažuje pohled na CVI spíše jako na onemocnění multifaktoriální a mnoho případů představuje sporadické postižení konkrétního pacienta.
Z jednodušších monogenních systémů definující klinické syndromy je známa asociace CVI s mutací transkripčního faktoru fork head box protein C2 (FOXC2). Obdobně může být mutován gen NOTCH3 v rámci syndromu CADASIL.
Mechanistický pohled na patogenezi CVI je zaměřen na změny strukturálních komponent žilní stěny. V tomto ohledu je významná regulace syntézy a odbourávání například kolagenu I matrixmetaloproteázami a jejich specifickými inhibitory.
V insuficientní žilní stěně dochází k separaci svalových vláken vyúsťující v žilní dilataci. Příčinou vzniku primárních varixů je zvýšení hladiny metaloproteinázy-2 a aktivity kolagenu v buněčné matrix [61]. Některé další metabolicky významné dráhy mohou také navozovat labilitu žilní stěny, jako je tomu například u hyperhomocysteinémie, či při mutacích a následné poruše funkce trombomodulinu. Vznik varixů podporuje i mutace genu desmuslin lokalizovaného na chromozomu 15q26.3. Desmuslin je přítomen v cytoplazmě hladkého svalu [33, 58, 62]. Protein desmuslin interaguje v intermediálních filamentech buněčné stěny hladkého svalu s desminem a alfa dystrobrevinem, a zajišťují tak jeho sílu.
Mezi klasické syndromy spojené se vznikem primárních varixů zapříčiněných chromozomální aberací (balancované translokace 8 : 14 a 5p:11q) patří Klippel-Trenaunay syndrom (kombinace varixů, port wine stain neboli kožní kapilární malformace a hypertrofie kostí a měkkých tkání jedné dolní končetiny). Podobný, ale geneticky odlišný je pak syndrom Parkes Weber s mutací RASA1. Dále se uvádí i mutace EII3K a VG5Q genu kódujícího angiogenní faktor, ke které dochází v šestém gestačním týdnu (vaskulární diferenciace a invaze cév do končetinových základů) či v osmém gestačním týdnu v důsledku selhání vývoje laterálních embryonálních okrajů končetin [35]. Obdobně může být asociována varikozita se syndromem Ehlerse-Danlose.
ANATOMIE
Žilní systém je nedílnou součástí kardiovaskulárního systému a jeho úkolem ve velkém krevním oběhu je odvádět odkysličenou krev z tkání a orgánů k srdci, kde dále cestou malého plicního krevního oběhu dojde opět k jejímu okysličení. Žíly představují také kapacitní součást cévního řečiště a jejich náplň tedy může být jako určitá zásoba redistribuována podle aktuální potřeby organismu.
Žilní systém dolních končetin (DK) začíná na periferii v kapilárním systému svalstva a ostatních tkání DK. Žilní systém DK anatomicky rozdělujeme na dvě skupiny žil. Toto určení je dáno jejich polohou vůči svalové fascii. Rozlišujeme tedy žíly povrchové (epifasciální) a žíly hluboké (subfasciální, či hypofasciální). Povrchové žíly na DK tvoří hustou síť, ale odvádějí z dolní končetiny přibližně jen 10 % cévního návratu. Většina je z končetiny odváděna cestou žil hlubokého systému. Tato bohatá epifasciální síť anastomozuje s hlubokým žilním systémem četnými perforátory, jejichž počet a poloha je individuálně velmi variabilní. Tok krve v perforátorech je fyziologicky jednosměrný a je usměrňován chlopněmi. Chlopně směřují tok krve z povrchového do hlubokého žilního systému. Povrchový i hluboký systém jsou také vybaveny četnými chlopněmi, které mají bránit ale zpětnému proudění krve do periferie končetiny – tj. distálně. Ztráta kompetence žilních chlopní vede k neadekvátnímu směru toku krve, tedy k stagnaci, městnání v distální části končetiny a k přetížení epifasciálního řečiště, které reaguje dilatací a vznikem tortuozit.
V povrchovém žilním systému DK jsou anatomicky definovány 3 významné žíly: vena saphena magna (VSM), v. saphena parva (VSP) a variabilně vytvořená v. femoropoplitea (VFP). Jako variabilní žíla se udává spojka mezi VSM a VSP dorzálně (v. Giacomini).
VSM (obr. 1) je kmenová žíla, v průměru dosahuje u zdravého dospělého přibližně 6 mm. VSM začíná ze žilních pletení na hřbetu nohy, míří proximálně před okrajem tibiálního kotníku na přední mediální okraj bérce a dále za mediální kondyl femuru a přetáčí se anteromediálně na stehno, kde směřuje k transfasciálnímu otvoru – tzv. hiatus saphenus. Zde VSM ústí do veny femoralis (tj. do hlubokého žilního systému). Ve svém průběhu je vybavena řadou chlopní a ústí do ní v celém průběhu bérce řada drobnějších podkožních žil: na stehně z podkožních žil na přední straně stehna a dále vena saphena accessoria – ant., lat., med., post. z daného podkoží stehna. V intimní blízkosti VSM probíhá senzitivní nervus saphenus.
Obr. 1. Vena saphena magna varikózně rozšířená 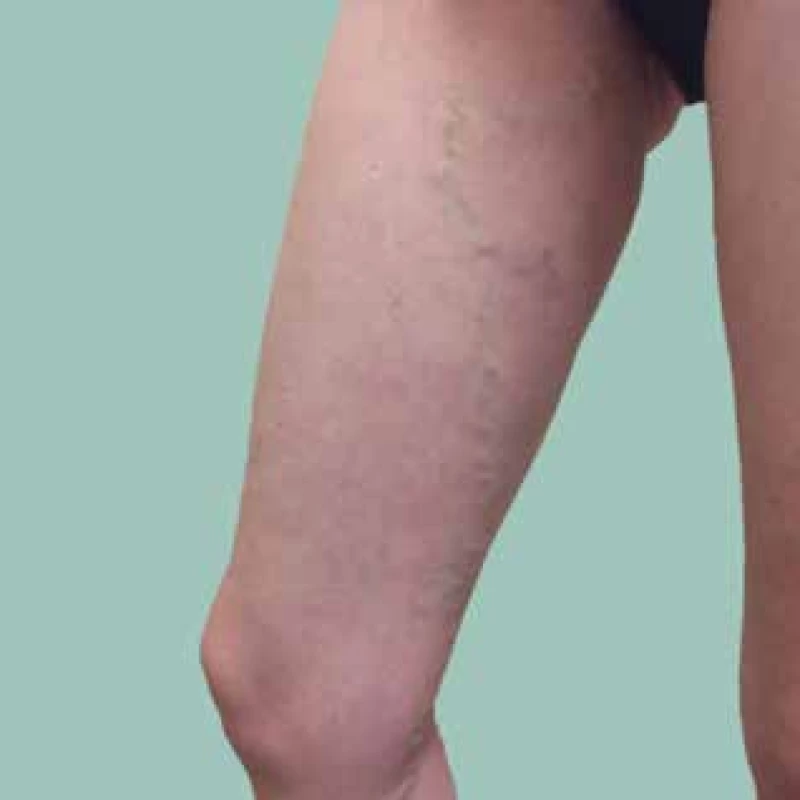
V oblasti hiatus saphenus VSM ústí do vena femoralis. Do terminálního úseku VSM či přímo do VF pak směruje několik typických žilních větví z podkoží, toto místo se nazývá Cocketova hvězdice a patří do ní: v. epigastrica superior, v. circumflexa ilium superficialis, v. thoracoepigastrica (z podkoží přední stěny hrudní a břišní), vv. pudendae externae (z genitálu). Jejich dilatace může evidentně při klinickém vyšetření svědčit pro žilní onemocnění.
VSP (obr. 2) je poněkud tenčí, lumen dosahuje zpravidla
3 mm. VSP též začíná na hřbetu nohy a přechází za fibulárním
kotníkem na zadní plochu lýtka při zevní straně Achillovy šlachy a poté již přibližně v ose lýtka vedené mezi oběma hlavami m. gastrocnemius nad fascií. Zde je doprovázena nervus suralis. Opět přibírá řadu drobnějších větví z podkoží zadní a zevní plochy lýtka, variabilně i ze stehna. Je i zde vytvořeno též množství perforátorů, které prochází povrchovou fascií a spojují řečiště VSP s hlubokým žilním systémem. Přibližně v proximální části lýtka proráží VSP povrchovou fascii spolu s nervus cutaneus surae medialis a jde mezi oběma hlavami m. gastrocnemius. Proximálně ve fossa poplitea je lokalizován soutok, kdy přibírá VFP, která odvádí krev z hýžďových svalů distálním směrem a za svého průběhu přibírá řadu větví z podkoží zadní plochy stehna.Obr. 2. Vena saphena parva – masivní varixy, pozdní záchyt 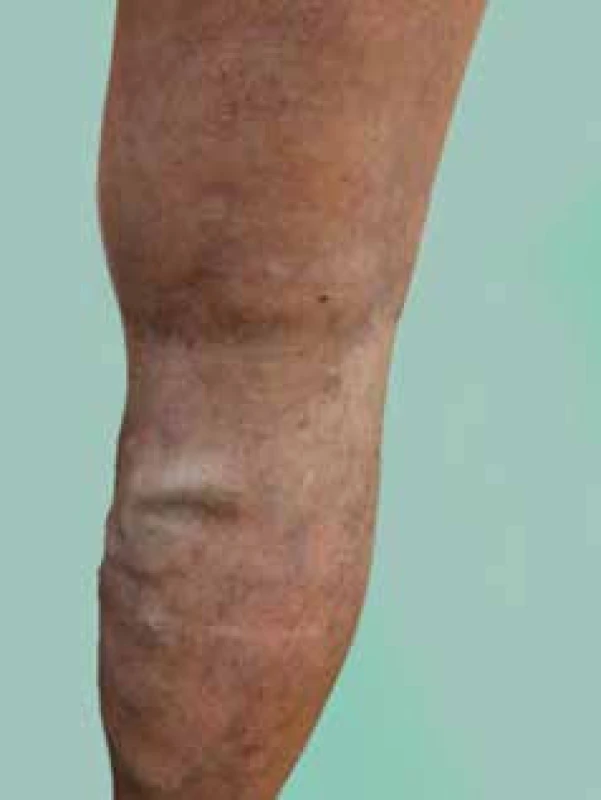
Jak již bylo uvedeno, jsou ve svém průběhu jmenované magistrální žíly vybaveny řadou často bezejmenných a interindividuálně variabilních spojek, kterými mnohonásobně anastomozují.
Subfasciálně uložený hluboký žilní systém DK tvoří v periferii většinou ve dvojicích uspořádané žíly, které doprovází tepenné kmeny. Tyto dvojice jsou proto nazývány venae comitantes. V proximální třetině lýtka se spojují
vv. tibiales posteriores a vv. tibiales anteriores a vzniká základ v. poplitea (VP). Se vstupem VSP a VFP pokračuje
většinou z počátku ještě dvojitý žilní kmen dále již jako
jednotná v. femoralis (VF). VF pak v canalis vastoadductorius
probíhá do trigonum femorale. V canalis femoropopliteus je VF uložena za arteria femoralis (je povrchněji) a ve fossa
iliopectinea je již uložena mediálně od arterie. VF za svého průběhu přibírá vv. comitantes ze svalů přední strany stehna a v. profunda femoris. V trigonum femorale přijímá jako přítok VSM. VF pak pokračuje do lacuna vasorum pod lig. inguinale a proximálně v pánvi přechází jako v. illiaca externa.Nutno zdůraznit, že žilní systém má velikou variabilitu, co se týče místa spojek a větvení.
Zejména v mladém věku je žilní systém vybaven velkým množstvím žilních chlopní, které brání zpětnému toku krve v obou systémech i v jejich perforátorech. Tok krve v DK proti gravitaci umožňuje svalová pumpa za podpory fungujících žilních chlopní. Takto to funguje u zdravých žil. S věkem, dědičně, hormonálně a z příčiny různých onemocnění dochází k poškození a následné insuficiencí chlopní i žilní stěny. To vede k městnání krve v žilním systému s následnou tvorbou žilních městků, varixů [32, 44].
HISTOLOGIE ŽILNÍ STĚNY
V oblasti dolních končetin je nejtenčí tunica intima ze všech míst na těle. Jsou zde prodloužené pásy hladké svaloviny. Tunica intima rovněž tvoří dvojcípé chlopně ve formě záhybů, které obsahují kolagenní vlákna. Tunica media je složena ze svalových vrstev probíhajících kruhovitě či spirálovitě, jsou řidší a někdy kompaktnější, dále se zde nachází šikmo uspořádané mřížky kolagenních vláken a širokých elastických vláken. Poslední, zevní vrstva, tunica externa neboli adventicia přechází do okolního vaziva. Skládá se z kolagenního vaziva a svalových vláken. Na větších žilách, které mají silnější stěnu, se nachází vyživovací síťovitě roztroušená spleť – vasa vasorum [32].
PATOFYZIOLOGIE
Při chronické žilní insuficienci (CVI) dochází ke změnám povrchového i hlubokého žilního systému vedoucím ke vzniku žilní hypertenze. V důsledku insuficience žilních chlopní dochází k žilnímu refluxu z hemodynamických důvodů (obrácení toku krve – tedy zpět do distálních úseků a potažmo do povrchových žil). Aktivita svalů dolních končetin neboli „svalová pumpa“ tento (patologický) proces již neovlivní. Důsledkem žilní hypertenze jsou změny v mikrocirkulaci (výměna tekutin mezi kapilárami, intersticiem a lymfatickými cévami) vedoucí k formaci edému (nerovnováha mezi hydrostatickým a osmotickým tlakem, zvýšená permeabilita kapilár převážně pro albumin a fibrinogen, který se postupně polymerizuje na fibrin) [11, 28].
Dalším etiopatogenetickým faktorem vzniku CVI je shlukování leukocytů v důsledku zpomalení žilního toku, proto leukocyty adherují k endotelu a uvolňují jak reaktivní formy kyslíku a dusíku, tak proteolytické lyzosomální enzymy. Výsledkem je další poškození endotelu a zhoršení mikrocirkulace [40]. Zpomalení žilního toku také vede ke shlukování erytrocytů intraluminárně s následným vznikem mikrotrombózy a nakonec dochází k ischémii postižené oblasti a destrukci tkáně [7, 12, 42].KLINICKÉ PROJEVY A KLASIFIKACE
CVI má velmi polymorfní příznaky v oblasti dolních končetin, které zahrnují kosmetickou nespokojenost pacienta, pocit tíhy, pocit svědění až pálení, během dne se zhoršující edém, převážně noční křeče, parestezie až bolesti doprovázející ulcus cruris. V identifikaci souvislosti takto mnohotvárných obtíží s žilní nedostatečností nám napomáhá klasifikace žilního postižení podle CEAP (tab. 1).
Tento klasifikační model nahradil starší zjednodušující schémata a osvojení si tohoto praktického rozdělení příznaků žilní nedostatečnosti přímo vede k snazší volbě vhodné terapie. Při správném zařazení pacienta podle dosaženého stadia CVI se zaměřujeme nejprve na klinické projevy, které indexujeme pod zkratkou „C“ – „clinics“. S terapeutickým výhledem, pokud se jedná o stadium C0–1 lze volit konzervativní přístup s preventivním nošením kompresních punčoch. Stadium C1 lze doplnit o ultrazvukové vyšetření, skleroterapii či perkutánní laser. Stadium C2 již představuje vhodné změny a můžeme řešit i některou cévní intervenční metodou. Zejména u stadia C3 je pak vyšetřovací metody nutno někdy doplnit o angiologické a lymfologické vyšetření a současně zvažovat případné interní komorbidity pacienta vedoucí k tvorbě edémů. Stadium C4, C5, C6 vyžaduje kromě expertní dermatologické péče i komplexní multidisciplinární přístup s přispěním obecného chirurga, internisty a dalších specialistů.Tab. 1. CEAP klasifikace 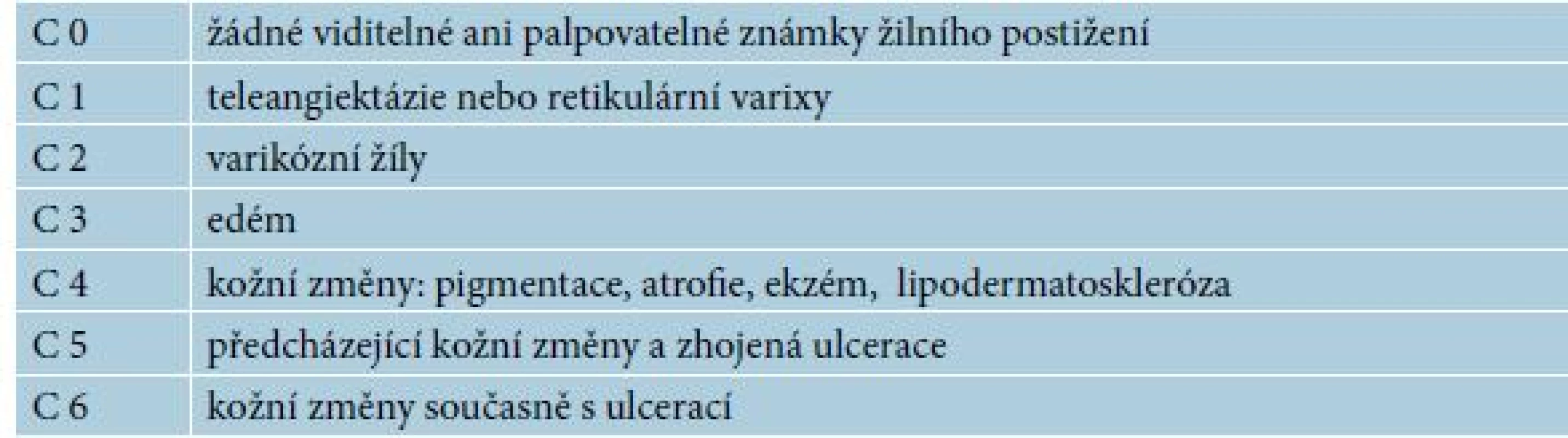
(C – klinické projevy, E c,p,s – etiologická klasifikace, A s,d,p – anatomická lokalizace postižení, P r,o,ro – patofyziologická dysfunkce) ETHIOLOGY c – kongenitální, p – primární (neznámá etiologie), s – sekundární ANATOMICAL, s – superficiální systém, d – hluboký (deep) systém, p – perforátory PATHOLOGY, r – reflux, o - obstrukce, r+o – kombinace refluxu s obstrukcí DIAGNOSTIKA
Po odběru anamnézy (cíleně se hodnotí rodinná zátěž, zaměstnání vyžadující dlouhá stání nebo sezení, proběhlé gravidity, hormonální léčba, proběhlá traumata či operace končetin, pánve a břicha) provádíme základní fyzikální vyšetření pacienta. Vyšetření probíhá, pokud možno ve stoje, což umožňuje hodnocení náplně a případného refluxu.
Fyzikální vyšetření zahrnuje objektivní popis typu varixů: teleangiektazie do 1 mm, retikulární varixy do 3 mm
a kmenové a postranní větve a kmeny nad 3 mm. Rovněž uvádíme jejich anatomické uložení. Všímáme si edému, známek zánětu a kožních změn spadajících pod klasifikaci CEAP C4 a C5 [28].Po zhodnocení lokálního nálezu odesíláme nemocného při potřebě k vyšetření duplexní sonografií. Sonografie je v diagnostických metodách nyní na prvním místě, jelikož invazivní flebografie se v podstatě neprovádí s výjimkou některých komplexních vaskulárních malformací. Dopplerovská ultrasonografie (obr. 3, 4) je hlavní a nedílnou součástí flebologické diagnostiky, zobrazí požadovanou část žilního řečiště na základě odrazu ultrazvukových vln na proudících erytrocytech, pomocí tohoto jevu diagnostikujeme patologický reflux krevního proudu v požadovaném žilním úseku. Čím větší je reflux (obr. 5) tím je CVI horší [23, 37,49].
Obr. 3. Dopplerovská ultrasonografie vena saphena magna 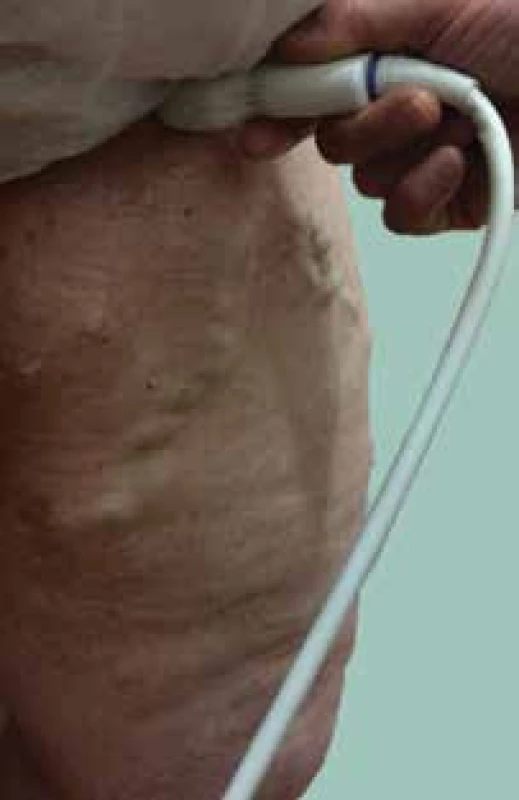
Obr. 4. Dopplerovská ultrasonografie vena saphena magna 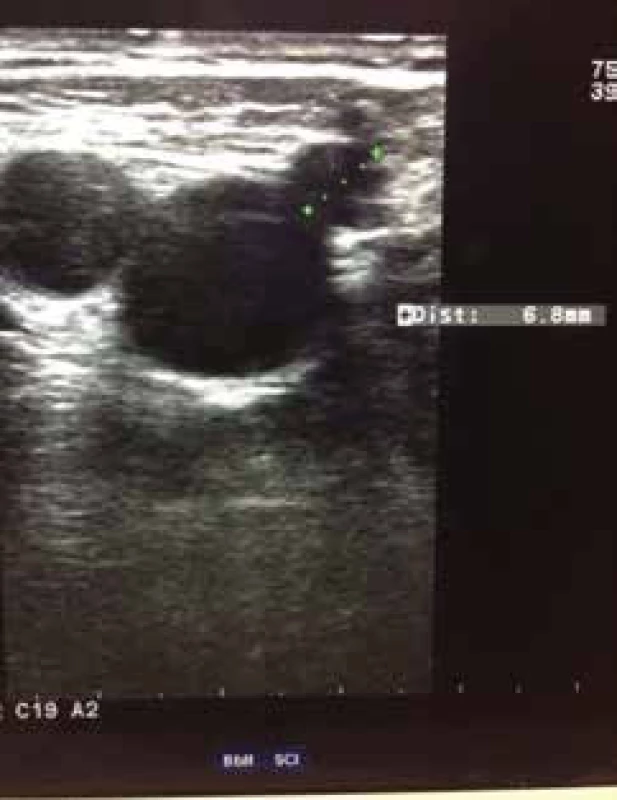
Obr. 5. Dopplerovská ultrasonografie vena saphena magna – Valsalvův fenomén a diametr žíly 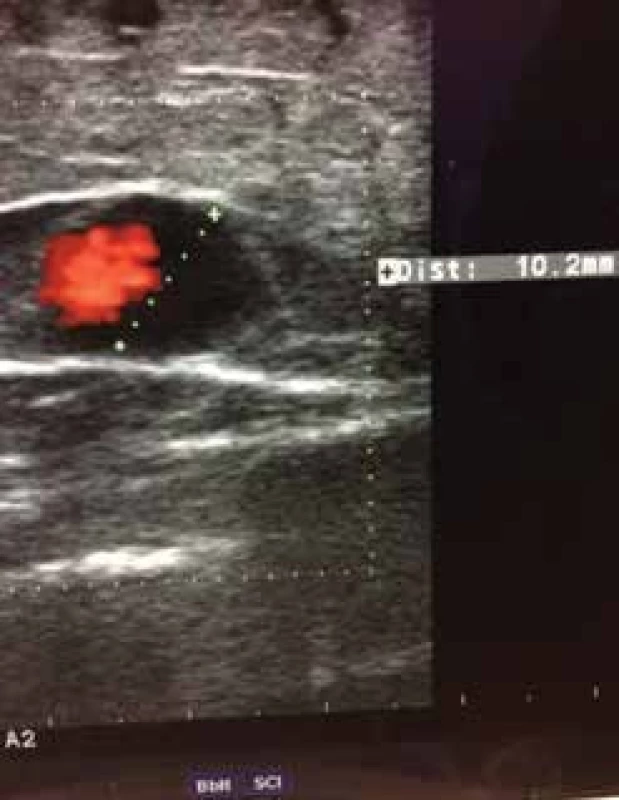
Sonografické vyšetření má zásadní vliv na diagnostiku a zejména pak pro plánování chirurgické intervence. Jde o metodu neinvazivní, bezpečnou a svou přesností převyšující klasické testy (Perthes, Trendelenburg apod.) vyžadující polohování pacienta a nakládání škrtidel do různých poloh. Dermatolog může v rámci svého oboru sám vyšetřovat nemocné například metodou digitální pletyzmografie, což je hemodynamická metoda porovnávající přítok a odtok z povrchové kožní oblasti žilního řečiště a vychází z měření objemových změn daných postupem ortográdní, či refluxní vlny v tomto žilním segmentu [58]. Vyšetření je vhodné spíše pro sledování funkčního výkonu žilního onemocnění než pro primární diagnostiku. Stejně tak vyšetření tužkovým dopplerem je spíše vhodné ke stanovení AB indexu a k vylučování arteriálního postižení ve sporných případech.
TERAPIE
Léčba CVI bývá dlouhodobá, či spíše doživotní a zahrnuje konzervativní i radikální postupy. Chirurgické intervence se obvykle doplňují režimovými opatřeními a kombinují s kompresivní terapií i farmakoterapií. Řešení refluxu je zásadním zásahem do patofyziologie onemocnění a opírá se o klasickou chirurgickou léčbu, popřípadě doplněnou novými endovaskulárními metodami. Spolehlivost chirurgických intervencí však nikdy není 100%, a ani dobré výsledky v prvních letech po operaci nezaručí, že během pozdějšího života nedojde k recidivě onemocnění.
Konzervativní léčba
K obecným opatřením patří dodržování životosprávy, nedílnou součástí je monitorování BMI. Ze sportovních aktivit jsou vhodné plavání a jízda na kole. V obou případech je možný pohyb končetinami s odlehčením a současně se u obézních vyhýbáme tvrdým dopadům. Provádění žilních cviků je založeno na střídání flexe a extenze, tedy na maximálním využití žilní svalové pumpy. Velmi výhodná je pak pro svou snadnost i rychlejší chůze, zejména doplněná o použití holí (nordic walking) vede k posturální stabilizaci pacienta a zapojení i svalstva horních končetin při souhybech. Toto vede ke zlepšenému dýchání a rozpínání hrudního koše a zlepšenému plnění srdce navrácenou krví.
Kompresivní terapie je základním konzervativním postupem. Aplikujeme ji buď formou elastické bandáže (používané v akutní fázi onemocnění), či pomocí kompresivních elastických punčoch (vhodné k chronické terapii). Tímto postupem dochází ke snížení žilního objemu povrchových žil a eliminaci přetlaku centripetálním usměrněním toku krve. Dilatovaná žíla při působení tlaku tak může obnovit svou valvulární kompetenci. Podle rozsahu insuficientního žilního segmentu lze použít podkolenky, (polo-)stehenní punčochy či punčochové kalhoty. Rozlišujeme kompresní třídy I. až IV. podle vyvíjeného kompresního tlaku na končetinu (v rozsahu cca od 15 mmHg používané i preventivně, po 49 mmHg indikované při lymfedému). Potřebnou velikost stanovíme měřením obvodů končetiny. V praxi je však vhodné, pokud si z konfekčně vyráběných produktů pacient může vybrat po vyzkoušení (měření často provádí proškolení pracovníci ve zdravotnických potřebách s přihlédnutím ke specifikům jednotlivých výrobců). Aplikace kompresivní terapie je standardně doporučována od rána (kdy končetiny nejsou oteklé) až do večera. Kontraindikací kompresivní léčby je pokročilá ischemická choroba dolních končetin, proto doporučujeme v rutinní praxi monitorování periferního arteriálního tlaku pomocí tužkového dopplera (AB index), dále pak akutní zánětlivé stavy jako lymfangoitida a celulitida. Zvýšená opatrnost se doporučuje u pacientů se srdečním selháváním. Dermatologická terapie zahrnuje indiferentní ošetřování k udržení hydratace pokožky, při potřebě kortikoidní externa k tlumení zánětlivých projevů (klinický stupeň C4) a dále diferentní externa určená k terapii bércového vředu podle různých stadií hojení rány (moderní krytí), popř. v kombinaci s různými chemickými, enzymatickými, či chirurgickými pokusy o debridement.
Farmakoterapie
Terapie venofarmaky je velmi populární, ale efektivně ji indikujeme spíše až na základě kombinace s dalšími postupy (konzervativními či chirurgickými). Venotonika mají vliv na makrocirkulaci (zlepšují žilní tonus) i na mikrocirkulaci (snižují permeabilitu kapilár, plazminogen i aktivaci leukocytů a zvyšují fibrinolýzu a lymfatickou drenáž). Složení přípravků může být plně přírodní, syntetické či kombinované. Mezi přírodní venofarmaka patří flavonoidy a glykosidy (rutin, diosmin, hesperidin). Mezi semisyntetické flavonoidy patří tribenosid a troxerutin. Syntetické jsou heptaminol a kalcium dobesilát. Podle literatury má zejména mikronizovaná flavonoidní frakce velmi dobrý efekt na hojení především menších vředů [6, 17, 47]. Indikací venotonik jsou na prvním místě edémy a mírnější kožní změny (stadium C4), ale předepisujeme je i z důvodu stesků na tíhu končetin, jejich pálení či bolest. V praxi se setkáváme často se stavem, že venotonický účinek deklarují i některé potravinové doplňky, které ale nejsou pro žilní onemocnění medicínsky relevantní.
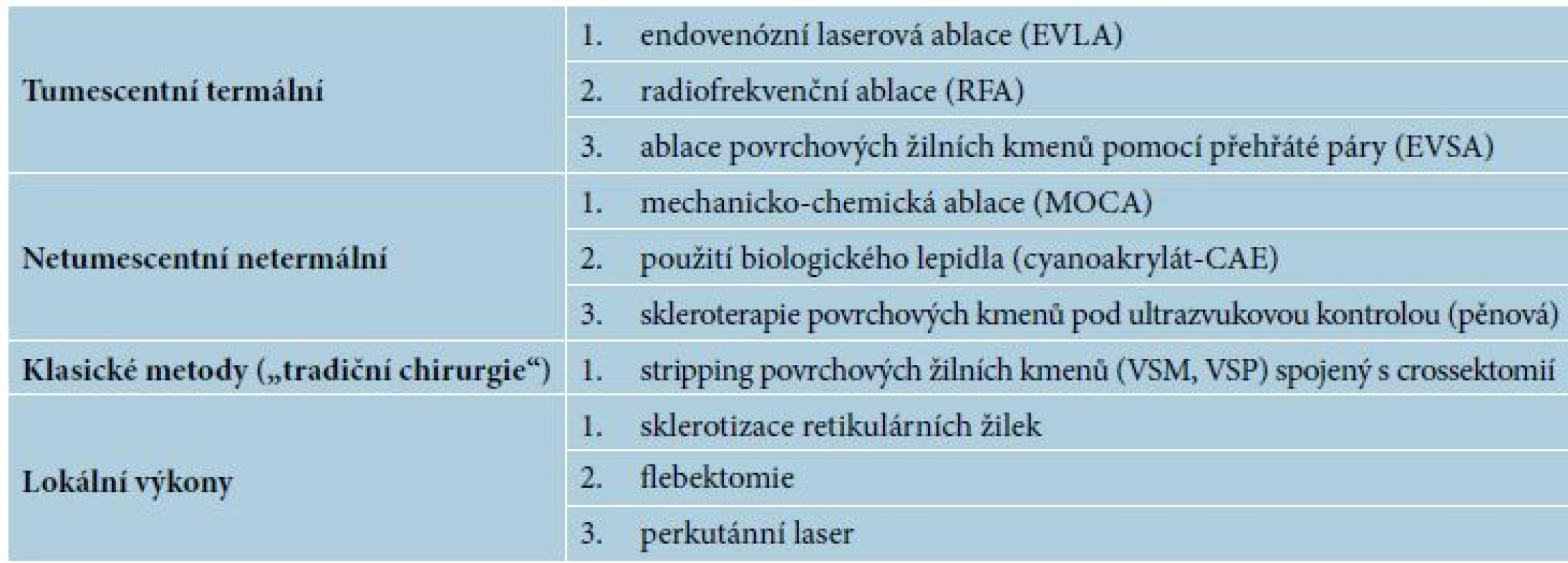
Intervenční terapie (viz tabulka 2)
Klasická chirurgická léčba varixů spočívá v odstranění insuficientní přívodné žíly podvazem (přerušením) a jejím mechanickým vyjmutím – stripping a crossekomie (Babcockova operace). Tato metoda je do současnosti považována za zlatý standard léčby.
Indikací chirurgické léčby je pokročilá CVI (významný reflux v oblasti kmenových žil, ulcerace či pacienti kontraindikovaní ke kompresivní terapii – např. pro infekce, ICHDK, kardiální příčiny, alergie) [38].
Kontraindikací chirurgické léčby je HŽT, lymfedém, pokročilé stadium ICHDK neumožňující hojení, gravidita, špatný celkový zdravotní stav pacienta, závažná porucha hemokoaguce. Přestože je tento základní způsob léčby efektivní, má řadu nevýhod, které převážně vyplývají z jeho značné invazivity.
Nejčastější komplikací je porušení senzitivní inervace – nervus saphenus (obvykle reverzibilní) a krvácení. Další nevýhodou je delší rekonvalescence. Mezi závažnější komplikace chirurgické intervence patří HŽT, plicní embolie (zřídka), tromboflebitida [19, 33, 51]. Výkon je prováděn v celkové, či svodné anestezii. Exstirpace se provádí speciálním nástrojem – endostriptorem (obr. 6). Snaha o limitovaný stripping z důvodu zachování žíly k revaskularizačním výkonům je samozřejmostí. Součástí výkonu je crossektomie, což je podvaz velké safény v blízkosti ústí do femorální žíly a flebektomie. Dříve preferovaná flebektomie Smetanovým nožem je nyní nahrazována jemnějším instrumentáriem – Varadyho háčky. Takzvanými Kocherovými opichy se podvazují varikózní žíly za účelem trombotizce jejich lumen. Toto opatření zruší její patologické refluxní proudění v ošetřeném rozsahu. Kocherovy opichy jsou již méně používaný způsob terapie varixů.
Obr. 6. Zavádění endostriptoru 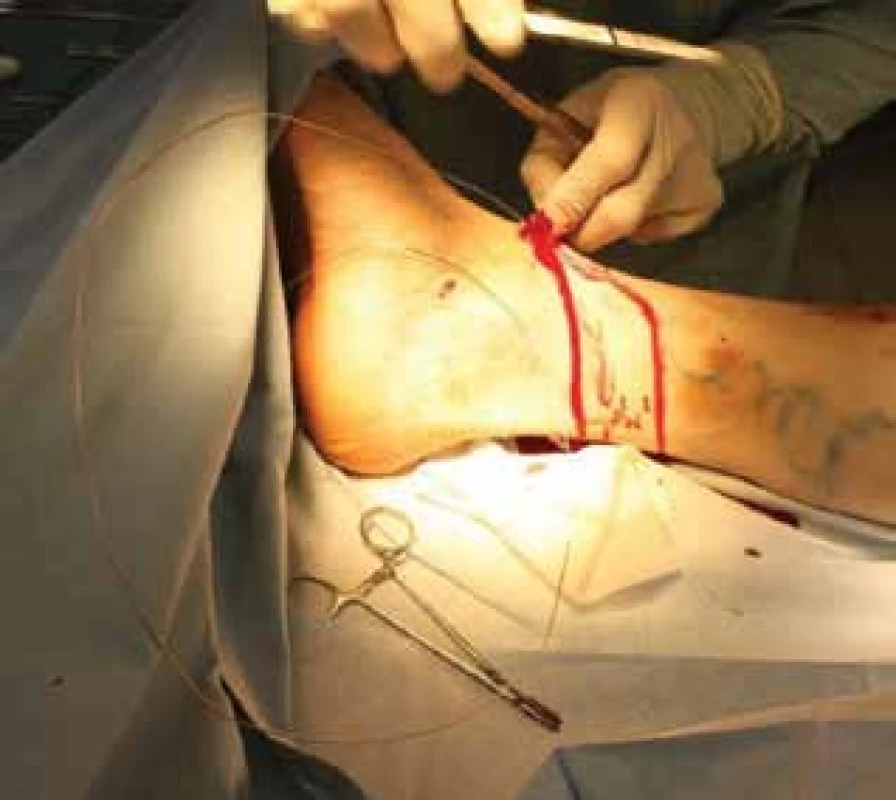
Mezi další možné chirurgické intervenční metody patří subfasciální endoskopické ošetření perforátorů, rekonstrukce žilních chlopní (CHIVA), či ošetření žilních stenóz angioplastikou s implantací stentu.
Svým charakterem (tj. spíše zevním působením) je možno k těmto metodám volně zařadit i některé metody preferované dermatology při estetickém řešení mírnějších forem žilní nedostatečnosti, či ke korigování pooperačních reziduálních projevů CVI. Principem laserterapie je transkutánní koagulace laserovým paprskem. Používají se vysokovýkonostní lasery – Nd YAG (1064 nm),
pulzní barvivový (595 nm), KTP (532 nm) a nověji diodové (1470 nm). Tato metoda je vhodná k léčbě maximálně retikulárních varixů. Nevýhodou jsou dočasné nežádoucí pigmentace.Mezi moderní minimálně invazivní ambulantní metody patří endovenózní laserová ablace (EVLA), radiofrekvenční ablace (RFA), mechanochemická ablace Clarivein, cyanoakrylátové lepidlo, či ultrazvukem kontrolovaná sklerotizace pěnou (UGFS) [8, 27]. Všechny tyto metody se ukázaly opakovaně jako bezpečné a vykazují výsledky srovnatelné s chirurgickou léčbou. Výhoda nízké invazivity je dosažena užitím katetrizační léčby. Nicméně bez ohledu na svou bezpečnost nejsou v ČR tyto metody hrazeny z veřejného zdravotního pojištění a pacient si je musí hradit přímo.
Tyto miniinvazivní metody jsou bezpečné a efektivní s ohledem na pravděpodobnost kvalitního uzávěru žíly [5, 10, 14, 15, 19, 30, 36, 46, 48]. Mnohé studie rovněž poukazují na jejich lepší výsledný kosmetický efekt ve srovnání s klasickými chirurgickými postupy [16, 28, 53].
Podle doporučených postupů [40] by z těchto důvodů měla být v současnosti optimální metodou první volby endovenózní ablace [13, 60]. Klasická chirurgická léčba byla odsunuta až na druhé místo, třetí volbou pak zůstává skleroterapie. Následná konzervativní léčba se pak využívá u všech metod [4, 28, 41]. Další výhodou miniinvazivních metod je jejich možné ambulantní provedení bez nutnosti pracovní neschopnosti, která se u klasických operačních výkonů pohybuje okolo tří týdnů.
Pro ilustraci technologických předpokladů jednotlivých endovaskulárních metod lze uvést následující fakta.
EVLA (endovenózní laserová ablace) je moderní katetrizační metoda terapie křečových žil. Principem metody je termální destrukce žilní tkáně za použití laserového paprsku cíleně vedeného do místa potřeby [26]. Efektivita uzávěru žíly odpovídá určitým parametrům, jako je vlnová délka zvoleného laseru a množství dodané energie [54]. Volba vlnové délky ovlivňuje absorpci laserové energie různými relevantními chromofory (mezi ně zde patří například hemoglobin, voda). Vlnová délka laseru tím pádem ovlivňuje žádoucí destrukci žilní stěny, či naopak tvorbu nežádoucího trombu umožňujícího následnou rekanalizaci vedoucí k selhání léčby [44]. Mezi lasery určené k této metodě patří na prvním místě diodové (1470 nm),
které se lépe vstřebávají ve vodě, a proto působí na stěnu žíly, a ne na hemoglobin, tím pádem vzikne menší trombus. Dále lze použít například neodymum-doped yttrium aluminium garnet (Nd:YAG) 1064 nm laser. Pro názornost tepelného účinku laseru na tkáň a její okolí lze použít termografickou zobrazovací metodu (obr. 7) [45].Obr. 7. Termokamera – při zavádění laserového vlákna do VSP 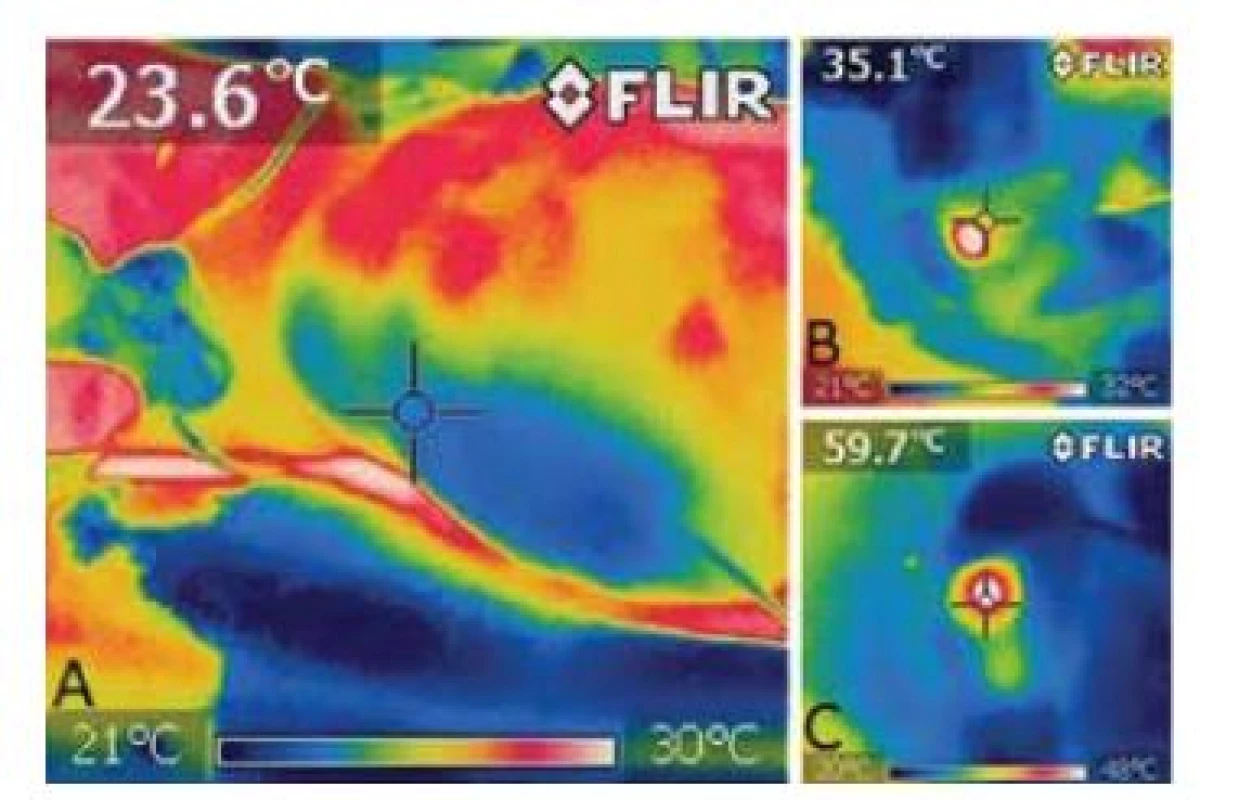
Endovaskulární výkony podléhají stejným právním postupům jako jiné invazivní procedury a je nutná dokladovatelná edukace pacienta podpis informovaného souhlasu. Významnou podmínkou úspěšného provedení a dosažení dobrých výsledků je totiž dokonalá compliance pacienta.
Mezi kontraindikace EVLA patří krátký nebo nevýznamný reflux, těsná blízkost kůže nebo cévního svazku, posttrombotické stavy na kmenových žilách, omezená mobilita a alergie na lokální anestetikum. Jako relativní kontraindikace je průměr VSM ve stoje nad 1,5 cm.
Rutinní předoperační vyšetření zahrnují běžná biochemická laboratorní vyšetření, významný je ale pak
krevní obraz a testy srážlivosti, dále EKG a tělesné konstituční údaje. Ultrasonografický (vstupní) nález je samozřejmostí, ale ještě těsně před operací provádíme opětovné sonografické vyšetření jednak k ověření správnosti indikace a za druhé k provedení anatomického mapování požadovaného výkonu a zakreslení situace nesmývatelným fixem v operačním poli. Operační výkon probíhá na operačním sále za dodržení antisepse a asepse. Poloha pacienta závisí na operované lokalitě – velká saféna vyžaduje polohu na zádech, malá na břiše. Operační stůl polohujeme do anti-Trendelenburgerovy polohy k požadované žilní dilataci (zvýšení žilního tlaku) [18]. Ultrazvuková sonda (obvykle 8 MHz) je během výkonu ve sterilním pouzdře. K punkci žíly používáme 19 G jehlu za použití Seldingerovy techniky (0.035“ J) zahnutý zavaděč, dilatátoru a kalibrovaného žilního katetru. Laserové vlákno poté zavádíme endovenózně (obr. 8). Touto metodou lze operovat více žilních úseků najednou.Obr. 8. Zavádění vlákna do vena saphena parva pod ultrazvukovou kontrolou 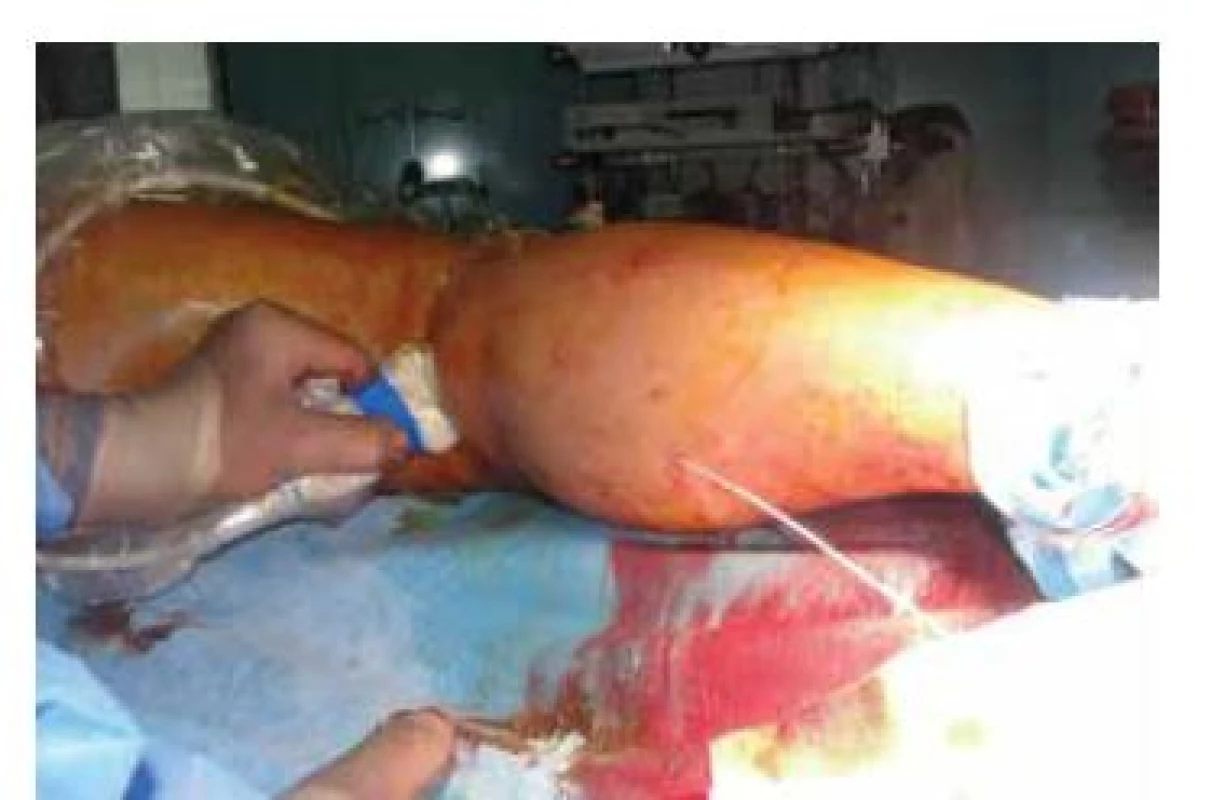
Laserové vlákno je zavedeno do žíly pod USG kontrolou precizně 1–2 cm od safenofemorální junkce. Následně lze pacienta uvézt do Trendelenburgerovy polohy za účelem co největšího vyprázdnění žilního systému. Používáme tumescenční anestezii, kdy jednou z možností je: 50 ml 2% bupivacainu + 500 ml FR + 8 ml 8,4% bikarbonátu + 1 ml 0,1% epinefrinu. Aplikace probíhá speciální pumpou do safenofemorálního kompartment (tzv. Faraonovo oko), opět pod USG kontrolou. Tumescenční metoda funguje výborně anesteticky a rovněž zabraňuje poškození okolních tkání, operované žíly a zvyšuje tlak v okolí operované žíly a napomáhá jejímu kolapsu. Nakonec propojíme laserové vlákno se samotným laserovým zdrojem, nastavíme přibližnou požadovanou energii (LEED-linear endovenous energy density) v J/cm rovnou průměru žíly v milimetrech krát 10. Metoda se typicky doplňuje miniflebektomií Varadyho háčky a mosquito klíšťkami ke zlepšení kosmetického efektu.
Pooperačně doporučujeme kompresní punčochy II. tří-
dy na alespoň 1 týden. První USG kontrola se provádí za 24–48 hodin po operaci k ověření efektu, zpravidla již ambulantně. Jako u všech miniinvazivních metod objevuje se i u EVLA vznik komplikací v místě aplikace, jmenovitě jde o hyperpigmentace, teleangiektazie, hypertrichózu, folikulitidu, iritační dermatitidu, místní urtikárii, ekchymózy, edém, ischémii, nekrózu, či ulcerace; dále pak přichází do úvahy poranění nervů, neúplný uzávěr, celková alergická reakce, vazovagální synkopa, intraarteriální aplikace léčiva, tromboflebitida HŽT, plicní embolie.RFA (radiofrekvenční ablace) je metoda, při které se nitrožilně uzavírá povrchový žilní kmen bipolární elektrodou, která se zavede do postižené kmenové žíly a pod kontrolou ultrazvuku ji operatér posune do periferie. Během výkonu se elektroda postupně vytahuje. Působením elektrického proudu dochází k denaturaci bílkovin tkáně žilní stěny, následně dochází k fibrotizaci a zániku žíly. Intravenózně dosahuje teplota asi 140 °C, ale i vyšší. Výkon se provádí rovněž v tumescentní lokální anestezii.
EVSA je katetrizační endovenózní ablace horkou sterilní parou o teplotě 120 stupňů Celsia. Pro svoji nižší efektivitu než EVLA či RFA se tato metoda provádí zřídka [54, 56].
U dalších metod používána kombinace s některou endovaskulárně aplikovanou látkou. Metoda MOCA je mechanochemická ablace za použití endovenózního rotačního katetru s následnou injektáží sklerotizační látky [56]. Principem skleroterapie je endovenózní aplikace sklerotizačního roztoku, který poškozuje endotelovou výstelku žíly, s následným uzávěrem lumen varikozity trombem vznikajícím na ploše obnaženého subendotelového vaziva. Metoda je běžně ambulantně používaná pro retikulární varixy a mikrovarixy. Jako sklerotizační látka se užívá polidocanol koncentrace až do 2 %. Látka se aplikuje inzulinovou stříkačkou nebo lépe setem na pěnovou skleroterapii. UZ kontrola se uplatňuje při ošetřování kmenových žil (VSM, VSP). Kontrast vzniklý aplikací pěny polidokanolu umožňuje bezpečnou aplikaci striktně intravenózně, což je výhoda zejména při použití vyšší koncentrace sklerotizující látky. Kosmetickou nevýhodou jsou různě vyjádřené pigmentace a funkční recidivy, které se objevují poměrně často.
CAE je katetrizační endovenózní aplikace cyanoakrylátového lepidla. Tato šetrná ultrazvukově naváděná metoda (jako všechny endovenózní ablace) má svoji nevýhodu ve vyšší ekonomické zátěži pro pacienta. Provádí se podobně jako MOCA – rovněž je endovenózně mechanicky narušena cévní stěna, následně se aplikuje
N2 butyl akrylát určený pro intravaskulární aplikaci. Výhodou je rovněž velmi krátká rekonvalescence v řádu několika dnů [1].Použití sonografie je univerzální jak v diagnostice, tak v navigaci těchto moderních metod, tak ke kontrole výsledků léčby. Cílem všech metod je dosažení co nejlepšího kosmetického efektu při zachování komfortu a co nejkratší rekonvalescence pacienta. Nejlepšího kosmetického efektu je často dosaženo až kombinací metod
[2, 3, 31].ZÁVĚR
CVI je častým problémem v ordinaci dermatologa. Přehled současných diagnostických a zejména terapeutických metod umožní takto erudovanému dermatologovi rychlejší orientaci v problému a potažmo i volbu efektivnějšího řešení obtíží nemocného, zkrácení doby jeho pracovní neschopnosti. Je nutno rovněž zdůraznit nutnou a přínosnou spolupráci s chirurgy, cévními chirurgy, angiology a lymfology. Svůj význam pro korekci příčiny žilní nedostatečnosti si udržují klasické i novější chirurgické metody a efektivního řešení je často dosaženo až v kombinaci s konzervativní terapií či farmakologickou léčbou.
Prohlášení o střetu zájmu
Autoři v souvislosti s tématem práce v posledních 12 měsících nespolupracovali s žádnou farmaceutickou firmou.
Do redakce došlo dne 20. 12. 2018.
Adresa pro korespondenci:
MUDr. Andrea Havlínová
Dermatovenerologická klinika 1. LF UK a VFN
U Nemocnice 499/2,
128 00, Praha 2
KONTROLNÍ TEST
1. Mezi hlavní klinické projevy chronické žilní nedostatečnosti patří:
- a) varixy
- b) edém
- c) ulcus cruris
- d) MOCA
2. Mezi moderní intervenční metody patří:
- a) EVSA
- b) CAE
- c) DOPSA
- d) EVLA
3. Edém:
- a) je příznakem chronické žilní nedostatečnosti
- b) je příznakem funkční poruchy žilní hemodynamiky
- c) je podle klasifikace CEAP stadium C3
- d) nevyžaduje sonografické vyšetření
4. Tumescenční anestezie je kombinace:
- a) bupivacain
- b) bikarbonát
- c) adrenalin
- d) lidocain
5. Varixy vznikají v důsledku:
- a) žilní hypertenze
- b) adherence leukocytů
- c) shlukování erytrocytů
- d) refluxu krve
6. KTS:
- a) součástí jsou arteriovenózní spojky
- b) je mutace EII3K a VG5Q genu
- c) k vývojové poruše dochází v 6. a 8. gestačním týdnu
- d) zahrnuje aplazii či hypoplazii hlubokého žilního systému
7. EVLA:
- a) metoda volby při incuficienci více kmenových žil
- b) provádí se v celkové anstezii
- c) je riziková strana rekonvalescence
- d) je metodou tzv. jednodenní chirurgie
8. Pěnová skleroterapie se využívá při terapii:
- a) metličkových varixů
- b) kmenových varixů
- c) perforátorů
- d) v kombinaci s ultrazvukovým naváděním
9. První intervenční volbou je:
- a) stripping
- b) endovenózní ablace
- c) „watch and wait“
- d) vteřinové lepidlo
10. Vena giacomini je spojkou:
- a) VSM a VSP
- b) VSAA a VSP
- c) VF a VSM
- d) VSP a VVPE
Správným zodpovězením otázek kontrolního testu získáte 2 kredity kontinuálního vzdělávání lékařů ČLK, které budou zasílány redakcí jedenkrát ročně po uzavření ročníku časopisu. Správné odpovědi na otázky kontrolního testu budou uveřejněny v příštím čísle časopisu. Odpovědi posílejte na e-mailovou adresu: kozni@lf1.cuni.cz vždy nejpozději do jednoho měsíce od vydání daného čísla.
Odpovědi na otázky kontrolního testu v č.6/2018: Hubka V. at al: Zoonotické dermatofytózy: klinický obraz, diagnostika, etiologie, léčba, epidemiologická situace u nás
Správné odpovědi: 1c, 2d, 3c, 4c, 5a, 6b, 7d, 8d, 9b, 10d
Zdroje
1. ALMEIDA, J. I., JAVIER, J. J., MACKAY, E. et al., First human use of cyanoacrylate adhesive for treatment of saphenous vein incompetence. J Vasc Surg Venous Lymphat Disord, 2013, 1(2), p. 174–180.
2. BECKER, F., MENASSA, M., GABRIELLE, F. et al. What complementary examinations to demand in chronic venous insufficiency? Phlebologie, 1992, 45(3), p. 297–303; discussion 304–306.
3. BERGAN, J. J., SCHMID-SCHONBEIN, G.W. Therapeutic management of chronic venous insuffi-
ciency: microcirculation as a target. Microcirculation, 2000, 7(6 Pt 2), p. S23–28.4. BERGAN, J. J., SCHMID-SCHONBEIN, G. W., SMITH, P. D. et al. Chronic venous disease. N Engl J Med, 2006, 355(5), p. 488–498.
5. BIEMANS, A. A., KOCKAERT, M., AKKERSDIJK, G. P. et al., Comparing endovenous laser ablation, foam sclerotherapy, and conventional surgery for great saphenous varicose veins. J Vasc Surg, 2013, 58(3), p. 727–734 e1.
6. BOISSEAU, M. R. Pharmacological targets of drugs employed in chronic venous and lymphatic insufficiency. Int Angiol, 2002, 21(2 Suppl 1), p. 33–39.
7. BOLLINGER, A., LEU, A. J., HOFFMANN, U. et al. Microvascular changes in venous disease: an update. Angiology, 1997, 48(1), p. 27–32.
8. BOOTUN, R., LANE, T. R., DAVIES, A. H. The advent of non-thermal, non-tumescent techniques for treatment of varicose veins. Phlebology, 2016, 31(1), p. 5–14.
9. BOURJEILY, G., PAIDAS, M., KHALIL, H. et al. Pulmonary embolism in pregnancy. Lancet, 2010, 375(9713), p. 500–512.
10. BRITTENDEN, J., COTTON, S. C., ELDERS, A. et al., A randomized trial comparing treatments for
varicose veins. N Engl J Med, 2014, 371(13), p.
1218–1227.11. BURNAND, K. G. The physiology and hemodynamics of chronic venous insufficiency. Handbook of venous disorders, 2nd ed. New York, NY: Arnold; 2001: p. 49–57.
12. CAPRINI, J. A., PARTSCH, H., SIMMAN, R. Venous Ulcers. J Am Coll Clin Wound Spec, 2012, 4(3), p.
54–60.13. CARRADICE, D. Superficial venous insufficiency from the infernal to the endothermal. Ann R Coll Surg Engl, 2014, 96(1): p. 5–10.
14. CARRADICE, D., MEKAKO, A. I., MAZARI, F. A. et al. Clinical and technical outcomes from a randomized clinical trial of endovenous laser ablation compared with conventional surgery for great saphenous varicose veins. Br J Surg, 2011, 98(8), p. 1117–1123.
15. CARRADICE, D., MEKAKO, A. I., MAZARI, F. A. et al., Randomized clinical trial of endovenous laser ablation compared with conventional surgery for great saphenous varicose veins. Br J Surg, 2011, 98(4), p. 501–510.
16. CARROLL, C., HUMMEL, S., LEAVISS, J. et al. Clinical effectiveness and cost-effectiveness of minimally invasive techniques to manage varicose veins: a systematic review and economic evaluation. Health Technol Assess, 2013, 17(48), p. i-xvi, 1–141.
17. COLERIDGE-SMITH, P., LOK, C., RAMELET, A. A. Venous leg ulcer: a meta-analysis of adjunctive therapy with micronized purified flavonoid fraction. Eur J Vasc Endovasc Surg, 2005, 30(2), p. 198–208.
18. COLLARES, F. B., FAINTUCH, S., Varicose Veins. Theime Publishers, 2017.
19. CRITCHLEY, G., HANDA, A., MAW, A. et al., Complications of varicose vein surgery. Ann R Coll Surg Engl, 1997, 79(2), p. 105–110.
20. DARWOOD, R. J., THEIVACUMAR, N., DELLAGRAMMATICAS, D. et al. Randomized clinical trial comparing endovenous laser ablation with surgery for the treatment of primary great saphenous varicose veins. Br J Surg, 2008, 95(3), p. 294–301.
21. DEVIS, P., KNUTTINEN, M. G. Deep venous thrombosis in pregnancy: incidence, pathogenesis and endovascular management. Cardiovasc Diagn Ther, 2017, 7(Suppl 3), p. S309–S319.
22. EKLOF, B., RUTHERFORD, R. B., BERGAN, J. J. et al. Revision of the CEAP classification for chronic venous disorders: consensus statement. J Vasc Surg, 2004, 40(6), p. 1248–1252.
23. ELIAS, S. Minimally invasive vein surgery: latest options for vein disease. Mt Sinai J Med, 2010, 77(3), p. 270–278.
24. ELIÁŠ, P., ŽIŽKA, J. Dopplerovská ultrasonografie. Nucleus, 1998, 1. vydání s. 150–155. 25. EVANS, C. J., FOWKES, F. G., RUCKLEY, C. V. et al. Prevalence of varicose veins and chronic venous insufficiency in men and women in the general population: Edinburgh
Vein Study. J Epidemiol Community Health, 1999, 53(3), p. 149–153.26. GALANOPOULOS, G., LAMBIDIS, C. Minimally invasive treatment of varicose veins: Endovenous
laser ablation (EVLA). Int J Surg, 2012, 10(3), p.
134–139.27. GLOVICZKI, P., COMEROTA, A. J., DALSING, M. C. et al. The care of patients with varicose veins and associated chronic venous diseases: clinical practice guidelines of the Society for Vascular Surgery and the American Venous Forum. J Vasc Surg, 2011, 53(5 Suppl), p. 2S48S.
28. GLOVICZKI, P., GLOVICZKI, M. L. Guidelines for the management of varicose veins. Phlebology, 2012, 27 Suppl 1, p. 2–9.
29. GSCHWANDTNER, M. E., EHRINGER, H., Microcirculation in chronic venous insufficiency. Vasc Med, 2001, 6(3), p. 169–179.
30. CHRISTENSON, J. T., GUEDDI, S., GEMAYEL, G. et al. Prospective randomized trial comparing endovenous laser ablation and surgery for treatment of primary great saphenous varicose veins with a 2-year follow-up. J Vasc Surg, 2010, 52(5), p. 1234–1241.
31. JANTET, G. Symptoms and signs in chronic venous insufficiency. Phlebolymphology, 27, p. 2–3.
32. KAPPERT, A. Angiológia učebnica a atlas. Choroby tepien, žíl, vlásečnic a lymfatických ciev. Osveta, 1987, s. 24.
33. MILLER, G. V., LEWIS, W. G., SAINSBURY, J. R. et al. Morbidity of varicose vein surgery: auditing the benefit of changing clinical practice. Ann R Coll Surg Engl, 1996, 78(4), p. 345–349.
34. MIZUNO, Y., PUCA, A. A., O‘BRIEN, K. F. et al.
Genomic organization and single-nucleotide polymorphism map of desmuslin, a novel intermediate filament protein on chromosome 15q26.3. BMC
Genet, 2001, 2, p. 8.35. MOORE, P. Zrození člověka. Embryologie s klinickým zaměřením. Praha ISV, 2002.
36. MORRISON, N., GIBSON, K., MCENROE, S. et al. Randomized trial comparing cyanoacrylate embolization and radiofrequency ablation for incompetent great saphenous veins (VeClose). J Vasc Surg, 2015, 61(4), p. 985–994.
37. NAVRÁTIL, L., ROSINA, J. et al. Medicínská biofyzika. Praha, Grada, 2005, 1. vydání: s. 524.
38. NAVRÁTILOVÁ, Z. Kompresivní terapie u žilních onemocnění. Interní Med, 2008(10), p. 449–455.
39. NEHLER, M. R., PORTER, J. M. The lower extremity venous system. Part II: The pathophysiology of chronic venous insufficiency. Perspect VascSurg, 1992(5), p. 81.
40. NICOLAIDES, A. N., ALLEGRA, C., BERGAN, J. et al. Management of chronic venous disorders of the lower limbs: guidelines according to scientific evidence. Int Angiol, 2008, 27(1), p. 1–59.
41. NICOLAIDES, A. N., CARDIOVASCULAR DISEASE, E., RESEARCH, T. et al. Investigation of chronic venous insufficiency: A consensus statement (France, March 5–9, 1997). Circulation, 2000, 102(20), p. E126–163.
42. O‘DONNELL, T.F., JR., PASSMAN, M. A. Clinical practice guidelines of the Society for Vascular Surgery (SVS) and the American Venous Forum (AVF) – Management of venous leg ulcers. Introduction.
J Vasc Surg, 2014, 60(2 Suppl), p. 1S–2S.43. PIAZZA, G. Varicose veins. Circulation, 2014, 130(7), p. 582–587.
44. PROEBSTLE, T. M., MOEHLER, T., HERDEMANN, S. Reduced recanalization rates of the great saphenous vein after endovenous laser treatment with increased energy dosing: definition of a threshold for the endovenous fluence equivalent. J Vasc Surg, 2006, 44(4), p. 834–839.
45. RASMUSSEN, L. H., BJOERN, L., LAWAETZ, M. et al. Randomised clinical trial comparing endovenous laser ablation with stripping of the great saphenous vein: clinical outcome and recurrence after 2 years. Eur J Vasc Endovasc Surg, 2010, 39(5), p. 630–635.
46. RASMUSSEN, L. H., LAWAETZ, M., BJOERN, L. et al. Randomized clinical trial comparing endovenous laser ablation, radiofrequency ablation, foam sclerotherapy and surgical stripping for great saphenous varicose veins. Br J Surg, 2011, 98(8), p. 107–187.
47. ROZTOČIL, K., Venotonika – komu a která? Angiologie, 2007, s. 51–53.
48. SANCHEZ, C., CHINN, B. T. Hemorrhoids. Clin Colon Rectal Surg, 2011, 24(1), p. 5–13.
49. SERVELLE, M. Klippel and Trenaunay‘s syndrome. 768 operated cases. Ann Surg, 1985, 201(3), p.
365–373.50. SIRIBUMRUNGWONG, B., NOORIT, P., WILASRUSMEE, C. et al., A systematic review and meta-analysis of randomised controlled trials comparing endovenous ablation and surgical intervention in patients with varicose vein. Eur J Vasc Endovasc Surg, 2012, 44(2), p. 214–223.
51. TASSIE, E., SCOTLAND, G., BRITTENDEN, J. et al. Cost-effectiveness of ultrasound-guided foam sclerotherapy, endovenous laser ablation or surgery as treatment for primary varicose veins from the randomized CLASS trial. Br J Surg, 2014, 101(12), p. 1532–1540.
52. VALENTA, J. Základy chirurgie. Karolinum, 2003.
2. vydání. s. 191, 192, 195.53. VAN DEN BOS, R. R., KOCKAERT, M. A., NEUMANN, H. A. et al., Technical review of endovenous laser therapy for varicose veins. Eur J Vasc Endovasc Surg, 2008, 35(1), p. 88–95.
54. VAN DEN BOS, R. R., MILLERET, R., NEUMANN, M. et al., Proof-of-principle study of steam abla-
tion as novel thermal therapy for saphenous varicose veins. J Vasc Surg, 2011, 53(1), p. 181–186.55. VAN EEKEREN, R. R., BOERSMA, D., KONIJN,
V. et al. Postoperative pain and early quality of life after radiofrequency ablation and mechanochemical endovenous ablation of incompetent great saphenous veins. J Vasc Surg, 2013, 57(2), p. 445–450.56. VAN RUIJVEN, P. W., VAN DEN BOS, R. R., ALAZARD, L. M. et al. Temperature measurements for dose-finding in steam ablation. J Vasc Surg, 2011, 53(5), p. 1454–1456.
57. VENTURI, M., BONAVINA, L., ANNONI, F. et al. Biochemical assay of collagen and elastin in the normal and varicose vein wall. J Surg Res, 1996, 60(1), p. 245–248.
58. WEST, J. B. The birth of clinical body plethysmography: it was a good week. J Clin Invest, 2004, 114(8), p. 1043–1045.
59. WHIDDON, L. L. Advances in the treatment of superficial venous insufficiency of the lower extremities. Proc (Bayl Univ Med Cent), 2007, 20(2), p.
136–139.60. XIAO, Y., HUANG, Z., YIN, H. et al. Desmuslin gene knockdown causes altered expression of phenotype markers and differentiation of saphenous vein smooth muscle cells. J Vasc Surg, 2010, 52(3), p. 684–690.
61. YIN, H., ZHANG, X., WANG, J. et al. Downregulation of desmuslin in primary vein incompetence.
J Vasc Surg, 2006, 43(2), p. 372–378.Štítky
Dermatológia Detská dermatológia
Článok vyšiel v časopiseČesko-slovenská dermatologie
Najčítanejšie tento týždeň
2019 Číslo 1- První zkušenosti s léčbou psoriázy bimekizumabem v české reálné praxi – kazuistika z FNUSA
- Na český trh přichází biosimilar adalimumabu s prokázanou terapeutickou ekvivalencí
- Nehoňte nemocné s mMCC od čerta k ďáblu!
- První a jediná schválená imunoterapie vzácného agresivního karcinomu kůže
-
Všetky články tohto čísla
- Diagnostika maligního melanomu s využitím celotělového skenu
- Kerion Celsi u dítěte – možnosti diagnostiky a léčby
- Klinický případ: Perianální eroze – stručný přehled
- Benigní papilomatózní léze?
- ERYSIPEL (syn. růže)
- 100 let časopisu České a Slovenské dermatologické společnosti
- Zápis ze schůze výboru ČDS Praha 15. 11. 2018
- Doc. MUDr. Jaromír Kejda, CSc. (10. 6. 1935 – 23. 11. 2018)
- Odborné akce 2019
- Invazivní metody při léčbě žilní insuficience
- Česko-slovenská dermatologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- ERYSIPEL (syn. růže)
- Invazivní metody při léčbě žilní insuficience
- Klinický případ: Perianální eroze – stručný přehled
- Diagnostika maligního melanomu s využitím celotělového skenu
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy