-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Nanopatologie - nový vědecký obor
Minireview
Nanopathology as a new scientific discipline
MinireviewThe detection of metal particles in the pathologically altered tissues (eg. in inflammatory lesions or tumors) led to the idea that they might be associated with emergence of some idiopathic diseases. To understand the etiopathogenesis of diseases associated with the presence of nanoparticles in the tissue there is a new area of patology - nanopathology. Numerous studies have shown that nanoparticles can enter the human body through inhalation or ingestion. Through the pulmonary alveoli, skin and intestinal mucosa, the nanoparticles may reach the blood and lymphatic system, which subsequently distributes them to other target organs. Epithelial surfaces of conjunctiva and skin represent another potential way of penetration of nanoparticles into the body. There is a number of studies, which described the adverse effects of ultrafine particles on respiratory and cardiovascular system. Recent studies have also shown that some nanoparticles are able to pass through the pores of the nuclear membrane, where they may pose a risk of damage to cells and genetic information and they are also potentially capable to cross the placental and hematoencephalic barriers. Further, their role in the induction of oxidative stress is significant in relation to the mutagenesis. Scanning electron microscopy with energy disperse spectroscopy (SEM-EDS) represents a suitable tool for identification of metal-based particles in tissues and body fluids. Importance of nanopathogy can be seen in the elucidation of the etiopathogenesis of many diseases, not only of respiratory and cardiovascular systems, but also of many other organ systems.
Keywords:
nanoparticles – nanopathology – diseases of nanoparticles (nanopathologies) – ESEM-EDS
Autoři: Jana Dvořáčková 1,2; Hana Bielniková 2; Jirka Mačák 1,2
Působiště autorů: Lékařská fakulta Ostravská univerzita v Ostravě 1; Ústav patologie, Fakultní nemocnice v Ostravě 2
Vyšlo v časopise: Čes.-slov. Patol., 49, 2013, No. 1, p. 46-50
Kategorie: Trendy v medicíně
Souhrn
Nálezy částic kovů v patologicky změněných tkáních, jako jsou zánětlivé léze, nádory a jiné, vedly k myšlence, že mohou souviset se vznikem některých idiopatických chorob. Pro pochopení etiopatogeneze nemocí, spojených s přítomností nano - a mikročástic v organizmu, vznikla nová oblast patologie - nanopatologie. Četné výzkumy prokázaly, že nanočástice mohou vstupovat do lidského organizmu vdechováním nebo požitím. Průchodem přes plicní alveoly, kůži nebo střevní sliznici se dostávají do krve a lymfy, kdy jsou dále rozváděny do dalších orgánů. Existuje řada studií, ve kterých byl popsán negativní vliv ultrajemných částic na respirační a kardiovaskulární systém. Rovněž dochází k ukládání těchto částic v tkáních. Výzkumy také prokázaly, že některé nanočástice jsou schopny procházet póry jaderné membrány, kdy hrozí riziko poškození genetické informace buňky. Rovněž jsou schopny procházet přes hematoencefalickou a placentární bariéru. Nelze také opomenout jejich úlohu v indukci oxidativního stresu. Hlavním nástrojem k identifikaci těchto částic je skenovací elektronová mikroskopie s energiově disperzní spektroskopií (ESEM-EDS). Na základě tohoto vyšetření lze zjistit přibližnou velikost, morfologii a elementární složení částic. Chybí však metodika, která by umožnila kvantitativní hodnocení. Potenciál nanopatologie lze spatřovat v objasnění etiopatogeneze řady onemocnění a to nejenom respiračního, kardiovaskulárního, ale i řady dalších orgánových systémů.
Klíčová slova:
nanočástice – nanopatologie – nemoci z nanočástic – ESEM-EDSPředmluva
Tímto článkem bychom rádi zvýšili povědomí odborné patologické veřejnosti o problematice nanočástic a nanotechnologiích, které v posledních letech zaznamenávají takřka ve všech odbornostech expanzívní rozvoj, a kromě výhod, které s sebou přinášejí, mohou způsobovat i zdravotní rizika lidské populaci. Objasnit úlohu potencionálního účinku nanočástic na zdraví člověka a zhodnocení environmentálních rizik nanočástic v pracovním i životním prostředí patří k prioritám výzkumných aktivit četných oborů zdravotnictví. Obor patologie by proto neměl zůstávat pozadu a měl by se urychleně zapojit do studia vlivu nanočástic na etiopatogenezu lidských onemocnění. Identifikace zdravotních rizik a hodnocení vlivu na zdraví, dále vývoj, ověření a validace nových citlivých biomarkerů expozice a účinků nanočástic, stejně jako individuální, genetické, behaviorální, socioekonomické, environmentální a institucionální determinanty zdraví a způsoby eliminace rizikových faktorů na všech úrovních, patří k hlavním nosným bodům vyhlášeného Resortního programu výzkumu a vývoje Ministerstva zdravotnictví III (RPV III)(1).
ÚVOD DO PROBLEMATIKY
Nano je předpona soustavy SI a znamená jednu miliardtinu. Pochází z řeckého slova νανοζ, což znamená trpaslík. Od přelomu 20. a 21. století je předpona také používána ve slově nanotechnologie. Jde o skupinu technologií, produkujících nanočástice, které se uplatňují v mnoha oborech. Zkoumání světa v takovýchto rozměrech může obohacovat lidstvo o mnoho poznatků, které postupně nacházejí uplatnění ve všech oborech lidské činnosti, medicínu nevyjímaje.
NANOMEDICÍNA
Nanomedicína je, podle společnosti European Science Foundation (2), definována jako soubor věd a technologií využívaných pro diagnózu, terapii, prevenci chorob a poranění, tišení bolesti i zlepšení lidského zdraví, které používají molekulární nástroje a znalosti o lidském těle na molekulární úrovni. Nanomedicína může být definována také jako prostředek sledování, opravování, stavby a kontroly organismu na molekulární úrovni biologickým systémem, který je tvořen z nanosoučástek a nanosystémů (3). Jako jeden ze zakladatelů nanotechnologie, třebaže ještě nepoužil toto slovo, je označován Richard Feynman, který základní myšlenky představil ve své slavné přednášce, kterou nazval „Tam dole je spousta místa” (There’s Plenty of Room at the Bottom). Přednesl ji v roce 1959 na výroční schůzi Americké společnosti fyziků pořádané na Caltechu (4).
Nanotechnologie využívají poznatků studia o možnostech manipulace s hmotou v atomárním a molekulárním měřítku, přičemž se uplatňují kvantově-mechanické jevy, které se diametrálně vymykají chápání světa v makroskopickém měřítku. Lze tedy říci, že hmota takovýchto rozměrů má vlastnosti zcela odlišné od hmoty makroskopicky patrné, protože se začínají projevovat vlastnosti kvantové fyziky. Díky těmto jevům, které popisuje kvantová fyzika, se otevírají nové perspektivy v oblasti medicíny, v magnetických záznamových mediích, ve výpočetní technice, elektronice, optice a dalších vědních oblastech. Podle Oborného (5), který se nanotechnologiím a jejich uplatnění v praxi dlouhodobě věnuje, dnes nanotechnologie nabízejí nová řešení pro přeměnu biologických systémů a poskytují širokou technologickou základnu i pro medicínu. Citujeme: „Můžeme jmenovat třeba odhalování a léčbu chorob, nahrazování částí lidského těla, regenerativní medicínu, nanometrickou chirurgii, syntézu a cílenou dodávku léků do organismu a podobně“. Předpovědi možností nanotechnologií, pracujících s nano - a mikročásticemi v medicíně, vyvolaly celosvětově velmi intenzívní výzkum.
NANOČÁSTICE
Definice nanočástic není jednotná a pojem zahrnuje několik strukturou rozdílných typů nanočástic. Zdá se, že nanočástice nejlépe vystihuje rozmezí definované metrickým systémem, kdy se jedná o všechny částice větší než 1 nm a menší než 100 nm (6,7).
Nanočástice také můžeme chápat jako seskupení atomů nebo molekul do podoby velmi malé částice. V medicíně se setkáváme s velkým množstvím nanočástic, byť je takto nenazýváme. Jde například o molekulu DNA, jejíž šroubovice má průměr 2,3 nm, nebo molekuly enzymů, jejichž velikosti dosahují několika nm. Ribozomy, proteozomy, protonová pumpa, viry, ATP systémy a fotosystémy jsou pak dokonalé stroje s nanometrickými rozměry.
Nano - a mikročástice jsou všudypřítomné, jsou to produkty nejen moderních nanotechnologií, ale také přírodních jevů typu vulkanické činnosti, či produkty antropogenních aktivit typu hutního průmyslu, rafinerií, elektráren a v neposlední řadě i válečných konfliktů. Velkým zdrojem těchto částic je i kouř cigaret, vaření, spalování v topeništích či nezbytné brzdění aut. Využití nanočástic je v mnoha směrech opravdu přínosné, i když se o jejich prospěchu stále vedou odborné diskuze. Nově publikované vědecké práce (8-11) upozorňují na vážná zdravotní rizika nanotechnologií a nanočástic jako takových. Jde o kardiovaskulární problémy, problémy dýchací soustavy související s fibrózou plic, různé typy artritid a dokonce i nádorové bujení. Nanočástice se dělí na ty, které vznikají jako nežádoucí produkt jiného procesu, a na uměle připravené. Do jaké míry jsou oba typy nanočástic pro člověka nebezpečné je dnes ještě stále předmětem výzkumu.
NANOPATOLOGIE
Problematika vlivu nanočástic na prostředí a zvláště na zdraví má relativně krátkou historii. Poprvé byl termín nanopatologie vysloven italskými vědci, v čele s Gatti a spol. v roce 2001 (12). Tato nová oblast výzkumu studuje interakce mezi organismem a částicemi velikosti v řádech nanometrů. Onemocnění vyvolaná nanočásticemi vznikají při proniknutí a hlavně ukládání anorganických mikročástic a nanočástic v lidském i zvířecím organismu. Gatti (12-15) přišla s myšlenkou, že některé idiopatické choroby onkologické či zánětlivé povahy, mohou souviset s ukládáním těchto částic ve tkáních. K této úvaze jí vedly nálezy mikročástic a nanočástic některých kovů, jako je například titan, železo, chrom, měď, zinek, hliník a další, ve tkáních pacientů s různými chorobami, ať už u kloubů typů artritid nebo plicních fibróz či maligních nádorů, zvl. sarkomů. Gatti tato onemocnění nazvala jako „nanopathologies“ (12,13), volně přeloženo jako onemocnění z nanočástic.
Přítomnost nanočástic je prokazována v různých tkáních lidí (plíce, žaludeční sliznice, játra, ledviny, kloubní pouzdro), kteří žijí v oblastech nebo blízko oblastí válečných konfliktů, jako byla válka v bývalé Jugoslávii či v Perském zálivu, stejně tak jako u vojáků a humanitárních pracovníků, kteří v těchto konfliktech byli účastni. Problematika psychické deprivace a únavového syndromu, kterými byla postižena většina těchto pacientů je známa i široké laické veřejnosti díky médiím. Další událostí, která rozdmýchala úvahy o škodlivosti nanočástic na zdraví, byl letadlový útok na dvojici mrakodrapů WTC v New Yorku, kdy se u zasahujících záchranářů, hasičů a dobrovolníků začaly po čase objevovat četné zdravotní komplikace zahrnující jak kloubní onemocnění, tak postižení kardiovaskulárního a dýchacího systému, dále únavový syndrom a různé psychické problémy (12-19).
Problematika nanočástic a rozvoj nanopatologie vede ke globální snaze o to, aby nově používané uměle vytvářené nanočástice podléhaly přísnému testování. V oboru nanotechnologií byly vyvinuty metodiky měření koncentrace používaných nanočástic. In vitro a in vivo jsou studovány procesy jejich vnikání do různých tkání organismu, ukládání v důležitých orgánech a zdravotní důsledky tělesné kontaminace (20-26). Toxicita nanočástic připravených pro určitou aplikaci musí být známá ještě před jejich praktickým využitím (27).
PRŮKAZ NANOČÁSTIC A JEJICH ÚČINKŮ
Hlavním nástrojem pro analýzu tkání a případnou detekci nanočástic je elektronový skenovací mikroskop s energiově disperzním X-ray spektroskopem (ESEM-EDS). Pomocí tohoto mikroskopu byly objasněny některé patologické nálezy související s četnými kryptogenními chorobami, což vedlo ke schválení Evropského projektu QLRT-2002-147, který je zaměřen na objasňování původu těchto částic a jejich vlivu na zdraví člověka.
Z hlediska toxického působení je důležitý rozměr částic a s ním související reaktivita povrchu a chemické složení. Velmi zajímavý experiment je popsán v práci Limbacha a spol. (28), který studoval nitrobuněčný oxidační proces po expozici lidských plicních epiteliálních buněk in vitro křemennými nanočásticemi legovanými železem, kobaltem manganem a titanem. Výsledkem tohoto velmi pečlivě provedeného experimentu bylo zjištění, že nanočástice se do buněk dostávaly mechanismem „trojského koně“ a vyvolávaly v případě kobaltu a manganu až 8x silnější oxidativní stres, než když byla identická tkáň exponována vodným roztokem stejných kovů. Studium nanočástic obsahujících železo ukázalo, že katalytická aktivita významně zvyšuje destrukční aktivitu nanomateriálů.
Toxicitu nanočástic studoval Xia a spol. (29). Zjistili, že je určena velikostí jejich povrchu, který dobře koreluje s jejich schopností vyvolávat oxidativní stres a aktivovat buňky k vyvolání zánětů. Oxidativní stres se jeví jako možný marker pro určení toxicity nanomateriálů, případně rizika poškození DNA.
Poslední výzkumy také prokázaly, že některé nanočástice jsou schopny procházet póry jaderné membrány, pronikají vnější membránovou obálkou mitochondrií a tím odstartují předčasnou naprogramovanou buněčnou smrt (apoptózu) (30-32). Toto oxidativní poškození buněčných membrán způsobené nanomateriály vyvolává prozánětlivé a profibrózní procesy v tkáni. Průnik do buněčného jádra a interference s genetickým materiálem buňky může vést k ovlivnění cyklu buněčného dělení. Hrozí riziko poškození genetické informace buňky a spolu s vlivem oxidačního stresu vyvolání kancerogeneze. Velikost nanočástic umožňuje procházet přes hematoencefalickou bariéru až do mozku, popřípadě transplacentárně do plodové vody a embrya (33-37). Na obrázku č. 1 demonstrujeme nanočástici wolframu v erytrocytu, kterou jsme náhodně zachytili při zkoumání mozkového glioblastomu.
Obr. 1. Snímek tkáně mozkového nádoru (glioblastom) s erytrocyty ze skenovacího elektronového mikroskopu s EDS detektorem s odpovídajícím EDS spektrem, který je výsledkem bodové analýzy. Píky označené písmenem W dokazují přítomnost nanočástice s obsahem wolframu v erytrocytu. 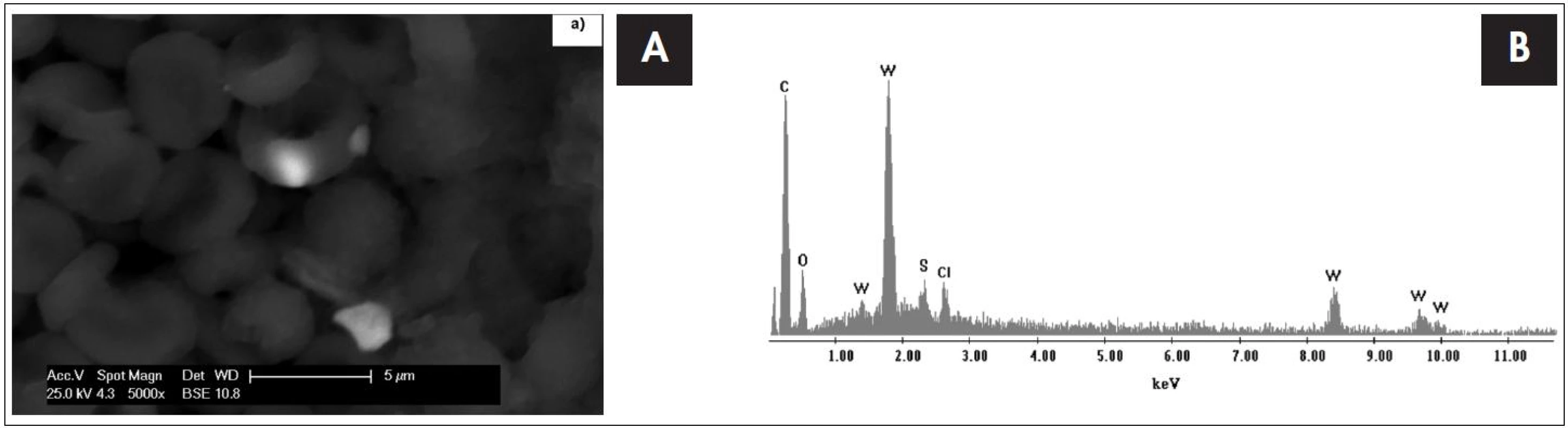
Vyšetření lidských tkání a tekutin X-ray spektroskopem
Ve spolupráci s Centrem nanotechnologií VŠB-TU v Ostravě jsme měli možnost provést řadu vyšetření lidských tonsil. Vyšetření skenovacím elektronovým mikroskopem s energiově dispersním X-ray spektroskopem (ESEM-EDS) při urychlovacím napětím 30 kV ve tkáních prokázalo přítomnost částic ve formě samostatných partikulí nebo shluků jednoho kovu (železa, mědi) či směsi několika kovů (chrom-železo-nikl). Metodika analýzy pomocí ESEM-EDS však neumožňuje kvantitativní hodnocení složení nanočástic. Grafická znázornění v podobě píků jsou výsledkem bodové analýzy ze skenovacího elektronového mikroskopu s EDS detektorem s odpovídajícím EDS spektrem. Píky jsou pouze orientační a vyjadřují maxima výskytu kovových prvků. Velikost nanočástic či jejich shluků kolísá od stovek nanometrů po desítky mikrometrů (obr. 2, 3).
Obr. 2. Snímek tkáně tonzily 4 letého dítěte s chronickou tonzilitidou ze skenovacího elektronového mikroskopu s EDS detektorem s odpovídajícím EDS spektrem, který je výsledkem bodové analýzy. Píky označené písmenem W dokazují přítomnost wolframu v tonsilární tkáni. 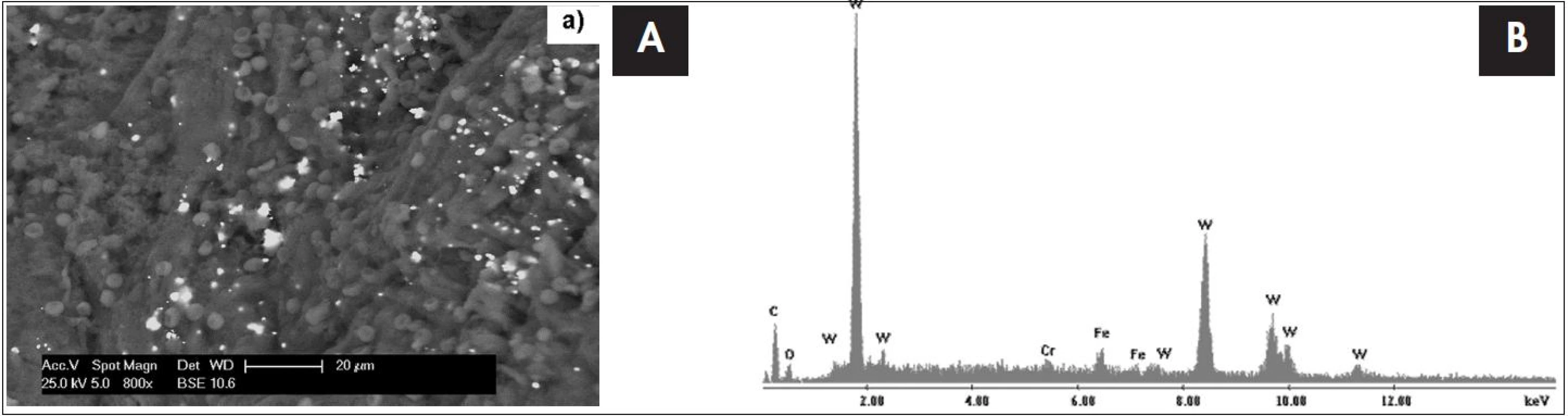
Obr. 3. Snímek tkáně tonsily 48 letého muže - hutníka se spinocelulárním karcinomem patrové mandle ze skenovacího elektronového mikroskopu s EDS detektorem s odpovídajícím EDS spektrem, který je výsledkem bodové analýzy. Píky označené písmenem Cu dokazují přítomnost mědi v nádorové tkáni. 
Výsledky našich pozorování byly již publikovány (38). Práce se zabývá problematikou vlivu nanočástic jako potenciálního vyvolavatele zánětlivých i neoplastických onemocnění v lidských patrových mandlích v souvislosti s demografickými údaji. Upozorňuje na nutnost řešení kvantitativního stanovení kovových prvků a jejich biokinetiku, které mohou podrobněji doložit vztah mezi diagnózou a přítomností specifických kovových nanočástic v tonzilární tkáni.
VZNIK ONEMOCNĚNÍ Z NANOČÁSTIC A DŮSLEDKY PRO OBOR PATOLOGIE
Snahou celosvětového výzkumu je zjistit nejen původ všech těchto částic, ale také vysvětlit biologické, chemické a toxické pochody, které vedou ke změně buněčného chování. Předpokládá se, že nanočástice mohou vznikat např. jako vedlejší produkty kouření cigaret. Ten může obsahovat kovy například hliník, kadmium, nikl, olovo a měď ve formě velmi malých částic. Jiné kovy, například železo, zinek, cín, baryum, antimon a titan, jsou ve formě nanostrukturovaných částic uvolňovány při spalování fosilních paliv, otěrem pneumatik o povrch silnic, otěrem brzdových destiček a otěrem kuchyňského nádobí (39-43). Významným zdrojem jsou i emise velkých průmyslových podniků. V pyrometalurgii při sváření jsou běžně popisovány stopové prvky jako je železo, chrom, mangan, nikl, měď, zinek a wolfram v bezprostředním okolí pracoviště. Baryum, berylium, kadmium, kobalt, molybden, niob, antimon a vanad jsou zase charakteristické pro uhelný prach (44-46). V poslední době bylo publikováno několik prací, z nichž nejrozšířenější jsou reference na výsledky studia v UCLA (University of California in Los Angeles), kde byl zjištěn vliv nejjemnější frakce částic z výfukových plynů. Ty způsobují tvorbu povlaků na endotelu arterií a deaktivují ochrannou funkci HDL (vysokodenzního lipoproteinu). Toto „mechanické“ poškození vede ke vzniku kardiopulmonálních, respiračních a dalších onemocnění (47).
K běžně používaným nanomateriálům patří oxid titaničitý, oxidy zinku a stříbra. Tyto jsou součástí bělidel, dezinfekčních prostředků a textilií. Obecně je známo jejich toxické působení například na bakterie Escheria coli, Staphylococcus aureus a jiné. Současně však byla posuzována i možná zdravotní rizika z jejich používání. Bylo zjištěno, že nanočástice stříbra zhoršují mitochondriální funkce, posilují tvorbu reaktivního kyslíku, spotřebovávají antioxidanty, poškozují DNA, což může vyústit v následnou cytotoxicitu (48). Nanočástice oxidu titaničitého či oxidu zinečnatého jsou obecně považovány za méně toxické. Z dosavadních výzkumů oxidu titanu se soudí, že zánětlivé plicní procesy včetně fibrózy mohou být způsobovány právě účinkem reaktivního kyslíku. Ten může být zdrojem dalších cytotoxických dopadů včetně iniciace kancerogeneze. Jeho přítomnost byla kromě plic pozorována i v ledvinách, játrech a mozku, což podtrhuje teorii transportu nanočástic krevní cestou (49).
SHRNUTÍ
Nanočástice snadno pronikají do těla a jsou biologicky aktivnější než částice větší, a to pravděpodobně v důsledku jejich většího měrného povrchu. Hovoříme o bioaktivitě nanočástic. Dalším významně nebezpečným faktorem je dlouhodobé přetrvávání nanočástic v prostředí a jejich kumulace v něm. Oblast výzkumu vlivu nanočástic na lidský organismus má stále spoustu nezodpovězených otázek, na které bude třeba najít odpovědi.
Dosud nejsou známy všechny příčiny podílející se na schopnosti nanočástic vyvolat patologickou reakci v lidském organismu. Problém nanočástic se může týkat psychických poruch, nárůstu sebevražd nebo souviset i s objasněním nespecifických nálezů náhlých úmrtí dospělých (50). Oboru patologie, genetiky i soudního lékařství se tak otevírají nové možnosti objasnění či přehodnocení etiopatogeneze řady onemocnění, včetně analýzy jejich morfologických změn, které s nimi souvisejí. Rozvoj a zapojení moderních molekulárně-genetických technologií na úrovni DNA, genů, genové exprese může přinést nové informace o vlivu a případné genotoxicitě nanočástic na organismus.
Závěr
Záměrem autorů tohoto textu bylo zvýšit povědomí odborné patologické veřejnosti o existenci problematiky nanočástic a jejich vlivů na zdraví. Byly publikovány stovky prací, které apelují na environmentální rizika související s naším způsobem života. Jde také o důsledky lidské činnosti při aplikaci nadčasových technologií, které s sebou přinášejí i určitá zdravotní rizika. Z množících se publikací oboru nanomedicíny a nanotoxikologie vyplývá pro obor patologie výzva, zda nebude nutno přehodnotit etiopatogenezi některých onemocnění. Jde o řadu onemocnění respiračního traktu, kardiovaskulárních a onkologických onemocnění, artritid a v neposlední řadě i psychiatrických a neurologických nemocí.
PODĚKOVÁNÍ
Poděkování doc. Mgr. Janě Kukutschové, Ph.D. z Centra Nanotechnologií VŠB TU v Ostravě za analýzu ESEM-EDS a věcné připomínky.
Adresa pro korespondenci:
MUDr. Jana Dvořáčková, Ph.D.
Ústav patologie FNO, Ostrava
17. listopadu 1790
708 00 Ostrava-Poruba
jana.dvorackova@fno.cz
Zdroje
1. http://iga.mzcr.cz/shareIGA/RPV_III.pdf
2. www.esf.org
3. Drexler KE. Engines of creation. The coming era of nanotechnology (1st ed.). Anchor Books: New York; 1986 : 320.
4. Drexler KE. Nanosystems: Molecular machinery, manufacturing and computation (1st ed.) Wiley: New York; 1992 : 576.
5. Ježek M. Nanomedicína jako standard, během několika let, říkají vědci. Zdravotnické noviny 2008; 47 : 22-24.
6. Bureau International des Poids et Mesures. Le SystŹme international d’unités (SI) – The International System of Units (SI) (8th ed). Paris: Stedi-Media; 2006 : 5, 32.
7. Hlaváček A. Nanočástice a jejich biokonjugáty. www.nanobio.cz/articles: 2011; 1.
8. Oberdörster G, Oberdörster E, Oberdörster J. Nanotoxicology: An emerging discipline evolving from studies of ultrafine particles. Environ Health Perspect 2005; 113(7): 823-839.
9. Shvedova AA, Kisin ER, Porter D, et al. Mechanism of pulmonary toxicity and medical applications of carbon nanotubes. Two face of Janus? Pharmacol Ther 2009; 121(2): 192-204.
10. Firme CP, Bandaru PR. Toxicity issues in the application of carbonanotubes to biological systems. Nanomed: Nanotech Biol Med 2010; 6(2): 245-256.
11. Hu X, Cook S, Wang P, Hwang H, Liu X, Williams QL. In vitro evaluation of cytotoxicity of engineered carbon nanotubes in selected human cell lines. Sci Total Environ 2010; 408(8): 1812-1817.
12. Gatti AM, Montanari S. Nanopathology. The health impact of nanoparticles (1st ed.) Singapore: Pan Stanford Publishing; 2008 : 312.
13. http://steng.giftfabrikken.nu/media/Nanopartikler.pdf
14. Hansen T, Clermont G, Gatti AM, et al. Biological tolerance of different materials in bulk and nanoparticulate form in a rat model. Sarcoma development by nanoparticles. J R Soc Interface 2006; 3(11): 767-775.
15. Peters K, Unger RE, Kirkpatrick CJ, Gatti AM, Monari E. Effects of nano-scaled particles on endothelial cell function in vitro: Studies on viability, proliferation and inflammation. J Mater Sci Mater Med 2004; 15(4): 32-325.
16. Chiu S, Niles JK, Webber MP, Zeig-Owens R, Gustave J, Lee R, Rizzotto L, Kelly KJ, Cohen HW, Prezant DJ. Evaluating risk factors and possible mediation effects in posttraumatic depression and posttraumatic stress disorder comorbidity. Public Health Rep. 2011; 126(2): 201-209.
17. Chiu S, Webber MP, Zeig-Owens R, Gustave J, Lee R, Kelly KJ, Rizzotto L, McWilliams R, Schorr JK, North CS, Prezant DJ. Performance characteristics of the PTSD Checklist in retired firefighters exposed to the World Trade Center disaster. Ann Clin Psychiatry. 2011; 23(2): 95-104.
18. Cukor J, Wyka K, Jayasinghe N, Weathers F, Giosan C, Leck P, Roberts J, Spielman L, Crane M, Difede J Prevalence and predictors of posttraumatic stress symptoms in utility workers deployed to the World Trade Center following the attacks of September 11, 2001. Depress Anxiety. 2011; 28(3): 210-217.
19. DiGrande L, Neria Y, Brackbill RM, Pulliam P, Galea S. Long-term posttraumatic stress symptoms among 3,271 civilian survivors of the September 11, 2001, terrorist attacks on the World Trade Center. Am J Epidemiol. 2011; 173(3): 271-281.
20. Zhou L; Wan-Xi Y, Nanoparticles and Spermatogenesis: How do Nanoparticles Affect Spermatogenesis and Penetrate the Blood–testis Barrier. Nanomedicine 2012; 7(4): 579-596.
21. Panyala N, Pena-Mendez E, Havel J. Silver or silver nanoparticles: a hazardous threat to the environment and human health. J Appl Biomed 2008; 6 : 117–129.
22. Hussain SM, Braydich-Stolle LK, Schrand AM, et al. Toxicity evaluation for safe use of nanomaterials: recent achievements and technical challenges. Adv Mater 2009; 21(16): 1549–1559.
23. Stern ST, McNeil SE. Nanotechnology safety concerns revisited. Toxicol Sci 2008; 101(1): 4–21.
24. Tsai C, Shiau A, Chen S, Chen Y, Cheng P, Chang M. Amelioration of collagen-induced arthritis in rats by nanogold. Arthritis Rheum. 2007; 56(2): 544–554.
25. Geiser M, Kreyling WG. Deposition and biokinetics of inhaled nanoparticles. Part Fibre Toxicol. 2010; 7(2): 1-17.
26. Gatti AM, Montanari S, Monari E, Gambarelli A, Capitani F, Parisini B. Detection of micro - and nano-sized biocompatible particles in the blood. J Mater Sci Mater Med. 2004; 15(4): 469-472.
27. http://ec.europa.eu/environment/chemicals/nanotech/pdf/commission_recommendation
28. Limbach LK, Bereiter R, Müller E, Krebs R, Gälli R, Stark WJ. Removal of oxide nanoparticles in a model wastewater treatment plant: Influence of agglomeration and surfactants on clearing efficiency. Environ Sci Technol 2008; 42(15): 5828-5833.
29. Xia T, Kovochich M, Brant J, et al. Comparison of the abilities of ambient and manufactured nanoparticles to induce cellular toxicity according to an oxidative stress paradigm. Nano Lett 2006; 6(8): 1794-1807.
30. Chen X, Deng C, Tang S, Zhang M. Mitochondria-dependent apoptosis induced by nanoscale hydroxiapatite in human gastric cancer SGC-7901 cells. Biol Pharm Bull 2007; 30(1): 128-132.
31. Wang J, Li N, Zheng L, et al. P38-Nrf-2 signaling pathway of oxidative stress in mice caused by nanoparticulate TiO2. Biol. Trace Elem. Res.2011; 140 (2): 186–197.
32. Gurr JR, Wang AS, Chen CH, Jan KY. Ultrafine titanium dioxide particles in the absence of photoactivation can induce oxidative damage to human bronchial epithelial cells. Toxicology 2005; 213(1–2): 66–73.
33. Hartwig A. Carcinogenicity of metal compounds: possible role of DNA repair inhibition. Toxicol Lett 1998; 102-103 : 235-239.
34. Mehta M, Chen LCh, Gordon T, Rom W, Tang MS. Particulate matterinhibits DNA repair and enhances mutagenesis. Mutat Res 2008; 657(2): 116-121.
35. Okada S. Iron-induced tissue damage and cancer: The role of reactive oxygen species-free radicals. Pathol Int 1996; 46(5): 311-332.
36. Reichrtová E, Dorociak F, Palkovičová L. Sites of lead and nickel accumulation in the placental tissue. Hum Exp Toxicol 1998; 17(3):176-181.
37. Claderon-Garciduenas L, Azzarelli B, Acuna H, et al. Air pollution and brain damage. Toxicol Pathol 2002; 30(3): 373-389.
38. Zeleník K, Kukutschová J, Dvořáčková J, Bielniková H, Peikertová P, Cábalová L, Komínek P. Possible role of nano-sized particles in chronic tonsillitis and tonsillar carcinoma: a pilot study. Eur Arch Otorhinolaryngol. In press 2013.
39. Liati A, Eggenschwiler PD. Characterization of particulate matter deposited in diesel particulate filters: Visual and analytical approach in macro-, micro-and nano-scales. Comb and Fl 2010; 157(9): 1658-1670.
40. Verhoeven JD, Pendray AH, Clark HF. Wear test of steel knife blades. Wear 2008; 265 : 1093-1099.
41. Kukutschová J, Moravec P, Tomášek V, et al. On airbone nano/micro-sized wear particles released from low-metallic automative brakes. Environ Poll 2011; 159(4): 998-1006.
42. Kreider ML, Panko JM, McAtee BL, Sweet LI, Finley BL. Physical and chemical characterization of tire-related particles: Comparison of particles generated using different methodologies. Sci Total Environ 2010; 408(3): 652-659.
43. Kukutschová J, Roubíček V, Malachová K, et al. Wear mechanism in automotive brake materials, wear debris and its potential environmental impact. Wear 2009; 267 : 807-817.
44. Seidlerová J. Metody hodnocení metalurgických odpadů, (1th end). Ostrava: Repronis; 2009.
45. Sezimová H, Malachová K, Rybková Z, Truxocá I, Krejčí B. Toxikologický a genotoxikologický screening kvality ovzduší v centru Ostravy, Acta Enviromentalica Universitatis Comenianae 2012; 20(1): 76-81.
46. Cheng YH, Chao YC, Wu CH, Tsai CJ, Uang SN, Shih TS. Measurements of ultrafine particle concentrations and size distributionin an iron foundry. J Hazard Mater 2008; 158(1): 124-130.
47. http://www.advisorybodies.doh.gov.uk/comeap/statementsreports/CardioDisease.pdf
48. Ahamed M, Alsahli MS, Siddiqui MK. Silver nanoparticle applications and human health. Clin Chem Acta 2010; 411(23-24): 1841-1848.
49. Nohavica D. Rizika nanomateriálů a nanotechnologií pro lidské zdraví a životní prostředí. Čs. Čas. Fyz. 2011; 61(3): 220-227.
50. Dvořáček I. Postup lékaře při úmrtí mimo zdravotnické zařízení a následná součinnost s orgány PČR. Soud lek. 2005; 4 : 54-56.
Štítky
Patológia Súdne lekárstvo Toxikológia
Článek Česká eponyma v patologii
Článok vyšiel v časopiseČesko-slovenská patologie

2013 Číslo 1-
Všetky články tohto čísla
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Patologie dolního GIT
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Pulmopatologie
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Patologie hlavy a krku
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Hematopatologie
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Patologie mammy
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Endokrinní patologie
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Cytopatologie
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Ortopedická patologie
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Hepatopatologie
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Nefropatologie
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Uropatologie
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Neuropatologie
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Novinky v molekulární patologii
- Možnosti průkazu biologicky relevantní papilomavirové infekce u maligních nádorů hlavy a krku v diagnostické patologii
-
UPDATE IN PATHOLOGY 2012
24. Evropský kongres patologie v Praze -
HLAVOVA CENA a LAMBLOVA CENA
za rok 2012 -
Dysplázie sliznice žaludku.
Klinickopatologická studie 35 případů - Autofagické vakuolární myopatie – aneb co nás naučila diferenciální diagnostika vakuol ve svalové biopsii
- O 24. evropském kongresu patologie v Praze s prezidentem místního organizačního výboru prof. Alešem Ryškou
-
Nanopatologie - nový vědecký obor
Minireview - With the president of the ESP - Prof. Carneiro - about the 24th European Congress of Pathology in Prague 2012
- Prof. MUDr. Zdeněk Nožička, DrSc., osmdesátiletý
- Česká eponyma v patologii
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Gynekopatologie
- 24th EUROPEAN CONGRESS OF PATHOLOGY 2012, PRAHA - Horní GIT a pankreas
- Česko-slovenská patologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Česká eponyma v patologii
-
Dysplázie sliznice žaludku.
Klinickopatologická studie 35 případů - Autofagické vakuolární myopatie – aneb co nás naučila diferenciální diagnostika vakuol ve svalové biopsii
- Možnosti průkazu biologicky relevantní papilomavirové infekce u maligních nádorů hlavy a krku v diagnostické patologii
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



