-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Tumor endolymfatického vaku – vzácná komplikace syndromu von Hippel-Lindau
Endolymphatic sac tumour – a rare complication associated with von Hippel-Lindau disease
We report the case of a 42-year – old female with familiar form von Hippel-Lindau disease (VHL) and recurrent endolymphatic sac tumour (ELST), which was presented like non-homogenous, solid and cystic expansion of the left petrous temporal bone. Histologically, there was found lamellae of bone with adjacent ligament and with papillary projections with fibrovascular core. The papillae were lined by a single layer of cuboidal epithelium with hyperchromatic and lightly pleomorphic nuclei. Sporadically, small cystic formations with eosinophilic, PAS positive secretion were noted. Imunohistochemically, the cuboidal cells showed diffuse positivity for vimentin, epithelial membrane antigen (EMA), cytokeratin AE1/AE3 and S100 protein (weakly). Other markers examined, including TTF1, PAX8 and CD10, were negative. Endolymphatic sac tumour is rare low-grade malignant epithelial tumour arising from the endolymphatic sac in the temporal bone, which occurs in 1 out of 30 000 births, with just fewer than 300 cases reported in the literature. About one third of cases are associated with von Hippel - Lindau disease, an autosomal dominant familial cancer syndrome.
Keywords:
temporal bone – endolymphatic sac tumour – von Hippel-Lindau disease
Autori: Mária Wozniaková 1,2; Vladimír Židlík 1,2; Jozef Škarda 1,2
Pôsobisko autorov: Ústav klinické a molekulární patologie a lékařské genetiky, Oddělené klinické a molekulární patologie, Fakultní nemocnice Ostrava, Ostrava 1; Ústav klinické a molekulární patologie a lékařské genetiky, Lékařská fakulta, Ostravská univerzita, Ostrava 2
Vyšlo v časopise: Čes.-slov. Patol., 59, 2023, No. 1, p. 32-35
Kategória: Původní práce
Súhrn
Prezentujeme případ 42leté ženy s potvrzeným zděděným syndromem von Hippel-Lindau (VHL) a s recidivujícím tumorem endolymfatického vaku (ELST) vlevo, který se prezentoval jako nehomogenní, solidně – cystická expanze pyramidy vlevo. Histologicky byly zastiženy lamely kosti s přilehlým vazivem a s přítomností léze papilárního vzhledu tvořenou centrálně vazivovou a cévnatou tkání, na jejíž papily nasedají poměrně drobné kubické elementy s lehce nepravidelnými hyperchromními jádry. Ojediněle byly zastiženy i drobné cystické formace s obsahem PAS pozitivního eozinofilního materiálu. Imunohistochemicky vykazovaly kubické elementy difuzní expresi vimentinu, epiteliálního membránového antigenu (EMA), cytokeratinu AE1/AE3 a S100 proteinu (pouze slabě). Další vyšetřované markery zahrnující TTF1, PAX8 a CD10 byly negativní. Tumor endolymfatického vaku je vzácný low-grade maligní epiteliální tumor vycházející z endolymfatického vaku v temporální kosti, s incidencí 1 : 30 000, s popsanými méně než 300 případy. Asi 1/3 z nich je asociována s VHL, autozomálně dominantním familiárním nádorovým syndromem.
Klíčová slova:
tumor endolymfatického vaku – syndrom von Hippel-Lindau – temporální kost
Tumor endolymfatického vaku (ELST) je vzácná nemetastazující papilární epiteliální neoplazie vycházející z endolymfatického vaku. Roste pomalu, je lokálně agresivní a manifestuje se jako expanzivní a lokálně destruktivní masa, která invaduje do temporální kosti a zadní jámy lební. Je také známý jako Heffnerův tumor nebo low-grade papilární adenokarcinom původem z endolymfatického vaku. Poprvé byl popsán v roce 1984 (1), ale až Heffner v roce 1989 charakterizoval ELST jako tumor vycházející z epitelu endolymfatického vaku vnitřního ucha a popisuje ho jako „low-grade adenokarcinom“. (2) Histologicky pozorujeme papilární, fokálně cysticky utvářený tumor s jednou vrstvou blandně vyhlížejících kubických až cylindrických buněk, bez mitóz a bez nekróz. Manski et al. uvádí, že incidence ELST je u dospělé populace 1 : 30 000 (3) a asi 1/3 případů je asociována s VHL, přičemž se objeví pouze u 10 % těchto pacientů. (4) U části z nich se vyskytuje dokonce bilaterálně. Obvykle způsobuje ztrátu sluchu, tinnitus, vertigo a dysfunkci faciálního nervu. Léčba zahrnuje resekci tumoru anebo radikální mastoidektomii, někdy v kombinaci s radioterapií. U velkých tumorů je kompletní excize téměř nemožná, proto u nich pozorujeme lokální rekurence. (5)
MATERIÁL A METODIKA
Materiál fixovaný v 10% formalínu byl zpracován standardním způsobem, zalit do parafínu (formalin-fixed paraffin-embedded, FFPE), nakrájen na mikrotomu a obarven hematoxilin-eosinem a dále speciálním barvením PAS. Imunohistochické vyšetření bylo provedeno metodou avidin-biotin komplex (ABC metoda) na reprezentativním bloku. Byly použity následující protilátky: vimentin (klon Vim3B4, 1 : 100, Dako), EMA (klon E29, 1 : 200, Bio SB), cytokeratin (klon AE1/AE3, 1 : 200, Zytomed), S100 protein (1 : 600, Dako), Ki67 (klon SP6, 1 : 200, Zytomed), TTF1 (klon 8G7G3/1, 1 : 300, Zytomed), PAX8 (klon MRQ-50, AUTO, Cell Marque) a CD10 (klon 56C6, 1 : 100, Novocastra).
POPIS PŘÍPADU
V tomto sdělení prezentujeme případ 42leté ženy s potvrzeným VHL, kterým trpěli i její otec, strýc a dědeček. Pacientka už v roce 1997 podstoupila revizi míšního konu pro histologicky verifikovaný hemangioblastom. Další ložiska hemangioblastomů (celkem 4), která jsou ošetřena pouze radioterapií, se nachází v zadní jámě. Postupně se u ní objevily poruchy sluchu a rovnováhy a na kontrolní MR (obr. 1) byla už v roce 2001 infratentoriálně zjištěna rozsáhlá, nehomogenní, solidně – cystická expanze pyramidy vlevo, která se propagovala do zadní jámy a do temporální oblasti, oplošťovala levou mozečkovou hemisféru a brachium pontis vlevo, celkové velikosti 47x52 mm. Radiologicky i klinicky imponovala jako dermoid. Byla jí proto provedena revize a částečná exstirpace s klinickým nálezem kostních cyst vyplněných hnědavou tekutinou. Nález byl uzavřen jako „agresivní papilární tumor temporální kosti a endolymfatického vaku“ /adenokarcinom nízkého stupně malignity/. Postupně ale došlo k progresi růstu a ke zhoršování vertiga, proto byla 19 let po první operaci indikována další exstirpace.
Obr. 1. MRI: Solidně – cystická masa pyramidy. 
K vyšetření jsme obdrželi vícečetné částice béžové barvy, velikosti do 15x10x10 mm, které byly kompletně zpracovány. Mikroskopicky se jednalo o vzorky převážně se strukurami papilárně utvářeného tumoru tvořeného centrálně cévnatě vazivovou tkání, ložiskově hyalinizovanou, na kterou nasedaly drobné kubické buňky s hyperchromními a lehce nepravidelnými jádry (obr. 2, 3, 8, 9). Ojediněle byly zastiženy i drobné propacystické formace, které obsahovaly PAS pozitivní eozinofilní materiál (obr. 4). Mitotická aktivita, nekróza, jaderné atypie ani vaskulární invaze nebyly zastiženy. Imunohistochemicky vykazovaly popsané buňky difuzní a silnou expresi vimentinu (obr. 5), EMA (obr. 6) a cytokeratinu AE1/AE3 (obr. 7). Protein S100 byl exprimován slabě. Proliferační aktivita detekována imunohistochemickým průkazem Ki67 nepřekročila 1 %. Reakce s protilátkami CD10, PAX8 a TTF1 byla negativní. Tento nález zapadá do diagnózy ELST.
Obr. 2. Přehledový snímek (HE, zvětšení 40x). 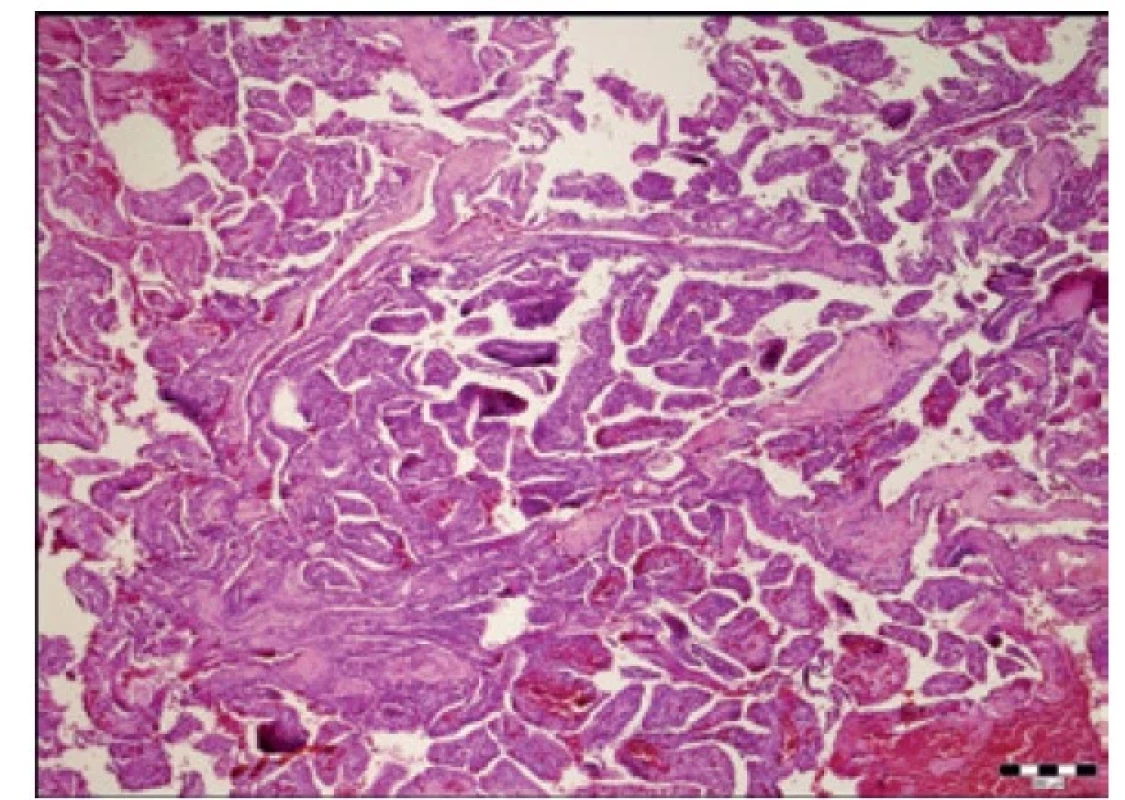
Obr. 3. Cévnaté papily kryté nízkým kubickým epitelem (HE, zvětšení 100x). 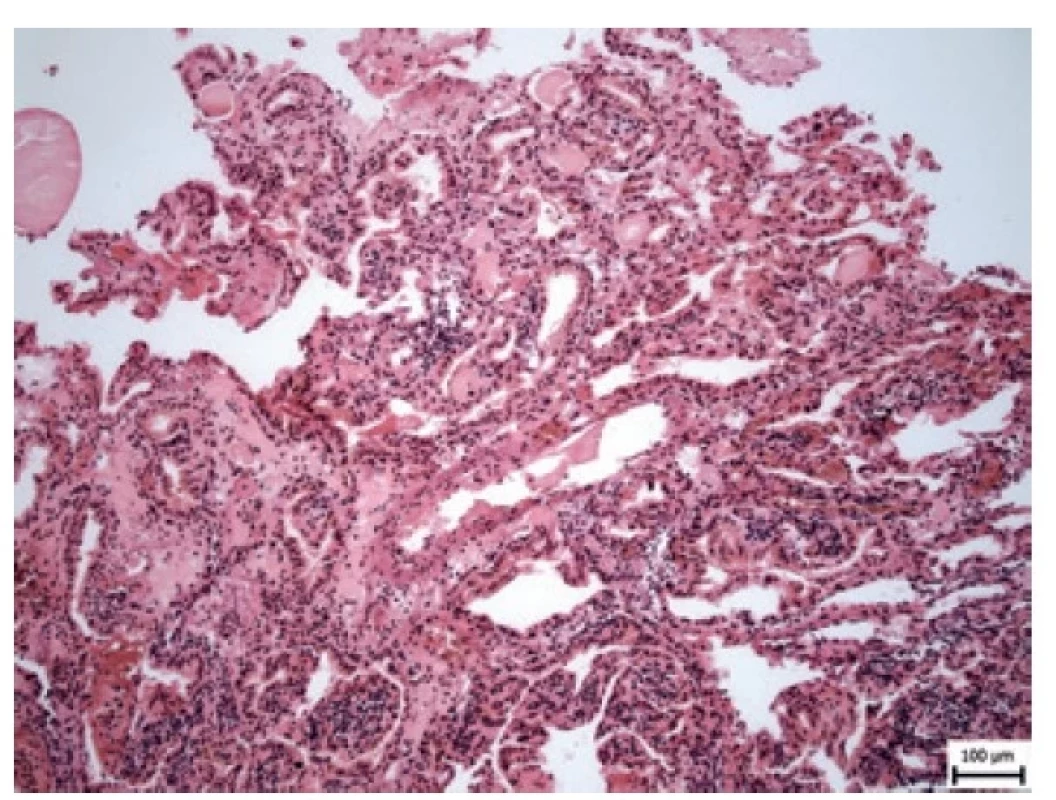
Obr. 4. Drobné cystické formace (PAS, zvětšení 100x). 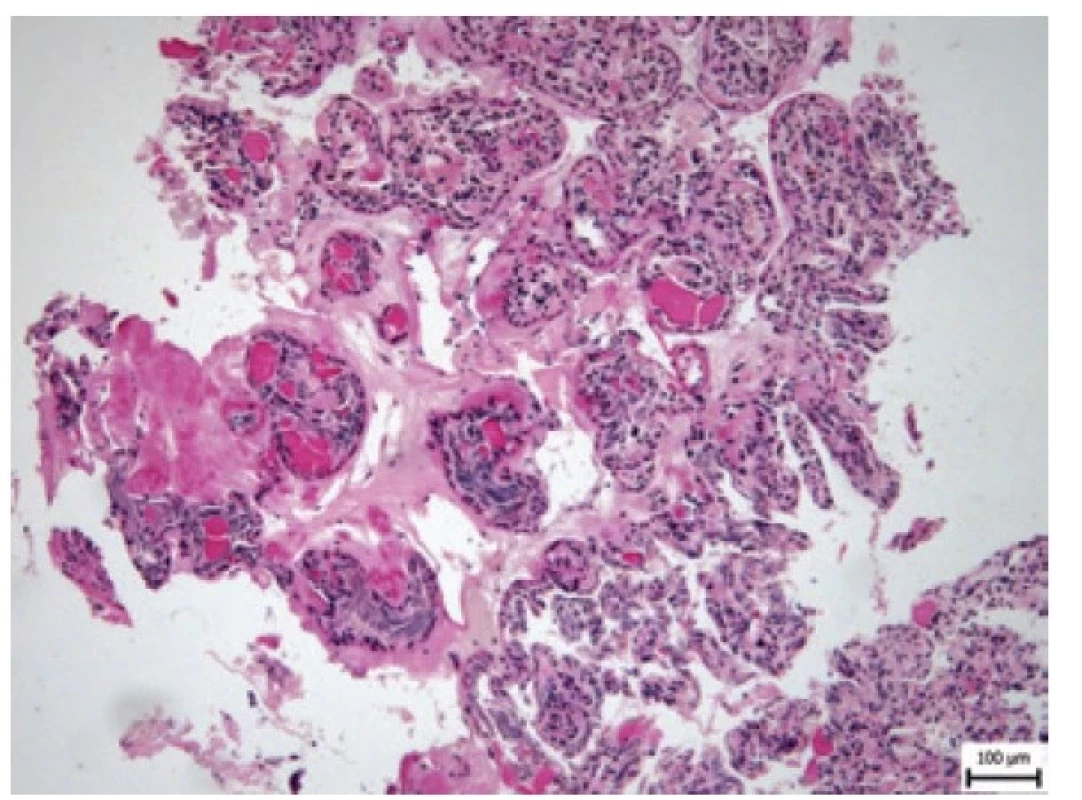
Obr. 5. Imunohistochemický průkaz vimentinu (zvětšení 100x). 
Obr. 6. Imunohistochemický průkaz EMA (zvětšení 100x). 
Obr. 7. Imunohistochemický průkaz cytokeratin AE1/AE3 (zvětšení 100x). 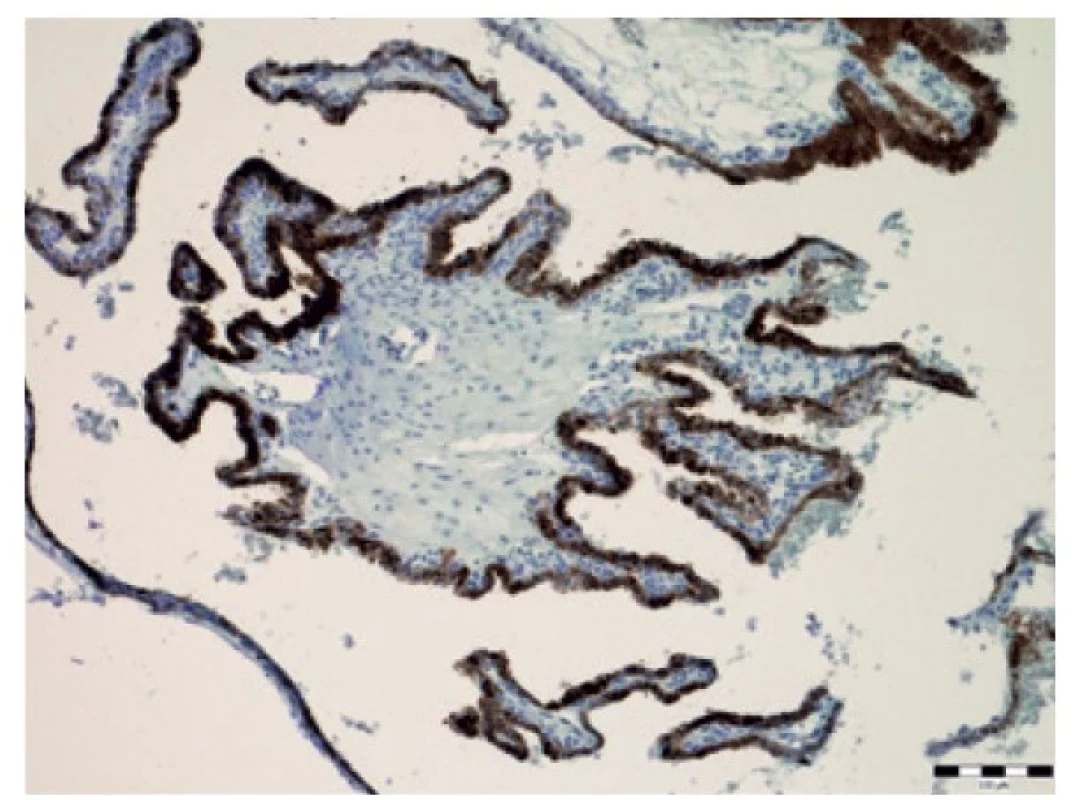
Obr. 8. Drobné cystické a papilární formace (HE, zvětšení 200x). 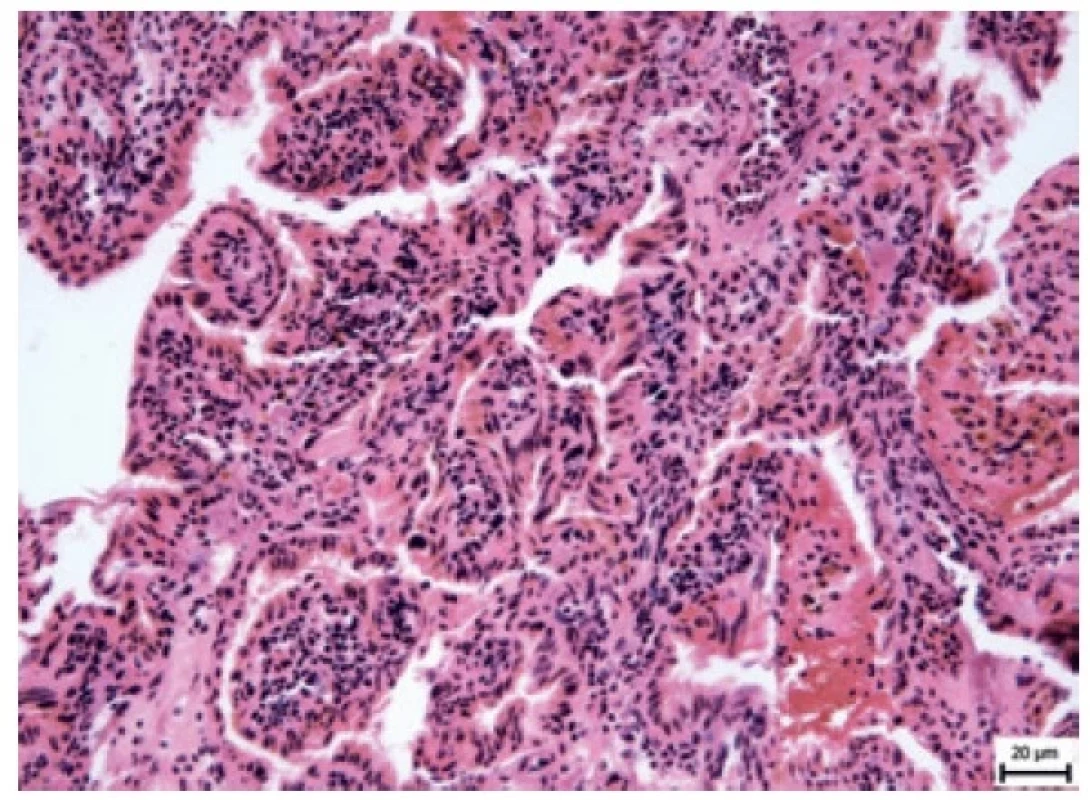
Obr. 9. Detail nádorových buněk (HE, zvětšení 400x). 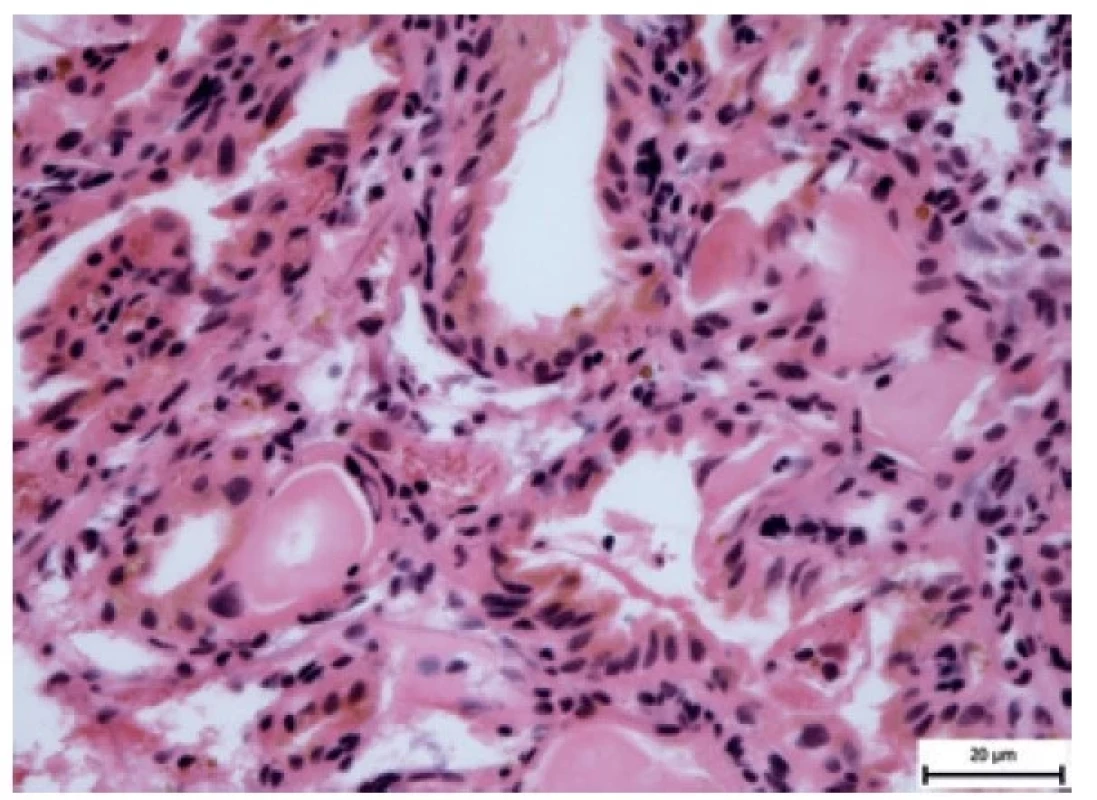
Pacientce exstirpace přinesla úlevu, nicméně má parézu levého lícního nervu a je hluchá na levé ucho. Kromě výše zmíněných hemangioblastomů a ELST zatím další tumory nemá.
DISKUZE
Syndrom von Hippel-Lindau je autozomálně dominantně dědičná porucha charakterizována rozvojem světlobuněčného renálního karcinomu, kapilárního hemangioblastomu CNS a retiny, feochromocytomu, tumorů pankreatu a vnitřního ucha. Jeho incidence je asi 1 na 36 000 živě rozených dětí. VHL je způsobený mutací VHL tumor supresorového genu na krátkém raménku chromozomu 3, který kóduje protein, jehož hlavní funkcí je regulace odpovědi na hypoxické stavy organismu. Pokud je gen VHL mutovaný, tak aktivuje řadu angiogenních, růstových a mitogenních faktorů (VEGF, PDGF beta, TGF alfa), což vede ke vzniku neoplazií. Střední délka života u pacientů s VHL je 49 let. Specifické genotypové a fenotypové korelace v postižených rodinách vedly dále k subklasifikaci VHL na typ 1 a 2, která je primárně založená na přítomnosti feochromocytomu. U typu 1 je riziko jeho vzniku velmi nízké, typ 2 se dále dělí na typ 2a (nízké riziko vzniku RCC), 2b (vysoké riziko vzniku RCC) a typ 2c (pouze feochromocytom). (6) Příčinou výrazné morbidity a mortality u těchto pacientů jsou zejména CNS neoplazie, které vznikají primárně pod tentoriem v oblasti mozečku, mozkového kmene, míchy i vnitřního ucha.
Tumor endolymfatického vaku je vzácný, pomalu rostoucí low-grade maligní tumor, který infiltrativně a destruktivně roste do temporální kosti a objevuje se u pacientů s věkovým průměrem 4 až 85 let, o něco víc u žen. (7) Spojení mezi VHL a ELST bylo prvně publikováno Ebym et al. v roce 1988, který popsal pacienta s VHL s bilaterální lézí a s pozitivní rodinnou anamnézou. (8) Pacienti pozorují nespecifické příznaky jako je ztráta sluchu, tinnitus a vertigo, což se na první pohled může jevit jako Menierova nemoc. Tyto příznaky jsou následkem hemoragie uvnitř labyrintu, endolymfatického hydropsu (blokáda endolymfatických cest či extenzivní peritumorální extravazace tekutiny) anebo přímé invaze do sluchového aparátu. (5) S jeho dalším růstem se dále často objevuje paralýza lícního nervu či poruchy mozečku. (4) Na zobrazovacích metodách imponuje jako lytická léze mastoidního výběžku petrózní kosti s propagací do okolních struktur (středního ucha, střední a zadní jámy lebeční nebo do mostomozečkového koutu). (5)
Histologicky je tumor papilárně cystickou žlázovou neoplazií s pestrými růstovými vzory. Papily jsou stejně jako cystické prostory kryté vrstvou oploštělého, nízce kubického až cylindrického epitelu. Jádra vykazují mírnou variabilitu ve velikosti a tvaru, bývají lokalizovaná centrálně nebo u apexu. Cytoplazma bývá bledě eozinofilní až světlá. Dále můžou být přítomny malé žlázky a folikulární struktury obsahující silně eozinofilní „colloid-like“ sekret, který je pozitivní v PAS reakci a připomíná tkáň štítné žlázy. Mitózy a nekrózy jsou vzácné. Stroma bývá bohatě vaskularizované, často s přítomností chronické zánětlivé celulizace. Dále bývají zastiženy i okrsky hypocelulární fibrózy, hemoragie, dystrofické kalcifikace, cholesterolové krystaly a na ně navazující reaktivní změny. Nádorové elementy typicky exprimují cytokeratiny, EMA, vimentin a S100. Důležitým diagnostickým znakem jsou dále i známky destrukce kosti nebo chrupavky. (7-10)
ELST vychází z endolymfatického vaku původem z neuroektodermu a nachází se mezi periostem porózní kosti a tvrdou plenou zadní jámy lební, za vnitřním zvukovým kanálem. Existují 4 potenciální cesty lokálního šíření tohoto tumoru: posteromediálně do mostomozečkového koutu, laterálně do středního ucha, nahoru do střední jámy lební a anteromediálně podél hřebene petrózní kosti do kavernózního a sfenoidálního sinu. (7)
Vzhledem k raritnímu výskytu může být ELST při diagnostice lehce zaměněn za jiné, zejména papilární léze. Základní diferenciální diagnostika zahrnuje proto paragangliom, papilom choroidálního plexu, papilární ependymom, adenom středního ucha (dle nové WHO klasifikace nádorů hlavy a krku z roku 2022 již neuroendokrinní tumor středního ucha – middle ear neuroendocrine tumor/MeNET), papilární meningiom a metastatický karcinom štítné žlázy, ledviny, prostaty, plíce a mléčné žlázy. (10) Jester et al. ve své práci popisují soubor pacientů s ELST, které exprimují renální markery (PAX8, PAX2 a CA-9), proto je nutné v rámci diferenciální diagnostiky metastatického světlobuněčného renálního karcinomu (ccRCC), který se často objevuje u pacientů s VHL, použít další vyšetření (např. CD10 a RCC). Reakce s protilátkou PAX8 byla v našem případě negativní, ačkoliv v literatuře se její exprese udává až v 85 % případů (11). Ve většině (58 %) zároveň prokázali kombinovanou ztrátu 3p (zahrnující VHL gen) a 9q, což naznačuje podobný původ ELST a ccRCC včetně genu VHL, který pravděpodobně hraje ústřední roli v jejich patogenezi. (12)
Zlatým standardem léčby je radikální chirurgická excize nebo mastoidektomie. Ta je ale možná pouze u tumorů malé velikosti. U lokálně pokročilých lézí, kde úplné odstranění není kvůli anatomickému uspořádání možné, se proto parciální exstirpace doplňuje adjuvantní pooperační radioterapií, která se rovněž využívá i u recidiv. Některá pracoviště využívají i embolizaci před operací, protože tumor má bohaté cévní zásobení. (5, 13)
ZÁVĚR
Závěrem lze shrnout, že ELST je velmi vzácný tumor, počet popsaných případů je méně než 300 (4) a je na něj nutno pamatovat zejména u pacientů, kteří mají diagnostikován tumor invadující do temporální kosti a se současně potvrzeným VHL. Morfologický obraz je poměrně charakteristický, imunohistochemické vyšetření nám tuto vzácnou lézi potvrdí. Správná diagnostika je klíčem k další terapii a dlouhodobému sledování pacienta, které je vzhledem k poměrně častým recidivám a infiltrativnímu růstu nutné.
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Adresa pro korespondenci:
MUDr. Mária Wozniaková
Fakultní nemocnice Ostrava
Ústav klinické a molekulární patologie a lékařské genetiky
Oddělení klinické a molekulární patologie
17. listopadu 1790/5, Ostrava, 708 52
tel.: +420775031754
email: maria.wozniakova@fno.cz
Zdroje
1. Hassard AD, Boudreau SF, Cron CC. Adenoma of the endolymphatic sac. J Otolaryngol 1984; 13 : 213-216.
2. Heffner DK. Low-grade adenocarcinoma of probable endolymphatic sac origin. A clinicopathologic study of 20 cases. Cancer 1989; 64 : 2292-2302.
3. Manski TJ, Heffner DK, Glenn GM, et al. Endolymphatic sac tumors: A source of morbid hearing loss in von Hippel-Lindau disease. JAMA 1997; 277 : 1461-1466.
4. Mendenhall WM, Suárez C, Skálová A, et al. Current Treatment of Endolymphatic Sac Tumor of the Temporal Bone. Adv Ther 2018; 35 : 887-898.
5. Wind JJ, Lonser RR. Management of von Hippel-Lindau disease-associated CNS lesions. Expert Rev Neurother 2011; 11(10): 1433-1441.
6. Varshney N, Kebede AA, Owusu-Dapaah H, Lather J, Kaushik M, Bhullar JS. A Review of Von Hippel-Lindau Syndrome. J Kidney Cancer VHL 2017; 4(3): 20-29.
7. Sun YH, Wen W, Wu JH, et al. Endolymphatic sac tumor: case report and review of the literature. Diagn Pathol 2012; 7 : 36.
8. Eby TL, Makek MS, Fisch U. Adenomas of the temporal bone. Ann Otol Rhinol Laryngol 1988; 97 : 605-612.
9. Malhotra S, Rao RV, Valiathan M, Mathew M, Nayak DR, Raja A. Low-grade adenocarcinoma of endolymphatic sac origin. Am J Otolaryngol 2006; 27 : 362-365.
10. Yang X, Liu XS, Fang Y, Zhang XH, Zhang YK. Endolymphatic sac tumor with von Hippel - Lindau disease: report of a case with atypical pathology of endolymphatic sac tumor. Int J Clin Exp Pathol 2010; 7(5): 2609-2614.
11. Thompson LDR, Magliocca KR, Andreasen S, et al. CAIX and pax-8 Commonly Immunoreactive in Endolymphatic Sac Tumors: A Clinicopathologic Study of 26 Cases with Differential Considerations for Metastatic Renal Cell Carcinoma in von Hippel-Lindau Patients. Head Neck Pathol 2019; 13 : 355-363.
12. Jester R, Znoyko I, Garnovskaya M, et al. Expression of renal cell markers and detection of 3p loss links endolymphatic sac tumor to renal cell carcinoma and warrants careful evaluation to avoid diagnostic pitfalls. Acta Neuropathologica Communications 2018; 6 : 107.
13. Alkhotani A, Butt B, Khalid M, Binmahfoodh M, Al-Said Y. Endolymphatic sac tumor at the cerebellopontine angle: A case report and review of literature. Int J Surg Case Rep 2019; 58 : 162-166.
Štítky
Patológia Súdne lekárstvo Toxikológia
Článek Novinky v pulmopatologiiČlánek 'NEUROPATOLOGIEČlánek 'NEFROPATOLOGIEČlánek 'GYNEKOPATOLOGIEČlánek 'HEPATOPATOLOGIEČlánek 'PATOLOGIE GITČlánek 'CYTODIAGNOSTIKAČlánek 'PATOLOGIE ORL OBLASTIČlánek 'KARDIOPATOLOGIEČlánek 'PULMOPATOLOGIEČlánek 'UROPATOLOGIE
Článok vyšiel v časopiseČesko-slovenská patologie

2023 Číslo 1-
Všetky články tohto čísla
- Novinky v pulmopatologii
- Patolog vychovává svého klinika a klinik patologa
- 'NEUROPATOLOGIE
- 'NEFROPATOLOGIE
- 'GYNEKOPATOLOGIE
- 'HEPATOPATOLOGIE
- 'PATOLOGIE GIT
- 'CYTODIAGNOSTIKA
- 'PATOLOGIE ORL OBLASTI
- 'KARDIOPATOLOGIE
- 'PULMOPATOLOGIE
- 'UROPATOLOGIE
- Současné možnosti odlišení histopatologického obrazu idiopatické plicní fibrózy od fibrotické hypersenzitivní pneumonie: Jak na to?
- Malobuněčný karcinom plic – nové poznatky o biologii nádoru
- Kazuistika – Warthin-like papilokarcinom štítné žlázy
- Metylační analýza jako pomocný nástroj v cytologické diagnostice vzácnějších anogenitálních lézí – pilotní studie
- Tumor endolymfatického vaku – vzácná komplikace syndromu von Hippel-Lindau
- Karel Rokitanský (1804 - 1878)
- Česko-slovenská patologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Metylační analýza jako pomocný nástroj v cytologické diagnostice vzácnějších anogenitálních lézí – pilotní studie
- Malobuněčný karcinom plic – nové poznatky o biologii nádoru
- Kazuistika – Warthin-like papilokarcinom štítné žlázy
- Tumor endolymfatického vaku – vzácná komplikace syndromu von Hippel-Lindau
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



