-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Diagnostický algoritmus potravinovej alergie v detskom veku
Diagnostic Algorithm of Food Allergy at the Child Age
Diagnostics of food allergy (FA) belongs to complicated matters of child immunoallergology and gastroenterology. Clinical diagnosis is established on the basis of results of individual standardized methods in vivo as well as in vitro. FA is based on immunological grounds and the specialist should uncover them.
The diagnostics of FA in clinical practice is based on a panel of standardized examinations which include: the determination of specific IgEs against food allergens, skin prick tests and atopic patch tests, elimination diets and oral load tests. In addition to these tests there is a group of other examinations which could soon become the part of standardized algorithms for FA: the test of activation and degranulation of basophiles and some new markers of allergic inflammation in stools, blood or urine (eosinophil protein X, eosinophil cationic protein, tryptase, α1-antitrypsin, leukotriene E4, eotaxin, TNF-α, histamine, methyl-histamine). On the other hand there is a group of diagnostic procedures of speculative nature which should not be further recommended as suitable methods (e.g. skin application food tests, labial load test, the determination of specific antibodies of class IgG, sublingual and intradermal provocation/neutralization tests, cytotoxic tests, applied kinesiology, electrodermal testing, etc.).
Diagnostics and therapy of food allergy belongs exclusively into the hands of an experienced specialist (child gastroenterologist in cooperation with immuno-allergologist and dermatologist) with extensive experience in interpretation of results of individual methods of examination, which are the basis for subsequent indication of a therapeutic diet or other therapeutic procedures.Key words:
atopic patch tests, diagnostic algorithm, child, elimination diet, skin prick tests, oral load tests, food allergy, specific IgEs, standardized tests
Autori: M. Jeseňák 1,2
; Z. Havlíčeková 1
; J. Buchanec 1; M. P. Villa 2; R. Ronchetti 2; Peter Bánovčin 1
Pôsobisko autorov: Klinika detí a dorastu, Univerzita Komenského, Jesseniova lekárska fakulta, Martin prednosta prof. MUDr. P. Bánovčin, CSc. 1; Clinica Pediatrica, Universita „La Sapienza“, Ospedale Sant’Andrea, Via Grottarossa, Rome, Italy prednosta prof. M. P. Villa, MD., PhD. 2
Vyšlo v časopise: Čes-slov Pediat 2008; 63 (5): 272-282.
Kategória: Postgraduální vzdělávání
Súhrn
Diagnostika potravinovej alergie (PA) patrí medzi komplikované kapitoly detskej imunoalergológie a gastroenterológie. Klinická diagnóza je stanovená na základe výsledkov jednotlivých štandardizovaných metód in vivo aj in vitro. PA musí mať imunologický podklad a úlohou špecialistu je ho objektivizovať.
Na diagnostiku PA máme v klinickej praxi k dispozícii panel štandardizovaných vyšetrení, medzi ktoré dnes radíme: stanovenie špecifických IgE proti potravinovým alergénom, kožné prick testy a atopické patch testy, eliminačné diéty a orálne záťažové testy. Popri týchto metódach existuje skupina testov, ktoré by sa perspektívne mohli v blízkej budúcnosti stať súčasťou štandardizovaných algoritmov PA: test aktivácie a degranulácie bazofilov a niektoré nové markery alergického zápalu v stolici, krvi či moči (eozinofilový proteín X, eozinofilový kationický proteín, tryptáza, α1-antitrypsín, leukotrién E4, eotaxín, TNF-α, histamín, metylhistamín). Na druhej strane existuje skupina diagnostických procedúr, ktoré majú pri diagnostike PA skôr „špekulatívne“ postavenie a nemožno ich stále odporúčať ako vhodné metódy (napr. kožné aplikačné potravinové testy, labiálny záťažový test, stanovenie špecifických protilátok z triedy IgG, sublingválne a intradermálne provokačné/neutralizačné testy, cytotoxické testy, aplikovaná kineziológia, elektrodermálne testovanie).
Diagnostika a liečba potravinovej alergie patrí výsostne do rúk skúseného odborníka (detský gastroenterológ v spolupráci s imuno-alergológom a dermatológom), ktorý má rozsiahle skúsenosti s interpretáciou výsledkov jednotlivých vyšetrovacích metód, na základe ktorých môže potom indikovať terapeutickú diétu, resp. iné liečebné postupy.Kľúčové slová:
atopické patch testy, diagnostický algoritmus, dieťa, eliminačná diéta, kožné prick testy, orálne záťažové testy, potravinová alergia, špecifické IgE, štandardizované testyÚvod
Potravinová alergia sprevádza ľudstvo od nepamäti. Už Hippokrates a Galén dokumentovali alergické reakcie po požití niektorých potravín, avšak vedomostný rozmach v tejto oblasti medicíny nastal až v dvadsiatom storočí. Poznatky o tomto pomerne častom ochorení sú značné, i keď na druhej strane treba priznať, že nie všetko chápeme do takých detailov, aby sme terapeuticky kauzálne „reštituovali“ porušenú funkciu imunity vedúcu k prejavom potravinovej alergie. Jej prevalencia, podobne ako aj v prípade mnohých iných alergických ochorení, stúpa, a to predovšetkým v detskom veku.
Na jednej strane existuje fenomén vyhasínania, vďaka ktorému väčšina detí zo svojej alergie na tú ktorú potravinu časom vyrastie (fenomén neskorého navodenia orálnej tolerancie), na strane druhej však majú v budúcnosti väčší predpoklad vývinu iného (obyčajne respiračného) alergického ochorenia ako ostatná časť populácie. Naliehavosť nájsť čo najoptimálnejší a najpraktickejší diagnostický test podčiarkuje aj negatívny vplyv v podstate jediného terapeutického prostriedku – eliminačných diét – na vyvíjajúci sa detský organizmus. Aj samotný „zlatý štandard“ v diagnostike potravinovej alergie – dvojito slepý, placebom kontrolovaný, orálny záťažový test – nie je jednoduché realizovať vzhľadom na jeho časovú náročnosť, nevyhnutnú spoluprácu pacienta, riziko anafylaktickej reakcie a niekedy aj problematické vyhodnotenie klinickej odpovede organizmu.
V priebehu rokov sa objavovali mnohé laboratórne, zobrazovacie či klinické diagnostické metódy s rôznou výpovednou hodnotou. Mnohé z nich sú zahrnuté v skupine štandardizovaných testov, avšak stále ostáva veľa takých, ktoré na svoje jednoznačné miesto v diagnostike potravinovej alergie ešte len čakajú.
Potravinová alergia
Je všeobecne známe, že v ostatných desaťročiach výskyt mnohých ochorení má výrazne stúpajúcu tendenciu. Medzi ne určite patrí aj skupina alergických ochorení s predominanciou najmä v nižšom veku. Potravinová alergia (PA) je menšou časťou veľkej skupiny klinických prejavov, ktoré súhrnne označujeme ako potravinová hypersenzitivita (nežiaduce alebo adverzné potravinové reakcie) [1].
Potravinovú hypersenzitivitu možno definovať ako akúkoľvek nepríjemnú, nežiadúcu reakciu organizmu na požitú stravu. Na rozdiel od potravinových intolerancií, pri ktorých vzniku nedokážeme účasť imunologických mechanizmov, PA je dôsledkom abnormálnej imunologickej odpovede organizmu na jednu alebo viaceré zložky požitej stravy. Ide o ochorenie, pri ktorom ingescia aj malého množstva kauzálnej potraviny spúšťa imunologicky sprostredkovanú klinickú odpoveď.
Podľa typu alergickej reakcie rozdeľujeme potravinové alergie na IgE sprostredkované („klasický“ typ PA) a non-IgE sprostredkované (tzv. „neatopické“ PA, na ktorých vzniku majú podiel najmä reakcie celulárnej imunity, ale aj 2. a 3. typ alergickej reakcie), obr. 1 [2]. Len u asi 1 z 15 detí, ktoré majú anamnestický údaj nežiadúcej reakcie na potraviny, sa PA potvrdí aj diagnosticky [3].
Obr. 1. Klasifikácia potravinovej hypersenzitivity. 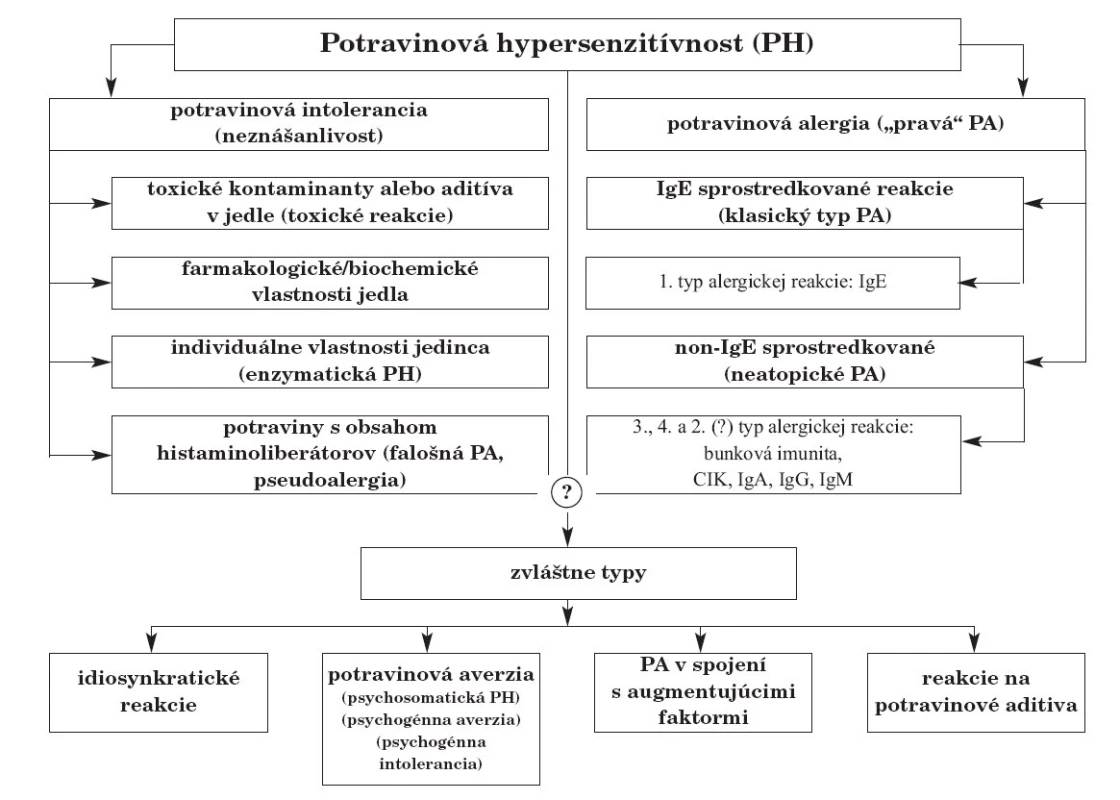
Diagnostika potravinovej alergie/intolerancie
Diagnostika potravinovej alergie/intolerancie patrí medzi komplikované kapitoly imunoalergológie a gastroenterológie detského veku. Klinická diagnóza je stanovená na základe výsledkov jednotlivých štandardizovaných metód in vivo aj in vitro, avšak ani jedna z nich nemá pri negativite výsledku 100% schopnosť PA definitívne vylúčiť. Potravinová alergia musí mať imunologický podklad a úlohou špecialistu je ho objektivizovať. Samotná existencia imunologickej hypersenzitivity (resp. senzitizácie) však ešte diagnózu neurčuje. Musí byť potvrdená príčinná súvislosť medzi laboratórnym nálezom, požitím suspektnej potraviny a klinickými príznakmi pacienta [4]. Presná diagnostika PA nie je dôležitá len pre správnu liečbu, ale aj vzhľadom na vyvarovanie sa zbytočným, často drastickým eliminačným diétam, ktoré majú extrémne negatívny vplyv na vyvíjajúci sa detský organizmus.
Na diagnostiku PA máme v klinickej praxi k dispozícii panel vyšetrení, ktoré sa navzájom rozlišujú svojou špecificitou, senzitivitou, prediktabilitou, reproducibilitou, klinickou využiteľnosťou a praktickosťou. Mnohé z vyšetrení v algoritmoch diagnostiky PA sú štandardizované, majú jasne definovaný postup, ako ich v klinickej či ambulantnej praxi prevádzať a zároveň majú presne daný návod na hodnotenie odpovede organizmu, určenie pozitívneho alebo negatívneho výsledku, prípadne aj odlíšenie falošne pozitívnych a negatívnych odpovedí (obr. 2).
Obr. 2. Štandardizované testy v diagnostike potravinovej alergie. 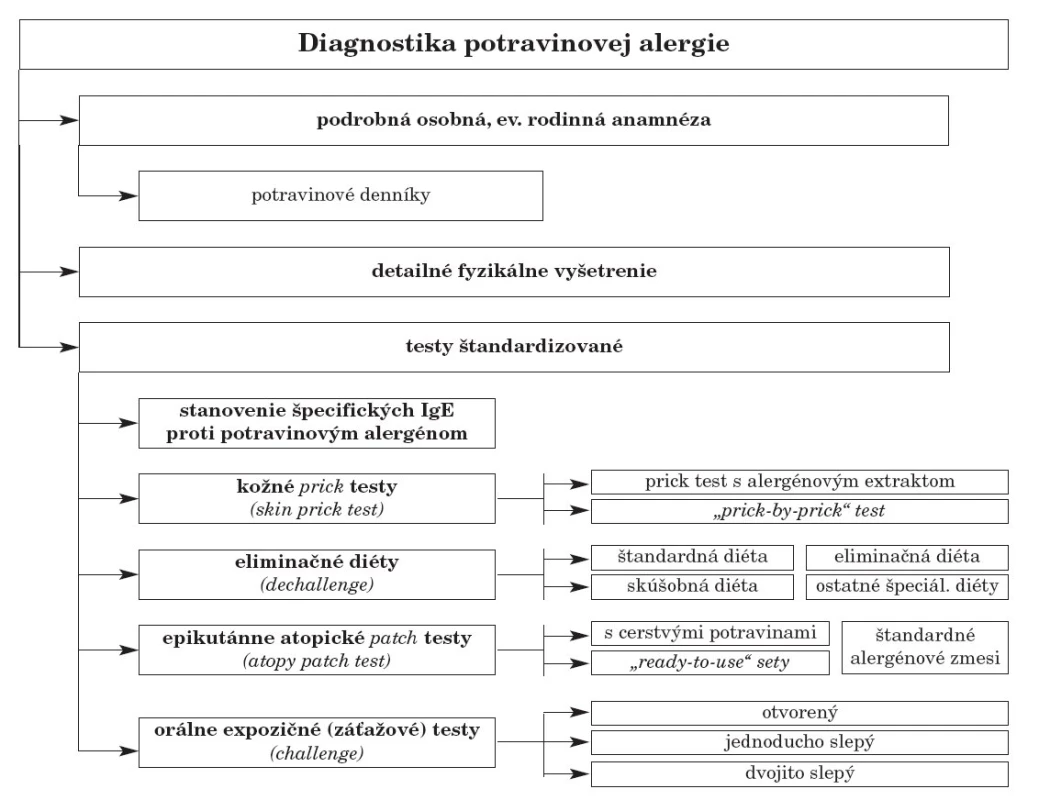
Ďalšiu zaujímavú skupinu diagnostických metód tvoria viaceré laboratórne ako i klinické testy, ktoré by sa na základe publikovaných štúdií mohli v krátkej budúcnosti zaradiť do algoritmov diagnostiky PA a tým napomôcť v zložitom manažmente tohto ochorenia. Na druhej strane existuje skupina mnohých diagnostických procedúr, ktoré sú obsolentné a nemožno ich odporúčať ako vhodné metódy s klinicky definovanou relevantnosťou [5, 6].
Pri diagnostike PA (obr. 3) postupujeme nasledovne:
Obr. 3. Stručný algoritmus diagnostiky potravinovej alergie. 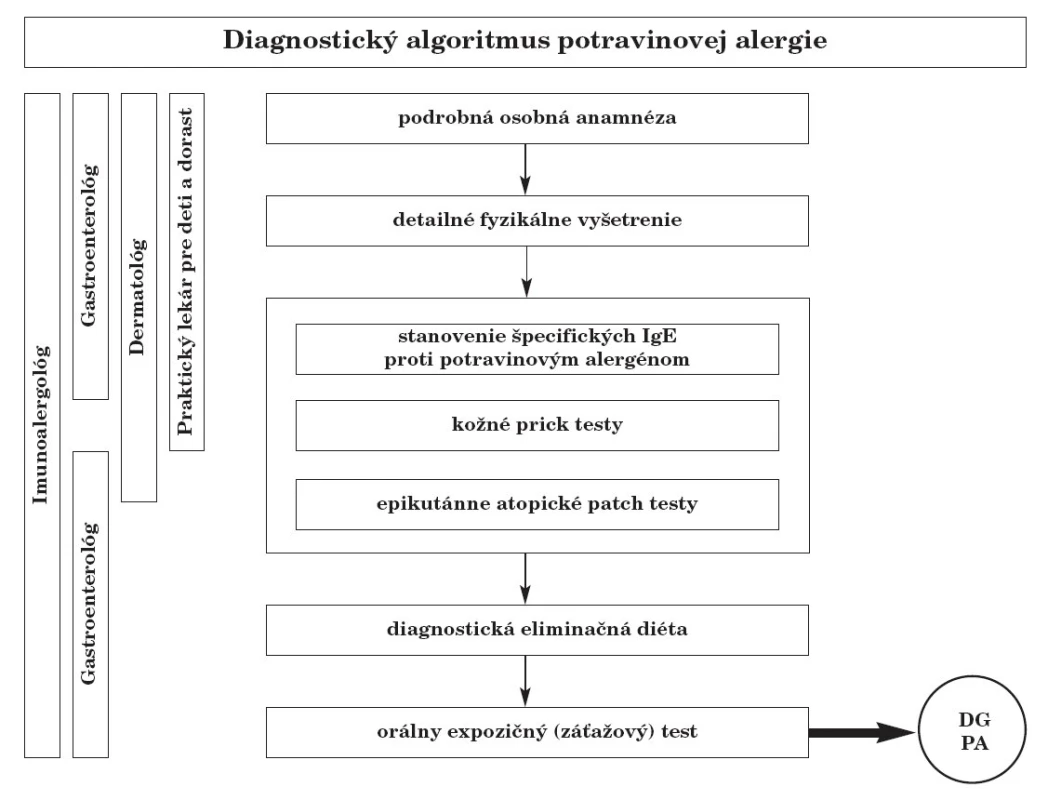
A. Podrobná osobná anamnéza s detailným fyzikálnym vyšetrením so zameraním sa na somatické prejavy potravinovej alergie
Pri zisťovaní anamnestických údajov nás zaujíma [7, 8]: druh, kvantita a kvalita (aj spôsob úpravy a prípravy) potraviny, ktorá je podozrivá, že spúšťa u postihnutého dieťaťa alergickú reakciu; latencia medzi ingesciou jedla a objavením sa príznakov (čím kratší interval, tým väčšia pravdepodobnosť PA); typ symptómov a pridružené vyvolávajúce faktory (napr. námaha, niektoré lieky); trvanie príznakov; reokurencia subjektívnych i objektívnych príznakov pri opätovnom požití daného jedla (tzv. reproducibilita príznakov); kedy naposledy pacient pozoroval príznaky PA a eventuálny potenciálny „cross-kontakt“ (napr. kontaminácia potraviny inou potravinou).
Vhodnou pomôckou sú aj tzv. potravinové denníky, v ktorých si pacient (alebo rodičia u detí) zapisuje systematicky všetky potraviny a nápoje, ktoré skonzumoval a zároveň hodnotí aj aktuálny klinický stav so zameraním sa na jednotlivé symptómy PA, resp. aj iné okolnosti (požitie liekov, menštruácia, námaha). Pri podrobnej analýze všetkých potravín skonzumovaných v dňoch, kedy boli pozorované klinické prejavy alergie, možno nájsť tú/tie potraviny, ktoré sú možnou príčinou alergickej reakcie. Potom na základe týchto pozorovaní možno previesť orálny expozičný test s podozrivými potravinami zistenými práve na základe potravinového denníka [9]. Výhodou potravinových denníkov je, že zbierajú informácie prospektívne, čiže nie sú na rozdiel od anamnézy závislé od pacientovej pamäti [8] a zároveň pacient nie je obmedzovaný žiadnymi diétnymi predpismi. Na druhej strane môže byť vedenie potravinových denníkov časovo náročné a pozorovania bývajú niekedy mätúce, najmä pri častom výskyte istých príznakov vo vzťahu k mnohým potravinám [9].
Klinický nález pri fyzikálnom vyšetrení, najmä u symptomatických pacientov, môže podporiť diagnózu PA alebo odhaliť iné alergické či nealergické ochorenie. Žiadny z klinických príznakov však nie je patognomický pre PA [9, 10]. Potravinová alergia môže postihnúť takmer ktorýkoľvek orgán alebo systém. V detskom veku sú najčastejšie príznaky z postihnutia gastrointestinálneho traktu (cca 2/3 všetkých reakcií), kože (1/2 reakcií), ale aj dýchacieho systému (asi 1/3 prejavov sa môže obmedziť len na edém, hypersekréciu a obštrukciu v dýchacích cestách). V dospelom veku prevládajú kožné, gastrointestinálne a respiračné príznaky, pričom cca 1 % všetkých reakcií sa prejaví anafylaxiou. Kombinácia postihnutia jednotlivých systémov je skôr pravidlom ako výnimkou (obr. 4) [4].
Obr. 4. Klinické príznaky potravinovej alergie. 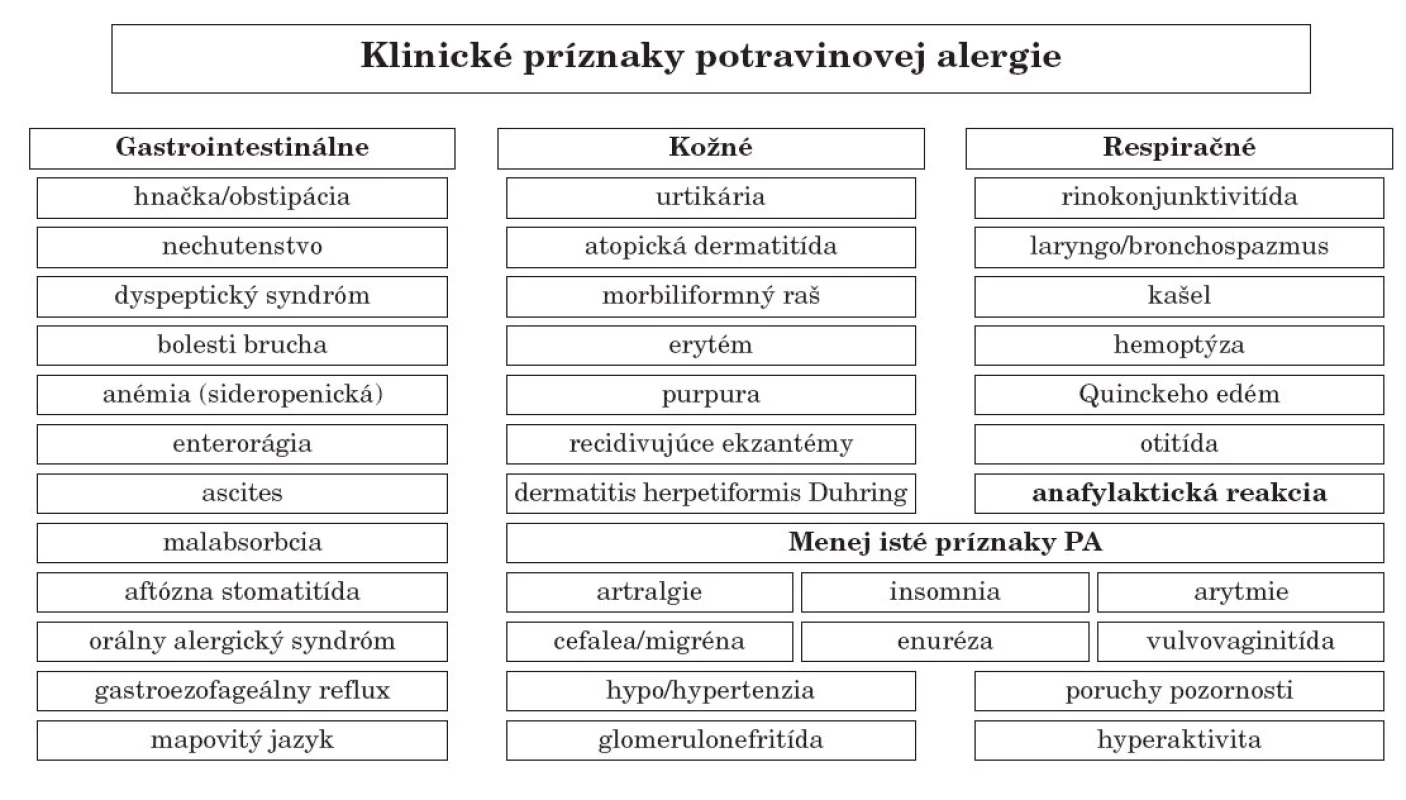
B. Štandardizované testy pre diagnostiku PA
Stanovenie špecifických IgE proti potravinovým alergénom (sIgE):
Meranie špecifických protilátok z triedy IgE má význam pri PA sprostredkovanej IgE (1. typ alergickej reakcie). T. č. máme k dispozícii mnoho nových laboratórnych metód pre kvantifikáciu alergén-špecifických IgE v sére a na povrchu bazofilov. Princípom tejto analýzy je detekcia naviazaných špecifických IgE zo séra pacienta na nosiči s antigénom pomocou rádioizotopových metodík – RAST (rádioalergosorbentový test), alebo pomocou enzymatických metód – ELISA (enzyme-linked, immunosorbent assay). Modernou modifikáciou týchto metód stanovenia sIgE je vysokoafinitná fluorenzymoimunoanalýza (FEIA) a dvojkroková chemiluminiscenčná metóda stanovenia sIgE [11].
Viacerí autori porovnávali koncentráciu špecifických IgE v sére s výsledkami orálnych expozičných testov (OET) s cieľom stanoviť hraničné hodnoty koncentrácie pre jednotlivé potravinové alergény určujúce pravdepodobnosť vzniku alergickej reakcie na danú potravinu u pacienta s touto definovanou koncentráciou sIgE. Pre niektoré potraviny sa podarilo túto hladinu stanoviť (napr. arašidy 14 kU/l, mlieko 15 kU/l, vajce 7 kU/l) [12, 13], pre iné potraviny sa tieto diagnostické prahové hodnoty naopak nepodarilo určiť (pšenica, sója) [12, 14].
Niektorí autori dokázali, že pokles sIgE proti danému potravinovému alergénu môže predpovedať vývoj klinickej tolerancie na potravinu [14]. Cenným ukazovateľom rozvoja tolerancie môžu byť peptid-špecifické IgE [15]. Meranie sIgE v pravidelných intervaloch môže pomôcť lekárom pri stanovovaní prognózy a určovaní primeraných časových intervalov pre opakovanie expozičných testov, čím sa zníži počet predčasných a zbytočných dvojito slepých, placebom kontrolovaných testov [5].
Kožné prick testy (SPT):
Mnoho desaťročí sa senzibilizácia pacientov na potravinové alergény hodnotila práve prostredníctvom kožných prick testov, ktoré možno označiť za nepriame provokačné testy, keďže ich pozitivita či negativita dokazuje senzibilizáciu organizmu bez informácie o reaktivite cieľových orgánov. Použitie SPT využíva fakt, že senzibilizovaný jedinec má sIgE proti alergénom nielen v cieľovom orgáne, v ktorom sa prejavujú klinické príznaky, ale aj na membránach mastocytov prítomných v koži. Vpravený alergén sa naviaže na molekuly sIgE na povrchu mastocytov a následne dôjde k ich degranulácii s uvoľnením mediátorov. Tie pôsobením na okolité cievy vyvolávajú tzv. Lewisov trias: erytém + edém + svrbenie. Reakcia začína cca po 5 minútách od vpravenia alergénu, vrcholí v dobe 15–20 minút, potom pomaly odoznieva. Neskorá fáza reakcie (väčšinou nenasleduje) sa prejaví až za niekoľko hodín a je spôsobená nahromadením neutrofilov a najmä eozinofilov v lokalite, kde bol aplikovaný alergén. Vzniká charakteristická zápalová indurácia, ktorá je na rozdiel od včasnej reakcie aj bolestivá [16].
U potravín väčšina autorov uprednostňuje natívne potraviny pred používaním komerčne dostupných alergénových extraktov. Pri použití natívnej potraviny ide o metódu tzv. „prick-by-prick“ (prick na prick test), čiže jeden „prick“ do skúmanej čerstvej potraviny a druhý „prick“ do kože pacienta [2, 17]. Výhodou je možnosť následného použitia tej istej potraviny aj pri orálnom expozičnom teste a lepšia porovnateľnosť výsledkoch oboch testov. Viacerí autori dokázali, že sledovanie zmien kožných reakcií pri SPT a koncentrácií sIgE v sére sú u malých detí s alergiou na bielkoviny kravského mlieka (ABKM) vhodným prognostickým ukazovateľom rozvoja tolerancie [14]. Vo vybraných prípadoch môžu definované prahové hodnoty pre sIgE protilátky v sére alebo pre priemer vzniknutej kožnej reakcie u SPT znížiť potrebu až nahradiť orálne expozičné testy [5, 18]. Vo všeobecnosti však treba považovať aj toto vyšetrenie za pomocné. Pozitivita poukazuje na možný podozrivý potravinový článok, avšak negatívny výsledok, vzhľadom na zložitosť metabolických procesov pri trávení, nie je dostatočnou príčinou na vylúčenie danej potraviny z radu „podozrivých“ [4, 17]. SPT možno používať bez ohľadu na vek, hoci u malých detí môže byť pre nespoluprácu niekedy náročné tieto kožné testy realizovať. Navyše, ak u dieťaťa pozorujeme ťažký priebeh ekzému, nemožno prerušiť liečbu antihistaminikami, čo je nevyhnutné pre získanie výsledkov s výpovednou hodnotou.
Epikutánne atopické patch testy (APT):
Ide o ďalší druh kožných testov, ktoré radíme medzi štandardizované diagnostické metódy PA (spolu s kožnými prick testami) pre všetky vekové kategórie (obzvlášť u malých detí). Na rozdiel od klasických epikutánnych testov (využívaných predovšetkým v dermatológii a pracovnom lekárstve), pri ktorých používame alergény vo forme hapténov (kovy, chemikálie, kozmetické prísady), pri APT aplikujeme pomocou testovacích setov na kožu intaktné proteínové alergény (potravinové, inhalačné) [19, 20].
Princípom APT je epikutánna aplikácia potravinových alebo inhalačných alergénov vyvolávajúcich kožnú reakciu s jej zhodnotením po 24 až 72 hodinách. Štandardizovaný protokol pre APT testovanie bol vypracovaný European Task Force on Atopic Dermatitis. Sety sa aplikujú na zdravú kožu hornej časti chrbta bez predchádzajúcej chemickej či fyzikálnej prípravy testovacieho miesta. Používajú sa testovacie komôrky Finn Chambers s priemerom 12 mm umiestnené na hypoalergénnej náplasti. Čas naloženia je 48 hodín a odpoveď sa odčítava 20 minút od začiatku testovania, 20 minút po zložení setu a definitívny výsledok hodnotíme po 72 hodinách od začiatku testovania. Ako alergény možno použiť tak čerstvé potraviny, ako aj štandardizované testovacie vazelínové zmesi, ktoré sú však pomerne zle dostupné na trhu [20, 21]. Ako pozitívnu odpoveď hodnotíme prítomnosť erytému s palpovateľnou infiltráciou alebo vezikulami v mieste kontaktu kože s alergénom. Diagnostika IgE mediovaných reakcií PA je pomerne jednoduchá kombináciou sIgE, SPT a OET, avšak ak ide o reakcie celulárnej imunity, prípadne kombinovanú etiológiu, môže byť diagnostika pomocou týchto metód pomerne zložitá. Nové možnosti ponúka práve APT testovanie [22]. Pri paralelnom testovaní SPT + APT je signifikantne vyššia pravdepodobnosť záchytu alergie na bielkoviny kravského mlieka ako aj iných PA, ako pri použití buď jedného alebo len druhého testu [19, 23, 24]. Z výsledkov štúdií vyplýva, že oba testy, APT aj SPT, sú napomocné v diagnostickom algoritme PA, pretože pri jej patofyziologickej podstate sa predpokladajú viaceré imunologické mechanizmy [13, 19], avšak nie je nevyhnutné kombinovať naraz všetky tri testy (APT, SPT, sIgE) [13].
Eliminačné diéty (dechallenge):
Eliminačná diéta môže byť užitočná u pacientov s perzistenciou príznakov. Na základe potravinových denníkov a laboratórnych vyšetrení (kožné prick testy, epikutánne atopické patch testy, špecifické potravinové protilátky z triedy IgE) možno pacientovi odporučiť eliminačnú diétu s vylúčením suspektnej potraviny zo stravy. Následne zhodnotením klinického obrazu s odstupom času možno na základe zlepšenia až vymiznutia klinických príznakov PA označiť výsledok eliminačnej diéty/testu za pozitívny (veľká pravdepodobnosť, že jedinec je na danú potravinu alergický) alebo negatívny (nedošlo ku zlepšeniu klinického obrazu po vylúčení podozrivej potraviny zo stravy) [25]. Diéta v dĺžke 2 až 3 týždne obyčajne stačí na potvrdenie suspektnej PA.
Eliminačná diéta vždy predchádza orálny záťažový test (v dĺžke minimálne 7–14 dní; v prípade niektorých ochorení GIT až 12 týždňov). Ak sa príznaky znovu objavia po reintrodukcii daného jedla do stravy, je nevyhnutné vykonať dvojito slepý, placebom kontrolovaný orálny záťažový test [13, 26].
Orálne expozičné (záťažové) testy (OET):
Predstavujú najcennejšiu metódu pre diagnostiku PA, pričom rozoznávame tri základné druhy týchto testov: otvorený slúži na priame potvrdenie/vylúčenie konkrétnej potraviny, pričom pacient aj lekár vedia, aká potravina sa podáva a placebo sa nepoužíva; jednoducho slepý je výhodný najmä na potvrdenie objektívnych príznakov, pričom pacient nevie, ale lekár vie, čo je placebo a čo je testovaný potravinový alergén, a dvojito slepý je vhodný na objektivizáciu subjektívnych symptómov, pričom ani pacient, ani lekár nevedia, čo je placebo a čo je testovaná potravina [27].
OET sa prevádzajú na jednej strane s cieľom dokázať, že za klinické ťažkosti jedinca je zodpovedný ten ktorý potravinový alergén a na druhej strane za účelom vylúčenia PA, aby sa pacient vyhol zbytočným, niekedy dokonca škodlivým eliminačným diétam. Tieto testy sú spomedzi všetkých možností na diagnostikovanie PA najcennejšie, avšak sú časovo náročné, pre pacientov problematické a nesú isté riziko ťažkých anafylaktických reakcií. Ak sú OET prevádzané pod vedením skúseného lekára na primerane vybavenom pracovisku, je riziko, ktoré so sebou toto testovanie nesie, prijateľné [17, 28]. OET by sa vždy mali vykonávať za kontrolovaných podmienok.
V dnešnej dobe sa za zlatý štandard v diagnostike PA považuje dvojito slepý, placebom kontrolovaný, orálny záťažový test (double-blind, placebo controlled, oral food challenge, DBPCOFCh) [29, 30] podľa štandardizovaných protokolov [13, 23]. U detí mladších ako jeden rok bez prejavov atopickej dermatitídy môžeme použiť aj otvorený expozičný test (v klinickom obraze PA sú dominantné objektívne príznaky), v ostatných prípadoch je nevyhnutné použiť spomenutý DBPCOFCh [5]. Otvorený a jednoducho slepý OET môže byť použitý na skríning podozrivých alergénov, ale pozitívny výsledok musí byť (s výnimkou malých detí alebo monovalentnej PA) potvrdený DBPCOFCh [8]. Otvorený OET je možné použiť aj v prípadoch niektorých ochorení GIT (enteropatií s malabsorbciou), kedy je na diagnózu nevyhnutné zhodnotenie bioptickej vzorky z čreva z období pred a po OET [8]. Na základe výsledkov tohto testu možno následne pacientovi odporučiť príslušnú špecifickú eliminačnú diétu a vyhnúť sa tak zbytočným polyvalentným diétam a zhoršovaniu klinického obrazu v prípade, že nebola inými metódami odhalená kauzálna potravina. Pri DBPCOFCh musí byť jedlo podávané vo forme, v akej ho pacient normálne konzumuje (napr. pražené arašidy), alebo vo svojej najalergénnejšej forme (surové vajce) [13]. Podávané potraviny majú zmenenú konzistenciu a upravenú chuť, aby ich pacient nemohol spoznať. Potraviny sa zomelú a podávajú sa silno ochladené, čím sa potlačí ich charakteristická chuť a vôňa a pacient ich konzumuje v rovnakej forme (podávané v rozpustnom škrobovom obale). Navyše potraviny sú v tejto forme označené číslami, čiže ani zdravotnícky personál nevie, akú potravinu pacient dostal (tým sa minimalizuje neobjektívne posúdenie klinickej reakcie).
Prognóza PA je vo všeobecnosti dobrá a u väčšiny detí sa časom vyvinie tolerancia na danú potravinu, a preto by sa OET mali pravidelne opakovať (s cieľom čo najskôr ukončiť eliminačnú diétu, ak už nie je indikovaná). Pre ABKM a alergiu na slepačie vajcia je medzi testami interval asi 12–18 mesiacov, naopak, u arašidov a ostatných druhov orechov, kedy sa s vývinom tolerancie stretávame zriedkavejšie, majú väčší zmysel dlhšie medzitestové intervaly [5]. Kontraindikáciou pre realizáciu OET je pozitivita kožných testov s jednoznačnou, jasnou anamnézou ťažkej anafylaktickej reakcie, ktorá nasledovala po ingescii špecifickej potraviny [28].
C. Doplňujúce a perspektívne testy pre diagnostiku PA
(obr. 5)
Obr. 5. Doplňujúce a perspektívne testy pre diagnostiku potravinovej alergie. 
Stanovenie špecifických protilátok z triedy IgG:
Viacerými autormi sú tieto parametre deklarované ako diagnostický prostriedok na určenie PA, ale na druhej strane je známy fakt, že je normálne vytvárať IgG alebo IgG4 proti bežne konzumovaným potravinám bez klinických prejavov alergickej reakcie ako následok expozície [9]. Podľa v súčasnosti dostupných údajov v literatúre nemá stanovenie špecifických IgG proti potravinovým alergénom svoje miesto v diagnostickom algoritme PA, okrem vzácneho Heinerovho syndrómu (potravinami indukovaná pľúcna hemosideróza) [31, 32].
Stručne možno zhrnúť, že vyšetrenie špecifických IgG alebo IgG4 neprináša pri diagnostike PA sprostredkovanej IgE žiadne doplňujúce informácie a je zbytočné. Istú úlohu by mohlo toto vyšetrenie hrať aj pri manažmente colon iritabile, ale sú potrebné ešte mnohé klinické štúdie, kým sa objasní rola, ktorú pri tomto ochorení hrajú špecifické IgG a IgG4 [5].
Test aktivácie bazofilov (basophil activation test, BAT) a test degranulácie bazofilov (cellular allergen stimulation test, CAST) in vitro:
Tento test je stále v štádiu experimentálneho použitia a skúmania jeho validity pri diagnostike PA. Ide o vyšetrenie slúžiace na stanovenie senzibilizácie sprostredkovanej sIgE. Pri tomto teste in vitro inkubujeme malú vzorku heparinizovanej krvi alebo separovaných krvných leukocytov s extraktom podozrivého potravinového alergénu. Ak sú prítomné sIgE proti použitým alergénom na povrchu bazofilov, do supernatantu bude uvoľnený histamín (a niektoré sulfidopeptidové leukotriény), čo môžeme kvantifikovať indexom reaktivity (test degranulácie bazofilov). Ak dochádza k aktivácii bazofilov počas inkubácie týchto buniek v zmesi s alergénom, pomocou prietokovej cytometrie môžeme následne stanoviť zvýšenú expresiu diferenciačného znaku CD63 na povrchu buniek (výsledkom testu je percento bazofilov, ktoré boli pri kontakte s alergénom aktivované, a preto majú na povrchu znak CD63, test aktivácie bazofilov) [11].
Tento test má podľa niektorých autorov porovnateľný výsledok s vyšetrením sIgE, podľa niektorých sa vyznačuje dokonca vyššou citlivosťou ako stanovenie cirkulujúcich sIgE. Predpokladá sa, že tento test by mohol byť v blízkej budúcnosti zaradený medzi štandardizované testy pri diagnostike PA a doplniť tak škálu týchto metód najmä u detí a pacientov s komplikovaným stavom [33, 34]. Dodnes bol úspešne použitý na diagnostiku alergie na zeler, ryby, arašidy a iné druhy orechov [11].
Bioptické vyšetrenie sliznice GIT:
Endoskopické biopsie hornej a dolnej časti tráviaceho traktu predstavujú dôležitú diagnostickú metódu pri niektorých syndrómoch potravinovej alergie, ako sú eozinofilná ezofagitída a gastritída, potravinovými proteínmi indukovaná enteropatia alebo proktokolitída, pričom biopsie by mali byť prevádzané pred kortikoidnou liečbou alebo nasadením eliminačnej diéty. Endoskopické vyšetrenie s biopsiou je dôležité aj pri diferenciálnej diagnóze PA, napr. pri vylúčení celiakie alebo Hirschsprungovej choroby [35].
Laktulózo-manitolový a iné testy vyšetrenia črevnej permeability:
Tieto testy sa zameriavajú na zhodnotenie črevnej intergrity, ktorá býva porušená najmä pri potravinovej alergii spojenej s enteropatiou a malabsorbciou. Opäť nejde o test špecifický pre PA, môže však poukázať na porušenie črevnej steny, ktoré býva pri prebiehajúcej PA časté. Výhodou je neinvazívnosť, časová nenáročnosť a možnosť opakovania testovania [36].
Rôzne markery alergického zápalu:
Eozinofilový proteín X (marker aktivácie eozinofilov) (•) [37, 39] a eozinofilový kationický proteín v stolici (•) [40, 38], tryptáza (marker aktivácie mastocytov) v stolici (•) [39], α1-antitrypsín v stolici (•) [38], leukotrién E4 v moči (•) [39], eotaxín v sére (‚) [39], tumor-nekrotizujúci faktor-α v stolici (•) [38], IgE v stolici (•), histamín v sére a metylhistamín v moči (•) – ako moderné markery potvrdzujúce aktiváciu zápalových buniek, alebo prítomnosť zápalu v sliznici GIT pri PA [38, 39]. Mnohé z nich by sa mohli stať v blízkej budúcnosti napomocnými pri diagnostike PA, najmä u pacientov s gastrointestinálnymi príznakmi.
D. Testy neštandardizované, alternatívne, obsolentné [5, 6, 13, 32]
(obr. 6)
Obr. 6. Testy štandardizované, alternatívne a obsolentné. 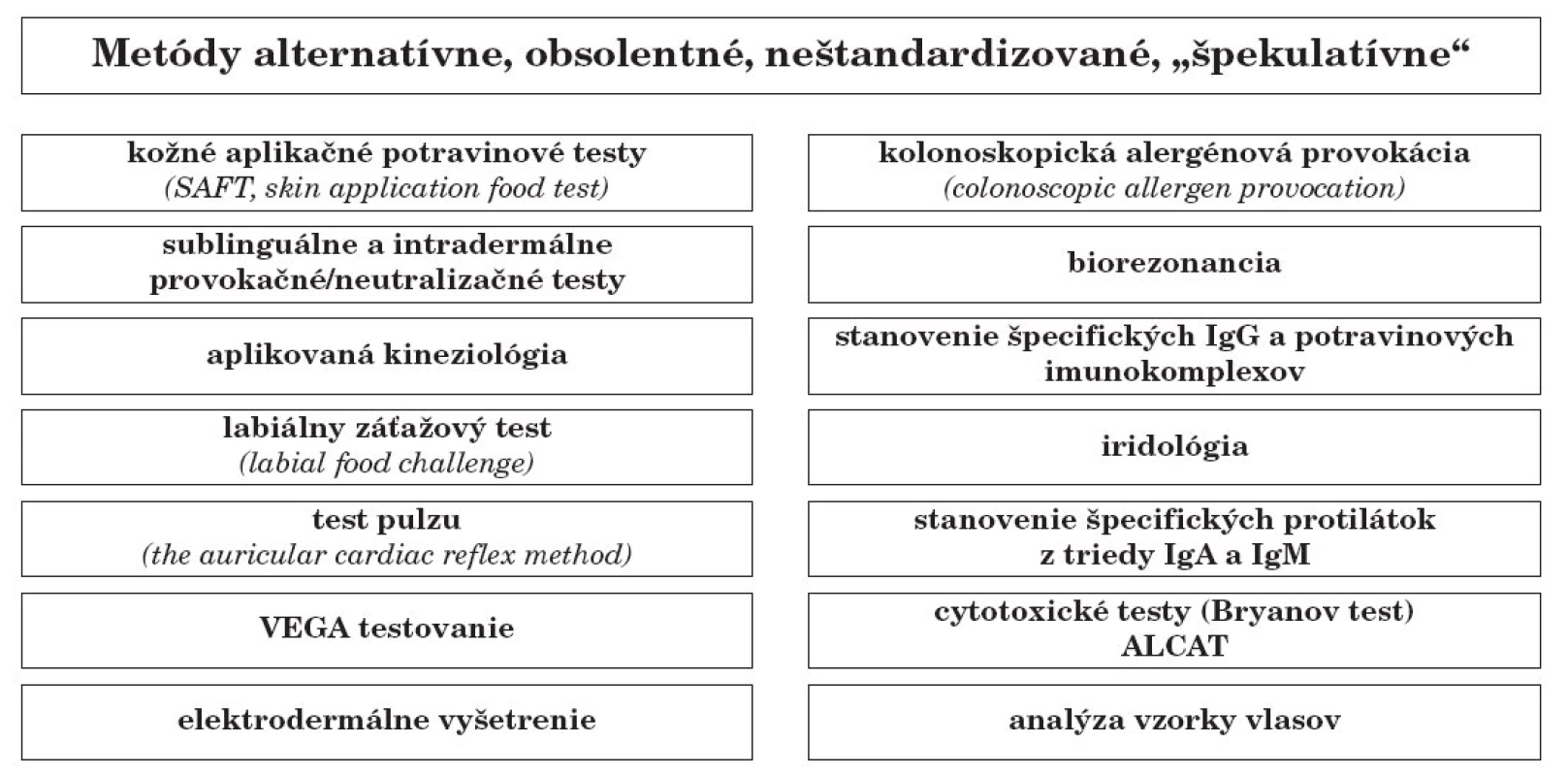
Do tejto skupiny možno zaradiť tieto vyšetrenia a testy, ktoré na základe publikovaných štúdií nemožno odporúčať pre diagnostiku PA:
kožné aplikačné potravinové testy (skin application food test); labiálny záťažový test (labial food challenge); sublinguálne a intradermálne provokačné/neutralizačné testy; intrakutánny progresívny dilučný multipotravinový test (intracutaneous progressive dilution multi-food test); vyšetrenie imunokomplexov s potravinovými alergénmi (Food Immune Complex Assays); aplikovaná kineziológia; cytotoxické testy (Bryanov test); elektrodermálne vyšetrenie; kolonoskopická alergénová provokácia (colonoscopic allergen provocation, endoskopický záťažový test); test pulzu (The auricular cardiac reflex method); testy proliferácie lymfocytov a uvoľnovania cytokínov po stimulácii potravinovým alergénom v podmienkach in vitro (Leukotriene LTC4 release, CAST); test inhibície migrácie lymfocytov; stanovenie diferenciačného znaku CD23 na povrchu lymfocytov; stanovenie špecifických protilátok z triedy IgA a IgM; expresia špecifických aktivačných molekúl (gp53) na povrchu bazofilov; produkcia IL-2 alebo inhibičných faktorov leukocytov; biorezonancia; VEGA testovanie; iridológia a analýza vzorky vlasov.
Záver
Aj napriek viacerým dostupným a prepracovaným diagnostickým metódam a testom, diagnostika potravinovej alergie naďalej predstavuje komplikovanú kapitolu detskej imunoalergológie, keďže jednotlivé metódy majú limitovanú hodnotu vzhľadom na potvrdenie alebo vylúčenie potravinovej alergie. Aj napriek množstvu rôznych vyšetrovacích metód a testov, „zlatým štandardom“ v diagnostike PA je dvojito zaslepený, placebom kontrolovaný, orálny záťažový test (v spojení s predchádzajúcou eliminačnou diétou). Všetky ostatné štandardizované metódy (kožné testy, vyšetrenie specifických IgE) považujeme len za metódy pomocné. Popri skupine štandardizovaných testov poznáme mnohé metódy (z ktorých sú viaceré dnes už obsolentné), ktoré ešte nemajú definované miesto v diagnostických postupoch potravinovej alergie a ktorých klinická výpovedná hodnota ostáva nejasná. U niektorých z nich však môžeme predpokladať, že sa v blízkej budúcnosti stanú nápomocnými popri dnes štandardne používaných metódach in vivo alebo in vitro a dopomôžu k skorej a presnejšej diagnostike potravinovej alergie v detskom veku.
Diagnostika a liečba potravinovej alergie patrí výsostne do rúk skúseného odborníka (detský gastroenterológ v spolupráci s imunoalergológom a dermatológom), ktorý má rozsiahle skúsenosti s interpretáciou výsledkov jednotlivých vyšetrovacích metód, na základe ktorých môže potom indikovať terapeutickú diétu, resp. iné liečebné postupy. Vzhľadom na potenciálne negatívny vplyv elemininačnej diéty (najmä polyvalentnej) na vyvíjajúci sa detský organizmus je potrebné čo najskôr, pomocou jednotlivých vyšetrovacích metód, odhaliť kauzálnu potravinu (ev. potraviny), čím sa počet eliminovaných potravín zmenší na minimum. Opakovaním jednotlivých vyšetrení v príslušných intervaloch možno následne pozorovať ev. neskorší nástup tolerancie na danú potravinu, čo vedie k ukončeniu eliminačnej diéty, ktorá už nie je indikovaná.
Došlo: 18. 12. 2007
Přijato: 4. 2. 2008
MUDr. Miloš Jeseňák, PhD.
Klinika detí a dorastu UK JLF a MFN
Kollárova 2
036 59 Martin
Slovenská republika
e-mail: jesenak@gmail.com
Redakční poznámka: Kontrolní otázky k tomuto článku jsou uveřejněny na vložené příloze v tomto čísle.
Zdroje
1. Johansson SGO, Bieber T, Dahl R, et al. Revised nomenclature for allergy for global use: Report of the Nomenclature Review Committee of the World Allergy Organization. J. Allergy Clin. Immunol. 2004;113 : 832–836.
2. Kayserová H. Potravinové alergie. Interná Medicína 2003;3 : 299–303.
3. Kristjansson I, Ardal B, Jonsson JS, et al. Adverse reactions to food and food allergy in young children in Iceland and Sweden. Scand. J. Prim. Health Care 1997;17 : 30–34.
4. Fuchs M. Potravinové alergie. Pediatrie po promoci 2004;1 : 26–35.
5. Beyer K, Teuber SS. Food allergy diagnostics: scientific and unproven procedures. Curr. Opin. Allergy Clin. Immunol. 2005;5 : 261–266.
6. Niggemann B, Grüber C. Unproven diagnostic procedures in IgE-mediated allergic diseases. Allergy 2004;59 : 806–808.
7. Ortolani C. Food allergies and food intolerances. Best Practice & Research Clinical Gastroenterology 2006;20 : 467–483.
8. Sampson HA. Update on food allergy. J. Allergy Clin. Immunol. 2004;113 : 805–819.
9. Bahna SL. Diagnosis of food allergy. Ann. Allergy Asthma Immunol. 2003;90(Suppl 3): 77–80.
10. Jakušová Ľ. Klinické príznaky alergie na bielkoviny kravského mlieka. Pediatria (Bratisl.). 2006;1 : 285–288.
11. Bartůňková J, Paulík M, Hölzerová J, et al. Vyšetřovací metody v imunologii. 1. vyd. Praha: Grada Publishing, 2005 : 1–176.
12. Celik-Bilgili S, Mehl A, Verstege A, et al. The predictive value of specific IgE levels in serum for the outcome of oral food challenges. Clin. Exp. Allergy 2005;35 : 268–273.
13. Niggemann B, Beyer K. Diagnostic pitfalls in food allergy in children. Allergy 2004;60 : 104–107.
14. Vanto T, Helppila S, Juntunen-Backman K, et al. Prediction of the development of tolerance to milk in allergy with cow´s milk hypersensitivity. J. Pediatr. 2004;144 : 218–222.
15. Beyer K. Characterization of allergenic food proteins for improved diagnostic methods. Curr. Opin. Allergy Clin. Immunol. 2003;3 : 189–197.
16. Hill DJ, Heine RG, Hosking CS. The diagnostic value of skin prick testing in children with food allergy. Pediatr. Allergy Immunol. 2004;15 : 435–441.
17. Niggemann B, Beyer K. Diagnosis of food allergy in children: toward a standardization of food challenge. J. Pediatr. Gastroenterol. Nutr. 2007;45 : 399–404.
18. Roehr CC, Reibel S, Ziegert M, et al. Atopy patch tests, together with determination of specific IgE levels, reduce the need for oral food challenges in children with atopic dermatitis. J. Allergy Clin. Immunol. 2001;107 : 548–553.
19. Niggemann B. Evolving role of the atopy patch test in the diagnosis of food allergy. Curr. Opin. Allergy Clin. Immunol. 2002;2 : 253–256.
20. Turjanmaa K, Darsow U, Niggemann B, et al. EAACI/GA2LEN Position paper: Present status of the atopy patch test. Allergy 2006;61 : 1377–1384.
21. Jeseňák M, Bánovčin P. Atopy patch test in the diagnosis of food allergy in children with atopic dermatitis. Acta Medica (Hradec Králové) 2006;49 : 199–201.
22. Spergel JM, Brown-Whitehorn T. The use of patch testing in the diagnosis of food allergy. Curr. Allergy Asthma Rep. 2005;5 : 86–90.
23. Isoulari E, Turjanmaa K. Combined skin prick and patch testing enhances identification of food allergy in infants with atopic dermatitis. J. Allergy Clin. Immunol. 1996;97 : 9–15.
24. Majamaa H, Moisio P, Holm K, et al. Cow’s milk allergy: diagnostic accurancy of skin prick and patch tests and specific IgE. Allergy 1999;54 : 346–351.
25. Bindslev-Jensen C. ABC of allergies: Food allergy. BMJ 1998;316 : 1299–1302.
26. Hegyi E, Hegyi V, Kolibášová K. Neznášanlivosť potravín. Slovenský Lek. 1998;22 : 34–38.
27. Bock SA. Diagnostic evaluation. Pediatrics 2003;111 : 1638–1644.
28. Perry TT, Matsui EC, Kay Conover-Walker M, et al. Risk of oral food challenges. J. Allergy Clin. Immunol. 2004;114 : 1164–1168.
29. Niggemann B, Rolinck-Werninghaus C, Mehl A, et al. Controlled oral food challenges in children: when indicated, when superfluous? Allergy 2005;60 : 865–870.
30. Sicherer SH. Food allergy: when and how to perform oral food challenges. Pediatr. Allergy Immunol. 1999;10 : 226–234.
31. Jeseňák M, Bánovčin P, Buchanec J. Heinerov syndróm (pľúcna hemosideróza indukovaná alergiou na bielkoviny kravského mlieka). Čes.-slov. Pediat. 2006;61 : 207–212.
32. Teuber SS, Porch-Curren C. Unproven diagnostic and therapeutic approaches to food allergy and intolerance. Curr. Opin. Allergy Clin. Immunol. 2003;3 : 217–221.
33. Honzová S, Havranová M, Daňková E, et al. Může test aktivace bazofilů pomoci při podezření na senzibilizaci na potravinové alergeny u dětí? (Naše první zkušenosti). Klin. Imunol. Alergol. 2003;13 : 14–15.
34. Sampson HA. In vitro diagnosis and mediator assays for food allergies. Allergy. Proc. 1993;14 : 259–261.
35. Allen KJ, Hill DJ, Heine RG. Food allergy. MJA 2006;185 : 394–400.
36. Jakušová Ľ, Bánovčin P, Schudichová J, et al. Využitie testu črevnej permeability v diagnostike alergie na bielkoviny kravského mlieka. In: Mikler J., Jurko A. Aktuality v pediatrii. Martin: Jesseniova lekárska fakulta UK Martin, 2000 : 61–64.
37. Lochman I, Lochmanová A, Kloudová A, et al. Úskalí laboratórní diagnostiky potravinových intolerancií a alergií. Klin. Imunol. Alergol. 1999;9 : 46.
38. Majamaa H, Miettinen A, Laine S, et al. Intestinal inflammation in children with atopic eczema: faecal eosinophil cationic protein and tumour necrosis factor-α as non-invasive indicators of food allergy. Clin. Exp. Allergy 1996;26 : 181–187.
39. Van Odijk J, Peterson CGB, Ahlstedt S, et al. Measurements of eosinophil activation before and after food callenges in adults with food hypersensitivity. Int. Arch. Allergy Immunol. 2006;140 : 334–341.
40. Bengtsson U, Knutson TW, Knutson L, et al. Eosinophil cationic protein and histamine after intestinal challenge in patients with cow’s milk intolerance. J. Allergy Clin. Immunol. 1997;100 : 216–221.
41. Sabbah A, Sainte-Laudy J, Drouet M, et al. Immunobiologic diagnosis of food allergy. Allerg. Immunol. (Paris) 1997;29 : 103–107.
Štítky
Neonatológia Pediatria Praktické lekárstvo pre deti a dorast
Článok vyšiel v časopiseČesko-slovenská pediatrie
Najčítanejšie tento týždeň
2008 Číslo 5- fSCIG v reálnej klinickej praxi u pacientov s hematologickými malignitami
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Facilitovaná subkutánna imunoglobulínová terapia u seniorov s imunodeficienciami v reálnej praxi
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
-
Všetky články tohto čísla
- O citáciách, impakte a o našom časopise
- Črevné duplikatúry v detskom veku
- Cholelitiáza u novorodencov – bežný nález
- Praktické aspekty 24hodinového ambulantního monitorování krevního tlaku
- Zmeny autonómneho nervového systému pri poruchách príjmu potravy (mentálna anorexia)
- Diagnostický algoritmus potravinovej alergie v detskom veku
- Doporučené terapeutické postupy k biologické léčbě IBD infliximabem
- Dny dětské endokrinologie 2008
- VIII. ČESKÝ PEDIATRICKÝ KONGRES S MEZINÁRODNÍ ÚČASTÍ
- Česko-slovenská pediatrie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Praktické aspekty 24hodinového ambulantního monitorování krevního tlaku
- Diagnostický algoritmus potravinovej alergie v detskom veku
- Zmeny autonómneho nervového systému pri poruchách príjmu potravy (mentálna anorexia)
- Cholelitiáza u novorodencov – bežný nález
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



