-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Hodnocení profylaktických opatření po expozici biologickému materiálu
Evaluation of prophylactic precautions after exposure to biological materials
Objectives:
Study of transmission rates of hepatitis B virus (HBV), hepatitis C virus (HCV), and human immunodeficiency virus (HIV) and effect of HBV vaccination after parenteral exposure to biological materials.Patients and Methods:
This was a retrospective study of 879 individuals (419 health care professionals and 460 persons from the general population) after blood and body fluid exposure examined at the Clinic of Infectious Diseases in Ostrava from 1999 to 2013. HBsAg, anti-HBs, anti-HBc, anti-HCV, anti-HIV, bilirubin, and ALT were tested in exposed patients and known sources at the baseline and, except anti-HBc, after 3, 6, and 12 months. Susceptible persons were vaccinated against HBV and screened for anti-HBs after 1–2 months. Antiretroviral prophylaxis was provided if reasonable.Results:
At the baseline, 42 exposed persons were HBV positive, six were HCV positive, and none was HIV positive. During the follow-up, no new HBsAg positivity was detected in exposed individuals, although 25 of 837 susceptible persons were exposed to HBsAg-positive sources. After vaccination, protective anti-HBs were detected in 707 (84.7%) of 837 susceptible persons and in 709 (97.8%) of 725 persons with known post-vaccination response. Fifty-six of 873 persons had been exposed to HCV-positive sources and HCV transmission was shown in three (two health care professionals) of them. No HIV transmission was observed, although 11 of 879 individuals had been exposed to HIV-positive sources, with antiretroviral prophylaxis provided to nine of them.Conclusions:
Contemporary post-exposure prophylactic precautions in the Czech Republic can be considered as adequate for the prevention of HBV and HIV, but health care professionals in particular are at risk of HCV transmission.Keywords:
hepatitis B – hepatitis C – HIV – parenteral exposure - vaccination
Autoři: I. Orságová 1; L. Rožnovský 1; L. Petroušová 1; A. Zjevíková 1; M. Konečná 1; A. Kloudová 2; J. Mrázek 3; H. Zelená 4
Působiště autorů: Klinika infekčního lékařství, Fakultní nemocnice Ostrava 1; Odbor imunologie a alergologie, Zdravotní ústav se sídlem v Ostravě 2; Oddělení molekulární biologie, Zdravotní ústav se sídlem v Ostravě 3; Virologické oddělení, Zdravotní ústav se sídlem v Ostravě 4
Vyšlo v časopise: Epidemiol. Mikrobiol. Imunol. 63, 2014, č. 1, s. 50-55
Kategorie: Souhrnná sdělení, původní práce, kazuistiky
Souhrn
Cíl:
Sledování četnosti přenosu viru hepatitidy B, C (HBV, HCV), HIV a účinnosti vakcinace proti hepatitidě B (VHB) u osob s parenterální expozicí biologickému materiálu.Soubor pacientů a metody:
Na Klinice infekčního lékařství v Ostravě bylo v letech 1999–2013 vyšetřeno po parenterální expozici 879 osob, 419 zdravotníků a 460 osob z běžné populace. U exponovaných osob a známých zdrojů bylo v úvodu stanoveno HBsAg, anti-HBs, anti-HBc, anti-HCV, anti-HIV, bilirubin a ALT, shodná vyšetření kromě anti-HBc byla provedena u exponovaných osob za 3, 6 a 12 měsíců. Vnímavé osoby byly očkovány proti VHB s vyšetřením anti-HBs za 1 až 2 měsíce po vakcinaci. V odůvodněných případech byla poskytnuta HIV profylaxe.Výsledky:
V úvodu byla zjištěna předchozí infekce HBV u 42 osob, HCV u 6 osob, HIV infekce nebyla prokázána. Během sledování nebyla u 837 vnímavých osob zjištěna nová pozitivita HBsAg, přitom 25 osob bylo exponováno HBsAg pozitivnímu zdroji. Po vakcinaci byla prokázána ochranná hladina anti-HBs u 709 z 837 (84,7 %) vnímavých osob, případně 709 ze 725 (97,8 %) osob se známou odpovědí po očkování. Přenos HCV byl prokázán u 3 osob (2 zdravotníků), přitom anti-HCV pozitivnímu zdroji bylo exponováno 56 osob. Infekce HIV nebyla prokázána, přitom 11 osob bylo exponováno HIV pozitivnímu zdroji, profylaxe byla poskytnuta 9 z nich.Závěr:
Současná profylaktická opatření v České republice lze považovat za dostatečná v prevenci přenosu HBV a HIV, ale přenos HCV je rizikový především pro zdravotníky.Klíčová slova:
hepatitida B – hepatitida C – HIV – parenterální expozice – očkováníÚVOD
Při parenterální expozici, která zahrnuje např. poranění jehlou nebo ostrým nástrojem, kontaminaci rány nebo sliznic biologickým materiálem jiné osoby, může dojít k přenosu více než 20 různých patogenů, z nichž nejvýznamnější jsou viry hepatitidy B, C a HIV [1, 2]. Riziko přenosu HBV při HBeAg pozitivitě zdroje je přibližně 30% (19–62%), při HBeAg negativitě kolem 5 % (1–37 %). Vakcinace proti VHB snižuje četnost infekcí, zejména u zdravotníků [1–4]. Riziko přenosu u HCV je jen 1,8 % (0–7 %), u HIV 0,3 % (0,2–0,5 %) [1–3, 5–8]. Podle údajů Světové zdravotnické organizace je každoročně asi 10 % zdravotníků vystaveno patogenům šířeným krví, navíc jsou často vystaveni čerstvému biologickému materiálu [2]. Profesní riziko zdravotníků oproti běžné populaci je u HBV 9krát, u HCV 15krát a u HIV dokonce 82krát vyšší [9].
V ČR byly dříve hlášeny desítky případů profesionální VHB, dnes jsou infekce raritní díky vakcinaci, která byla u zdravotníků zahájena roku 1983. V současnosti je očkována většina zdravotníků, dětí a mladistvých do 23 let [7, 10–14].
Při expozici v běžné populaci ČR je riziko přenosu HBV, HCV a HIV malé vzhledem k nízké promořenosti populace. Navíc je biologický materiál často dekontaminován delším působením zevních fyzikálních podmínek. Podle sérologického přehledu z roku 2001 byla pozitivita HBsAg zjištěna u 0,56 % osob a anti-HCV u 0,2 % osob. K 31. 5. 2013 bylo v ČR hlášeno 2 339 HIV pozitivních, podíl HIV pozitivních narkomanů je u nás doposud nízký (5%) [5, 15].
Závazné předpisy pro postexpoziční profylaxi byly v ČR opakovaně novelizovány [7, 10–14, 16]. Od roku 1998 platila doporučení pro zdravotníky, kterým se kromě vakcinace často podával hyperimunní globulin proti hepatitidě B (HBIg) [16]. V roce 2001 byla opatření rozšířena o neprofesionální poranění, výrazně se omezilo užití HBIg a současně byla zavedena aktivní a pasivní imunizace proti hepatitidě A (VHA) [11]. V roce 2004 bylo upuštěno od pasivní imunizace proti VHA a v roce 2007 byla zrušena i vakcinace proti VHA [13, 14]. Profylaxe HIV infekce v ČR byla novelizována v roce 2012 [8].
V následujícím textu jsou uvedeny výsledky čtrnáctiletého sledování souboru 879 osob exponovaných biologickému materiálu.
SOUBOR PACIENTŮ A METODY
Na Klinice infekčního lékařství Fakultní nemocnice v Ostravě bylo v letech 1999–2013 vyšetřeno po parenterální expozici biologickému materiálu 879 osob, jednalo se o 419 zdravotníků (76 mužů a 343 žen) a 460 osob z běžné populace, tzv. nezdravotníků (274 mužů, 186 žen), přičemž dětí do 15 let bylo 138 (grafy 1 a 2, tab. 1). Celkem 17 osob (14 zdravotníků) bylo exponováno dvakrát, 3 osoby dokonce třikrát.
Graf 1. Věkové kategorie Figure 1. Age groups 
Graf 2. Počet vyšetřených v jednotlivých letech Figure 2. Number of examined patients in individual years 
Tab. 1. Profese exponovaných zdravotníků Table 1. Health care workers’ professions 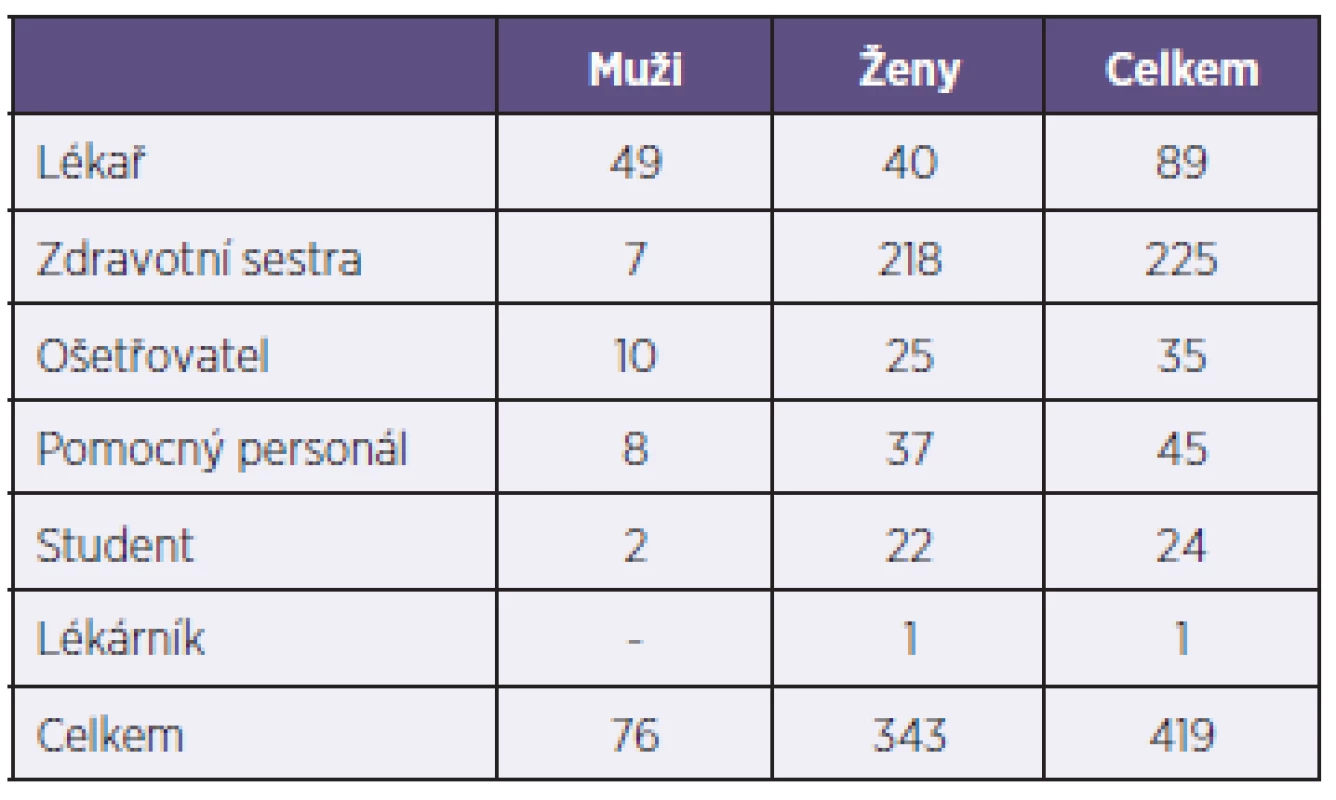
Exponované osoby byly sledovány 12 měsíců při respektování aktuálně platných doporučení v ČR [10–14, 16]. Úvodní vyšetření zahrnovalo stanovení HBsAg, anti-HBs, anti-HBc, anti-HCV, anti-HIV včetně antigenu p24, bilirubinu a ALT, shodné vyšetření (kromě anti-HBc) bylo provedeno za 3, 6 a 12 měsíců. U očkovaných proti VHB byly za 1–2 měsíce po vakcinaci (eventuálně i po 2. dávce vakcíny) vyšetřeny protilátky anti-HBs. U exponovaných HCV pozitivnímu zdroji byla vyšetřována virémie (HCV RNA) v úvodu, za 3 a 6 měsíců po poranění. U některých osob exponovaných HIV pozitivnímu zdroji byla vyšetřována i virémie (HIV RNA).
U známých zdrojů bylo provedeno jedno vyšetření HBsAg, anti-HCV a anti-HIV. HBsAg byl prokázán u 24 ze 70 (34 %) vyšetřených zdrojů, pozitivita anti-HCV u 56 z 93 (60 %) zdrojů a anti-HIV u 10 ze 40 (25 %) zdrojů.
Vakcinace proti VHB byla nabídnuta vnímavým osobám s negativitou HBsAg, anti-HBc a anti-HBs < 10 IU/ml. Aplikována byla vakcína Engerix B s obsahem 20 µg HBsAg (10 µg do 15 let). Po preexpoziční vakcinaci byly přeočkovány pouze osoby bez protilátek anti-HBs a zdravotníci exponovaní HBsAg pozitivnímu zdroji, u osob s neúplnou vakcinací bylo očkování dokončeno. Při postexpoziční vakcinaci bylo použito standardní schéma 0, 1 a 6 měsíců, revakcinace byla nabídnuta osobám bez protilátek anti-HBs po očkování. HBIg byl aplikován pouze u 4 neimunních zdravotníků.
Exponovaným HIV pozitivnímu zdroji byla nabídnuta profylaktická léčba 2–4 preparáty podle míry expozice na 4 týdny [6, 8].
V souboru byla hodnocena četnost klinicky významných infekcí. Přenos HBV byl definován pozitivitou HBsAg, infekce HCV pozitivitou anti-HCV, eventuálně HCV RNA, přenos HIV pozitivitou anti-HIV nebo antigenu p24. Účinnost vakcinace proti VHB byla definována zastoupením osob s ochrannou hladinou anti-HBs.
VÝSLEDKY
Virová hepatitida B
Pozitivita anti-HBc byla v úvodu prokázána u 42 z 879 exponovaných osob (4,7 %), současná HBsAg pozitivita byla zjištěna u 5 osob (0,6 %) – tabulka 2. Ze 42 infikovaných bylo 15 osob (14 zdravotníků) také preexpozičně očkováno proti VHB. Předchozí infekce nebyla prokázána u žádného ze 138 dětí do 15 let.
Tab. 2. Sérologické nálezy u 42 osob s předchozí infekcí HBV Table 2. Serological findings in 42 patients with previous HBV infection 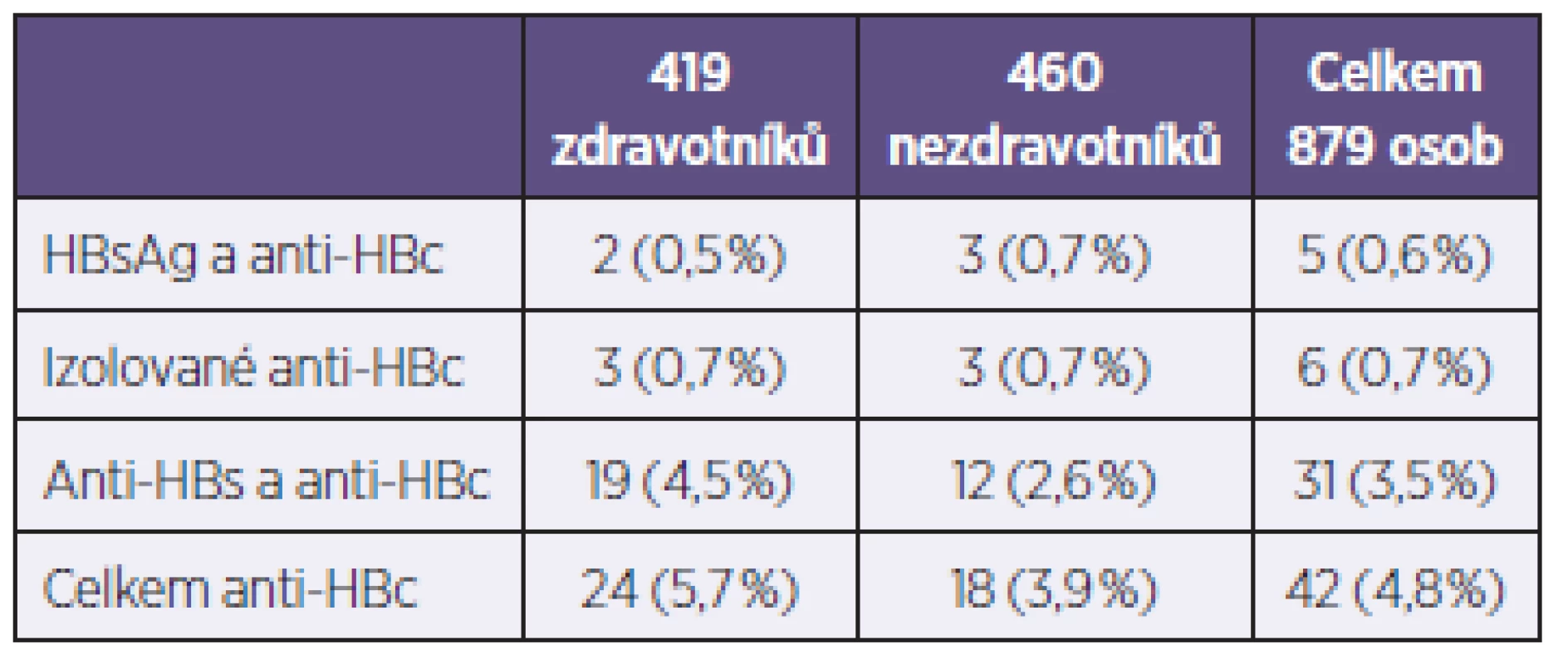
Bez předchozí infekce HBV bylo 837 z 879 exponovaných osob, u žádné nebyla v průběhu zaznamenána nová pozitivita HBsAg, přitom déle než půl roku (maximální inkubační doba VHB), bylo sledováno 557 osob. Ve vyšším riziku přenosu HBV bylo 396 osob bez ochranné hladiny anti-HBs v úvodu, déle než půl roku bylo sledováno 271 osob. V nejvyšším riziku bylo 25 osob exponovaných HBsAg pozitivnímu zdroji (1 zdroj exponoval 2 osoby), přitom 3 z nich měly pozitivitu anti-HBc. V podskupině 22 vnímavých osob bylo déle než půl roku sledováno 14 osob.
Vakcinace proti VHB
Soubor 837 vnímavých osob zahrnoval 518 osob s preexpoziční vakcinací VHB a 319 nevakcinovaných osob. Ochranná hladina anti-HBs byla v úvodu zjištěna pouze u osob s preexpoziční vakcinací, jednalo se o 441 z 518 (85,1 %) osob, přitom protilátky byly přítomny u 83 z 91 dětí (91,2 %) do 15 let, ale jen u 82 ze 108 osob (75,9 %) nad 40 let věku. Skupina 77 z 518 osob bez ochranné hladiny anti-HBs v úvodu zahrnovala 8 osob s neúplnou a 69 osob s úplnou vakcinací. Vakcinace byla dokončena u 6 osob, ochrannou hladinu anti-HBs vytvořilo 5 osob, z nichž 2 až po revakcinaci. Revakcinace byla provedena u 65 osob bez anti-HBs, ochrannou hladinu vytvořilo 47 z 59 (79,7 %) vyšetřených, z toho všech 7 dětí do 15 let, ale jen 15 z 21 osob nad 40 let. Druhá revakcinace byla provedena u 5 osob, u všech byla následně prokázána ochranná hladina anti-HBs.
V souboru 518 osob s preexpoziční vakcinací a revakcinací byla prokázána ochranná hladina anti-HBs u 498 osob (96,1 %), při vztažení k podskupině 506 osob se známou odpovědí po očkování dokonce u 98,4 % osob.
Postexpoziční vakcinace byla zahájena u 309 z 319 vnímavých osob, ukončena byla u 246 z nich, ochrannou hladinu anti-HBs vytvořilo 196 z 207 (94,7 %) vyšetřených (tab. 3). Jedna revakcinace byla provedena u 5 osob, z nichž 3 vytvořily ochrannou hladinu anti-HBs.
Tab. 3. Úplná postexpoziční vakcinace u 309 osob Table 3. Complete post-exposure vaccination in 309 persons 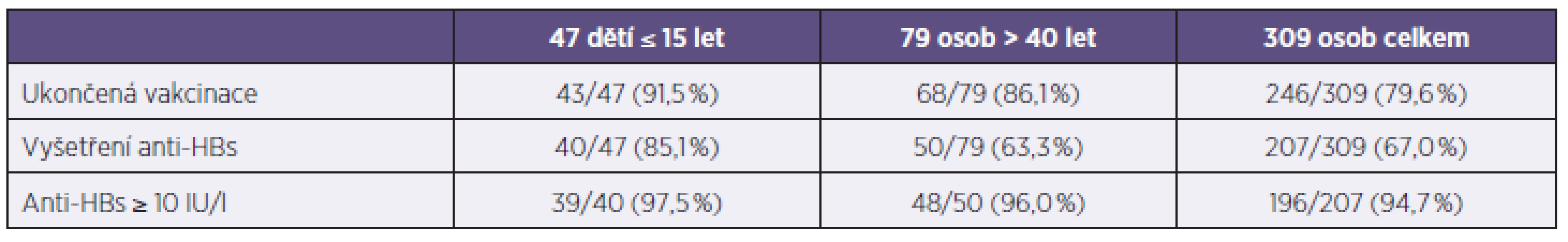
Po 2. dávce vakcíny vytvořilo ochrannou hladinu anti-HBs 70 ze 146 (47,9 %) vyšetřených osob, rozdíly v závislosti na věku uvádí tabulka 4.
Tab. 4. Postexpoziční vakcinace – anti-HBs po 2 dávkách vakcíny Table 4. Post-exposure vaccination – anti-HBs after 2 doses of vaccine 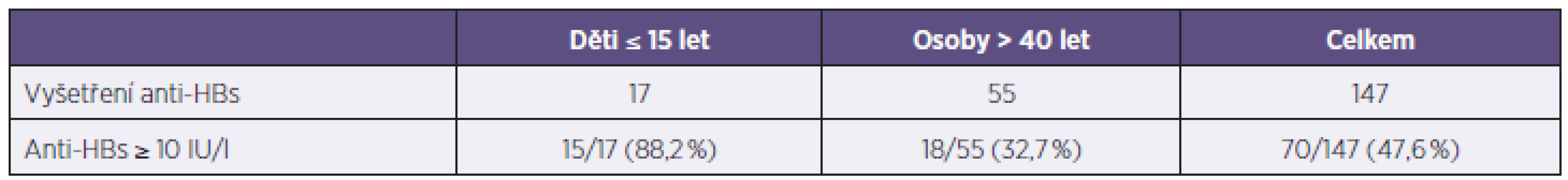
Ve skupině 319 osob s postexpoziční vakcinací byla prokázána ochranná hladina anti-HBs u 211 (66,1 %) osob, mezi které bylo zahrnuto i 12 nedoočkovaných osob, které měly ochrannou hladinu anti-HBs po 2. dávce vakcíny, při vztažení k 219 osobám se známou odpovědí po očkování to bylo 96,3 % osob.
V celém souboru 837 vnímavých osob byla prokázána ochranná hladina anti-HBs u 709 (84,7 %) osob, při vztažení k podskupině 725 osob se známou odpovědí po očkování to bylo 97,8 % osob.
Virová hepatitida C
V úvodu byla zjištěna pozitivita anti-HCV u 6 osob, a to u 3 ze 416 zdravotníků (0,7 %) a 3 ze 460 nezdravotníků (0,7 %) – tabulka 5. Pozitivní HCV RNA byla u jednoho ze dvou vyšetřených zdravotníků.
Tab. 5. Počty infikovaných v souboru 879 exponovaných osob Table 5. Number of infected patients in population of 879 exposed persons 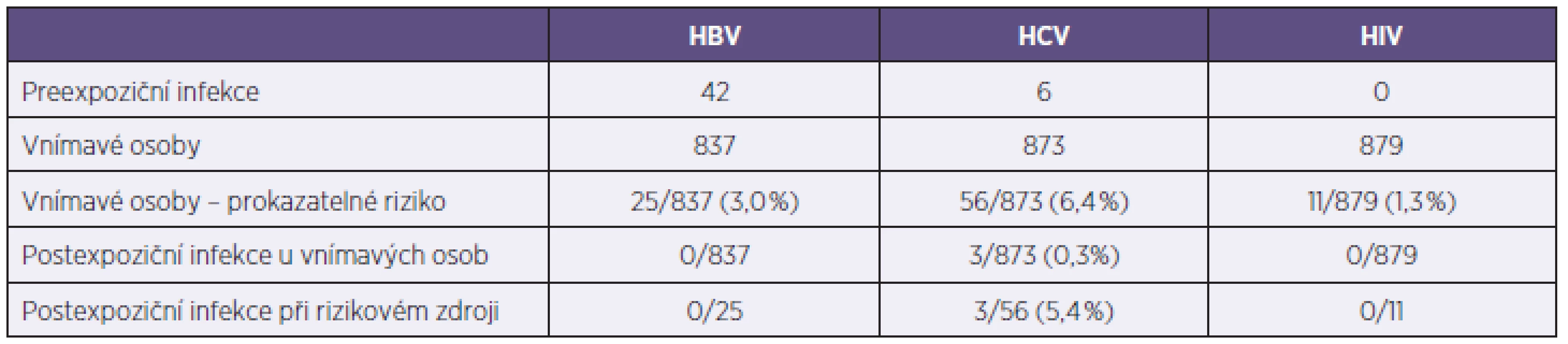
V souboru byla prokázána nově vzniklá anti-HCV pozitivita u 3 z 873 (0,3 %) dříve neinfikovaných osob (2 zdravotníci, 1 nezdravotník), déle než půl roku (nejdelší inkubační doba HCV) bylo sledováno 612 osob. Všichni 3 infikovaní (5,4 %) patřili do podskupiny 56 osob (43 zdravotníků) exponovaných anti-HCV pozitivnímu zdroji, v uvedené skupině s prokazatelným rizikem bylo déle než půl roku sledováno 36 osob. Pozitivita HCV RNA byla prokázána u 6 z 9 vyšetřených zdrojů, genotyp nebyl vyšetřen. Údaje o infikovaných osobách jsou uvedeny v tabulce 6.
Tab. 6. Pacienti s hepatitidou C Table 6. Patients with hepatitis C 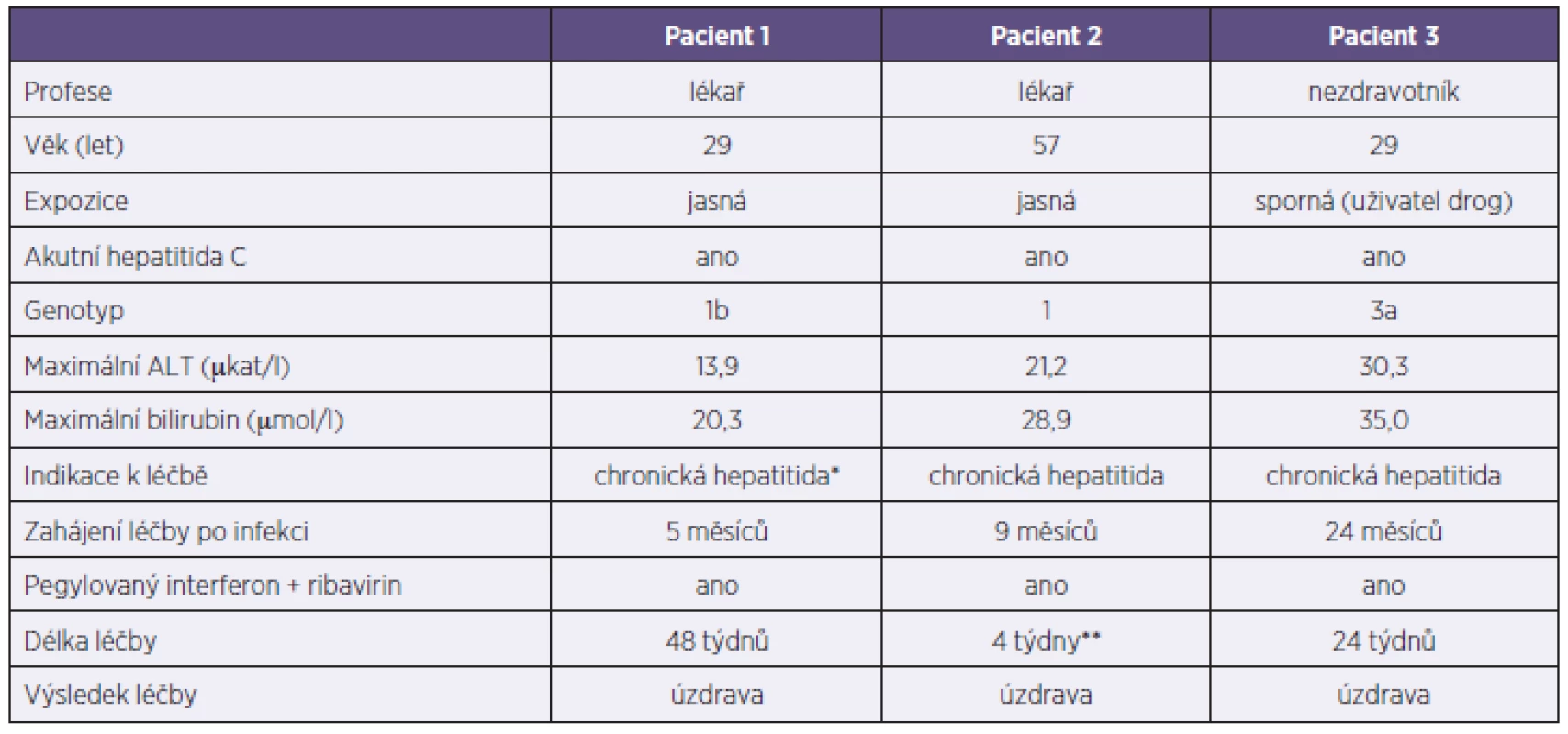
* vzestup virémie ve 4. měsíci infekce ** léčba předčasně ukončena pro závažné nežádoucí účinky HIV infekce
V celém souboru 879 osob nedošlo k přenosu HIV, přitom 586 z nich bylo sledováno déle než půl roku. Celkem 11 osob (9 zdravotníků) bylo exponováno HIV-pozitivnímu zdroji (1 zdroj exponoval 2 osoby), v této rizikové skupině bylo 6 osob sledováno déle než půl roku. Profylaxe s podáním 2-4 antivirotik byla poskytnuta 9 exponovaným osobám, 2 osoby ji odmítly. Vyšetření HIV RNA bylo provedeno u 3 exponovaných za 1 měsíc, u 4. osoby po 6 měsících, výsledek byl vždy negativní.
DISKUSE
V našem souboru 879 osob exponovaných biologickému materiálu nebyla prokázána infekce HBV a HIV, ale 3 osoby se infikovaly HCV. Rovněž i naše výsledky potvrzují, že samotná aktivní imunizace proti VHB je vysoce účinná a omezení indikace HBIg po roce 2000 bylo racionální [11, 16]. V našem souboru byla potvrzena vysoká účinnost vakcinace proti VHB ve všech věkových skupinách. Pouze u osob nad 40 let ve srovnání s dětmi byla prokázána nižší účinnost revakcinace a nižší tvorba protilátek anti-HBs po aplikaci 2. dávky vakcíny, ale počty vyšetřených osob byly relativně malé [19].
S vakcinací proti VHB souvisel i pokles profesních infekcí, do roku 2000 bylo v ČR očkováno přes 100 000 zdravotníků, v letech 1996–2007 onemocnělo VHB 239 osob, v roce 2011 dvě osoby, v roce 2012 jediná [4, 17, 18]. V našem souboru byla zjištěna u zdravotníků i nezdravotníků obdobná prevalence HBsAg (0,5 % vs. 0,7 %) a anti-HBc (5,7 % vs. 3,9 %), což je analogické jako v sérologickém přehledu z roku 2001 [5].
V našem souboru bylo vyšetřeno relativně málo zdrojů, ale současně bylo prokázáno vysoké zastoupení rizikových zdrojů s pozitivitou HBsAg u 34 % a anti-HCV u 60 % zdrojů. Tyto údaje neodpovídají četnosti výskytu virů v populaci, ale spíše ukazují, že vyšetření vyhledávají zejména zdravotníci exponovaní rizikovým zdrojům.
Vzhledem k nedostupnosti vakcinace zůstává VHC z hlediska profylaxe nejproblematičtější. V letech 1996–2007 v ČR onemocnělo VHC 122 zdravotníků, počty hlášených onemocnění kolísaly mezi 5–14 případy ročně, v letech 2011 a 2012 bylo hlášeno onemocnění vždy jen 1 zdravotníka. Závažné je, že 86 % infekcí bylo diagnostikováno až v chronickém stadiu a 16 % zdravotníků bylo mladších než 30 let, což zvyšuje riziko následného rozvoje jaterní cirhózy nebo hepatocelulárního karcinomu [17, 18]. Snižující se četnost profesních VHC pravděpodobně souvisí se zlepšením osobní ochrany zdravotníků, ale i s podhlášeností asymptomatické akutní infekce. Vyšší riziko expozice přetrvává v chirurgických oborech a na hemodialýzách [22].
V našem souboru byla zjištěna shodná prevalence anti-HCV (konfirmované reaktivity) u zdravotníků i nezdravotníků (vždy 0,7 %), což je vyšší než v sérologickém přehledu z roku 2001 (0,2 %) [5]. Námi zjištěná prevalence asi více odpovídá reálnému výskytu anti-HCV v populaci, protože do sérologických přehledů nejsou zařazovány osoby s rizikovým chováním.
V našem souboru byla prokázána HCV infekce u 3 z 56 osob (5,4 %) exponovaných anti-HCV pozitivnímu zdroji, což odpovídá literárním údajům o riziku přenosu HCV od viremického zdroje v 0–7 % [3, 22]. V současnosti není po expozici doporučena profylaktická protivirová léčba VHC, hlavně pro její časté nežádoucí účinky, rovněž názory na léčbu akutní VHC vysokými dávkami interferonu alfa nejsou jednotné, zejména pro možnost spontánního vyloučení viru u 15–25 % infikovaných [2, 3, 20-22]. Po expozici anti-HCV pozitivnímu zdroji může časné vyšetření HCV RNA urychlit průkaz infekce. U infikovaných osob považujeme za vhodné sledovat vývoj virémie, její pokles v prvních měsících upozorňuje na spontánní vyloučení viru, naopak trvající virémie nebo její vzestup signalizuje přechod do chronicity s možností zahájit standardní protivirovou léčbu chronické VHC, což bylo použito u jednoho našeho pacienta.
Profylaxe HIV se zahajuje ideálně do 4 hodin, maximálně do 48 hodin po expozici, podle rizika se užívají 2–4 preparáty, většinou tenofovir s emtricitabinem, eventuálně zidovudin s lamivudinem a lopinavir s ritonavirem [8]. Sérokonverze u infikovaných bývají detekovány do 6–12 týdnů, u většiny osob do 6 měsíců, vzácně po delší době, a proto se doporučuje roční sledování exponovaných osob [6]. Vyšetřování antigenu p24, který se objevuje u infikovaných do 2–3 týdnů, může zkrátit dobu průkazu infekce. U zdravotníků jsou HIV infekce vzácné, např. v letech 1985–2001 bylo v USA hlášeno 57 potvrzených a 138 možných profesionálních nákaz [2, 6]. V našem souboru bylo exponováno prokazatelně HIV pozitivnímu zdroji pouze 11 osob, proto není překvapivé, že infekce nebyla prokázána. Počet HIV pozitivních je v ČR zatím nízký, liší se v jednotlivých regionech, vyšší riziko je především v Praze s centralizací HIV pozitivních osob. Přesto i v dalších regionech lze výhledově počítat s častějším užíváním HIV profylaxe u exponovaných osob.
ZÁVĚR
Současná profylaktická opatření po parenterální expozici biologickému materiálu v ČR lze považovat za dostatečná v prevenci přenosu HBV a HIV. Přenos HCV při absenci očkování představuje určité riziko především pro zdravotníky.
Do redakce došlo dne 30. 8. 2013.
Adresa pro korespondenci:
MUDr. Irena Orságová
Klinika infekčního lékařství FN Ostrava
17. listopadu 1790
708 52 Ostrava
e-mail: irena.orsagova@fno.cz
Zdroje
1. Moloughney BW. Transmission and postexposure management of bloodborne virus infections in the health care setting: Where are we now? CMAJ, 2001;165(4):445–451.
2. Center for Disease Control and Prevention. Updated U.S. Public Health Service Guidelines for the Management of Occupational Exposures to HBV, HCV, and HIV and Recommendations for Postexposure Prophylaxis. 2001;50(RR11):1–42.
3. Varghese GM et al. Post-exposure prohylaxis for blood borne viral infections in healthcare workers. Postgrad Med J, 2003;79 : 324–328.
4. Částková J, Beneš Č. Vývoj nemocnosti virovou hepatitidou B u zdravotnických pracovníků v České republice. České pracov lék, 2001;2(2):75–78.
5. Němeček V. Sérologický přehled ČR v roce 2001 – virová hepatitida A, B, C. Zprávy CEM, 2003;12(příloha 1):55-61.
6. Landovitz RJ. Occupational and Nonoccupational Postexposure Prophylaxis for HIV in 2009. Top HIV Med, 2009;361(18): 104–108.
7. Halířová R. Rizika poranění zdravotníků ostrým předmětem. Interní medicína pro praktické lékaře, 2004;1 : 53-54.
8. Rozsypal H, Staňková M, Sedláček D, Snopková S, et al. Doporučený postup péče o dospělé infikované HIV a postexpoziční profylaxe HIV, listopad 2012. Dostupné na www: http://www.infekce.cz/DoporART12.htm.
9. Wicker S, Cinatl J, Berger A, Doerr HW, et al. Determination of risk of infection with blood-borne pathogens following a needlestick injury in hospital workers. Ann Occup Hyg, 2008;52(7):615–622.
10. Vyhláška Ministerstva zdravotnictví ze dne 29. ledna 1991, o očkování proti přenosným nemocem. Sbírka zákonů, 1991, č. 48.
11. Metodický návod č. 12/2000 Prevence virové hepatitidy typu A (HA), typu B (HB), typu C (HC), typu D (HD) a typu E (HE). Věstník MZ ČR, 2000, částka 12, s. 3–4.
12. Vyhláška Ministerstva zdravotnictví ze dne 6. prosince 2000, o očkování proti infekčním nemocem. Sbírka zákonů, 2000, č. 439, částka 121, s. 5788–5792.
13. Vyhláška Ministerstva zdravotnictví č. 439/2000 Sb., o očkování proti infekčním nemocem, ve znění vyhlášky č. 478/2002 Sb. a vyhlášky č. 30/2004 Sb., s. 2–3.
14. Vyhláška Ministerstva zdravotnictví ze dne 29. listopadu 2006, o očkování proti infekčním nemocem. Sbírka zákonů, 2006, č. 537, částka 174, s. 7282–7287.
15. Petráš P. Nové případy HIV infekce v České republice podle regionu. Údaje ke dni 31. 5. 2013. Zprávy CEM, 2013;22 : 188–190.
16. Metodický návod č. 11/1998 Prevence virového zánětu jater typu A (HA), typu B (HB), typu C (HC), typu D (HD) a typu E (HE). Věstník MZ ČR, 1998, částka 8, s. 22–38.
17. Fenclová Z, Urban P, Pelcová D, Voříšková M, et al. Profesionální onemocnění hlášená v České republice v roce 2012. Prakt lék, 2013;93(3):93–99.
18. Fenclová Z, Urban P, Pelcová D, Šuvarinová N. Zdravotníci a nemoci z povolání v České republice, Medicína pro praxi, 2009;6(2):69–71.
19. Chlíbek R, Smetana J, Boštíková V, Špliňo M. Očkování proti virové hepatitidě A a B u dospělých starších 40 let věku – sledování přetrvávání protilátek a imunitní odpovědi. Epidemiol Mikrobiol Imunol, 2011;60(3):99–108.
20. Urbánek P, Husa P, Galský J, Šperl J. Standardní diagnostický a terapeutický postup chronické infekce virem hepatitidy C (HCV), leden 2012. Gastroent Hepatol, 2013;67(2):95–97.
21. Deterding K, Grüner N, Buggisch P, Wiegand J at al. Delayed versus immediate treatment for patients with acute hepatitis C: A randomised controlled non-inferiority trial. Lancet Infect Dis, 2013;13(6):497–506.
22. Hoffmann C, Buchholz L, Schnitzler P. Reduction of needlestick injuries in healthcare personnel at a university hospital using safety devices. J Occup Med Toxicol, 2013;29(8): 20. doi: 10.1186/1745-6673-8-20.
Štítky
Hygiena a epidemiológia Infekčné lekárstvo Mikrobiológia
Článok vyšiel v časopiseEpidemiologie, mikrobiologie, imunologie
Najčítanejšie tento týždeň
2014 Číslo 1- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Očkování proti virové hemoragické horečce Ebola experimentální vakcínou rVSVDG-ZEBOV-GP
- Koronavirus hýbe světem: Víte jak se chránit a jak postupovat v případě podezření?
-
Všetky články tohto čísla
- Chřipka v sezonách 2009-2013 ve Fakultní nemocnici Hradec Králové, východní Čechy
- Bakterie komplexu Burkholderia cepacia – epidemiologie a diagnostika infekcí u pacientů s cystickou fibrózou
- Epidemiologické faktory ovlivňující vznik rekurentní a těžké infekce Clostridium difficile
- Úvodník
- Výsledky genotypizace, laboratorní diagnostika a epidemiologie viru příušnic cirkulujícího v České republice v roce 2012
- Klinické a epidemiologické charakteristiky pacientů hospitalizovaných pro těžký průběh chřipky v sezoně 2012–2013
- Legionelové infekce – opomíjený problém
- Hodnocení profylaktických opatření po expozici biologickému materiálu
- Epidemiologické šetření v pěti ambulancích Kliniky zubního lékařství LF UP v Olomouci a FN Olomouc
- Sekvenační analýza antigenů zařazených v čtyřkomponentní vakcíně proti meningokoku B v českých izolátech Neisseria meningitidis v období 2007–2013
- Epidemiologie kmenů Cronobacter spp. izolovaných z hospitalizovaných pacientů FN Olomouc (Česká republika)
-
Biologické a chemické zbrane
Pripravenosť a odpoveď - Významné životné jubileum RNDr. Ing. Josefa Janoška
- Zemřel prof. MUDr. Vladislav Potužník, DrSc. (*6. 1. 1924–†9. 12. 2013)
- Zemřel MUDr. Vladimír Plesník (*6. 11. 1931–†4. 2. 2014)
- Epidemiologie, mikrobiologie, imunologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Legionelové infekce – opomíjený problém
- Bakterie komplexu Burkholderia cepacia – epidemiologie a diagnostika infekcí u pacientů s cystickou fibrózou
- Epidemiologické šetření v pěti ambulancích Kliniky zubního lékařství LF UP v Olomouci a FN Olomouc
- Klinické a epidemiologické charakteristiky pacientů hospitalizovaných pro těžký průběh chřipky v sezoně 2012–2013
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



