-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Chronická pankreatitida ve stáří
Chronic pancreatitis in the old age
Chronic pancreatitis (ChP) is a progressive inflammatory process, characterized by successive fibrotization of the gland. The incidence of chronic pancreatitis in the Czech Republic is almost at 8 new cases/100 000 inhabitants/year. The genesis of chronic pancreatitis after sixty years of age is rare, in most cases the disease begins in earlier life periods. The aetiology factors of ChP are summarized in the TIGAR-O classification. The most common cause of chronic pancreatitis is alcoholism. In the case of late onset of the disease in elderly people it is necessary to think of biliary or autoimmune aetiology, but often the aetiology remains unclear. The abdominal pain is frequent in younger people, but it may not dominate in older patients if sensitive neural terminals are destroyed. The main signs of pancreatic insufficiency are malabsorption and malnutrition, in advanced stages diabetes mellitus tends to develop as well. Routine laboratory examination shows little sensitivity and specificity in ChP. The most important role in diagnostics is played by imaging techniques (computed tomography and nuclear magnetic resonance imaging). Besides conservative treatment, the newer invasive procedures, or in some indicated cases surgery, are available as well.
Keywords:
chronic pancreatitis – TIGAR-O classification – steatorrhoea – malnutrition – pancreatine
Autori: M. Berková; Z. Berka; E. Topinková
Vyšlo v časopise: Geriatrie a Gerontologie 2015, 4, č. 2: 81-86
Kategória: Přehledové články
Súhrn
Chronická pankreatitida (ChP) je progresivní zánětlivé onemocnění slinivky břišní, charakterizované postupnou fibrotizací žlázy. Incidence chronické pankreatitidy v České republice představuje téměř 8 nových případů/100 000 obyvatel/rok. Vznik chronické pankreatitidy po šedesátém roce života není častý, většinou se setkáváme s chorobou, která začala již v dřívějších životních údobích. Klasifikace TIGAR-O třídí formy ChP podle etiologie. Nejčastější příčinou rozvoje ChP je alkoholismus. U seniorů s pozdním vznikem choroby je třeba pomýšlet i na biliární či autoimunitní etiologii, nezřídka však zůstává příčina neobjasněná. Abdominální bolest je častá u mladších osob, ale nemusí dominovat při destrukci senzitivních nervových zakončení u starších pacientů. Hlavními příznaky insuficience pankreatu je malabsorpce a malnutrice, v pokročilých stadiích i rozvoj diabetes mellitus. Běžné laboratorní vyšetření je v praxi většinou málo senzitivní a málo specifické. Dominantní postavení v diagnostice zaujímají zobrazovací metody (počítačová tomografie, nukleární magnetická rezonance). V terapii se kromě konzervativních postupů nabízí řešení novějšími invazivními postupy a v některých případech i léčba chirurgická.
Klíčová slova:
chronická pankreatitida – klasifikace TIGAR-O – steatorea – malnutrice – pankreatinDefinice, Incidence
Chronická pankreatitida (ChP) je progresivní zánětlivé onemocnění slinivky břišní, charakterizované postupnou náhradou funkčního parenchymu vazivovou tkání. Nedostatečná exokrinní funkce pankreatu ústí v maldigesci, malabsorpci a malnutrici. V pokročilých stadiích může být postižena i endokrinní funkce se vznikem diabetes mellitus. Chronická pankreatitida snižuje kvalitu života a je rizikovým faktorem vzniku karcinomu pankreatu. Hlavní klinické a morfologické znaky chronické pankreatitidy shrnuje tabulka 1.Incidence chronické pankreatitidy pomalu, ale jistě stoupá. V České republice činí výskyt nově diagnostikovaných případů bezmála 8 na 100 000 oby-vatel/rok. Přestože je alkohol jedním z nejrizikovějších faktorů vzniku ChP, nejvyšší incidence chronické pankreatitidy v Evropě byla zjištěna ve Finsku (23 případů/100 000 oby-vatel/rok), které je známo přísnou kontrolou prodeje alkoholických nápojů(1). Chronická pankreatitida je diagnostikovaná průměrně ve věku 58 let a více než polovinu tvoří muži(2). Nově vzniklá chronická pankreatitida ve věku nad 60 let je poměrně vzácná. Ve starším věku vidíme většinou pokročilý stupeň onemocnění, které začalo již v mládí nebo ve středním věku.
Tab. 1. Klinické a morfologické znaky chronické pankreatitidy 
Etiologie
Etiologie chronické pankreatitidy je rozmanitá a shrnuje ji klasifikace TIGAR-O (tab. 2). Pokud chronická pankreatitida vzniká nově v seniorském věku, je nutno uvažovat o biliární a autoimunitní etiologii. Často však zůstává etiologie neznámá.
Tab. 2. Klasifikace chronické pankreatitidy 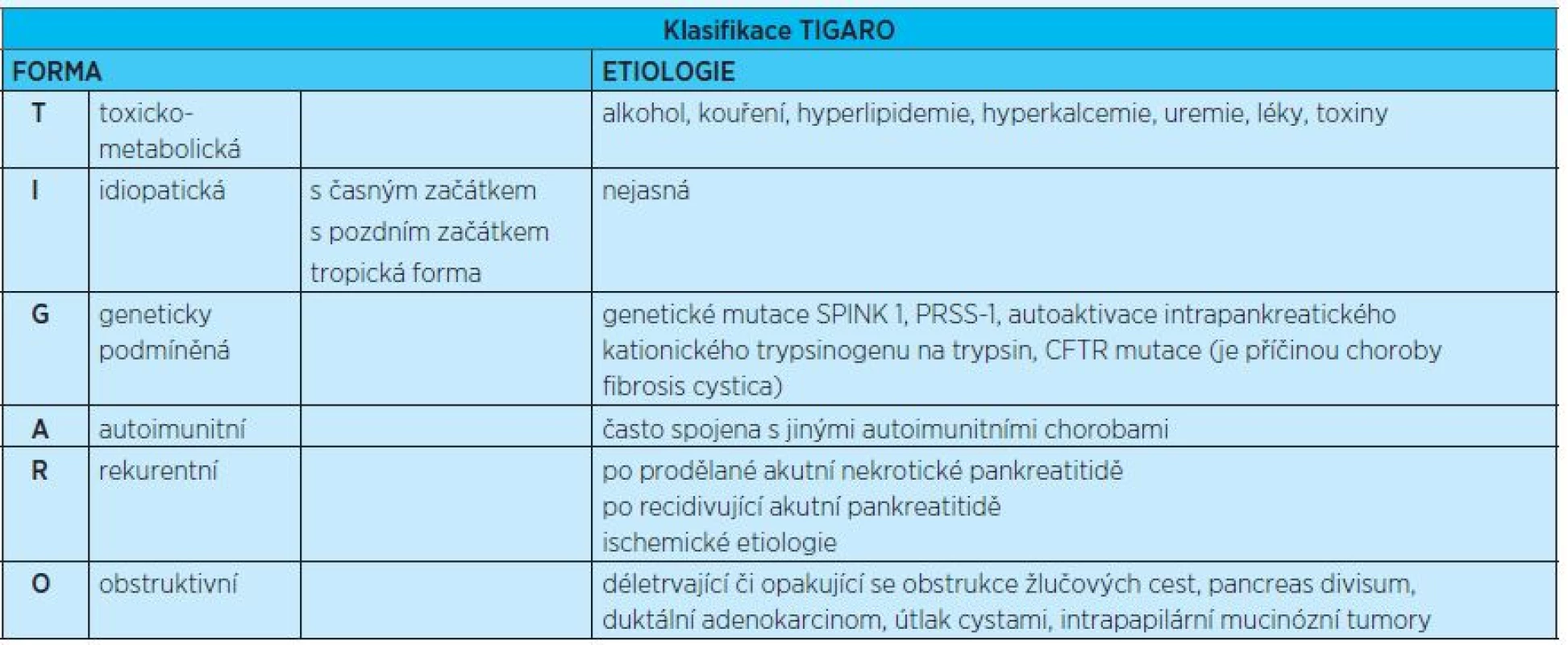
Patogeneze
Ke vzniku chronické pankreatitidy vede primární poškození slinivky známou noxou či neznámým etiologickým činitelem s následnou zánětlivou odpovědí. Uvolněné cytokiny modulují funkční aktivitu na zánětu participujících buněk, zejména leukocytů, které ve větší či menší míře infiltrují postiženou tkáň. Do místa poškození migrují aktivované stelární (hvězdicovité) buňky, zodpovědné za fibroprodukci a náhradu poškozeného parenchymu nefunkčním vazivem. Rozsah, forma a intenzita zánětu se liší podle vyvolávajícího faktoru.
Chronická alkoholická pankreatitida
Alkohol je nejčastější příčinou (více než 75 % všech případů) chronické pankreatitidy. Přesto se ChP vyvine pouze u 3 % osob nadměrně holdujících alkoholu. Musí tedy současně působit ještě další faktory, které potencují účinek alkoholu. K nim se přičítá zejména kouření, u kterého bylo prokázáno, že je nezávislým rizikovým faktorem rozvoje ChP. Předpokládá se několik mechanismů, kterými alkohol poškozuje pankreatický parenchym:
- Přímý toxický vliv alkoholu. Alkohol je metabolizován v acinárních buňkách pankreatu oxidační a neoxidační cestou. Při neoxidačním odbourávání etanolu vznikají ethylestery mastných kyselin, které se mohou akumulovat v pankreatických buňkách a vyvolat jejich tukovou degeneraci a nekrózu.
- Oxidační stres. Při abúzu alkoholu je zvýšená aktivita jaterních oxidáz, které se podílejí na odbourávání toxinů. Vedlejším produktem jejich činnosti je tvorba kyslíkových a peroxidových radikálů, které poškozují buněčné membrány, organely, zejména mitochondrie a jejich funkci.
- Proteinové zátky a mikrolitiáza. Nadměrná konzumace alkoholu vede k hypersekreci hyperkoncentrované (supersaturované) pankreatické šťávy s nedostatkem litostatinu (bílkovina produkovaná acinárními buňkami pankreatu) a citrátu, které za fyziologických okolností zabraňují precipitaci pankreatické šťávy. To vede k vysrážení bílkovin a tvorbě tzv. bílkovinných zátek, do kterých se ukládají vápenaté soli. Obstrukce drobných pankreatických vývodů proteinovými zátkami a mikrolitiázou vede k duktální hypertenzi s poškozením epitelu pankreatických vývodných cest.
- Postnekrotické změny. Chronické poškození parenchymu slinivky břišní vzniká po opakovaných atakách akutní alkoholické pankreatitidy.
Popsané mechanismy vedou ke zničení parenchymu slinivky břišní s typickými morfologickými změnami (tab. 1).
Idiopatické formy chronické pankreatitidy
Idiopatické formy představují ChP, u které se její příčinu nepodařilo prokázat. Tvoří asi 10 % všech ChP. Často se jedná o alkoholickou etiologii ChP, kde se nám nepodařilo abúzus alkoholu odhalit. Do kategorie idiopatické ChP se zařazuje i tropická pankreatitida (chronická kalcifikující nealkoholická pankreatitida). Poprvé byla popsána v Indonésii v roce 1959 a poté v dalších rozvojových částech světa (Indie, Afrika, Jižní Amerika). Její etiologii přesně neznáme, ale víme, že se vyvíjí obvykle na pozadí chudoby a malnutrice. Dává se do souvislosti s nedostatkem některých stopových prvků nebo s přítomností toxinů ve stravě. Tyto rizikové faktory působí pravděpodobně v geneticky predisponovaném terénu. Onemocnění je 3x častější u mužů než u žen; vyvíjí se od mládí a většinou se projeví do 40 let věku bolestmi břicha, maldigescí a hubnutím. V pokročilém stadiu při rozvinutí diabetu se označuje jako fibrokalkulózní pankreatický diabetes (FCPD)(3). Patologicko-anatomicky je charakteristická progresivní fibróza se zmenšením objemu žlázy, kalcifikacemi a dilatací pankreatických vývodů.
Geneticky podmíněné chronické pankreatitidy
Jsou poměrně vzácné (1–5 % ze všech případů ChP). Jsou spojeny s nejvyšším výskytem karcinomu pankreatu. Vznikají v důsledku těchto genových mutací:
- mutace genu, který kóduje protein, tzv. transmembránový regulátor vodivosti (cystic fibrosis transmembrane conductance regulator; zkratka CFTR)
- mutace genu kódujícího serinovou proteázu – kationický trypsinogen (zkratka PRSS-1)
- mutace genu pro proteázový inhibitor SPINK-1 (nemutovaná funkční forma zabraňuje autoaktivaci trypsinogenu v pankreatické tkáni).
Typ dědičnosti genů podmiňujících hereditární pankreatitidu ukazuje tabulka 3.
Tab. 3. Dědičnost hereditárně podmíněných typů chronické pankreatitidy 
Gen pro CFTR je asociován s multiorgánovým onemocněním – cystickou fibrózou (nazývanou též mukoviscidóza)(4). Při tomto onemocnění vázne transport chloridových iontů na apikálních membránách epiteliálních buněk exokrinních žláz. To vede k zahuštění jejich sekretu. Postiženy jsou v různé míře všechny žlázy s vnější sekrecí. Charakteristický je zvýšeně slaný pot. Nejzávažnější bývá postižení plic a pankreatu. Vazký hlen v průduškách snižuje pohyb řasinek bronchiálního epitelu a usnadňuje uchycení infekce. Vývodné cesty žlučové a pankreatické bývají obturovány zahuštěnou žlučí a pankreatickými šťávami. Rozvíjí se chronická pankreatitida s fibrotickou přestavbou a tvorbou cyst. Choroba vede k terminální respirační insuficienci. Vzhledem ke zlepšené péči o pacienty s cystickou fibrózou není toto onemocnění již jen diagnózou dětského věku, ale jedna třetina postižených se dožívá dospělosti a délka života se prodlužuje.
Přítomnost mutovaných genů pro PRSS-1 a SPINK-1 umožňuje intraacinární autoaktivaci trypsinogenu na aktivní trypsin, který destruuje pankreatickou tkáň. Tvoří se mikroskopické ložiskové nekrózy s následnou reparativní fibrózou. Mutace genu PRSS-1 s sebou nese největší riziko rakoviny slinivky břišní, které je 50–60krát vyšší než u ostatních typů chronické pankreatitidy(5).
Autoimunitní forma chronické pankreatitidy
Tvoří asi 5 % ze všech chronických pankreatitid. Vzniká postižením pankreatické tkáně zánětem na autoimunitním podkladě. Rozlišujeme 2 typy chronické autoimunitní pankreatitidy:
1. typ
Vyskytuje se spíše v Asii u starších mužů ve věku mezi 60–70 lety(6). Patří do skupiny autoimunitních onemocnění, pro která je společným znakem zvýšená hladina IgG4 (patří sem také retroperitoneální fibróza, sklerozující cholangoitida a sialoadenitida)(7). V pankreatické tkáni se hromadí periduktálně a v pokročilejších fázích i intralobulárně množství lymfoplazmatických buněk, které produkují imunoglobuliny typu IgG4(8). Tyto protilátky jsou však prokazatelné jen asi u 50 % pacientů s autoimunitní ChP 1. typu(9). Kromě zvýšených hladin IgG4 bývají přítomny protilátky proti plazminogen vázajícímu proteinu (PBP – plasminogen-binding protein), který je součástí bakteriální buňky Helicobacter pylori. Anti-BPB protilátka, namířená primárně proti bakteriální komponentě, působí u predisponovaných jedinců vzhledem k podobnosti molekul jako protilátka proti vlastní tkáni(10). Pozitivní bývá také řada dalších protilátek, které uvádí tabulka 4. Vývodné pankreatické cesty jsou utlačovány zánětlivou infiltrací a zmnoženým vazivem. Epitel vývodných cest zůstává obvykle intaktní. Zánětlivá infiltrace a fibróza postihuje také retroperitoneum.
Tab. 4. Imunologické vyšetření protilátek při podezření na autoimunitní formu chronické pankreatitidy 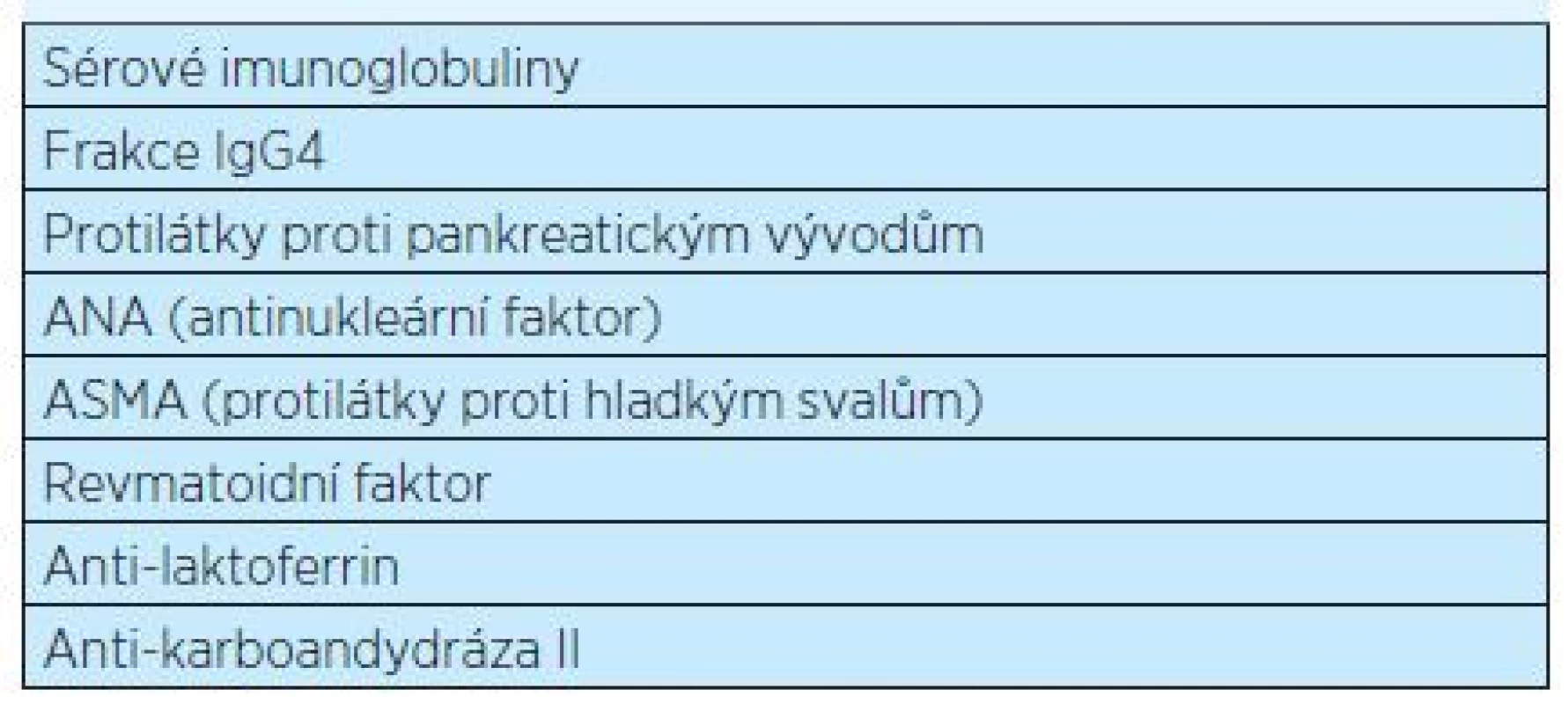
2. typ
Bývá často diagnostikován v koincidenci s Crohnovou chorobou nebo ulcerózní kolitidou(11,12). Postihuje mladší osoby, průměrně ve věku 40–48 let. Nejcharakterističtějšími znaky, kterými se 2. typ odlišuje od 1. typu autoimunitní ChP, jsou intra - a periduktální infiltrace neutrofily(12), epiteliální léze vývodných pankreatických cest a mikroabscesy. Vnitřní povrch hlavního pankreatického vývodu je nerovný, s typickými strikturami a poststenotickými dilatacemi(13). Fibrotizace nedosahuje takové míry jako u typu 1(14). Pro autoimunitní formu není typická tvorba cyst a pseudocyst. Rozdíly mezi oběma typy autoimunitní ChP shrnuje tabulka 5.
Tab. 5. Diferenciální diagnostika 1. a 2. typu chronické autoimunitní pankreatitidy 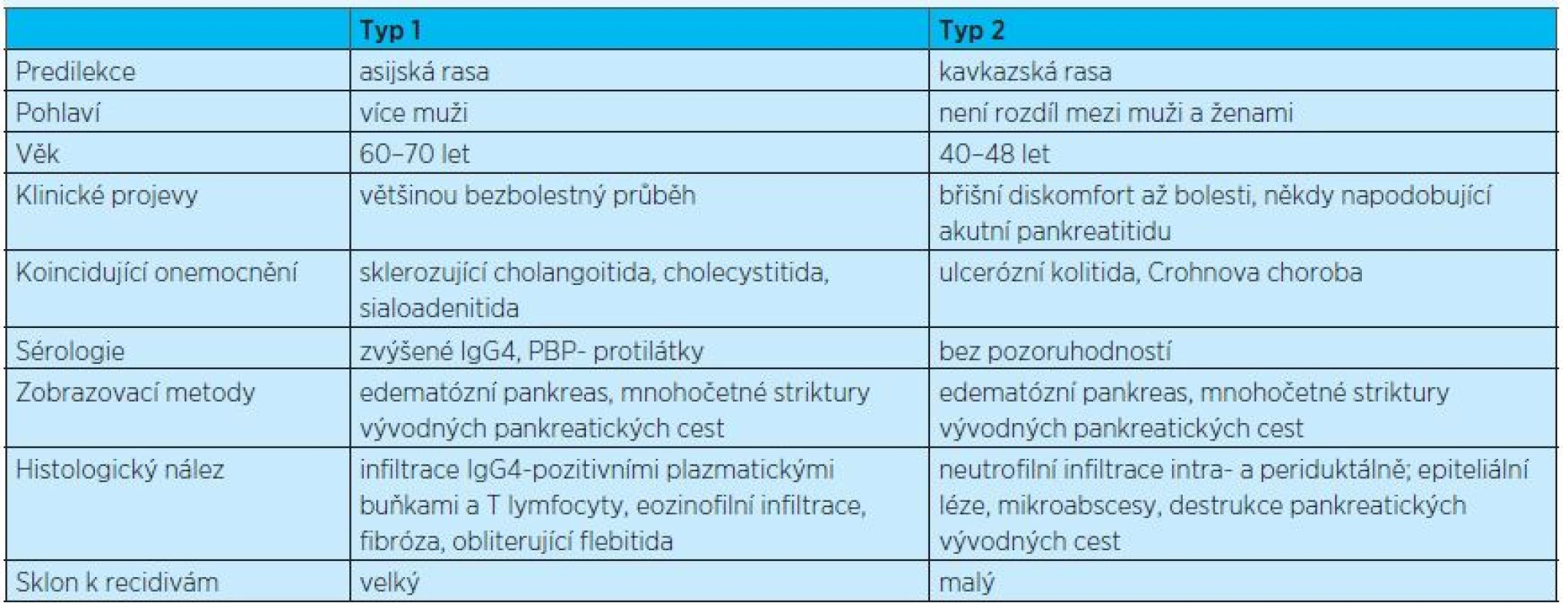
Obstruktivní forma chronické pankreatitidy
Představuje asi 7 % všech chronických pankreatitid(15). Navazuje na opakovanou nebo protrahovanou biliární obstrukci (choledocholitiáza, fibrózní změny vaterské papily, ampulomy). Zvýšený tlak v choledochu se přenáší i do menších vývodných cest. Důsledkem je tkáňová ischemie s poškozením parenchymu slinivky břišní a následnou fibrotickou přestavbou.
Akutně recidivující forma chronické pankreatitidy
Je způsobena opakujícími se záchvaty, klinicky připomínajícími akutní pankreatitidu i s krátkodobým zvýšením sérových amyláz a lipáz, např. při dyskinezi Oddiho svěrače nebo výskytu pancreas divisum (1). K přechodu do chronické pankreatitidy může také dojít po opakovaných akutních zánětech slinivky s různě rozsáhlými nekrózami a následným hojením méněcennou vazivovou tkání.
Klinický obraz
Nemoc má plíživý začátek, pokud se nerozvíjí na bázi již dříve probíhajících atak akutní pankreatitidy. Avšak postupně, dříve či později, většinu pacientů trápí bolesti břicha. Jsou kontinuální, většinou dlouhodobé, trvalého charakteru s epizodami intenzivnějších atak, které nutí pacienty zaujímat úlevu v předklonu nebo v genokubitální poloze. Maximum bolesti je kolem pupku, odkud se šíří pod oba oblouky žeberní. Vyvolávajícím momentem je obvykle požití tučného jídla, ale i většího množství dietní stravy. Ve starším věku, v pokročilých stadiích onemocnění při destrukci senzitivních nervových zakončení však bolesti nemusí stát v popředí a dominují příznaky z insuficientní funkce slinivky. Častá je nauzea a zvracení, zvláště u alkoholické formy. Výraznou bolestivostí bývá provázena idiopatická forma ChP začínající v mladším věku 20–25 let, zatímco typ „stařecký“, s klinickými projevy po 50. roce života, je většinou bez výrazné bolestivosti nebo jen s břišním diskomfortem. Vznik bolesti u ChP vysvětluje tabulka 6.
Tab. 6. Vznik bolesti u chronické pankreatitidy 
Nedostatečné trávení při exokrinní insuficienci pankreatu vede k průjmům a malabsorpci. Stolice je objemná, kopiózní, mastná, zapáchající, s nestrávenými zbytky (steatorea). Trávicí potíže a obavy pacienta z příjmu potravy vedou k váhovému úbytku. Tuhá tkáň vazivově změněného pankreatu může utlačovat intrapankreatickou část choledochu se vznikem obstrukčního ikteru nebo i s cholangoiditou. K méně častým příznakům patří střevní dyskineze, ascites a fluidothorax (s vysokým obsahem amyláz, event. lipáz), známky střevní obstrukce, splenomegalie nebo portální hypertenze při trombóze portální žíly. V pokročilých stadiích choroby, kdy je destruováno více než 85–90 % Langerhansových ostrůvků, se objevuje diabetes mellitus.
Vyšetřovací metody
Při většinou chudém fyzikálním nálezu mají diagnostický význam laboratorní a zobrazovací metody.
Laboratorní vyšetření:
Sérové hodnoty amyláz a lipáz: malá senzitivita a specifita
Sérové hladiny trypsinogenu: malá senzitivita
Pankreatická elastáza 1 ve stolici: malá senzitivita
Analýza sběru stolice za 72 hodin: zlatý standard v laboratorní diagnostice malabsorpce, není ale schopna odlišit její pankreatickou a extrapankreatickou etiologii a pro povahu provedení není příliš oblíbená.
Funkční testy slinivky břišní: např. sekretin-cholecystokininový stimulační test – spočívá v analýze duodenálního obsahu po stimulaci enterohormony; vysoce senzitivní i specifický, ale laboratorně a časově náročný, proto se v běžné praxi příliš nepoužívá.
Dechové testy MTG (mixed triglyceride test): při tomto testu se podávají perorálně triglyceridy se značeným uhlíkem C13. Triglyceridy jsou štěpeny v duodenu působením pankreatické lipázy a odštěpené mastné kyseliny s atomy uhlíku C13 se metabolizují v játrech. Vznikající oxid uhličitý (CO2) se značeným uhlíkem je měřen ve vydechovaném vzduchu. Toto vyšetření není rozšířeno pro finanční nákladnost a absenci jednotného protokolu vyšetření.
Imunologické vyšetření protilátek: při suspekci na autoimunitní formu (viz tab. 4).
Vyšetření CFTR, SPINK-1 a PRSST-1: při podezření na geneticky podmíněnou ChP.
Zobrazovací metody
Dominantní postavení v diagnostice chronické pankreatitidy mají zobrazovací metody:
Abdominální ultrasonografie je jednoduchá a dobře dostupná metoda, ale pankreas bývá často překryt střevními plyny, navíc změny při chronické pankreatitidě nemusejí být samy o sobě dobře zobrazitelné. Hodnotíme velikost žlázy, homogenitu tkáně, eventuální ložiskové změny a šíři žlučových cest.
Počítačová tomografie a magnetická rezonance s cholangiopankreatografií jsou v dnešní době nejpřínosnějšími metodami a představují zlatý standard k rozlišení morfologických změn při ChP. Mezi morfologickým a funkčním nálezem však nemusí být jednoznačná přímá úměra. Diagnostickou rozvahu může doplnit výsledek endoskopické ultrasonografie s odběrem a vyšetřením bioptického vzorku. Endoskopická retrográdní cholangiopankreatografie (ERCP) se dnes vzhledem ke své invazivitě rezervuje pro terapeutické výkony na žlučových cestách; přesto je v literatuře popisována jako přínosná při autoimunitní ChP pro zobrazení změn na vývodných pankreatických cestách(13).
Diferenciální diagnostika
Od chronické pankreatitidy je nutno odlišit malabsorpční syndrom jiné etiologie, rakovinu pankreatu, dyskinezi žlučových cest, prostou funkční dyspepsii, někdy i anginózní bolesti při ischemické chorobě srdeční.
Léčba
Chronická pankreatitida je obtížně léčitelná. Pro terapii jsou důležitá doporučení:
Konzervativní terapie
1. Přísný zákaz alkoholu. Při pokračující konzumaci 50 % pacientů umírá do 10 let.
2. Dietní opatření:
- příjem potravy v menších a častějších porcích
- omezení tuků, nahrazení živočišných tuků rostlinnými
- strava bohatá na bílkoviny s vysokým obsahem esenciálních aminokyselin
- nutriční podpora (sipping, při těžkém stavu enterální výživa)
- omezení cukrů, popřípadě i aplikace inzulinu u pankreatogenního diabetu.
3. Perorální farmakologická substituce pankreatických enzymů – podávají se přípravky obsahující tzv. pankreatin – extrakt z vepřových slinivek. Největší efekt na léčbu steatorey mají přípravky s vysokým obsahem lipáz. Preferujeme léky ve formě kapslí, které obsahují mikropelety o velikosti 1–1,5 mm. Mikropelety jsou pokryty acidorezistentním povrchem, aby byly pankreatické enzymy chráněny před účinkem žaludeční kyseliny. Starší pacienti, kteří mají potíže s polykáním celých kapslí, mohou jejich obsah vysypat a nerozkousané mikrogranule polknout. Léky se užívají během jídla, s dostatkem tekutin, aby mohlo dojít k potřebnému promísení s potravou. Během 30 minut po požití se uvolní až 50 % obsahu enzymů. Obvyklá dávka je 3x 25 000 j. až 3x 50 000 j. lipázy denně, při úplné afunkci slinivky se může ještě zvýšit. Pacient by však měl užívat nejnižší účinnou dávku, nutnou k adekvátnímu trávení tuků podle složení a množství jídla. U pacientů léčených vysokými dávkami pankreatických enzymů (jsou to zejména pacienti s cystickou fibrózou) byly popsány komplikace v podobě syndromu obstrukce distálního střeva (obturace střeva zahuštěným obsahem) a striktury v ileocekální oblasti a vzestupného tračníku při fibrotizující kolonopatii(17,18,19).
4. Léčba bolesti. Asi u 20 % pacientů má analgetický efekt substituce pankreatickými enzymy s vysokým obsahem proteáz(20). V této indikaci se doporučují preparáty bez acidorezistentní vrstvy, které jsou účinné již v duodenu(21). Tyto lékové formy však nejsou u nás dostupné. Při nedostatečném analgetickém účinku lze podat paracetamol v analgetické dávce, Novalgin či Tramadol. V léčbě neuropatické bolesti se osvědčila tricyklická antidepresiva (amitriptylin, nortriptylin), inhibitory zpětného vychytávání serotoninu (SSRI) a antikonvulziva (pregabalin, gabapentin). Postupujeme od méně silných analgetik k silnějším. Cílem je dosažení ústupu bolesti co nejslabšími analgetiky v co nejmenších dávkách. Silným opioidům se snažíme vyhnout a rezervujeme je pro jinak neřešitelné stavy s neztišitelnou bolestí. Pokud se bolest nedaří zvládnout farmakoterapií, je vhodné zvážit endoskopickou či chirurgickou intervenci.
5. Imunosupresivní léčba je indikována u chronické autoimunitní pankreatitidy. Tato forma ChP má většinou dobrou prognózu a u některých pacientů dochází i ke spontánní remisi. Je významně responzibilní na terapii kortikoidy. Relapsy onemocnění jsou však časté především u 1. typu ChP. Při selhání kortikoterapie lze pomýšlet na léčbu účinnějšími imunosupresivy (azathioprin, mykofenolát mofetil), jejich efekt však nebyl ověřen v klinických studiích(13). Nadějně se jeví léčba monoklonální protilátkou zaměřenou proti B lymfocytům nesoucím antigen CD20 – rituximabem(22, 23).
Invazivní výkony:
1. Endoskopická retrográdní cholangiopankreatografie (ERCP) je indikována při obstrukci vývodných pankreatických či biliárních cest (papilosfinkterotomie, extrakce kamene, zavedení jednoho či více plastikových nebo metalických stentů; plastikové stenty, na rozdíl od metalických, je nutno vyměňovat každé 3 měsíce; nevýhodou metalických stentů je jejich cena).
2. Extrakorporální litotripse je vhodná k léčbě wirsungolitiázy. Slouží k rozbití kamene rázovou vlnou. Zavedení stentu umožní spontánní odchod fragmentů nebo jsou fragmenty kamene odstraněny při ERCP(24).
3. Endoskopická drenáž pseudocyst pod endosonografickou kontrolou je dnes preferována před chirurgickými drenážními výkony pro menší invazivitu a větší bezpečnost. Pokud je výkon neúspěšný, lze endoskopický přístup upgradovat na chirurgický. K drenáži jsou určeny symptomatické pseudocysty, samotná velikost pseudocysty není indikací k výkonu. Komunikaci mezi pseudocystou a zažívací trubicí zajišťují stenty, které se zavádějí transpapilárně nebo transmurálně přes stěnu žaludku nebo duodena(25) a ponechávají se alespoň 6 týdnů. Po úspěšném výkonu dochází k vymizení pseudocysty a ústupu symptomů.
4. Blokáda plexus coeliacus se pro sporný efekt používá vzácně.
Chirurgická terapie
Indikací k chirurgickým výkonům jsou závažné a/nebo jinými metodami neřešitelné stavy:
- bolesti refrakterní na medikamentózní či endoskopickou léčbu
- stenózy pankreatických a/nebo žlučových cest
- pseudocysta pankreatu
- maligní bujení.
Chirurgický přístup představují:
- drenážní výkony (drenáž pseudocysty; drenáž ductus Wirsungi – spočívá v podélném protětí pankreatického vývodu s pankreatikojejunoanastomózou side to side)
- resekční výkony (odstranění bolestivé zánětlivě změněné hlavy pankreatu nebo zhoubného nádoru).
Prognóza a prevence
Chronická pankreatitida významně zhoršuje kvalitu života. Je rizikovým faktorem vzniku rakoviny slinivky břišní. Přes diagnostické a terapeutické pokroky je mortalita pacientů s ChP stále 4x vyšší než v běžné populaci(26). Horší prognózu mají pacienti s významnou podvýživou. Zejména pro osoby staršího věku může významná podvýživa znamenat závažný stav ohrožení. Relativně dobrou prognózu představuje autoimunitní forma onemocnění. V prevenci je důležité dodržovat správnou výživu a vyvarovat se rizikových faktorů, zejména abúzu alkoholu a kouření.
Autoři prohlašují, že v souvislosti s publikací článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny farmaceutickou firmou.
MUDr. Marie Berková, Ph.D.1
MUDr. Zdeněk Berka2
prof. MUDr. Eva Topinková, CSc.1
1Geriatrická klinika 1. LF UK a VFN Praha
2II. interní klinika LF UP a FN Olomouc
MUDr. Marie Berková, Ph.D.
e-mail: Marie.berkova@lf1.cuni.cz
Pracuje na Geriatrické klinice 1. LF UK a VFN v Praze.
Zdroje
1. Dítě P, Trna J, Floreanová K, Geryk E. Chronická pankreatitida. Med praxi 2011; 8(11): 455–458.
2. Yadav D, Timmons L, Benson JT, et al. Incidence, prevalence, and survival of chronic pancreatitis: a population-based study. Am J Gastroenterol 2011;106(12):2192–2199.
3. Barman K, Premalatha G, Mohan V. Tropical chronic pancreatitis. Postgrad Med J 2003; 79(937): 606–615.
4. Brock C, Nielsen LM, Lelic D, Drewes AM. Pathophysiology of chronic pancreatitis. World J Gastroenterol 2013; 19(42): 7231–7240.
5. Ševčíková A. Od chronické nehereditární pankreatitidy k pankreatickému karcinomu. Sborník přednášek Aktuální gastroenterologie XVII. X/05.
6. Sah RP, Chari ST, Pannala R, et al. Differences in clinical profile and relapse rate of type 1 versus type 2 autoimmune pancreatitis. Gastroenterology 2010; 139 : 140–148.
7. Kamisawa T, Anjiki H, Egawa N. Rapid changes in sclerosing cholangitis associated with autoimmune pancreatitis. Pancreas 2009; 38 : 601–602.
8. Detlefsen S, Bräsen JH, Zamboni G, et al. Deposition of complement C3c, immunoglobulin (Ig)G4 and IgG at the basement membrane of pancreatic ducts and acini in autoimmune pancreatitis. Histopathology 2010; 57 : 825–835.
9. Chari ST, Longnecker DS, Klöppel G. The diagnosis of autoimmune pancreatitis: a Western perspective. Pancreas 2009; 38 : 846–848.
10. Frulloni L, Lunardi C, Simone R. Identification of a novel antibody associated with autoimmune pancreatitis. N Engl J Med 2009; 361 : 2135–2142.
11. Deshpande V, Gupta R, Sainani N, Sahani DV, et al. Subclassification of autoimmune pancreatitis: a histologic classification with clinical significance. Am J Surg Pathol 2011; 35 : 26–35.
12. Klöppel G, Detlefsen S, Chari ST, et al. Autoimmune pancreatitis: the clinicopathological characteristics of the subtype with granulocytic epithelial lesions. J Gastroenterol 2010; 45 : 787–793.
13. Wang Q, Zhang X, Zhang F. Autoimmune pancreatitis: current concepts. Sci China Life Sci 2013; 56(3): 246-253.
14. Zamboni G, Lüttges J, Capelli P. Histopathological features of diagnostic and clinical relevance in autoimmune pancreatitis: a study on 53 resection specimens and 9 biopsy specimens. Virchows Arch 2004; 445 : 552–563.
15. Lowes JR, Rode W, Lees WR, et al. Obstructive pancreatitis: Unusual causes of chronic pancreatitis. Br J Surgery 1988; 75(11): 1129–1133.
16. Buscher HC, Wilder-Smith OH, van Goor H. Chronic pancreatitis patients show hyperalgesia of central origin: a pilot study. Eur J Pain 2006; 10 : 363–370.
17. Smyth RL. Fibrosing colonopathy in cystic fibrosis. Arch Dis Child 1996; 74(5): 464–468.
18. Bansi DS, Price A, Russell C, Sarner M. Fibrosing colonopathy in an adult owing to over use of pancreatic enzyme supplements. Gut 2000; 46 : 283–285.
19. Vávrová V. Fibrotizující kolonopatie. In: Vávrová V. Cystická fibróza. Grada Publishing 2006 : 307–308.
20. Warshaw AL, Banks PA, Fernandez-del Castillo C. AGA technical review. Treatment of pain in chronic pancreatitis. Gastroenterology 1998; 115 : 765–776.
21. Gachago C. Draganov PV. Pain management in chronic pancreatitis. World J Gastroenterol 2008; 14 : 3137–3148.
22. Topazian M, Witzig TE, Smyrk TC, et al. Rituximab therapy for refractory biliary strictures in immunoglobulin G4-associated cholangitis. Clin Gastroenterol Hepatol 2008; 6 : 364–366.
23. Khosroshahi A, Bloch DB, Deshpande V, Stone JH. Rituximab Therapy Leads to Rapid Decline of Serum IgG4 Levels and Prompt Clinical Improvement in IgG4-Related Systemic Disease. Arthritis Rheum 2010; 62(6): 1755–1762.
24. Tandan M, Reddy DN, Santosh D, et al. Extracorporeal shock wave lithotripsy and endotherapy for pancreatic calculi-a large single center experience. Indian J Gastroenterol 2010; 29 : 143–148.
25. Aghdassi AA, Mayerle J, Kraft M, et al. Pancreatic pseudocysts – when and how to treat? HPB (Oxford) 2006; 8(6): 432–441.
26. Nøjgaard C. Prognosis of acute and chronic pancreatitis – a 30-year follow-up of a Danish cohort. Dan Med Bull 2010; 57(12): B 4228.
Štítky
Geriatria a gerontológia Praktické lekárstvo pre dospelých Protetika
Článek Editorial
Článok vyšiel v časopiseGeriatrie a Gerontologie
Najčítanejšie tento týždeň
2015 Číslo 2- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
-
Všetky články tohto čísla
- Atypický průběh disekce hrudní aorty u 80leté ženy
- Geriatrie 2015 v Evropě a u nás
-
Recenze knihy:
Ošetřovatelství v geriatrii – hodnoticí nástroje - Editorial
- Jsou senioři s duševní poruchou více nemocní a medicínsky náročnější?
- Vnímání psychické dimenze kvality života seniory s chronickou nenádorovou bolestí
- Chronické srdeční selhání – specifika léčby seniorů
- Chronická pankreatitida ve stáří
- Nutriční podpora u nemocných s demencí
- Recenze anglické směrnice o omezovacích prostředcích
- Využití podtlakové terapie v lokální terapii chronických a obtížně hojitelných ran
- Geriatrie a Gerontologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Chronická pankreatitida ve stáří
- Nutriční podpora u nemocných s demencí
- Chronické srdeční selhání – specifika léčby seniorů
- Atypický průběh disekce hrudní aorty u 80leté ženy
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy




