-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Klinické studie: ukončené, přednesené nebo publikované v poslední době
Autori: E. Dvořáková; J. Špinar
Pôsobisko autorov: LF MU a FN Brno, pracoviště Bohunice ; Interní kardiologická klinika
Vyšlo v časopise: Kardiol Rev Int Med 2006, 8(1-2): 76-79
Kategória: Klinické studie
Uvádíme další klinické studie prezentované na kongresu European Society of Cardiology, 3-7. 9. 2005 ve Stockholmu, a na American Heart Association, 13.-16. 11. 2005 v Dallasu.
REPAIR AMI [1]
(Reinfusion of Enriched Progenitor cells And Infarct Remodelling in Acute Heart Failure) a ASTAMI (Autologous Stem cell Transplantation in Acute Myocardial Infarction)
Výsledky REPAIR-AMI byly prezentovány Wolkerem Schachingerem (J.W. Goethe Universität, Frankfurt nad Mohanem, Německo). Výsledky ASTAMI byly prezentovány Ketilem Lundem (Rikhospitalet University Hospital, Oslo, Norsko). Obě tyto dobře designované randomizované kontrolované studie prezentované na AHA se týkají pacientů po infarktu myokardu.
Náhrada ztracených kardiálních myocytů by mohla být cenným přínosem v péči nebo prevenci srdečního selhání. Za poslední dekádu byly učiněny pokusy o implantaci kosterních myoblastů nebo pluripotentních kmenových buněk do poškozeného nebo selhávajícího myokardu. V současné době není jasné, zda je taková intervence bezpečná či efektivní. Mechanizmus efektu je tedy nejistý. Implantace kmenových buněk může zapříčinit neovaskularizaci, pozměnit funkci myokardu nebo se mohou buňky vyvíjet do funkčních kardiálních myocytů.
Léčebnou strategií je dotvořit populaci poškozeného myokardu. Intervence, která je příliš časná, může selhat vzhledem k neadekvátní perfuzi nebo vysokému oxidativnímu stresu či zánětu, a pokud by se uskutečnila příliš pozdě, mohla by se vzhledem k existenci organizované myokardiální jizvy ukázat jako neefektivní. Nicméně až 2 třetiny z dysfunkčních segmentů po infarktu myokardu tvoří omráčený, hibernovaný nebo částečně nemocný myokard a je možné, že intervence kmenovými buňkami může ovlivnit funkci právě těchto segmentů.
Studie REPAIR-AMI randomizovala 204 pacientů z Německa a Švýcarska, kterým byly podány kmenové buňky z kostní dřeně nebo extrakt bez buněk průměrně 4. den po infarktu myokardu. Buňky byly získány aspirací, v obou skupinách 50 ml kostní dřeně z lopaty kyčelní kosti. Za 4 měsíce vzrostla ejekční frakce levé komory u obou skupin, ale vzestup byl signifikantně větší u pacientů, kterým byly podány kmenové buňky (48 % a 54 %) na rozdíl od 2. kontrolní skupiny (47 % a 50 %, p = 0,021). Větší prospěch měli pacienti, kteří byli léčeni za více než 5 dní od infarktu myokardu. V obou skupinách se vyskytla 2 úmrtí: v placebo skupině se u 2 pacientů rozvinulo srdeční selhání a 5 pacientů mělo opětovný infarkt myokardu; ani jedna z těchto příhod nesouvisela s implantací kmenových buněk. Více pacientů vyžadovalo revaskularizaci v placebo skupině (28 oproti 19 %). Tyto malé rozdíly v rychlosti výskytu rekurentního infarktu myokardu a nutnosti revaskularizace mohou být náhodné.
Na rozdíl od této studie zahrnovala ASTAMI studie z Norska 100 pacientů s infarktem myokardu přední stěny, kteří buď dostali kmenové buňky, nebo placebo a to 5.-8. den od vzniku infarktu myokardu. Pacienti byly průběžně vyšetřování pomocí PET, echokardiograficky a pomocí nukleární magnetické rezonance. Nebyl shledán žádný benefit v průběhu 6 měsíců, dokonce ejekční frakce výrazněji vzrostla u kontrolní skupiny (+ 1,2 % oproti + 4,3 %, p = 0,05).
Existuje taktéž celá řada jiných studií, zabývajících se podobnou problematikou. Studie MAGIC se např. zabývá využitím autologních kosterních svalových buněk u pacientů se srdečním selháním, kteří prodělali chirurgickou revaskularizaci či dostali ICD, druhá zmíněná skupina v důsledku možného vzestupu rizika náhlé srdeční smrti spojené s touto formou léčby. Kmenové buňky se mohou vyvíjet do různých buněk; u myoblastů se zdá, že mohou vytvářet pouze svalové buňky. BOOST II studie randomizuje 200 pacientů s rozsáhlým infarktem a signifikantně sníženou funkcí LK, kteří obdrží kostní dřeň - u těchto pacientů bude sledována regionální a globální funkce levé komory po dobu 3 let.
REVIVE II a SURVIVE [1]
(Randomised multicentre EValuation of IntraVenous levosimendan Efficacy versus placebo in the short tem treatment of decompensated heart failure)
(Survival of patients with acute heart failure in need of intravenous inotropic support trial)
Levosimendan má inotropní a vazodilatační účinky zprostředkované pomocí kalciové senzitizace a otevřením draslíkových kanálů. Celkem 3 studie vycházely z předpokladu, že krátkodobé podání (6-24 hod) levosimendanu by mohlo vylepšit symptomy srdečního selhání a snížit mortalitu v následujících 180 dnech.
Výsledky REVIVE II byly prezentovány Miltonem Packerem (University of Texas Southwestern Medical Center, Texas, USA). Výsledky SURVIVE byly prezentovány Alexandrem Mebuzzou (Hospital Lariboisiere, Paříž, Francie).
Studie REVIVE II porovnává levosimendan a placebo u pacientů, kteří byli přijati do nemocnice s primární či sekundární diagnózou srdečního selhání a s ejekční frakcí LK pod 35 %, u kterých trvá respirační insuficience i po podání diuretik a vazodilatace. Podle protokolu by měli být pacienti zařazeni do studie do 48 hod od přijetí, ale je umožněno randomizovat je i později. Je tedy zřejmé, že tato studie je zaměřena zejména na pacienty s vážným srdečním selháním, kteří nereagují na standardní terapii, a u kterých ještě léčba levosimendanem neproběhla.
Vylučovacími kritérii byla nutnost ventilační podpory, systolický krevní tlak pod 90 mm Hg a hladina sérového kreatininu nad 450 μmol/l.
Primární cíl byl komplexem složeným z několika parametrů, kritéria byla pozměněna na základě předchozí pilotní studie REVIVE I. Výsledně byli pacienti ve 3 skupinách. První část tvořili pacienti, u kterých došlo ke zmírnění symptomů po 6, 24 hodinách a 5 dnech. Druhou potom pacienti, u kterých došlo ke zhoršení symptomů v jakémkoliv z uvedených období či přetrvávaly takové závažné symptomy, které vyžadovaly léčbu i.v. diuretiky, inotropními či vazodilatačními látkami po více než 24 hodinách. Poslední skupinou byli pacienti, u kterých se stav nezměnil.
Průměrný věk z 600 pacientů randomizovaných do studie byl 63 let, 72 % z nich byli muži. Průměrná hodnota LVEF byla 23 %, přes 70 % byly edematózní pacienti, 68 % pacientů mělo šelesty a průměrný systolický krevní tlak byl 116 mm Hg. ACE-inhibitory, betablokátory, digoxin a spironolakton mělo předepsáno 85 %, 78 %, 60 % a 41 % pacientů.
Primární cíl prokázal při podávání levosimendanu větší míru zlepšení stavu pacientů (6 %) a méně zhoršení stavu pacientů (7 %) na 0,015 hladině významnosti. 15 % pacientů ze skupiny léčené levosimendanem vyžadovalo další záchranou léčbu, zejména diuretika, oproti 26 % z kontrolní skupiny. Plazmatická koncentrace BNP se snížila zhruba o 250 pg/ml a doba hospitalizace se zkrátila asi o 2 dny (p = 0,001), ale toto nebylo doprovázeno snížením mortality (ačkoliv snížení BNP bývá obvykle dobrým prognostickým ukazatelem). V průběhu 90 dní bylo 35 úmrtí v placebo skupině a 45 ve skupině s levosimendanem, tedy v léčené skupině byla vyšší mortalita.
Z nežádoucích účinků bylo po levosimendanu více případů hypotenze (50 % vs 36 %) a fibrilace síní (8 % vs 2 %) i komorových arytmií včetně izolovaných komorových extrasystol.
SURVIVE studie porovnává levosimendan a dobutamin a zaměřuje se na jednu z nejrizikovějších populací, vůbec kdy zařazených do studie se srdečním selháním. Více než 1 ze 4 pacientů zemřel do 6 měsíců i přes moderní léčbu, což je více než v jakékoliv jiné studii akutního srdečního selhání a podobné jako u studie CONSENSUS.
Vstupní kritéria do studie jsou následující:
- vstupní přijímací diagnóza akutního srdečního selhání
- LVEF pod 30 %
- přetrvávající dušnost i přes podání diuretik i.v.a vazodilatace
- příznaky z nízkého srdečního výdeje (oligurie, chladná periferie a nízký arteriální tlak).
Pacienti by měli mít systolický krevní tlak od 80 do 130 mm Hg a sérovou hladinu kreatininu pod 450 µmol/l.
Primárním cílem byla mortalita za 180 dní a tento cíl byl založen na předpokladu, že krátkodobá léčba může mít dlouhodobější účinky, podobně jako trombolýza či antiagregace po infarktu myokardu. Jednalo se o konvenční randomizovanou kontrolovanou studii s krátkodobobým podáním levosimendanu a dobutaminu použitím dvojitě zaslepené techniky.
Dohromady bylo randomizováno 1 327 pacientů. Průměrný věk byl 67 let, 72 % byli muži, 88 % byli pacienti ji se známým srdečním selháním, LVEF byla 24 %, 76 % mělo srdeční selhání ischemické etiologie, průměrný arteriální tlak byl 116 mm Hg a plazmatická koncentrace BNP byla hodně zvýšená.
Výsledky studie ukazuje tab 1.
Tab. 1. Výsledky studie SURVIVE. 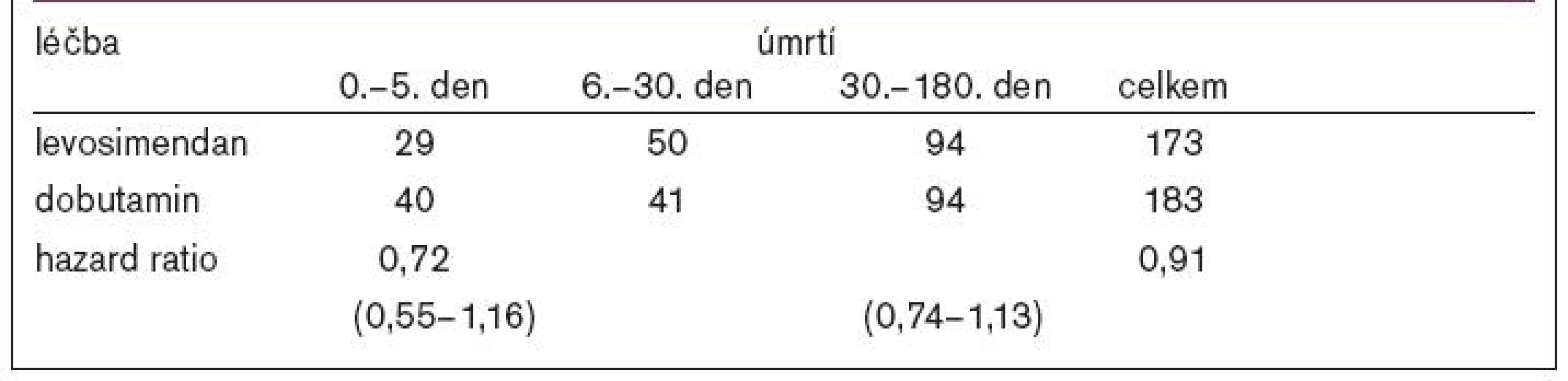
Byl prokázán časný benefit pacientů po levosimendanu, tento však netrval delší dobu, než je hemodynamická účinnost léku. Léčba levosimendanem byla spojena s výrazným snížením hladiny BNP, více než u dobutaminu - tento efekt trval 5 dní. Nebyly žádné rozdíly v obou skupinách v hladině sérového kreatininu či výskytu hypotenze. Levosimendan byl spojen v porovnání s dobutaminem s podstatným snížením relativního rizika úmrtí v průběhu prvních 30 dní. U pacientů léčených levosimendanem došlo méně často ke zhoršení srdečního selhání (12,3 % vs 17 %, p < 0,02)
U pacientů se častěji objevila fibrilace síní (9,1 % vs 6,1 %, p < 0,05)
Zda jsou tyto data dostatečná k tomu, aby se rozšířilo podávání levosimendanu, zatím závisí na klinické praxi každého z nás. Je zde daleko více důkazů o bezpečnosti nebo působení levosimendanu, než je tomu u jiných intravenózních inotropních či vazodilatačních látek, jako jsou např. nitráty. Další klinické studie porovnávající levosimendan vůči placebu, dobutaminu či intravenózním nitrátům se jistě budou těšit velkému zájmu. Do budoucna se plánují i studie s perorálně podávaným levosimendanem.
PROACTIVE [1]
(PROspective pioglitAzone Clinical Trial In macro Vascular Events)
Výsledky byly prezentovány Erlandem Erdmannem (Universität zu Köln, Kolín nad Rýnem, Německo). Glitazony jsou kontraindikovány u pacientů se srdečním selháním. Piogiltazone ovlivňuje kardiovaskulární rizikový profil snižováním hladiny triglyceridů a LDL-cholesterolu a zvyšováním hladiny HDL-cholesterolu. Je značná nejistota, jak vést léčbu u pacientů diabetiků se srdečním selháním nebo po infarktu myokardu.
PROACTIVE studie randomizovala 5 238 pacientů s diabetes mellitus 2.typu a s makrovaskulárními komplikacemi do 2 skupin: s placebem a s pioglitazonem. Pacienti byli sledování 2,85 let. Pacienti s předchozím (více jak 6 měsíců) infarktem myokardu tvořili velkou podskupinu pacientů se zvýšeným rizikem LVSD a srdečního selhání.
Výsledky studie jsou povzbuzující a kardiovaskulární benefit při léčbě glitazonem je podobný jako při léčbě statiny. Ve skupině s glitazonem došlo ke snížení rizika dalších koronárních příhod a byl také patrný trend k nižší mortalitě na kardiální onemocnění. Bylo zde nepatrně vyšší riziko vzniku edému a srdečního selhání, ale toto riziko nevedlo ke zvýšení rizika úmrtí na srdeční selhání.
Do budoucna by jistě byla vítána data, která by prověřila bezpečnost, působení a toleranci těchto léků u pacientů po akutním infarktu myokardu či u pacientů se srdečním selháním.
ESSENTIAL [2]
Výsledky studie ESSENTIAL byly prezentovány na European Congress of Cardiology (prof. Marco Metra, Brescia, Itálie). V této studii byl zkoumán efekt dlouhodobé léčby nízkými dávkami perorálního enoximonu (25-50 mg 3krát denně tohoto inhibitoru fosfodiesterázy III) u pacientů s pokročilým srdečním selháním. Předpokládalo se, že enoximone může snížit počet hospitalizací z kardiovaskulárních (KV) příčin, celkovou mortalitu, zvýšit submaximální pracovní kapacitu a zlepšit symptomy srdečního selhání.
Do studie, která probíhala v Americe i v Evropě, bylo zařazeno 1 854 pacientů s ischemickou nebo neischemickou kardiomyopatií, srdečním selháním NYHA III-IV a s ejekční frakcí levé komory < 30 %, tito byli rozděleni do 2 skupin. V první skupině byli pacienti dostávající enoximone (n = 926), v druhé potom pacienti s placebem ( n= 928).
Průměrný věk nemocných byl 62 let, ischemická KMP byla přítomna u 56 % pacientů, NYHA III mělo 91 %, průměrná ejekční frakce levé komory byla 23,6 % a téměř 90 % pacientů užívalo betablokátory a ACE-inhibitory. Američtí pacienti měli při vstupu signifikantně nižší ejekční frakci levé komory, nižší pracovní toleranci, a dlouhodobější anamnézu srdečního selhání.
Během 16,4 ± 0,2měsíčního sledování enoximonu a placeba nedošlo ke snížení počtu hospitalizací z KV-příčin ani ke snížení celkové mortality u skupiny s enoximonem (49,5 % vs 50,1 %, p = 0,71), ani samotné celkové mortality (21,7 % vs 22,6 %, p = 0,73). Nicméně signifikantně vzrostla pracovní tolerance (ověřená pomocí 6minutového walking testu) u amerických pacientů užívajících enoximon v porovnání s placebem (o 10 metrů). U evropských pacientů tomu tak nebylo (1,5 metru). Dále bylo popisováno podobné zlepšení symptomů u obou skupin pacientů.
Mnohem častěji se ve skupině s enoximonem vyskytly nežádoucí účinky jako je průjem a palpitace. S ohledem na bezpečnost, enoximon neměl proarytmický efekt, jak bylo dokázáno na riziku náhlé smrti a fibrilace síní, které bylo stejné u obou skupin
Můžeme tedy konstatovat, že se léčba perorálním enoximonem u pacientů s pokročilým srdečním selháním, kteří jsou již optimálně léčeni betablokátory a ACE-inhibitory, neukázala ani prospěšnou ani škodlivou.
IMAGINE [2]
Studie IMAGINE byla prezentována prof. Wiekem van Gilstem (Groningen, Nizozemí). Autoři studie předpokládali, že časné zavedení léčby quinaprilem může zlepšit výsledky u pacientů po CABG-operaci.
Primární cíle:
- čas do prvního výskytu:
- úmrtí z kardiovaskulárních příčin
- nefatálního infarktu myokardu
- koronární revaskularizace
- hospitalizace pro nestabilní AP
- dokumentované AP bez nutnosti hospitalizace.
Původně bylo plánováno zařazení 2 200 pacientů, nakonec počet vzrostl na 2 553. Pacienti byli do studie zařazeni, pokud byli stabilní do 7 dnů od CABG, byli starší 18 let a měli EF LK ≥ 40 %. Hlavními vylučovacími kritérii byla náhrada chlopně, snížení renálních funkcí, perioperační infarkt myokardu a indikace pro léčbu ACE-inhibitory. Z 2 553 pacientů 1 280 dostávalo quinapril (40 mg 1krát denně) a 1 273 placebo, pacienti byli sledování po dobu 3 let. Průměrný věk byl 61 let, předchozí IM mělo 40 %, průměrná ejekční frakce levé komory byla 60 %, betablokátory užívalo 80 % pacientů, ASA 98 % a statiny 90 %.
Ve výsledku nebyl prokázán prospěch u pacientů léčených quinaprilem. Úmrtí z KV-příčin dosáhlo míry 1,3 % u skupiny s quinaprilem a 1,3 % u skupiny s placebem, výskyt nefatálního infarktu myokardu byl 1,3 % vs 1,6 %. Navíc byl i vyšší výskyt nežádoucích účinků v prvních 3 měsících jako je hypotenze (9,2 % vs 3,9 %) nebo kašel (14,0 % vs 7,5 %). Tedy u optimálně léčených nízce rizikových pacientů podání quinaprilu do 7 dnů od CABG nebylo přínosné a dokonce se ukázalo, že by mohlo být i škodlivé.
OASIS 5 [2]
Výsledky studie OASIS 5 prezentovali dr. Shamirem Mehtou a dr. Salimem Yusufem (Hamilton, Kanada). Tato multicentrická studie porovnávala účinnost a bezpečnost léčby fondaparinem (syntetický pentasacharid specificky inhibující faktor Xa přes antitrombin III, 2,5 mg 1krát denně) v porovnání s léčbou enoxaparinem (1 mg/kg 2krát denně).
Pacienti s akutním koronárním syndromem bez ST-elevací museli splňovat 2 ze 3 kritérií (změny ST-úseků, pozitivní kardispecifické enzymy, věk nad 60 let), aby mohli být zařazeni.
U 20 078 pacientů byl podáván fondaparin či enoxaparin po dobu průměrně 5 dní. Jednalo se v 60 % o muže, 70 % pacientů mělo pozitivní troponin, 50 % deprese ST-úseků, 25 % předchozí anamnézu IM, 14 % předchozí anamnézu srdečního selhání.ASA, klopidogrel a betablokátory užívalo 98,67,87% pacientů.
Primárním kompozitním cílem byl výskyt úmrtí, infarktu myokardu a refrakterní ischemie v 9. dni od zařazení do studie a u pacientů léčených fondaparinem činil 5,9 % a u pacientů s enoxaparinem 5,8 %, současně byl signifikantně nižší výskyt krvácení u pacientů s fondaparinem. Také došlo k signifikantní redukci mortality a výskytu infarktu myokardu v průběhu 6 měsíců (10,3 % u fondaparinu vs 11,2 %, p = 0,036), přičemž hlavní příčinou rozdílů v dlouhodobé mortalitě se zdá být nadměrné krvácení. Ukázalo se tedy, že podávání fondaparinu (navíc 1krát denně, bez nutnosti dávkování podle hmotnosti) u pacientů s akutním koronárním syndromem bez ST-elevací je stejně efektivní v prevenci časných ischemických příhod jako enoxaparin, ale snižuje dlouhodobou mortalitu, což může souviset se snížením rizika krvácivých komplikací.
ASSENT-4 PCI [2]
První výsledky multicentrické studie ASSENT-4 PCI studie byly prezentovány prof. Fransem van de Werfem (Leuven, Belgie). Studie vycházela z předpokladu, že plně dávkovaná fibrinolýza předcházející PCI/facilitované PCI by mohla zlepšit klinické výsledky v porovnání s primární PCI u pacientů s infarktem myokardu a ST-elevacemi a očekávaným delay do primární PCI více než 60 minut.
Pacienti do 6 hodin od výskytu symptomů, s ST-elevacemi nad 6 mm dohromady byli rozděleni na 2 skupiny, u jedné byla podávána fibrinolýza (TNK-tPA) následovaná PCI, u druhé skupiny byla prováděna samotná PCI. Celkově bylo randomizováno 1 667 pacientů (46 % v PCI-centru).
Primárním cílem bylo úmrtí nebo kardiogenní šok nebo městnané srdeční selhání v následujících 90 dnech. Studie byla předčasně ukončena v důsledku vzestupu mortality u facilitované PCI a byly prezentovány jen 30denní výsledky. <
30 denní mortalita u 827 pacientů léčených TNK + PCI byla 6% vs 3,8% u 838 pacientů léčených pouze PCI (p = 0,04).
U 1. skupiny se častěji vyskytl rekurentní infarkt myokardu (4,1 % vs 1,9 %, p = 0,01). Průměrný čas mezi podáním fibrinolýzy a balonkovou angioplastikou byl 104 minut a neočekávaně u 43,5 % pacientů byl po podání fibrinolýzy TIMI flow méně než 3. Častější byly krvácivé příhody u pacientů s TNK + PCI (31,3 % vs 23,4 %, p < 0,001). U pacientů pouze s PCI se nevyskytly mozkové příhody, zatímco u 2. skupiny 0,97 % pacientů mělo intrakraniální krvácení a 0,6 % pacientů ischemický iktus. 6% mortalita u pacientů s TNK + PCI odpovídá výsledkům z předchozích pokusů s fibrinolýzou. Z výše uvedeného vyplývá, že facilitovaná PCI společně s plně dávkovanou fibrinolýzou nemůže být doporučována.
TARGET [3]
(Do Tirofiban and ReoPro Give Similar Efficacy Outcome)
Studie TARGET klade otázku, zda tirofiban a abciximab zaručují podobnou účinnost u pacientů, kteří podstoupili neemergentní PCI s implantací stentu. Studie prezentovala 1roční mortalitu.
Některé studie prokázaly účinnost intravenózních inhibitorů glykoproteinů IIb/IIIa při snížení 30denní mortality, infarktu myokardu a urgentní revaskularizace - tyto studie porovnávaly placebo a inhibitory glykoproteinů IIb/IIIa, ale studie TARGET porovnává účinnost a bezpečnost tirofibanu vs abciximabu.
Do studie byli zařazeni pacienti, kteří podstoupili neemergentní PCI de novo vzniklé stenózy nebo restenózy nativní tepny nebo bypassu. Vyloučeni byli pacienti se STEMI, kardiogenním šokem, kreatininem nad 2,5 mg/dl, krvácivou dietézou. Pacienti byli vybráni v severní Americe, Austrálii a 14 evropských státech. Všichni pacienti dostali Aspirin před zákrokem a bylo přísně doporučeno nejméně 2 hodiny před katetrizací podání 300 mg klopidogrelu p.o.; heparin se během katetrizace podával podle APTT (nad 250 s), zkoumané látky byly podány bezprostředně před revaskularizací. Tirofiban nejprve bolus 10 µg/kg následovaný 18-24 hod infuzí 0,15 µg /kg /min a abciximab 0,25 mg/kg bolus a následně 12hodinová infuze rychlostí 0,125 µg /kg/min. ASA v kombinaci s klopidogrelem byly podávány ještě následující 1 měsíc a bylo doporučeno dlouhodobé podání ASA. Primární cíle byly složeny z úmrtí, nefatálního IM, nebo urgentní cílené revaskularizace ve 30 dnech. 6měsíční výskyt výše zmíněných primárních cílů a roční mortalita byly sekundárními cíly, data byla sbírána prospektivně.
Výsledky studie byly následující: 46 pacientů, kteří dostávali tirofiban - tj. 1,6 % zemřelo do 1 roku, ve 2. skupině bylo 42 úmrtí (1,7 %, p = 0,660). Roční mortalita pacientů s akutním koronárním syndromem v 1. skupině byla 2,3% v porovnání s druhou, kde činila 2,2 % (p = 0,897), u pacientů bez akutního koronárního syndromu s tirofibanem 1,4 % a s abciximabem 1,0 % (p = 0,530). V podskupině pacientů s DM zemřelo do 1 roku 12 pacientů léčených tirobifanem (2,1 %) a 16 pacientů léčených abciximabem (2,9 %, p = 0,436). Ke zhodnocení nezávislých predikátorů 1roční mortality byl použit Coxův model, který byl přizpůsoben vzhledem k věku, pohlaví, typu léčby, BMI, přítomnosti Q-IM, přítomnosti akutního koronárního syndromu, srdečního selhání, předchozí anamnéze periferního cévního onemocnění, léčbě betablokátory, nesteroidními antiflogistiky, perorálními antidiabetiky; výsledky ukazuje tabuka 2.
Tab. 2. Multivariabilní prediktory 1roční mortality. 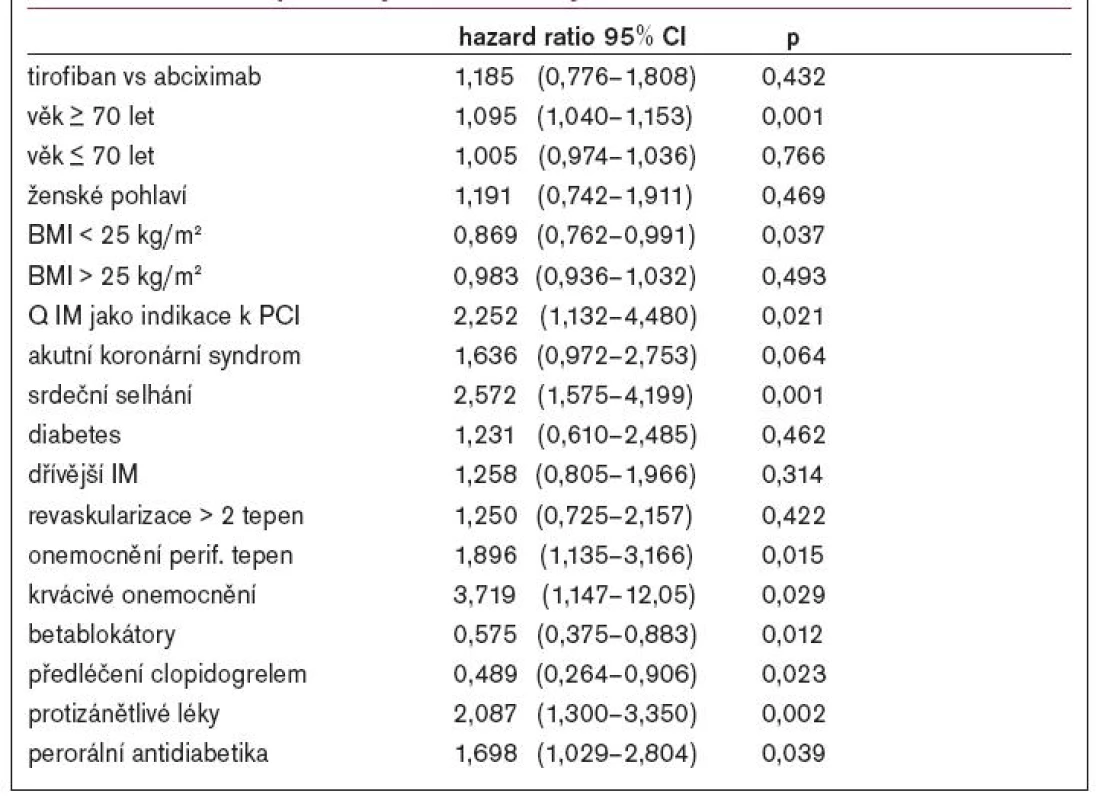
Věk nad 70 let, Q-IM, srdeční selhání, existence periferního vaskulárního onemocnění a užití nesteroidních antiflogistik byli každý zvlášť spojeny se signifikantně vyšší 1roční mortalitou. Podání klopidogrelu a betablokátoru před zařazením do studie bylo spojeno s vyšší šancí na přežití. Léčba klopidogrelem byla spojena se signifikantně nižší 1roční mortalitou (1,7 % vs 3,6 %, p = 0,023), což bylo způsobeno redukcí mortality ve skupině s tirofibanem, zatímco ve skupině s abciximabem tomu tak nebylo. Ve 30 dnech se vyskytlo úmrtí, IM a nutnost urgentní cílené revaskularizace častěji u skupiny s tirofibanem. Významné krvácení se vyskytlo v obou skupinách stejně, menší krvácení a trombocytopenie byla méně častější ve skupině s tirofibanem. Společný výskyt úmrtí a infarktu myokardu je nižší u pacientů s abciximabem v 6 měsících, zejména u těch s akutním koronárním syndromem. Ve výsledku nebyly zjištěny významné rozdíly v celkové roční mortalitě u pacientů s tirofibanem ve srovnání s abciximabem. Terapie abciximabem byla spojena s 1,5% redukcí výskytu časného infarktu myokardu (vs 5,4 %, p = 0,04), ale vyšší výskyt časných infarktů myokardu v tirofibamové skupině nezpůsoboval vyšší 6měsíční ani roční mortalitu.
Farmakokinetická, farmakodynamická a klinická data s tirofibanemem jakožto inhibitorem GP IIb/IIIa u pacientů, kteří podstoupili PCI, ukazují, že současná dávka léku by mohla být suboptimální a v současnosti jsou testovány vyšší dávky (dosažení inhibice 95% dest. agregace), stejně jako nové kombinace proceduálně používané antikoagulace jako užití clopidogrelu společně s bivalirudinem.
Doručeno do redakce 21. 3. 06
Přijato k otištění po recenzi 17. 4. 06
MUDr. Eva Dvořáková
prof. MUDr. Jindřich Špinar, CSc., FESC
Interní kardiologická klinika
LF MU a FN Brno, pracoviště Bohunice
Zdroje
1.Cleland JGF, Freemantle N, Coletta AP, Clark AL. Clinical trials update from the American Heart Asociation: REPAIR-AMI, ASTAMI, JELIS, MEGA, REVIVE-II, SURVIVE, and PROACTIVE. Eur J Heart Fail 2006; 8 : 105-110.
2.Hotline Sessions of the 27th European Congress of cardiology. Eur Heart J 2005; 6 : 2596-2599.
3.Mukherjee D, Topol EJ, Bertrand ME et al. Mortality at 1 year for the direct comparison of tirofiban and abciximab during percutaneous coronary revascularization: do tirofiban and ReoPro give similar efficacy outcomes at trial 1-year follow-up. Eur Heart J 2005; 26 : 2524-2528.
Štítky
Detská kardiológia Interné lekárstvo Kardiochirurgia Kardiológia
Článek Domácí měření krevního tlaku
Článok vyšiel v časopiseKardiologická revue – Interní medicína
Najčítanejšie tento týždeň
2006 Číslo 1-2- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Intermitentní hladovění v prevenci a léčbě chorob
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Náhlá srdeční smrt: jak jí předcházet
- Skupiny nemocných s akutním infarktem myokardu se zvýšeným rizikem nebo vyžadující specifický léčebný a diagnostický přístup
- Akutní infarkt myokardu u mladých pacientů: etiologie , rizikové faktory, genetika
- Nekompaktní myokard levé komory
- Domácí měření krevního tlaku
- Hypertenze u dětí a adolescentů
- Nefarmakologická léčba arteriální hypertenze
- Zánětlivé a virové kardiomyopatie
- Význam dvourozměrné (2D) echokardiografie v diagnostice hypertrofické kardiomyopatie
- Diagnostické možnosti u postižení periferních tepen.
- Akutní aortální regurgitace v podmínkách Nigerie: kazuistika
- Čtyřcípá aortální chlopeň – vzácný echokardiografický nález: kazuistika
- Onemocnění trikuspidální chlopně
- Buněčná léčba v kardiologii: přehled aktuálních dat za rok 2005
- Charisma – the Clopidogrel for High Atherotrombotic Risk and Ischemic Stabilisation, Management, and Avoidance
- Klinické studie: ukončené, přednesené nebo publikované v poslední době
-
Plicní hypertenze a cor pulmonale
Komentář k poznámkám MUDr. Pavla Jerie - Kardiologická revue 2005;7(4) - 42nd Annual Meeting the Society of Thoracic Surgeons: zpráva (29. 1.-3. 2. 2006, Chicago, USA)
- Kardiologická revue – Interní medicína
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Hypertenze u dětí a adolescentů
- Onemocnění trikuspidální chlopně
- Diagnostické možnosti u postižení periferních tepen.
- Náhlá srdeční smrt: jak jí předcházet
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



