-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Vývoj a implementace metody stanovení volných metanefrinů v plazmě pomocí kapalinové chromatografie s tandemovou hmotnostní detekcí pro rutinní využití v diagnostické laboratoři
Development and implementation of method for analysis of free metanephrines in plasma by the liquid chromatography tandem mass spectrometry for routine use in clinical laboratory.
Objective:
The development and implementation of method for the determination of free metanephrines in plasma by the liquid chromatography tandem mass spectrometry (LC-MS/MS) suitable for routine practice in diagnostic laboratory which overcomes inconveniences related with classical liquid (HPLC) or gas chromatography (GC) and immunoassay approaches, like extensive sample preparation, the step of derivatization or interfering substances.Design:
Analytical method development. Assessment of suitability for routine practice in diagnostic laboratory.Settings:
Department of Clinical Biochemistry – Instrumental methods section, Spadia lab, a.s., Dr. Slabihoudka 6232/11, 708 52 OstravaMaterial and Methods:
Method development and validation were performed on Agilent 6490 Triple Quadrupole LC-MS/MS system. Chromatographic separation was achieved on SeQuant®ZIC®HILIC HPLC 3,5 µm, 100Å, PEEK 100 x 2,1 mm metal-free HPLC Column (Merck KGaA, Germany) by gradient elution. For determination of analytical parameters lyophilised plasma calibrators (purchased from RECIPE Chemicals and Instruments GmbH, Germany) and controls (purchased from Recipe Chemicals and Instruments GmbH and Chromsystems Instruments α Chemicals GmbH, Germany) were used. The study included 40 patients with diagnosis arterial hypertension.Results:
The analytical performance of the new developed method is satisfactory. The intra-assay and inter-assay coefficients of variation (CV) were below 10 %. Recoveries determined by standard addition were from 89 to 98 %. The limit of quantification for MN was 0.035 nmol/l, for NMN was 0.049 nmol/l. This method fulfilled requirements for validation parameters for both analytes. Comparison of three methods for quantification of free metanephrines in plasma was performed – 2-MET Plasma ELISAFast Track (Labor Diagnostika Nord GmbH, Germany), FEO Kit (VUOS a.s., Czech Republic) dedicated for HPLC-ECD systems and developed LC-MS/MS method. Statistical analysis was performed using the MedCalc 16.1 (Medcalc Software bvba, Belgium) using the Passing Bablok regression.Conclusions:
Neuroendocrine tumors represent a clinically and etiologically diverse group of disorders. Neuroendocrine tumors, such as pheochromocytomas or paragangliomas, exhibit a persistent or pyroxysmal excessive catecholamines production. 3-O-methylated catecholamine metabolites, metanephrine (MN) and normetanephrine (NMN), are prioritized for diagnosis of pheochromocytoma due to their highest diagnostic sensitivity and specificity. Presented LC-MS/MS method overcomes classical HPLC and immunoassay approaches. Method provides simple step of sample preparation, short runtime and required analytical parameters.Keywords:
free plasma metanephrines, pheochromocytoma, LC-MS/MS.
Autori: M. Rajská; P. Procházková; D. Bartoníková; L. Weiperová; P. Loučka; J. Minář; M. Radina
Pôsobisko autorov: Spadia lab, a. s., Dr. Slabihoudka 6232/11, 708 52 Ostrava
Vyšlo v časopise: Klin. Biochem. Metab., 24, 2016, No. 4, p. 191-197
Súhrn
Cíle studie:
Vývoj a implementace metody stanovení volných metanefrinů v plazmě pomocí kapalinové chromatografie s tandemovou hmotnostní detekcí (LC-MS/MS) pro rutinní použití v diagnostické laboratoři, která eliminuje omezení klasické kapalinové (HPLC) nebo plynové chromatografie (GC) a imunoanalytických metod, jako jsou náročná příprava vzorků, derivatizace a interferující substance.Typ studie:
Vývoj analytické metody. Posouzení vhodnosti pro rutinní použití v diagnostické laboratoři.Název a sídlo pracoviště:
Laboratoř klinické biochemie – Oddělení instrumentálních metod, Spadia lab, a.s., Dr. Slabihoudka 6232/11, 708 52 Ostrava.Materiál a metody:
Vývoj a validace metody byly provedeny na LC-MS/MS systému Agilent 6490 Triple Quadrupole. Pro chromatografickou separaci byla použita kolona SeQuant®ZIC®HILIC HPLC 3,5 mm, 100Å, PEEK 100 x 2,1 mm metal-free (Merck KGaA, Německo) a gradientová eluce. Pro stanovení analytických parametrů metody byly použity lyofilizované kalibrační a kontrolní materiály z firmy Recipe Chemicals and Instruments GmbH (Německo) a Chromsystems Instruments α Chemicals GmbH (Německo). Do studie bylo zařazeno 40 pacientů s diagnózou arteriální hypertenze.Výsledky:
Analytické parametry nově vyvinuté metody jsou vyhovující. Variační koeficienty (CV) preciznosti v sérii a mezilehlá preciznost se pohybovaly pod 10 %. Výtěžnost, určená metodou standardního přídavku se pohybovala v rozmezí 89 až 98 %. Limit stanovitelnosti pro MN byl 0,035 nmol/l, pro NMN 0,049 nmol/l. Metoda splňuje požadavky validace pro oba analyty. Bylo provedeno srovnání tří metod stanovení volných metanefrinů v plazmě: 2-MET Plasma ELISAFast Track (Labor Diagnostika Nord GmbH, Něměcko), HPLC metoda s elektrochemickou detekcí (ECD) a komerčně dodávaná diagnostická souprava FEO Kit (VUOS a.s., Česká republika) a nově vyvinutá LC-MS/MS metoda. Statistická analýza byla provedena pomocí programu MedCalc 16.1 (Medcalc Software bvba, Belgie) s využitím Passing Bablokovy regresní analýzy.Závěr:
Neuroendokrinní tumory představují heterogenní skupinu onemocnění s různou klinickou symptomatologií a etio-patogenezí. Neuroendokrinní tumory, jako jsou feochromocytom nebo paragangliom, vykazují setrvalou nebo paroxyzmální nadměrnou produkci katecholaminů. Jejich 3-O-methylované metabolity, metanefrin (MN) a normetanefrin (NMN), jsou preferovány pro diferenciální diagnostiku feochromocytomu vzhledem k jejich vysoké diagnostické senzitivitě a specificitě. Prezentovaná LC-MS/MS metoda eliminuje nevýhody klasických chromatografických technik a imunoanalytických metod, přičemž zásadními aspekty jsou: jednoduchá příprava vzorku, krátká doba analýzy a požadované analytické parametry.Klíčová slova:
volné plazmatické metanefriny, feochromocytom, LC-MS/MS.Úvod
Neuroendokrinní tumory představují heterogenní skupinu onemocnění s různou klinickou symptomatologií a etiopatogenezí. Neuroendokrinní tumory, které pocházejí z chromafinní tkáně sympatického nebo parasympatického nervového systému, jako jsou feochromocytom nebo paragangliom, vykazují setrvalou nebo paroxyzmální nadměrnou produkci katecholaminů. Jejich 3-O-methylované metabolity, metanefrin (MN) a normetanefrin (NMN), jsou preferovány pro diferenciální diagnostiku feochromocytomu vzhledem k jejich vysoké diagnostické senzitivitě a specificitě [1, 3, 5]. Pokud je feochromocytom správně diagnostikován, může být úspěšně odstraněn a vyléčen až v 90 % případů [2]. V případě, že tyto tumory nejsou diagnostikovány, mohou mít fatální následky pro lidský organismus a končit smrtí v důsledku maligní hypertenze, srdečního selhání, infarktu myokardu, arytmií, cévní mozkové příhody nebo metastáz. Včasná diagnostika, založená na biochemickém průkazu nadprodukce katecholaminů a jejich metabolitů, má proto zcela zásadní význam [2].
V laboratorní diagnostice jsou pro stanovení volných plazmatických metanefrinů využívané metody klasické kapalinové chromatografie s následnou spektrofotometrickou, fluorescenční či elektrochemickou (ECD) detekcí, metody plynové chromatografie nebo imunoanalytické metody. Tyto metody mají mnoho nevýhod a omezení, jako je např. náročná příprava vzorku a dlouhý čas analýzy u HPLC metod, nutný krok derivatizace u GC metod či interferující substance u imunoanalytických metod [1, 4].
Cílem této práce byl vývoj metody stanovení volných metanefrinů v plazmě pomocí kapalinové chromatografie ve spojení s tandemovou hmotnostní spektrometrií (LC-MS/MS), která eliminuje výše uvedená omezení a následná implementace metody do rutinní praxe v diagnostické laboratoři.
Materiál a metoda
Soubor pacientů
Do studie bylo zařazeno 40 pacientů s diagnózou arteriální hypertenze. K definování analytických parametrů metody byly použity jak lyofilizované komerčně dostupné materiály, tak vzorky pacientů. 20 pacientských vzorků a kontrolní materiály byly využity při vývoji metody a pro stanovení analytických parametrů LC-MS/MS metody, dalších 20 pacientských vzorků a čtyři kontrolní vzorky byly využity pro stanovení koncentrací MN a NMN za účelem srovnání tří různých metod.
Volné metanefriny u osmi pacientských vzorků a u tří kontrolních materiálů byly stanoveny pomocí tří odlišných metod – ELISA, HLPC s ECD detekcí a LC-MS/MS (Tabulka 1, n=11). U dalších 12 pacientských vzorků a 1 kontrolního vzorku bylo stanovení provedeno pouze pomocí chromatografických metod (Tabulka 2, n=24). Pro statistickou analýzu dat byl použit statistický program MedCalc 16.1 (Medcalc Software bvba, Belgie).
Tab. 1. The parameters of statistical analysis for FEO and ELISA methods 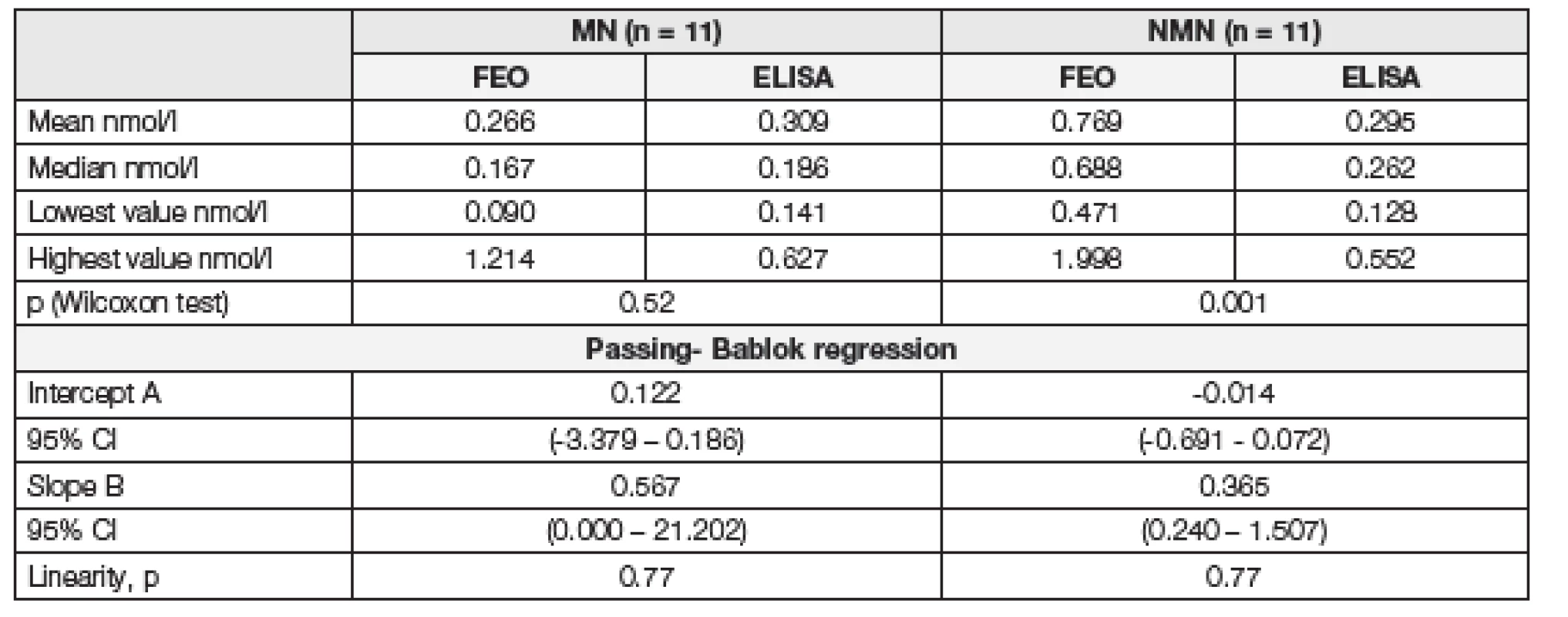
Tab. 2. The parameters of statistical analysis for FEO and LC-MS/MS methods 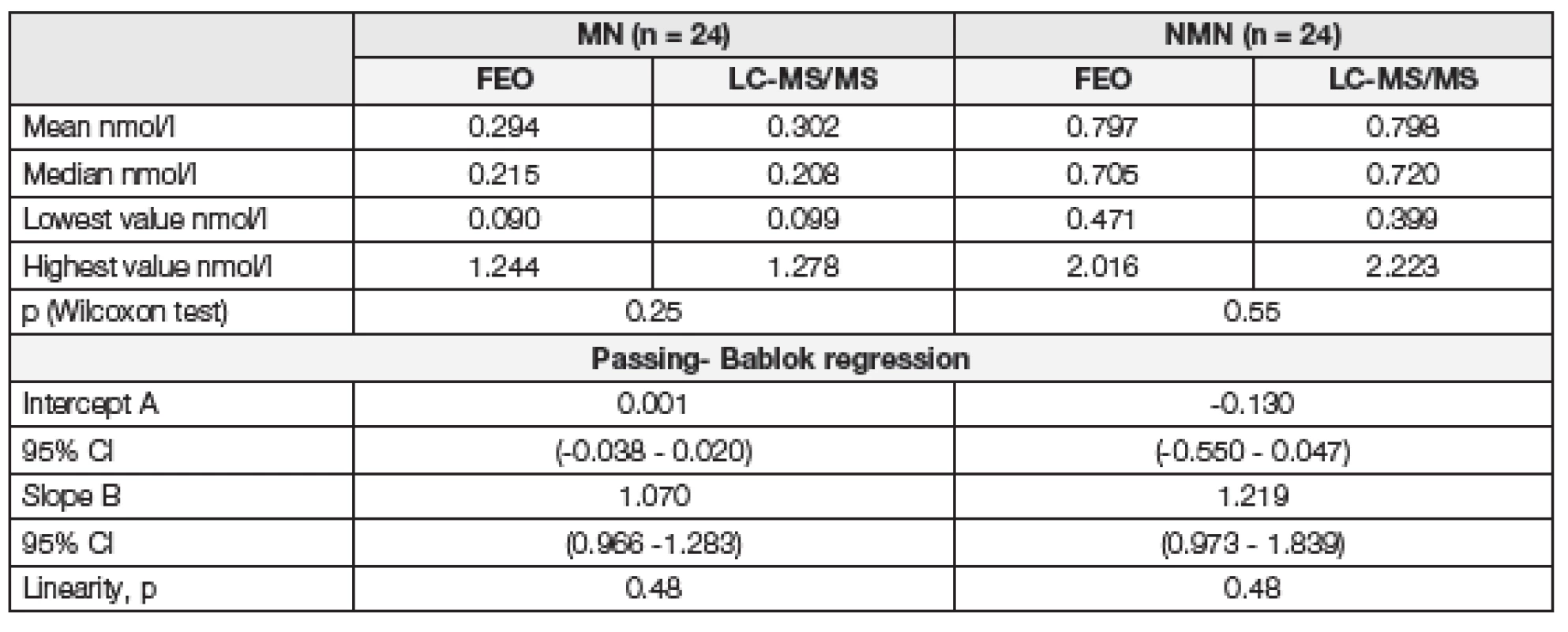
Chemikálie
Lyofilizované kalibrátory ClinCal®Serum Calibrator Set for Metanephrines (RECIPE Chemicals and Instruments GmbH, Německo) a kontroly (ClinChek®Serum Control for Metanephrines RECIPE Chemicals and Instruments GmbH, Germany a Endocrine Plasma Controls Chromsystems Instruments α Chemicals GmbH, Německo), interní standardy - Metanephrine-d3, Normetanephrine-d3 (Sigma-Aldrich, USA), rozpouštědla - isopropanol (Sigma-Aldrich, USA), acetonitril, methanol, voda (Vitrum VWR, Česká republika).
Přístrojové vybavení
LC-MS/MS systém - Agilent Technologies 1290 Infinity kapalinový chromatograf ve spojení s tandemovým hmotnostním spektrometrem Agilent Technologies 6490 Triple Quadrupole, MRX Microplate Reader (Dynex), Coulochem III HPLC Systém (ESA Biosciences Inc., USA), Eppendorf Centrifuge 5804R, Eppendorf Centrifuge 5424.
Zpracování vzorků
Před odběrem periferní žilní krve bylo potřeba dodržet speciální dietní opatření, z jídelníčku bylo nutné vyřadit potraviny bohaté na tyrosin - banány, ořechy, sýr. Pokud je to možné, po konzultaci s ošetřujícím lékařem, bylo nutné vysazení některých léčiv: alfa-methyldopa a jiná centrálně působící antihypertenziva, lokální anestetika, inhibitory MAO, antiarytmika. Vyšetření také ovlivňují alkohol, benzodiazepiny, opioidy apod. [5, 6]. Odběr byl proveden do odběrové soupravy s antikoagulačním činidlem EDTA v souladu s pokyny pro preanalytickou fázi [7]. Po odběru byla krev centrifugována 10 min při 4000 g a získaná plazma byla do provedení analýzy uchována při -20 °C. Před analýzou byla plazma temperována na laboratorní teplotu.
LC-MS/MS analýza
K 200 µl vzorku (kalibrátoru, kontroly, plazmy) bylo přidáno 50 µl interního standardu (0,25 ng MN-d3 a 0,25 ng NMN-d3) a krátce promícháno na vortexu. Vzorky byly precipitovány v 1 ml isopropanolu, 30 sec míchány na vortexu a následně centrifugovány 10 min při 13 000 g. 1 ml supernatantu byl převeden do čisté skleněné zkumavky a pod mírným proudem dusíku odpařen. Po rekonstituci ve 100 µl ACN/H2O (90 : 10) byly vzorky centrifugovány 10 min při 13 000 g. K současnému stanovení volných metanefrinů (metanefrinu a normetanefrinu) v plazmě bylo pro nástřik k LC-MS/MS analýze použito 5 µl supernatantu.
Pro analýzu byla použita kolona SeQuant®ZIC®HILIC HPLC 3,5 mm, 100Å, PEEK 100 x 2,1 mm metal-free HPLC Column (Merck, Německo) a analyty byly separovány gradientovou elucí mobilních fází A (50 mM vodný roztok NH4COOH) a B (acetonitril) při průtokové rychlosti 0,3 ml/min a teplotě 45 °C s následnou hmotnostní detekcí (parametry iontového zdroje a MRM přechody – Tabulka 3). Celková doba analýzy byla 6 min a retenční časy separovaných analytů byly 2,4 min pro MN a 2,6 min pro NMN (obr. 1).
Tab. 3. Mass spectrometry and mass transition conditions. (*quantifier) 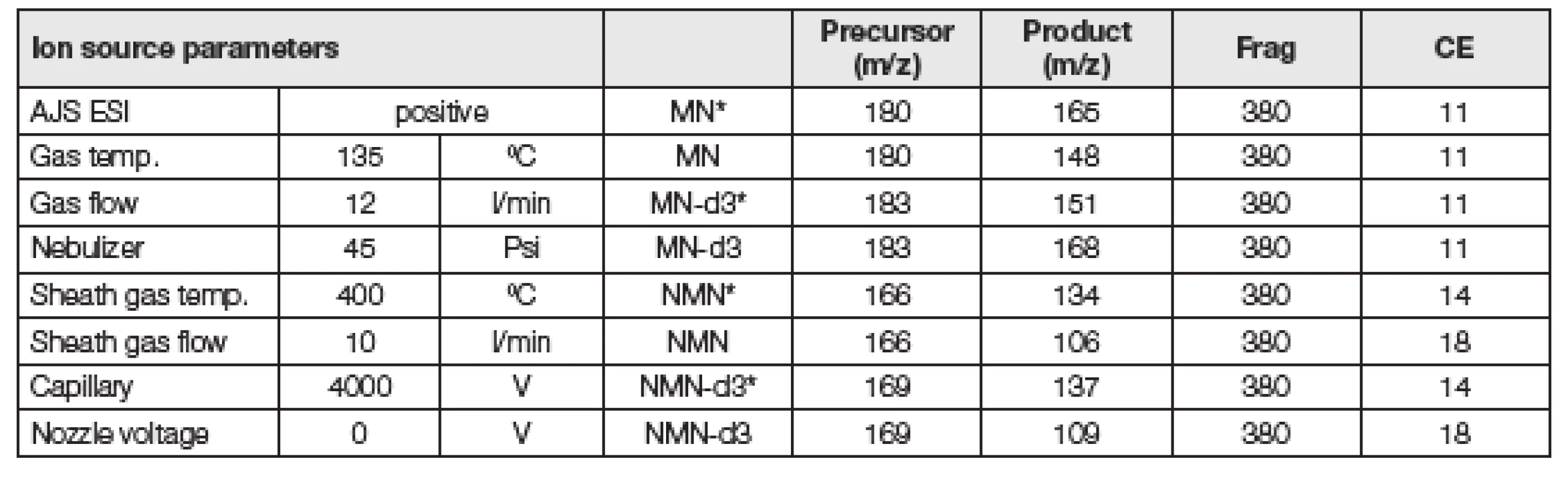
Fig. 1. Chromatogram of MN and NMN. 
Fig. 2.: Graphical representation of measured values obtained by FEO Kit and 2-MET Plasma ELISA<sup>Fast Track</sup>. 
Komerčně dostupné metodiky – IVD diagnostické kity
U komerčních metod bylo postupováno podle návodů v příbalových letácích k IVD diagnostickým kitům 2-MET Plasma ELISAFast Track (Labor Diagnostika Nord GmbH, Německo) s následnou fotometrickou detekcí (MRX Microplate Reader) a FEO Kit (VUOS a.s., Česká republika) s následnou elektrochemickou detekcí (Coulochem III HPLC Systém, ESA Biosciences Inc., USA).
Výsledky
Vyvinutá metoda stanovení volných metanefrinů v plazmě pomocí kapalinové chromatografie ve spojení s tandemovou hmotnostní spektrometrií (LC-MS/MS) poskytla vyhovující analytické parametry pro oba analyty. Rozsah kalibrace pro metanefrin byl 0,035 – 7,175 nmol/l s limitem kvantifikace 0,035 nmol/l (CV = 4,8 %). Rozsah kalibrace pro normetanefrin byl 0,049 – 9,956 nmol/l s limitem kvantifikace 0,049 nmol/l (CV = 6,7 %). Limit kvantifikace byl stanoven experimentálně měřením postupně ředěného kontrolního materiálu a určením nejnižší hodnoty, při které bylo dosaženo CV<20 % (za podmínek opakovatelnosti) a výtěžnosti ± 20 %. Výtěžnost, určená metodou standardního přídavku se pohybovala v rozmezí 89 – 98 %. Variační koeficienty (CV) preciznosti v sérii a mezilehlé preciznosti se pohybovaly pod 10 %. Pro určení preciznosti v sérií (intraassay precision) byl použit pool pacientských vzorků (počet stanovení n=12), pro určení mezilehlé preciznosti (interassay precision) byly použity kontrolní materiály ClinChek® for Metanephrines (počet stanovení n=20), viz. Tabulka 4.
Tab. 4. Intraassay and interassay precision 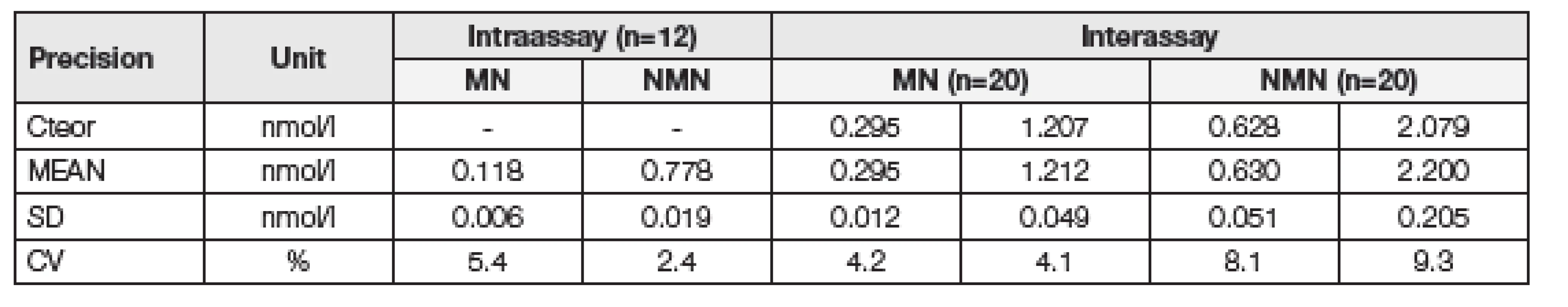
Pro posouzení vhodnosti vyvinuté metody pro rutinní použití v diagnostické laboratoři bylo provedeno srovnání dříve používané metodiky 2-MET Plasma ELISAFast Track a nově vyvinuté LC-MS/MS metody s komerčně dostupnou metodikou FEO Kit s ECD detekcí. Pro statistickou analýzu dat byl použit statistický program MedCalc 16.1. Základní statistické parametry všech srovnávaných skupin jsou uvedeny v Tabulce 1 a Tabulce 2. Byla testována normalita rozložení dat testem D’Agostino-Pearson test s výsledkem zamítnutí normality dat a pro další porovnání byl využit neparametrický Wilcoxonův test. Dále byly výsledky statisticky zpracovány Passing-Bablokovou neparametrickou regresí (Obr. 4) a Bland-Altmanovým diagramem na srovnání metodik (Obr. 6). Pro grafickou vizualizaci rozložení dat byl použit box-and-whisker graf (Obr. 3 a 5).
Fig. 3.: Box-and-whisker graphs of FEO Kit and 2-MET Plasma ELISA<sup>Fast Track</sup>. 
Fig.4.: Passing-Bablok regression – comparison of FEO kit and LC-MS/MS. 
Fig. 5.: Box-and-whisker graphs of FEO Kit and LC-MS/MS. 
Fig. 6.: Blandt-Altman difference graph for FEO Kit and LC-MS/MS 
Srovnání metodik FEO kit a 2-MET Plasma ELISAFast Track
Metanefrin a normetanefrin v plazmě
Jako referenční metoda byla použita metodika FEOkit. Výsledky vyhodnocení Passing-Bablokovou regresí jsou uvedeny v Tabulkách 1 a 2. V případě úseku A, pro MN i NMN, zahrnuje 95% interval spolehlivosti 0, což poukazuje na nepřítomnost systematické chyby měřícího systému. V případě směrnice B, pro MN i NMN, zahrnuje 95% interval spolehlivosti 1, což vylučuje přítomnost proporcionální chyby měření. Ke stejnému závěru jsme došli pomocí Wilcoxonova párového testu pro MN (p=0,52). Pro normetanefrin Wilcoxonův párový test poukázal na statisticky významný rozdíl mezi srovnávanými metodami (p=0,001).
I přes uvedené skutečnosti je patrné, že pro validní posouzení shody těchto metod na základě výše uvedených statistických testů byl k dispozici malý počet dat, n=11. Po pečlivé vizuální analýze dat je patrné (viz. Tabulka 3, Obr. 2. a Obr. 3.), že minimální a maximální hodnoty koncentrace a interval mezi 1. a 3. kvartilem pro výsledky stanovené metodikou FEO Kit a metodikou 2-MET Plasma ELISAFast Track se významně liší. Metodika 2-MET Plasma ELISAFast Track neumožňuje správné zachycení zvýšených hladin normetanefrinu v plazmě.
Srovnání metodik FEO kit a vyvinuté LC-MS/MS metody
Metanefrin a normetanefrin v plazmě
Pro srovnání chromatografických metod byl použit větší soubor vzorků (n=24). Jako referenční metoda byla použita metodika FEOkit. Výsledky vyhodnocení Passing-Bablokovou regresí jsou uvedeny v Tabulce 2. V případě úseku A, pro MN i NMN, zahrnuje 95% interval spolehlivosti 0, což vylučuje přítomnost systematické chyby měřícího systému v celém rozsahu měření. V případě směrnice B, pro MN i NMN, zahrnuje 95% interval spolehlivosti 1, což vylučuje přítomnost proporcionální chyby měření. K posouzení rozdílů mezi výsledky byl použit diferenční Bland-Altmanův graf (Obr. 6). Při pohledu na graf vidíme, že hodnoty jsou rovnoměrně rozloženy a neprojevuje se trend, který by signalizoval přítomnost systematické chyby (pro metanefrin jeden odlehlý bod, pro normetanefrin dva odlehlé body). 95% interval spolehlivosti průměru diferencí zahrnuje 0, z čehož vyplývá, že mezi metodami není statistický rozdíl. Ke stejnému závěru jsme došli pomocí Wilcoxonova párového testu (p=0,25 pro MN, p=0,55 pro NMN). Grafická vizualizace rozložení dat pomocí box-and-whisker grafu (Obr. 5) výsledky výše uvedené statistické analýzy podporuje.
Závěr
Včasná diagnostika feochromocytomu je zcela zásadní pro léčbu a chirurgickou intervenci. Diagnostický algoritmus neuroendokrinních tumorů je založen na několika aspektech: klinická symptomatologie, laboratorní diagnostika a zobrazovací techniky. Laboratorní průkaz nadprodukce katecholaminů a/nebo jejich metabolitů tumorem je limitován řadou faktorů: zvýšení hladin katecholaminů, které nemusí být specifické pro feochromocytom (produkce sympatickým nervovým systémem), přítomnost „němých“ feochromocytomů nebo epizodické vylučování katecholaminů. 3-O-methylované metabolity katecholaminů, metanefrin (MN) a normetanefrin (NMN), jsou preferovány pro diferenciální diagnostiku feochromocytomu vzhledem k jejich vysoké diagnostické senzitivitě a specificitě. Nádorové buňky uvolňují volné metanefriny plynule a nezávisle na produkci katecholaminů [2,4].
Cílem prezentované práce byl vývoj analytické metody a posouzení vhodnosti pro rutinní použití v diagnostické laboratoři. K přednostem prezentované metody patří relativně nenáročná příprava vzorků, krátký čas analýzy a splněné požadované analytické parametry. Příprava vzorků je založena na precipitaci proteinů isopropanolem a následném odpaření pod proudem dusíku, nevyžaduje extrakci na tuhé fázi [3]. Limitací prezentované metody je skutečnost, že i když separace analytů je dosažena použitím 5 min gradientu, před nástřikem dalšího vzorku je kolonu nutné ekvilibrovat 80% mobilní fází B, aby se předešlo ztrátě intenzity píku normetanefrinu. Prezentovaná LC-MS/MS metoda splňuje požadavky kladené na analytické parametry a statistická analýza provedená pomocí Passing-Bablokovy regrese a Bland-Altmanových diagramů pro srovnání s referenční metodikou (FEO Kit) potvrdila vhodnost použití tohoto postupu pro stanovení volných metanefrinů v plazmě v rutinní diagnostické laboratoři. Metoda eliminuje nevýhody klasické HPLC metody s ECD detekcí, tj. především náročná příprava vzorku a dlouhý čas analýzy (50 min). Metoda rovněž eliminuje omezení imunoanalytických metod, jako jsou interferující substance a falešně negativní výsledky. Statistická analýza a srovnání metodiky 2-MET Plasma ELISAFast Track s referenční metodou FEO Kit ukazuje na významnou rozdílnost mezi hodnotami stanovenými pomocí ELISA a pomocí chromatografických metod.
Do redakce došlo 24. 3. 2016
Adresa pro korespondenci
Mgr. Magdalena Rajska
Dr. Slabihoudka 6232/11
708 52 Ostrava
e-mail: magdalena.rajska@spadia.cz
Zdroje
1. de Jong, W., de Vries, E., Kema, I. P. Current status and future developments of LC-MS/MS in clinical che-mistry for quantification of biogenic amines. Clinical Biochemistry, 2011, 44, p. 95 – 103
2. Marney, L. C., Laha, T. J., Baird, G. S., Rainey, P. M., Hoofnagle, A. N. Clinical Chemistry, 2008, 54 : 10, p. 1729 – 1732
3. Cryer, P. E. Pheochromocytoma. West. J. Med., 1992, 156: p. 399-407
4. Stejskal, D., Lačňák, B., Václavík, J., Zuber, R. Volné plazmatické metanefriny a jejich využití v diagnostice feochromocytomu. Klin. Biochem. Metab., 2005, 13 (34), No. 4, p. 201 - 206
5. Brabcova Vrankova, A., Portychova, L., Nyvltova, Z., Widimsky, J., Zelinka, T., Škrka, J., Horna, A. Vývoj nového kitu pro stanovení volných plazmatických metanefrinů. Sborník přednášek mezinárodní odborné konference XXXV. Moderní Elektrochemické Metody 2015, s. 13 – 16.
6. Mayo Clinic. Metanephrines, Fractionated, Free, Plasma [online]. UK, Rochester, MN 55901, 1995-2016 [cit. 2016-01-11]
7. Ministerstvo zdravotnictví České republiky, Číselníky dasta, Metanefrin (P; látková konc. [nmol/l] chromatografie-HPLC) [online]. ČR, Palackého nám. 375, Praha 2, 128 00, [cit. 2016-01-16]. Dostupné z: http://ciselniky.dasta.mzcr.cz/CD/hypertext/_KOMP_201512140902METANEPH.htm#_TAB_P_METANEPH_HPLC
Štítky
Biochémia Nukleárna medicína Nutričný terapeut
Článek Nové trendy v imunochemii
Článok vyšiel v časopiseKlinická biochemie a metabolismus
Najčítanejšie tento týždeň
2016 Číslo 4
-
Všetky články tohto čísla
- Jubilanti roku 2016 a časopis Klinická biochemie a metabolismus
- Nové trendy v imunochemii
- Variabilita mezi šaržemi reagencií a kalibrátorů a její důsledky pro verifikaci měření
- Porovnání stanovení katalytické koncentrace ALP rutinní metodou ALP (Roche Diagnostics) a metodou Alkalická fosfatáza (BLW Diagnostics)
- Soubor nově diagnostikovaných monoklonálních gamapatií v regionální laboratoři v osmiletém časovém období
- Preciznost a bias metod měření dle EP15-A3
- Vývoj a implementace metody stanovení volných metanefrinů v plazmě pomocí kapalinové chromatografie s tandemovou hmotnostní detekcí pro rutinní využití v diagnostické laboratoři
- Metabolismus bilirubinu a jeho biologické účinky
- Rejstřík autorů + klíčová slova
- Klinická biochemie a metabolismus
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Preciznost a bias metod měření dle EP15-A3
- Metabolismus bilirubinu a jeho biologické účinky
- Nové trendy v imunochemii
- Porovnání stanovení katalytické koncentrace ALP rutinní metodou ALP (Roche Diagnostics) a metodou Alkalická fosfatáza (BLW Diagnostics)
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy








