-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Pacientka se třemi EGFR mutacemi – postupný rozvoj rezistence na předchozí cílenou léčbu
Patient with Three EGFR Mutations – Gradual Development of Resistance to Previous Targeted Treatment
Background:
Patients with sensitive EGFR mutations are already being treated with first and second generation tyrosine kinase inhibitors (TKIs). However, resistance to these drugs occurs over time, and over half of all cases is caused by a mutation (T790M) in the EGFR kinase domain. Osimertinib offers a new treatment option that overcomes this problem. Unfortunately, resistance to this drug also develops after several months of treatment and is caused by another mutation (C797S) in EGFR.Case report:
Our case report provides evidence for the progressive development of EGFR-TKI resistance in a patient with a deletion of exon 19 in the EGFR gene. First, based on a mutation (T790M) identified after afatinib treatment and a subsequent mutation (C797S) mutation identified after osimertinib treatment. We mention overcoming this resistance (C797S) mutation by using 4th generation EGFR-TKI and other alternative procedures (chemotherapy, immunotherapy, and combinations of older EGFR-TKI generations). We also mention a rare case of peritoneal metastasis that occurred after previous treatment with osimertinib that we attempted to ameliorate by using erlotinib because the impaired condition of the patient did not allow treatment by chemotherapy. There are documented cases in which erlotinib has been successfully given to patients with peritoneal metastases and patients with the EGFR mutation C797S following progression to afatinib. This was not the case in our patient, probably because of the remaining EGFR mutation T790M.Conclusion:
In our case report, erlotinib did not show efficacy after progression to osimetinib. Nowadays, chemotherapy is the only possible treatment in patients with good a performance status. The next-generation of TKIs are undergoing promising developments.Key words:
EGFR – deletion on exon 19 – mutation T790M – mutation C797S – afatinib – osimertinibSubmitted:
12. 9. 2017Accepted:
12. 10. 2017
This project was supported by grant AZV 17-30 748A.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE recommendation for biomedical papers.
Autori: Martin Svatoň 1; Miloš Pešek 1; Jan Baxa 2; Petr Mukenšnabl 3; Lucie Benešová 4; Marek Minárik 4,5
Pôsobisko autorov: Klinika pneumologie a ftizeologie LF UK a FN Plzeň 1; Klinika zobrazovacích metod LF UK a FN Plzeň 2; Šiklův ústav patologie, LF UK a FN Plzeň 3; Genomac výzkumný ústav, s. r. o. 4; Katedra analytické chemie, PřF UK v Praze 5
Vyšlo v časopise: Klin Onkol 2018; 31(1): 53-58
Kategória: Kazuistika
doi: https://doi.org/10.14735/amko201853Súhrn
Východiska:
Pacienti se senzitivními EGFR mutacemi jsou již standardně léčeni tyrozinkinázovými inhibitory (TKI) 1. a 2. generace. Nicméně na tyto preparáty vzniká po čase rezistence, která je u více než poloviny případů zapříčiněna EGFR rezistentní mutací T790M. Osimertinib je nová léčebná možnost, jak ji překonat. Bohužel i na tento preparát po několika měsících léčby vzniká rezistence. Jednou z jejích příčin je EGFR mutace C797S, o které pojednává naše kazuistika.Případ:
Naše kazuistické sdělení přináší průkaz postupného vývoje rezistence k EGFR-TKI u pacientky s delecí na exonu 19 genu EGFR. Nejprve na základě získané mutace T790M při léčbě afatinibem a posléze na podkladě mutace C797S při terapii osimertinibem. Též se věnujeme úvahám o překonání této rezistentní mutace jak pomocí EGFR-TKI 4. generace, tak i případnými alternativními postupy (chemoterapie, imunoterapie, kombinace EGFR-TKI starších generací). Rovněž zmiňujeme vzácný případ nemocné s metastázami na peritoneu po předchozí léčbě osimertinibem. Tento nepříznivý stav jsme se vzhledem k již zhoršenému výkonnostnímu stavu nemocné pokusili ovlivnit erlotinibem, který neumožňoval podání chemoterapie. Jsou doložené případy, kdy erlotinibem byli úspěšně léčeni pacienti s peritoneálními metastázami a též nemocní s EGFR mutací C797S po progresi na afatinibu. To však v našem případě nenastalo, patrně pro přetrvávající EGFR mutaci T790M.Závěr:
V naší kazuistice erlotinib nejevil účinnost po progresi na osimertinibu. Jedinou možnou léčbou se v tomto případě prozatím jeví chemoterapie u pacientů v dobrém klinickém stavu. TKI nové generace procházejí nadějným vývojem.Klíčová slova:
EGFR – delece na exonu 19 – mutace T790M – mutace C797S – afatinib – osimertinibÚvod
Cílená léčba přinesla v posledních letech výrazné prodloužení doby přežití i zlepšení kvality života pacientů s generalizovanými plicními adenokarcinomy [1]. Prvními cílenými preparáty byly tyrozinkinázové inhibitory (TKI) mířící na mutovaný gen EGFR [1]. Jejich nedostatkem byla jednak horší citlivost na tzv. vzácné EGFR mutace, jednak postupný rozvoj rezistence do obvykle 1 roku léčby [2,3]. Toto se snažil překonat afatinib, TKI 2. generace, který díky ireverzibilní vazbě na EGFR prokázal o něco nadějnější výsledky ve srovnání s 1. generací [2,4]. Nicméně ani u něj se nepodařilo zabránit rozvoji rezistence, zejména v souvislosti s mutací T790M [5]. Tuto překážku překonal až osimertinib, TKI 3. generace, ale i u něj se rozvíjí postupem času rezistence k léčbě [6]. Jednou z možností je i EGFR mutace C797S. O tomto případu pojednává i naše sdělení. Dle našich znalostí jde o první publikovanou práci o prokázané rezistenci k osimertinibu na podkladě mutace C797S v ČR.
Kazuistika
Dvaačtyřicetiletá žena, exkuřačka (celkem cca 10 krabičkoroků), vyjma kožní formy psoriázy vážněji nestonající, se dostavila v září 2015 na Kliniku pneumologie a ftizeologie FN Plzeň pro námahovou dušnost, subfebrilie, kašel s mírnou hemoptýzou a bolestí na pravém boku. Vzhledem k elevaci zánětlivých parametrů a vstupnímu skiagramu plic bylo zprvu uzavíráno jako oboustranná pneumonie s pravostranným výpotkem. Ten byl punktován a byla zahájena empirická antibiotická terapie, též byla nastavena symptomatická léčba přidružených obtíží. Nález na skiagramu plic se však nelepšil, v mezidobí byly z výpotku charakteru exsudátu cytologicky určeny atypické buňky, kdy k vyloučení malignity bylo doporučeno provedení cytobloku. Pro recidivující výpotek byla následně provedena hrudní drenáž. V cytobloku byl popsán adenokarcinom plicního původu (obr. 1) s geneticky prokázanou EGFR delecí na exonu 19 (Glu746_Ala750del), KRAS mutace ani ALK translokace nebyly prokázány. V rámci stagingu bylo doplněno PET/CT, kde byl popsán rozsáhlý, metabolicky aktivní infiltrát tumorózního vzhledu v horním a středním laloku pravé plíce s oboustrannými plicními a pleurálními metastázami, dále postižení oboustranných hilových, mediastinálních a krčních uzlin a suspektní metastáza v játrech. Bronchoskopicky byly prokázány extramurální stenózy odstupů pravého horního a středního bronchu. Z odebraných vzorků byl potvrzen plicní adenokarcinom. Následně bylo přistoupeno k talkáži pravé pohrudniční dutiny. Onemocnění bylo stážováno jako T4N3M1b, stadium IV, stav výkonnosti nemocné ECOG PS 1 (Eastern Cooperative Oncology Group performance status).
Obr. 1. A. Výrazně buněčný řez z cytobloku s četnými buňkami adenokarcinomu plic buď jednotlivými nebo tvořícími dilatované tubulární a papilární struktury (barvení hematoxylin eozin). B. Imunohistochemický průkaz TTF 1 v buňkách plicního adenokarcinomu. C. Imunohistochemický průkaz cytokeratinu 7 v buňkách plicního adenokarcinomu. D. Imunohistochemický průkaz napsinu A v buňkách plicního adenokarcinomu. 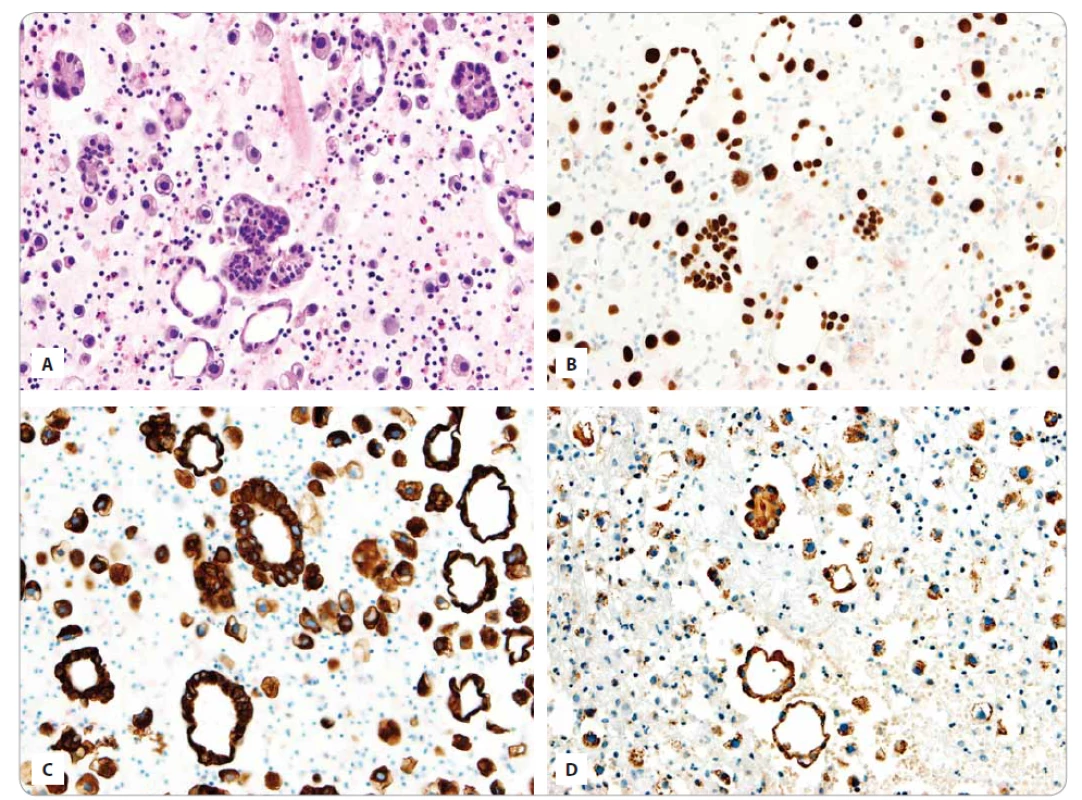
TTF 1 – tyreoidní transkripční faktor 1 V říjnu 2015 byla zahájena léčba afatinibem. Již po měsíci léčby došlo k částečné regresi nálezu na skiagramu plic i subjektivnímu zlepšení bolestí na hrudi (s možností vysazení silného opiátu) a námahové dušnosti. Z nežádoucích účinků (NÚ) léčby se objevil lehký průjem (stupně 1–2) a vyrážka (stupně 2). Částečná regrese tumoru byla potvrzena i následným CT vyšetřením (regrese primárního tumoru, lymfadenopatie neregistrována, metastázy stacionárního vzhledu). Průjmy byly účinně korigovány loperamidem, pro trvající vyrážku a nově vzniklá paronychia na dvou prstech horních končetin (stupně 2) byla nabrána hladina afatinibu, která byla v normě. Obtíže proto byly řešeny symptomaticky ve spolupráci s Dermatovenerologickou klinikou FN Plzeň s dobrým efektem nastavené medikace a laserového ošetření paronychií. Kontrolní CT v květnu 2016 dle kritérií RECIST bylo hodnoceno jako ještě stabilní onemocnění, bylo proto pokračováno v léčbě afatibem až do července 2016. Tehdy CT již prokázalo jednoznačnou progresi nálezu dle RECIST kritérií, navíc se zhoršily i popisované obtíže nemocné, afatinib byl vysazen, doba do progrese onemocnění (progression-free survival – PFS) dosáhla 8 měsíců.
Byla provedena kontrolní bronchoskopie s rebiopsií ze stenotických odstupů pravého horního bronchu. Geneticky byla prokázána jak původní EGFR delece na exonu 19, tak nově i rezistentní mutace T790M na exonu 20. Terapie osimertinibem však nebyla v této době v ČR dostupná, a proto byla zahájena 2. linie léčby pomocí chemoterapie pemetrexedem. K další progresi nálezu ale došlo již koncem srpna 2016, kdy nejenže se objevila atelektáza středního laloku při progresi primární tumorózní infiltrace, ale byly patrné i nové plicní metastázy (obr. 2). Navíc došlo k zvýraznění bolestí nemocné a váhovému úbytku (o 2,5 kg) při nechutenství pacientky, léčba byla dále komplikována rozvojem parézy nervus peroneus vlevo. Terapie pemetrexedem byla proto ukončena, neurolog doporučil rehabilitační cviky, váhový úbytek byl korigován sippingem.
Obr. 2. CT nález s progresí onemocnění při ukončení terapie pemetrexedem. 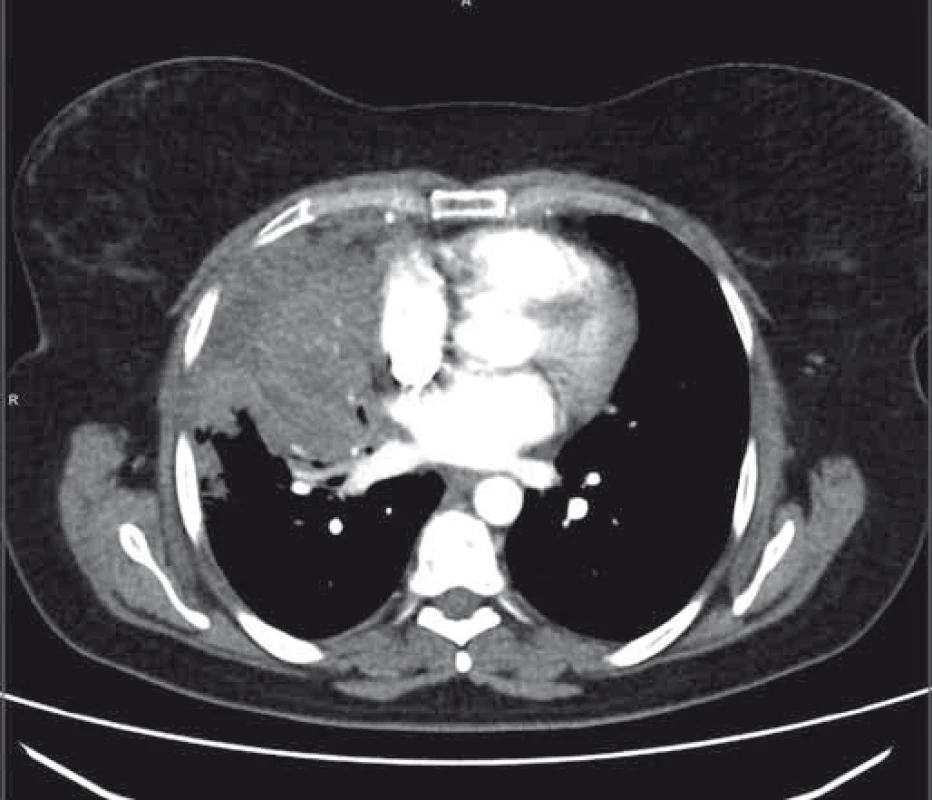
Počátkem září 2016 se podařilo pro pacientku získat osimertinib. Již po měsíci léčby došlo k výrazné regresi nálezu na skiagramu plic, kterou následně potvrdilo i CT vyšetření (výrazné zmenšení tumorózní infiltrace v pravé plíci, výrazné zmenšení ložisek bilaterálně v plicích, parciální regrese atelektázy středního laloku – obr. 3). Subjektivně došlo k ústupu veškerých předchozích obtíží, pacientka opět aktivně sportovala. Jako NÚ osimertinibu se objevila mírná vyrážka (stupně 1) a paronychium jednoho prstu horní končetiny (stupně 2), oboje bylo úspěšně řešeno s kožním lékařem. Počátkem února 2017 se stav nemocné opět zhoršil, objevil se bolestivý ascites s opětovnou dušností. Cytologické vyšetření z punktátu ascitu prokázalo buňky plicního adenokarcinomu. Bylo proto indikováno kontrolní PET/CT vyšetření (obr. 4), které potvrdilo metastazování na peritoneum a omentum, navíc se objevil objemný pleurální výpotek vlevo. Výpotek byl punktován s též nálezem maligních buněk vzhledu adenokarcinomu. Doplněné genetické vyšetření prokázalo přetrvání obou předchozích EGFR mutací (delece na exonu 19, bodová mutace T790M na exonu 20) a navíc mutaci C797S na exonu 20 (metodika stanovení popsána níže). Léčba osimertinibem byla proto po 5 měsících ukončena.
Obr. 3. Parciální regrese nálezu na CT při terapii osimertinibem. 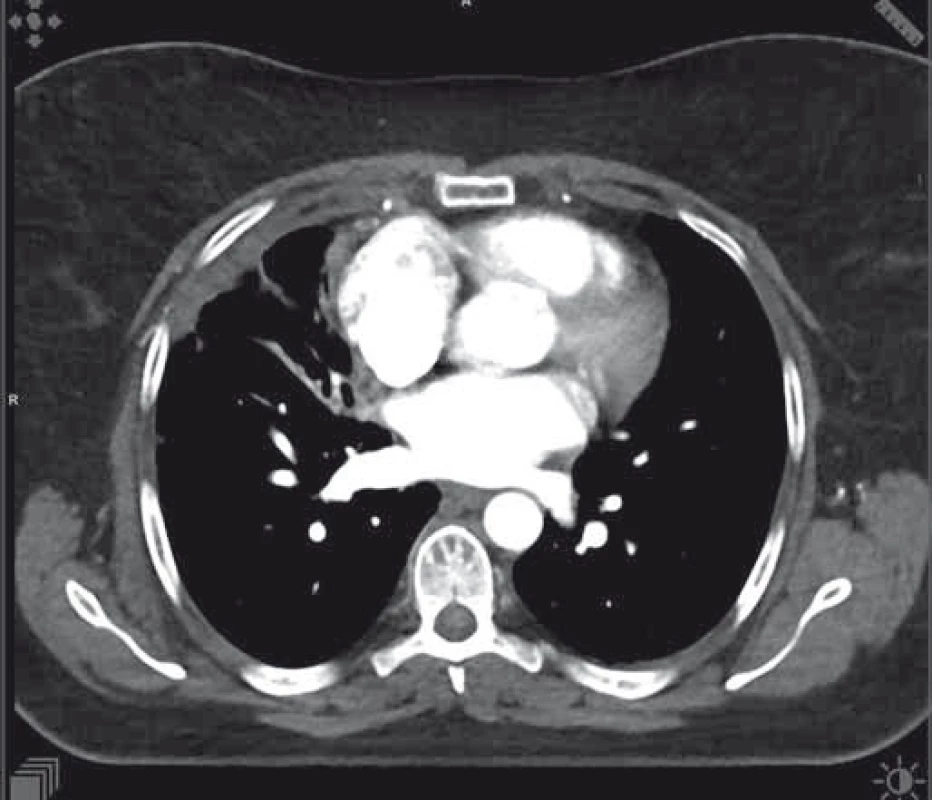
Obr. 4. PET/CT nález po progresi na léčbě osimertinibem. 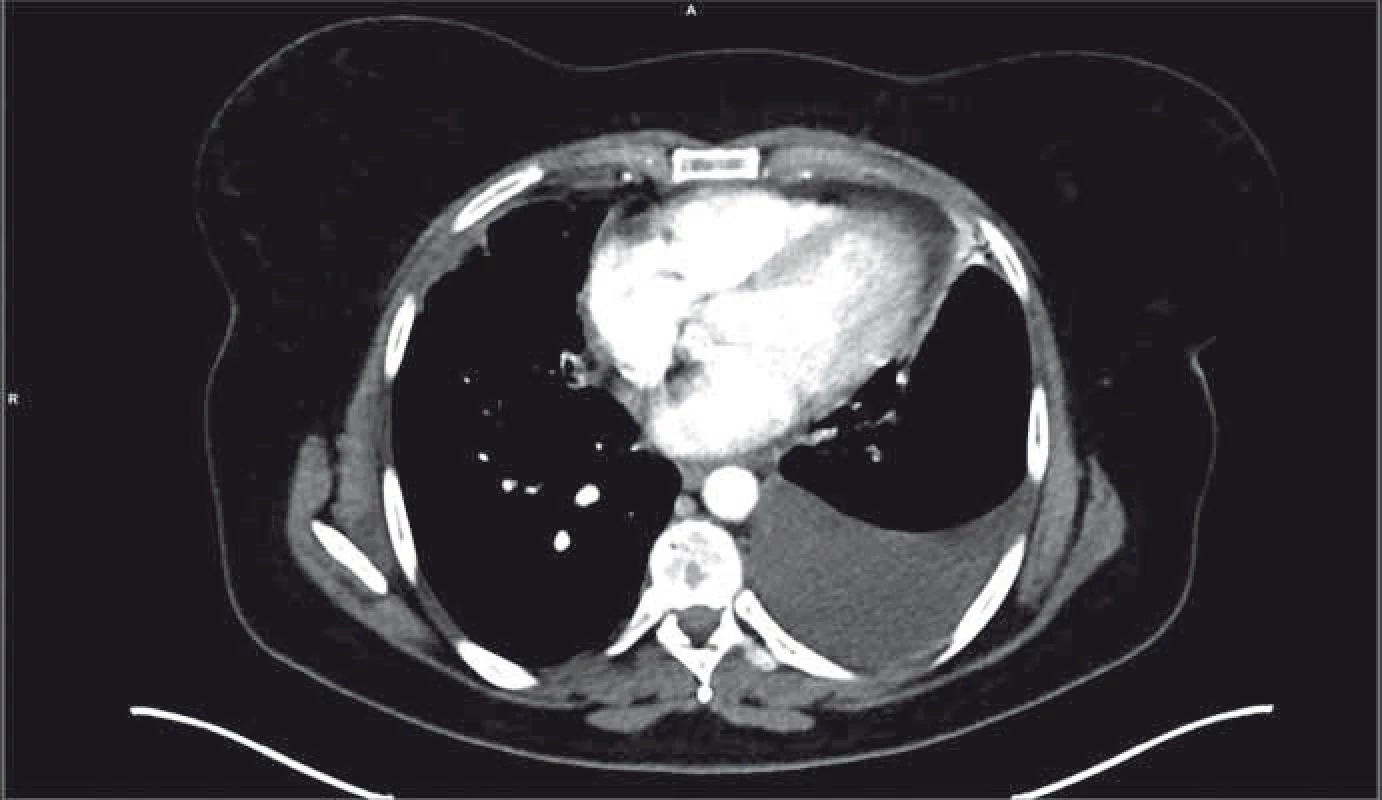
Dále byl zvažován pokus o zahájení další linie chemoterapie. Stav pacientky však výrazně progredoval a v březnu 2017 byla přijata na naši kliniku pro bolesti zad, nechutenství, zvracení, dysurie a otoky dolních končetin. Laboratorně byly průkazné známky renální insuficience a elevace zánětlivých parametrů s výraznou leukocytózou. Byla upravována symptomatická léčba a podávána empiricky antibiotická terapie. Po stabilizaci stavu pacientky (s ECOG PS2) a částečném zlepšení laboratorních hodnot byla zahájena terapie erlotinibem při vědomí přetrvávání senzitivní mutace v genetickém preparátu a odstupu od léčby afatinibem. Avšak po krátké době musela být nemocná znovu hospitalizována pro dehydrataci s těžkými průjmy (stupně 3–4). Navíc došlo opětovně k renální insuficienci (v.s. prerenální) a nárůstu zánětlivých parametrů s extrémní leukocytózou (85,10 × 9/l) a elevací alkalické fosfatázy (alkaline phosphatase – ALP) a laktát dehydrogenázy (LD) suspektně při infiltraci kostní dřeně (jednoznačně neprokázáno). I přes celkovou léčbu stav nemocné nadále progredoval a pacientka koncem března 2017 zemřela.
Metodika „tekuté biopsie“
Řídící EGFR mutace byly vyšetřovány pomocí tekuté biopsie ze 2 ml periferní krve pacienta odebírané do zkumavky obsahující stabilizační činidlo (OncoCEDNA, Carolina Biosystems, CZ). Po dodání vzorků do laboratoře byla z extrahované plazmy izolována DNA s využitím kitu QIAamp® Circulating Nucleic Acid Kit (Qiagen, Německo). Vlastní detekce mutací v izolovaném DNA materiálu byla založena na potlačení amplifikace nenádorové DNA složky pomocí metodiky Target-Selector ctDNA assay (Biocept, San Diego, Spojené státy) a následné specifické amplifikace a sekvenace cirkulující nádorové DNA (ctDNA) [7]. Tento postup vykazuje citlivost umožňující detekci jediné mutované kopie DNA v ml plazmy.
Diskuze
EGFR-TKI 1. a 2. generace přinášejí u pacientů se senzitivnímu EGFR mutacemi (delece na exonu 19, mutace L858R na exonu 21) výrazné prodloužení PFS ve srovnání se standardně podávanou chemoterapií [1]. Afatinib navíc prokázal u delece na exonu 19 i prodloužení celkového přežití a dle studie LUX-Lung 7 se zdá být o něco účinnější ve srovnání s gefitinibem [1,4]. U křehkých či špatně spolupracujících pacientů mohou budit obavu některé jeho NÚ [2], což však nebyl případ naší nemocné. I u ní se objevily očekávané průjmy, vyrážka a paronychia nízkého stupně závažnosti, ale při podpůrné medikaci se je podařilo dobře zkorigovat, v čemž má dle našich zkušeností neocenitelnou roli správná edukace nemocné před zahájením léčby.
Mutace T790 je nejčastějším zdrojem rezistence na EGFR-TKI 1. a 2. generace [5]. Její současný výskyt s původní mutací není vzácný, naopak byl pozorován obvyklý výskyt těchto mutací na stejné alele genu EGFR [8]. Výběr chemoterapie u pacientů s nově prokázanou mutací T790M není dle současných dat jasný, kdy dle menší klinické práce nejevila žádná z podávaných látek jasnou superioritu vůči ostatním možnostem [1]. V našem případě jsme volili osvědčený pemetrexed s dobrým bezpečnostním profilem [9], který však nebyl účinný. Obdobně i ve studii AURA3 se PFS podávané chemoterapie s pemetrexedem jevila o něco nižší než dle výsledku předchozích registračních studií, otázkou je, nakolik to bylo ovlivněno již de facto léčbou 2. linie [6].
Následně podávaný osimertinib je nyní, na základě již zmíněné studie AURA3, léčbou volby pro pacienty s mutací T790 [6]. Obvykle je dobře snášen, kožní toxicity nižšího stupně závažnosti se většinou daří zvládnout, obdobně jako u naší nemocné. Problémem léčby je, stejně jako u předchozích generací EGFR-TKI, postupně se rozvíjející rezistence k léčbě, která může mít několik důvodů [6]. Dle dosavadních poznatků se může jednat o různé bypass cesty (HER2 amplifikace, MET amplifikace, KRAS či BRAF mutace), tak i amplifikaci původní delece exonu 19 či nové EGFR mutace (především dále popsána mutace C797S) [10–13]. Byl popsán i výskyt několika nových EGFR mutací současně [11]. Nejčastějším zdrojem rezistence k osimertinibu je mutace EGFR mutace C797S, která se objevuje u 20–40 % pacientů [11,13]. V prostoru dané mutace je totiž místo ireverzibilní kovalentní vazby osimertinibu, jehož prostorové uspořádání se naruší, a tento lék tak nemůže dosahovat potřebné účinnosti. K rezistenci tato mutace vedla i u naší nemocné, ačkoli nemůžeme spolehlivě vyloučit podíl i jiných bypass mechanizmů, které nebyly stanovovány.
O překonání této rezistence se pokouší řada vědeckých týmů. Byla popsána důležitost druhu mutace C797S [13,14]. Pokud se mutace nachází vůči mutaci T790M v poloze trans (tedy na jiné alele), byla dokumentována citlivost ke kombinaci TKI 1. a 3. generace, naopak pokud byly v pozici cis (na stejné alele), byla pozorována rezistence ke všem klinicky používaným EGFR-TKI [15]. Nicméně trans typ mutace je velice vzácný a navíc po expozici zmíněné kombinované léčbě přechází do stavu cis, čímž se stává rezistentní [15]. Klinický význam rozlišení trans a cis formy mutace C797S je tedy diskutabilní. Další cestou je vývoj nových EGFR-TKI. Řada preparátů se nachází v preklinickém vývoji, kdy nové práce poukazují na možné reverzibilní/ireverzibilní inhibitory cílící na ATP (adenosine triphosphate) vazebné místo pacientů se třemi mutacemi (původní senzitivní mutace + T790M + C797S) s odlišnými preparáty zvažovanými pro mutaci L858R a pro deleci na exonu 19 [16–18]. Též existuje preklinická práce, která ukazuje na možnou efektivitu brigatinibu (ALK inhibitor, ačkoli původně vyvíjen jako EGFR + ALK inhibitor) spolu s EGFR protilátkou (vedoucí k potřebnému snížení EGFR exprese) [12]. Původně brigatinib u senzitivních mutací nedosahoval v klinické praxi dostatečných odpovědí na léčbu, nicméně je možné, že při odlišném prostorovém uspořádání ATP vazebného místa může být (navíc spolu s EGFR protilátkou) jeho kompetitivní inhibice účinnější. Všechny výše zmíněné preparáty však narážejí na riziko vzniku další mutace v ATP vazebném místě a ztrátě jejich účinku. Tuto překážku lze překonat nově vyvíjenými inhibitory bez nutnosti vazby na tuto část EGFR genu [19,20]. Nejslibněji se jeví alosterický inhibitor EIA045 [19,20], který představuje zcela nový typ EGFR inhibice. Jeho výhodou je též velmi nízká účinnost vůči wild-type EGFR. Pro prostorovou asymetričnost EGFR dimerů (mutovaný protein + wild-type EGFR) je jeho účinnost in vitro i in vivo (na myším modelu) závislá též na podání EGFR protilátky (cetuximab). Navíc se zdá, že nebude účinný pro pacienty s delecemi na exonu 19. Stejně jako ostatní zmíněné molekuly zatím nepřekonal fázi preklinických zkoušek, a proto veškeré tyto preparáty byly pro naši nemocnou nedostupné.
Peritoneální metastázy, které se objevily u naší pacientky po podání osimertinibu, jsou poměrně vzácným místem šíření plicních tumorů [21]. Jejich četnost je uváděna do 1 % případů, kdy obvykle vznikají až v průběhu onemocnění [21,22]. Jejich přítomnost je spojena s horší prognózou pacientů [21] a stejně jako u naší nemocné jsou obvykle spojeny s pohrudničními maligními výpotky [14]. Kazuisticky byla doložena regrese tohoto typu metastáz po erlotinibu, který navíc dle jiné práce dokládal slibnou účinnost po léčbě afatinibem se získanou mutací C797S a delecí na exonu 19 [23,24]. V našem případě tato léčba však benefit nepřinesla, patrně pro současně přítomnou mutaci T790M. Navíc byla provázena závažným průjmem, což bylo překvapivé vzhledem k poměrně dobré toleranci afatinibu, kde bychom spíše očekávali závažnější obtíže tohoto typu [25]. Užití TKI po progresi na osimertinibu tak nemusí odpovídat předchozím zkušenostem s léčbou EGFR-TKI, kdy byla doložena u části pacientů úspěšná léčba afatinibem, erlotinibem i gefitinibem po předchozím podání EGFR-TKI 1. generace [26–32] s mediánem TTP obvykle mezi 3 a 4 měsíci. Přičemž se zdá, že větší benefit měli pacienti, u kterých předchozí TKI dosáhl léčebné odpovědi či alespoň stabilizace onemocnění na více měsíců, což byl i případ naší nemocné [28,30]. Nejistý je vliv v mezidobí podávané chemoterapie [31,33]. Vzhledem k obvykle popisované vysoké kontrole onemocnění (až 75 %) je patrné, že i u mutace T790 by mohla vést léčba dalším TKI k účinku alespoň u některých nemocných, což potvrzují i dva prokázané případy ze studie LUX-Lung 4 [30,34]. Bohužel nejsou známa data, zda se tento efekt může projevit i po léčbě osimertinibem, naše zkušenost svědčí spíše proti této domněnce. Další popisovanou možností je podání téhož TKI po tzv. lékových prázdninách s kontrolou onemocnění až u 43 % pacientů [35]. Stran osimertinibu však tento jev dle našich znalostí nebyl zatím popsán. U asymptomatické pomalé progrese nebo pouze lokální progrese zvládnutelné obvykle stereotaktickou radioterapií byla též popsána úspěšná léčba stejným TKI i po progresi onemocnění [23,29,33,36], a to i u pacientů s mutací T790M [37]. Osimertinib ukazoval podobné údaje též ve studii AURA3, kde medián pacientů léčených po progresi dosáhl 4,1 měsíce [6]. Nicméně naše pacientka vykazovala symptomatickou rychlou progresi, a proto jsme ji indikovali ke změně léčebného postupu. Při nemožnosti podání chemoterapie vzhledem k celkovému stavu nemocné a uváděné neúčinnosti imunoterapie u pacientů s EGFR mutacemi [34,38] byl dle našeho názoru erlotinib racionální léčebnou možností, byť s vědomím malé šance na úspěch.
Závěr
Cílená léčba dokázala prodloužit životní vyhlídky pacientů s pokročilými plicními adenokarcinomy, její nevýhodou je však postupný rozvoj rezistence k léčbě. Částečně jej lze překonat preparáty vyšších generací. Ty se však vzhledem k heterogenitě genetických podkladů vzniku rezistence nehodí pro všechny nemocné. Východiskem by se mohla zdát imunoterapie, ale její citlivost k pacientům s EGFR mutacemi není vysoká. Proto prozatím nezbývá, než hlouběji poznávat cesty rozvoje rezistence na TKI a hledat nové způsoby léčby těchto pacientů. Jednou z možností se zdá být 4. generace TKI citlivá na EGFR mutace C797S.
Obdrženo: 12. 9. 2017
Přijato: 12. 10. 2017
Projekt byl podpořen grantem AZV 17-30748A.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Martin Svatoň
Klinika pneumologie a ftizeologie LF UK a FN Plzeň
Edvarda Beneše 1128/13
305 99 Plzeň
e-mail: svatonm@gmail.com
Zdroje
1. Svatoň M. Současný stav a vyhlídky cílené léčby nemalobuněčného plicního karcinomu (NSCLC). Onkologie 2016; 10 (1): 15–18.
2. Svatoň M. Afatinib – cílená léčba nemalobuněčného plicního karcinomu (NSCLC) druhé generace. Postgradual Med 2014; 16 (2): 219–224.
3. Svaton M, Pesek M, Chudacek Z et al. Current two EGFR mutations in lung adenocarcinoma – case report. Klin Onkol 2015; 28 (2): 134–137. doi: 10.14735/amko2015134.
4. Svatoň M, Pesek M. LUX-LUNG 7 – nový pohled na první linii u pacientů s častými EGFR mutacemi? Akutální témata v onkologii očima českých lékařů 2016; 1 (4): 64–69.
5. Svaton M, Pesek M, Mukensnabl P et al. Tumor rebiopsy – Guide to targeted therapy. Eur Surg 2016; 48 (Suppl 3): S194–S196.
6. Svatoň M, Hrda K, Pesek M. Osimertinib – nová volba léčby pro pacienty s mutací EGFR T790M. Onkologie 2017; 11 (2): 72–77.
7. Minarik M, Belsanova B, Fiala O et al. Validation of the denaturing capillary electrophoresis (DCE) assay for non-invasive liquid biopsy in lung carcinoma: A study of concordance with the cobas EGFR mutation test v2. J Clin Oncol 2017; 35 (Suppl 15): e23040.
8. Hidaka N, Iwama E, Kubo N et al. Most T790M mutations are present on the same EGFR allele as activating mutations in patients with non-small cell lung cancer. Lung Cancer 2017; 108 : 75–82. doi: 10.1016/j.lungcan.2017.02.019.
9. Rossi A, Maione P, Santabarbara G et al. The safety of second-line treatment options for non-small cell lung cancer. Expert Opin Drug Saf 2017; 16 (4): 471–479. doi: 10.1080/14740338.2017.1297795.
10. Knebel FH, Bettoni F, Shimada AK et al. Sequential liquid biopsies reveal dynamic alterations of EGFR driver mutations and indicate EGFR amplification as a new mechanism of resistance to osimertinib in NSCLC. Lung Cancer 2017; 108 : 238–241. doi: 10.1016/j.lungcan.2017.04.004.
11. Ou SI, Cui J, Schrock AB et al. Emergence of novel and dominant acquired EGFR solvent-front mutations at Gly796 (G796S/R) together with C797S/R and L792F/H mutations in one EGFR (L858R/T790M) NSCLC patient who progressed on osimertinib. Lung Cancer 2017; 108 : 228–231. doi: 10.1016/j.lungcan.2017.04.003.
12. Uchibori K, Inase N, Araki M et al. Brigatinib combined with anti-EGFR antibody overcomes osimertinib resistance in EGFR-mutated non-small-cell lung cancer. Nat Commun 2017; 8 : 14768. doi: 10.1038/ncomms14768.
13. Wang S, Song Y, Yan F et al. Mechanisms of resistance to third-generation EGFR tyrosine kinase inhibitors. Front Med 2016; 10 (4): 383–388. doi: 10.1007/s11684-016-0488-1.
14. Patel H, Pawara R, Ansari A et al. Recent updates on third generation EGFR inhibitors and emergence of fourth generation EGFR inhibitors to combat C797S resistance. Eur J Med Chem 2017; 142 : 32–47. doi: 10.1016/j.ejmech.2017.05.027.
15. Wang Z, Yang JJ, Huang J et al. Brief Report: Lung adenocarcinoma harboring EGFR T790M and in trans C797S responds to combination therapy of first and third generation EGFR-TKIs and shifts allelic configuration at resistance. J Thorac Oncol 2017; 12 (11): 1723–1727. doi: 10.1016/j.jtho.2017.06.017.
16. Günther M, Lategahn J, Juchum M et al. Trisubstituted pyridinylimidazoles as potent inhibitors of the clinically resistant L858R/T790M/C797S EGFR mutant: targeting of both hydrophobic regions and the phosphate binding site. J Med Chem 2017; 60 (13): 5613–5637. doi: 10.1021/acs.jmedchem.7b00316.
17. Park H, Jung HY, Mah S et al. Discovery of EGF receptor inhibitors that are selective for the d746-750/T790M/C797S mutant through structure-based de novo design. Angew Chem Int Ed Engl 2017; 56 (26): 7634–7638. doi: 10.1002/anie.201703389.
18. Juchum M, Günther M, Döring E et al. Trisubstituted imidazoles with a rigidized hinge binding motif act as single digit nm inhibitors of clinically relevant EGFR L858R/T790M and L858R/T790M/C797S mutants: an example of target hopping. J Med Chem 2017; 60 (11): 4636–4656. doi: 10.1021/acs.jmedchem.7b00178.
19. Günther M, Juchum M, Kelter G et al. Lung Cancer: EGFR Inhibitors with Low Nanomolar Activity against a Therapy-Resistant L858R/T790M/C797S Mutant. Angew Chem Int Ed Engl 2016; 55 (36): 10890–10894. doi: 10.1002/anie.201603736.
20. Jia Y, Yun CH, Park E et al. Overcoming EGFR (T790M) and EGFR (C797S) resistance with mutant-selective allosteric inhibitors. Nature 2016; 534 (7605): 129–132. doi: 10.1038/nature17960.
21. Niu FY, Zhou Q, Yang JJ et al. Distribution and prognosis of uncommon metastases from non-small cell lung cancer. BMC Cancer 2016; 16 : 149. doi: 10.1186/s12885-016-2169-5.
22. Tanriverdi O, Barutca S, Meydan N. Relapse with isolated peritoneal metastasis in lung adenocarcinoma: case report and review of the literature. Contemp Oncol (Pozn) 2012; 16 (6): 586–589. doi: 10.5114/wo.2012.32495.
23. Kamaleshwaran KK, Joseph J, Kalarikal RK et al. Image findings of rare case of peritoneal carcinomatosis from non small cell lung cancer and response to erlotinib in F-18 FDG positron emission tomography/computed tomography. Indian J Nucl Med 2017; 32 (2): 140–142. doi: 10.4103/0972-3919.202239.
24. Kobayashi Y, Azuma K, Nagai H et al. Characterization of EGFR T790M, L792F, and C797S mutations as mechanisms of acquired resistance to afatinib in lung cancer. Mol Cancer Ther 2017; 16 (2): 357–364. doi: 10.1158/1535-7163.MCT-16-0407.
25. Losanno T, Gridelli C. Safety profiles of first-line therapies for metastatic non-squamous non-small-cell lung cancer. Expert Opin Drug Saf 2016; 15 (6): 837–851. doi: 10.1517/14740338.2016.1170116.
26. Schuler M, Fischer JR, Grohé C et al. Experience with afatinib in patients with non-small cell lung cancer progressing after clinical benefit from gefitinib and erlotinib. Oncologist 2014; 19 (10): 1100–1109. doi: 10.1634/theoncologist.2014-0103.
27. Katakami N, Atagi S, Goto K et al. LUX-Lung 4: a phase II trial of afatinib in patients with advanced non-small-cell lung cancer who progressed during prior treatment with erlotinib, gefitinib, or both. J Clin Oncol 2013; 31 (27): 3335–3341. doi: 10.1200/JCO.2012.45.0981.
28. Grossi F, Rijavec E, Dal Bello MG et al. The administration of gefitinib in patients with advanced non-small-cell lung cancer after the failure of erlotinib. Cancer Chemother Pharmacol 2012; 69 (6): 1407–1412. doi: 10.1007/s00280-012-1848-4.
29. Faehling M, Eckert R, Kamp T et al. EGFR-tyrosine kinase inhibitor treatment beyond progression in long-term caucasian responders to erlotinib in advanced non-small cell lung cancer: a case-control study of overall survival. Lung Cancer 2013; 80 (3): 306–312. doi: 10.1016/j.lungcan.2013.02.010.
30. Saito H, Murakami S, Kondo T et al. Effectiveness of erlotinib in advanced non-small cell lung cancer in cases of gefitinib resistance after treatment of more than 6 months. Onkologie 2012; 35 (1–2): 18–22. doi: 10.1159/000335736.
31. Cho KM, Keam B, Kim TM et al. Clinical efficacy of erlotinib, a salvage treatment for non-small cell lung cancer patients following gefitinib failure. Korean J Intern Med 2015; 30 (6): 891–898. doi: 10.3904/kjim.2015.30.6.891.
32. Wu WS, Wu CH, Lai SL et al. Erlotinib salvage therapy in pulmonary adenocarcinoma patients with disease progression after previous EGFR-TKI treatment. Am J Clin Oncol 2016; 39 (6): 556–562. doi: 10.1097/COC.0000000000000096.
33. Chen Q, Quan Q, Ding L et al. Continuation of epidermal growth factor receptor tyrosine kinase inhibitor treatment prolongs disease control in non-small-cell lung cancers with acquired resistance to EGFR tyrosine kinase inhibitors. Oncotarget 2015; 6 (28): 24904–24911. doi: 10.18632/oncotarget.4570.
34. Gainor JF, Shaw AT, Sequist LV et al. EGFR mutations and ALK rearrangements are associated with low response rates to PD-1 pathway blockade in non-small cell lung cancer: a retrospective analysis. Clin Cancer Res 2016; 22 (18): 4585–4593. doi: 10.1158/1078-0432.CCR-15-3101.
35. Song T, Yu W, Wu SX. Subsequent treatment choices for patients with acquired resistance to EGFR-TKIs in non-small cell lung cancer: restore after a drug holiday or switch to another EGFR-TKI? Asian Pac J Cancer Prev 2014; 15 (1): 205–213.
36. Liao BC, Lin CC, Lee JH et al. Optimal management of EGFR-mutant non-small cell lung cancer with disease progression on first-line tyrosine kinase inhibitor therapy. Lung Cancer 2017; 110 : 7–13. doi: 10.1016/j.lungcan.2017.05.009.
37. Li W, Ren S, Li J et al. T790M mutation is associated with better efficacy of treatment beyond progression with EGFR-TKI in advanced NSCLC patients. Lung Cancer 2014; 84 (3): 295–300. doi: 10.1016/j.lungcan.2014.03.011.
38. Lee CK, Man J, Lord S et al. Checkpoint inhibitors in metastatic EGFR-mutated non-small cell lung cancer-a meta-analysis. J Thorac Oncol 2017; 12 (2): 403–407. doi: 10.1016/j.jtho.2016.10.007.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2018 Číslo 1- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejasný stín na plicích – kazuistika
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Kurkumin (Kurkumovník dlouhý – Curcuma longa) jako podpůrný fytoterapeutický prostředek v onkologii
- Kontroverze protonové terapie u nádorů centrálního nervového systému
- Protinádorovou léčbou indukované změny renálních funkcí u pacientů s tumory – update aktuálních poznatků
- Editorial
- Současné postavení checkpoint inhibitorů v léčbě nádorů jícnu a žaludku – přehled studií
- Nemelanómové zhubné nádory kože – klinicko-patologická štúdia pacientov s bazocelulárnym karcinómom a skvamocelulárnym karcinómom
- Chirurgická léčba ampulárního adenokarcinomu – zkušenosti jednoho centra a přehled literatury
- Pacientka se třemi EGFR mutacemi – postupný rozvoj rezistence na předchozí cílenou léčbu
- Stopkované laloky jako jedna z možností rekonstrukce hlavy a krku
-
Organizace a hodnocení kvality onkologické péče v České republice
Věstník Ministerstva zdravotnictví České republiky 2017; 13: 83–92 - Aktuality z odborného tisku
- prof. MUDr. Juraj Švec, DrSc. (16. 1. 1938–17. 2. 2017) K nedožitým 80. narodeninám emeritného prednostu Onkologickej kliniky LF UK v Bratislave
- Testování varianty androgenového receptoru AR-V7 pro výběr pacientů s kastračně refrakterním metastazujícím karcinomem prostaty k léčbě novými hormonálními léky
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Chirurgická léčba ampulárního adenokarcinomu – zkušenosti jednoho centra a přehled literatury
- Kurkumin (Kurkumovník dlouhý – Curcuma longa) jako podpůrný fytoterapeutický prostředek v onkologii
- Stopkované laloky jako jedna z možností rekonstrukce hlavy a krku
- Současné postavení checkpoint inhibitorů v léčbě nádorů jícnu a žaludku – přehled studií
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



