-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
XX. Gynekologická onkologie
Vyšlo v časopise: Klin Onkol 2021; 34(Supplementum 2): 69-74
Kategória:
XX/ 97. PŘEDOPERAČNÍ DIAGNOSTIKA A INDIVIDUALIZACE OPERAČNÍ LÉČBY CERVIKÁLNÍCH KARCINOMŮ
ROB L., ROBOVÁ H., HALAŠKA M., TIKOVSKÝ K., PICHLÍK T., DROZENOVÁ J., MALÍKOVÁ H.
3. LF UK Praha a FN Královské Vinohrady, Praha
Screening cervikálních karcinomů v ČR vede k poklesu incidence invazivních cervikálních karcinomů. V roce 2018 dle ÚZIS byla incidence 13,6/ 100 000 žen, tj. v absolutních číslech 734 nových karcinomů. Ve stadiu I bylo pouze 303 nových karcinomů, navíc téměř jednu třetinu detekovaných karcinomů stadia I tvoří mikrokarcinomy. Tento trend jednoznačně zdůrazňuje význam centralizace radikální chirurgické léčby do onkogynekologických center. Vysoká léčitelnost operabilních časných stadií otevírá řadu otázek, kdy a jak identifikovat podskupinu žen vhodných k radikální operační léčbě, jaká je optimální radikalita, jak minimalizovat morbiditu námi léčených žen a jak dosáhnout co nejlepší kvalitu života. Zpochybnění onkologických výsledků miniinvazivních metod laparoskopie a robotické chirurgie publikovanými studiemi LACC a analýzou SEER dat se otevřela další velké kontroverze v operační léčbě časných stadií cervikálních karcinomů. Standardem léčby invazivních karcinomů v roce 2021 je abdominální radikální hysterektomie. Trendem je snaha o redukci radikality a tím snížení morbidity bez ovlivnění onkologických výsledků. Nové technologie nám k tomu pomáhají. Předoperační ultrazvukové vyšetření a vyšetření magnetickou rezonancí kvalitním přístrojem a erudovaným hodnotitelem, detekce sentinelových uzlin s kvalitním histopatologickým vyšetřením a využití moderních koagulačních technologií jsou v současnosti klíčovými postup v individualizované léčbě invazivních cervikálních karcinomů. Sami více než 20 let používáme laparoskopické operace pouze u časných stadií prognosticky příznivých nádorů do 2 cm s invazí méně než poloviny stromatu pouze v protokolu LAP I a LAP III u fertilitu zachovávajících operací a LAP II se schválením etické komise. Co lze považovat za největší přínosy pro management chirurgické radikální léčby v posledním deceniu, se pokusíme shrnout v několika následujících bodech: 1) předoperační identifikaci objemu nádoru v děložním hrdle; 2) peroperační detekci sentinelových uzlin a jejich histopatologické zpracování; 3) využití nových koagulačních technik, zejména řízené bipolární koagulace technologií LigaSureTM. Chirurgický management má redukovat časnou a pozdní morbiditu bez zhoršení onkologických výsledků. Centralizace operační léčby do onkogynekologických center, zejména v kontextu příznivého trendu poklesu invazivních karcinomů, je správným trendem.
XX/ 98. GYNEKOLOGICKÉ MALIGNITY U NEJSTARŠÍ VĚKOVÉ SKUPINY
ŠPAČEK J.
Porodnická a gynekologická klinika LFHK UK a FN Hradec Králové
Východiska: Nárůst počtu případů nádorových onemocnění ve věku nad 85 let je evidentní. Kromě stadia onemocnění a typu nádoru je nejvýznamnějším prognostickým faktorem celkový výkonnostní stav, který reflektuje i závažnost komorbidit. Samotný věk je neoddělitelnou součástí, která by měla zejména akcentovat faktor kvality života. Základní léčebnou modalitou zůstává také v této věkové skupině chirurgie a plánované operace je možné považovat i u starších osob za relativně bezpečné. Častým podceňováním klinické symptomatologie se však o to častěji setkáváme v tomto věkovém období s pokročilejšími případy nevyjímaje ani eventuální nutnost akutní chirurgické intervence. Neplánované výkony jsou mnohdy prováděny v rámci ústavní pohotovostní služby (zejména tělo děložní, ovarium, vejcovod, peritoneum) a prognóza těchto pacientek je o to závažnější. Ohledně radioterapie platí to, že pacientky v dobrém výkonnostním stavu tolerují léčbu zářením velmi dobře a tato léčebná modalita může být vhodnou alternativou k chirurgickému výkonu zejména pro nemocné, které jsou limitované kardiopulmonální nedostatečností a nemohou podstoupit chirurgický výkon (zevní genitál, pochva, čípek). Největší omezení však platí v tomto věkovém období pro systémovou léčbu. Věk nad 65 let je obecným rizikovým faktorem pro útlum krvetvorby. Chemoterapii je proto nutné provádět u starších pacientek vždy se zvýšenou opatrností. Pečlivé sledování běžně monitorovaných parametrů včetně funkcí ledvin je samozřejmostí. Využití cílené léčby u pacientek starších 80 let není v gynekologické onkologii indikované. Závěr: Proces stárnutí souvisí s postupným úbytkem funkčních rezerv tělesných orgánů a nárůstem výskytu dalších onemocnění. Neopominutelnou součástí diagnosticko-léčebného algoritmu by mělo být multiparametrické geriatrické vyšetření, které zahrnuje nejen vyhodnocení závažnosti přidružených chorob, ale též zhodnocení funkčního, mentálního a nutričního stavu pacientky. Vždy je však nutné pečlivě zvažovat prospěch a možná rizika. Zásadní otázkou potom zůstává, do jaké míry máme zohledňovat samotný faktor věku. Otázka radikálního a paliativního záměru by proto neměla být ovlivněna stářím nemocné, ale jejím celkovým stavem – biologickým věkem.
XX/ 99. ROBOTICKÁ CHIRURGIE V LÉČBĚ KARCINOMU HRDLA DĚLOŽNÍHO – UPDATE
PILKA R.
Porodnicko-gynekologická klinika LF UP a FN Olomouc
Minimálně invazivní chirurgie (MICH) se v průběhu posledních tří dekád stala nedílnou součástí gynekologického chirurgického repertoáru. U žen podstupujících hysterektomii, myomektomii, sakrokolpopexi, výkony na adnexech a stagingové výkony u vybraných gynekologických zhoubných nádorů demonstrují randomizované kontrolované prospektivní studie a vybrané retrospektivní studie spojení MICH s nižšími krevními ztrátami, kratší délkou hospitalizace, menším výskytem peroperačních a pooperačních komplikací a zvýšenou kvalitou života ve srovnání s operacemi prováděnými laparotomicky. Robotická chirurgie představuje jednu z nejnovějších verzí MICH, která je široce adoptována v řadě zemí světa. Navzdory cytologickému screeningu a HPV vakcinaci zůstává karcinom hrdla děložního významnou globální příčinou morbidity a mortality. Je čtvrtým nejčastěji diagnostikovaným karcinomem u žen a čtvrtou nejčastější celosvětovou příčinou smrti u žen. Dle doporučených postupů National Comprehensive Cancer Network (NCCN) and European Society of Gynecological Oncology (ESGO) je radikální hysterektomie zlatým standardem chirurgické léčby FIGO stadií IA2–IB1. Po řadu desetiletí byla u žen s karcinomem hrdla děložního prováděna abdominální radikální hysterektomie s vynikajícími výsledky. V roce 1992 byla poprvé popsána laparoskopicky asistovaná radikální hysterektomie. Robotem asistovaná laparoskopická radikální hysterektomie nabízí lepší kontrolu a vizualizaci operačního pole než laparoskopie. Retrospektivní studie demonstrovaly srovnatelné výsledky robotické a otevřené chirurgie ve smyslu rekurencí a přežití. Po zveřejnění LACC studie (Laparoscopic Approach to Cervical Cancer) v říjnu 2018 byla však bezpečnost minimálně invazivního přístupu u radikální hysterektomie pro časná stadia karcinomu hrdla děložního zpochybněna. Radikální hysterektomie představuje ve své podstatě komplexní chirurgický výkon s nezbytnou délkou learning curve. Pokud je prováděna minimálně invazivně, např. laparoskopicky, může vést k řadě variací v souvislosti s technikou a osvojenými dovednostmi. Tři nedávno publikované studie zkoumaly dopad learning curve na onkologické výsledky po robotické radikální hysterektomii pro časná stadia karcinomu hrdla děložního a zjistily zlepšení přežívání s nárůstem zkušeností chirurga.
XX/ 100. IMUNOTERAPIE V GYNEKOLOGICKÉ ONKOLOGII
NÁLEŽINSKÁ M.1, LAKOMÝ R.2, CHOVANEC J.3
1Oddělení gynekologické onkologie, MOÚ Brno, 2Klinika komplexní onkologické péče LF MU a MOÚ Brno, 3Klinika operační onkologie LF MU a MOÚ Brno
Imunoterapie vstupuje do terapeutického portfolia v gynekologické onkologii se značným zpožděním. Hlavním důvodem je obecný profil gynekologických malignit, které jsou z imunologického pohledu charakteristické nízkou mutační náloží a vysoce imunosupresivním nádorovým prostředím. Z tohoto důvodu se v klinických studiích ukázalo jako výhodnější kombinovat dosud známé modality lokální i systémové konvenční terapie s cílenou léčbou a s inhibitory kontrolních bodů imunitní reakce. Nejlepší výsledky byly popsány ve studiích s pokročilým karcinomem endometria (kombinace antiangiogenního preparátu levantinibu a checkpoint inhibitoru pembrolizumabu). V přehledovém sdělení jsou prezentovány výsledky klinických studií zaměřené na zapojení imunoterapeutik do managementu pokročilých a recidivujících gynekologických nádorů, tak jak byly publikovány a prezentovány na odborných sympoziích. Současně platí, že vedoucí terapeutickou modalitou časných stadií maligních nádorů rodidel zůstává onkochirurgie.
XX/ 101. ÚLOHA RADIOTERAPIE V ONKOGYNEKOLOGII
PRINC D.
Klinika radiační onkologie LF MU a MOÚ Brno
Východiska: Radioterapie využívá ionizující záření v léčbě nádorových i nenádorových onemocnění. Hraje důležitou úlohu také v terapii gynekologických malignit buď samostatně, nebo jako součást multimodálního přístupu. V léčbě gynekologických malignit se uplatňuje jak zevní radioterapie, tak i brachyterapie. Ozařování se často používá v léčbě nádorů zevního genitálu, pochvy, hrdla děložního, těla děložního a spíše výjimečně u nádorů vaječníků. U gynekologických malignit můžeme radioterapii indikovat s kurativním, adjuvantním i paliativním léčebným záměrem. Obecně můžeme říct, že časná stadia gynekologických malignit je většinou možné řešit operační léčbou a adjuvantní radioterapie je indikována v případě zvýšeného rizika lokální recidivy. Kurativní radioterapii zase častěji používáme u lokálně pokročilých stadií onemocnění, inoperabilních nálezů nebo v případě kontraindikace operačního výkonu. Paliativní ozařování je důležitou součástí léčby symptomů velmi pokročilého, resp. diseminovaného onemocnění s cílem zlepšení kvality života pacientky a úlevy od potíží. Cíl: Prezentace se zaměřuje na konkrétní možnosti využití radioterapie u jednotlivých gynekologických nádorů. Podrobně rozebírá indikace léčby zářením a klade důraz na změny a novinky v doporučených postupech léčby ozařováním zejména u nádorů děložního hrdla a těla. Konkrétně popisuje moderní techniky zevní radioterapie a brachyterapie. Zabývá se také doporučenými dávkami na cílové objemy a rizikové orgány. V neposlední řadě se věnuje i nežádoucím účinkům radioterapie, doporučenému sledování pacientek po léčbě zářením a léčebným výsledkům u jednotlivých diagnóz. Závěr: Radioterapie hraje zásadní roli v léčbě gynekologických malignit a je nedílnou součástí multimodálního přístupu v onkogynekologii. Pro určení správného léčebného postupu, šitého na míru konkrétní pacientce, je důležitá multioborová spolupráce radiačního onkologa, gynekologa a klinického onkologa, ideálně v rámci onkogynekologické indikační komise.
XX/ 102. PROBLEMATIKA EXENTERAČNÍCH VÝKONŮ V ONKOGYNEKOLOGII
JELENEK G., CHOVANEC J., FERANEC R.
Oddělení gynekologické onkologie, MOÚ Brno
Pánevní exenterace je specifická, komplexní a rozsáhlá operace umožňující erudovanému týmu při vhodné selekci pacientky s pánevní recidivou dosáhnout jejího vyléčení. Výkon je radikalitou a specificitou potřebných chirurgických zkušeností výjimečný a vyžaduje multioborový tým a centralizaci. Operace obnáší u totální exenterace při abdominální fázi operace „en-bloc“ odstranění ženských pohlavních orgánů (dělohy, vejcovodů, vaječníků, pochvy), závěsného aparátu dělohy (parametrií), distální části uropoetického systému (močového měchýře, uretry), anorekta a části levátorových svalů. U přední exenterace je zachováno rektum, u zadní exenterace je zachován močový měchýř a uretra. Součástí perineální fáze operace je v ně kte rých případech resekce anu, uretry, části vulvy. Exenterační operace nemá svůj standardní výkon a je modifikovaná dle peroperačního nálezu, lokalizace nádoru, technických a anatomických možností, i s ohledem na absolvovanou radioterapii a přání pacientky. Většinou je operace indikovaná při centrální rekurenci gynekologického nádoru jako poslední možnou volbou k záchraně života – salvage operace s 5letým přežitím přibližně 50 %.
XX/ 168. NEWS IN OVARIAN CANCER TREATMENT
ZVARÍKOVÁ M.
Department of Comprehensive Cancer Care, Masaryk MMCI, Brno, Czech Republic
Epithelial ovarian cancer is the most common cause of death in patients with gynaecological malignancy. The five-year survival ranges between 46%, which can be explained by the fact, that more than 60% of patients are diagnosed in advanced stages of the disease. The main treatment modality is cytoreductive surgery with sequential chemotherapy based on the platin derivative with adjuvant or neoadjuvant purpose. The neoadjuvant chemotherapy is then followed by interval debulking surgery (IDS). More than 75% of patients with advanced ovarian cancer relapse despite high sensitivity to the primary treatment. Thus, there is an urge to find novel therapeutic possibilities due to the high risk of relapse and bad prognosis of patients with advanced epithelial ovarian cancer. Although the cytostatics and maximal surgical eff orts stay the basic pillars of ovarian cancer treatment, the targeted therapy becomes nowadays an integral part of the therapeutic regimens. With their increased use, poly-ADP-ribose polymerase inhibitors (PARP inhibitors) have improved the progressionfree survival in the first line of the palliative treatment as well as in patients with recurrent disease. At present, there are three registered PARP inhibitors in diff erent indications; together, they are registered for the maintenance therapy in diseases sensitive to the platin derivative. Even if the specific indications of PARP inhibitors recommend genetic testing of the germ-cell mutations in all patients with epithelial ovarian cancer, new drug approvals indicate that patients could benefit even from the somatic mutation analysis. With developing data about the surgical techniques and targeted therapy (including antiangiogenic agents, PARP inhibitors, immunotherapy, novel therapeutic agents, and their combinations), we believe that epithelial ovarian cancer will transform from a mainly deadly disease into a more and more curable one.
XX/ 210. ZMĚNY N-GLYKANOVÝCH PROFILŮ V SÉRECH A TKÁNÍCH PACIENTEK S KARCINOMEM VAJEČNÍKŮ PŘEDPOVÍDALY REZISTENCI K CHEMOTERAPEUTICKÉ LÉČBĚ NA BÁZI PLATINY
HERNYCHOVÁ L.1, IHNÁTOVÁ I.2, LATTOVÁ E.2, BENEŠOVÁ I.1, URMINSKÝ A.1, UHRÍK L.1, HENEK T.1, NÁLEŽINSKÁ M.3, CHOVANEC J.3, NENUTIL R.4
1RECAMO, MOÚ Brno, 2PřF MU, Brno, 3Oddělení gynekologické onkologie, MOÚ Brno, 4Úsek diagnostické bioptické patologie, MOÚ Brno
Východiska: Glykosylace je posttranslační modifikace proteinů, která se zapojuje do mnoha biologických procesů a významně zasahuje i do dějů spojených s karcinogenezí a progresí. Přítomnost proteinů s abnormální glykosylací v séru je spojována s jejich uvolňováním z nádoru. U mnoha onkologických onemocnění je proto jejich přítomnost spojována s diagnostikou, progresí, prognózou onemocnění nebo účinností léčby. Právě léková rezistence se stala hlavní překážkou úspěšné léčby pacientů s pokročilými stadii onemocnění. Materiál a metody: Sérum pacientek (n = 83) s karcinomem vaječníků bylo odebráno před léčbou s následným zjištěním rezistence nebo citlivosti k chemoterapeutické léčbě založené na platinových derivátech. Odebrané tkáně byly rozděleny do dvou skupin podle velikosti ponechaného pooperačního nádoru. N-glykany uvolněné z tkání a sér byly permetylovány a analyzovány pomocí hmotnostní spektrometrie. Výsledky založené na rozdílech relativní kvantifikace signálů N-glykanů ve spektrech byly hodnoceny biostatistickými nástroji. Výsledky: Z hmotnostně spektrometrických dat bylo detekováno 68 (tkáně) a 63 (sérum) spektrálních signálů patřících N-glykanům. Osm glykanů izolovaných z tkání s ponechaným postoperačním reziduem a jeden izolovaný ze séra vykazovaly vyšší relativní intenzity spektrálních signálů u pacientek rezistentních k léčbě ve srovnání se skupinou senzitivní k léčbě. Z toho šest tkáňových komplexních glykanových struktur bylo statisticky významně spojených s primární rezistencí k léčbě, s poloviční dobou celkového přežití a přežití bez progrese. Žádné statisticky významné glykany nebyly nalezeny v tkáních a sérech pacientek bez ponechaného rezidua nádorové tkáně. Závěr: Přítomnost glykanů v tkáních s ponechaným reziduem nádoru (m/ z 3053,54; 3880,96; 4055,04; 4128,09; 4603,20 a 4777,39) by mohla predikovat alternativní léčebné postupy pro danou skupinu pacientek. Stále však velkou překážkou zůstává vysoká heterogenita nádorů a tedy variabilita glykanových struktur.
Podpořeno: Evropský fond pro regionální rozvoj – ENOCH (CZ.02.1.01/ 0.0/ 0.0/ 16_019/ 0000868) a MZ ČR – RVO (MOÚ, 00209805).
XX/ 220. MIKRORNA V PORUCHÁCH ŽENSKÉHO REPRODUKČNÉHO SYSTÉMU
KALINOVÁ K., BIŠČÁKOVÁ Z., MAREKOVÁ M., RABAJDOVÁ M.
LF UPJŠ v Košiciach, Slovenská republika
Onkologické ochorenia ženského reprodukčného systému majú v súčasnosti vysokú prevalenciu a sú jednou z hlavných príčin mortality žien. Včasná diagnostika gynekologických malignít môže pozitívne prispieť k celkovej prognóze ochorenia ako aj k samotnému priebehu ochorenia. Genetické regulácie spojené s mikroRNA (miRNA) predstavujú nový rozmer v molekulárnej epidemiológii nádorových ochorení. miRNA môže fungovať ako onkogén alebo ako nádorový supresor. Onkogénna miRNA má v nádorovej bunke zvýšenú hladinu a reguluje nádorové supresory, zatiaľ čo expresia nádorovej supresorovej miRNA je v nádore znížená a reguluje onkogény. Zmeny hladín relatívnej expresie miRNA naznačujú jej možné využitie pri diagnostike prekanceróznych stavov alebo onkologických ochorení. Aktuálne neexistuje spoľahlivý marker vývoja a progresie gynekologických malignít z moču pacientov. Využitie analýzy nekódujúcich RNA je možnou perspektívou pre diferenciálnu diagnostiku endometriózy a karcinómu endometria. Štúdium molekulových zmien expresie miR-17-5p a miR-99 pri vybraných malignitách ženského reprodukčného systému – endometrióza, karcinóm endometria corpus uteri, karcinóm cervix uteri. Experimentálna skupina (n = 19) bola tvorená pacientkami s vybranými ochoreniami ženského reprodukčného systému – endometrióza, karcinóm corpus uteri, karcinóm cervix uteri. Hladina expresie miR-17-5p a miR-99 bola detegovaná zo vzoriek moču pomocou qRT-PCR a výsledky boli porovnané s kontrolnou skupinou bez predošlej pozitívnej anamnézy (n = 5). Hladina expresie miR-17-5p bola o 92,53 % vyššia u pacientov s endometrióznymi ložiskami na sakrouterinných ligament a o 634,31 % vyššia u pacientov s „frozen pelvis“ v porovnaní s kontrolnou skupinou. Expresia miR-99 bola u pacientov s endometrióznymi ložiskami na sakrouterinných ligament down-regulovaná o 47,33 % v porovnaní s kontrolnou skupinou. Zmeny expresie spomínaných miRNA boli rovnako pozorované aj v skupine pacientov s karcinómom krčka maternice, hladina expresie miR - 17-5p bola o 69,89 % vyššia oproti kontrolnej skupine, porovnaním s kontrolnou skupinou sa zistilo zvýšenie hladiny expresie miR-99 o 37,41 %. V skupine pacientov s karcinómom corpus uteri bola hladina expresie miR-99 zvýšená o 35,89 % v porovnaní s kontrolnou skupinou. Zmeny expresie miR-17-5p boli zvýšené o 106,81 % v porovnaní so zdravou kontrolou. Signifikantné pozorované zmeny hladiny expresie miRNA miR-17-5p a miR - 99 boli analyzované na hladine významnosti s p ≤ 0,05. Výsledky rozdielnych hladín relatívnej expresie miR-17-5p a miR-99 naznačujú možné využitie v diferenciálnej diagnostike.
XX/ 251. NEVYZPYTATELNOST PONECHÁNÍ OVARIÍ PŘI TERAPII CERVIKÁLNÍHO KARCINOMU DĚLOHY
MOUKOVÁ L.1, FERANEC R.1, KOLÁŘOVÁ H.1, ZATOČIL P.1, KREJČÍ E.2, CHOVANEC J.1
1Oddělení gynekologické onkologie, MOÚ Brno, 2Úsek diagnostické bioptické patologie, MOÚ Brno
Východisko: U spinocelulárních karcinomů děložního hrdla je možné v rámci operační léčby ponechat ovaria s jejich transpozicí, zejména v zájmu zachování hormonální substituce žen. Popis případu: U pacientky narozené v roce 1972 byl diagnostikován spinocelulární karcinom děložního hrdla G3 z konizace děložního čípku v 10/ 2010 v Kyjově. Následovala radikální hysterektomie gr. III s transpozicí ovarií, pánevní lymfadenektomií a appendektomií v MOÚ v 1/ 2011. Dle definitivní histologie bylo popsáno reziduum CIN III v junkci, invaze nenalezena, uzlinové metastázy nenalezeny, klasifikace pT1b1 pN0(0/ 34) M0 dle původní klasifikace. Následně pacientka absolvovala pravidelné dispenzární kontroly. Koncem 7/ 2011 si pacientka začala stěžovat na tlaky podbřišku. Provedeno přešetření PET, CT s dg. TU pelvis – v.s. ovarii, s podezřením na MTS peritonea. Současně elevace nádorových markerů. V 8/ 2011 provedena v MOÚ bilaterální adnexektomie a totální omentektomie. Histologicky potvrzen G3 serózní adenokarcinom obou ovarií, nádorová infiltrace cavum Douglasi, nádorové buňky v ascitu, mikrometastázy v omentu, metastázy v probatorních excizích ze serózy sigmoidea, přední stěny břišní pravého mezogastria a pliky močového měchýře, FIGO IIIc. Poté pacientka absolvovala 6 sérií chemoterapie v režimu Taxol/ CBDCA do 1/ 2012. V 8/ 2012 si pacientka vyhmatala MTS ve stěně břišní a současně v polypu pochvy histologicky prokázána recidiva invazivního serózního papilárního karcinomu ovariálního typu. K další léčbě se již pacientka odmítla dostavit, naposledy v MOÚ v 10/ 2012, genetické testování odmítla. Volila alternativní cestu. Zemřela v 11/ 2013. Závěr: U spinocelulárních karcinomů děložního hrdla není provedení bilaterální ovarektomie vždy nutné pro zachování hormonální substituce v aktivním věku ženy. Provedení rozsahu výkonu záleží i na přání pacientky. V současné době jsou u pacientek s ovariálním karcinomem nové možnosti biologické i imunologické terapie, k čemuž nám napomáhá i genetické vyšetření. Finálně je vše o tom, jaký k léčbě pacientka zaujme postoj.
Podpořeno MZ ČR – RVO (MOÚ, 00209805).
XX/ 252. VÝZNAM KOMPLEXNÍ ONKOLOGICKÉ LÉČBY U ŽENY S PRIMÁRNÍM PERITONEÁLNÍM KARCINOMEM
MOUKOVÁ L.1, KALÁBOVÁ R.1, KOLÁŘOVÁ H.1, FERANEC R.1, LŽIČAŘOVÁ E.2, ŠACHLOVÁ M.3, ZATOČIL P.1, PRINC D.4, ONDRÁK M.5, KLEINOVÁ J.3
1Oddělení gynekologické onkologie, MOÚ Brno, 2Úsek diagnostické bioptické patologie, MOÚ Brno, 3Gastroenterologické oddělení, MOÚ Brno, 4Klinika radiační onkologie LF MU a MOÚ Brno, 5Oddělení chirurgické onkologie, MOÚ Brno
Východiska: Komplexnost onkologické léčby je nesmírně důležitá pro osud pacientů. Multioborová spolupráce je základem k úspěšnosti léčby. Popis případu: Pacientka narozená 1978 odeslána do MOÚ ke kolonoskopii, kde nalezena tu infiltrace střeva. V anamnéze žena udávala půl roku trvající zácpu – řešeno laxativy. Dle gynekologického a stagingových vyšetření suspektní Ca ovaria gr. III. V 9/ 2005 provedena debulking operace s exstirpací MTS cavum Douglasi, s resekcí omenta, ovarií, APPE, exstirpací MTS mesenterii a jejuni a paliativní ileostomie – radikálně inoperabilní nález. Histologicky verifikován serosní papilární karcinom s psammomaty, low-grade, primární peritoneální. Popsána mikroskopická ložiska na povrchu ovarií, ložiska v omentu a apendixu, nádorové buňky v laváži dutiny břišní. Uzavřeno jako Ca peritonei IIIC pT3c pNx pM0. Následovala chemoterapie I. linie v režimu paklitaxel/ CBDCA do 5/ 2005 s regresí 70 % v pánvi. V 8/ 2006 provedena revize dutiny břišní, salpingektomie vpravo, dále inoperabilní. Pokračováno v chemoterapii II. linie v režimu CAP. V 5/ 2007 provedena debulking oboustranná adnexektomie (děloha inoperabilní). Histologicky regrese se sporadickými mikrorezidui serózního karcinomu na obou ovariích. Poté aplikována III. linie chemoterapie v režimu „paclitaxel weekly“ do 3/ 2008. V 11/ 2008 dle PET a TUM prokázána recidiva nemoci. Aplikovány 2 série IV. linie chemoterapie v režimu CBDCA/ CFA – ukončena pro závažný křečový stav a alergickou reakci. Navázáno V. linií chemoterapie v režimu „topotecan weekly“ do 5/ 2009. V období 8–9/ 2009 provedena paliativní radioterapie na oblast tumorózní infiltrace pánve (40 Gy) a paliativně per os podávána VI. linie VP. Dle CT 11/ 2010 progrese s MTS v oblasti hilu sleziny a v pánvi. Do 5/ 2011 aplikována VII. linie chemoterapie v režimu „docetaxel weekly“. V 5/ 2011 diagnostikována recidiva v oblasti pochvy s následnou brachyterapií (7,0 Gy) v 6/ 2011 a pokračováno v aplikaci VIII. linie chemoterapie v režimu Caelyx. Po 2 sériích ukončeno pro kožní toxicitu gr. IV. Od 11/ 2011 paliativně podávána IX. linie chemoterapie v režimu CFA per os. V 5/ 2012 onkologická léčba ukončena. Pacientka zemřela 9/ 2012. Závěr: Pacientka s primárním peritoneálním tumorem, který opakovaně radikálně inoperabilní, dokázala přežít 7 let díky komplexní onkologické léčbě v Masarykově onkologickém ústavu. Bohužel, svůj boj prohrála. Nové možnosti léčby v podobě biologické léčby a imunoterapie nám v současné době přináší naději na lepší zítřky.
Podpořeno MZ ČR – RVO (MOÚ, 00209805).
XX/ 253. CHARAKTERIZÁCIA ÚČINKU A TERAPEUTICKEJ FUNKCIE KOMPLEXOV NESTEROIDNÝCH ANTIFLOGISTÍK NA ĽUDSKÉ ENDOMETRIÁLNE BUNKY
ABRAHAMOVSKÁ M., SMOLKO L., KLEPCOVÁ Z., MAREKOVÁ M., RABAJDOVÁ M.
Ústav lekárskej a klinickej biochémie, LF UPJŠ v Košiciach, Slovenská republika
Endometrióza je zápalové ochorenie definované prítomnosťou funkčného endometria v atypickej oblasti mimo dutiny maternice. Primárnou liečbou aplikovanou vo väčšine prípadov endometriózy je terapia liekmi. Nedávne štúdie naznačujú, že niektoré komplexy prechodných kovov vykazujú oproti pôvodnému liečivu zlepšenú protizápalovú, antioxidačnú aj protirakovinovú aktivitu. Existujú komplexy, ktoré vykazujú podstatné vlastnosti špecifického viazania DNA, čo naznačuje ich potenciál modifikácie bunkového metabolizmu aj na transkripčnej úrovni. Špecifické rozpoznávanie väzobnej sekvencie súvisí so štruktúrou a tvarom komplexných molekúl. Nový zinočnatý komplex s kyselinou niflumovou a neukuproínom so zložením (Zn(neo)(nif)2), bol pripravený dvojkrokovou syntézou a bol izolovaný v kryštalickej forme. Centrálne atómy Zn(II) v komplexných molekulách sú tetrakoordinované dvoma atómami kyslíka nif ligandov a dvoma atómami dusíka chelátovo viazaného neo. Pripravený komplex bol charakterizovaný elementárnou analýzou, IR, UV/ VIS a fluorescenčnou spektroskopiou a jeho molekulová štruktúra bola stanovená röntgenovou štruktúrnou analýzou. Nedávno publikované štúdie konformačných zmien DNA a chromatínu pomocou mikroskopie atómových síl poukazujú na prítomnosť definitívnych zmien v štruktúre DNA u pacientov s potvrdenou endometriózou a karcinómom endometria corpus uteri, čo naznačuje potencionálnu schopnosť komplexu selektívnej väzby štruktúrne zmenených oblastí DNA. Cytotoxické účinky komplexu boli študované in vitro na dvoch bunkových líniách endometria (hTERT a 12Z) analýzou buniek bez označenia v reálnom čase (xCELLigence) a jeho väzbové vlastnosti k DNA boli skúmané spektroskopickými metódami. Z výsledkov analýz vyplýva, že komplex vykazuje významne vyššiu cytoxicitu pre endometriotickú bunkovú líniu 12Z s hodnotou indexu selektivity (IC50 (hTERT)/ IC50 (12Z)) 4,58, zatiaľ čo voľná kyselina niflumová ovplyvňuje bunkovú líniu hTERT viac ako 12Z. Hodnoty IC50 získané z meraní xCELLigence ukázali, že komplex je veľmi aktívny už pri nízkej koncentrácii. Pokračovanie pilotnej štúdie môže dopomôcť k získaniu nových informácií pri charakterizácií účinku a terapeutickej funkcie nových vysoko špecifických komplexov na báze kovov so selektívnou cytotoxicitou na endometriotické bunky.
Táto práca bola podporovaná z projektu VEGA 1/ 0620/ 19 a VEGA 1/ 0540/ 2021.
XX/ 254. VYUŽITIE FLUORESCENČNÉHO FINGERPRINTINGU PRI DIAGNOSTIKE ENDOMETRIÓZ
ŠVECOVÁ M., DUBAYOVÁ K., BIŠČÁKOVÁ Z., RABAJDOVÁ M., MAREKOVÁ M.
UPJŠ v Košiciach, Slovenská republika
Východiská: Endometrióza predstavuje estrogén dependentné ochorenie charakterizované ektopickým výskytom endometriálneho tkaniva. Táto prekanceróza komplikuje tehotenstvo a môže viesť až k infertilite. Dodnes neexistuje spoľahlivý marker vývoja a progresie endometriózy z moču pacientok. Použitie spektrálnych metód je jednou z možných perspektívnych ciest pri získavaní nových informácií o výskyte endometrióz. Fluorescenčná analýza telových tekutín, ako sú krv a moč, sa v poslednej dobe čoraz častejšie v rôznych podobách aplikuje na monitoring rôznych chorobných procesov. Ciele: Cieľom predkladanej práce bolo využitie fluorescenčného fingerprintingu na detekciu rôznych foriem endometrióz na základe snímania synchrónnych fluorescenčných spektier moču a ich spracovania do grafického formátu fluorescenčných koncentračných matríc. Metódy: Fluorescenčná analýza bola realizovaná na vzorkách moču gynekologických pacientok s rôznou formou endometrióz. Porovnávaciu skupinu tvorili zdravé ženy bez gynekologických ochorení s negatívnym močom. Detekcia zmien v zložení moču bola realizovaná pomocou fluorescenčných koncentračných matríc. Pre posúdenie rozdielov v zložení biologického materiálu boli sledované hladiny vybraných endogénnych fluorofórov: aromatické aminokyseliny a ich metabolity, NADH a FAD. Synchrónne excitačné spektrá boli merané luminiscenčným spektrofotometrom Perkin Elmer LS 55. Synchrónne vrstevnicové mapy boli vytvorené manuálne v počítačovom programe WinLab. Výsledky: Z grafického zobrazenia fluorescenčných koncentračných matríc bol už na základe vizuálneho porovnania zrejmý rozdiel v zložení moču v jednotlivých skupinách pacientok (obr. 1). Hodnoty sledovaných parametrov boli výrazne odlišné u pacientok s karcinómom endometria oproti porovnávacej skupine zdravých žien a pacientok s nenádorovými zmenami ako sú cysty či zápalové ochorenia. U pacientok s endometriózou boli sledované parametre odlišné od zdravých žien, ale ešte nedosahovali hodnoty pacientok s karcinómom endometria, čo potvrdzuje prekancerózny stav a zvýšenú obozretnosť pre ďalšie pravidelné sledovanie týchto pacientok. Záver: Výrazné rozdiely medzi skupinou zdravých žien, sledovanou skupinou endometrióz a karcinómu endometria potvrdzujú optimistický predpoklad aplikácie fluorescenčného neinvazívneho diagnostického monitoringu, avšak vyžadujú väčší súbor pacientok. Výhodou tohto prístupu je zvýšený komfort vyšetrenia pre pacientky.
Táto práca bola podporovaná z projektu VEGA 1/ 0620/ 19.
Obr. 1. Fluorescenčné koncentračné matrice močov gynekologických pacientok. 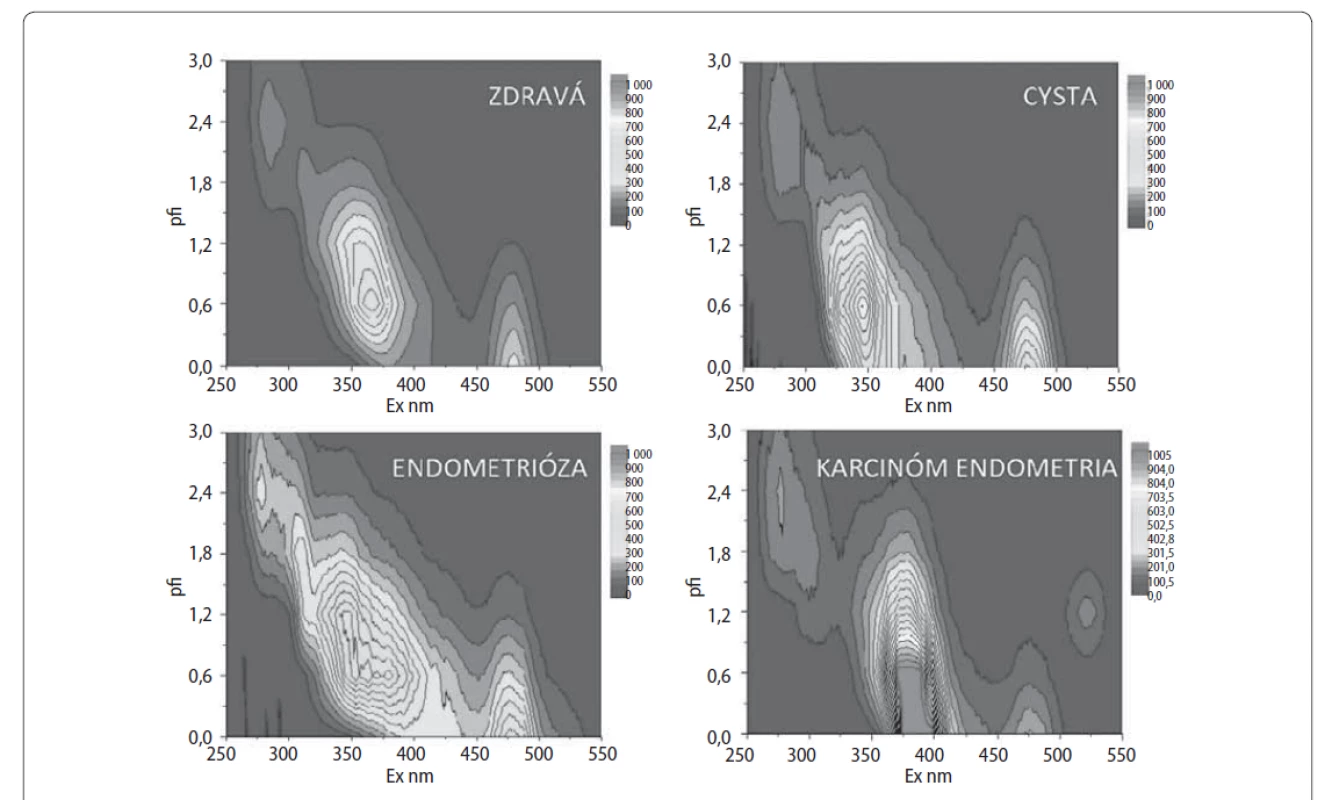
XX/ 256. ANALÝZA ANGIOGÉNNYCH FAKTOROV U ŽIEN PRI PATOLÓGIÁCH UTERU
KLEPCOVÁ Z.1, NAGYOVÁ A.2, RABAJDOVÁ M.1
1Ústav lekárskej a klinickej biochémie, LF UPJŠ v Košiciach, Slovenská republika, 2Gynekologicko-pôrodnícka klinika UN L. Pasteura, Košice, Slovenská republika
Východiská: Endometrióza (EE) spolu s endometriálnym karcinómom (EC) patria medzi najčastejšie sa vyskytujúce gynekologické patológie u žien. EE je charakteristická výskytom ektopického endometriálneho tkaniva mimo uteru a je často asociovaná s EC v dôsledku spoločného mechanizmu stimulácie s estrogénmi a chronickým zápalom. Karcinómu endometria corpus uteri často predchádza endometriálna hyperplázia a je sprevádzaný deregulovanou bunkovou proliferáciou, migráciou, diferenciáciou a apoptózou. V dospelosti sa angiogenéza vyskytuje len sporadicky a to za fyziologických podmienok počas menštruačného cyklu, resp. pre vznik receptívneho endometria, naopak nekontrolovateľná angiogenéza je charakteristická pri raste, metastázovaní a progresii nádorov. Normálna (tzv. self-limited) angiogenéza závisí od rovnováhy medzi pozitívnymi a negatívnymi angiogénnymi faktormi a zahàňa aktiváciu niekoľkých molekúl vrátane proteínov extracelulárnej matrix, proteolytických enzýmov a angiogénnych faktorov ako napr. placentárny rastový faktor (PlGF) a endoglín. PlGF zvyšuje stabilitu ciev a spolu s endoglínom regulujú bunkovú proliferáciu, diferenciáciu, migráciu a adhéziu. Keďže je angiogenéza kľúčová pre progresiu endometriotických lézií a nádorov, rozhodli sme sa študovať tieto angiogénne faktory, nakoľko akákoľvek nerovnováha môže viesť k progresii ochorenia. Cieľ: Cieľom tejto práce bola detekcia angiogénnych proteínov PlGF a endoglínu v sére pacientiek s endometriózou a karcinómom endometria. Metódy: Experimentálna skupina (n = 47) pozostávala z pacientiek s endometriózou (EE) (n = 37) a karcinómom endometria corpus uteri (CE) (n = 10). Na kvantitatívne stanovenie vybraných proteínov bola použitá metóda ELISA. K špecifikácii a kvantifikácii rozdielov štatisticky významných proteínov slúžil Student-Newmanov test a Spearmanova korelácia. Výsledky: Analyzované proteíny preukázali štatistickú významnosť (p ≤ 0,05) a Spearmanov korelačný koeficient (r) sa pohyboval na úrovni -0,4. Pri PlGF bola zistená stredne silná vzájomná závislosť (r = -0,411, p = 0,004) a pre endoglín bola zistená slabá korelačná interakcia (p = 0,007, r = −0,387) medzi pacientkami s endometriózou a karcinómom endometria. Záver: Detekcia špecifických angiogénnych proteínov môže napomôcť pri včasnej diferenciálnej diagnostike.
Táto práca bola podporovaná z projektov VEGA 1/ 0620/ 19, VEGA 1/ 0540/ 2021.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článek EditorialČlánek VI. Radioterapeutické metodyČlánek XI. Psychosociální péčeČlánek XIII. Nádory prsuČlánek XIV. Nádory jícnu a žaludkuČlánek XVIII. Nádory hlavy a krkuČlánek XXI. UroonkologieČlánek XXIV. HematoonkologieČlánek XXVII. COVID-19
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2021 Číslo Supplementum 2- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejasný stín na plicích – kazuistika
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Editorial
- I. Onkologická prevence a screening
- II. Epidemiologie nádorů, klinické registry, zdravotnická informatika
- III. Vzdělávání, kvalita a bezpečnost v onkologické praxi
- IV. Diagnostické metody v onkologii
- V. Onkochirurgie, rekonstrukční chirurgie
- VI. Radioterapeutické metody
- VII. Nežádoucí účinky protinádorové léčby
- VIII. Paliativní péče a symptomatická léčba
- IX. Nutriční podpora v onkologii
- X. Ošetřovatelská péče a rehabilitace
- XI. Psychosociální péče
- XII. Hereditární nádorové syndromy
- XIII. Nádory prsu
- XIV. Nádory jícnu a žaludku
- XV. Nádory tlustého střeva a konečníku
- XVI. Nádory slinivky, jater a žlučových cest
- XVII. Nádory skeletu a sarkomy
- XVIII. Nádory hlavy a krku
- XIX. Nádory hrudníku, plic, průdušek a pleury
- XX. Gynekologická onkologie
- XXI. Uroonkologie
- XXII. Neuroendokrinní a endokrinní nádory
- XXIII. Nádory nervového systému
- XXIV. Hematoonkologie
- XXV. Vývoj nových léčiv, farmakoekonomika, klinická farmacie v onkologii
- XXVI. Základní a aplikovaný výzkum v onkologii
- XXVII. COVID-19
- XXVIII. Varia (ostatní, jinde nezařazené příspěvky)
- Predikce odpovědi na léčbu imunoterapií checkpoint inhibitory u pacientů s pokročilými solidními nádory
- Protektivní faktory prožívaného stresu u pacientů s mnohočetným myelomem
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- XVI. Nádory slinivky, jater a žlučových cest
- VII. Nežádoucí účinky protinádorové léčby
- XV. Nádory tlustého střeva a konečníku
- VIII. Paliativní péče a symptomatická léčba
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



