-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Vasa praevia: incidence, diagnostika, doporučené postupy
Vasa praevia: incidence, diagnosis, recommendations
Objective:
To report up–to date knowledge on diagnostic methods and recommended practices for vasa praevia in pregnancy.Study design:
Review.Methods:
Analysis of available literature resources.Conclusion:
Vasa praevia is among the major pregnancy complications with a low incidence. If they are not diagnosed prenatally, pose a high risk to the fetus. Early prenatally established diagnosis significantly decrease perinatal morbidity and mortality of the newborn. The diagnostic method of choice is ultrasound scan using colour Doppler image. In the case of diagnosis of vasa praevia prenatally, it is recommended termination of the pregnancy by elective cesarean section before the onset of labor activity or rupture of membranes.Key words:
antenatal ultrasound diagnosis – morbidity and mortality of newborn –vasa praevia
Autori: Andrea Galčíková
Pôsobisko autorov: Gynekologicko-porodnické oddělení nemocnice Kyjov
Vyšlo v časopise: Prakt Gyn 2016; 20(1): 49-52
Kategória: Perinatologie: Přehledový článek
Súhrn
Cíl práce:
Podat přehled o diagnostických metodách a doporučených postupech pro vcestné cévy (vasa praevia) v těhotenství.Typ studie:
Souhrnný článek.Metodika:
Analýza dostupných literárních zdrojů.Závěr:
Vasa praevia patří mezi závažné těhotenské komplikace s nízkou incidencí. Pokud nejsou vcestné cévy diagnostikovány prenatálně, představují vysoké riziko pro plod. Včasná prenatálně stanovená diagnóza významně snižuje perinatální morbiditu a mortalitu novorozence. Diagnostickou metodou volby je ultrasonografické vyšetření s použitím barevného dopplerovského zobrazení. V případě stanovení diagnózy vasa praevia prenatálně je doporučováno ukončení těhotenství elektivním císařským řezem dříve, než dojde k nástupu porodní činnosti nebo odtoku plodové vody.Klíčová slova:
morbidita a mortalita novorozence – prenatální ultrasonografická diagnostika – vasa praeviaÚvod
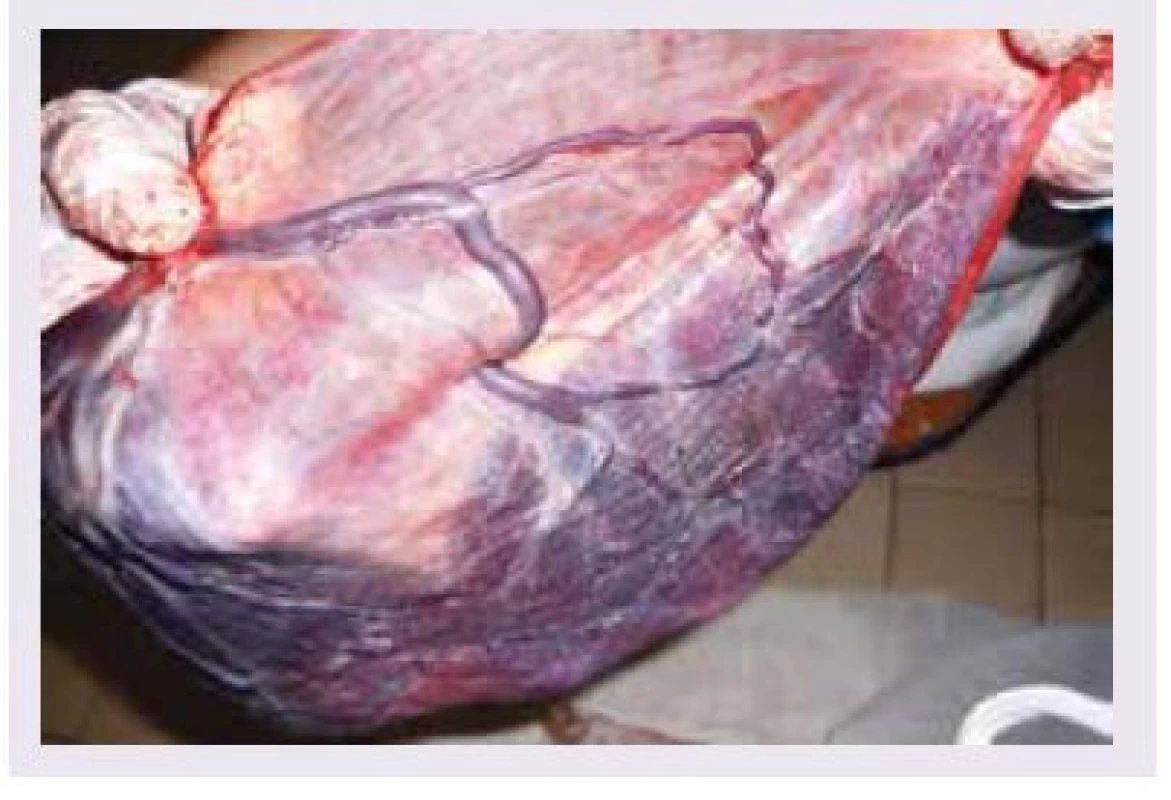
Vasa praevia (vcestné cévy) jsou cévy, které probíhají volně v plodových obalech mimo placentární tkáň a pupečník (obr. 1). Jsou lokalizovány pod naléhající částí plodu v dolním děložním segmentu [1]. Vasa praevia je možné dělit na 2 typy:
typ 1 – pupečník se upíná přímo do obalů (velamentózní úpon) blízko cervikálního kanálu nebo nad ním.
typ 2 – jsou přítomny přídatné laloky placenty a cévy probíhají v blanách mezi jednotlivými laloky [2,3].
Protože vcestné cévy jsou chráněny pouze amniem, ne Warthonovým rosolem, jsou lehce zranitelné a může dojít k jejich roztržení při spontánní nebo arteficiální ruptuře plodových obalů s následným krvácením, které bezprostředně ohrožuje plod. Objem krve plodu ve 2. a 3. trimestru je přibližně 80–100 ml/kg, tedy i relativně malá ztráta krve může mít pro plod závažné následky s nutností podání krevních transfuzí. V krajních případech hrozí vykrvácení plodu [4]. První zmínka o ruptuře vasa praevia byla publikována Lobsteinem v roce 1801 [5]. Tato porodnická komplikace je spojená s vysokou novorozeneckou morbiditou a mortalitou. Pokud nejsou vasa praevia diagnostikovány prenatálně, mortalita novorozenců se pohybuje kolem 50–70 %. Kombinace mortality a morbidity u prenatálně nepoznaných případů dosahuje 70–100 % v případě předčasného porušení plodových obalů a 50–60 % při intaktních plodových obalech před nástupem porodní činnosti [6].
Incidence a rizikové faktory
Incidence vasa praevia kolísá dle různých zdrojů mezi 1 : 1 200 těhotenství až 1 : 6 000 těhotenství [2,7–9]. Počty mohou být podhodnocené, protože některé případy vasa praevia nejsou diagnostikovány prenatálně ani po porodu. Pokud není diagnóza stanovena prenatálně, málokdy uvedou lékaři při antepartálním nebo intrapartálním krvácení jako hlavní diagnózu vasa praevia, často se tato komplikace skrývá pod diagnózu antepartálního krvácení nebo abrupce placenty. Zvýšený výskyt je popisován u gravidit po IVF (in vitro fertilization). Udává se přibližně 1 : 300 těhotenství [10]. Tato asociace není zcela objasněna, předpokládá se podíl narušené orientace blastocysty při implantaci a zvýšená frekvence morfologických variací placenty. Mezi další rizikové faktory pro výskyt vasa praevia patří placentární anomálie jako nízce nasedající placenta, placenta praevia, placenta biloba, multilobární placenta, úpon pupečníku v blanách, placenta membranacea. V některých studiích se až 10 % vasa praevia vyskytuje u dvojčetných gravidit [11]. Asi u 89 % případů vasa praevia je přítomen jeden z výše zmíněných rizikových faktorů [12]. Přibližně 60 % žen s vasa praevia má při ultrasonografickém (USG) vyšetření ve 2. trimestru diagnostikovanou nízce nasedající placentu nebo vcestnou placentu. Asi u 20 % případů vasa praevia je při porodu přítomná nízce nasedající placenta [3].
Diagnostika
K diagnostice vasa praevia lze využít zobrazovací metody (ultrasonografické vyšetření, magnetická rezonance), palpační vaginální vyšetření, amnioskopii nebo průkaz fetální krve při intrapartálním krvácení. Řada případů vasa praevia prenatální diagnostice unikne a je zachycena až intrapartálně na základě klinických příznaků, případně postnatálně. Část případů není zachycena vůbec. Mezi typické klinické příznaky patří bezprostřední krvácení po porušení plodových obalů (spontánním či arteficiálním), na CTG-záznamu (CTG – kardiotokografie) obraz rychle progredujícího distresu plodu, v krajním případě až intrauterinní úmrtí plodu. Intrapartálně při absenci krvácení a zachovaných plodových obalech lze vasa praevia vyhmatat při vaginálním vyšetření jako pulzující rezistenci v blanách, kterou nelze odsunout stranou. Potvrzení diagnózy lze provést vizuálně pomocí amnioskopie, pokud toto vyšetření umožňuje nález na děložním hrdle. Někdy se mohou vasa praevia projevit pouze změnami na CTG-záznamu při útlaku cév naléhající částí plodu. Popisovány jsou decelerace variabilního typu, bradykardie, sinusoida [13,14,15]. Při vaginálním krvácení lze přítomnost fetálního hemoglobinu prokázat pomocí testů, kterými je možné odlišit mateřský a fetální hemoglobin (Kleihauerův-Betkeův test, Apt test, denaturační testy). Testy se ale v klinické praxi téměř nevyužívají pro jejich časovou náročnost nebo nízkou specificitu.
V současnosti je metodou volby v diagnostice vasa praevia USG-vyšetření. Pomocí USG-vyšetření byly vasa praevia popsány poprvé v roce 1987 [11]. V roce 1990 bylo popsáno použití barevného dopplerovského zobrazení při diagnostice vasa praevia [16]. Ultrasonograficky jsou vasa praevia zobrazovány jako lineární struktury nad děložním hrdlem s absencí Warthonova rosolu [17]. Při použití barevného dopplerovského vyšetření se zobrazují pulzace shodné se srdeční frekvencí plodu (obr. 2). Od kličky pupečníku je rozlišíme tím, že při změně polohy matky nemění pozici. Diferenciálně diagnosticky je nutno dále odlišit varikózní cévy dělohy, separace amnia a choria, marginální placentární sinus a amniální pruh. Při použití pouze transabdominální či transvaginální sondy může být USG-zobrazení vasa praevia ztíženo obezitou pacienky, polohou plodu nebo špatným úhlem. Proto se doporučuje kombinovat transabdominální a transvaginální přístup s použitím barevného dopplerovského vyšetření. Pomocí USG lze dle některých studií diagnostikovat antepartálně až 78 % případů vasa praevia [1]. V práci Ruitera et al byla hodnocena přesnost USG-prenatální diagnostiky vasa praevia [18]. Do února 2014 bylo vyhledáno v databázích Medline, Embase, the Cochrane Library a PubMed 583 publikací týkajících se vasa praevia. Autoři vybrali 8 studií, které odpovídaly kritériím QUADAS 2 (Quality Assessment of Diagnostic Accuracy Studies tool) a které se zabývaly USG-diagnostikou vasa praevia. V těchto publikacích se pohybovala úspěšnost prenatální diagnostiky vasa praevia pomocí USG mezi 53–100 %. Ve 2 prospektivních studiích byly zachyceny všechny případy vasa praevia pomocí transvaginálního barevného dopplerovského vyšetření (senzitivita 100 %, specificita 99–99,8 %). Falešná pozitivita USG-diagnostiky je pro nedostatek informací obtížně hodnotitelná. Bronsteen et al popisují ve své studii 5 falešně pozitivních případů, které ale blíže nespecifikují. Normiyama et al uvádějí jeden falešně pozitivní případ a Catanzarite et al popisují také pouze jeden falešně pozitivní případ [2,19,20]. Falešná pozitivita USG-vyšetření ve 2. trimestru pro diagnostiku vasa praevia se pohybuje mezi 10–16 %. Při opakovaném USG-vyšetření ve 3. trimestru se procento falešně pozitivních nálezů může snížit [2,17]. Většina autorů se shoduje, že při použití transvaginálního USG-vyšetření v kombinaci s barevným dopplerovským vyšetřením je přesnost USG-prenatální diagnostiky vasa praevia vysoká. Medián prenatální detekce se pohybuje kolem 93 % a specificita mezi 99–100 %. Podle gestačního stáří převažoval v uvedených studiích záchyt vasa praevia mezi 18.–26. týdnem těhotenství. Přehled studií a počty případů vasa praevia ukazuje tab. 1.
Obr. 2. Ultrasonografické zobrazení vasa praevia 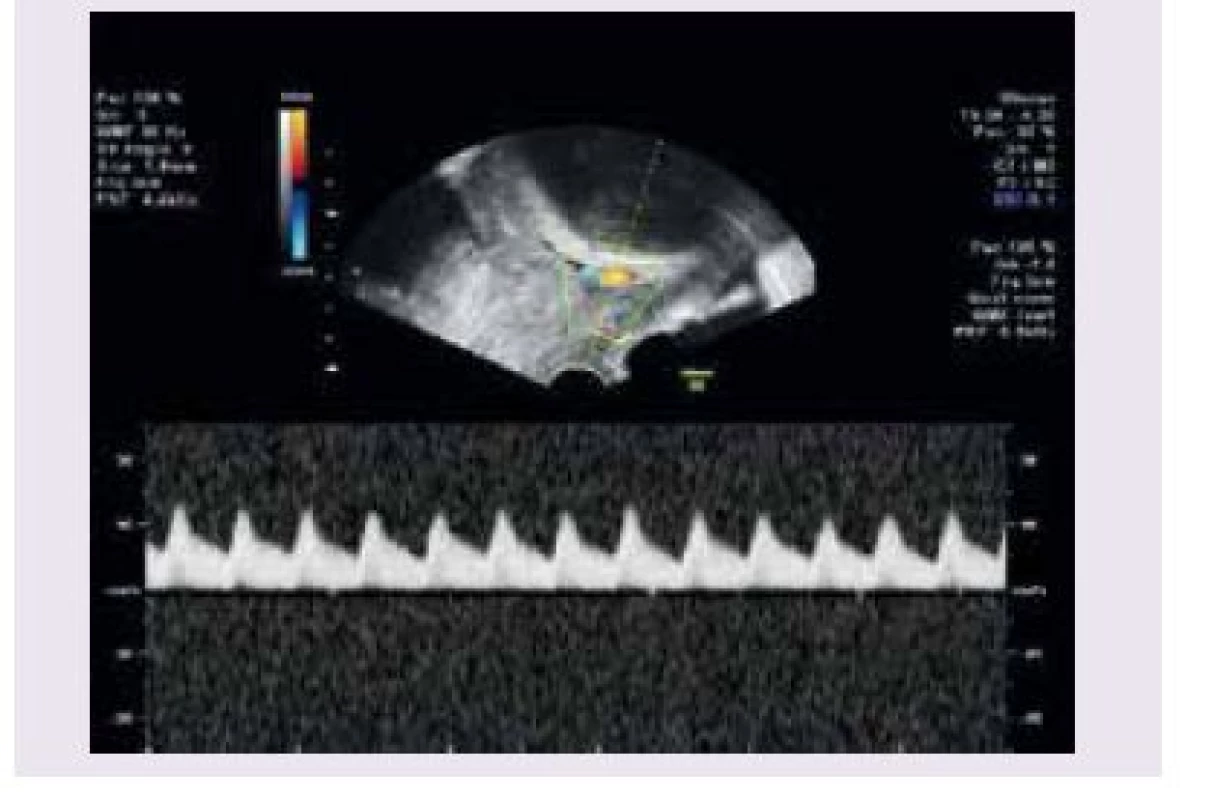
Tab. 1. Přehled studií zabývajících se USG-diagnostikou vasa praevia. 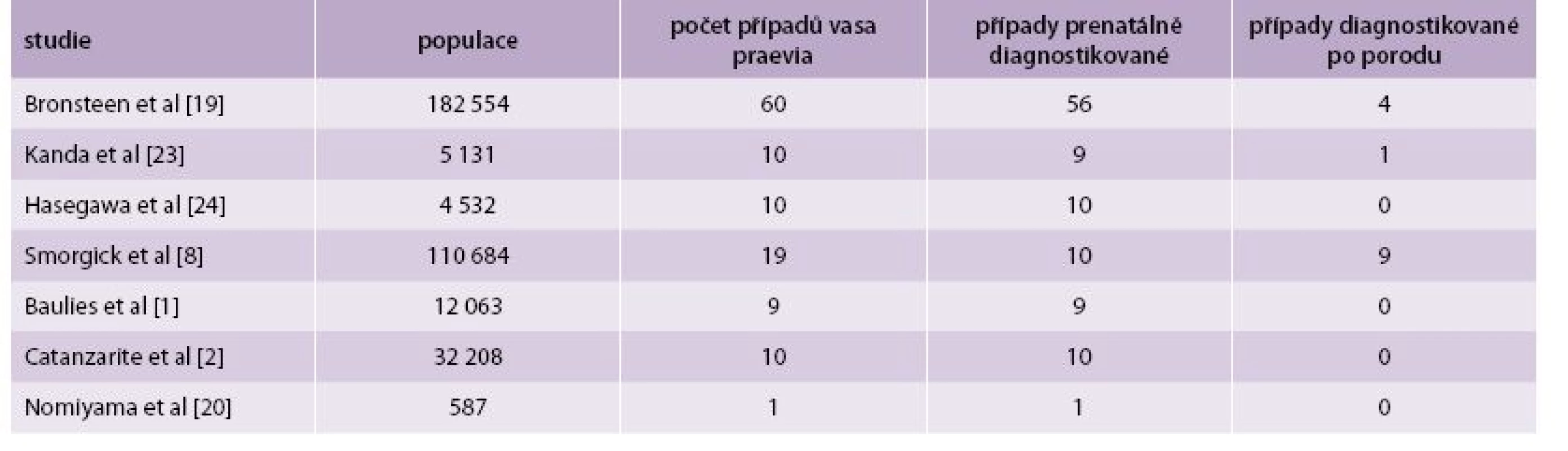
Upraveno dle [19] Jsou popisovány i případy mizejících vcestných cév. Catanzanite a Bronsteen uvádějí, že asi 15 % případů vasa paevia vymizí mezi 2. a 3. trimestrem [2,19]. Proto, pokud je diagnóza stanovena ve 2. trimestru, je nutno zopakovat USG-vyšetření i ve 3. trimestru. V současnosti není doporučováno plošné screeningové USG-vyšetření pro vyhledávání vasa praevia. Většina autorů však doporučuje cílené vyšetření u pacientek s rizikovými faktory pro vasa praevia (gravidita po IVF, vícečetné těhotenství, placenta praevia, rozdělená či přídatná placenta) [3].
V diagnostice vasa praevia lze také použít 3D USG-vyšetření. Je možné jej využít na přesné zobrazení uložení cév před operačním ukončením těhotenství. Dalším vyšetřením, které lze využít k diagnostice vasa praevia, je magnetická rezonance. Omezená dostupnost a vysoká cena toto vyšetření však výrazně limitují.
Prenatální diagnostika vasa praevia je důležitá, protože může významně ovlivnit perinatální morbiditu a mortalitu. Jedna z největších studií Oyelese et al, v níž bylo identifikováno 155 případů vasa praevia, ukázala, že novorozenecká křivka přežití stoupla v případě včasného prenatálního záchytu vasa paevia ze 44 % na 97 % [3]. Nutnost podání transfuze u novorozenců klesla z 58,5 % na 3,4 %. Apgar score živých novorozenců, u kterých nebyla stanovena diagnóza prenatálně, dosahovalo v první minutě průměrné hodnoty 1 a v páté minutě 4. V případě prenatálního stanovení diagnózy dosahovala hodnota Apgar score v 1. minutě 8 a v 5. minutě 9. Výsledky studie potvrdily zásadní význam antenatálního záchytu vcestných cév. Při každém druhotrimestrálním USG-vyšetření by měl být identifikován úpon pupečníku.
Doporučené postupy
Kanadská společnost gynekologů a porodníků vydala v roce 2009 doporučené postupy pro vasa praevia [21], poté v roce 2011 vydala doporučené postupy i Britská společnost gynekologů a porodníků (RCOG) [22]. Doporučení těchto společností jsou:
- pokud je na druhotrimestrálním USG-vyšetření zjištěna nízce nasedající placenta, měl by být zobrazen úpon pupečníku
- transvaginální USG-vyšetření by mělo být provedeno u žen s rizikovými faktory pro vasa praevia
- když je podezření na přítomnost vasa praevia, transvaginální barevné dopplerovské USG-vyšetření může ulehčit diagnostiku
- při stanovení diagnózy antenatálně je nejbezpečnější formou ukončení těhotenství elektivní císařský řez ještě před nástupem kontrakční činnosti nebo před odtokem plodové vody
- u pacientek s diagnostikovanými vasa praevia jsou těhotenství ukončována výrazně dříve před stanoveným termínem porodu, proto je doporučováno zvážit mezi 28.–32. týdnem těhotenství aplikaci kortikosteroidů k indukci plicní maturace plodu
- ve 30.–32. týdnu gravidity je doporučováno u pacientek s rizikem předčasného porodu zvážit hospitalizaci v centrech 3. typu s adekvátní péčí o nezralého novorozence a je nutné počítat s podáním krevních transfuzí novorozenci
- u pacientek bez známek hrozícího předčasného porodu lze zvolit ambulantní sledování s týdenními kontrolami a USG-cervikometrií
- optimální týden ukončení není jasně stanoven, doporučuje se těhotenství ukončit elektivním císařským řezem v období mezi 34.–37. týdnem těhotenství; zásadní je spolupráce s neonatology; je vhodné mít připraveny transfuze 0 Rh negativní krve pro eventuální nutnost podání novorozenci
- při krvácení z vasa praevia po předčasném prasknutí plodových obalů je nutný emergentní císařský řez. Ve vysokém procentu případů je nutná substituce novorozence krevními transfuzemi
Zmíněné postupy mohou zvýšit křivku přežití novorozenců na 97 % [7].
Existuje i mezinárodní nadace pro vasa praevia, která podává informace o diagnostice a doporučených postupech pro vasa praevia pro odbornou i laickou veřejnost (www.vasaprevia.org). Podobnou charitativní organizaci můžeme najít i ve Velké Británii – Vasa Praevia rating awareness (www.vasapraevia.co.uk). Obě nadace se snaží tuto diagnózu objasnit laické veřejnosti, ale poskytují také informace odborné veřejnosti.
Závěr
Incidence vasa preavia je nízká. Většina publikovaných studií je retrospektivních a zahrnuje malé soubory. Z dosavadních studií a klinických zkušeností vyplývá, že cílená prenatální diagnostika vasa praevia může významně zlepšit perinatální výsledky. Nejvhodnější diagnostickou metodou je USG-vyšetření s použitím barevného dopplerovského zobrazení. Na tuto diagnózu je nutné myslet zejména, pokud jsou přítomny rizikové faktory (gravidita po IVF, vcestná placenta, vícečetná gravidita, rozdělená nebo přídatná placenta, velamentózní úpon pupečníku). Vhodným obdobím pro stanovení diagnózy je 2. trimestr a začátek 3. trimestru. Prenatálně stanovená diagnóza s provedením elektivního císařského řezu před nástupem kontrakční činnosti a odtokem plodové vody významně snižuje morbiditu a mortalitu novorozence.
Doručeno do redakce 27. 1. 2016
Přijato po recenzi 29. 2. 2016
MUDr. Andrea Galčíková
agalcikova@azet.sk
Gynekologicko-porodnické oddělení nemocnice Kyjov
Zdroje
1. Baulies S, Maiz N, Munoz A et al. Prenatal ultrasound diagnosis of vasa previa and analysis of risk factors. Prenat Diagn 2007; 27(7): 595–599.
2. Catanzarite V, Maida C, Thomas W et al. Prenatal sonographic diagnosis of vasa previa: ultrasound findings and obstetric outcome in ten cases. Ultrasound Obst Gynecol 2001; 18(2): 109–115.
3. Oyelese Y, Catanzarite V, Prefumo F et al. Vasa previa: the impact of prenatal diagnosis on outcomes. Obstet Gynecol 2004; 103(5 Pt 1): 937–942.
4. Derbala Y, Grochal F, Jeanty P. Vasa previa. J Prenat Med 2007; 1(1): 2–13.
5. Lobstein J. Archives de L´art des Accouchements. Strasbourg 1801.
6. Canterino JC, Mondestin-Sorrentino M et al. Vasa previa: prenatal diagnosis and evaluation with 3-dimensional sonography and power angiography. J Ultrasound Med 2005; 24(5): 721–724.
7. Olexese KO, Turner M, Lees C et al. Vasa previa: an avoidable obstetric tragedy. Obstet Gynecol Surv 1999; 54(2): 138–145
8. Smorgick N, Tovbin Y, Ushakov F et al. Is neonatal risk from vasa previa preventable? The 20-year experience from a single medical center. J Clin Ultrasound 2010; 38(3): 118–122.
9. Stafford IP, Neumann DE, Jarrell H. Abnormal placental structure and vasa previa: confirmation of the relationship. J Ultrasound Med 2004; 23(11): 1521–1522.
10. Schachter M, Tovbin Y, Arieli SY et al. In vitro fertilization is a risk factor for vasa previa. Fertil Steril 2002; 78(3): 642–643.
11. Gianopoulos J, Carver T, Tomich PG et al. Diagnosis of vasa previa with ultrasonography. Obstet Gynecol 1987; 69 (3 Pt 2): 488–491.
12. Lijoi AF, Brandy J. Vasa previa diagnosis and management. J Am Board Fam Pract 2003; 16(6): 543–548.
13. Antoine C, Young BK, Silverman F et al. Sinusoidal fetal heart rate pattern with vasa previa in twin pregnancy. J Reprod Med 1982; 27(5): 295–300.
14. Curl CW, Johnson WL. Vasa previa, antepartum diagnosis. Report of a case. Obstet Gynecol 1968; 31(3): 328–330.
15. Naftolin F, Mishell DR Jr. Vasa previa. Report of 3 cases. Obst Gynecol 1965; 26(4): 561–565.
16. Nelson LH, Melone PJ, King M. Diagnosis of vasa previa with transvaginal and color flow Doppler ultrasound. Obstet Gynecol 1990; 76(3 Pt 2): 506–509.
17. Lee W, Lee VL, Kirks JS et al. Vasa previa: prenatal diagnosis, natural evolution, and clinical outcome. Obstet Gynecol 2000; 95(4): 572–576.
18. Ruiter L, Kok N, Limpens J et al. Systematic review of accuracy of ultrasound in the diagnosis of vasa previa. Ultrasound Obstet Gynecol 2015; 45(5): 516–522.
19. Bronsteen R, Whitten A, Balasubramanian M et al. Vasa previa: clinical presentations, outcomes, and implications for management. Obstet Gynecol 2013; 122(2 Pt 1): 352–357.
20. Nomiyama M, Toyota Y, Kawano H. Antenatal diagnosis of velamentous umbilical cord insertion and vasa previa with color Doppler imaging. Ultrasoun Obstet Gynecol 1998; 12(6): 426–429.
21. Gagnon R, Morin L, Bly S et al. Guidelines for the Management of Vasa Previa. J Obstet Gynaecol Can 2009; 31(8): 748–760.
22. Royal College of Obstetricians and Gynaecologists. Placenta Praevia, Placenta Praevia Accreta and Vasa previa: Diagnosis and Management. RCOG Green-top Guidelline No.27. January 2011. Dostupné z WWW: <https://www.rcog.org.uk/globalassets/documents/guidelines/gtg_27.pdf>.
23. Kanda E, Matsuda Y, Kamitomo M et al. Prenatal diagnosis and management of vasa previa: a 6 years review. J Obstet Gynaecol Res 2011; 37(10): 1391–1396.
24. Hasegawa J, Farina A, Nakamura M et al. Analysis of the ultrasonographic findings predictive of vasa previa. Prenat Diagn 2010; 30(12–13): 1121–1125.
Štítky
Detská gynekológia Gynekológia a pôrodníctvo Reprodukčná medicína
Článok vyšiel v časopisePraktická gynekologie
Najčítanejšie tento týždeň
2016 Číslo 1- Ne každé mimoděložní těhotenství musí končit salpingektomií
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Gynekologické potíže pomáhá účinně zvládat benzydamin
- Mýty a fakta ohledně doporučení v těhotenství
-
Všetky články tohto čísla
- Jaká je adekvátní velikost kónusu?
- Riziko nádorů štítné žlázy u žen léčených pro infertilitu
- Fertilitu šetřící léčba u žen s karcinomem endometria
- Prevence nádorových onemocnění u žen – výzkumné šetření o využití možností prevence nádorových onemocnění v ženské populaci
- Editorial
- Fyzioterapie po operaci prsu
- Implementace přípravku klasické čínské medicíny do obvyklé léčby vulvovaginálního diskomfortu
- Dysfunkční krvácení v období dospívání
- Myoinositol a jeho léčebné možnosti
- Vasa praevia: incidence, diagnostika, doporučené postupy
- Význam cholinu v nutriční suplementaci u těhotných
- Chirurgické řešení náhlé příhody břišní v graviditě: kazuistika
-
Bikram jóga
Rozhovor s Terezou Bonnet Šenkovou -
PragueONCO – již 7. pražské mezioborové onkologické kolokvium
Zpráva z onkogynekologické sekce, 27.–29. ledna 2016, Praha - Michael J. Halaška, Lukáš Rob a kolektiv. Onkologická onemocnění během těhotenství
-
Emoční konflikty - možná příčina onko(gyneko)logických onemocnění a jak se s nimi vypořádat
Rozhovor s Gabrielou Benešovou
- Praktická gynekologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Vasa praevia: incidence, diagnostika, doporučené postupy
- Dysfunkční krvácení v období dospívání
- Jaká je adekvátní velikost kónusu?
-
Emoční konflikty - možná příčina onko(gyneko)logických onemocnění a jak se s nimi vypořádat
Rozhovor s Gabrielou Benešovou
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy