-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Septický šok u pacienta s Fourniérovou gangrénou s fatálním koncem
Septic Shock in a Patient with the Fourniér Gangrene with Fatal Outcome
Aim:
The authors present a case of a patient with developed Fourniér gangrene and septic shock. Fourniér gangrene belongs to the group of local non-specific infection of soft tissues (NSTI). Its incidence is relatively low, but the infection is extraordinary aggressive with a possible lethal end.Material and Method:
39 years old patient with 4 days history of Fournier gangrene’s development was admitted in irreversible septic shock. The initial APACHE II score was 36. The delay in treatment was an important factor in the further course of illness with lethal end.Results:
Above the mentioned 39 years old patient died because of septic shock. The hemorrhagic cystitis was the original source of infection with further development of Fourniér gangrene according to the pathological record.Conclusion:
We often come across all different kinds of stages of sepsis from the MODS to the septic shock for patients with Fourniér gangrene. Causal treatment should be started early. The local surgical excision and wide broad antibiotic administrations are basic treatments in the context of other treatment modalities according to the current patient’s needs. The adjuvant hyperbaric oxygen treatment takes place in patients with Fourniér gangrene as well and is beneficial. The following factor even worsens the illness prognosis: delay in diagnostic, higher age, anorectal origin of infection, the amount of organ with dysfunction or failure, diabetes mellitus and significant immunodeficiency.Key words:
Fourniére – gangrene – focal – NSTI – sepsis
Autori: P. Zonča; T. Mrázek; A. Matušek; Hájek M.. Štiglerová S. 1 1; A. Jurytko; C. Kučera 1; M. Nieslanik 2
Pôsobisko autorov: Chirurgické a traumatologické oddělení, MN Ostrava, primář: MUDr. T. Mrázek, Ph. D. ; Oddělení ARO, pracoviště Hyperbarické komory, MN Ostrava, primář: MUDr. C. Kučera 1; Oddělení patologie, MN Ostrava, emeritní primář: MUDr. M. Nieslanik 2
Vyšlo v časopise: Rozhl. Chir., 2009, roč. 88, č. 7, s. 398-402.
Kategória: Monotematický speciál - Původní práce
Súhrn
Cíl:
Autoři prezentují kazuistiku pacienta s rozvinutou Fourniérovou gangrénou a septickým šokem. Fourniérova gangréna patří do skupiny lokálních nespecifických infekcí měkkých tkání (NSTI). Její incidence je relativně nízká, avšak jde o mimořádně agresivní infekci s možným fatálním koncem.Materiál a metoda:
39letý pacient se čtyřdenní anamnézou rozvoje Fourniérovy gangrény byl přijat k hospitalizaci ve stadiu septického šoku, který byl již ireverzibilní. Vstupní hodnota APACHE II skóre byla 36. Pozdní zahájení léčby sehrálo významnou roli v dalším průběhu onemocnění s letálním koncem.Výsledky:
Výše uvedený 39letý pacient zemřel na septický šok. Příčinou Fourniérovy gangrény podle pitvy byla rozsáhlá hemoragická cystitida.Závěr:
S různě pokročilým stavy sepse od MODS až po septický šok se u pacientů s Fourniérovou gangrénou setkáváme relativně často. Je nutné včas zahájit kauzální léčbu. Lokální léčba chirurgickou excizí a léčba širokospektrými antibiotiky je bazální léčbou v kontextu dalších léčebných opatření podle aktuálního celkového stavu pacienta. Adjuvantní léčba v hyperbarické komoře má rovněž své místo, která přináší svůj benefit. Prognózu pacientů zhoršují následující faktory: pozdní diagnóza, vyšší věk, anorektální příčiny infekce, počet selhávajících orgánů při přijetí, DM a významný imunodeficit.Klíčová slova:
Fourniére – gangréna – lokální – NSTI – sepseÚVOD
Léčba sepse a septických komplikací patří ke každodenní praxi chirurgických oddělení a chirurgických jednotek intenzivní péče. Úmrtí na septické onemocnění podle údajů SepNetu stojí na třetím místě příčin smrti. Incidence těžké sepse popřípadě septického šoku je 116/100000 (SepNet). Léčba sepse představuje závažný medicínský, ale i ekonomický problém Uvádí se, že asi 30 % rozpočtu jednotek intenzivní péče je věnováno léčbě septických stavů. Jednou z možných příčin sepse, se kterou se setkáváme na chirurgických odděleních, jsou nekrotizující infekce měkkých tkání (NSTI). Existuje řada jejich forem. Fourniérova gangréna se řadí mezi fokální NSTI.
Fourniérova gangréna je definována jako rychle se rozvíjející nekrotizující infekce subkutánních a epifasciálních tkání perianogenitální oblasti [1].
Cílem této práce je ukázat na kazuistice pacienta s fatálním koncem na závažnost a možný razantní průběh Fourniérovy gangrény. Fourniérova gangréna s sebou přináší nejenom lokální destrukci tkání, ale také způsobuje závažnou alteraci celého organismu. Infekce může vést až k septickému šoku a smrti pacienta. Pouze včasná adekvátní terapie dokáže zabránit možným důsledkům nebo je může alespoň zmírnit. Léčba sepse ve stadiu šoku je už velmi náročná a je provázená vysokou mortalitou.
První literární zmínky o tomto onemocnění jsou od Jeana Fourniéra, pařížského dermatologa a venerologa, který v roce 1883 popsal v literatuře toto onemocnění u 5 pacientů. Tehdy definoval jako zásadní znaky onemocnění náhlý začátek u zdravých mladých mužů, rychlý rozvoj gangrény a absenci jednoznačné příčiny zánětu [2]. Baurienne popsal tento typ onemocnění již v roce 1764. Meleny v roce 1924 v Číně popsal generalizovanou formu onemocnění pod názvem streptokoková gangréna [3]. Již tehdy poukázal na nutnost včasné léčby. V roce 1952 referoval Wilson o nekrotizující fasciitidě. V 90. letech 20. století byly publikovány práce o „masožravých“ bakteriích. Není bez zajímavosti, že prof. Jan Hirschmann z Washingtonské Univerzity na Klinické patologické konferenci v Baltimore prezentoval práci o příčině smrti krále Heroda Velikého, která mohla být způsobena Fourniérovou gangrénou. Prezentoval teorii, že původní infekce Schistosoma hematobium způsobila renální selhání a následně vznik píštělí se vznikem Fourniérovy gangrény a rozvojem sepse.
KAZUISTIKA
Autoři prezentují kazuistiku 39letého pacienta s Fourniérovou gangrénou a rozvinutým septickým šokem.
Z osobní anamnézy byla u pacienta přítomna mentální retardace. Žádné ze sledovaných chorob nebyly přítomné včetně onemocnění s imunodeficitem. Pacient byl bez trvalé medikace. Právě tak nebyla známa žádná alergie. V předchorobí figurovala blíže nespecifikovaná operace ledvin v dětském věku.
Pacient měl čtyřdenní anamnézu rozvoje Fourniérovy gangrény. První den byl ošetřen podle záznamu u obvodního lékaře lokálním antimykotikem pro opruzeniny na zevním genitálu. Druhý a třetí den zůstal v domácím léčení. Čtvrtý den po zhoršení lokálního nálezu a zhoršení celkového stavu s dušností a neklidem následovala hospitalizace na jiném pracovišti. Zde po neodkladném lokálním ošetření a provedení epicystostomie byl pacient přeložen na septickou chirurgickou JIP našeho pracoviště, která se specializuje mimo jiné na léčbu NSTI a je vybavena hyperbarickou komorou.
Při přijetí u pacienta dominovala kvantitativní porucha vědomí na úrovni kómatu, hemodynamická instabilita se systémovým TK 60/40 mm Hg a HR 140/min a RR 25/min se zapojováním auxiliární svaloviny. Pacient byl při přijetí afebrilní s tělesnou teplotou 36,0 °C.
Lokální nález při přijetí je prezentován na fotografii (Obr. 1).
Obr. 1. Iniciální lokální ošetření pacienta incizemi a kontraincizemi s drenáží z původního pracoviště (vhodná je excize tkání) Pic. 1. The initial patient’s local treatment using the incision and secondary incisions with drainage from previous hospital (excision of tissue is proper) 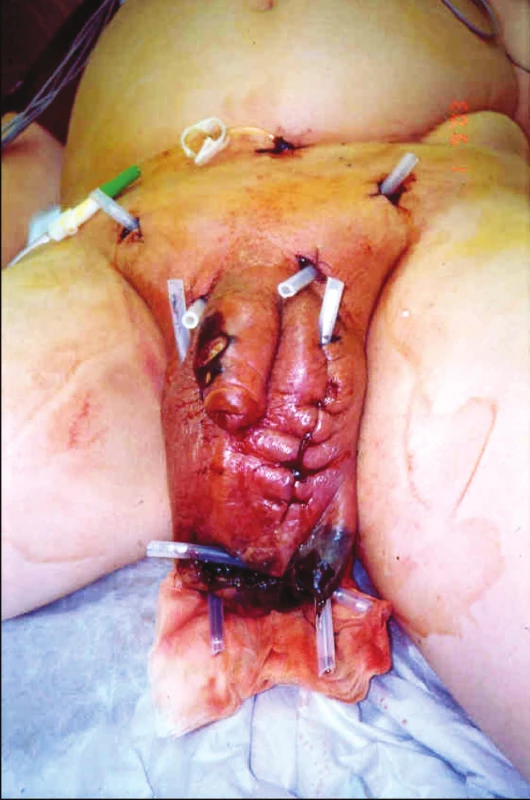
Z laboratorních výsledků byla přítomná leukocytóza 32 tis/mm3, CRP 244 mg/l, prokalcitonin 9 ng/ml, urea 44,8 mmol/l, kreatinin 646 mmol/l a albumin měl hodnotu 14 g/l. PaO2 mělo hodnotu 7,1 kPa. Vstupní APACHE II skóre bylo 36, což odpovídá predikci úmrtí 85,1 %. Výše uvedené klinické a laboratorní parametry odpovídají septickému šoku.
Při přijetí byla nutná okamžitá orotracheální intubace s následnou arteficiální ventilací. Byla použita řízená ventilace s dechovými objemy 6 ml/kg a plateau bylo udržováno pod 30 cm H2O. Pacient byl analgosedován nízkou dávkou metamizolu a sufentanilu. Byla aplikována masivní volumová náhrada kombinací krystaloidů a koloidů centrálním venózním katétrem. Byly aplikovány katecholaminy (noradrenalin, dobutamin) a rovněž byly provedeny další opatření včetně aplikace širokospektrých ATB a antimykotik. Vzhledem k nedostatečné odpovědi na vysoké dávky katecholaminů byla kontinuálně podávána nízká dávka terlipresinu. Byla podána nízká dávka kortikoidů (hydrocortison 100 mg). Hodnota PaO2 /FiO2 < 300 mm Hg ukazovala rovněž na akutní plicní poškození. Cílem úvodní terapeutické intervence byla snaha o rychlou přípravu pacienta k radikální excizi postižených tkání. V rámci této přípravy k chirurgické sanaci infekčního ložiska byla rovněž modulace hemokoagulačního systému (substituce AT III, Protromplex). Na druhé straně byl rovněž podán LMWH. Dále byla použita veškerá dostupná standardní léčba a ošetřovatelská péče. Přes veškerá léčebná opatření pacient zemřel 2 hodiny po přijetí na naše pracoviště na septický šok. Vzhledem k tomu, že nebylo dosaženo ani relativní hemodynamické stability, nebyl časový prostor k provedení původně plánovaných chirurgických excizí infikovaných tkání. Rovněž nebyla aplikována léčba v hyperbarické komoře.
Podle provedené pitvy byla příčinou Fourniérovy gangrény u tohoto pacienta hemoragická cystitida (Obr. 2). Výsledky kultivace z ran a hemokultur identifikovaly smíšenou aerobní a anaerobní flóru.
Obr. 2. Závěr pitevního protokolu Pic. 2. The result of postmortem record 
Mentální alterace pacienta sehrála pravděpodobně největší roli v pozdní hospitalizaci.
DISKUSE
Fourniérova gangréna může postihovat všechny věkové skupiny. V literatuře byly popsány dokonce případy postižení u novorozenců. Přestože toto onemocnění je typické pro muže, byly popsány i případy genitální gangrény u žen. Někdy se uvádí, že toto onemocnění je asociované s horšími socioekonomickými podmínkami. Na druhé straně se uvádí, že nejvyšší incidence je v USA a Kanadě. Onemocnění v Africe a Asii se svojí etiologií liší od forem onemocnění v Evropě a Americe. Kůže jako zdroj sepse je častější v rozvojových zemích a mortalita při tomto typu infekce je nižší [4, 5]. Fourniérova gangréna se vyskytuje v souvislosti se systémovými onemocněními. Jde především o diabetes mellitus, maligní onemocnění a další onemocnění provázené sníženou imunitou. Rovněž se uvádí chronický alkoholismus. U HIV pozitivních pacientů může být Fourniérova gangréna jednou z prvních známek HIV infekce. Rovněž se uvádí možnost výskytu Fourniérovy gangrény v případě systémových onemocněních jako jsou vaskulitidy a další [6]. Mortalita na Fourniérovu gangrénu se podle literatury pohybuje mezi 7–50 % [7]. Histologicky je Fourniérova gangréna charakterizovaná obliterující endarteritidou a trombózou cév v podkoží, fasciální nekrózou a infiltrací leukocytů. Směrem laterálním a směrem dorzálním jsou díky anatomickým poměrům limitované možnosti šíření infekce, avšak směrem kraniálním se může infekce volně šířit. Vzhledem k tomu, že testikulární arterie jsou přímou větví aorty, je postižení varlat extrémně vzácné. Nekrotizující fasciitida je způsobená polymikrobiální nebo monomikrobiální infekcí. Na tomto základě se někdy dělí na typ I a typ II. Typ I je způsoben smíšenou aerobní a anaerobní flórou. Nejčastěji jsou identifikovány Escherichia coli, Bacteroides, Streptokoky, Staphylokoky, Peptostreptokoky a Clostridia. Typ II je způsobený skupinou A streptokoků. Bývá spojován s tupým nebo penetrujícím traumatem, varicellou nebo užíváním NSAID [8]. Ačkoliv původní autor prof. Fourniér toto onemocnění označil jako onemocnění bez zřejmé příčiny, většina současných autorů se shoduje, že je možné vystopovat příčinu infekce [9, 10]. Soudí se, že v případě neidentifikování příčiny Fourniérovy gangrény, je tato příčina prostě přehlédnuta. Obecně můžeme příčiny rozdělit na urogenitální, anorektální a kožní. K nejčastějším urogenitální příčinám patří periuretrální infekce, uretrální striktury, karcinom močového měchýře, dlouhodobé zavedení permanentního močového katétru, traumatická katetrizace, epididymo-orchitida a biopsie prostaty. K anorektálním příčinám patří perianální abscesy a píštěle, komplikace kolorektálního karcinomu, hemoroidektomie, anální divulze, rektální biopsie, divertikulitida, perforace rekta a Crohnova nemoc. Ke kožním příčinám patří okultní trauma a komplikace vazektomie, orchidektomie, operace tříselné kýly a povrchové kožní abscesy. Klinicky se Fourniérova gangréna projevuje typickou triádou: těžká bolest, otok, teplota a další příznaky infekce. Lokálně nacházíme buly, krepitus a celkové příznaky gangrény. Příznaky objevující se na kůži jsou jen špičkou ledovce. Laboratorní hodnoty vykazují známky zánětu s další alteraci podle přítomnosti nebo nepřítomnosti MODS či sepse. RTG může ukázat charakteristické známky emfyzému, zejména v případě anaerobní infekce. USG vyšetření je užitečné v rozlišení Fourniérovy gangrény od intraskrotální patologie. CT nebo MRI pomohou ozřejmit hranice procesu a určit případný zdroj infekce v intraabdominálním nebo retroperitoneálním procesu. Dále se k diagnostice používá „Finger test“. Provádí se v lokální anestezii v místě předpokládané lokalizace gangrény. Po provedení cca 2 cm dlouhé incize následuje probatorní manévr zanořením prstu směrem k hluboké fascii. Pokud je možno proniknout bez odporu přes podkoží, je test pozitivní. Navíc chybění krvácení je zřejmou známkou nekrotizujícího procesu. V mnoha případech dochází k sekreci tekutiny, která je charakterizována jako voda ze špinavého nádobí. Další diagnostickou možností je rychlá biopsie na zmrzlo [11]. Zásadní v léčbě je včasná diagnóza s chirurgickou radikální excizí a okamžitým zahájením antibiotické event. i antimykotické léčby. V případě rozvinutého onemocnění jsou důležitá veškerá opatření vedoucí k hemodynamické stabilizaci pacienta a zabránění rozvoje multiorgánové dysfunkce či multiorgánového selhání. Samozřejmý je rovněž lokální odběr vzorků k mikrobiologickému vyšetření a odběr krevních kultur. Mikrobiologická monitorace se provádí v průběhu celého onemocnění. Opakované chirurgické revize jsou nevyhnutelné. Zásadní pro chirurgickou léčbu je excize postižené tkáně až do oblasti zdravé tkáně. Pouhé incize s kontraincizemi jsou nedostatečné. Někteří autoři v literatuře uvádějí miniinvazivní zákroky. Tyto jsou ale podle našich zkušenosti u plně rozvinutých forem Fourniérovy gangrény nevhodné. Zpočátku revize provádíme v celkové anestezii. Posléze pokud to stav dovolí, tak provádíme intervence ve svodné anestezii. Převazy je nutné provádět 2–4x denně podle aktuálního stavu [12]. Na základě lokálního stavu je třeba zvážit diverzi. S výhodou používáme hyperbarickou léčbu [13]. Hyperbarická oxygenace zlepšuje tkáňovou oxygenaci, optimalizuje funkci neutrofilů, inhibuje růst anaerobních bakterií, zvyšuje tvorbu volných radikálů, zlepšuje transport antibiotik přes bakteriální stěnu, zlepšuje formaci kolagenu, růst fibroblastů a angiogenezi, snižuje systémovou toxicitu a zlepšuje demarkaci infekce. Defekty ponecháváme k sekundárnímu hojení, eventuálně po zvládnutí infekce je možno zvážit překrytí defektů kožními štěpy event. myokutánními laloky. Často se setkáváme s velkými systémovými komplikacemi, které musí být adekvátně léčeny. Musíme řešit GIT krvácení, srdeční selhávání, renální selhávání a další komplikace. Častý je rovněž výskyt pneumonie v terénu oslabeného organismu. Na zvážení je rovněž imunomodulační léčba. Nesmí se zapomínat na adekvátní výživu pacienta. Špatnými prognostickými známkami je vyšší věk, anorektální příčiny infekce, počet selhávajících orgánů při přijetí, DM a rovněž se uvádí horší prognóza u žen. Wong a kol. jednoznačně ukázali, že prodleva mezi nástupem symptomů a operací vede ke zhoršení přežití [14].
Závažným medicínským problémem je pak již léčba ve stádiu těžké sepse nebo septického šoku. Incidence septických stavů má stoupající tendenci. Je k dispozici řada studií a guidelinů zabývajících se léčbou sepse. V současnosti neexistuje žádný jednotlivý parametr, který by vedl k diagnóze sepse. Diagnóza se stanovuje vždy na základě kombinace klinického nálezu, vitálních parametrů, laboratorních hodnot, hemodynamických parametrů a orgánových funkcí. Dalším zásadním problémem je to, že bakteriemii prokážeme pouze u 30 % pacientů s těžkou sepsí nebo septickým šokem [15]. Celkově asi u 30 % pacientů není prokázáno mikrobiologicky žádné agens i přesto, že infekce je podle klinického nálezu vysoce pravděpodobná [16]. V případě, že je prokázáno infekční agens, je často interpretace mikrobiologického nálezu problematická, protože se může jednat pouze o kolonizaci. Kritičtí nemocní pacienti často vykazují SIRS a MODS, avšak jednoznačná spojitost s infekcí nemusí být prokázána. Diagnostická kritéria pro sepsi, těžkou sepsi a septický šok byla stanovena na konsenzuální konferenci ACCP/SCCM [17]. Diagnostická kritéria jsou dána přítomnosti infekce, která může být potvrzena mikrobiologicky nebo na základě klinických kritérií. Dále je významné hodnocení zánětlivé odpovědí a akutní orgánová dysfunkce. Významnou platformou jsou International Sepsis Forum (ISF) a Surviving Sepsis Campaign (SSC), kde je možno najít aktuální zprávy o diagnostických, preventivních možnostech sepse a o posledních novinkách v léčbě sepse. Léčbu je možno rozdělit na kauzální, podpůrnou a adjunktivní.
Kauzální léčbou je chirurgická sanace infekčního ložiska a antibiotická léčba podle výše uvedených zásad.
Sanace chirurgického ložiska je doporučena na základě důkazů Ic (klasifikační kritéria Oxford Centre of Evidence Based Medicine) [18]. Časná intravenózní anti - biotická léčba redukuje letalitu u pacientů s gramnegativní bakteriemii, grampozitivní bakteriemii a sepsi [19]. Je důležité zahájit léčbu co nejčasněji po stanovení diagnózy sepse [20]. Tato opatření jsou doporučena na základě důkazů IIIb. Významné je to, že antibiotický režim musí být každých 48–72 hodin na základě klinických a mikrobiologických kritérií znovu zhodnocen. Musí být vyhodnoceno antimikrobiální spektrum, riziko rezistence, toxicita a náklady léčby. Délka antibiotické léčby se řídí klinickou odpovědí. Obecně by ale neměla překročit 7–10 dní. Tato doporučení jsou doporučeními expertů (stupeň důkazů V). Dalším významným faktorem v léčbě sepse je hemodynamická stabilizace pacienta. Cílem hemodynamické stabilizace je dosažení adekvátní dodávky kyslíku buňkám při těžké sepsi nebo septickém šoku [21]. Uvádí se, že využití rozšířené hemodynamické monitorace nemá vliv na zlepšení přežití a morbiditu, přesto je však doporučeno při použití vyšších dávek vazopresorů (stupeň důkazů V). K iniciálním krokům hemodynamické stabilizace patří aplikace objemové terapie. K tomuto slouží aplikace 500–1000 ml krystaloidů nebo 300–500 ml koloidů během 30 minut. Opakování objemové výzvy se řídí klinickou odezvou a tolerancí. Současná data nedoporučují zcela jednoznačné použití určitého vazopresoru, ale všeobecně je noradrenalin doporučován jako lék první volby [22]. Důležité je dosažení ScvO2 více než 70 %. Toto je dosaženo aplikací tekutin, při nízké hodnotě hemoglobinu aplikací transfuzí nebo event. podáním dobutaminu (stupeň důkazů Ib). Existuje řada dalších doporučení pokud jde o hemodynamickou stabilizaci. K adjunktivní terapii patří podávání kortikoidů a rekombinantního aktivovaného proteinu C, které jsou doporučeny za specifických situací. Léčba antitrombinem III není doporučována. Další doporučení týkající se léčby imunoglobuliny, selenem, ibuprofenem, růstovém hormonem, prostaglandiny, pentoxifylinem, vysokých dávek N-acetylcysteinu, plazmaferézou, hemodiafiltrací, profylaxe trombózy, výživy, aplikace imunonutrice, inzulinoterapie, antiulcerózní terapie, aplikace krevních derivátů, sedace, analgezie, neuromuskulární blokády a dalších jsou přehledně shrnuty v doporučeních léčby sepse.
Při léčbě Fourniérovy gangrény se nesmí podcenit první příznaky. Léčbu je třeba zahájit včas v plném rozsahu. Nezbytná je dostatečně radikální excize postižených tkání spolu s aplikací antibiotik jako kauzální léčby. V případě rozvinuté systémové infekce ve formě těžké sepse nebo septického šoku se pak léčba stává po všech stránkách náročnější. Kromě kauzální léčby infekce je nutná komplexní terapie s cílem podpory jednotlivých selhávajících orgánových systémů.
MUDr. Pavel Zonča, Ph.D., FRCS
Siegfried Leopold Str. 51
53225 Bonn
Germany
Zdroje
1. Smith, G. L., Bunker, C. B., Dinneen, M. D. Fourniér gangrene. Br. J. Urol., 1998, 81 : 347–355.
2. Fournier, J. A. Gangrene foudroyante de la verge. Medecin Pratique, 1883, 4 : 589–597.
3. Meleney, F. L. Hemolytic streptococcus gangrena. Arch. Surg., 1924, 9, 317–364.
4. Stephens, B. J., Lathrop, J. C., Rice, W. L., Gruenber, J. C. Fourniér‘s gangrene, historic (1764–1978) versus contemporary (1979–1988) differences in etiology and clinical importace. Am. Surg., 1993, 59, 149–154.
5. Tripathi, F. M., Khanna, N. N., Venkateshwarlu, V., Sinha, J. K. Gangrene of the scrotum: a series of 20 cases. Br. J. Plast. Surg., 1978, 31 : 242–243.
6. Baskin, L. S., Dixon, C., Stoller, M. L., Carroll, P. R. Pyoderma gangrenosum presenting as Fourniér‘s gangrene. J. Urol., 1990, 144, 984–986.
7. Ersay, A., Yilmaz, G., Akgun, Y., Celik, Z. Factors Affecting Mortality of Fourniér’s Gangrene, Review of 70 Patients. ANZ J. Surg., 20007, 77 (1–2), 43–48.
8. Elliott, D., Kucera, J. A., Myers, R. A. The Microbiology of Necrotizing Soft Tissue Infections. Am. J. Surg., 2000, 179(5), 361–366.
9. Clayton, M. D., Fowler, J. E. jr., Sharifi, R., Pearl, R. K. Cause, presentation and survival of fifty-seven patients with necrotizing fasciitis of the male genitalia. Surg. Gynecol. Obstet, 1990, 170, 49–55.
10. Veselský, Z., Macek, P., Rýdel, L., Prošvic, P., Förstl, M., Plíšek, S. Fourniérova gangréna. Rozhl. Chir., 2002, 81 (7), 357–359.
11. Eke, N. Fourniér‘s gangrena, the Nigerian experience. Nig. Postgrad. Med. J., 1999, 6, 99–102.
12. Matušek, A., Martínek, L., Chmelař, D., Krásová, Z. Fourniérova gangréna. Rozhl. Chir., 1998, 77(1), 24–26.
13. Hollabaugh, R. S., Dmochowski, R. R., Hickerson, W. L., Cox, C. E. Fourniér‘s gangrene: therapeutic impact of hyperbaric oxygen. Plast. Reconstr. Surg., 101, 94, 1998.
14. Wong, C., Chang, H., Pasupathy, S., Khin, L., Tan, J., Low, C. Necrotizing fasciitis: clinical presentation, mikrobiology, and determinants of mortality. JBJS 2003, 85, 1454–1460.
15. Martin, G. S., Mannino, D. M., Baton, S., Moss, M. The epidemiology of sepsis in the United States from 1979 through 2000. N. Engl. J. Med., 2003, 348 : 1546–1554.
16. Alberti, C., Brun-Buisson, C., Burchardi, H., et al. Epidemiology of sepsis and infection in ICU patients from an international multicentre kohort study. Intensive Care Med., 2002, 28 : 108–121.
17. ACCP/SCCM Consensus Conference Committee. Definition for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. Crit. Care Med., 1992, 20 : 864–874.
18. Kaiser, R. E., Cerra, F. B. Progressive necrotizing surgical infections – a unified approach. J. Trauma, 1981, 21, 349–355.
19. Harbarth, S., Ferriere, K., Hugonnet, S., Ricou, B., Suter, P., Pittet, D. Epidemiology and prognostic determinant of bloodstream infections in surgical intensive care. Arch. Surg., 2002, 137, 1353–1359.
20. Dellinger, R. P., Carlet, J., Masur, H., et al. Surviving Sepsis Campaign for management of severe sepsis and septic shock. Crit. Care Med., 2004, 32, 858–872.
21. Rivers, E., Nguyen, B., Havstad, S., et al. Early goal-directed therapy in the treatment of severe sepsis and septic shock. N. Engl. J. Med., 2001, 345, 1368–1377.
22. Meier-Hellmann, A. Hamodynamische Stabilisierung in der Sepsis. Anasthesiologie et Intensivmedizin, 2000, 41, 601–613
Štítky
Chirurgia všeobecná Ortopédia Urgentná medicína
Článok vyšiel v časopiseRozhledy v chirurgii
Najčítanejšie tento týždeň
2009 Číslo 7- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
-
Všetky články tohto čísla
- Jaké jsou současné úkoly intenzivní péče v chirurgii?
- Infekce náhrad abdominální aorty
- Perioperační metabolická péče u diabetického pacienta – doporučení
- Antibiotická profylaxe v urologii
- Levostranné resekce pankreatu: indikace, chirurgická technika a komplikace
- Experimentální terapie nádoru pomocí intratumorózní aplikace dendritických buněk
- Minimalizace krevních ztrát v jaterní chirurgii
- Úloha klasickej chirurgie pri liečbe náhlych príhod brušných u onkologických pacientov
- Nekrotizující infekční komplikace u syndromu diabetické nohy a jejich řešení
- Moderní radioterapie v komplexní léčbě sarkomů měkkých tkání a kostí u dospělých – aktuální přehled a vlastní zkušenosti
- Komplikace IPOM plastiky – naše zkušenosti
- Septický šok u pacienta s Fourniérovou gangrénou s fatálním koncem
- Komplikace periproktálního abscesu – Fourniérova gangréna nebo nekrotizující fasciitida? Kazuistika
- Nutriční intervence v chirurgii
- The Occurrence of Gallbladder Carcinoma in Yemeni Patients Undergoing Cholecystectomy in Two Hospitals
- Rozhledy v chirurgii
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Septický šok u pacienta s Fourniérovou gangrénou s fatálním koncem
- Komplikace IPOM plastiky – naše zkušenosti
- Komplikace periproktálního abscesu – Fourniérova gangréna nebo nekrotizující fasciitida? Kazuistika
- Antibiotická profylaxe v urologii
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



