-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Akutní mediastinitida
Acute Mediastinitis
The authors give an outline of the issue of acute mediastinitis. It is a severe infection of connective tissue of the mediastinum. Timing of recognition and accuracy of drainage are the most essential conditions of successful treatment. Acute mediastinitis may be divided in the postoperative sternal infections with infection of the mediastinum, mediastinitis due to perforation of the aero-digestive tract and descending necrotizing mediastinitis. The authors describe etiopathogenesis, diagnostics and therapy in each particular type of mediastinitis.
Key words:
mediastinitis – infection – perforation – esofagus – thoracic surgery – drainage – stent
Autori: T. Bohanes; Č. Neoral
Pôsobisko autorov: I. chirurgická klinika LF UP a FN Olomouc, přednosta: doc. MUDr. Čestmír Neoral, CSc.
Vyšlo v časopise: Rozhl. Chir., 2011, roč. 90, č. 11, s. 604-611.
Kategória: Monotematický speciál - Původní práce
Súhrn
Autoři ve své práci, napsané jako vzdělávací článek, podávají přehled problematiky akutní mediastinitidy.
Akutní mediastinitida jakožto prudká infekce pojiva mezihrudí je nadále velmi závažným onemocněním, u nějž je rychlost rozpoznání a preciznost provedené drenáže základem úspěšné léčby. Lze ji rozdělit na pooperační infekce sterna s infekcí mezihrudí, mediastinitidu z perforace aerodigestivního traktu a sběhlou nekrotizující mediastinitidu.
Autoři u každého typu mediastinitidy přinášejí přehled etiopatogeneze, diagnostiky a terapie.Klíčová slova:
mediastinitida – infekce – perforace – jícen – hrudní chirurgie – drenáž – stentÚVOD
Akutní mediastinitida je prudká flegmonózní infekce mediastinální pojivové tkáně. Šíří se velmi rychle po mediastinu, jelikož zde chybí výrazné anatomické překážky, takže může vést velmi záhy i k rozvoji fulminantní sepse, už proto, že nezřídka je prodleva do stanovení správné diagnózy poměrně významná. Nejčastěji je akutní mediastinitida způsobena perforací aerodigestivního traktu, případně komplikuje výkony prováděné ze sternotomie, prognosticky velmi závažné jsou sběhlé nekrotizující mediastinitidy, komplikující infekce orofaryngeální oblasti [1]. Jakkoliv diagnostika a léčba je principiálně ve všech případech podobná, vzhledem k určitým odlišnostem budou jednotlivé příčiny probrány níže samostatně.
POOPERAČNÍ INFEKCE STERNA S MEDIASTINITIDOU
Etiopatogeneze
Mediastinitida po operacích ze sternotomie přestavuje, spolu s osteomyelitidou sterna, jednu z nejzávažnějších komplikací tohoto výkonu [2]. Jde o infekci pojiva předního mediastina, která může být spojena se zmíněnou osteomyelitidou sterna a/nebo instabilitou sterna. Incidence této formy mediastinitidy se udává v rozmezí 0,2–5 % [3], její letalita je uváděna v rozmezí 10–50 % [1], avšak jsou i práce, které prezentují letalitu až 70 % [4].
Příčina vzniku infekce není dosud jednoznačně stanovena, nicméně zřejmě existuje několik mechanismů. Jeden z nich je propagace osteomyelitidy sterna ze sternotomie do mediastina, dále se může instabilita sterna podílet na vzniku kožní dehiscence, která poté představuje bránu pro vstup infekce. Kolekce v nedostatečně drénovaném retrosternálním prostoru může rovněž představovat živnou půdu pro usazení patogenních bakterií, zejména při případné konkomitantní infekci (pneumonii apod.) [1]. Predisponujícími faktory pro rozvoj pooperační mediastinitidy jsou z hlediska předoperačního stavu pacienta pak zejména diabetes, obezita, chronická obstruktivní plicní nemoc, imunosuprese, městnavá slabost srdeční, vyšší věk apod., z perioperačních faktorů je třeba zmínit např. déle trvající umělou plicní ventilaci, užití kostního vosku na sternum.
Nejčastějšími patogeny, které jsou odpovědné za tuto formu mediastinitidy, jsou Staphylococcus aureus a Staphylococcus epidermidis [2], což podporuje teorii o perioperační kontaminaci operačního pole. K tomu může přispívat i případná incize na dolní končetině v případě odběru v. saphena. Dalšími možnými patogeny jsou gram-negativní bakterie rodů Pseudomonas, Serratia či Klebsiella, vesměs v rámci nozokomiálních nákaz, nebo vzácněji i kvasinky. Až ve 40 % je zjišťována smíšená flóra [1].
Tab. 1. Přehled příčin akutní mediastinitidy Tab. 1. Overview of causes of acute mediastinitis 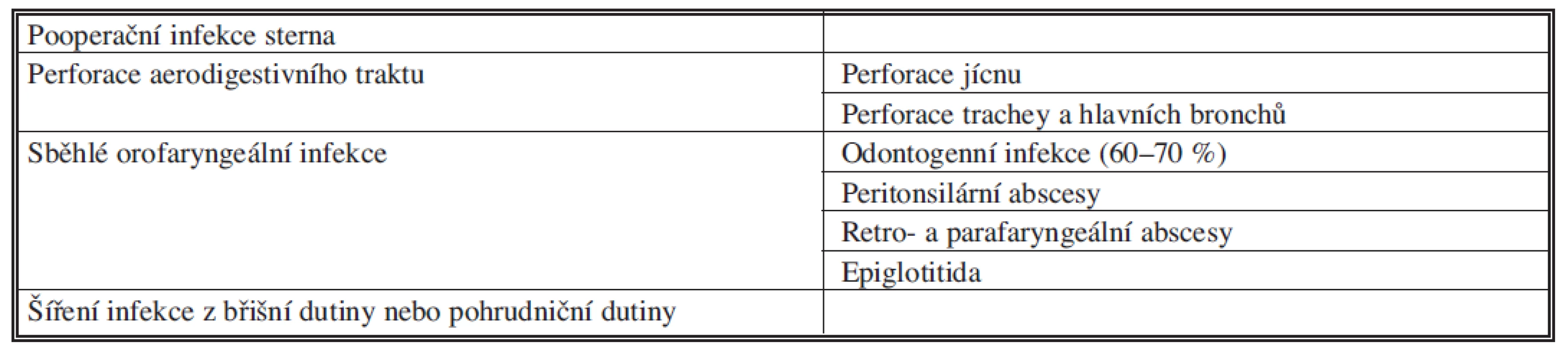
Klasifikace
Pooperační komplikace po sternotomii se mohou vyskytovat v různých formách, od pouhé sterilní dehiscence rány až po supurativní mediastinitidu, navíc se někdy používají různé termíny pro tutéž komplikaci. Proto pro sjednocení terminologie prezentovali R. El Oakley s J. E. Wrightem v roce 1996 klasifikaci, kterou prezentují tabulky 2 a 3 [2].
Tab. 2. Klasifikace komplikací po sternotomii [2] Tab. 2. Classification of complications following sternotomy [2] ![Klasifikace komplikací po sternotomii [2]
Tab. 2. Classification of complications following sternotomy [2]](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/f19b1b093e5f334a973dfba4c1956e73.png)
Tab. 3. Klasifikace mediastinitidy po sternotomii [2] Tab. 3: Classification of mediastinitis following sternotomy [2] ![Klasifikace mediastinitidy po sternotomii [2]
Tab. 3: Classification of mediastinitis following sternotomy [2]](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/ba3029bf6628b5a14e260950f63cf39a.png)
1 Rizikové faktory identifikované ve třech nebo více hlavních studiích. V současné době jsou akceptovány tyto rizikové faktory: diabetes, obezita a imunosupresivní léčba 2 Selhání terapeutického pokusu zahrnuje jakoukoliv chirurgickou intervenci s cílem léčby mediastinitidy Symptomatologie a diagnostika
Na pooperační mediastinitidu je třeba myslet především vždy, kdy je přítomna ranná infekce v ráně po sternotomii, resp. dojde k dehiscenci této rány. Pacienti mohou rovněž pociťovat bolest při dýchání nebo v poloze vleže na boku. Nezřídka lze zjistit projevy instability osteosyntézy sterna, kdy se dvě poloviny sterna pohybují vůči sobě při bimanuálním vyšetření hrudníku. Typické projevy však mohou zcela chybět a na možnost infekční komplikace je třeba myslet především při přítomnosti obecných známek zánětu, tj. horečce a elevaci zánětlivých laboratorních parametrů, případně při vyvíjející se sepsi.
K objektivizaci nálezu slouží CT vyšetření, které ukáže retrosternální prosáknutí nebo přímo kolekci, i když často lze diagnózu stanovit již klinicky. Pokud se týče scintigrafie, jindy úspěšně využívané u osteomyelitid jiných lokalizací, v této indikaci se její výsledky jeví přinejlepším kontroverzní [5].
Terapie
Klasická terapie komplikací hojení rány po sternotomii spočívá v časném rozpuštění rány a debridementu, většinou s následnými převazy a proplachy rány desinfekčními roztoky či roztoky antibiotik. U hluboké infekce je u klasické terapie metodou volby využití Redonových drénů, zavedených do retrosternálního prostoru. Tento postup samotný ovšem často selhává a bývá doporučováno využít svalový lalok z pektorálního svalu, popřípadě ještě lépe omentální lalok k vyplnění prostoru retrosternálně k zamezení perzistence infekce [6, 7].
Zavedení metody vakuum asistovaného hojení otevřených ran, poprvé prezentovaného Argentou a Morykwasem v roce 1997 [8] ovlivnilo i terapii infekce po sternotomii. V této indikaci byla metoda poprvé prezentována Obdeinem a spolupracovníky v roce 1999 [9] a stává se postupně zlatým standardem. Výhodou metody, aplikující podtlak do hojící se, případně infikované tkáně, je zvýšení průtoku krve tkání, snížení otoku, redukce bakteriální kontaminace, odstranění stagnující tekutiny a tkáňového detritu a podpora granulace [1, 10]. Tato metoda, ve srovnání se všemi typy klasické terapie, vykazuje výhody ve smyslu snížení letality, snížení počtu selhání lokální terapie a zkrácení hospitalizace [10]. Z praktického hlediska se doporučuje u těchto pacientů aplikovat podtlak kontinuálně, což napomáhá stabilizaci hrudní stěny. Pěna, sloužící k odsávání, by neměla být v kontaktu s obnaženými cévami a srdcem, takže mezi pěnu a hlouběji ležící struktury je třeba vložit několik vrstev neadhezivního materiálu.
PERFORACE AERODIGESTIVNÍHO TRAKTU
Etiopatogeneze
Perforace aerodigestivního traktu je častou příčinou mediastinitidy, jde přitom zpravidla o iatrogenní nebo spontánní perforaci jícnu, která způsobí kontaminaci mediastinálního prostoru orofaryngeálními bakteriemi a žaludečním obsahem. Nejčastější příčinou jsou bohužel především různé instrumentální výkony, především endoskopie či dilatace jícnu, popřípadě obtížná intubace. Iatrogenní příčiny jsou odpovědné až za 59 % jícnových perforací [11]. Další možností je též únik z anastomózy na jícnu po výkonech na jícnu, případně na žaludku. V případě perforace dýchacího stromu není infekce mediastina častá, jakkoliv i na tuto možnost je třeba myslet. Přehled příčin perforace aerodigestivního traktu přináší tabulka 4.
Tab. 4. Příčiny perforace aerodigestivního traktu Tab. 4. Causes of aerodigestive tract perforations 
Ze zvláštních příčin perforace jícnu je vhodné připomenout především tzv. Boerhaaveho syndrom, spontánní rupturu distálního jícnu během explozivního opakovaného zvracení. Tento syndrom popsal poprvé holandský lékař a botanik Hermann Boerhaave (1668–1738) při pitvě holandského velkoadmirála barona Jana van Wassenaera, který zemřel v roce 1724 po požití velkého množství jídla a pití, následovaném snahou vyvolat zvracení pomocí kapek z ipecacuanhy (česky hlavěnka dávivá). Ante mortem popsal poprvé Boerhaaveho syndrom Meyer v roce 1952, úspěšná léčba byla poprvé publikována v roce 1947 nezávisle na sobě Barrettem a několika dalšími autory [12, 13]. Etiologicky je Boerhaaveho syndrom způsoben prudkým nárůstem intraluminárního tlaku v jícnu během zvracení, který působí proti uzavřenému krikofaryngeálnímu svěrači a způsobí rupturu stěny jícnu, nejčastěji v celé tloušťce v oblasti distálního hrudního jícnu (distálních 6–8 cm). Zde se předpokládá určité oslabení stěny jícnu jako důsledek distribuce svalových vláken ve stěně jícnu, podle jiné teorie zde rovněž chybí opora okolních tkání [12]. Vzácněji se může vyskytnout i parciální submukózní disekce, ta se může šířit i na proximální žaludek, kde může dojít i k profuznímu krvácení, popsanému poprvé Mallorym a Weissem v roce 1927 [14]. V případě kompletní ruptury je naproti tomu významnější krvácení vzácné [12].
Obr. 1a. Insuficience krční anastomózy s abscesem mediastina – transverzální řez Fig. 1a. Insufficiency of cervical anastomosis with mediastinal abscess – transverse section 
Obr. 1b. Ten samý pacient v sagitálním řezu Fig. 1b. The same patient – saggital sections 
Obr. 1c. Regrese dutiny v mediastinu po transcervikální drenáži (šipka ukazuje konec drénu), vedlejším nálezem je progrese reaktivního fluidotoraxu bilaterálně Fig. 1c. Regression of the mediastinal cavity following transcervical drainage (the arrow points at the drain ending), bilateral progression of reactive fluidothorax is a secondary finding 
Diagnostika
Rozvoj mediastinitidy je tím, čím perforace aerodigestivního traktu nemocné ohrožuje především. Základním úkolem je proto perforaci co nejdříve rozeznat a řešit a tak infekci mediastina předejít, anebo dobu expozice jejímu zdroji co nejvíce zkrátit [15, 16].
Symptomatologie pacientů závisí na rozsahu a lokalizaci perforace. V popředí příznaků stojí především lokalizovaná bolest v krku, především při polykání, resp. bolest na hrudi, v prekordiu, popř. i v epigastriu, obvykle doprovázená dysfagií. Další příznaky jsou pak spojeny především s kontaminací okolních tkání a struktur a infekcí těchto tkání. Na krku se objevuje otok a zarudnutí, nastupuje febrilie, dysfonie, lze zjistit krepitaci při podkožním emfyzému. Postupně se vyvíjí absces, který může i perforovat navenek píštělí. Při perforaci hrudního jícnu se může vyvinout pleurální dráždění při šíření infekce do pleurálních dutin – při perforaci distálně obvykle dochází k šíření především doleva, při perforaci středního jícnu pak dochází k šíření infekce především doprava, vždy ale může dojít k bilaterálnímu postižení, stejně tak jako infekci perikardu. Postupně se vyvíjí febrilie, může se rozvíjet respirační insuficience. Klinicky zjistíme vyvíjející se podkožní emfyzém a příznaky hydropneumotoraxu.
Základním diagnostickým postupem jsou radiografické metody. Konveční RTG ukazuje projasnění na krku, rozšíření mediastina, resp. obraz pneumomediastina, posléze i obraz fluidopneumothoraxu. Radiologický nález ovšem může být v 12–33 % normální [12]. Zpřesnění diagnózy lze dosáhnout především pomocí kontrastního vyšetření s využitím ve vodě rozpustné kontrastní látky. Tuto je třeba preferovat před využitím barya, které by v případě extravazace komplikovalo stav i operační výkon. Přesnější informaci poskytne CT, místo perforace lze rovněž přehlédnout pomocí endoskopu.
Terapie
V případě minimální perforace či v případě nejistoty je možné postupovat konzervativně. To spočívá v zamezení perorálního příjmu, zajištění výživy jiným způsobem a zejména podávání širokospektrých antibiotik.
Chirurgické řešení u perforace krčního jícnu spočívá v drenáži krčních viscerálních kompartmentů a dále v zamezení pokračující kontaminace. Z řezu před kývačem se uvolní postižený jícen a následuje sutura perforace. Pokud ovšem zánětlivé změny znemožňují bezpečnou suturu, je třeba zajistit důkladnou drenáž a postupovat dále konzervativně (viz výše), s doplněním o odsávání orofaryngeálních sekretů podle možností. Nejnověji je alternativou tohoto postupu implantace biodegradabilního stentu [17], přesto že v případě postižení krčního jícnu je tato možnost limitována vzdáleností k hornímu jícnovému svěrači. Smrt je každopádně v tomto případě spíše vzácná a vždy souvisí s rozvojem mediastinitidy [12].
Obr. 2a. Řešení insuficience jícnové anastomózy pomocí biodegradabilního stentu – nález úniku Fig. 2a. Management of insufficiency of esophageal anastomosis using biodegradable stent-detection of leakage 
Obr. 2b. Stav po stentáži, bez známek úniku kontrastní látky z lumen neojícnu Fig. 2b. Condition following stentage, no signs of the contrast matter leakage from the neo-esophageal lumen 
Obr. 1. Šíření infekce na krku probíhá ve třech anatomických prostorech Fig. 3. Spread of infection on the neck concerns three anatomical spaces 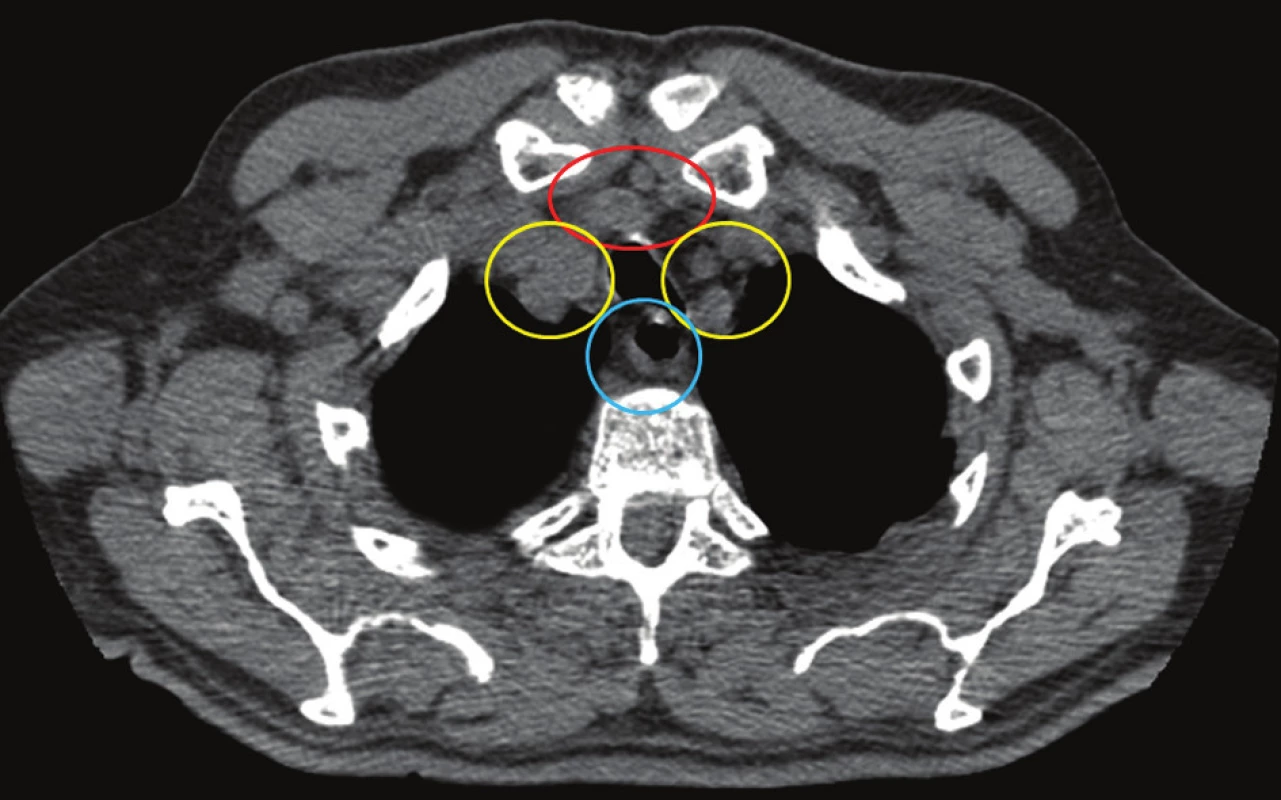
červeně – pretracheální, žlutě – perivaskulární, modře – prevertebrální red – pretrachal, yellow – perivascular, blue – prevertebral Při terapii perforace nitrohrudního jícnu je třeba rovněž dodržet čtyři základní, již zmíněné principy: zamezení pokračující kontaminace, široká chirurgická drenáž, širokospektrá antibiotika a zajištění přiměřené výživy [18]. Většina perforací hrudního jícnu je primárně indikována k chirurgickému řešení. Dosud je obecně akceptován názor, že tato intervence by měla proběhnout během 24 hodin od vzniku perforace, kdy je největší šance na úspěšnou primární suturu, nicméně některé práce ukazují, že význam časnosti intervence nemusí mít až takový význam, jaký jí byl přisuzován [19]. Nabízí se více možností, jak chirurgicky defekt jícnu reparovat, od prosté sutury přes suturu pojištěnou interkostomuskulárním lalokem, bylo referováno úspěšné využití fibrinových lepidel ať už pro vlastní uzávěr defektu či k pojištění sutury. V případě ireparabilních defektů, zvláště v případě přítomnosti distálněji situované stenózy jícnu jakékoliv etiologie, se nabízí i exstirpace postiženého jícnu s vyvedením krční esofagostomie a výživné gastrostomie s následnou rekonstrukcí jícnu ve druhé době. Při přítomnosti stenózy distálně od perforace je každopádně třeba vždy řešit stenózu v jedné době, jinak nemá sutura šanci na úspěch. Tyto všechny chirurgické metody jsou prováděny obvykle cestou torakotomie, jakkoliv jsou referovány i případy torakoskopické reparace [20].
Perspektivní minimálně invazivní metodou z poslední doby, která může pomoci řešit perforaci jícnu, je implantace samoexpandibilního povlečeného jícnového stentu, který překryje defekt stěny jícnu. Tak zamezí další kontaminaci mediastina a okolí, další výhodou je také udržení průsvitu jícnu v případné stenóze pod perforací, která někdy komplikuje terapii. Dosavadní výsledky ukazují úspěšnost terapie v 63–100 % [21, 22, 23], potenciálními komplikacemi mohou být ale migrace stentu, ulcerace a perforace jícnu stentem či mukózní hyperplazie [21, 23], navíc další komplikace se mohou objevit při extrakci stentu. Proto se jako vhodnější jeví použití biodegradabilního stentu, který je degradován během 2–3 měsíců, není nutná tedy ani extrakce stentu v případě jeho dislokace [17, 24]. Vzhledem k menšímu tlaku na stěnu jícnu je zde rovněž menší riziko vzniku dekubitu stěny. Třebaže tato metoda ještě vyžaduje další výzkum a případná technická vylepšení, zatím se jeví jako perspektivní k řešení jícnových perforací, a to nejen u pacientů, kde není primární chirurgická sutura pro latenci od vzniku indikována, ale i jako alternativa k chirurgické léčbě. Je ale nutné vždy pamatovat na nutnost drenáže případných zánětlivých kolekcí, ať už chirurgickou nebo minimálně invazivní pod CT kontrolou.
Mediastinitida z perforace jícnu již dnes není, díky úspěchům komplexní terapie, tou fatální diagnózou, jako jí byla v nedávné minulosti. Analýzou mnoha souborů vychází průměrná letalita 6,81 % v intervalu 0–24,2 % [12]. V každém případě, jak už bylo zmíněno, klíčovým faktorem pro příznivý výsledek je včasnost diagnózy a dokonalá drenáž infekčního fokusu v mediastinu, která zamezí rozvoji septických komplikací, které jsou jinak odpovědné za fatální konec.
SBĚHLÁ NEKROTIZUJÍCÍ MEDIASTINITIDA
Etiopatogeneze
Tato forma mediastinitidy byla definována Estrerou a spol. [25] jako akutní purulentní mediastinitida, způsobená sestupující orofaryngeální infekcí. Zdrojem infekce v oblasti orofaryngu je nejčastěji, až v 60-70%, odontogenní infekce, dále pak peritonsillární a para - a retrofaryngeální abscesy, epiglotitida, krční lymfadenitida či sekundární infekce hematomů po úrazu krku a oblasti dolní čelisti [1, 25].
Infekce se z oblasti krku dostává do mediastina třemi anatomickými prostory, a to pretracheálně, perivaskulárně a zejména prevertebrálně. Řídká pojivová tkáň, neschopná zánět ohraničit tvorbou adhezí, klade jen minimální odpor šíření infekce a ta se vlivem gravitace a rovněž i nasávání negativním tlakem při nádechu snadno dostává do mediastina a k pleuře [26]. Tak může dojít i k šíření infekce skrze otvory v bránici z dutiny břišní. Bakteriální flóra, která je původcem nekrotizující mediastinitidy, je zpravidla smíšená, aerobní i anaerobní, odpovídá bakteriální flóře z dutiny ústní. Nejčastěji jde o zástupce rodů Streptococcus, Bacteroides, Actinomyces, Haemophillus, Peptostreptococcus aj. [1].
Mathieu a spol. [27] prezentovali rizikové faktory této formy mediastinitidy, mezi něž patří především diabetes, alkoholismus, nádory a radionekróza. Zejména pak věk přes 70 let v kombinaci s diabetem představuje dle jejich zjištění obzvláštní riziko.
Sběhlá nekrotizující mediastinitida představuje nadále život ohrožující stav, kdy navzdory pokrokům v diagnostice i terapii, jeho letalita v různých studiích kolísá od 0 % do 83 % [28]. V poslední době se uvádí zpravidla kolem 15 % [1].
Obr. 2. Bubliny plynu v prevertebrálním a perivaskulárním prostoru Fig. 4. Gas bubbles within the prevertebral and perivascular space 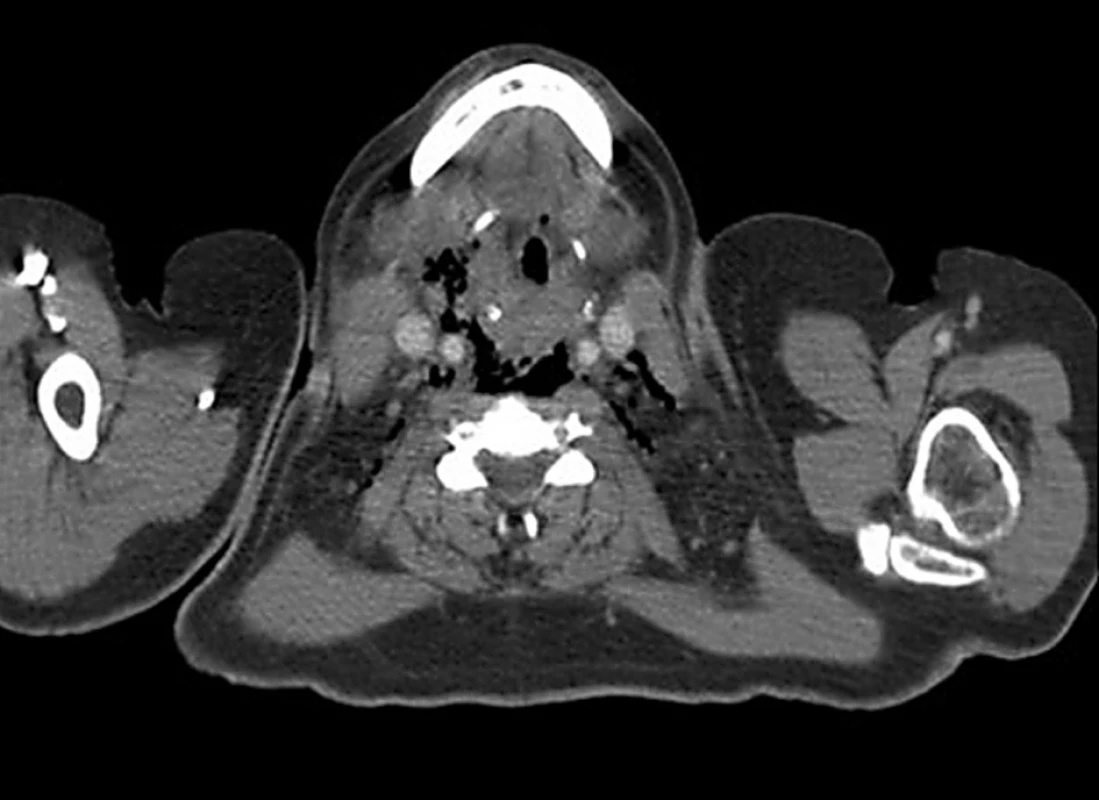
Obr. 3. Clamshell incision, řez označen tečkovaně Fig. 5. Clamshell incision, the incision is marked by a dotted line 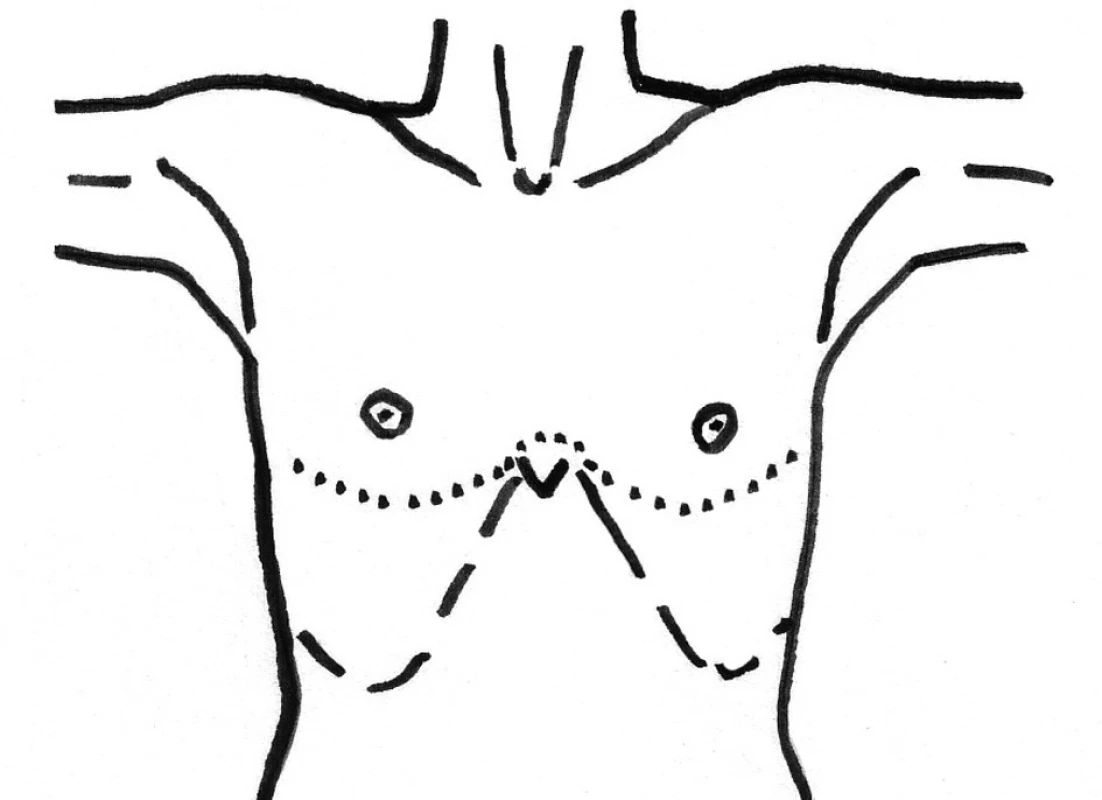
Diagnostika
Kritéria pro stanovení diagnózy této formy mediastinitidy definovali Estrera se spolupracovníky [25]. Tato kritéria zahrnují: 1. klinické známky prudké orofaryngeální infekce, 2. rentgenologické známky mediastinitidy, 3. průkaz nekrotizující mediastinální infekce v době chirurgické intervence nebo post mortem a 4. zjištění souvislosti mediastinitidy s orofaryngeální infekcí.
Klinické příznaky probíhající infekce bývají zpočátku netypické, v podstatě onemocnění probíhá pod obrazem krční infekce s bolestí na krku a ve faryngu, horečkou, dysfagií a otokem krku. Při rozvoji mediastinitidy, která může vzniknout již během 12 hodin, nebo i až po 2 týdnech (nejčastěji ale během 48 hodin) [1], se pak objevuje bolest na hrudi, dyspnoe a sepse.
Případná histologická analýza prokazuje nekrotizující proces na bázi obliterativní vaskulitidy s mikrotrombózami na hranicích ložiska infekce. V okolní tkáni probíhá akutní zánět s edémem v podkožním tuku. V pozdějších fázích se objevuje krvácení a sepse [29].
Základem diagnostiky jsou radiologické metody, především pak CT. Typické radiologické nálezy u nekrotizující mediastinitidy popsal Estrera se spolupracovníky [25]: rozšíření retrofaryngeálního prostoru s nebo bez hydroaerického fenoménu, deviace vzduchového sloupce trachey ventrálně, mediastinální emfyzém a ztráta normální lordózy krční páteře. Typickými nálezy na CT jsou pak formace abscesů, infiltrace tkání se setřením typických struktur, absence výrazné lymfadenopatie a přítomnost plynových bublin ve tkáních [30]. Na základě CT nálezu pak Endo se spolupracovníky [31] vytvořili klasifikaci, zohledňující stupeň šíření infekce. Typ I znamená lokalizovanou mediastinitidu, kde se infekce šíří jen po úroveň kariny. V případě postižení dolního předního mediastina, jde o typ IIA, je-li postiženo jak přední, tak i zadní dolní mediastinum, pak jde o typ IIB.
Terapie
Základem terapie sběhlé nekrotizující mediastinitidy je chirurgická drenáž, antibiotická terapie širokospektrými antibiotiky a péče o dýchací cesty [1]. V primární terapii je rovněž na předním místě sanace primárního fokusu a drenáž krčních prostor z široké krční laterální incize. Rána se ponechává otevřená, takže je možné provádět opakované výplachy a debridement.
Chirurgický přístup ke drenáži mediastina se liší podle rozsahu postižení. Podle většiny autorů je možné infekce, zasahující jen po úroveň bifurkace trachey ventrálně, resp. 4. hrudního obratle dorzálně, tedy odpovídající typu Endo I, řešit drenáží pouze z krčního přístupu, který je v tomto případě dostačující [25, 32], případně s využitím videoasistované mediastinoskopie [33]. Pokud je přítomen pleurální výpotek, měla by být doplněna hrudní drenáž [34]. Pokud infekce zasahuje kaudálněji, pak je třeba stav řešit z hrudního přístupu. U typu Endo IIA je některými autory doporučován přístup ze sternotomie či subxifoidálního řezu [31], většinou však z posterolaterální torakotomie [1, 28], která je pak hlavním přístupem k řešení mediastinitidy typu Endo IIB. Častěji se provádí pravostranná torakotomie, která umožňuje po ligaci oblouku v. azygos poměrně rozsáhlý debridement celého mediastina, ale může být výhodné zvolit stranu, kde je současně přítomen empyém či maximum postižení mediastina [35]. S výhodou může být u rozsáhlého postižení využita i clamshell incision (tj. transsternální bilaterální přední torakotomie, Obr. 5), umožňující přístup do mediastina i obou hemitoraxů [36, 37]. Nověji někteří autoři rovněž poukazují na výhody minimálně invazivního přístupu [26, 38], především nižší zátěž nemocného a nižší bolestivost. Torakoskopický přístup lze pak s výhodou kombinovat s krčním přístupem.
Obr. 4. Retrosternální drenáž u sběhlé mediastinitidy, šipky ukazují uložené Redonovy drény Fig. 6. Retrosternal drainage in mediastinitis, the arrows point at introduced Redon drains 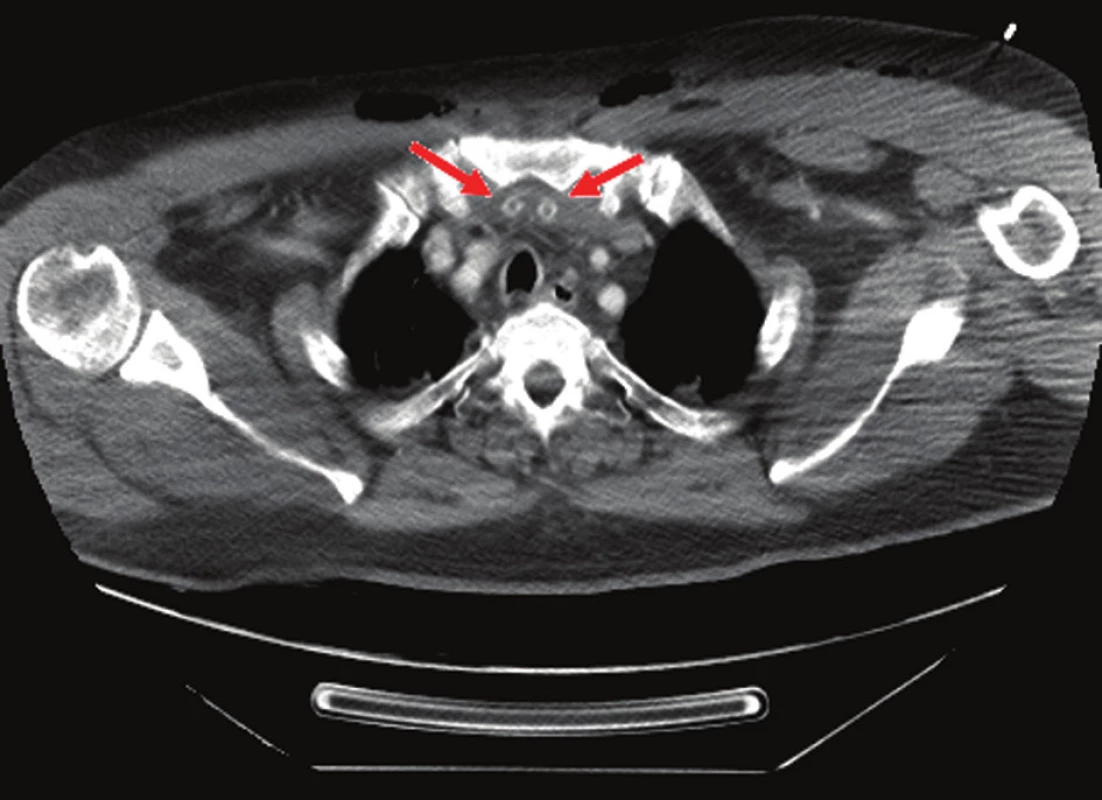
Někdy se rovněž doporučuje další podpůrná terapie, která by mohla pomoci snížit letalitu. Je to jednak podávání imunoglobulinu i.v. u pacientů s infekcí streptokoky skupiny A a dále hyperbarická oxygenoterapie. Mechanismus účinku imunoglobulinu je vysvětlován inhibicí superantigenní aktivity se vztahem k exotoxinům, produkovaným těmito streptokoky [29]. Hyperbarická oxygenoterapie má patrně baktericidní efekt, způsobuje aktivaci leukocytů a zlepšuje hojení [39].
Zvláštní otázkou je indikace k založení tracheostomie. Ta může být vhodná ke zlepšení péče o dýchací cesty. Na druhou stranu může sama existence tracheostomie usnadňovat přechod infekce mezi přední a zadní částí mediastina, takže indikci je třeba zvažovat.
ZÁVĚR
Akutní mediastinitida zůstává nadále velmi závažným onemocněním, u nějž je rychlost rozpoznání a preciznost provedené drenáže základem úspěšné léčby. Je typickou ukázkou toho, jak je efekt chirurgické terapie zásadní, přesně podle klasické poučky: „Ubi pus, ibi evacua!“ Ani nejmodernější antibiotika totiž nemohou v tomto případě bez cílené chirurgovy intervence stav nemocného vyřešit.
Poděkování:
Autoři děkují lékařům Radiologické kliniky FN Olomouc MUDr. Marii Černé, Ph.D., a MUDr. Filipu Čtvrtlíkovi, Ph.D., za poskytnutí radiologické dokumentace.
MUDr. Tomáš Bohanes
Jungmannova 11
779 00 Olomouc
e-mail: bohanest@gmail.com
Zdroje
1. Liptay, M. J., Kim, A. W. Acute and chronic mediastinal infections. In: Shields, T. W, Locicero III, J., Reed, C. E., Feins, R. H., eds.: General thoracic surgery. 7th edition. Philadelphia, Lippincott Williams &Wilkins, 2009 : 2181–2186.
2. El Oakley, R. M., Wright, J. E. Postoperative mediastinitis: classification and management. Ann. Thorac. Surg., 1996;61 (3):1030–1036.
3. Sá, M. P., Silva, D. O., Lima, E. N. de S., et al. Postoperative mediastinitis in cardiovascular surgery. Analysis of 1038 consecutive surgeries. Čas. Rev. Bras. Cir. Cardiovasc., 2010; 25(1): 19–24.
4. Tarelli, G., Maugeri, R., Pedretti, R., et al. The use of bilateral mammary artery in myocardial revascularization. The risc factors emergent from multivariate analysis conducted on 474 patients. G. Ital. Cardiol., 1998; 28 (11): 1230–1237.
5. Francel, T. J., Kouchoukos, N. T. A rational approach to wound difficulties after sternotomy: the problem. Ann. Thorac. Surg., 2001; 72 (4): 1411–1429.
6. Karra, R., McDermott, L., Connelly, S., et al. Risk factors for 1-year letality after postoperative mediastinitis. J. Thorac. Cardiovasc. Surg., 2006; 132 (3): 537–543.
7. Milano, C. A., Georgiade, G., Muhlbaier, L. H., Smith, P. K., Wolfe, W. G. Comparison of omental and pectoralis flap for poststernotomy mediastinitis. Ann. Thorac. Surg., 1999; 67 (2): 377–380.
8. Argenta, L. C., Morykwas, M. J. Vacuum-assisted closure: a new method for wound control and treatment: clinical experience. Ann. Plast. Surg., 1997; 38 (6): 563–576.
9. Obdeijn, M. C., de Lange, M. Y., Lichtendahl, D. H., de Boer, W. J. Vacuum-assisted closure in the treatment of poststernotomy mediastinitis. Ann. Thorac. Surg., 1999; 68 (6): 2358–2560.
10. Fuchs, U., Zittermann, A., Stüttgen, B., et al. Clinical outcome of patients with deep sternal wound infection managed by vacuum-assisted closure compared to conventional therapy with open packing: a retrospective analysis. Ann. Thorac. Surg., 2005; 79 (2): 526–531.
11. Brinster, C. J., Singhal, S., Lee, L., et al. Evolving option in the management of esophageal perforation. Ann. Thorac. Surg., 2004; 77 : 1475–1483.
12. Guitron, J., Howington, J. A., LoCicero III, J. Esophageal trauma. In: Shields, T. W, Locicero III, J., Reed, C. E., Feins, R. H., eds.: General thoracic surgery. 7th edition. Philadelphia, Lippincott Williams &Wilkins, 2009 : 1851–1865.
13. Barrett, N. R. Report of a case of spontaneous perforation of the esophagus successfully treated by operation. Br. J. Surg., 1947; 35 : 216.
14. Mallory, G. K., Weiss, S. Hemorrhage from lacerations of the cardiac orifice of the stomach due to vomiting. Am. J. Med. Sci., 1929; 178 : 506.
15. Onat, S., Ulku, R., Cigdem, K. M., et al. Factor affecting the outcome of surgically treated non-iatrogenic traumatic cervical esophageal perforation: 28 years experience at a single centre. J. Cardiothorac. Surg., 2010; 5 : 46.
16. Schmidt, S. C., Strauch, S., Rösch, T. Management of esophageal perforations. Surg. Endosc., 2010; 24 (11): 2809–2813.
17. Černá, M., Köcher, M., Válek, V., et al. Covered biodegradable stent: New therapeutic option for management of esophageal perforation or anastomotic leak. Cardiovasc. Intervent. Radiol., 2011, epub 7. 1. 2011.
18. Mayer, J. E. Jr., Murray, C. A., Varco, R. L. The treatment of esophageal perforation with delayed recognition and continuing sepsis. Ann. Thorac. Surg., 1977; 23 (6): 586–573.
19. Jougon, J., Mc Bride, T., Delcambre, F., Minniti, A., Velly, J. F. Primary esophageal repair for Boerhaave’s syndrome whatever the free interval between perforation and treatment. Eur. J. Cardiothorac. Surg., 2004; 25 : 475–479.
20. Scott, H. J., Rosin, R. D. Thoracoscopic repair of a transmural rupture of the esophagus (Boerhaave’s syndrome). J. R. Soc. Med., 1995; 88 : 414P–415P.
21. Eloubeidi, M. A., Lopes, T. L. Novel removable internally fully covered self-expanding metal esophageal stent: feasibility, technique of removal and tissue response in humans. Am. J. Gastroenterol., 2009; 104 : 1374–1381.
22. Salminen, P., Gullichsen, R., Laine, S. Use of self-expandable metal stents for the treatment of esophageal perforations and anastomotic leaks. Surg. Endosc., 2009; 23 : 1526–1530.
23. Leers, J. M., Vivaldi, C., Schafer, H., et al. Endoscopic therapy for esophageal perforation or anastomotic leak with a self-expandable metallic stent. Surg. Endosc., 2009; 23 : 2258–2262.
24. Fry, S. W., Fleischer, D. E. Management of a refractory benign esophageal stricture with a new biodegradable stent. Gastrointest. Endosc., 1997; 45 : 179–182.
25. Estrera, A. S., Landay, M. J., Grisham, J. M., Sinn, D. P., Platt, M. R. Descending necrotizing mediastinitis. Surg. Gynecol. Obstet., 1983; 157 (6): 545–552.
26. Min, H. K, Choi, Y. S., Shim, Y. M., Sohn, Y. I., Kim, J. Descending necrotizing mediastinitis: a minimally invasive approach using video-assisted surgery. Ann. Thorac. Surg., 2004; 77 : 306–310.
27. Mathieu, D., Neviere, R., Teillon, C., Chagnon, J. L., Lebleu, N., Wattel, F. Cervical necrotizing fasciitis: clinical manifestations and management . Clin. Infect. Dis., 1995; 21 : 51–56.
28. Sandner, A., Börgermann, J. Update on necrotizing mediastinitis: Causes, approaches to management, and outcomes. Curr. Infect. Dis. Rep., 2011; 13 : 278–286.
29. Wolf, H., Ovesen, T. Necrotizing fasciitis in the head and neck region. Ugeskr. Laeger., 2008; 170 : 2563–2566.
30. Carrol, C. L., Jeffrey, R. B. Jr., Federle, M. P., Vernacchia, F. S. CT evaluation of mediastinal infections. J. Comput. Assist. Tomogr., 1987; 11 : 449–454.
31. Endo, S. M., Hasegawa, T., Yamamoto, S., et al. Guidline of surgical management based od diffusion of descending necrotizing mediastinitis. Jpn. Thorac. Cardiovasc. Surg., 1999; 47 (1): 14–19.
32. Hsu, R. F., Wu, P. Y., Ho, C. K. Transcervical drainage for descending necrotizing mediastinitis may be sufficient. Otorynolaryngol. Head Neck Surg., 2011, epub 26. 4. 2011.
33. Shimizu, K., Otani, Y., Nakano, T., et al. Successful video-assisted mediastinoscopic drainage of descending necrotizing mediastinitis. Ann. Thorac. Surg., 2006; 81 : 2279–2281.
34. Karkas, A., Chahine, K., Schmerber, S., Brichon, P. Y., Righini, C. A. Optimal treatment of cervical necritizing fasciitis associated with descending necrotizing mediastinitis. Br. J. Surg., 2010; 97 : 609–615.
35. Klečka, J., Šimánek, V., Vodička, J., Špidlen, V., Pradl, R., Ferda, J. Akutní mediastinitis – optimální diagnostická a léčebná opatření. Rozhl. Chir., 2009; 88 (5): 253–258.
36. Bains, M. S, Ginsberg, R. J., Jones, W. D. II., et al. The clamshell incision: An improvement approach to bilateral pulmonary and mediastinal tumor. Ann. Thorac. Surg., 1994; 58 : 30–33.
37. Ris, H. B., Banic, A., Furrer, M., Caversaccio, M., Cerny, A., Zbären, P. Descending necrotizing mediastinitis surgical treatment via clamshell approach. Ann. Thorac. Surg., 1996; 62 : 1650–1654.
38. Roberts, J. R., Smythe, W. R., Weber, R. W., Lanutti, M., Rosengard, B. R., Kaiser, L. R. Thoracoscopic management of descending necrotizing mediastinitis. Chest, 1997; 112 : 850–854.
39. Watanabe, S., Kariatsumari, K., Sakasegawa, K., et al. A new combined surgical procedure for severe descending necrotizing mediastinitis with bilateral empyema. Thorac. Cardiovasc. Surg., 2002; 50 : 380–310.
Štítky
Chirurgia všeobecná Ortopédia Urgentná medicína
Článok vyšiel v časopiseRozhledy v chirurgii
Najčítanejšie tento týždeň
2011 Číslo 11- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
-
Všetky články tohto čísla
- Budoucnost hrudní chirurgie v České republice
- Akutní mediastinitida
- Transplantace plic
- Využitie epiteliálnych buniek príjemcu pri allotransplantácii trachey v experimente – prvé výsledky
- Je něco nového v léčbě spontánního pneumotoraxu?
- Je oprávněné provedení pneumonektomie v léčbě plicních metastáz?
- Spontánní pneumomediastinum – kazuistika
- Principy ošetření poranění hrudní stěny
- Penetrující poranění hrudníku a břicha: diagnostický a léčebný postup
- Perforace jícnu
- Četnost metatastického postižení mediastinálních uzlin během plicní metastasektomie
- Perforace pravé komory srdeční úlomkem žebra po tupém úrazu hrudníku
- Rozhledy v chirurgii
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Akutní mediastinitida
- Transplantace plic
- Perforace jícnu
- Je něco nového v léčbě spontánního pneumotoraxu?
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



