-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Fasciitis necrotisans – duplicitas casuum
Fasciitis necrotisans – duplicitas casuum
Necrotizing fasciitis is a dangerous bacterial infectious disease that is not commonplace in Czech society. On the other hand, neither is it so rare that the majority of surgeons should not come across it occasionally. In the early stages, pathological changes in fascia, subcutaneous tissue and even skin may run an inconspicuous course. However, this can rapidly deteriorate into shock and sepsis which may lead to multi-organ failure and an imminent life-threatening condition. The fatality rate of necrotizing fasciitis among high-risk groups (e.g. diabetics, patients who are immuno-compromised, obese and/or elderly, malnourished, or with a history of drug use), is particularly steep, reaching as high as 73%. Treatment for this condition consists of early, radical surgical intervention in conjunction with targeted antibiotherapy. Complex resuscitative and intensive care, including rehabilitation, are standard components of post-surgical management. Use of hyperbaric oxygen therapy, if such an opportunity exists, is also recommended. Interdisciplinary collaboration is a vital prerequisite for successful treatment. This article describes two case-studies of necrotizing fasciitis that occurred in men of similar age during a three-year period. Both patients presented with very similar and complicated disease courses, and both were successfully treated by the same interdisciplinary team comprised of clinicians from various specialized departments.
Key words:
necrotizing fasciitis − radical necrectomy – antibiotherapy − hyperbaric oxygen therapy − complex resuscitative and intensive care
Autoři: L. Klein 1,2; R. Fabian 3; P. Šafránek 4; P. Paterová 5; I. Slaninka 1; E. Havel 4; P. Dostál 6; M. Serbák 7
Působiště autorů: Oddělení plastické chirurgie a léčby popálenin chirurgické kliniky Lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Hradec Králové 1; Katedra vojenské chirurgie, Fakulta vojenského zdravotnictví Univerzity obrany, Hradec Králové 2; Anesteziologicko-resuscitační oddělení Nemocnice Na Homolce, Praha 3; Jednotka intenzivní péče chirurgické kliniky Lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Hradec Králové 4; Ústav klinické mikrobiologie Lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Hradec Králové 5; Klinika anesteziologie, resuscitace a intenzivní medicíny Lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Hradec Králové 6; Chirurgické oddělení, Litomyšlská nemocnice, Litomyšl 7
Vyšlo v časopise: Rozhl. Chir., 2018, roč. 97, č. 9, s. 432-441.
Kategorie: Kazuistika
Souhrn
Nekrotizující fasciitida je nebezpečné bakteriální infekční onemocnění, které v našich podmínkách není příliš časté, ale současně není natolik vzácné, aby se s ním občas nesetkal téměř každý chirurg. Postižení fascie, podkoží i kůže může mít zpočátku nenápadný průběh, který však záhy přechází v šokový stav a sepsi s multiorgánovým selháním a bezprostředním ohrožením života nemocného. Letalita onemocnění, zejména u rizikových skupin pacientů (diabetici, pacienti s oslabenou imunitou, nemocní obézní nebo vysokého věku, v malnutrici, užívající drogy) je vysoká a dosahuje až 73 %. Celková léčba spočívá v časném radikálním chirurgickém ošetření v kombinaci s cílenou léčbou antibiotiky za podmínek komplexní resuscitační a intenzivní péče včetně následné rehabilitace. Existuje-li taková možnost, doporučuje se rovněž využít hyperbarickou oxygenoterapii. Fungující interdisciplinární spolupráce je přitom nezbytným předpokladem i nutností. Ve sdělení prezentujeme dva případy tohoto onemocnění u mužů obdobného věku s velmi podobným, komplikovaným průběhem, při jejichž léčbě v intervalu tří let, při uplatnění uvedených principů, spolupracovaly stejné týmy několika pracovišť.
Klíčová slova:
nekrotizující fasciitida − radikální nekrektomie − antibiotická léčba − hyperbarická oxygenoterapie − komplexní resuscitační a intenzivní péče
Úvod
Nekrotizující fasciitida (NF) je nebezpečné bakteriální infekční onemocnění, které v našich podmínkách sice není příliš časté, ale současně není natolik vzácné, aby se s ním občas nemohl setkat téměř každý chirurg. Zejména v počátečních stadiích je na tuto diagnostickou možnost nutno pamatovat i na stanicích lékařských pohotovostních služeb a odděleních urgentní medicíny. NF patří do skupiny klinicky rozmanitých syndromů v literatuře označovaných jako nekrotizující infekce měkkých tkání (necrotizing soft tissue infections – NSTI) [1]. Postihuje především fascie svalové, okolní podkožní tkáně i hlubší dermální vrstvy kůže. Onemocnění je nebezpečné svým plíživým průběhem s náhlým neočekávaným přechodem v šokový stav, končící často smrtí. Nejčastěji vzniká toto onemocnění sekundárně v místě drobných poranění (exkoriace, lacerace, bodnutí hmyzem, rána kousnutím zvířetem i člověkem apod.) anebo i v souvislosti s chirurgickým výkonem [2,3]. O primární nebo idiopatické NF mluvíme tehdy, když nenalézáme bránu vstupu infekce nebo etiologický faktor [4]. Z mikrobiologického hlediska jde o infekce častěji polymikrobiální; nejčastěji izolovanými původci jsou streptokoky skupiny A, Streptococcus pyogenes, koaguláza negativní stafylokoky, z gramnegativních aerobů Escherichia coli, Enterobacter cloacae, Klebsiela spp., Proteus spp., Serratia spp., z anaerobů Bacteroides spp. a Clostridium spp. Méně často – asi ve 20 % − jde o monomikrobiální procesy způsobené hlavně streptokoky sk. A [1,5]. Léčebný postup spočívá ve včasné chirurgické intervenci – incizích, drenážích, dermofasciotomiích a nekrektomiích s podpůrnou cílenou léčbou antibiotickou a celkovou intenzivní, resp. resuscitační. Je-li dostupná léčba hyperbarickou oxygenoterapií, doporučuje se ji rovněž provést. Letalita onemocnění i přesto zůstává vysoká v desítkách procent [6,2].
V našem sdělení referujeme o dvou klinických případech NF s podobným průběhem i celkovým léčebným postupem, na kterém se v intervalu 3 let podílely stejné týmy několika zúčastněných pracovišť.
Kazuistika 1
53letý dosud zdravý stavební dělník, mírný kuřák, vyhledal 12. 6. 2014 praktickou lékařku pro 4 dny postupně se zvyšující tělesnou teplotu, dva dny narůstající kruté bolesti v oblasti pravé hýždě a stehna, pro které nemohl spát, nemohl se postavit na končetinu a nebyl schopen pohybu v kolenním kloubu. Hůře se mu dýchalo. Byl odeslán na ambulanci interního oddělení spádové nemocnice, kde v objektivním nálezu dominoval šokový stav – bledost s cyanózou rtů, schvácenost, tachypnoe s povrchním dýcháním, TK 75/40, TF 120/min., TT 38 °C. Bylo výrazné tuhé prosáknutí pravého boku, hýždě, stehna a proximální poloviny bérce, silné bolesti i při minimálním pohybu PDK, na břiše a obou stehnech napjatá mramorovaná kůže s lividním zbarvením. Provedla se standardní klinická a laboratorní vyšetření včetně CT vyšetření břicha, které prokázalo při peritoneální dutině bez kolekce zřetelnou infiltraci měkkých tkání ve fossa ischiorectalis vpravo vel. 60x30x30 mm s bublinami plynu. Další bubliny byly v měkkých tkáních pravého stehna v dorzální a laterální svalové skupině až ke kolennímu kloubu (Obr. 1a,1b). Plyn byl distribuován podél fascií a pod gluteálními svaly. Následovalo přijetí s diagnózou sepse, septického šoku s podporou oběhu, MODS (oběh, játra, renální funkce) na podkladě ischiorektálního abscesu vpravo s propagací infiltrace na PDK a nekrotizující fasciitidy, na ARO stejné nemocnice. Zde se pokračovalo v rehydrataci, analgezii, empiricky se podala antibiotika (penicilin G, gentamicin, metronidazol) a provedla se pasivní i aktivní imunizace proti tetanu. Dále chirurg provedl revizi v celkové anestezii – z periproktální incize vpravo pronikl do ischiorektálního prostoru, kde bylo jen minimum sekretu, digitálně per rectum stěna rekta byla bez rezistence, bez infiltrace, bez defektu. Dále provedl rozsáhlou dermofasciotomii na dorzální a laterální straně stehna a proximální polovině bérce. Objevila se až rozbředlá nekróza fascia lata i dalších fasciálních vrstev, svalová tkáň se jevila vitální. Následovaly výplachy H2O2 a Braunolem, drenáž ischiorektální jámy. Končetina byla poté zabalena do několika chirurgických roušek smočených v H2O2 a Braunolu. V průběhu operace byl pacient nestabilní, měl těžkou sepsi, metabolickou acidózu, byla nutná podpora oběhu katecholaminy. Po výkonu se pacient vrátil zpět na ARO, odkud lékaři konzultovali ARO Nemocnice Na Homolce (NNH) ohledně možnosti provedení hyperbarické oxygenoterapie (HBOT) pro podezření na anaerobní infekci.
Obr. 1. a, b: CT− zánětlivá infiltrace ve fossa ischiorectalis vpravo s propagací na stehno, tvorba plynu
Fig. 1a, b: CT − inflammatory infiltration in the right ischiorectal fossa spreading to the thigh, gas formation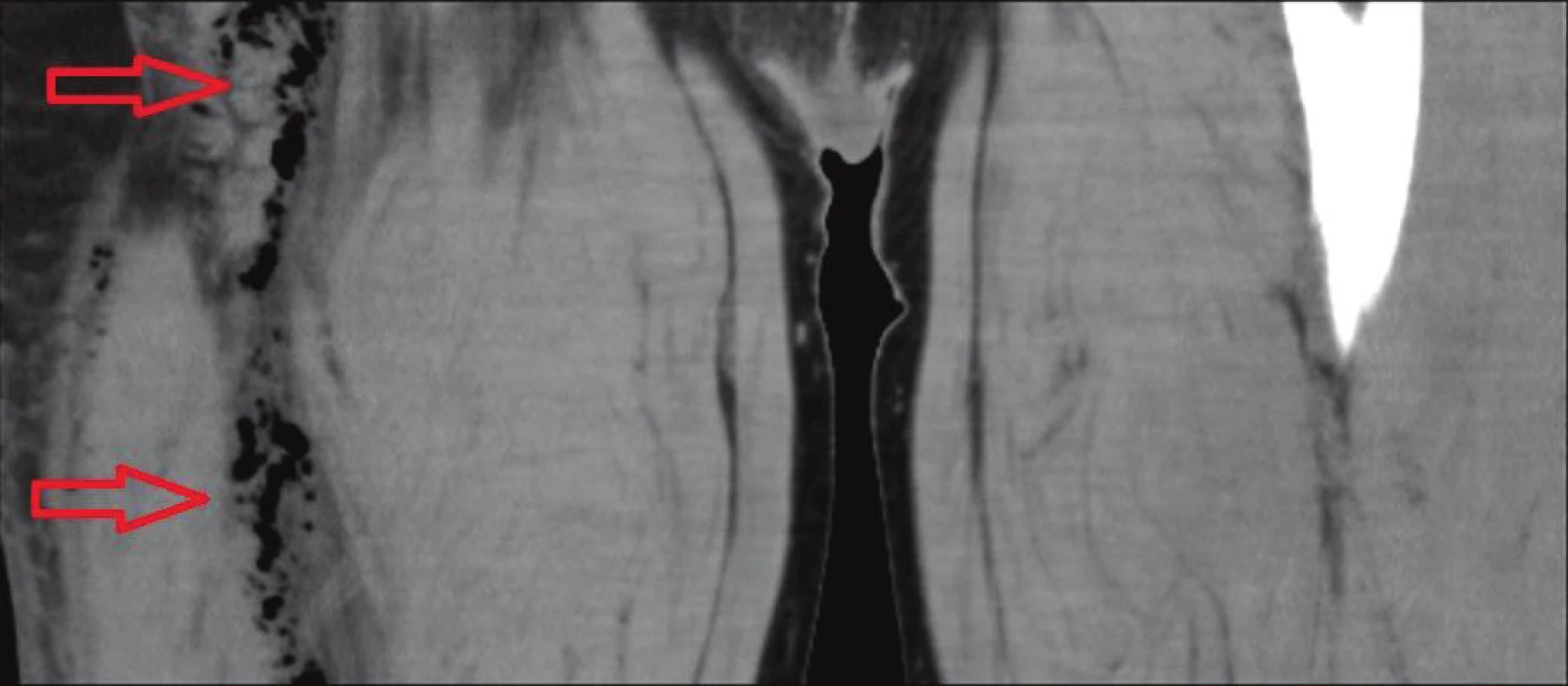
Dne 13. 6. 2014 byl nemocný přeložen na ARO NNH. Při příjmu byl na UPV, analgosedovaný a relaxovaný, oběhově nestabilní, febrilní 39,5 °C. Chirurg provedl převaz postižené končetiny a otorinolaryngolog paracentézu bubínků. Zahájila se HBOT – expozice 60 minut (FiO2 1,0; přetlak 1,5 ATA). Dále pokračovala komplexní resuscitační péče při těžké sepsi. Léčba antibiotiky ve vysokých dávkách se rozšířila o cefotaxim na čtyřkombinaci. Převazy PDK se prováděly 2x denně s 0,25% persterilem, proplachy H2O2 vždy před HBOT. Dne 14. 6. 2014 byl pac. febrilní 38,4 °C, s mírnou stabilizací oběhu, tekutinovou bilancí od příjmu +4370 ml, laboratorně CRP 382, funkce ledvin uspokojivá. 16. 6. 2014 byl stav celkově stabilizován, avšak ventilace se mírně zhoršila, bylo podezření na počínající ARDS. 17. 6. 2014 jsme považovali septický stav za definitivně zvládnutý. Založili jsme punkční dilatační tracheostomii (PDTS) pro potřebu dlouhodobé intenzivní péče včetně UPV. Celkem jsme provedli 10 expozic hyperbarickéoxygenoterapie (Obr. 2). Nemocný byl stabilizován s poklesem zánětlivých parametrů (CRP 45, PCT 8,5), oběh byl stabilní na minimální podpoře, ventilace uspokojivá, renální funkce dobré, pacient začínal mobilizovat tekutiny. Dne 19. 6. 2014 byl nemocný přeložen na KARIM FN Hradec Králové k další intenzivní a chirurgické rekonstrukční léčbě. Pokračovalo se v celkové intenzivní péči s podpůrnou ventilací, s převazy na operačním sále obden plastickým chirurgem. Při posledních 2 výkonech jsme nastavili na rannou plochu VAC systém (Renasys®, Smith & Nephew, London, UK) v módu kontinuálního podtlaku 100–150 mm Hg jako přípravu spodiny k autotransplantaci.
Obr. 2. Pravá dolní končetina při převazu – rozsáhlé dermofasciotomie (19. 6. 2014)
Fig. 2: Right lower extremity during dressing change – extensive dermofasciotomies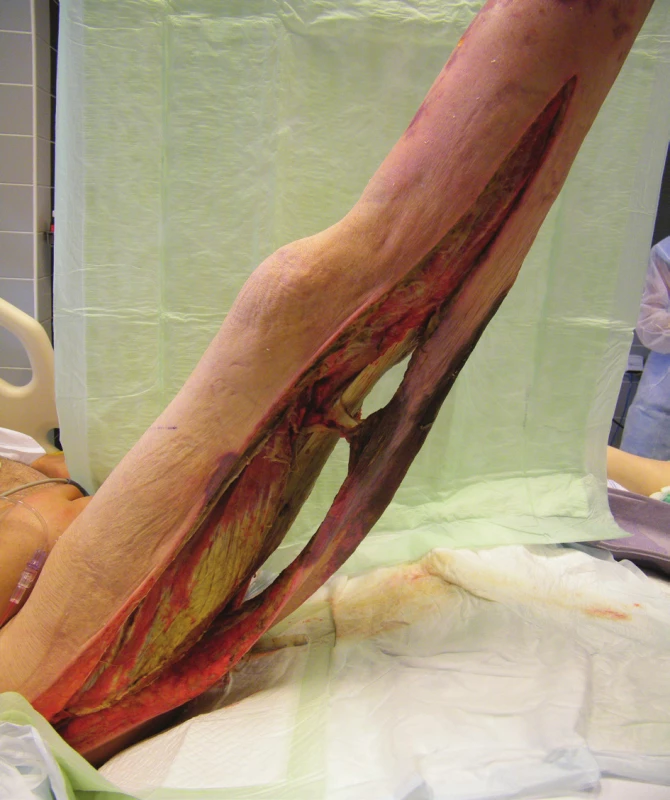
Od 26. 6. 2014 nastal pokles zánětových markerů, pacient trvale spontánně ventiloval, avšak byly známky těžké myoneuropatie kriticky nemocných. 2. 7. 2014 jsme pacienta přeložili na JIP chirurgické kliniky. Nemocný byl spontánně ventilující přes tracheostomickou kanylu, oběh byl stabilizován. Zjevné bylo zpomalené psychomotorické tempo s minimální spontánní hybností končetin při polyneuromyopatii kriticky nemocných. Dne 8. 7. 2014 se provedla rekonstrukční operace – autotransplantace kůže středně silnými dermoepidermálními štěpy odebranými cirkulárně ze stehna druhé končetiny, meshovanými v poměru 1 : 3. Při následných převazech bylo hojení ran klidné, bez komplikací a 10. pooperační den byly všechny štěpy přihojeny (Obr. 3), odběrová plocha se zhojila do 14. dne. V průběhu pobytu na JIP byla výživa zajištěna nasojejunální sondou kontinuálním podáváním proteinového polymerního přípravku (Nutrison Advanced Protison 80 ml/hod.) a současným podáváním kontinuální infuze aminokyselinového roztoku (Neonutrin 15% 500 ml/den). Perorální příjem jsme zahájili až 11. 7. 2014 dávkou 2770 kcal/dena 219 g bílkoviny/den. Přehled operačních výkonů a přehled mikrobiálních kultivačních nálezů a anti-biotické léčby je uveden v Tab. 1 a 2. Celkový stav nemocného se postupně zlepšoval, při trvale prováděné rehabilitaci se zvyšovala svalová síla i zlepšovala hybnost. 15. 7. 2014 jsme zrušili tracheostomii a pacienta18. 7. 2014 přeložili na standardní oddělení chirurgické kliniky. K dalšímu doléčení, resp. rehabilitaci byl pacient celkově v relativně dobrém stavu s plně zhojenými defekty měkkých tkání přeložen dne 22. 7. 2014 na chirurgické oddělení nemocnice Litomyšl.
Obr. 3. 14. den po transplantaci – všechny štěpy přihojeny (18. 7. 2014)
Fig. 3: 14 days after grafting – all grafts healed in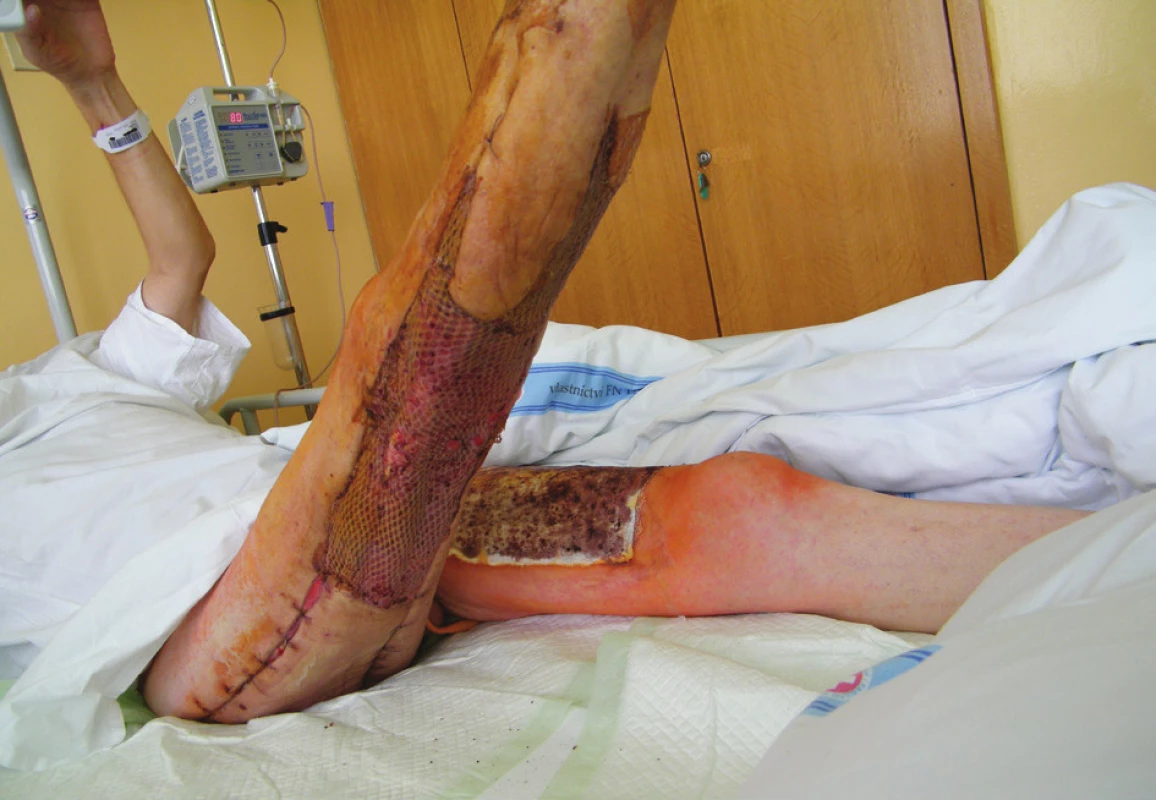
Tab. 1. Přehled operačních výkonů
Tab. 1: Surgical procedures – overview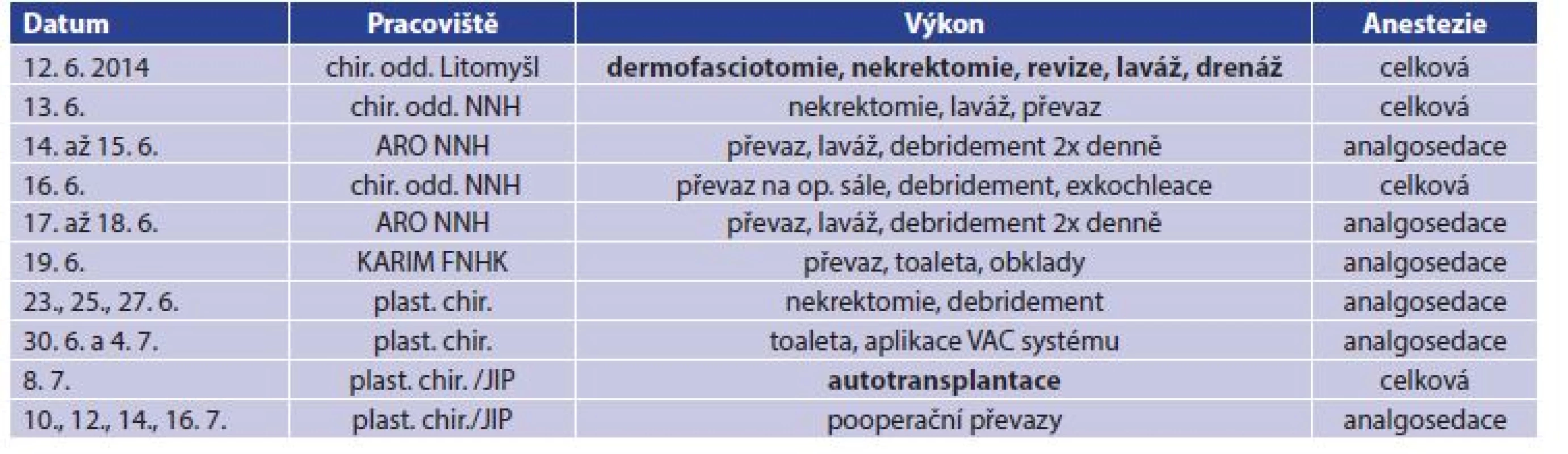
Tab. 2. Celkový přehled kultivačních nálezů a antibiotické léčby
Tab. 2: General overview of microbiological findings and antibiotherapy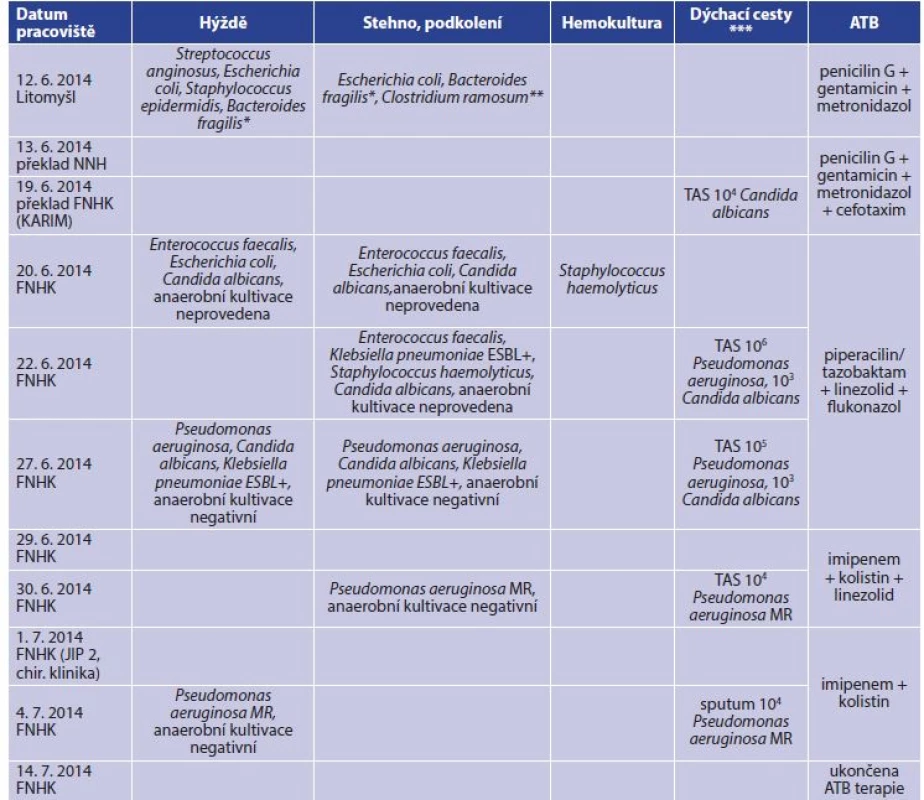
Vysvětlivky: ESBL+ pozitivní produkce širokospektré betalaktamázy, MR − multirezistentní, TAS − tracheální aspirát; *anaerobní gram-negativní tyčinky, součástí mikroflóry trávicího traktu; **anaerobní gram-pozitivní tyčinky, součástí mikroflóry trávicího traktu; *** hodnoty v CFU/ml. Při ambulantní kontrole 22. 1. 2015 byly všechny transplantované i odběrová plocha zhojeny, extenze kolenního kloubu plná, flexe omezená na 90 st., při chůzi ještě byla nutná podpora francouzskými holemi (FH). Při kontrole za tři a půl roku, 27. 11. 2017, byl tento muž v invalidním důchodu, kratší úseky chůze zvládal dobře i na schodech, při delší chůzi používal oporu jedné FH. Byly zřejmé příznivé barevné změny ploch odběrových i transplantovaných (Obr. 4). Flexe v koleni byla zlepšena na cca 110 st. Na novou životní situaci se tento muž dobře adaptoval, byl si vědom závažnosti překonané nemoci i bezprostředního ohrožení života, které mu reálně hrozilo.
Obr. 4. Stav 3,5 roku po prodělaném onemocnění (27. 11. 2017)
Fig. 4: Status 3.5 years after the treatment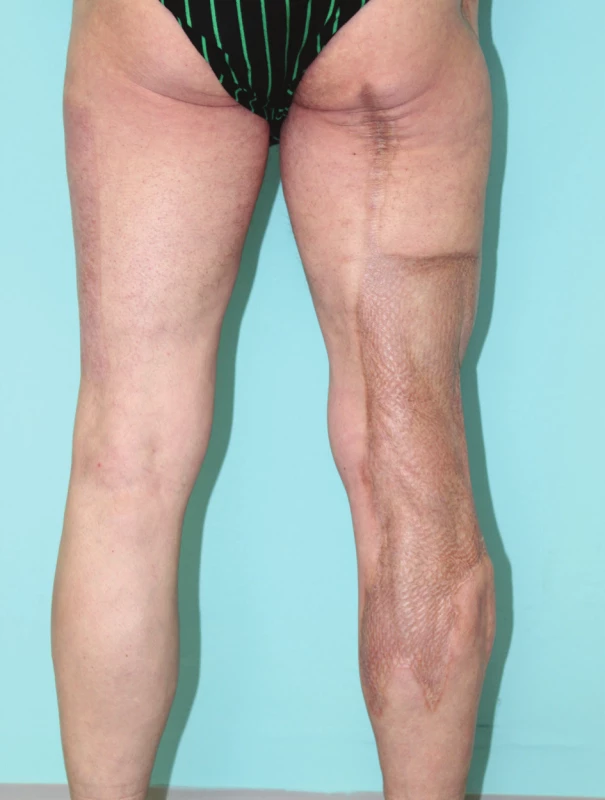
Kazuistika 2
61letý muž, v částečném invalidním důchodu, se zkrácením LDK pro vrozenou dysplasii kyčelního kloubu, kuřák, léčený pro ICHS s prodělaným infarktem myokardu a proběhlou perkutánní koronární intervencí (PCI) se založením stentu pro nemoc dvou tepen, arteriální hypertenzi, smíšenou poruchu metabolismu lipidů, hyperurikemii a chronickou hepatopatii. Medikace: Betaloc, Gopten, Plendil, Stacyl, Omeprazol, Atoris. V časných ranních hodinách 6. 7. 2017 byl přivezen RLP na ambulanci chirurgického oddělení spádové nemocnice pro bolestivé zduření a zarudnutí v pravém třísle, otok na zadní straně pravého stehna, bolesti v dané oblasti. Udával, že obtíže začaly asi před týdnem, 1x došlo ke spontánnímu prasknutí útvaru v třísle a vyprázdnění hnisu. Při přijetí nebyla dušnost ani cyanóza, hydratace byla dobrá. TK 115/60, TF 80/min., TT neuvedena. Místně byly zarudnutí a otok v pravém třísle zasahující dorzálně do gluteální krajiny a dorzomediálně až do dolní třetiny stehna, kde byly dva nekrotické defekty s hnisavou zapáchající sekrecí, nebyla krepitace. Nemocný byl přijat, zahájila se infuzní léčba, analgetizace, nasadil se klindamycin a připravoval se k výkonu na operační sál. Při revizi v celkové anestezii se provedla excize nekrotických defektů, incize z gluteální krajiny po zadní straně stehna až do podkolení, odstranilo se nekrotické podkoží i fascie v celém rozsahu zadní strany stehna včetně kůže. Svaly se zdály vitální. Rány byly opakovaně omyty H2O2 a Braunolem. Peroperačně byl podán penicilin G. Během výkonu došlo k progresi oběhové nestability s nutností volumoterapie a podpory oběhu noradrenalinem. Po výkonu se pacient přeložil na ARO, kde pokračovala UPV s rozvojem poruchy oxygenace a hyposaturací. V popředí byl klinický obraz ARDS, oligurie při septikemii, rozvíjející se septický stav. Vzhledem k podezření na anaerobní původ infekce se konzultovala možnost provedení hyperbarické oxygenoteparie (HBOT), ke které se pacient přeložil následující den na ARO NNH.
Při příjmu byl pacient subfebrilní, v kontinuální analgosedaci s oběhem na středně vysoké podpoře noradrenalinem. Chirurg provedl převaz a otorinolaryngolog paracentézu bubínků a zahájili jsme HBOT s parametry FiO2 1,0; přetlak 1,5 ATA, trvání expozice 60 min. V následujících dnech se pokračovalo v komplexní resuscitační a intenzivní péči a chirurgických převazech PDK s celkovou toaletou a oplachy rány H2O2 (Obr. 5). Od 17. 7. 2017 jsme používali Prontosan® (B. Braun Medical AG, Sempach, Švýcarsko) a rannou plochu jsme kryli syntetickou náhradou kožního krytu COM® (Výzkumný ústav pletařský, Brno). Denně pokračovala expozice HBOT, celkem 6x. Od 9. 7. 2017 byl nemocný ve stabilizovaném stavu, zlepšila se funkce GIT. Ve výši L3/4 jsme zavedli epidurální katétr ke kontinuální analgezii směsí Marcain + Sufentanil. 12. 7. 2017 jsme založili punkční dilatační tracheostomii (PDTS). V této fázi jsme konzultovali oddělení plastické chirurgie chirurgické kliniky FNHK ohledně možností řešení rozsáhlých defektů měkkých tkání a 25. 7. 2017 jsme nemocného přeložili na JIP chirurgické kliniky FNHK.
Obr. 5. Rozsáhlý defekt po nekrektomiích na pravé dolní končetině (18. 7. 2017)
Fig. 5: Extensive defect after necrectomies on the right lower extremity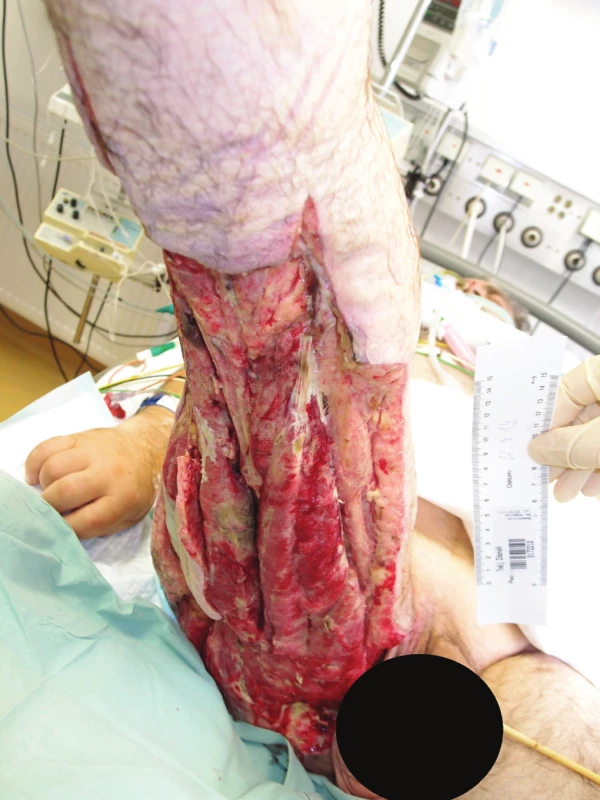
Pacient byl při přijetí na UPV v analgosedaci s kvadruparézou až kvadruplegií při polyneuromyopatii kriticky nemocných. Byl febrilní 39 °C, s průjmy při střevní dysmikrobii a intoleranci enterální výživy, klostridiovou enterokolitidu jsme vyloučili. Pokračovalo se v komplexní intenzivní péči se zvláštním důrazem na metabolicko-nutriční podporu, cílenou antibiotickou léčbu v koordinaci s chirurgickými výkony. Dávka ordinované výživy byla 3340 kcal/den a 64 g bílkoviny/den. Přehled operačních výkonů a přehled mikrobiálních kultivačních nálezů a antibiotické léčby je uveden v Tab. 3 a 4. Dne 6. 8. 2017 jsme nemocného odpojili od UPV a následně 11. 8. 2017 zrušili tracheostomii. Se zlepšováním svalové síly a pokračující rehabilitací postupně odeznívala i polyneuromyopatie kriticky nemocných. Dne 31. 7. 2017 jsme provedli autotransplantaci středně silnými dermoepidermálními štěpy odebranými ze stehna druhé končetiny, meshovanými v poměru 1 : 3. Následovaly převazy obden, hojení bylo příznivé, všechny štěpy se přihojily s výjimkou plochy 5x5 cm na přechodu stehna a gluteální krajiny. Náročnost chirurgické pooperační péče spočívala mj. i v zajištění polohování nemocného vzhledem k lokalizaci transplantátů v gluteální a dorzální krajině pravého stehna. Od 16. 8. 2017 při převazech na JIP jsme prováděli též hydroterapii sprchováním s mikromasáží zhojených ploch (Obr. 6). Pacient pokračoval v rehabilitaci a mobilizaci, zvyšovala se jeho svalová síla a zlepšila se hybnost natolik, že byl schopen chůze v chodítku. 23. 8. 2017 jsme přeložili prakticky zhojeného pacienta na chirurgické oddělení nemocnice v Litomyšli k pokračování v rehabilitaci.
Obr. 6. 16. den po transplantaci, štěpy přihojeny, 2 malé granulační plošky
Fig. 6: 16 days after autografting, grafts healed in, 2 small residual granulation areas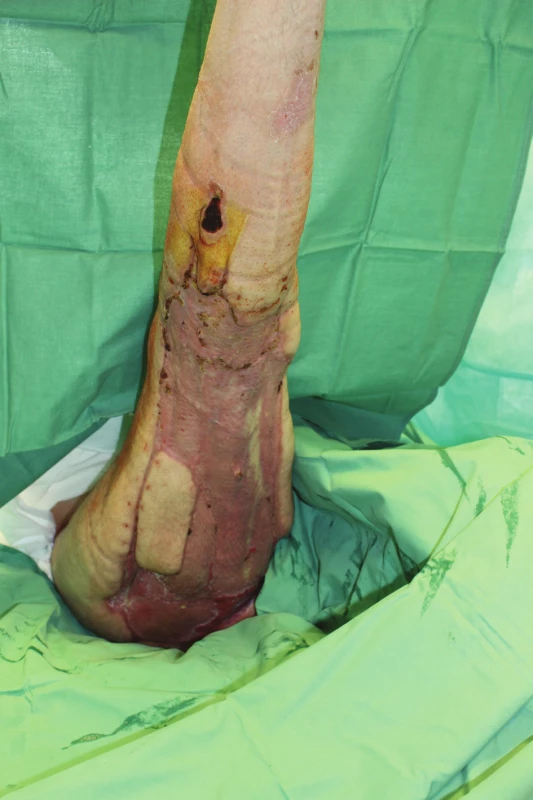
Tab. 3. Přehled operačních výkonů
Tab. 3: Surgical procedures – overview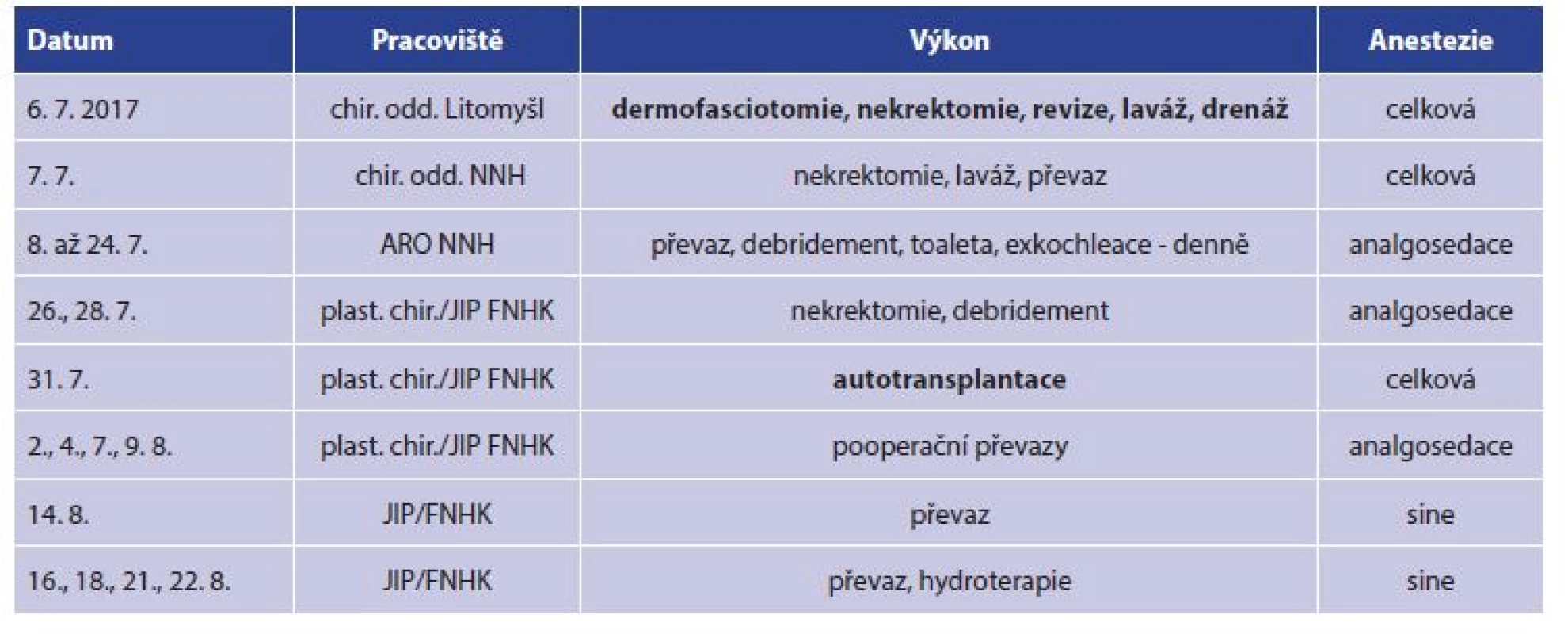
Tab. 4. Celkový přehled kultivačních nálezů a antibiotické léčby
Tab. 4: General overview of microbiological findings and antibiotherapy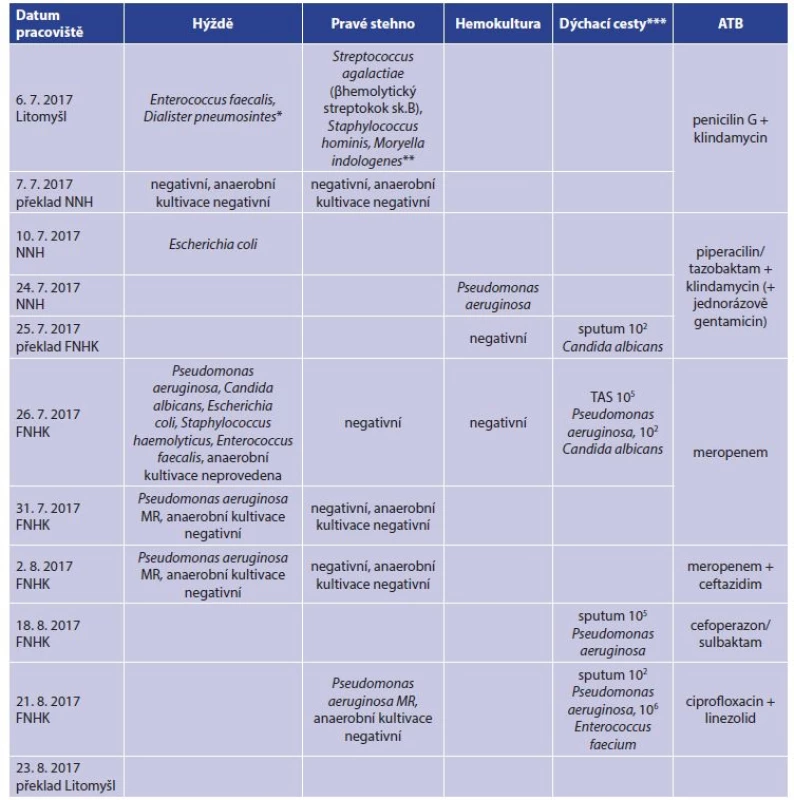
Vysvětlivky: MR − multirezistentní, TAS− tracheální aspirát; *anaerobní gram-negativní kokobacily, součástí orální mikroflóry; **anaerobní gram-pozitivní tyčky, příbuzné Clostridium clostridioforme; ***hodnoty v CFU/ml. Při ambulantní kontrole 2. 10. 2017 se pacient subjektivně cítil dobře, hybnost horních končetin byla v normálním rozsahu. Transplantované plochy PDK byly zhojeny, zbývaly jen dvě malé granulační plošky do 1 cm2 na horním konci stehna dorzálně. Odběrové plochy na levém stehně byly zhojeny. Při následné kontrole 6. 11. 2017 byl pacient komponován, pokračoval v individuální rehabilitaci, zvládal chůzi i na schodech. Místně až na drobný kožní defekt na zevní straně pravého bérce byl zhojen (Obr. 7).
Obr. 7. Stav při ambulantní kontrole 6. 11. 2017
Fig. 7: Status during the outpatient check on 6 November 2017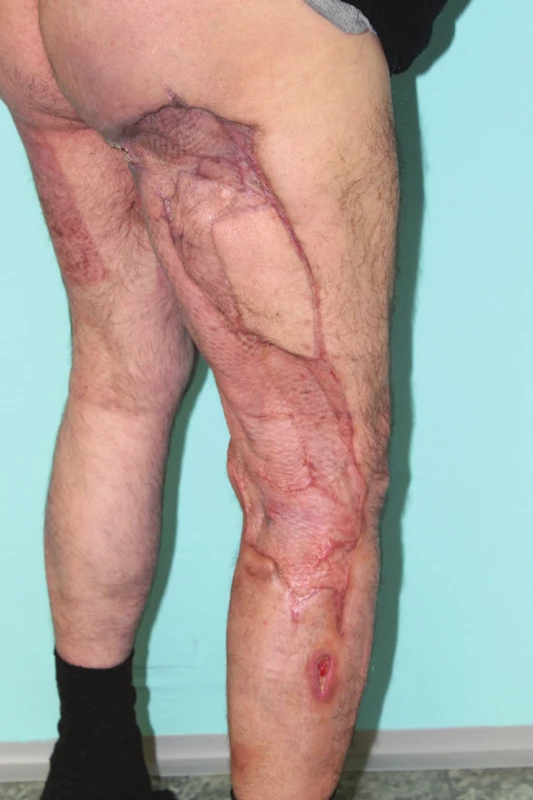
Diskuze
U obou referovaných nemocných s NF – shodou okolností léčených s tříletým odstupem i stejnými týmy shodných zúčastněných pracovišť – lze nalézt několik podobných momentů. Šlo o věkově blízké muže (53 a 61 let) se stejnou lokalizací procesu – oblast pravého třísla, hýžďové krajiny a dorzomediální strany pravé dolní končetiny. Postižení podkožních měkkých tkání i kůže může být lokalizováno kdekoli, avšak nejčastější lokalizací jsou končetiny, zejména dolní, perineum a trup [4,6]. Typický je primárně jednostranný výskyt, ale objevují se i práce popisující multifokální synchronní afekci na několika končetinách současně. Lee et al. popsali v letech 2004–2012 soubor 18 takových případů. Z toho 72 % nemocných mělo oboustranně postižené dolní končetiny, 17 % horní končetiny a 11 % jednu horní a jednu dolní končetinu [7]. Za idiopatickou fasciitidu je považován stav, kdy se nepodaří prokázat místo vstupu infekce (nejčastěji se jedná o drobné kožní oděrky, lacerace, ale i hmyzí bodnutí, rány kousnutím nebo operační rány aj.), jak tomu bylo u našich nemocných. Vstupní bránu infekce se nepodařilo určit ani u jednoho z nich. První muž byl dosud zdráv, nebyl si vědom sebemenšího kožního poranění, jeho onemocnění po netypických prodromech mělofoudroyantní průběh. Druhý muž byl kuřák, kardiak, trpící metabolickými poruchami, hepatopatií. Ani on neudával poranění kožního povrchu či jiný inzult. Podrobnou anamnézou jsme však zjistili, že žije v domácnosti s invalidní manželkou, která trpí otevřenými bércovými vředy a o niž se stará. Navíc v domácnosti s nižším hygienickým standardem jsou kočka a dva psi. Tyto faktory jistě mohly hrát určitou roli. U tohoto nemocného byl počáteční průběh pozvolnější, týden trvající, když udával spontánní prasknutí útvaru v pravém třísle s hnisavou sekrecí. Přestože jistě muselo jít o bolestivou afekci, lékařské ošetření nevyhledal. Popsány jsou i případy vzniku NF po chirurgických výkonech, např. po minimálně invazivní osteosyntéze bérce u zavřené kominutivní fraktury tibie [2], po nitrobřišních operacích [1,4] nebo gynekologicko-urologických operacích [3]. Naopak případ bez jakéhokoli poranění kožního krytu, který začal u dekompenzovaného diabetika jako svědící oblast na stehně a v průběhu 5 dnů se rozvinul do těžké formy NF, popsali Stead a Hedna [8].
Oba referovaní pacienti podstoupili záhy po přijetí rozsáhlou chirurgickou intervenci spočívající v dermofasciotomiích, evakuaci hnisavých ložisek a nekrotických tkání a drenáži. Opakované vydatné oplachy H2O2 vzhledem k možnosti etiologie anaerobními mikroby a dezinfekčními roztoky patří mezi standardní postupy. Další chirurgická lokální péče spočívá v četných převazech ran s kontrolou vývoje stavu tkání a případných pokračujících debridement a nekrektomiích nevitálních částí. V některých závažných případech a v kontextu s celkovým stavem pacienta je nutno zvažovat i provedení amputace končetiny z vitální indikace [9]. Přestože koncept léčby NF v hyperbarické komoře není dosud obecně přijímán, poněvadž zatím chybějí dobře kontrolované, randomizované klinické studie, které by prokázaly její statisticky významný přínos, celá řada autorů se shoduje v názoru, že pokud taková možnost existuje a není-li HBOT z nějakého jiného důvodu kontraindikována, jsou stavy s nekrotizující fasciitidou, n.b. při kultivačním průkazu anaerobních mikrobiálních agens, jednoznačně doporučovány k přetlakové kyslíkové léčbě [1,9,10]. Trend v klinických studiích ukazuje, že HBOT terapie může snížit počet amputací a zvýšit počet zachráněných končetin. Tato zjištění vyžadují multicentrickou, prospektivní studii k posouzení možného přínosu adjuvantní HBOT u NF [11]. V případě, že je stanovená diagnóza NF, chirurgická intervence a zahájení ATB terapie musí vždy předcházet použití HBOT a v žádném případě nesmí dojít k prodlevě [12,13]. U našich pacientů byla na základě klinických nálezů ihned, ještě před znalostí výsledků kultivačních vyšetření, zvažována možnost využití HBOT. Oba byli přeloženi časně, již následující den po přijetí k hospitalizaci a po chirurgické intervenci, do zařízení, které je schopno příslušnou léčbu provést. Pracoviště v NNH má s danou metodou bohaté, většinou dobré zkušenosti, nejen u NF, ale i u jiných diagnóz. Nejvíce zkušeností je s expozicemi při akutních otravách oxidem uhelnatým (řádově desítky až několik stovek případů), dále při tinnitu a u akutní hluchoty (u nichž se však jeví výsledky jako sporné). Z chronických indikací jde nejčastěji o nehojící se trofické defekty dolních končetin a posthypoxickou encefalopatii. U obou nemocných proběhlo celkem 10 a 6 expozic ve standardní délce po 60 minutách, při přetlaku 1,5 ATA a FiO2 1, s dobrým klinickým efektem a zlepšením lokálního i celkového stavu pacienta, samozřejmě za podmínek probíhající kontinuální intenzivní péče. Někdy se doporučuje aplikace HBOT 2x denně v délce trvání expozice 90 minut, při přetlaku 2,5–3 ATA [4]. Sami se přikláníme k názoru, že využití HBOT, existuje-li tato možnost, je vhodné, i když metoda sama jistě nemusí stačit k odvrácení fatálního průběhu onemocnění [9,10]. Z etiologického hlediska jsou u NF rozlišovány dvě rozdílné bakteriální jednotky: typ I s polymikrobiální etiologií a typ II obvykle monobakteriální, způsobený převážně β-hemolytickými streptokoky sk. A (Streptococcus pyogenes) nebo některými dalšími bakteriemi. Streptokoky mohou také produkovat exotoxiny, které vedou k produkci a uvolnění cytokinů (TNF α, TNF β, IL-1, IL-2, IL-6). Působení toxinů vysvětluje většinu klinických symptomů nekrotizující fasciitidy (tkáňová destrukce, šok, orgánová selhání). U typu I je vždy přítomna alespoň jedna anaerobní bakterie (nejčastěji Bacteroides spp., Clostridium spp., peptostreptokoky), která je izolována současně s jedním nebo více fakultativně anaerobními streptokoky (jinými než sk. A) a také s enterobakteriemi (nejčastěji Escherichia coli, Enterobacter spp., Klebsiella spp.). Obligátní aerob (jako např. Pseudomonas aeruginosa) je izolován vzácněji, spíše sekundárně jako kolonizace ranných ploch [14]. U obou našich pacientů se jednalo o polymikrobiální etiologii NF. Na začátku onemocnění byla diagnostikována směs aerobních a anaerobních bakterií. Vždy byl izolován β-hemolytický streptokok Streptococcus agalactiae (Kazuistika 2) a Streptococcus anginosus (Kazuistika 1). V obou případech byla na počátku hospitalizace pozitivní anaerobní kultivace (směs grampozitivních i gramnegativních anaerobních bakterií: bakteroidy, klostridia) a také enterobakterie (Escherichia coli). V průběhu ATB terapie docházelo k selekci rezistentních bakterií (Enterococcus faecalis, Klebsiella pneumoniae produkující širokospektrou β-laktamázu ESBL, Pseudomonas aeruginosa). Tyto kmeny byly před výskytem v ranných plochách většinou izolovány nejdříve ve screeningovém výtěru z rekta nebo z dýchacích cest, jednalo se tedy o endogenní zdroj. Výskyt kvasinek (Candida albicans) považujeme za kolonizaci. Složení smíšené infekce většinou odpovídá lokalizaci procesu; NF hlavy a krku je způsobena nejčastěji bakteriemi, které jsou součástí mikroflóry dutiny ústní a horních cest dýchacích (fuzobakterie, anaerobní streptokoky, bakteroidy a spirochety). Pokud je infekce lokalizována v dolní části těla (břicho, hýždě, dolní končetiny), bývá způsobena flórou gastrointestinálního traktu (klostridia, bakteroidy, prevotely) [15]. Této teorii odpovídají i nálezy u našich pacientů.
Optimální empirická ATB terapie nekrotizující fasciitidy není jasná. Vzhledem k tomu, že na počátku onemocnění nelze etiologii odlišit, obecně by terapie měla zahrnovat široké spektrum grampozitivních, gramnegativních a anaerobních bakterií, se zvláštní pozorností k Streptococcus pyogenes a klostridiím. Vhodná volba zahrnuje betalaktamové ATB s inhibitorem betalaktamázy (ampicilin/sulbaktam, amoxicilin/klavulanát, piperacilin/tazobaktam) nebo karbapenem v kombinaci s klindamycinem [10]. Předpokládá se, že ATB s inhibičním účinkem na proteosyntézu (klindamycin, linezolid) jsou schopny redukovat uvolňování exotoxinů z grampozitivních bakterií. V oblastech se zvýšeným výskytem Staphylococcus aureus MRSA je vhodné připojit do úvodní terapie i ATB účinné na MRSA (vankomycin, linezolid, ceftarolin). Neutropeničtí a imunosuprimovaní pacienti nesou vyšší riziko výskytu Pseudomonas aeruginosa a multirezistentních bakterií, a proto je doporučováno v širokospektré empirické ATB terapii vždy počítat s protipseudomonádovým ATB v kombinaci s glykopeptidy nebo linezolidem [16]. Velkým úskalím ATB léčby akutní nekrotizující fasciitidy je nebezpečné poddávkování ATB. Nedostatečné dávky mohou být následkem zažitých dávkovacích schémat, která nerespektují tělesnou hmotnost pacienta a zvýšený distribuční objem v šokovém stavu [17]. Po zjištění výsledků mikroskopie a kultivace je vhodné ATB léčbu s ohledem na ně upravit. V případě pozitivity Streptococcus pyogenes by měla být terapie změněna na penicilin v kombinaci s klindamycinem. Optimální délka ATB terapie není definována, závisí na okolnostech konkrétního pacienta a klinickém stavu, v závažných případech by měla dosahovat 14−21 dní [16]. Atributivní letalita NF byla v roce 1995 30−60 % [15]. Pokrok v klinické péči, interdisciplinární spolupráce a účinnější ATB vedly k jejímu snížení. Ve studii z roku 2012 je udávaná letalita 20,8 % [18]. Incidence závažných infekcí kůže a měkkých tkání se v posledních letech signifikantně zvýšila [16]. Avšak v této době proběhly také velké etiologické změny, současně narůstá počet imunosuprimovaných osob a ukazuje se také vyšší incidence multirezistentních patogenů. Tyto faktory mohou současný trend změnit a představují tak trvalou výzvu pro budoucnost. Rozvoj NF je obvykle provázen sepsí s rozvojem syndromu multiorgánové dysfunkce [19,20]. Nemocní mohou v určité fázi léčby vyžadovat mimo výše uvedené terapeutické kroky nejvyšší stupeň komplexní intenzivní péče s podporou selhávajících orgánových systémů včetně farmakologické podpory oběhu, nutriční podpory, umělé plicní ventilace a náhrady funkce ledvin [13]. Protrahovaný charakter onemocnění a opakované inzulty operační povahy, kterým jsou nemocní často vystaveni, jsou důvodem dlouhodobého a těžkého katabolického stavu [21] s vysokým rizikem vzniku vzdálených infekčních komplikací a opožděného hojení ran [22]. Závažným problémem může být tzv. polyneuromyopatie kriticky nemocných, která spolu s dlouhodobou imobilizací a katabolismem komplikuje rekonvalescenci nemocných z akutní fáze [23]. Vysoký standard intenzivní péče a zajištění kvalitní analgezie jsou nezbytnými předpoklady úspěšného převedení nemocných akutní fází onemocnění [13]. U obou našich nemocných bylo možno kontinuálně při všech překladech na jednotlivá pracoviště tuto péči zabezpečit. Díky vysoké kvalitě zajištění celkového stavu nemocných mohly být prováděny jednotlivé chirurgické intervence, které umožnily definitivní zhojení z hlediska obnovy tělesného povrchu a zhojení defektů měkkých tkání.
Vzhledem k rozsahu vzniklých defektů měkkých tkání dolních končetin u obou pacientů bylo nutno stav řešit autotransplantací kůže. V přípravě ranných ploch jsme postupovali standardním způsobem, opakovaným mechanickým debridement s podporou tvorby granulací syntetickým krytem COM (Výzkumný ústav pletařský, Brno) a rovněž podtlakovým mechanismem využitím systému VAC (Vacuum Assisted Closure). Kožní transplantáty byly meshovány v poměru 1 : 3 s cílem expanze získané kůže, umožnění odtoku ranného sekretu i lepšího přilnutí ke spodině. Důsledná pooperační místní péče, pečlivé převazování, správná obvazová technika včetně polohování nemocného jsou nezbytným požadavkem pro příznivý průběh hojení jak transplantovaných, tak i odběrových ploch [24]. U obou našich pacientů došlo k přihojení štěpů mezi 10. a 14. dnem s primárně zhojenými odběrovými plochami na druhostranné končetině. Přímé sutury vzniklých defektů bývají málokdy možné, a proto nejčastějším způsobem rekonstrukce kožního povrchu jsou transplantace volných kožních štěpů. Objevují se však i zprávy o využití volných myokutánních laloků přenášených mikrochirurgickou technikou, zejména po amputačních výkonech. Gawaziuk a spol. použili v 7letém období 12x přenos volného laloku – nejčastěji (10x) z anterolaterální strany stehna, 1x m. latissimus dorsi a 1x tzv. čínský lalok z předloktí. Rekonstruovaná recipientní místa byla 6x na horních končetinách, 4x na dolních, 1x na hlavě a krku a 1x v oblasti hráze a zevního genitálu. Všechny laloky se přihojily bez komplikací [6].
Nedílnou součástí komplexní léčby je rehabilitace jednak celková a jednak cíleně zaměřená na oblasti s omezením funkce, zejména končetiny. U obou našich nemocných došlo v důsledku nutnosti resuscitační a následné intenzivní péče ke vzniku polyneuromyopatie kriticky nemocných. Tato však s postupující vertikalizací a cvičením odeznívala. Při ambulantních kontrolách s dlouhodobým odstupem u prvního nemocného přetrvává oslabená síla svalová při stisku levé ruky, u druhého z nich došlo v tomto smyslu prakticky k úplné restituci (listopad 2017).
Souhrnně je možno konstatovat, že všechny recentní práce našich i zahraničních autorů zdůrazňují, a naše zkušenosti to potvrzují, že pro řešení závažných stavů při nekrotizující fasciitidě je nezbytný mezioborový přístup a spolupráce. Stěžejní jsou co nejčasnější radikální chirurgické intervence, doplněné cílenou antibioterapií a zajištění intenzivní, resp. resuscitační péče s případným využitím hyperbarické oxygenoterapie. Obnovení tělesného krytu může, zejména u rozsáhlých defektů, vyžadovat zapojení i plastického chirurga do této spolupráce.
Závěr
Nekrotizující fasciitida je velmi závažné, akutní infekční onemocnění, se kterým se, byť ne příliš často, může setkat prakticky každé chirurgické pracoviště. Onemocnění je spojeno se závažnou morbiditou a vysokou letalitou. Má-li být léčba úspěšná, vyžaduje aktivní radikální chirurgický přístup podporovaný účinnou antibioterapií se zajištěním adekvátní celkové resuscitační, resp. intenzivní péče včetně následné rehabilitace. V našich kazuistikách je popsána koordinovaná multioborová spolupráce několika pracovišť, která nepochybně umožnila zdárný průběh léčení obou kriticky nemocných.
Seznam zkratek
ARDS – syndrom akutní dechové tísně
ARO – anesteziologicko-resuscitační odd.
ATA – atmosféra technická absolutní
ATB – antibiotikum, antibiotika, antibiotický
CFU – colony forming unit
CRP – C-reaktivní protein
CT – počítačová tomografie
ESBL+ – pozitivní produkce širokospektré betalaktamázy
FH – francouzské hole
FiO2 – inspirační frakce kyslíku
FNHK – Fakultní nemocnice Hradec Králové
GIT – gastrointestinální trakt
HBOT – hyperbarická oxygenoterapie
ICHS – ischemická choroba srdeční
JIP – jednotka intenzivní péče
KARIM – klinika anesteziologie, resuscitace a intenzivní medicíny
MODS – syndrom multiorgánové dysfunkce
MR – multirezistentní
MRSA – meticilin-rezistentní zlatý stafylokok
NF – nekrotizující fasciitida
NNH – Nemocnice Na Homolce
PCI – perkutánní koronární intervence
PCT – prokalcitonin
PDK (LDK) – pravá (levá) dolní končetina
PDTS – punkční dilatační tracheostomie
RLP – rychlá lékařská pomoc
TAS – tracheobronchiální aspirát
TF – tepová frekvence
TK – tlak krevní
TT – tělesná teplota
UPV – umělá plicní ventilace
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
doc. MUDr. Leo Klein, CSc.
Oddělení plastické chirurgie a léčby popálenin
Chirurgická klinika LFUK a FN
Sokolská 581
500 05 Hradec Králové
e-mail: leo.klein@fnhk.cz
Zdroje
-
Jandík J, Vokůrka J. Nekrotizující fasciitida břišní stěny po cholecystektomii – kazuistika. Rozhl Chir 2009;88 : 35−9.
-
Shang S, Zhang R, Hou Z. Necrotizing fasciitis – A catastrophic complication following routine tibia fracture surgery. Medicine 2017. Available from: http://dx.doi.org/10.1097/MD.0000000000006908.
-
Kerbaj J, Aubry C, Prost C, et al. Thigh abscess and necrotizing fasciitis following an inside-out transobturator tape intervention: a case report. J of Med Case Reports 2016. Available from: DOI 10.1186/s13256-016-0942-3.
-
Svatoň R, Neumann C, Hanslianová M. Nekrotizující fasciitida, vzácná komplikace laparoskopické apendektomie. Rozhl Chir 2009;88 : 27−31.
-
Makadia J, Bhanot N, Mancini SA, et al. Clinical evolution, management, and resolution of type II necrotizing fasciitis. Intern Emerg Med 2015;10 : 389−1.
-
Gawaziuk JP, Liu T, Sigurdson L, et al. Free tissue transfer for necrotizing fasciitis reconstruction: A case series. Burns 2017. Available from: http://dx.doi.org/10.1016/j.burns.2017.04.007.
-
Lee ChY, Li YY, Huang TW, et al. Synchronous multifocal necrotizing fasciitis prognostic factors: a retrospective case series study in a single center. Infection 2016;44 : 757−63.
-
Stead TS, Hedna VS. Necrotizing fasciitis presenting as an itchy thigh. Case reports in emergency medicine 2016. Available from: http://dx.doi.org/10.1155/2016/6376301.
-
Kojič M, Mikič D, Nožič D, et al. Streptococcal necrotizing fasciitis with toxic shock syndrome and rapid fatal outcome. Srp Arh Celok Lek 2015;143 : 476−9.
-
Gürlich R, Adámková V, Ulrych J, et al. Infekce kůže a měkkých tkání. Rozhl Chir 2016;95 : 141−6.
-
Hassan Z, Mullins RF, Friedman BC, et al. Treating necrotizing fasciitis with or without hyperbaric oxygen therapy. Undersea Hyperb Med 2010;37 : 115−23.
-
Stevens DL, Bisno AL, Chambers HF, et al. Practice guidelines for the diagnosis and management of skin and soft tissue infections: 2014 update by the infectious diseases society of America. Clin Infect Dis 2014;59 : 147−59.
-
Hakkarainen TW, Kopari NM, Pham TN, et al. Necrotizing soft tissue infections: review and current concepts in treatment, systems of care, and outcomes. Curr Probl Surg 2014;51 : 344−62.
-
Versalovic J. Manual of clinical microbiology. Washington, ASM Press 2011 : 834−58.
-
Brook I, Frazier EH. Clinical and microbiological features of necrotizing fasciitis. Journal of Clinical Microbiology 1995;33 : 2385−7.
-
Montravers P, Snauwaert A, Welsch C. Current guidelines and recommendations for the management of skin and soft tissue infection 2016. Curr Opin Infect Dis 2016;29 : 131−8.
-
Adámková V. Antibiotická léčba infekcí kůže a měkkých tkání – současné možnosti a limity. Remedia 2015;2 : 150−3.
-
Tsitsilonis S, Druschel C. Necrotizing fasciitis: is the bacterial spectrum changing? Langenbeck Arch Surg 2013;398 : 153−9.
-
Misiakos EP, Bagias G, Patapis P, et al. Current concepts in the management of necrotizing fasciitis. Frontiers in Surgery 2014;1 : 36.
-
Bhatia, N, Castro-Borobio M, Greene J, et al. Necrotizing fasciitis secondary to eromonas Infection presenting with septic shock. Case Reports in Emergency Medicine 2017. Available from: htpps://doi.org/10.1155/2017/4607582.
-
Graves C, Saffle J, Morris S, et al. Caloric requirements in patients with necrotizing fasciitis. Burns 2005;31 : 55−9.
-
Light TD, Choi KC, Thomsen TA. Long-term outcomes of patients with necrotizing fasciitis. J Burn Care Res 2010;31 : 93−9.
-
Friedrich O, Reid MB, Van den Berghe G, et al. The sick and the weak: Neuropathies/myopathies in the critically Ill. Physiological Reviews 2015;95 : 1025−1109.
-
Königová R, Bláha J a kol. Komplexní léčba popáleninového traumatu. Univerzita Karlova v Praze, Praha, Nakladatelství Karolinum 2010.
Štítky
Chirurgia všeobecná Ortopédia Urgentná medicína
Článok vyšiel v časopiseRozhledy v chirurgii
Najčítanejšie tento týždeň
2018 Číslo 9- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
-
Všetky články tohto čísla
- Doporučené postupy v medicíně
- Současné poznatky o regeneraci ischemických tkání a zlepšení prokrvení pomocí kmenových buněk – možnosti využití u nerevaskularizovatelné kritické končetinové ischemie
- Preventivní opatření rozvoje hluboké sternální infekce po kardiochirurgických výkonech − přehled
- RFITTH – radiofrekvenčně indukovaná termoterapie hemoroidů, 10 let zkušeností
- Kompresia truncus coeliacus – princípy diagnostiky a chirurgickej liečby
- Zemřel docent Jiří Šiller
- Asynchronní kvadruplicitní výskyt nádorového onemocnění: adenokarcinomu rektosigmatu, karcinomu ledviny, adenokarcinomu prostaty a neuroendokrinního malobuněčného karcinomu plic – kazuistika
- Fasciitis necrotisans – duplicitas casuum
- Světlobuněčný sarkom šlach a aponeuróz s lokalizací v pravé genitofemorální rýze – kazuistika
- Rozhledy v chirurgii
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Kompresia truncus coeliacus – princípy diagnostiky a chirurgickej liečby
- RFITTH – radiofrekvenčně indukovaná termoterapie hemoroidů, 10 let zkušeností
- Světlobuněčný sarkom šlach a aponeuróz s lokalizací v pravé genitofemorální rýze – kazuistika
- Preventivní opatření rozvoje hluboké sternální infekce po kardiochirurgických výkonech − přehled
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy




