-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Alemtuzumab v terapii chronické lymfocytární leukemie: retrospektivní analýza a hodnocení léčebné odpovědi podle cytogenetického rizika
Alemtuzumab in chronic lymphocytic leukemia treatment: retrospective analysis of outcome according to cytogenetics
Alemtuzumab is effective in B-cell chronic lymphocytic leukemia (CLL) with 17p deletion, which responds poorly to chemotherapeutic agents. Our retrospective study evaluated the benefit of alemtuzumab monotherapy in unselected patients with advanced CLL, categorized by cytogenetic profile. Data were collected from 74 consecutive who had received alemtuzumab. Median of previous therapies was 2. The incidence of cytogenetic abnormalities was: trisomy 12, 10%; 13q deletion, 13%; 11q deletion 25%; 17p deletion, 26%; none of these, 26%. The overall response rate was 65% (11% complete remission, 54% partial remission) in the whole cohort. From start of alemtuzumab therapy, median progression‑free survival was 217 days, median time to alternative treatment was 287 days, and median overall survival was 999 days in the total cohort, respectively. Alemtuzumab was effective across all cytogenetic categories evaluated. There were no statistically significant differences between subgroups in the level of efficacy.
Key words:
alemtuzumab – chronic lymphocytic leukemia – cytogenetic risk – treatment
Autoři: M. Doubek 1; A. Jungová 2; M. Brejcha 3; A. Panovská 1; Y. Brychtová 1; Z. Pospíšil 4; J. Mayer Za Českou Leukemickou Skupinu Pro Život (cell 1; The Czech Leukemia Study Group For Life)
Působiště autorů: Interní hematoonkologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Jiří Vorlíček, CSc. 1; Hematologicko‑onkologické oddělení FN Plzeň, přednosta prim. MUDr. Vladimír Koza 2; Hematologické oddělení Onkologického centra J. G. Mendela Nový Jičín, přednosta prim. MUDr. Martin Brejcha 3; Ústav matematiky a statistiky Přírodovědecké fakulty MU Brno, ředitel prof. RNDr. Jiří Rosický, DrSc. 4
Vyšlo v časopise: Vnitř Lék 2009; 55(6): 549-554
Kategorie: Původní práce
Souhrn
Alemtuzumab je účinný lék v terapii chronické lymfocytární leukemie (CLL) s delecí 17p, která bývá rezistentní na chemoterapeutika. V naší retrospektivní analýze jsme se zaměřili na sledování účinků alemtuzumabu v monoterapii u neselektované skupiny pacientů s CLL, kteří byli stratifikováni podle cytogenetického rizika. Analyzována byla data od 74 konsekutivních nemocných, kteří dostávali alemtuzumab. Medián předešlých terapií byl 2. Výskyt cytogenetických nálezů v souboru byl následující: 10 % trisomie 12, 13 % delece 13q, 25 % delece 11q, 26 % delece 17p a 26 % normální nález. Celková příznivá léčebná odpověď v souboru byla zaznamenána u 65 % pacientů (11 % kompletních remisí a 54 % parciálních remisí). Ode dne zahájení terapie alemtuzumabem byl medián přežití bez progrese nemoci 217 dnů, medián času do další terapie 287 dnů a medián celkového přežití 999 dnů. Alemtuzumab byl účinný u všech cytogenetických podskupin CLL. Nezaznamenali jsme žádný statisticky významný rozdíl v účinnosti léku mezi těmito skupinami.
Klíčová slova:
alemtuzumab – chronická lymfocytární leukemie – cytogenetické riziko – léčbaÚvod
Chronická lymfocytární leukemie (CLL) je nejčastější leukemií bělochů. Ukazuje se, že toto onemocnění je stran prognózy i volby optimální terapie značně heterogenní. Jednou z léčebných možností u CLL je použití monoklonálních protilátek (v monoterapii nebo kombinaci s dalšími léky) namířených proti antigenům na povrchu maligních buněk. V současnosti nejčastěji používanými monoklonálními protilátkami v léčbě CLL jsou rituximab a alemtuzumab [1].
Alemtuzumab (MabCampath®, BayerSchering Pharma AG, Berlín, Německo) je humanizovaná monoklonální protilátka namířená proti znaku CD52. Alemtuzumab po navázání na antigen CD52, který je fyziologicky nejvíce exprimován především T - a B‑lymfocyty, ale i monocyty a dalšími buňkami, spouští komplementem zprostředkovanou lýzu buňky, startuje protilátkou zprostředkovanou na buňkách závislou cytotoxickou reakci (ADCC), ovlivňuje funkci kalciových kanálů a indukuje apoptózu [2,3]. Antigen CD52 je jednou z nejpočetnějších molekul na povrchu lymfocytů. Lidské lymfocyty nesou podle Haleho na své membráně až 450 000 molekul CD52, což představuje pokrytí až 5 % jejich povrchu [3].
V současné době je alemtuzumab v běžné praxi indikován v monoterapii zejména u pacientů s rezistentní nebo relabovanou CLL, případně jako lék pro pacienty s CLL a delecí nebo mutací genu p53, pro něž představuje nejúčinnější léčebnou možnost, pomineme‑li alogenní transplantaci krvetvorných buněk [1,4,5]. Ačkoliv alemtuzumab je lék známý od 80. let 20. století a první zprávy o jeho použití u CLL pochází z 90. let 20. století, stále je jeho postavení v léčbě CLL nejasné. Pomineme‑li pokusy podávat alemtuzmab v kombinaci s dalšími léky, používat jej u CLL jako lék první volby nebo jej indikovat k léčbě zbytkové nemoci, jsou nejasné i jeho účinky na jednotlivé rizikové skupiny pacientů s CLL [1,6]. Dosud jen jedna in extenso publikovaná práce si všímala účinku alemtuzumabu u cytogenetických podskupin CLL [7].
Cílem naší analýzy bylo zmapovat reálnou praxi podávání alemtuzumabu u nás (nepočítáme‑li klinické studie) jako terapie další linie u CLL. Zaměřili jsme se na indikace alemtuzumabu, výsledky léčby a vedlejší efekty tohoto léku. Naší prioritou byla analýza léčebné odpovědi vztažená k cytogenetickému nálezu u pacientů.
Pacienti a metody
Provedli jsme retrospektivní sběr dat dotazníkovou metodou. Sběru dat se zúčastnila 3 česká hematoonkologická pracoviště: Interní hematoonkologická klinika LF MU a FN Brno‑Bohunice, Hematologicko‑onkologické oddělení FN Plzeň a Onkologické centrum J. G. Mendela Nový Jičín. Tato pracoviště poskytla data o všech svých nemocných léčených alemtuzumabem mimo klinické studie. Dotazník obsahoval pro každého pacienta 45 položek (mimo jiné identifikační data nemocných, pohlaví, stadium nemoci, počty předchozích terapií, předchozí efekt fludarabinu, parametry krevního obrazu před léčbou a v průběhu léčby, cytogenetické nálezy před podáním alemtuzumabu (fluorescenční in situ hybridizace, FISH) a další nové prognostické faktory [6], celkovou dávku alemtuzumabu, léčebnou odpověď a vedlejší efekty léčby).
Statistická analýza výsledků zahrnovala výpočet celkového přežití (OS), přežití bez progrese nemoci (PFS) a času do alternativní (další) terapie (TTAT) od zahájení podávání alemtuzumabu podle Kaplanovy-Meierovy metody. Statistická významnost rozdílů mezi jednotlivými hodnocenými skupinami byla počítána pomocí Gehanova-Wilcoxonova testu. Za hranici statistické významnosti byla považována hodnota p = 0,05.
Výsledky
Zpracována byla data od 74 nemocných (27 žen a 47 mužů). Medián jejich věku při stanovení diagnózy CLL byl 57 let (průměr 56,7; 41–71).
Lék byl podáván ve standardním dávkování 30 mg i.v. nebo s.c. 3krát týdně (po úvodní eskalaci dávky) podle platných doporučení [8]. Profylakticky byl nejčastěji podáván cotrimoxazol (480 mg denně) a acyklovir (800 mg denně). Jako prevence s infuzí nebo injekcí spojených nežádoucích účinků byla používána kombinace paracetamol + antihistaminikum + kortikoid. Detailní analýza profylaktických opatření ale nebyla cílem této naší studie.
Medián počtu předchozích terapií před podáním alemtuzumabu byl 2 (průměr 2,1; 0–6). Režimem obsahujícím fludarabin bylo před alemtuzumabem léčeno 60 nemocných (81 %). CLL rezistentní na fludarabin mělo 25 z 59 nemocných (42 %), u nichž bylo možné rezistenci hodnotit. Další charakteristiky souboru nemocných před zahájením terapie alemtuzumabem udává tab. 1. Léčba alemtuzumabem byla indikována i u 18 nemocných, kteří měli stadium CLL 0 nebo I podle Raie. Tito nemocní byli léčeni proto, že u nich byly přítomny symptomy nemoci (B symptomy). Cytogeneticky (FISH) byly zjištěny tyto prognostické kategorie [9]: del 17p u 19 pacientů (26 %), del 11q u 18 (25 %), + 12 u 7 (10 %), normální karyotyp u 19 (26 %) a del 13q u 9 (13 %) (tab. 2).
Medián doby podávání alemtuzumabu byl 9 týdnů (průměr 8,9; 1–23). Medián kumulativní dávky alemtuzumabu byl 354,5 mg (průměr 480,2; 3–1280).
Léčebná odpověď [10] byla zhodnocena u 71 nemocných. U 8 nemocných (11 %) bylo dosaženo kompletní remise (CR), u 38 (54 %) parciální remise (PR), u 10 (14 %) bylo zaznamenáno stabilní onemocnění (SD) a u 15 (21 %) byla zjištěna v průběhu terapie progrese CLL (tab. 3).
Nežádoucí účinky léčby alemtuzumabem shrnuje tab. 4. K nejčastějším nežádoucím účinkům patřily infekční komplikace (64 %, včetně reaktivace cytomegaloviru), vedlejší efekty spojené s aplikací léku (38 %) a hluboká neutropenie pod 0,5 × 109/l (31 %).
Medián PFS počítaný od 1. dne aplikace alemtuzumabu byl v našem souboru 217 dní. Statisticky významně se nelišil v žádné z cytogenetických podskupin. Medián TTAT byl 287 dní. Také tento se nelišil v žádné z cytogenetických podskupin. Medián OS byl 999 dní a i ten se významně nelišil u žádné z cytogenetických podskupin. Při srovnání cytogeneticky nepříznivých CLL (del 17p + del 11q) s cytogeneticky příznivými CLL (ostatní) byly zjištěny statisticky nevýznamně lepší PFS, TTAT i OS ve skupině cytogeneticky příznivých CLL (tab. 5 a obr. 1–6).
Obr. 1. Přežití bez progrese nemoci (PFS) celého souboru CLL pacientů. 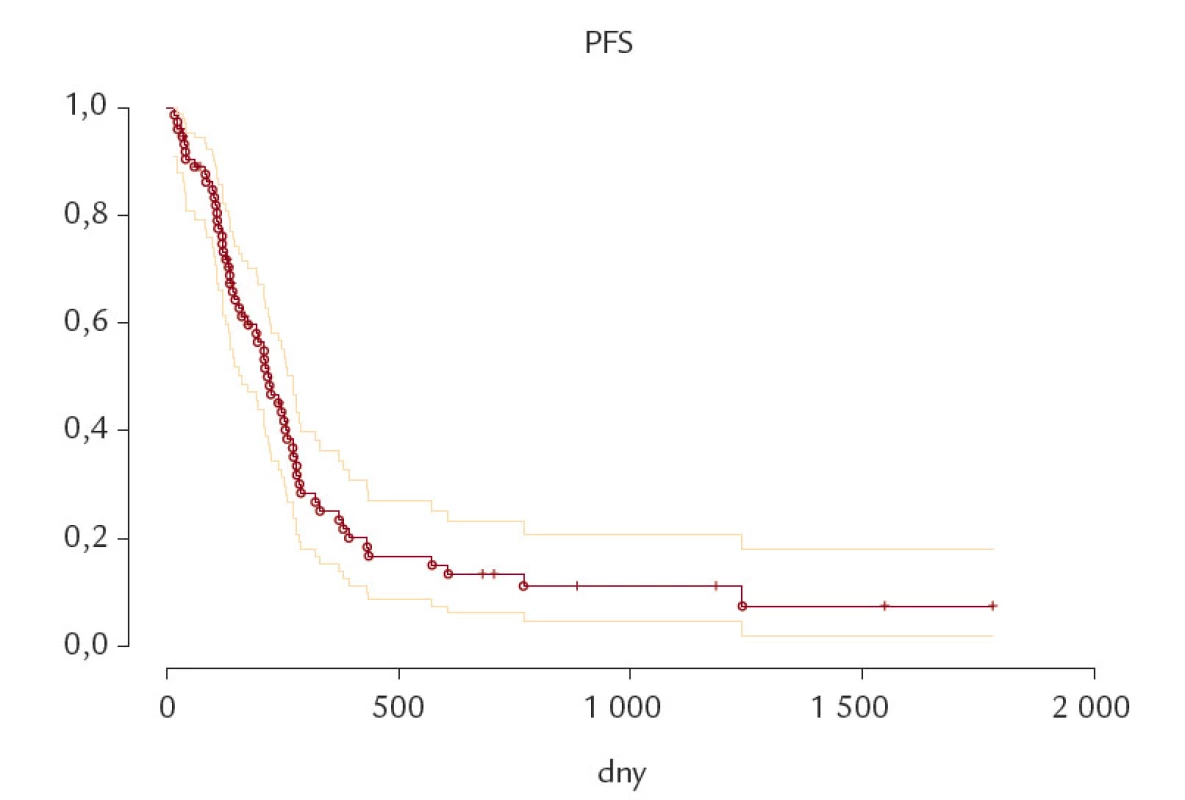
Obr. 2. Přežití bez progrese nemoci (PFS) u skupiny cytogeneticky nepříznivých (unfavourable, del 17p + del 11q) a cytogeneticky příznivých (favourable, ostatní) chronických lymfocytárních leukemií. p – statisticky nevýznamné 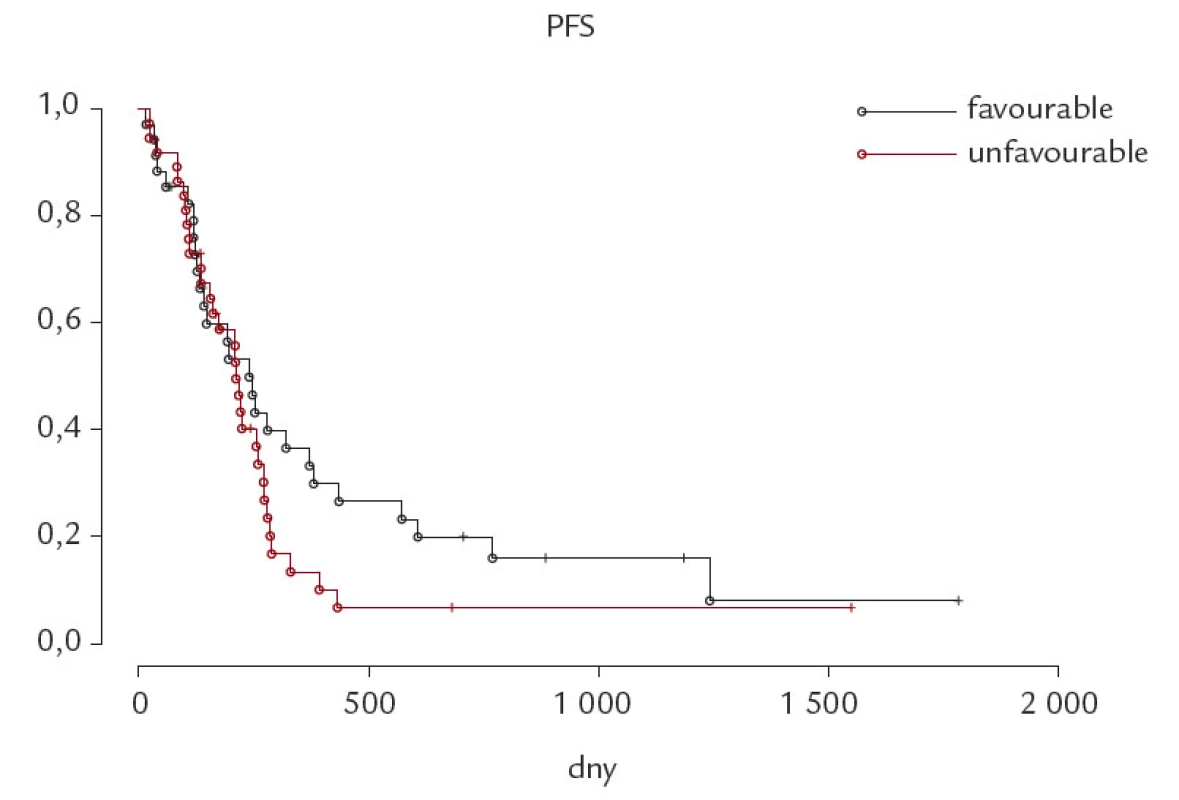
Obr. 3. Čas do další terapie (TTAT) celého souboru CLL pacientů. 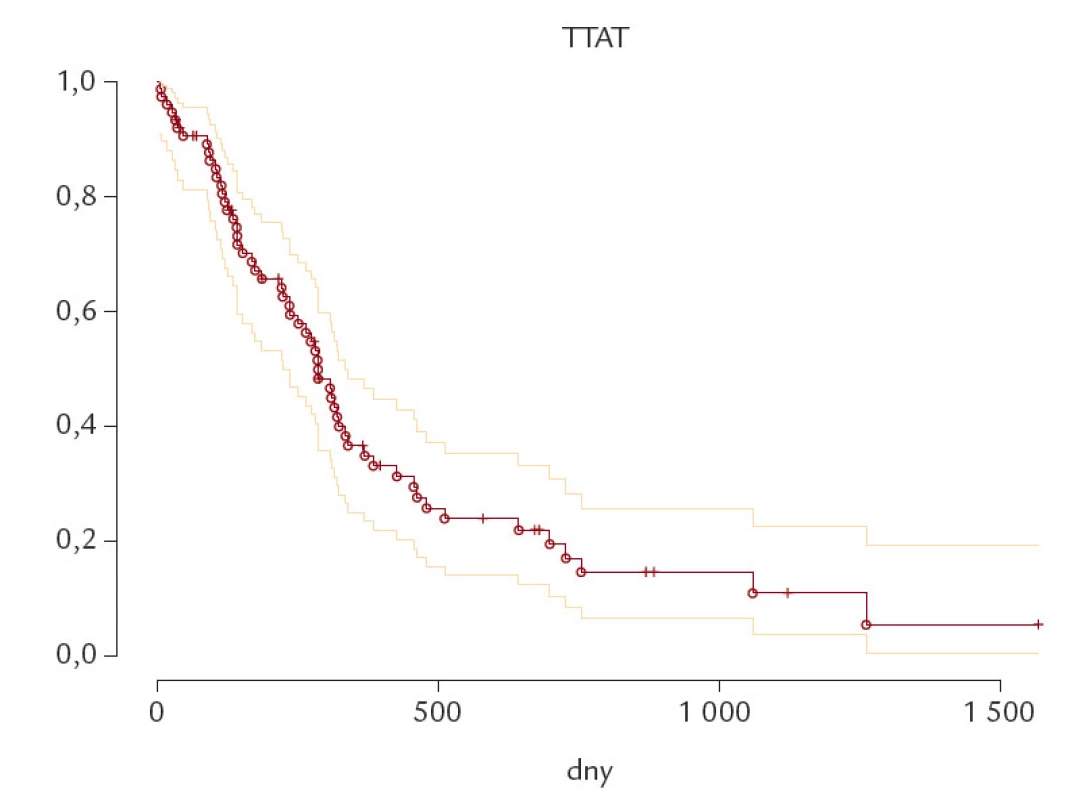
Obr. 4. Čas do další terapie (TTAT) u skupiny cytogeneticky nepříznivých (unfavourable, del 17p + del 11q) a cytogeneticky příznivých (favourable, ostatní) chronických lymfocytárních leukemií. p – statisticky nevýznamné 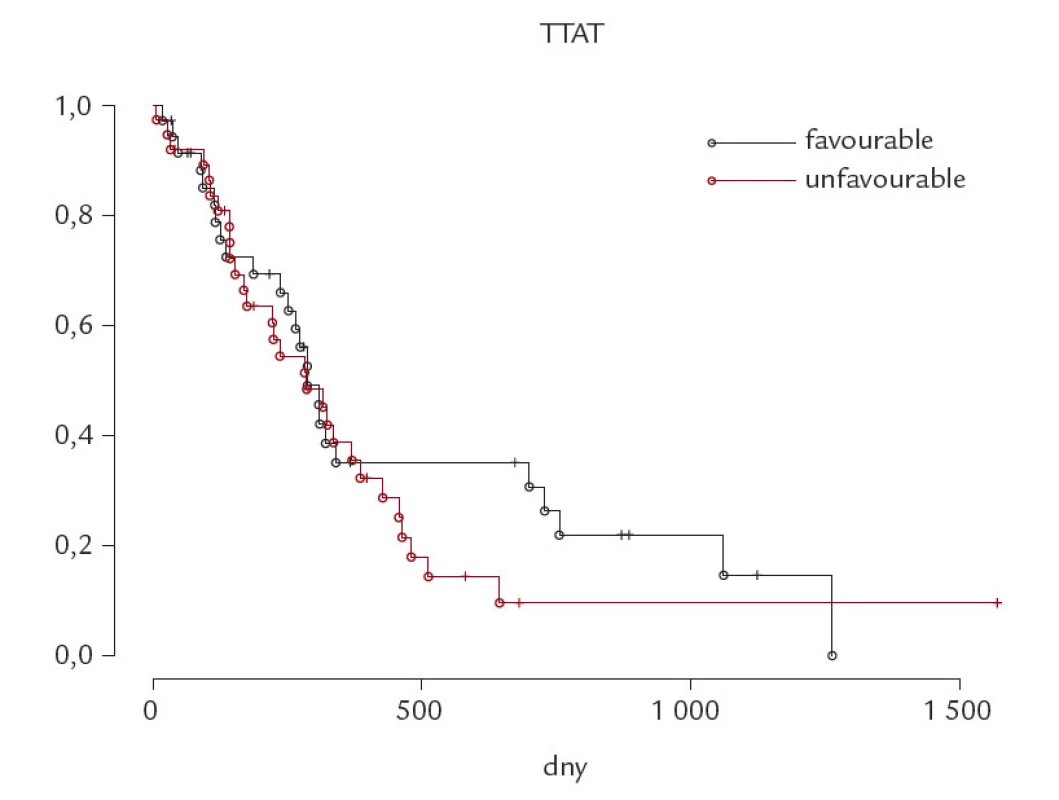
Obr. 5. Celkové přežití (OS) celého souboru CLL pacientů. p – statisticky nevýznamné 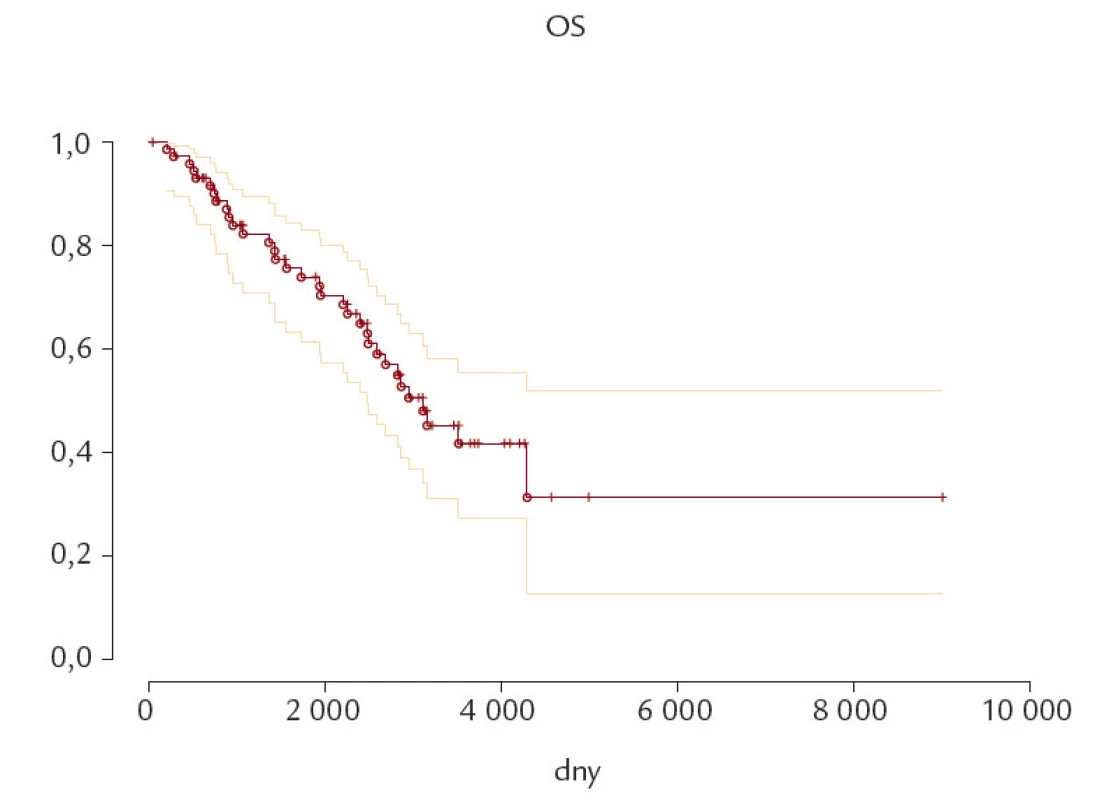
Obr. 6. Celkové přežití (OS) u skupiny cytogeneticky nepříznivých (unfavourable, del 17p + del 11q) a cytogeneticky příznivých (favourable, ostatní) chronických lymfocytárních leukemií. p – statisticky nevýznamné 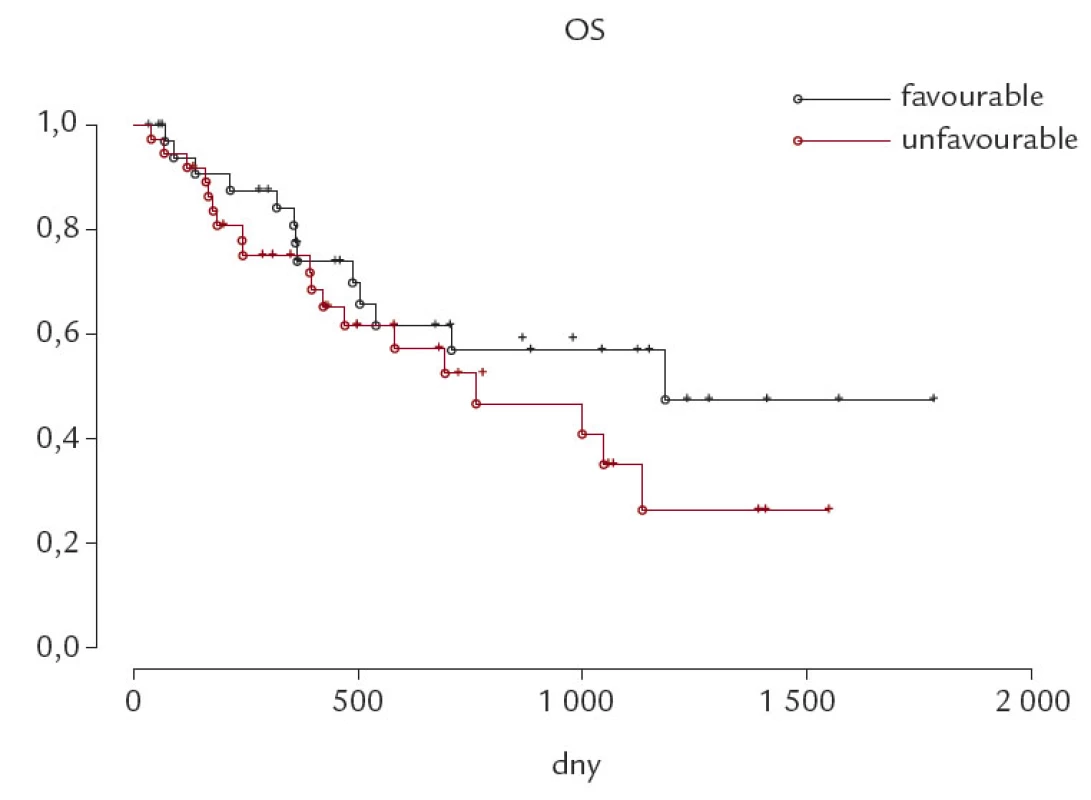
Diskuze
Alemtuzumab je v léčbě CLL používán už více než 10 let [11]. Nejdříve byl dáván v monoterapii u pacientů s rezistentní a relabovanou CLL, později v monoterapii jako lék první linie [12], posléze byly zkoušeny kombinace alemtuzumabu s jinými léky [1,13] nebo alemtuzumab v léčbě zbytkové nemoci u CLL [14,15]. Nicméně, pomineme‑li analýzy účinků alemtuzumabu u CLL se změnami genu p53 [4,5,16], tak pouze jedna velká práce si dosud všímala efektu alemtuzumabu u jednotlivých cytogenetických podskupin CLL. Šlo o studii CAM307 [7].
Výsledky první velké mezinárodní studie (CAM211), která hodnotila účinky alemtuzumabu (30 mg 3krát týdně po dobu 12 týdnů) u nemocných, u nichž selhal fludarabin, uveřejnili Keating et al [17]. Z 93 pacientů dosáhlo léčebné odpovědi 33 %. Avšak jen 2 % remisí byly CR. Medián času do progrese byl u nemocných, kteří remise dosáhli, 9,5 měsíce (medián trvání remise 8,7 měsíců). Medián celkového přežití byl 16 měsíců pro všechny nemocné a 32 měsíců pro pacienty, kteří dosáhli léčebné odpovědi. 55 % nemocných mělo v průběhu léčby alespoň jednu infekční komplikaci. Infekční komplikace byly méně časté u nemocných, kteří dosáhli remise.
Studie CAM307 srovnávala alemtuzumab s chlorambucilem v první linii léčby CLL u 297 pacientů [7]. CAM307 ukázala, že dosud neléčení pacienti s delecí 17p (p53) mají mnohem lepší léčebné výsledky, dostávají‑li alemtuzumab (CR + PR 64 % u alemtuzumabu vs 20 % u chlorambucilu). PFS byl 10,7 měsíce u skupiny s delecí 17p dostávající alemtuzumab a jen 2,2 měsíce ve skupině s chlorambucilem. Tomuto údaji odpovídají i naše data PFS, což je velmi dobrý výsledek, neboť u našich nemocných nebyl alemtuzumab lékem první linie. Ve studii CAM307 bylo dále dosaženo těchto výsledků CR + PR: skupina s delecí 11q 87 % (medián PFS 8,5 měsíce), skupina s +12 83 % (medián PFS 18,3 měsíce), skupina s normálním karyotypem 84 % (medián PFS 19,9 měsíce), skupina s delecí 13q 91 % (medián PFS 24,4 měsíce). V našem soboru nebyly rozdíly mezi jednotlivými skupinami tak výrazné, nicméně na základě dat studie CAM307 i naší analýzy je možné konstatovat, že alemtuzumab je méně účinný u pacientů s delecí 11q. Jedním z možných vysvětlení této skutečnosti je, že u nemocných s delecí 11q často dominuje výrazná lymfadenopatie a organomegalie, což jsou případy, kdy je alemtuzumeb méně efektivní [18].
Naše studie, podobně jako obdobné retrospektivní zahraniční práce, ukázala, že výsledky léčby (léčebná odpověď i snášenlivost léku) jsou i v „reálném životě“, u neselektované skupiny nemocných, srovnatelné s výsledky studií prospektivních [19,20].
Závěr
Zjistili jsme, že v současné době je alemtuzumab v České republice indikován velmi racionálně (jako léčba 3. linie). Výsledky naší léčby alemtuzumabem jsou při srovnání se zahraničními daty lepší [17] nebo přibližně stejné [7]. Nicméně je také zřejmé, že v monoterapii představuje alemtuzumab pouze paliativní léčbu CLL. Získali jsme prioritní data o efektu alemtuzumabu u jednotlivých cytogenetických podskupin CLL. Za zamyšlenou stojí fakt, že naši pacienti dostali relativně nízkou kumulativní dávku léku.
Touto studií bychom rádi vyzvali všechna pracoviště a lékaře, kteří se s pacienty s CLL setkávají, k diskuzi o indikacích léku, o profylaxi nežádoucích účinků léku a o provedení ještě větší a zevrubnější analýzy.
Doručeno do redakce: 22. 10. 2008
Přijato po recenzi: 21. 1. 2009
doc. MUDr. Michael Doubek, Ph.D.
www.fnbrno.cz
e‑mail: mdoubek@fnbrno.cz
Zdroje
1. Doubek M, Ráčil Z, Mayer J. Klinické využití humanizované monoklonální protilátky alemtuzumab. 1. vyd. Brno: Masarykova univerzita 2006.
2. Dyer MJ. The role of CAMPATH-1H antibodies in the treatment of lymphoid malignancies. Semin Oncol 1999; 26 (5 Suppl 14): S52–S57.
3. Hale G. The CD52 antigen and development of the CAMPATH antibodies. Cytotherapy 2001; 3 : 137–143.
4. Lozanski G, Heerema NA, Flinn IW et al. Alemtuzumab is an effective therapy for chronic lymphocytic leukemia with p53 mutations and deletions. Blood 2004; 103 : 3278–3281.
5. Stilgenbauer S, Döhner H. Campath-1H‑induced complete remission of chronic lymphocytic leukemia despite p53 gene mutation and resistance to chemotherapy. N Engl J Med 2002; 347 : 452–453.
6. Mayer J, Schwarz J, Doubek M et al. Co nám v každodenní praxi skutečně říkají tzv. moderní prognostické faktory u chronické lymfatické leukemie? Transf Hemat Dnes 2007; 13 : 106–116.
7. Hillmen P, Skotnicki AB, Robak T et al. Alemtuzumab compared with chlorambucil as first‑line therapy for chronic lymphocytic leukemia. J Clin Oncol 2007; 25 : 5616–5623.
8. Keating MJ, Coutré S, Rai K et al. Management guidelines for use of alemtuzumab in B-cell chronic lymphocytic leukemia. Clin Lymphoma 2004; 4 : 220–227.
9. Döhner H, Stilgenbauer S, Benner A et al. Genomic aberrations and survival in chronic lymphocytic leukemia. N Engl J Med 2000; 343 : 1910–1916.
10. Hallek M, Cheson BD, Catovsky D et al. Guidelines for the diagnosis and treatment of chronic lymphocytic leukemia: a report from the International Workshop on Chronic Lymphocytic Leukemia updating the National Cancer Institute-Working Group 1996 guidelines. Blood 2008; 111 : 5446–5456.
11. Österborg A, Dyer MJS, Bunjes D et al. Phase II multicenter study of human CD52 antibody in previously treated chronic lymphocytic leukemia. European Study Group of CAMPATH-1H treatment in chronic lymphocytic leukemia. J Clin Oncol 1997; 15 : 1567–1574.
12. Lundin J, Kimby E, Björkholm M et al. hase II trial of subcutaneous anti‑CD52monoclonal antibody alemtuzumab (Campath-1H) as first‑line treatment for patients with B-cell chronic lymphocytic leukemia (B-CLL). Blood 2002; 100 : 768–773.
13. Elter T, Borchmann P, Schulz H et al. Development of a new, four‑weekly schedule (FluCam) with concomitant aplication of Campath-1H and fludarabine in patients with relapsed/refractory CLL. Proc Am Soc Clin Oncol 2003; 22. Abstract 2331.
14. Montillo M, Tedeschi A, Rossi V et al. Alemtuzumab as consolidation after a response to fludarabine is effective to purge residual disease in patients with chronic lymphocytic leukemia. Blood 2004; 104. Abstract 479.
15. Moreton P, Kennedy B, Rawstron A et al. The correlation between the eradication of minimal residual disease (MRD) following alemtuzumab for CLL and overall survival. Proc Am Soc Clin Oncol 2004; 23. Abstract 6566.
16. Stilgenbauer S, Kröber A, Winkler D et al. Efficacy of subcutaneous alemtuzumab (Campath-1H) in genetic high‑risk, fludarabine-refractory CLL: CLL2H study of the German CLL Study Group (GCLLSG). Ann Oncol 2005; 43. Abstrakt 041.
17. Keating MJ, Flinn I, Jain V et al. Therapeutic role of alemtuzumab (Campath-1H) in patients who failed fludarabine: results of a large international study. Blood 2002; 99 : 3554–3561.
18. Dickinson JD, Gilmore J, Iqbal J et al. 11q22.3 deletion in B-chronic lymphocytic leukemia is specifically associated with bulky lymphadenopathy and ZAP-70 expression but not reduced expression of adhesion/cell surface receptor molecules. Leuk Lymphoma 2006; 47 : 231–244.
19. Fiegl M, Falkner A, Hopfinger G et al. Austrian Collaborative Study Group on Alemtuzumab in Chronic Lymphocytic Leukemia. Routine clinical use of alemtuzumab in patients with heavily pretreated B-cell chronic lymphocytic leukemia: a nation-wide retrospective study in Austria. Cancer 2006; 107 : 2408–2416.
20. Hui D, Lam W, Toze C et al. Alemtuzumab in clinical practice: a British Columbia experience. Leuk Lymphoma 2008; 49 : 218–226.
21. National Cancer Institute Common Terminology Criteria for Adverse Events v3.0 (CTCAE). Available from: http://ctep.cancer.gov/forms/CTCAEv3.pdf.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2009 Číslo 6- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Pleiotropní účinky statinů na kardiovaskulární systém
- Index SAMS-CI pro odhad souvislosti myopatií s léčbou statiny
- Metabolit živočišné stravy produkovaný střevní mikroflórou zvyšuje riziko závažných kardiovaskulárních příhod
- Jak podpořit využití železa organismem bez nežádoucích účinků
-
Všetky články tohto čísla
- Využití farmakogenetiky při léčbě warfarinem – editorial
- Dvacet let péče o dospělé nemocné s cystickou fibrózou v České republice
- Alemtuzumab v terapii chronické lymfocytární leukemie: retrospektivní analýza a hodnocení léčebné odpovědi podle cytogenetického rizika
- Je průkaz adenomu nadledviny u pacientů s primárním hyperaldosteronizmem dostatečný pro indikaci adrenalektomie?
- Vztah hormonů tukové tkáně a ghrelinu ke kostnímu metabolizmu
- Využití farmakogenetiky při léčbě warfarinem
- Léčba selhání ledvin u mnohočetného myelomu
- Od diagnostiky celiakie až k možnostiam legislatívnych zmien
- Případ familiární adenomatózní polypózy a návrh systému dispenzarizace
- Lokalizovaná tracheobronchiální amyloidóza typu AA a její odlišení od systémové amyloidózy v praxi
- Vénová tromboembólia u onkologického pacienta
- Ascites u Mulibrey syndromu
- Recenze
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Léčba selhání ledvin u mnohočetného myelomu
- Je průkaz adenomu nadledviny u pacientů s primárním hyperaldosteronizmem dostatečný pro indikaci adrenalektomie?
- Případ familiární adenomatózní polypózy a návrh systému dispenzarizace
- Využití farmakogenetiky při léčbě warfarinem
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy








