Organizace karotického programu a výsledky endovaskulární léčby karotické stenózy ve Vítkovické nemocnici
Results of endovascular treatment and management of carotid stenosis at the Vítkovice Hospital
Internal carotid artery (ICA) stenosis is one of the most common causes of ischaemic stroke. The gold standard in the treatment of ICA stenosis is carotid endarterectomy (CEA), while carotid artery stenting (CAS) is considered as an alternative. Indications for CAS are restenosis after prior CEA, stenosis after radiotherapy, high position of carotid bifurcation, tandem stenosis, contralateral head nerves palsies, ICA dissection or previous neck surgery. CAS safety has been well studied in many trials. In our hospital we have long-term experience with CAS. Particular cases are discussed and the best method for ICA stenosis treatment is chosen by a board composed of a neurologist, vascular surgeon and interventional radiologist. We observe the patients at the neurology department and immediately after CAS, patients are observed at the neuro-intensive care unit for one day. We have our own registry of complications and restenosis cases after CAS, which helps us improve our efforts. Between 2010 and 2014, we implanted 242 stents into ICA. The 30-day overall mortality and morbidity (death, stroke, acute myocardial infarction) was 4.96%, in the asymptomatic ICA stenosis group it was 2.88%, in symptomatic 7.77%. We did not find any in-stent restenosis. We consider well-indicated CAS as a safe alternative to CEA.
Keywords:
carotid stenosis – stents – registries – postoperative complications
Authors:
O. Pavlík 1; D. Kučera 2,3
Authors‘ workplace:
Vzdělávací a výzkumný institut Agel, Neurologické oddělení, Vítkovická nemocnice a. s., Ostrava
1; Vaskulární centrum, Vítkovická nemocnice a. s., Ostrava
2; II. interní klinika kardiologie a angiologie 1. LF UK a VFN v Praze
3
Published in:
Kardiol Rev Int Med 2016, 18(3): 157-162
Overview
Stenóza vnitřní karotické tepny (ACI) je jednou z nejčastějších příčin ischemické cévní mozkové příhody (CMP). V léčbě stenózy ACI dlouhodobě dominuje karotická endarterektomie (CEA), alternativní metodou je karotický stenting (CAS). Indikacemi CAS je restenóza po CEA, postradiační stenóza ACI, vysoko uložená bifurkace, tandemové stenózy, parézy hlavových nervů kontralaterálně, disekce ACI či předchozí operace na krku. Bezpečnost CAS byla ověřena v mnoha studiích. Na našem pracovišti máme dlouhodobé zkušenosti s CAS. Na indikaci k výkonům se podílí komise složená z neurologa, cévního chirurga a endovaskulárního specialisty. Hospitalizace pacientů probíhá na neurologickém oddělení, po výkonu jsou pacienti pozorováni na neurologické jednotce intenzivní péče. Dlouhodobě vedeme vlastní registr komplikací a restenóz po CAS, který nám pomáhá ve zlepšování péče. V letech 2010–2014 jsme zavedli celkem 242 stentů do ACI, celkový výskyt komplikací do 30 dnů od výkonu (úmrtí, CMP, infarkt myokardu) byl 4,96 %, ve skupině asymptomatických stenóz 2,88 %, ve skupině symptomatických stenóz 7,77 %. Významnou restenózu jsme nezachytili ani jednou. Při dobře zvolené indikaci považujeme CAS za bezpečnou alternativu CEA.
Klíčová slova:
karotická stenóza – stent – komplikace – restenózy
Cévní mozková příhoda (CMP) je třetí hlavní příčina mortality a první příčina trvalé invalidity u pacientů v ČR. Mezi hlavní příčiny ischemické CMP patří onemocnění malých tepen (tzv. mikroarteriopatie), onemocnění velkých tepen (makroarteriopatie) a embolizace do mozkových tepen ze srdce [1]. Makroarteriopatie, mezi které se řadí i stenóza vnitřní krkavice (ACI), se podílí na vzniku ischemických CMP dle různých zdrojů v až 50 % [1,2]. Výskyt asymptomatické stenózy ACI v populaci pod 50 let věku se udává 0,1 % u mužů a 0 % u žen, v populaci nad 80 let je to už 3,1 % u mužů a 0,9 % u žen. [3]. U pacientů s CMP lze stenózu ACI najít až v 10 % případů [4].
Zlatým standardem v intervenční léčbě stenózy ACI je karotická endarterektomie (CEA) [5], která se používá v této indikaci již od 50. let minulého století. Alternativní metodou k CEA je karotický stenting (CAS), metoda o tři dekády mladší, jejíž první provedení se připisuje Kerberovi v roce 1980 [6]. Od té doby prošel CAS bouřlivým vývojem, jeho bezpečnost se ověřovala a srovnávala s CEA v mnoha studiích (z těch nejznámějších to jsou studie CAVATAS, CREST, SAPPHIRE, SPACE, EVA-3S, ICSS) a řadí se k nejvíc studovaným medicínským metodám vůbec. Za dobu své existence se CAS etabloval v určitých indikacích jako metoda volby v léčbě karotické stenózy. Mezi tyto indikace patří restenóza a postradiační stenóza ACI, vysoko uložená bifurkace, tandemové stenózy, parézy hlavových nervů kontralaterálně, disekce ACI či předchozí operace na krku [7].
Publikace českých autorů postavení CAS jako alternativní a bezpečné metody v léčbě karotické stenózy potvrzují. Dle Bradáče [7] je CAS vyhrazen pouze pro přísně indikované případy (viz výše) a výsledky z jejich pracoviště, kdy retrospektivně analyzovali 815 případů CEA a 656 případů CAS, jasně favorizují CEA. Dle Kulihy je u CEA významně nižší riziko výskytu nových ischemických lézí na magnetické rezonanci (MR) mozku po výkonu než u CAS [8]. Krajíčková popisuje na souboru 442 pacientů bezpečnost a účinnost CAS u správně indikovaných pacientů [9] stejně jako Lacman na souboru 444 pacientů po CAS ze svého pracoviště [10].
Organizace karotického programu
Pacienti se stenotickým postižením extrakraniálních i intrakraniálních tepen a jejich nálezy na zobrazovacích metodách z různých ambulancí a oddělení ve spádové oblasti Vítkovické nemocnice, Vaskulárního a Iktového centra, jsou konzultováni na neurovaskulárním semináři. Seminář probíhá jednou týdně za účasti neurologa zaměřeného na cerebrovaskulární problematiku, cévního chirurga a endovaskulárního specialisty.
Hlavním přínosem této multidisciplinární diskuze je zvolení optimální metody k řešení stenotického postižení. Samotná indikace k výkonu je obvykle v rukou neurologa, jehož úkolem je zhodnotit klinické nálezy u pacienta v souladu se zobrazovacími metodami a odpovědět na otázku, jestli se jedná o stenózu symptomatickou či asymptomatickou. Indikační kritéria obvykle přejímáme z nejnovějších doporučení American Heart a American Stroke Association [11]. V případě asymptomatických nálezů, které jsou hraniční ve své významnosti, indikuje neurolog další vyšetření, která pomohou lépe charakterizovat významnost stenózy. Mezi tato vyšetření patří nativní vyšetření mozku počítačovou tomografií (CT) či MR, kde pátráme zejména po němých infarktech mozku, dále posouzení perfuze mozku v povodí stenotické tepny pomocí CT perfuze, vyšetření vazoreaktivity mozkových tepen pomocí transkraniálního dopplerovského vyšetření (TCD) a také sonografické vyšetření tepny k posouzení charakteristiky plátu, kdy za rizikové považujeme převážně anechogenní a exulcerované pláty.
Dalším krokem u pacienta, který byl na základě zhodnocení dostupných dat indikován k revaskularizačnímu výkonu, je výběr optimální metody. Zcela zásadní je zhodnocení dostupné obrazové dokumentace (nejčastěji CT angiografie v korelaci se sonografickým vyšetřením tepen, méně často MR angiografie či panangiografie mozkových tepen) a její opětovná analýza se zaměřením na zhodnocení významnosti stenózy zkušenými vaskulárními specialisty a řady dalších parametrů. Mezi ně patří poloha karotické bifurkace a její vztah k úhlu mandibuly, typ plátu, jeho velikost a přítomnost kalcifikací, stav kontralaterálního řečiště a anamnestická data pacienta (restenóza po předchozí operaci, postradiační stenóza, parézy hlavových nervů, operace na krku, významné komorbidity, neurologický status). Na základě shody mezi neurologem, cévním chirurgem a endovaskulárním specialistou je následně vybrána vhodná metoda léčby karotického postižení.
Karotický stenting
Pacient je na výkon připraven duální antiagregační léčbou – kyselina acetylsalicylová v dávce 100 mg a klopidogrel v dávce 75 mg na den. K výkonu pacient přichází nalačno. Některá pracoviště z obavy protrahované vazovagální reakce vysazují ranní antihypertenzní a bradykardizující medikaci. Vzhledem k velkému procentu pacientů s prognosticky významnou kardiální anamnézou podstupující CAS vysazení těchto látek na našem pracovišti nedoporučujeme, a to jednak pro nebezpečí rozvoje akutního srdečního selhání při nekontrolované hypertenzi a jednak pro vznik refrakterní anginy pectoris a infarktu myokardu (IM) při vysazení betablokátoru a nitrátů. Nezanedbatelné je taktéž nebezpečí vzniku mozkového krvácení při obnovení toku krve do oblasti mozkové cirkulace s vyčerpanou vazoreaktivitou na podkladě těsné stenózy krkavice s absencí kolaterálního toku z druhostranného karotického povodí či vertebro-bazilární cirkulace.
Nejčastějším přístupovým místem do cévního řečiště je společná femorální tepna, méně častým přístupem je radiální či brachiální tepna či přímý přístup přes společnou karotidu. Výkon je prováděn v lokální anestezii a periprocedurálně se k zabránění trombotických komplikací jak v místě přístupu, tak v místě implantace stentu aplikuje 100 j/kg váhy nefrakcionovaného heparinu i.v. či i.a. Vlastní výkon na karotické tepně začíná kontrolní karotickou angiografií se znázorněním nejen místa stenotizace vnitřní krkavice, ale i odpovídající mozkové cirkulace z důvodu detekce možné periferní embolizace, která může doprovázet implantaci stentu. Následně se pod oblast stenózy zavede z třísla dlouhý zavaděč (sheath) nebo preformovaný vodicí katetr (guiding katetr), přes které se vlastní výkon provádí.
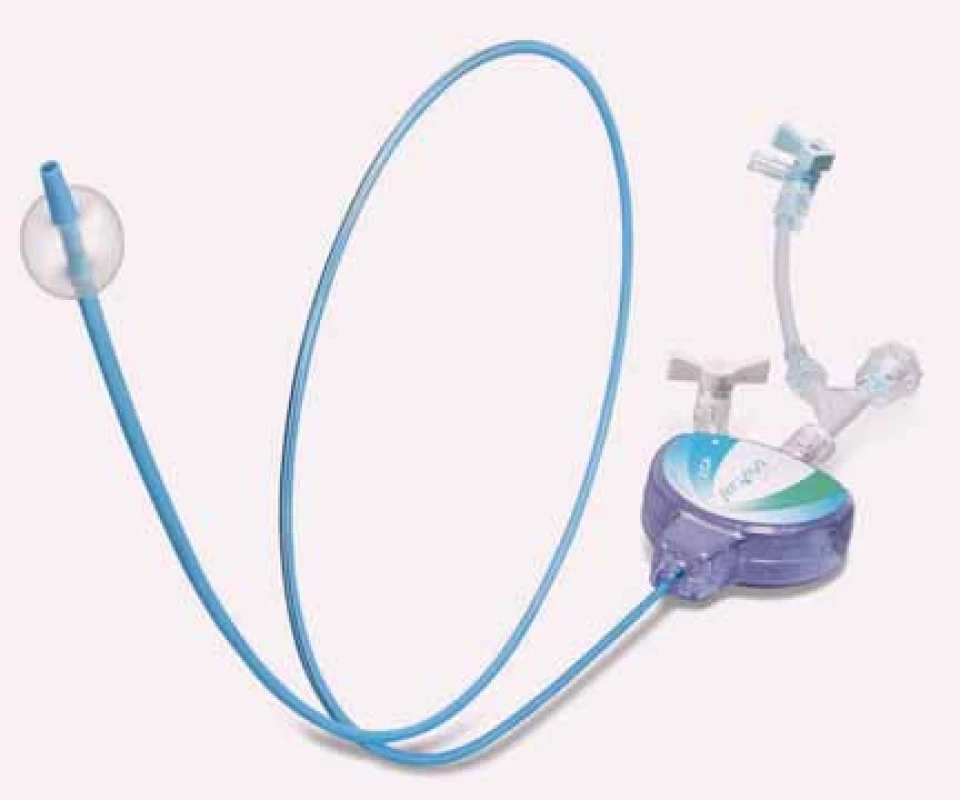
Po zavedení sheathu se zavede do místa intervence mozková protekce, která brání mozkové embolizaci během vlastního výkonu. Nejčastějším typem protekce je nitinolový košíček umístěný na ultratenkém vodiči, který zachovává tok krve v oblasti krkavice během výkonu (obr. 1, 2). Výhodami tohoto typu protekce jsou jednoduchá manipulace a dobrá tolerance pacientem. Nevýhodou je nemožnost proniknout přes těsnou, kalcifikovanou stenózu a v některých případech nedostatečné doléhání košíčku ke stěně tepny s možností periferní embolizace. Odlišným způsobem protekce je systém založený na otočení toku krve ve vnitřní krkavici uzavřením toku v oblasti společné a zevní krkavice balonky, které velmi účinně brání periferní embolizaci, ale které nemusí být tolerovány především pacienty s kontralaterální okluzí krkavice (obr. 3). Další nevýhodou je technicky složitější manipulace se systémem, která je však vykompenzována účinnější mozkovou protekcí především u symptomatických stenóz.


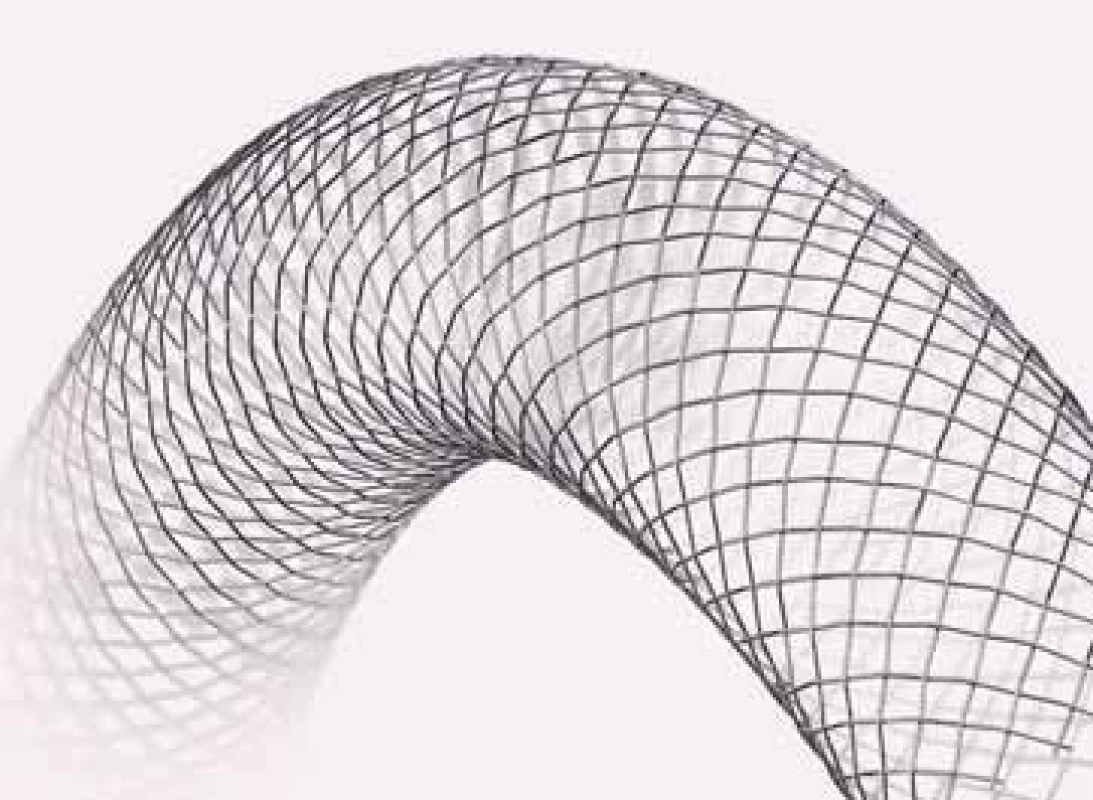
Stejně jako si můžeme vybrat pro pacienta nejvhodnější systém protekce, můžeme si vybrat i z různých druhů stentů, které mají odlišné charakteristiky i vlastnosti. Tak jako v periferním cévním řečišti jsou i v karotickém povodí postupně vytlačovány stenty z ušlechtilé ocele stenty nitinolovými, které mají lepší fyzikální i mechanické vlastnosti, a to především radiální sílu (odolnost vůči tlaku zvenčí) a schopnost samovolně se v čase rozpínat na rozměr udaný výrobcem. Zásadním konstrukčním prvkem, který ovlivňuje dobré pokrytí aterosklerotického plátu stentem, je jejich technické řešení charakteru otevřených (obr. 4) či uzavřených (obr. 5) buněk, které taktéž významně ovlivňuje jejich fyzikální vlastnosti. Kombinací je tzv. hybridní stent, kde se na krajích stentu nacházejí otevřené buňky a uprostřed, v místě, které by mělo naléhat přímo na sklerotický plát, se nalézají buňky uzavřené (obr. 6). Konstrukční vlastnosti zásadním způsobem ovlivňují nejen chování stentu v cévě, ale i kvalitu pokrytí aterosklerotického plátu, a tím i nebezpečí periprocedurální či odložené periferní embolizace po implantaci stentu. Ve své podstatě otevřené buňky umožňují větší ohebnost stentu, ale hůře pokrývají aterosklerotický plát a implantují se především do vinutých, stabilních, asymptomatických lézí, zatímco uzavřené buňky vedou k větší rigiditě stentu, ale lépe pokrývají sklerotický plát, takže se implantují především do stenóz symptomatických, nestabilních, v rovnějších úsecích cév. Hybridní řešení stentu je dobrým kompromisem spojujícím především výhody konstrukčního řešení otevřených a uzavřených buněk.


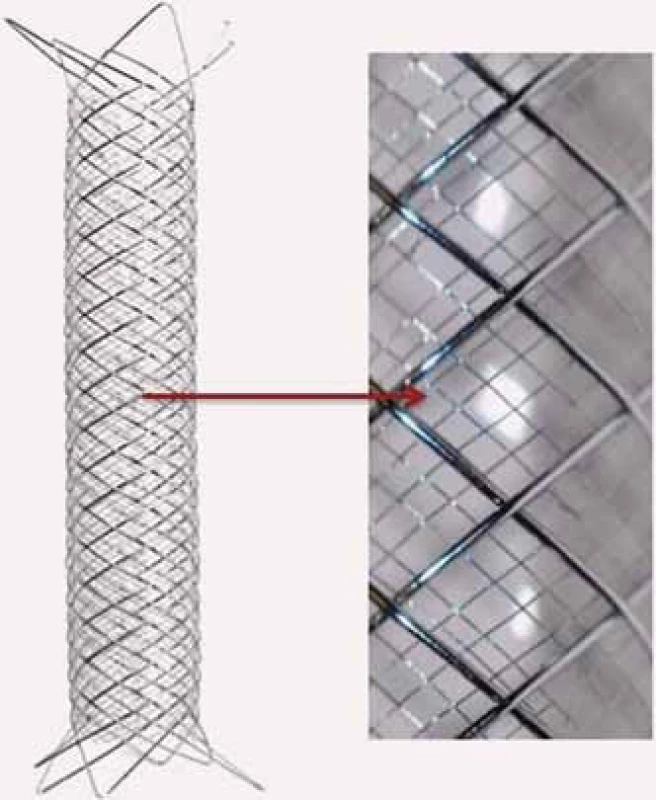
Úplně novým typem stentu, který by mohl podstatně zlepšit klinické výsledky CAS, je tzv. Double Layer Mesh Stent Technology (obr. 7), což je kombinace nitinolového samoexpandibilního stentu, který je směrem zvnitřku cévy pokryt hustou nitinolovou sítí, čímž se dociluje optimálního pokrytí aterosklerotického plátu se zabráněním prolapsu plátu skrz oka stentu a periferní embolizaci. Je zřejmé, že na základě anatomických charakteristik přístupového řečiště a karotického postižení (obr. 8, 9) musíme pro každého pacienta naplánovat optimální strategii výkonu, typ karotické protekce i typ užitého stentu, čímž můžeme docílit podstatně lepších výsledků CAS.
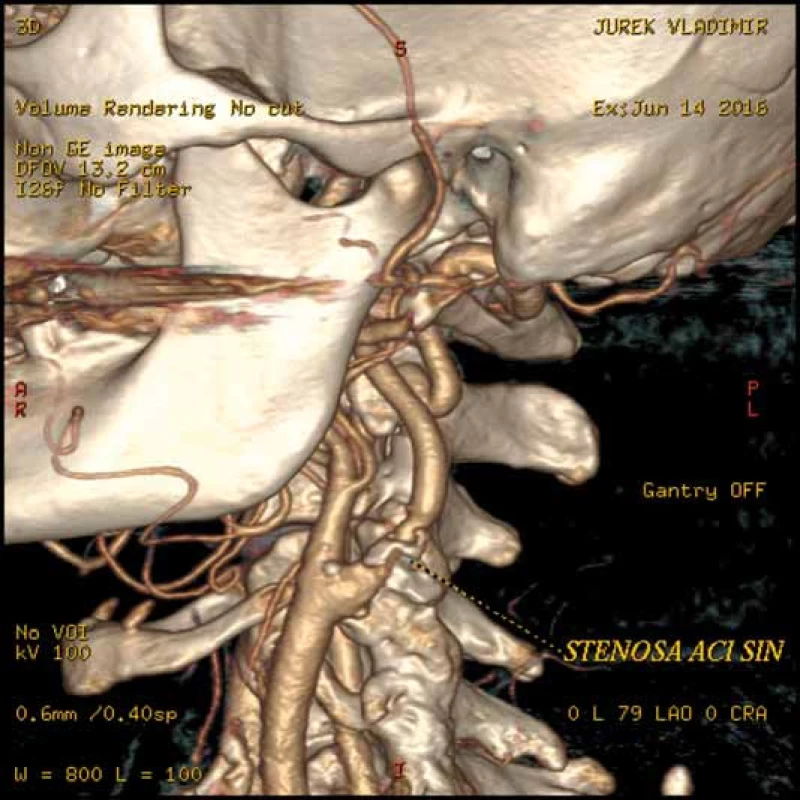
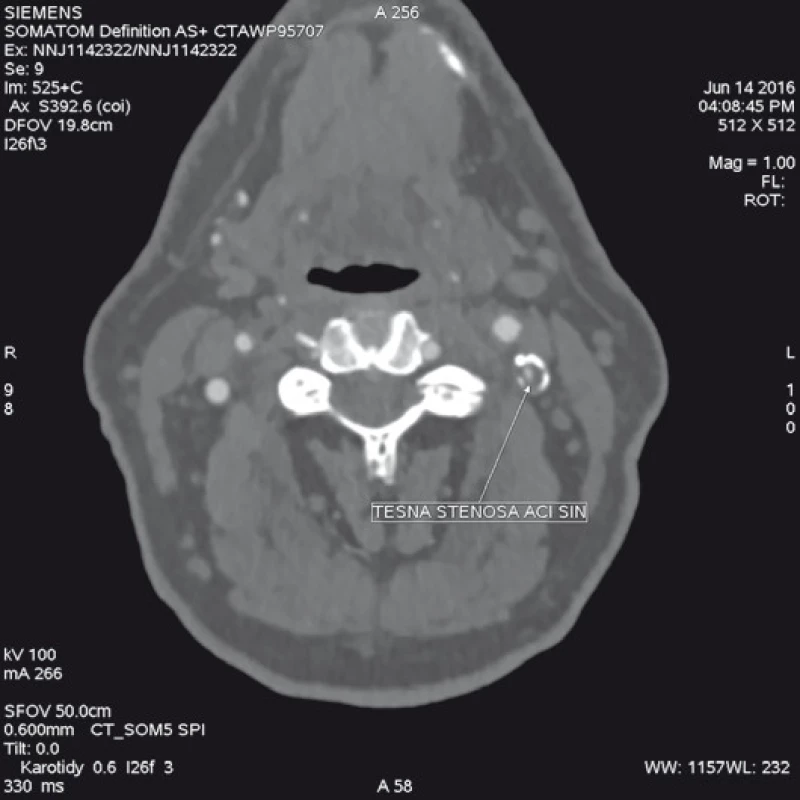
Po zavedení námi zvolené karotické protekce (obr. 10, 11) je implantován do místa postižení stent, a to buď bez predilatace stenózy, což je postup preferovaný většinou pracovišť, anebo při těsné, kalcifikované stenóze se léze nejprve predilatuje a následně implantuje stent. Před dodilatací stentu na optimální referenční průměr (obr. 12) aplikujeme 0,5 mg atropinu i.v. jako prevenci možné vazovagální reakce. Výkon ukončujeme stažením protekce a kontrolní angiografií jak oblasti implantovaného stentu (obr. 13), tak odpovídající intrakraniální cirkulace k vyloučení mozkové embolizace v průběhu výkonu.
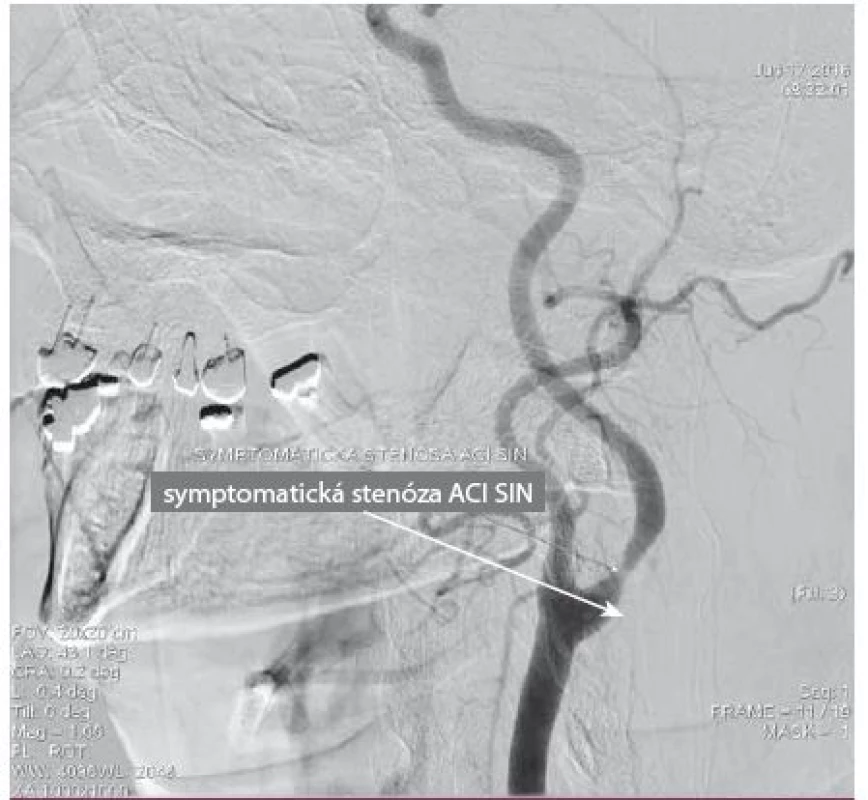
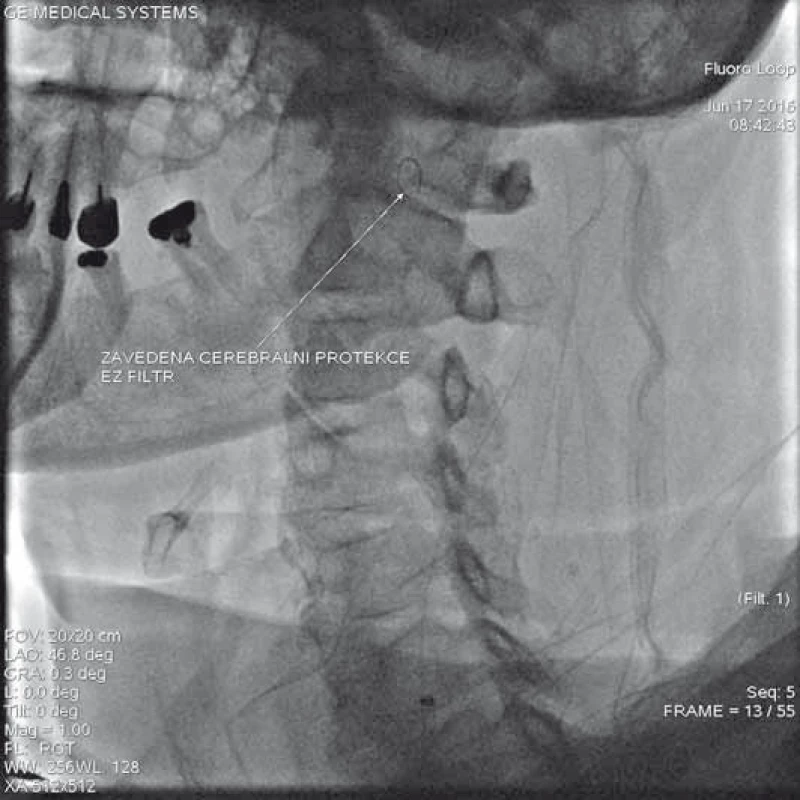
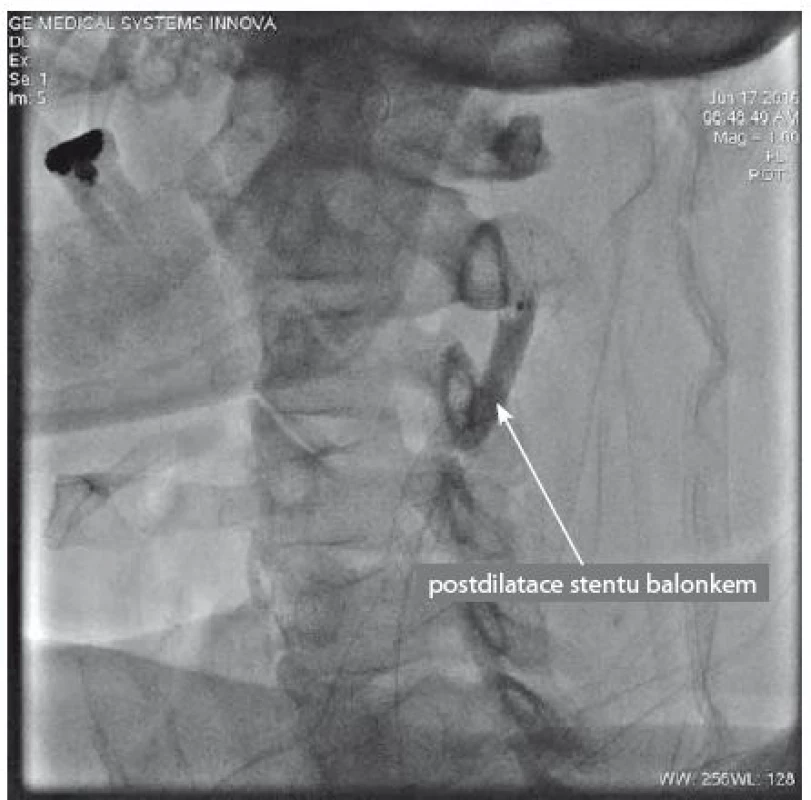
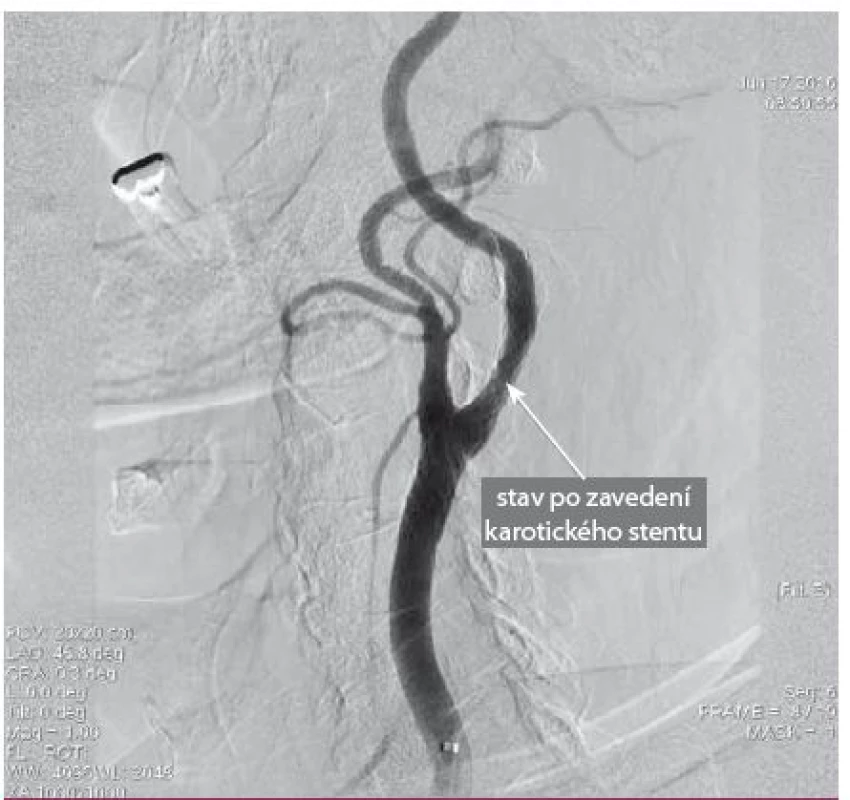
Za zásadně nevhodné anatomické indikace k CAS považujeme především masivně kalcifikované stenózy karotid, kde hrozí riziko, že stenózu po implantaci stentu nebudeme moci roztáhnout na odpovídající průměr cévy, a extrémně vinuté karotické řečiště s nemožností zavedení mozkové protekce či stentu a s rizikem zalomení stentu po implantaci. Z klinických indikací je poté absolutní kontraindikací alergie na kontrastní látku s rozvojem anafylaktického šoku a nespolupráce pacienta při výkonu.
Organizace péče o pacienta
Pacienti jsou před výkonem i po výkonu hospitalizováni na neurologickém oddělení zejména z důvodu výskytu komplikací, které jsou nejčastěji neurologické povahy. Ihned po výkonu je pacient pozorován na neurologické jednotce intenzivní péče, nejčastěji do druhého dne. Mezi nejzávažnější komplikace patří nově vzniklý neurologický deficit, který může mít několik příčin. Nejčastěji se jedná o embolizaci do mozkových tepen během výkonu, vzácněji o intracerebrální hemoragii v rámci hyperperfuzního syndromu, trombózu ve stentu, disekci, rupturu či spazmus tepny [1]. V poslední době jsme zaznamenali i třikrát status epilepticus v návaznosti na revaskularizační výkon. Z extracerebrálních komplikací je nejzávažnější pokles krevního tlaku (TK) po výkonu, který je v nejtěžších případech nutno řešit i farmakologicky. Pokles TK po výkonu snižuje perfuzi mozkových tepen a schopnost vymýt emboly z mozkového řečiště a podílí se na zvýšeném výskytu nových ischemických lézí mozku po CAS [12], které nicméně zůstávají ve většině případů asymptomatické [13]. Do 48 hod po výkonu provádíme sonografické vyšetření implantovaného stentu a cerebrálního řečiště. Pacienta obvykle druhý pooperační den propouštíme do domácí péče.
Kontrolní neurologické vyšetření, kontrolní sonografické vyšetření stentu a extrakraniálního řečiště provádíme přibližně měsíc po výkonu a dále v 6–12měsíčních intervalech. Do první kontroly pacienta ponecháváme na kombinované antiagregaci, poté doživotně na prosté antiagregaci.
Registr karotid a výsledky endovaskulární léčby
Pravidelné sledování klinického stavu pacienta a sonografický nález na tepnách je podkladem pro registr karotických intervencí naší nemocnice, který dlouhodobě vedeme. Společně s pacienty po CAS sledujeme i pacienty, kteří podstoupili CEA.
Registr je výsledkem retrospektivního sběru dat a jeho každoroční analýzy. Klasifikace sledovaných komplikací po revaskularizačních výkonech obecně není standardizovaná a je v různých studiích koncipována jinak. V našem registru jsou hlavní sledované parametry výskyt nové CMP jakéhokoli typu, akutního IM a úmrtí pacienta z jakékoli příčiny (major adverse cardiac and cerebrovascular event – MACCE), nicméně sledujeme např. i výskyt tranzitorní ischemické ataky (TIA) periprocedurálně. Úmrtí pacienta do 30 dnů v souvislosti s akutní CMP vzniklou po výkonu chápeme jako jednu komplikaci. Pacienti také podstupují pravidelné sonografické kontroly ke sledování počtu restenóz.
V letech 2010–2014 jsme v naší nemocnici plánovaně zavedli celkem 242 stentů do ACI. Z indikace symptomatické stenózy ACI bylo provedeno 103 výkonů, 139 z indikace asymptomatické stenózy.
Celkový výskyt komplikací do 30 dnů od výkonu v našem uvedeném souboru je 4,96 % (tab. 1). Zaznamenali jsme úmrtí dvou pacientů do 30 dnů od výkonu, jednou v souvislosti s fatální intracerebrální hemoragií po CAS, druhý pacient zemřel na kardiální selhání při tachyarytmii. Výskyt CMP po výkonu jsme zaznamenali u devíti pacientů, z toho se jednalo o pět tzv. minor stroke (odeznění neurologického deficitu do 30 dnů) a čtyři případy major stroke (neurologický deficit přetrvává více než 30 dnů). TIA jsme zaznamenali celkem v šesti případech (2,48 %), vždy se ale jednalo o přechodný neurologický deficit periprocedurálně s krátkým nebo žádným postprocedurálním trváním, žádná TIA nebyla zachycena více než 24 hod po výkonu.
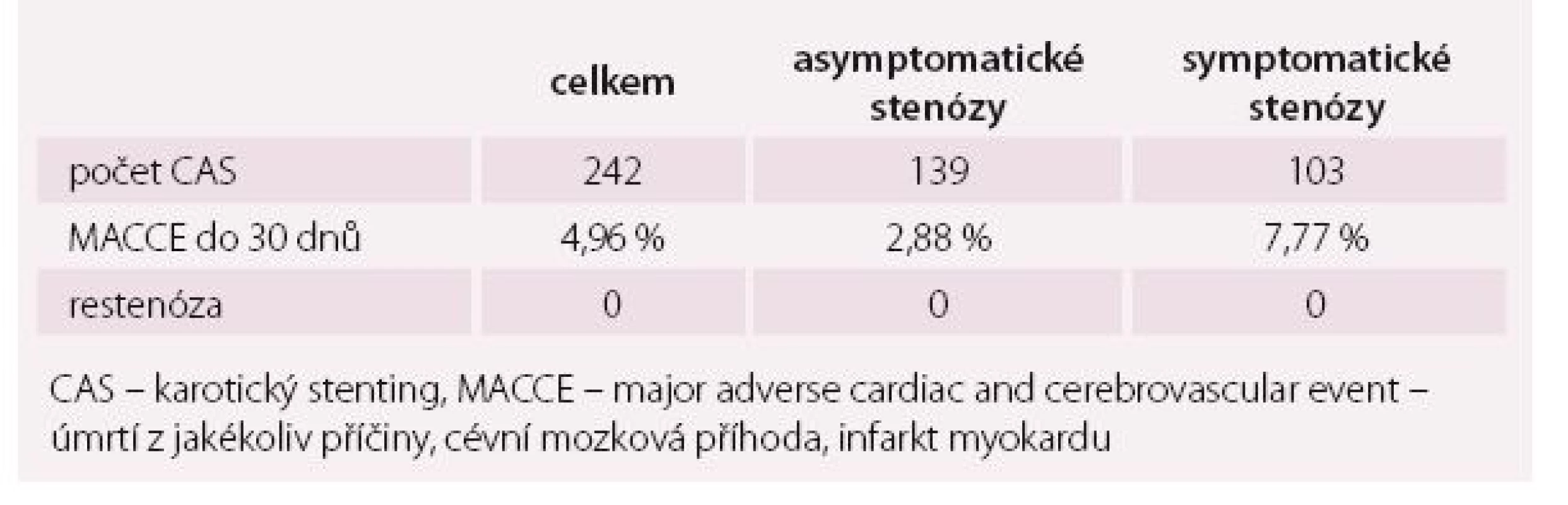
Ve skupině asymptomatických stenóz (n = 139) jsme zaznamenali celkově 2,88 % sledovaných komplikací do 30 dnů od výkonu, z toho dvě ischemické CMP (1× minor stroke, 1× major stroke), 1× fatální intracerebrální hemoragii, 2× akutní IM. Výskyt TIA byl 2,88 %.
Ve skupině symptomatických stenóz (n = 103) jsme zaznamenali celkově 7,77 % sledovaných komplikací do 30 dnů od výkonu, z toho jedno úmrtí pacienta na srdeční selhání u tachyfibrilace, jeden akutní IM a šest ischemických CMP (4× minor stroke, 2× major stroke). Výskyt TIA byl 1,94 % (tab. 2).
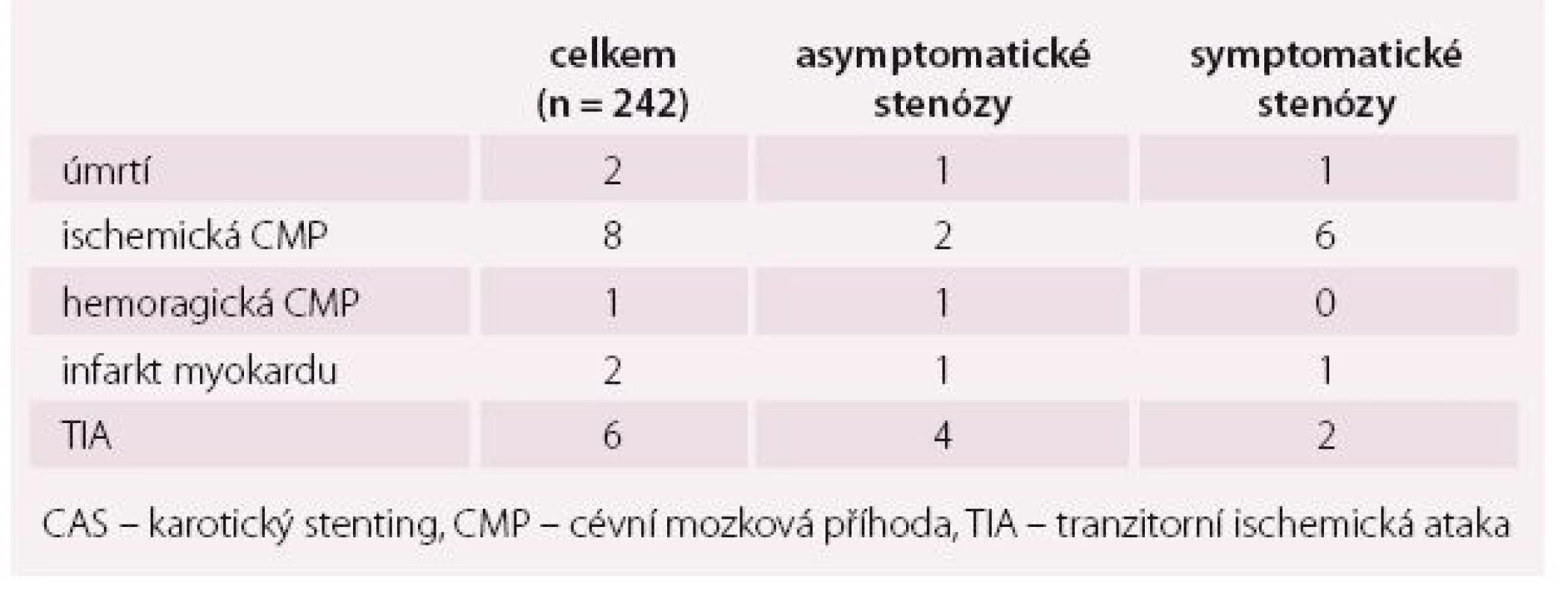
Pacienty po CAS se snažíme i nadále dispenzarizovat a provádět i dlouhodobé sledování. U celkem 170 pacientů z uvedeného souboru jsme po roce či více zaznamenali sonografické vyšetření karotických tepen bez jediné významné restenózy ve stentu, tj. restenóza > 70 %.
U 184 pacientů máme zdokumentovaný zdravotní stav jeden rok či více po výkonu z pravidelných kontrol či záznamů v dokumentaci. Ze sledovaných parametrů jsme nezaznamenali žádnou ze sledovaných komplikací v rozsahu jeden měsíc až přibližně jeden rok po výkonu. Všechny komplikace, které byly výše uvedeny, proběhly do 30 dnů od CAS.
Nashromážděná data v registru každoročně analyzujeme. Významné případy komplikací po výkonu jsou přezkoumány, vč. správné indikace a technického provedení CAS. Takto získané informace nám slouží k dalšímu upřesňování indikačních kritérií, zlepšování managementu péče o pacienty před výkonem i po výkonu a volbě doplňkových vyšetření k vytipování komplikovaných pacientů ještě před výkonem.
Závěr
Karotický stenting je zavedenou a bezpečnou alternativou ke karotické endarterektomii. V centrech s vysokým objemem pacientů lze dosáhnout dobrých výsledků v efektu CAS, minimalizaci komplikací po výkonu a výskytu restenóz. Indikace k výkonu by však měla být pacientovi ušita na míru na základě mezioborové shody.
Doručeno do redakce: 1. 8. 2016
Přijato po recenzi: 12. 8. 2016
MUDr. Ondřej Pavlík
nemocnicevitkovice.agel.cz
ondrej.pavlik@vtn.agel.cz
Sources
1. Bednařík J, Ambler Z, Růžička E et al. Klinická neurologie. 1. vyd. Praha: Triton 2010.
2. Kalina M. Cévní mozková příhoda v medicínské praxi. 1. vyd. Praha: Triton 2008.
3. de Weerd M, Greving JP, Hedblad B et al. Prevalence of asymptomatic carotid artery stenosis in the general population: an individual participant data meta-analysis. Stroke 2010; 41 : 1294–1297. doi: 10.1161/STROKEAHA.110.581058.
4. Lojík M, Krajíčková D, Krajina A. Stenózy karotických tepen – endovaskulární léčba. Postgrad Med 2008; 2 : 143–147.
5. Liistro F, Di Mario C. Carotid artery stenting. Heart 2003; 89 : 944–948. doi: 10.1136/heart.89.8.944.
6. Stankovic G, Liistro F, Moshiri S et al. Carotid artery stenting in the first 100 consecutive patients: results and follow-up. Heart 2002; 88 : 381–386. doi: 10.1136/heart.88.4.381.
7. Bradáč O, Mohapl M, Kramář F et al. Carotid endarterectomy and carotid artery stenting: changing paradigm during 10 years in a high-volume centre. Acta Neurochirurgica 2014; 156 : 1705–1712. doi: 10.1007/s00701-014-2166-x.
8. Kuliha, M, Roubec, M, Procházka V et al. Randomized clinical trial comparing neurological outcomes after carotid endarterectomy or stenting. Br J Surg 2015; 102 : 194–201. doi: 10.1002/bjs. 9677.
9. Krajíčková D, Krajina A, Lojík M et al. Periprocedurální komplikace a dlouhodobý efekt karotických angioplastik – výsledky z praxe. Cesk Slov Neurol N 2016; 79/112 : 317–322.
10. Lacman J, Charvát F, Mašková J et al. Léčba aterosklerotických stenóz bifurkace karotických tepen: sedmileté zkušenosti z jednoho pracoviště. Ces Radiol 2009; 63 : 113–121.
11. Brott TG, Halperin JL, Abbara S et al. 2011 ASA/ACCF/AHA/AANN/AANS/ACR/ASNR/CNS/SAIP/SCAI/ /SIR/SNIS/SVM/SVS guideline on the management of patients with extracranial carotid and vertebral artery disease: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines, and the American Stroke Association, American Association of Neuroscience Nurses, American Association of Neurological Surgeons, American College of Radiology, American Society of Neuroradiology, Congress of Neurological Surgeons, Society of Atherosclerosis Imaging and Prevention, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of NeuroInterventional Surgery, Society for Vascular Medicine, and Society for Vascular Surgery. Circulation 2011; 124 : 54–130. doi: 10.1161/CIR.0b013e31820d8c98.
12. Altinbas A, Algra A, Bonati LH et al. Periprocedural hemodynamic depression is associated with a higher number of new ischemic brain lesions after stenting in the International Carotid Stenting Study – MRI substudy. Stroke 2013; 45 : 146–151. doi: 10.1161/STROKEAHA.113.003397.
13. Bijuklic K, Wandler A, Tübler T et al. Impact of asymptomatic cerebral lesions in diffusion-weighted magnetic resonance imaging after carotid artery stenting. JACC Cardiovasc Interv 2013; 6 : 394–398. doi: 10.1016/j.jcin.2012.10.019.
Labels
Paediatric cardiology Internal medicine Cardiac surgery CardiologyArticle was published in
Cardiology Review

2016 Issue 3
-
All articles in this issue
- Komplexní endovaskulární revaskularizace aterotrombotického uzávěru popliteální tepny a bércových tepen u polymorbidního pacienta – kazuistika
- Endovaskulární léčba ileofemorální hluboké žilní trombózy
- Betablokátory, které nejméně negativně ovlivňují kardiorespirační zdatnost u zdravých osob
- Projekt MedPed – pacienti s familiární hypercholesterolemií ve středu pozornosti
- Význam periprocedurálního poklesu tlakového gradientu ve výtokovém traktu levé komory po alkoholové septální ablaci u pacientů s hypertrofickou obstrukční kardiomyopatií
- Endovaskulární léčba ischemické cévní mozkové příhody
- Organizace karotického programu a výsledky endovaskulární léčby karotické stenózy ve Vítkovické nemocnici
- Endovaskulární léčba disekce aorty typ B a ischemických komplikací provázejících aortální disekce
- Disekce aorty typu B s těžkou viscerální a končetinovou ischemií řešená kompletní endovaskulární revaskularizací – kazuistika
- Možnosti endovaskulární léčby akutní končetinové ischemie
- Organizace podiatrické péče u pacientů s kritickou končetinovou ischemií
- Cardiology Review
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Betablokátory, které nejméně negativně ovlivňují kardiorespirační zdatnost u zdravých osob
- Endovaskulární léčba ileofemorální hluboké žilní trombózy
- Možnosti endovaskulární léčby akutní končetinové ischemie
- Disekce aorty typu B s těžkou viscerální a končetinovou ischemií řešená kompletní endovaskulární revaskularizací – kazuistika
