Výsledky terapie metastatického renálního karcinomu lékem everolimus – analýza údajů z klinického registru RENIS
Metastatic Renal Cell Carcinoma Treated with Everolimus – Data from the RENIS Clinical Registry
Everolimus is an oral mTOR kinase inhibitor approved for the treatment of patients with metastatic renal cell carcinoma (mRCC) progressing during or after treatment with vascular endothelial growth factor (VEGF)-targeted agents. Using the national RENIS clinical registry, we have retrospectively analysed outcomes of patients treated for mRCC with everolimus. A total of 78 patients were evaluable. Median progression-free survival from the start of everolimus therapy was 7 months (95% confidence interval 2–12 months). Partial response or stable disease was achieved in 69% of patients. Treatment toxicity was predictable and serious adverse events occurred in only 6% of patients the most common being respiratory toxicity. Everolimus therapy provides significant clinical benefit for heavily pretreated mRCC patients after failure of VEGF-targeted therapy
Key words:
everolimus – renal cell carcinoma – therapy
The team of autors declares a support of Novartis.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Submitted:
14. 6. 2011
Accepted:
18. 7. 2011
Authors:
T. Büchler 1; L. Dušek 2; J. Fínek 3; A. Poprach 4; D. Budňáková 2; V. Kandrnal 2; Jiří Jarkovský 2
; Z. Bortlíček 2; D. Klimeš 2; J. Abrahámová 1; R. Vyzula 4
Authors‘ workplace:
Onkologické oddělení, Fakultní Thomayerova nemocnice a 1. lékařská fakulta Univerzity Karlovy, Praha
1; Institut biostatistiky a analýz, Lékařská a Přírodovědecká fakulta Masarykovy univerzity, Brno
2; Radioterapeutické a onkologické oddělení, Fakultní nemocnice Plzeň
3; Klinika komplexní onkologické péče, Masarykův onkologický ústav, Brno
4
Published in:
Klin Onkol 2011; 24(5): 389-392
Category:
Reports from Clinical Registries
Overview
Everolimus je perorální inhibitor kinázy mTOR indikovaný k léčbě metastatického renálního karcinomu (mRCC) s progresí během terapie cílené na vaskulární endoteliální růstový faktor (VEGF) nebo po ní. Cílem naší práce bylo retrospektivně zhodnotit výsledky terapie lékem everolimus v České republice podle údajů z klinického registru RENIS. Nalezli jsme hodnotitelné údaje o 78 pacientech. Medián přežití bez progrese od zahájení terapie everolimem byl 7 měsíců (95% interval spolehlivosti 2–12 měsíců). Parciální remise nebo stabilizace onemocnění dosáhlo 69 % pacientů. Toxicita terapie byla predikovatelná a závažné nežádoucí účinky se vyskytly jen u 6 % nemocných, nejčastěji šlo o pneumotoxicitu. Léčbou everolimem lze tedy dosáhnout významného klinického prospěchu v populaci těžce předléčených pacientů s mRCC po selhání terapie cílené na VEGF.
Klíčová slova:
everolimus – renální karcinom – terapie
Úvod
V terapii metastatického renálního karcinomu (mRCC) bylo v posledních pěti letech dosaženo významného pokroku. U nádoru dříve považovaného za rezistentní vůči systémové léčbě byla prokázána účinnost řady cílených léků zaměřených na ovlivnění metabolických kaskád spojených zejména s vaskulárním endoteliálním růstovým faktorem (VEGF) a centrální regulační molekulou mTOR (mammalian target of rapamycin).
Everolimus je perorálním inhibitorem kinázy mTOR s antiangiogenními a antiproliferačními účinky. V randomizované studii RECORD-1 byla prokázána jeho účinnost a bezpečnost v léčbě mRCC s progresí na sunitinibu, sorafenibu či sekvenci těchto tyrozinkinázových inhibitorů (TKI) [1]. V současnosti je everolimus jediným lékem s prokázaným účinkem v této indikaci. V Evropské unii byl everolimus (Afinitor, Novartis) zaregistrován pro léčbu mRCC v roce 2009 [2] a rozhodnutí o jeho úhradě z veřejného zdravotního pojištění v České republice platí od podzimu 2010.
Cílem naší práce je poskytnout přehled o dosavadních výsledcích terapie everolimem a srovnat výsledky dosahované v České republice s výsledky registrační studie RECORD-1.
Pacienti a metody
Pacienti s mRCC byli léčeni everolimem v 13 komplexních onkologických centrech. Údaje o jejich základních charakteristikách, průběhu a výsledcích terapie byly získány z klinické databáze RENIS a hodnoceny retrospektivně. Uzávěrka dat byla 10. 4. 2011.
Everolimus byl podáván v dávce 10 mg denně (s možností redukce dávky na 5 mg denně) do progrese nebo limitující toxicity. Restaging byl prováděn dle zvyklostí jednotlivých pracovišť, obvykle však jednou za 3 měsíce nebo při klinických známkách progrese. Léčebná odpověď byla hodnocena standardně podle systému RECIST. Přežití bez progrese (PFS) a celkové přežití (OS) pacientů léčených everolimem bylo odhadováno podle Kaplan-Meierova modelu. V popisu základních charakteristik souboru pacientů a toxicity bylo využito sumární statistiky.
Výsledky
Základní charakteristiky pacientů
V registru RENIS byly k datu analýzy údaje o 1 331 pacientech léčených cílenými léky pro mRCC, z toho 78 pacientů bylo léčeno everolimem. Základní charakteristiky pacientů jsou shrnuty v tab. 1. Všichni pacienti byli předléčeni sorafenibem, sunitinibem nebo oběma léky. U 65/78 (83 %) byla důvodem k ukončení terapie TKI progrese.
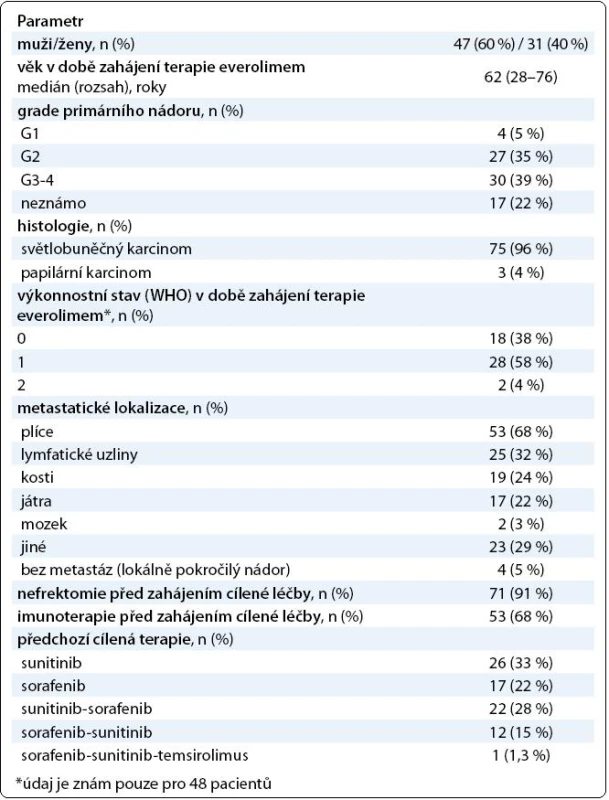
Průběh terapie a nežádoucí účinky
Počáteční dávka everolimu byla 10 mg u 73 pacientů (94 %) a 5 mg u 5 pacientů (6 %). U 4 pacientů (5 %) byla dávka léku během terapie snížena z 10 mg na 5 mg denně pro nežádoucí účinky. K datu analýzy ukončilo terapii 28/78 pacientů (36 %), z toho 21 (75 %) pro progresi. U 3 pacientů (11 %) byla terapie ukončena pro nežádoucí účinek, u 1 pacienta (4 %) na přání pacienta a u 2 pacientů (7 %) pro těžkou infekci. V jednom případě nebyl důvod ukončení terapie uveden. Medián doby léčby u 28 nemocných s ukončenou terapií byl 2,8 měsíce (rozsah 1–13 měsíců). K datu analýzy žije 66 pacientů (85 %), 10 nemocných (13 %) zemřelo a o osudu 2 pacientů nebyly známé další informace. Výskyt nežádoucích účinků shrnuje tab. 2. Celkem bylo zaznamenáno 23 nežádoucích příhod u 14 pacientů (18 %), z toho 6 nežádoucích příhod u 5 pacientů (6 %) bylo hodnoceno jako závažné.
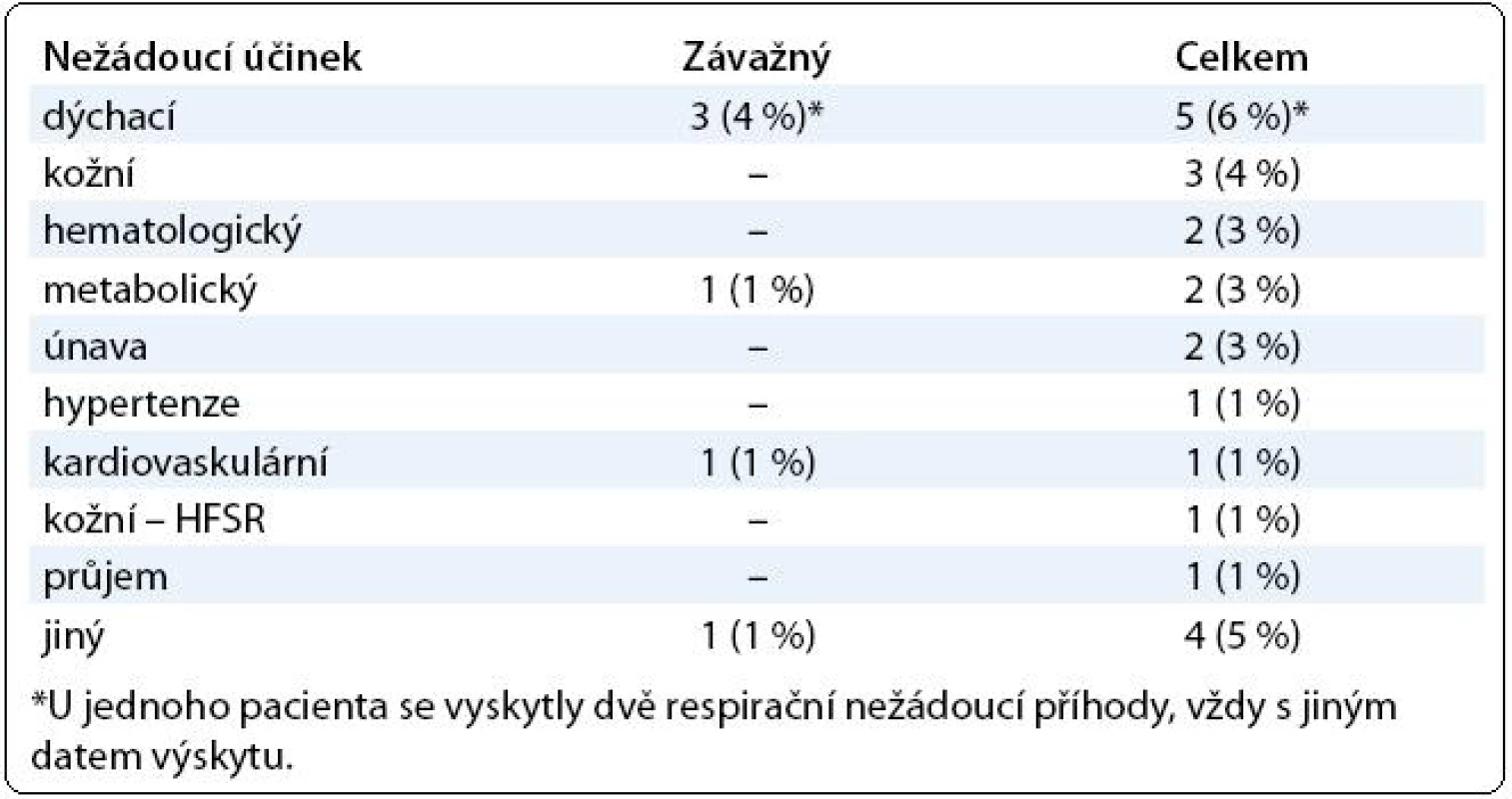
Výsledky terapie
Přehled výsledků terapie je uveden v tab. 3, na obr. 1 jsou zobrazeny křivky pro OS (a) a PFS (b). Podle očekávání nebylo dosaženo kompletních remisí. Prospěch z léčby (tj. procento CR + PR + SD) mělo 69 % nemocných léčených everolimem. V jednom roce od zahájení terapie everolimem přežívalo bez progrese 27 % pacientů (95% IS 9–46 %) a celkem přežívalo 78 % nemocných (95% IS 60–95 %).
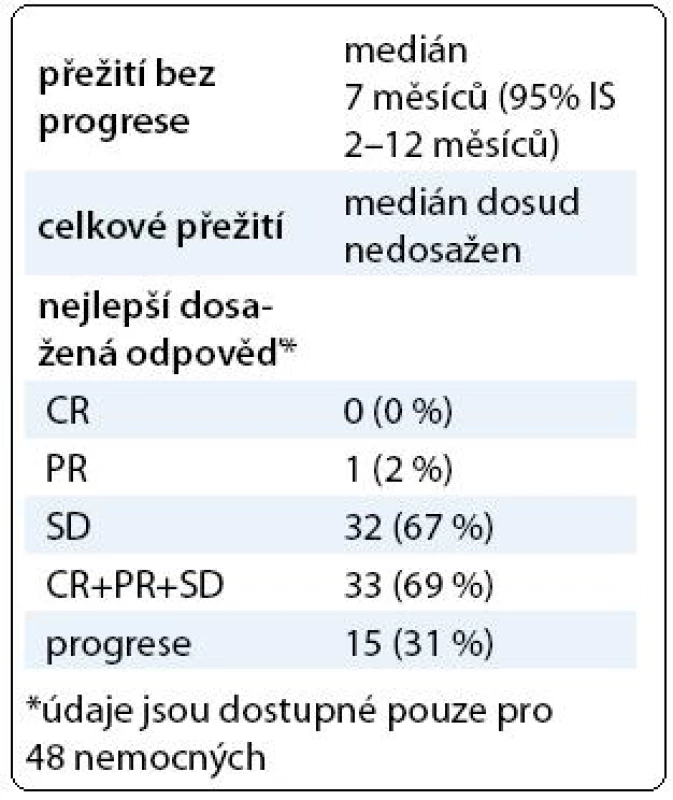
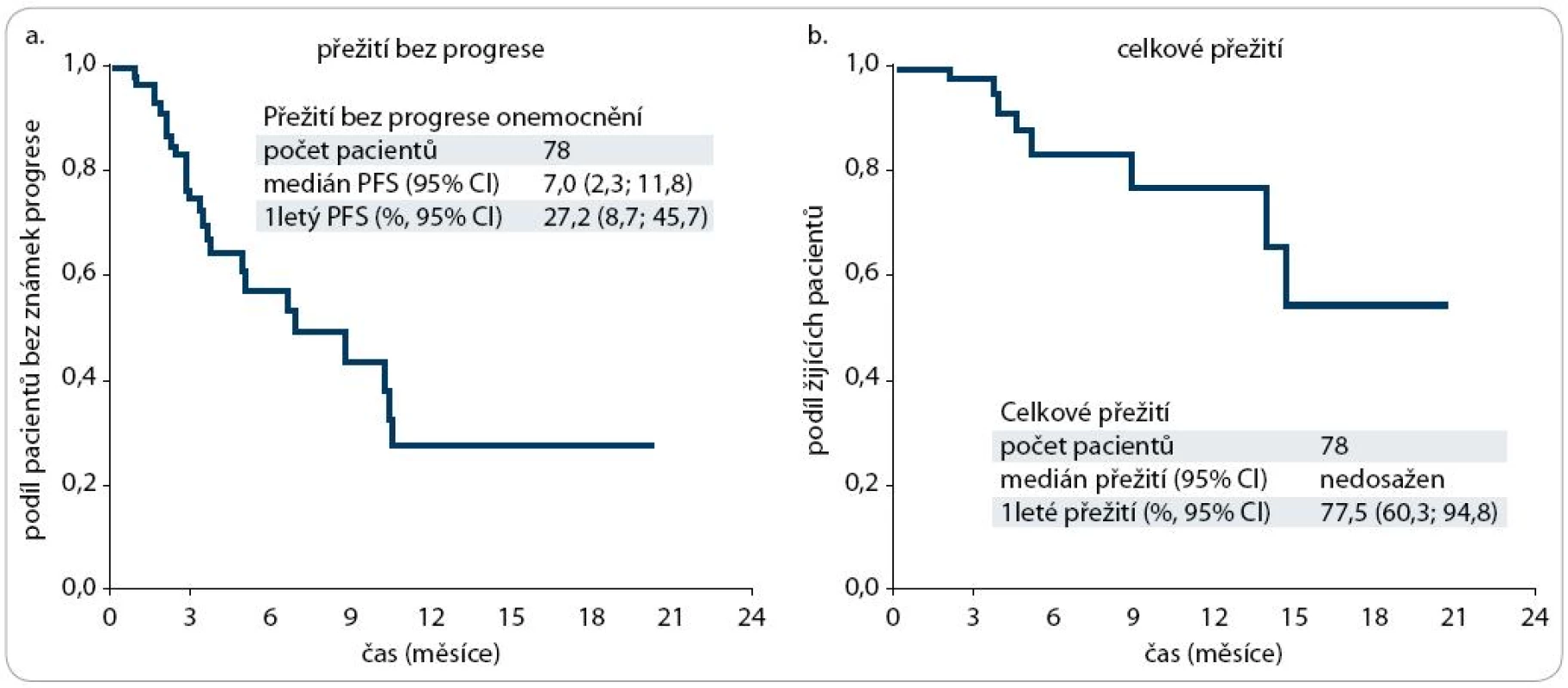
Diskuze
Česká republika má ze zatím neobjasněných důvodů nejvyšší incidenci karcinomu ledviny na světě. Incidence renálního karcinomu u nás v roce 2007 byla 27/100 000 obyvatel při mortalitě 12/100 000 obyvatel [3]. Asi u 25–30 % pacientů s renálním karcinomem jsou metastázy zjevné již v době diagnózy, u dalších 20–30 % pacientů s nepokročilým nádorem dojde ke generalizaci po nefrektomii.
Everolimus je lékem s mnoha klinickými aplikacemi. Kromě léčby mRCC se používá jako imunosupresivum při orgánových transplantacích a pro zlepšení průchodnosti stentů v kardiologii [4]. K jeho registraci v léčbě mRCC vedly výsledky randomizované studie RECORD-1, v níž byl everolimus srovnáván s placebem u nemocných po selhání sorafenibu, sunitinibu nebo obou těchto TKI. Celkem 416 pacientů bylo randomizováno v poměru 2 : 1 do ramene s everolimem v dávce 10 mg/den (n = 277) nebo do ramene s placebem (n = 139). Studie byla dvojitě zaslepená a jejím hlavním cílem bylo prokázat rozdíl v PFS a ověřit bezpečnost terapie [1,5]. Podle hodnocení nezávislého panelu dosáhl medián PFS 4,9 měsíce (everolimus) ve srovnání s 1,9 měsíce (placebo). Léčba everolimem snížila riziko progrese o 67 % (p < 0,001). U 64 % nemocných se podařilo dosáhnout kontroly nemoci (PR + SD). Rozdíl v OS nebyl statisticky významný (14,8 měsíce versus 14,4 měsíce, p = 0,162), ale tento výsledek mohl být významně ovlivněn překřížením ramen – až 80 % pacientů randomizovaných původně k placebu dostalo při progresi everolimus.
Nezávislými prognostickými faktory spojenými s kratším OS byly horší výkonnostní stav pacientů (performance status, PS), hyperkalcemie, anémie a předchozí léčba sunitinibem [5]. Nebyl zaznamenán významný rozdíl v kvalitě života mezi pacienty léčenými everolimem a placebem [6].
Ve srovnání se studií RECORD-1 měli naši pacienti o něco lepší PS (100 % Karnofsky, 28 % ve studii RECORD-1 vs 38 % PS 0 RENIS). Procento nemocných po nefrektomii bylo podobné (97 % RECORD-1 vs 91 % RENIS). Téměř polovina našich pacientů byla předléčena sunitinibem i sorafenibem (44 %), zatímco ve studii RECORD-1 bylo těchto pacientů jen 26 %. Již samotná schopnost podstoupit sekvenční léčbu přitom pravděpodobně koreluje s relativně dlouhým přežitím u mRCC [7]. Dalším potenciálně důležitým rozdílem byla skutečnost, že 17 % pacientů v našem souboru neukončilo předchozí terapii TKI pro progresi, nýbrž z jiných důvodů (zpravidla pro toxicitu). Ve studii RECORD-1 byla naproti tomu progrese na TKI jednou ze základních podmínek pro zařazení pacientů. Tyto rozdíly mohou být příčinou relativně lepšího PFS v našem retrospektivním souboru ve srovnání se studií RECORD-1. Procento nemocných s prospěchem z léčby (CR + PR + SD) je v našem souboru prakticky stejné jako v randomizované studii (69 % vs 64 %). Samozřejmě, počet nemocných v registru RENIS je dosud relativně malý a doba jejich léčení krátká.
Závažnými nežádoucími příhodami u pacientů léčených everolimem ve studii RECORD-1 byly zejména infekce (incidence 10 %), dušnost (7 %) a únava (5 %) [5]. Symptomatická pneumonitida se vyskytuje u asi 10 % pacientů léčených everolimem (u přibližně 4 % dosahuje stupně 3, tj. interferuje s běžnými aktivitami a/nebo vyžaduje oxygenoterapii). Ve většině případů jsou klinické projevy pneumotoxicity everolimu reverzibilní po redukci dávky nebo přerušení terapie. Radiologické známky plicní toxicity se objevují dokonce až u 40 % pacientů léčených everolimem [8]. Respirační nežádoucí příhody byly zaznamenány i v našem souboru u 5/78 pacientů (6 %), z toho u 3 (4 %) nemocných byly hodnoceny jako závažné. Údaje o infekčních komplikacích léčby nebylo možné z registru RENIS zjistit.
Podle první analýzy nemocných s mRCC z registru RENIS dosahuje tedy everolimus i mimo klinickou studii dobrého efektu při přijatelné tolerabilitě. Klinického prospěchu z léčby bylo dosaženo u téměř 70 % těžce předléčených nemocných s mRCC
Autorský tým deklaroval podporu od společnosti Novartis.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do bi omedicínských časopisů.
MUDr. Tomáš Büchler, Ph.D.
Fakultní Thomayerova nemocnice
Vídeňská 800
140 59 Praha 4
e-mail: tomas.buchler@ftn.cz
Obdrženo: 14. 6. 2011
Přijato: 18. 7. 2011
Sources
1. Motzer RJ, Escudier B, Oudard S et al. Efficacy of everolimus in advanced renal cell carcinoma: a double-blind, randomised, placebo-controlled phase III trial. Lancet 2008; 372(9637): 449–456.
2. Afinitor – souhrn infomací o přípravku. Poslední aktualizace 17. 05. 2010. European Medicines Agency. Available from: http://www.ema.europa.eu/docs/cs_CZ/document_library/EPAR_-_Product_Information/human/001038/WC500022814.pdf.
3. Dušek L, Mužík J, Gelnarová E et al. Cancer incidence and mortality in the Czech Republic. Klin Onkol 2010; 23(5): 311–324.
4. Gabardi S, Baroletti SA. Everolimus: a proliferation signal inhibitor with clinical applications in organ transplantation, oncology, and cardiology. Pharmacotherapy 2010; 30(10): 1044–1056.
5. Motzer RJ, Escudier B, Oudard S et al. Phase 3 trial of everolimus for metastatic renal cell carcinoma : final results and analysis of prognostic factors. Cancer 2010; 116(18): 4256–4265.
6. Beaumont JL, Butt Z, Baladi J et al. Patient-reported outcomes in a phase iii study of everolimus versus placebo in patients with metastatic carcinoma of the kidney that has progressed on vascular endothelial growth factor receptor tyrosine kinase inhibitor therapy. Oncologist 2011; 16(5): 632–640.
7. Buchler T, Klapka R, Melichar B et al. Sunitinib followed by sorafenib or vice versa for metastatic renal cell carcinoma – data from the Czech registry. Ann Oncol. 2011. Epub ahead of print.
8. White DA, Camus P, Endo M et al. Noninfectious pneumonitis after everolimus therapy for advanced renal cell carcinoma. Am J Respir Crit Care Med 2010; 182(3): 396–403.
Labels
Paediatric clinical oncology Surgery Clinical oncologyArticle was published in
Clinical Oncology

2011 Issue 5
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
- Metamizole vs. Tramadol in Postoperative Analgesia
- Spasmolytic Effect of Metamizole
- Metamizole in perioperative treatment in children under 14 years – results of a questionnaire survey from practice
-
All articles in this issue
- Hsp90 – cíl protinádorové terapie
- Předoperační chemoradioterapie v kombinaci s bevacizumabem u karcinomu konečníku
- Co pacientky potřebují vědět před operací mamárního karcinomu
- Neuroendoskopická biopsie tumoru mozku
- Adaptivní IG-IMRT karcinomu prostaty
- Parciální regrese ložisek Erdheimovy-Chesterovy nemoci v CNS po léčbě 2-chlorodeoxyadenosinem a jejich kompletní vymizení při léčbě lenalidomidem
- Sekundární angiosarkomy po konzervativní léčbě nádorů prsu
- Výsledky terapie metastatického renálního karcinomu lékem everolimus – analýza údajů z klinického registru RENIS
- Cetuximab zvyšuje antiproliferativní účinek trastuzumabu u buněk karcinomu prsu s nadměrnou expresí ERBB2 – předběžná studie
- Clinical Oncology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Parciální regrese ložisek Erdheimovy-Chesterovy nemoci v CNS po léčbě 2-chlorodeoxyadenosinem a jejich kompletní vymizení při léčbě lenalidomidem
- Neuroendoskopická biopsie tumoru mozku
- Sekundární angiosarkomy po konzervativní léčbě nádorů prsu
- Co pacientky potřebují vědět před operací mamárního karcinomu
