Fullerenový nanotransportér doxorubicinu pro cílenou interakci s mutovaným genem BRCA2
Fullerene Doxorubicin Nanotransporter for Target Interaction with mutated gene BRCA2
Background:
Malignant breast tumors are in developed countries, the most common cancer affecting mainly women. It is estimated that approximately 5–10% of breast cancers are conditioned by genetic family burdens, caused by mutation in the BRCA2 gene. In the course of the treatment doxorubicin is frequently used therapeutics. Despite its therapeutic efficacy, however, it shows high cardiotoxicity. Possibility to increase the therapeutic window, represent nanotransporters. Fullerenes are nanoparticles composed of carbon atoms whose physical-chemical properties indicate high stability. The complex of fullerene and doxorubicin enables the targeted method for the treatment. The aim of this work is to develop a nanotransporter system with an expected cytostatic effect without significant toxic effects.
Material and Methods:
To 5 mg of fullerene 0.5 ml of distilled water was added and solution was subsequently placed for 30 min in an ultrasonic bath (50 W). Fullerenes with bound doxorubicin (DOXO) were purified from unbound DOXO by centrifugation (16,000 g). For DOXO analysis acetate buffer was used. Fe2O3-NPs were prepared by reduction with borohydride and ammonia. Thereafter Fe2O3-AuNPs were prepared by thermal synthesis.
Results:
Carbon nanotransporter (fullerene) for binding of doxorubicin (FULLER-DOXO) was designed and subsequently studied by biophysical methods. We have found that FULLER-DOXO size is larger than 100 nm and the zeta potential is around 24 mV. DOXO, interacts with FULLER by the electrostatic interaction, and its volume increases with the applied concentration (R2 = 0.96). In the following experiment FULLER-DOXO was modified with oligodeoxynucleotide (ODN; 10 µg/ml), and this way was FULLER-DOXO-ODN1 complex prepared. Bound ODN represents a specific sequence for targeting the complex to a point mutation in the BRCA2 gene. In order to prove the interaction magnetic gold nanoparticle modified with the complementary sequence to the test nanotransporter was designed (ODN2-Fe2O3-AuNPs). Formed complex (FULLER-DOXO-ODN1-ODN2-Fe2O3-AuNPs) was subsequently confirmed by several independent techniques.
Conclusion:
We assume that the proposed nanoconstruct will be able to use for genetic targeting of anticancer drug.
Key words:
doxorubicin – breast cancer – fullerenes – magnetic gold nanoparticles
The work was realized with the support of the project NANO LPR 2017 Liga proti rakovině Praha and The European Technology Platform for Nanomedicine.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE recommendation for biomedical papers.
Submitted:
6. 3. 2017
Accepted:
26. 3. 2017
Authors:
S. Skaličková 1; M. Löfelmann 2; M. Gargulák 2; M. Dočekalová 2; B. Ruttkay-Nedecký 2; P. Suchý 1; M. Kepinská 3; Kizek R. 1–3
Authors‘ workplace:
Ústav humánní farmakologie a toxikologie, Farmaceutická fakulta, Veterinární a farmaceutická univerzita Brno
1; Centrální laboratoře, Farmaceutická fakulta, Veterinární a farmaceutická univerzita Brno
2; Ústav biomedicínských a environmentálních analýz, Wroclaw Medical University, Wroclaw, Polsko
3
Published in:
Klin Onkol 2017; 30(Supplementum1): 177-179
Category:
Article
Overview
Východiska:
Zhoubné nádory prsu jsou v rozvinutých zemích nejčastějším nádorovým onemocněním, postihující převážně ženy. Odhaduje se, že přibližně 5–10 % karcinomů prsu je podmíněno rodinnou genetickou zátěží, způsobenou mutací genu BRCA2. Při léčbě je často používaným terapeutikem doxorubicin. Přes svou terapeutickou účinnost však vykazuje vysokou kardiotoxicitu. Možnost, jak zvýšit terapeutické okno, představují nanotransportéry. Fullereny jsou nanočástice tvořené atomy uhlíku jejichž fyzikálně chemické vlastnosti jim udávají vysokou stabilitu. Komplex fullerenu a doxorubicinu (DOXO) umožňuje cílenou metodu léčby. Cílem této práce je vyvinout nanotransportérový systém s předpokládaným účinkem cytostatika bez výrazných toxických efektů.
Materiál a metody:
K 5 mg fullerenu bylo přidáno 0,5 ml destilované vody a roztok byl následně vložen na 30 min do ultrazvukové lázně (50 W). Fullereny s navázaným DOXO byly purifikovány od nenavázaného DOXO pomocí centrifugace (16 000 g). Pro analýzu DOXO byl použit acetátový pufr. Fe2O3-NPs byly připraveny redukcí s borohydridem a amoniakem. Poté byly připravené Fe2O3-AuNPs termální syntézou.
Výsledky:
Byl navržen a následně studován biofyzikálními metodami uhlíkový nanotransportér (fulleren) pro vazbu doxorubicinu (FULLER-DOXO). Zjistili jsme, že velikost FULLER-DOXO je větší než 100 nm a zeta potenciál se pohybuje kolem 24 mV. DOXO interaguje s FULLER elektrostatickou interakcí a jeho množství se zvyšuje s aplikovanou koncentrací (R2 = 0,96). V následujícím experimentu byl FULLER-DOXO modifikován oligodeoxynukleotidem (ODN; 10 µg/ml), a byl tak vytvořen komplex FULLER-DOXO-ODN1. Vázaný ODN představuje specifickou sekvenci, pro zacílení komplexu na bodovou mutaci v genu BRCA2. Pro prokázání interakce byla navržena magnetická zlatá nanočástice modifikovaná komplementární sekvencí k testovanému nanotransportéru (ODN2-Fe2O3-AuNPs). Vytvořený komplex (FULLER-DOXO-ODN1-ODN2-Fe2O3-AuNPs) byl následně potvrzen několika nezávislými technikami.
Závěr:
Předpokládáme, že navržený nanokonstrukt bude možné využít pro geneticky cílené směřování protinádorového léčiva.
Klíčová slova:
doxorubicin – rakovina prsu – fullereny – magnetické zlaté nanočástice
Úvod
Zhoubné nádory prsu jsou v rozvinutých zemích nejčastějším nádorovým onemocněním, postihující převážně ženy [1]. Odhaduje se, že přibližně 5–10 % karcinomů prsu je podmíněno rodinnou genetickou zátěží, způsobenou mutací genu BRCA2 [2]. Při léčbě je často používaným terapeutikem doxorubicin (DOXO). Nicméně, DOXO a další cytostatika ze skupiny antracyklinových antibiotik vykazují v závislosti na aplikované dávce nezanedbatelnou kardiotoxicitu [3]. Tento vedlejší efekt limituje kumulativní aplikovaná dávka. Uvádí se, že poškození srdečního svalu se vyskytuje u 3 % pacientů při dávce 400 mg/ml, 7 % při dávce 500 mg/ml a u více jak 15 % pacientů dochází k poškození srdečního svalu při dávce 700 mg/ml. Vývoj nových léčiv je tedy zaměřen na snížení kardiotoxicity antracyklinových antibiotik. Metody nanomedicíny za využití různých nanokonstruktů by pomohly snížit vedlejší efekty spojené s léčbou nádorového onemocnění [4,5]. Fullereny jsou nanočástice tvořené atomy uhlíku, jejichž fyzikálně chemické vlastnosti jim udávají vysokou stabilitu [6]. Jednou z významných vlastností fullerenů jsou jejich fyzikálně-chemické vlastnosti, které umožňují interakci s chemoterapeutiky [7,8]. Řada studií prokázala synergický efekt DOXO a fullerenu na inhibici metastáz a snížení jeho toxicity u zvířecích modelů. Tento efekt může být vysvětlen schopností aromatických molekul tvořit nekovalentní hetero-komplex v roztocích. Vznikem heterokomplexu DOXO s fullerenem se také snižuje jeho negativní vliv na srdeční tkáň. Komplex fullerenu a DOXO představuje cílenou metodu léčby [9]. Cílem této práce je vyvinout nanotransportérový systém využívající uhlíkové struktury fullerenu pro vazbu DOXO.
Materiál a metody
K 5 mg fullerenu bylo přidáno 0,5 ml destilované vody a roztok byl následně vložen na 30 min do ultrazvukové lázně (50 W). Fullereny s navázaným DOXO byly purifikovány od nenavázaného DOXO pomocí centrifugace (16 000 g). Fe2O3-NPs byly připraveny redukcí s borohydridem a amoniakem. Poté byly připravené Fe2O3-AuNPs termální syntézou. Velikost částic byla zjištěna koloidním analyzátorem. Stanovení DOXO probíhalo elektrochemicky pomocí adsorptivní přenosové techniky a standardní cely se třemi elektrodami. Elektroda ze skelného uhlíku byla pracovní elektroda. Ag/AgCl/3M KCl elektroda byla referenční a platinová elektroda byla pomocná. Pro analýzu DOXO byl použit acetátový pufr (0,2 M acetát sodný) při pH 5,0, který byl použit jako pomocný elektrolyt. Parametry měření DOXO byly následující: počáteční potenciál –0,8 V, konečný potenciál –0,4 V, doba akumulace 120 s, krok potenciální 5 mV, modulační amplituda 25 mV, objem vzorku 10 µl, objem měřicí cely 2 ml. Parametry pro měření Zn2+: počáteční potenciál –1,2 V, konečný potenciál –0,7 V, doba akumulace 60 s, krok potenciální 5 mV, modulační amplituda 25 mV, objem vzorku 10 µl, objem měřicí cely 2 ml. Vazba oligonukleotidů byla provedena ve fosfátovém pufru (pH 7,0) po dobu 24 hod. Hybridizační experimenty byly provedeny ve fosfátovém pufru (pH 7,0 a 0,1 M NaCl).
Výsledky
Byl navržen a následně studován biofyzikálními metodami uhlíkový nanotransportér (fulleren) pro vazbu doxorubicinu (FULLER-DOXO). Zjistili jsme, že velikost FULLER-DOXO je větší než 100 nm a zeta potenciál je kolem –25 mV, což naznačuje dobrou stabilitu koloidního systému. DOXO interaguje s FULLER elektrostatickou interakcí. Aby byla ověřena tato interakce, k FULLER o koncentraci 1–10 mg/ml byl přidán DOXO (30 µM). Elektrochemickým stanovením heterokomplexu FULLER-DOXO byla zjištěna zvyšující se koncentrace DOXO v závislosti na koncentraci (R2 = 0,96). V následujícím experimentu byl FULLER-DOXO modifikován oligodeoxynukleotidem (ODN; 10 µg/ml) a byl tak vytvořen komplex FULLER-DOXO-ODN1. Pro prokázání interakce byly použity magnetické zlaté nanočástice modifikované komplementární sekvencí k testovanému nanotransportéru (ODN2-Fe2O3-AuNPs). Výhodou použití magnetických částic je snadná purifikace nanočástic pomocí magnetu od nenavázaných částí komplexu. Vazba AuNPs k ODN2 byla prověřena elektrochemicky (redoxní signál CA, –1,45 V). Z výsledků je patrné, že se zvyšující se koncentrací komplexu (ODN2-Fe2O3-AuNPs) se zvyšuje elektrochemický signál ODN2 (R2 = 0,93). V dalším experimentu byl detailně studován vytvořený komplex (FULLER-DOXO-ODN1-ODN2-Fe2O3-AuNPs). Tvorba předpokládaného komplexu byla následně potvrzena elektrochemickou analýzou DOXO a signálu CA.
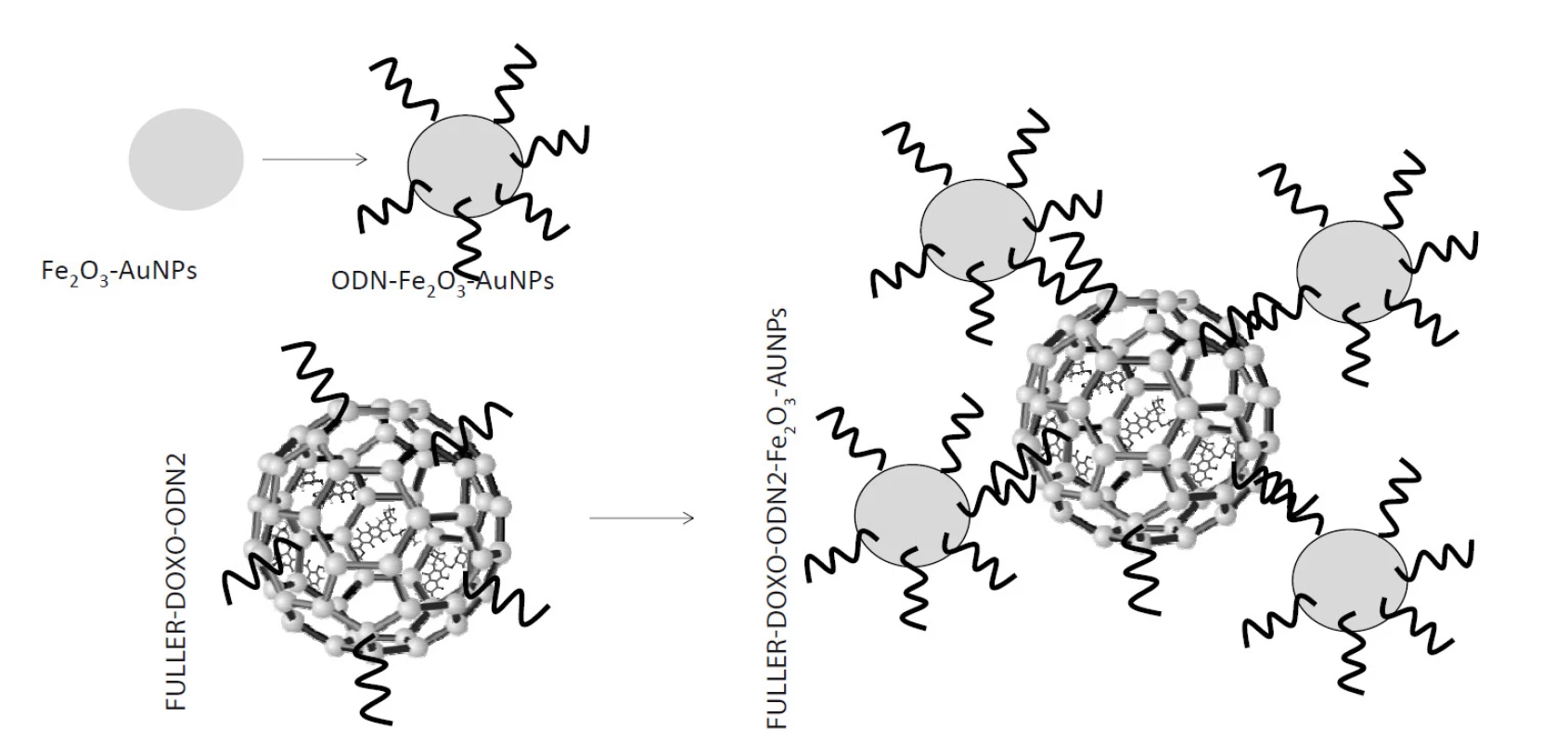
Závěr
V této prvotní studii jsme prokázali modifikaci fullerenu s antracyklinovým antibiotikem doxorubicinem a antisense oligodeoxynukleotidem k potencionálním využití v oblasti cílené léčby nádorů prsu. Předpokládáme, že navržený nanokonstrukt bude možné využít pro geneticky cílené směřování protinádorového léčiva.
Práce byla realizována za podpory projektu NANO LPR 2017 Liga proti rakovině Praha a The European Technology Platform for Nanomedicine.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Ing. Sylvie Skaličková, Ph.D.
Ústav humánní farmakologie a toxikologie
Farmaceutická fakulta
Veterinární a farmaceutická univerzita Brno
Palackého třída 1946/1
612 42 Brno
e-mail: sylvie.skalickova@gmail.com
Submitted: 6. 3. 2017
Accepted: 26. 3. 2017
Sources
1. Martinez-Outschoorn UE, Peiris-Pages M, Pestell RG et al. Cancer metabolism: a therapeutic perspective. Nat Rev Clin Oncol 2017; 14 (1): 11–31. doi: 10.1038/nrclinonc.2016.60.
2. Narod SA. BRCA mutations in the management of breast cancer: the state of the art. Nat Rev Clin Oncol 2010; 7 (12): 702–707. doi: 10.1038/nrclinonc.2010.166.
3. Kizek R, Adam V, Hrabeta J et al. Anthracyclines and ellipticines as DNA-damaging anticancer drugs: recent advances. Pharmacol Ther 2012; 133 (1): 26–39. doi: 10.1016/j.pharmthera.2011.07.006.
4. Blazkova I, Nguyen HV, Kominkova M et al. Fullerene as a transporter for doxorubicin investigated by analytical methods and in vivo imaging. Electrophoresis 2014; 35 (7): 1040–1049. doi: 10.1002/elps.201300393.
5. Drbohlavova J, Chomoucka J, Adam V et al. Nanocarriers for anticancer drugs – new trends in nanomedicine. Curr Drug Metab 2013; 14 (5): 547–564.
6. Lynchak OV, Prylutskyy YI, Rybalchenko VK et al. Comparative analysis of the antineoplastic activity of c-60 fullerene with 5-fluorouracil and pyrrole derivative in vivo. Nanoscale Res Lett 2017; 12 (1): 8. doi: 10.1186/s11671-016-1775-0.
7. Panchuk RR, Prylutska SV, Chumak VV et al. Application of C-60 fullerene-doxorubicin complex for tumor cell treatment in vitro and in vivo. J Biomed Nanotechnol 2015; 11 (7): 1139–1152.
8. Wang H, Agarwal P, Zhao ST et al. A biomimetic hybrid nanoplatform for encapsulation and precisely controlled delivery of therasnostic agents. Nat Commun 2015; 6 : 10081. doi: 10.1038/ncomms10081.
9. Shi JJ, Wang BH, Wang L et al. Fullerene (C-60) -based tumor-targeting nanoparticles with “off-on” state for enhanced treatment of cancer. J Control Release 2016; 235 : 245–258. doi: 10.1016/j.jconrel.2016.06.010.
Labels
Paediatric clinical oncology Surgery Clinical oncologyArticle was published in
Clinical Oncology

2017 Issue Supplementum1
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
- Metamizole vs. Tramadol in Postoperative Analgesia
- Spasmolytic Effect of Metamizole
- Metamizole in perioperative treatment in children under 14 years – results of a questionnaire survey from practice
-
All articles in this issue
- Analýza mikroRNA u epiteliálního karcinomu vaječníku
- Využití porózního hydrogelu jako 3D scaffoldu pro růst leukemických B lymfocytů
- Ascitická tekutina u nádoru vaječníků může poskytnout informace vhodné pro diagnostiku
- Diagnostický a terapeutický potenciál membránového HSP90
- Everolimus v denní klinické praxi se zaměřením na problematiku postižení sliznice dutiny ústní – zkušenost onkologického centra v průběhu roku 2016
- Stanovení DNA metylace v BRCA2 genu na elektrodových biočipech
- Molekulární patologie kolorektálního karcinomu, mikrosatelitová nestabilita – způsob detekce, vztah k patofyziologii a prognóze
- Laktátdehydrogenáza – starý nádorový marker ve světle současných poznatků a v preanalytických souvislostech
- Využití metody PLA pro detekci komplexů p53/p63/p73 in situ v nádorových buňkách a nádorové tkáni
- Význam deregulace mikroRNA v molekulární patogenezi a histologické transformaci folikulárního lymfomu
- Cirkulující myeloidní supresorové buňky a jejich úloha v nádorové imunologii
- Je možné pozorovat etnickou diferenci v základních krevních testech? Údaje z programu onkologické prevence v komplexním onkologickém centru v České republice
- Zinečnatými ionty modifikovaný nanotransportér antracyklinových antibiotik pro cílenou terapii nádoru prsu
- Fullerenový nanotransportér doxorubicinu pro cílenou interakci s mutovaným genem BRCA2
- Clinical Oncology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Ascitická tekutina u nádoru vaječníků může poskytnout informace vhodné pro diagnostiku
- Laktátdehydrogenáza – starý nádorový marker ve světle současných poznatků a v preanalytických souvislostech
- Molekulární patologie kolorektálního karcinomu, mikrosatelitová nestabilita – způsob detekce, vztah k patofyziologii a prognóze
- Cirkulující myeloidní supresorové buňky a jejich úloha v nádorové imunologii
