Kvantifikace postižení u pacientů s lumbální spinální stenózou
Quantification of Impairment in Patients with Lumbar Spinal Stenosis
Quantification of impairment in patients with lumbar spinal stenosis (LSS) should be based on assessment of the severity of clinical impairment and its impact on patient disability, rather than derived from a relative analysis of radiological findings. A range of scores and scales are used to assess patient status and there are several valid reasons why impairment should be quantified, including accurate assessment of patient status, evaluation of long-term clinical outcome and therapeutic efficacy, and help with the choice of optimal treatment modality. This article addresses the scales, questionnaires and quantified assessments that the authors often use in patients with LSS, namely a visual analogue scale for pain or a pain intensity numerical rating scale, the neurological impairment score in lumbar spinal stenosis, the Oswestry Disability Index and measuring of distance covered on a treadmill. We propose criteria for the assessment of LSS severity that may be useful in selecting a treatment (conservative or surgical therapy). These are based on the evaluation of pain using a pain intensity numerical rating scale, assessment of disability using the Oswestry Disability Index and analysis of distance covered on a treadmill.
Key words:
lumbar spinal stenosis – The Oswestry Disability Index – neurogenic claudication –pain assessment
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Authors:
B. Mičánková Adamová 1,2; S. Voháňka 1,2
Authors‘ workplace:
Neurologická klinika LF MU a FN Brno
1; CEITEC – Středoevropský technologický institut, MU, Brno
2
Published in:
Cesk Slov Neurol N 2013; 76/109(5): 570-574
Category:
Review Article
Overview
Kvantifikace postižení u pacientů s lumbální spinální stenózou (LSS) by měla být založena na zhodnocení tíže klinického postižení a jeho dopadu na kvalitu života pacienta, neměla by vycházet z posuzování tíže radiologických změn. Pro tyto účely se používají různé hodnotící škály a skóre. Důvodů pro provádění kvantifikace je více: umožňuje přesnější posouzení stavu pacienta, má svůj význam při hodnocení dlouhodobého klinického vývoje pacienta i hodnocení efektu léčby a rovněž napomáhá při výběru nejvhodnějšího léčebného postupu u pacienta. V článku jsou probrány škály, skóre a měření, která běžně využíváme v klinické praxi u pacientů s LSS. Mezi ně patří vizuální analogová škála bolesti či numerická škála intenzity bolesti, skóre neurologického postižení u lumbální spinální stenózy, Oswestry dotazník, zhodnocení ušlé vzdálenosti na mechanickém chodníku. Na základě zhodnocení bolesti pomocí numerické škály intenzity bolesti, disability pomocí Oswestry dotazníku a ušlé vzdálenosti hodnocené na mechanickém chodníku navrhujeme kritéria pro orientační zhodnocení tíže LSS a z tohoto vyplývající volbu léčebného postupu (konzervativní či operační terapie).
Klíčová slova:
lumbální spinální stenóza – Oswestry dotazník – neurogenní klaudikace – hodnocení bolesti
Použité zkratky
DKK dolní končetiny
LSS lumbální spinální stenóza
NIS ‑ LSS Neurological Impairment Score in Lumbar Spinal Stenosis (skóre neurologického postižení u lumbální spinální stenózy)
NK neurogenní klaudikace
ODI Oswestry Disability Index
PI ‑ NRS Pain Intensity Numerical Rating Scale (numerická škála intenzity bolesti)
VAS vizuální analogová škála
Úvod
Lumbální spinální stenóza (LSS) je definována jako zúžení páteřního nebo kořenového kanálu osteoligamentózního původu v bederním úseku páteře, které je klinicky manifestní [1]. Za lumbální spinální stenózu se nepovažuje zúžení páteřního kanálu na podkladě akutního výhřezu meziobratlového disku. LSS se vyznačuje zmenšením prostoru pro nervové a cévní struktury v bederní páteři, přičemž symptomy jsou způsobeny buď přímou mechanickou kompresí, nebo nepřímou vaskulární kompresí nervových kořenů nebo kaudy equiny [2]. Většina autorů se domnívá, a klinická praxe to potvrzuje, že se jedná o častou chorobu vyššího věku, která přispívá k omezení mobility starších pacientů. Převažujícím věkem začátku potíží je 6. dekáda.
LSS se může manifestovat neurogenními klaudikacemi, radikulárním syndromem či syndromem kaudy equiny. Tradičně jsou do obrazu LSS řazeny i bolesti dolní části zad, nejde však o projev stenózy jako takové, ale o projev spondylózy a spondylartrózy, které jsou hlavní příčinou stenozujícího procesu. Neurogenní klaudikace jsou pro LSS charakteristickým příznakem a vyznačují se tím, že po určité době stání či chůze ve vzpřímené poloze vznikají bolesti, parestezie a následně i slabost dolních končetin, která může vést až k pádům.
Je známo, že u pacientů s bolestmi dolní části zad je běžně pozorována neshoda mezi radiologickým a klinickým nálezem. Posuzování tíže lumbální spinální stenózy by mělo být založeno na zhodnocení míry klinického postižení a jeho dopadu na disabilitu pacienta, nemělo by vycházet z posuzování tíže radiologických změn. Pro tyto účely používáme různé hodnotící škály a skóre, o kterých bude dále pojednáno.
Důvody kvantifikace postižení
Kvantifikace postižení u vertebrogenních pacientů, a tedy i u pacientů s LSS, se používá nejen v klinických studiích, ale i v běžné klinické praxi. Důvodů pro užívání kvantifikace je více: umožňuje přesnější a měřitelné posouzení stavu pacienta, má svůj význam při hodnocení dlouhodobého klinického vývoje pacienta a hodnocení efektu léčby a rovněž napomáhá při výběru nejvhodnějšího léčebného postupu.
Velmi důležitá je klinická interpretace výsledku získaného vyhodnocením dotazníku. I když změna skóre může být statisticky signifikantní, nemusí to nezbytně znamenat, že změna je klinicky významná. Byl proto definován pojem „minimální klinicky významný rozdíl“, a to jako nejmenší rozdíl ve skóre, který pacient vnímá jako užitečný [3]. Problémem je rovněž vztah minimálního klinicky významného rozdílu a nepřesnosti dotazníku. Existuje riziko, že změna ve skóre vyjadřuje pouze nepřesnost dotazníku a ne pravý rozdíl. Pokud tedy nepřesnost přesahuje minimální klinicky významný rozdíl, užitečnost dotazníku může být sporná [4].
Možnosti kvantifikace postižení
U pacientů s bolestí dolní části zad jsou využívány různé hodnotící škály a skóre. V současnosti se stále větší pozornost věnuje škálám, ve kterých hodnotí svůj stav sám pacient, což je dáno tím, že cílem léčby je zejména zlepšení funkčního stavu a kvality života pacienta. Do pozadí tedy ustupuje dříve běžně užívané hodnocení lékařem (výsledek léčby byl často hodnocen jako výborný, dobrý, přijatelný nebo špatný) a stále více se uplatňuje hodnocení bolesti a disability samotným pacientem [4].
Při vyhodnocení stavu pacienta a výsledků léčby je nutné analyzovat více faktorů. Hodnocení nemocného s bolestí dolní části zad je možné obecně provést ze tří aspektů:
- zhodnocení objektivního nálezu (např. kvantifikace neurologického nálezu),
- zhodnocení výkonnosti nemocného (např. schopnost ujít určitou vzdálenost, schopnost sedět, stát či nést určité břemeno),
- posouzení sociální disability a životní spokojenosti.
Škály a měření lze tedy použít při hodnocení řady údajů a nálezů, např. anamnestických dat, objektivního neurologického nálezu, zhodnocení zdravotního stavu, a to jak celkového, tak ve vztahu ke specifickému onemocnění, posouzení spokojenosti s léčbou. Příklady dotazníků, měření a škál využívaných při hodnocení pacientů s LSS jsou uvedeny v tab. 1. Dále budou podrobněji probrány škály a skóre, které běžně využíváme v klinické praxi u pacientů s LSS.
![Vyšetření, škály a dotazníky užívané při hodnocení pacientů s LSS (modifikováno dle Fritzové et al) [5].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/ad225b9b021edfc54c4e2a172a67410e.png)
Vizuální analogová škála bolesti (VAS) se využívá ke kvantifikaci bolesti, což provádí sám pacient. VAS umožňuje vyjádřit bolest graficky, používá se úsečka o délce 10 cm, vypadá jako pravítko, její levý konec je označen jako „žádná bolest“ (0) a pravý konec jako „nejhorší bolest, jakou si umím představit“ (10). Pacient na úsečce označí bod, který znázorňuje intenzitu vnímané bolesti, při hodnocení se odečítá počet centimetrů od levého okraje.
Místo škály od 0 do 10 je možno využít škálu 0 až 100 (při hodnocení se odečítá počet milimetrů od levého okraje). Za minimální klinicky významný rozdíl u této škály jsou považovány hodnoty 18 až 19. VAS je pokládána za dostatečně citlivou pro detekci minimálních klinicky významných změn [4]. U pacientů s LSS je vhodné odděleně zjišťovat úroveň bolesti v dolních končetinách a v zádech a dále i úroveň bolesti klidové (vsedě, vleže) a při stání či chůzi, což je dáno tím, že pacient s LSS může mít pouze neurogenní klaudikace a nemusí mít žádné klidové bolesti.
Dále se využívá i 11bodová numerická škála intenzity bolesti (Pain Intensity Numerical Rating Scale, PI ‑ NRS), kdy pacient verbálně hodnotí svou bolest číslem od 0 do 10. Hodnota 0 znamená žádná bolest, hodnota 10 nejhorší bolest, jakou si pacient umí představit. Hodnoty 1 – 3 se považují za mírnou bolest, 4 – 6 za střední bolest a 7 – 10 za těžkou bolest. Za klinicky významný rozdíl je většinou považována redukce o 2 body nebo o 30 % na této škále [14]. NRS ve srovnání s VAS je jednodušší, užití nevyžaduje žádné pomůcky, stačí pouze verbální kontakt, je tedy vhodná i pro telefonický kontakt s pacientem. S VAS mohou mít potíže starší pacienti, pacienti s vizuálním či kognitivním postižením. Byla zjištěna významná a staticky signifikantní korelace mezi VAS a NRS (r = 0,847; p < 0,001) [15].
Skóre neurologického postižení u lumbální spinální stenózy (NIS ‑ LSS, Neurological Impairment Score in Lumbar Spinal Stenosis), dříve označované jako skóre Ada ‑ Vo (zkratka Ada ‑ Vo byla odvozena od počátečních písmen autorů tohoto skóre – Adamová, Voháňka), bylo vypracováno na našem pracovišti pro zhodnocení neurologického nálezu na dolních končetinách u pacientů s LSS (tab. 2). Důvodem pro vytvoření tohoto skóre byla skutečnost, že dosud neexistovalo obdobné běžně rozšířené skóre. Skóre zahrnuje hodnocení šlachových a okosticových reflexů na DKK, taktilního a vibračního čití na DKK, hodnotí přítomnost paréz (schopnost stoje na špičkách, na patách a dřep) a dále schopnost chůze a běhu. Výsledek může nabývat hodnot od 0 do 33 bodů, přičemž plný počet bodů znamená zcela normální neurologický nález na dolních končetinách, 0 bodů pak úplnou neschopnost samostatné lokomoce. Skóre je jednoduché a lze jej stanovit při běžném neurologickém vyšetření DKK.
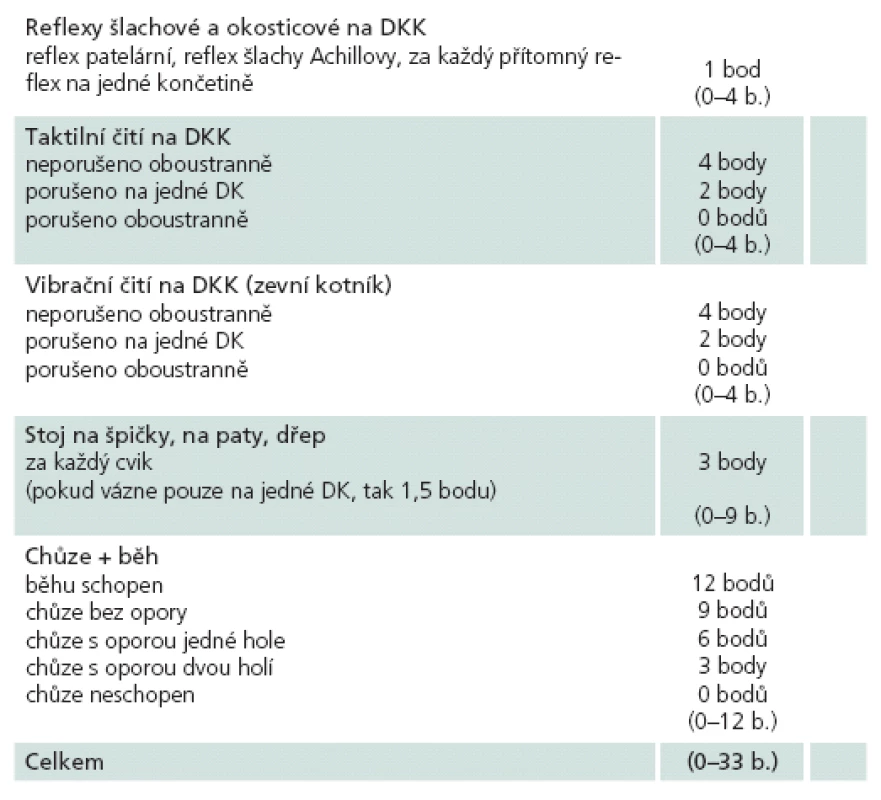
Rovněž jsme provedli standardizaci a validaci NIS ‑ LSS. Prokázali jsme, že skóre signifikantně odlišuje pacienty s LSS od zdravých osob, a byla prokázána korelace mezi tímto skórem a disabilitou pacientů s LSS [6]. Byla stanovena i optimální cut‑off hodnota, která činí 32, přičemž senzitivita je 85,5 % a specificita 81,3 % (p < 0,001). Ověřili jsme tedy dobrou použitelnost skóre NIS ‑ LSS u pacientů s LSS. Toto skóre má však i svá omezení. Není vhodné pro polymorbidní pacienty, u kterých výsledek skóre může být ovlivněn jinými nemocemi (např. přítomností polyneuropatie, přítomností koxartrózy a gonartrózy limitujících hybnost atd.). Jeho přínos a využití vidíme zejména při dlouhodobém sledování a hodnocení efektu léčby pacientů s LSS.
Patognomickým příznakem LSS jsou neurogenní klaudikace, které omezují pacienta při chůzi. Z tohoto důvodu je cenné vyšetření na mechanickém (pohyblivém) chodníku [treadmill], jež objektivizuje pacientovy potíže při chůzi a hodnotí vzdálenost, kterou nemocný ujde do vzniku potíží. Při tomto vyšetření se mohou rovněž manifestovat reflexologické změny či parézy [16]. Vyšetření na mechanickém chodníku je považováno za bezpečný, jednoduše proveditelný a kvantifikovatelný prostředek pro stanovení základního funkčního stavu u pacientů s LSS a NK. Test je rovněž užitečný pro zhodnocení výsledku chirurgické léčby, má dobrou reprodukovatelnost a nebyl zjištěn vliv opakovaného provádění testu na výsledek [17]. Neurogenní klaudikace je možno nejlépe prokázat při konstantní pomalejší chůzi (při rychlosti kolem 2 km/ h). Během testování na mechanickém chodníku je nutné, aby pacient zůstal ve vzpřímené poloze a nepředkláněl se, protože by mohlo dojít k ústupu neurogenních klaudikací (při předklonu se páteřní kanál rozšiřuje). Pro vyšetření na mechanickém chodníku je dostačující 15 min, protože pokud do této doby nevznikly neurogenní klaudikace, je málo pravděpodobné, že by se při dalším pokračování rozvinuly [18,19].
Při vyhodnocování testu na mechanickém chodníku je nutné si uvědomit, že omezení kapacity chůze může mít řadu jiných příčin (např. dušnost, celkovou slabost, dekondici, cévní klaudikace, kloubní bolesti) a že je třeba pečlivé analýzy, aby nedošlo k chybné interpretaci ve smyslu NK [20]. V literatuře se udává, že treadmill test může být užitečný v diferenciální diagnostice LSS, zejména při odlišení cévních a neurogenních klaudikací [21]. Význam testování na mechanickém chodníku podtrhuje zjištění, že subjektivní odhad ušlé vzdálenosti pacientem bývá chybný. V literatuře je opakovaně zdůrazňována potřeba objektivního měření úrovně aktivity u pacientů s LSS [22,23].
Oswestry dotazník (Oswestry Disability Index – ODI) hodnotí omezení běžných denních aktivit bolestí dolní části zad, kvantifikuje tedy subjektivní potíže pacienta a vyjadřuje míru disability [9,24]. Oswestry dotazník je komplexní, zahrnuje otázky na fyzickou disabilitu (omezení schopnosti sedět, stát, zvedání břemen a chůze), hodnotí i sociální hendikep (společenský život, sexuální život, cestování, osobní péče) a hodnotí rovněž bolest a spánek. Dotazník obsahuje 10 otázek, z nichž každá má šest alternativ odpovědí, přičemž odpovědi jsou skórovány odshora dolů, kdy se k první možnosti odpovědi přiřazuje 0 bodů a k poslední 5 bodů (tato představuje nejvyšší stupeň disability u dané otázky). Míra disability se vyjadřuje v procentech a vypočítá se z celkového skóre (ze součtu bodů u všech 10 otázek). ODI může nabývat hodnot 0 až 100 %. Pacient potřebuje k vyplnění dotazníku většinou 3,5 – 5 min a asi 1 min zabere jeho vyhodnocení. Za minimální klinicky významný rozdíl ODI jsou považovány dle různých autorů hodnoty 5,2 až 16,3 procentních bodů [25,26].
První verze tohoto dotazníku byla publikována v roce 1980 [9]. Dotazník existuje ve více verzích [24,27], přičemž autoři ODI doporučují nyní užívat verzi 2.1a, která je k dispozici i v českém jazyce a byla jazykově validována. V naší předchozí práci, v níž je i prezentována nová verze ODI, jsme potvrdili, že nová česká verze Oswestry dotazníku (2.1a) je plně zaměnitelná se starší verzí ODI a pro dosažení jednotnosti by měla být používána. ODI dobře odlišuje pacienty s LSS od zdravých dobrovolníků a jeho používání u pacientů s LSS k posouzení jejich disability se jeví jako přínosné. Výsledná hodnota napomáhá i při rozhodování o dalším léčebném postupu [28].
Pro užívání ODI je nutno získat povolení od „MAPI Research Trust“ ve Francii, který je možno kontaktovat na www.mapi ‑ trust.org.
O ostatních dotaznících a škálách zmíněných v tab. 1 je podrobněji pojednáno v naší monografii „Lumbální spinální stenóza“ [29].
Tíže LSS a volba léčebného postupu
V současné době neexistují jednotná a všeobecně uznávaná kritéria pro stanovení tíže LSS. Jak již bylo výše uvedeno, zhodnocení tíže LSS by mělo být založeno na stanovení stupně klinického postižení, což je podstatné i pro další volbu léčebného postupu (tj. rozhodnutí, zda zvolit spíše konzervativní postup či operační léčbu).
Na základě literárních údajů i vlastní klinické zkušenosti navrhujeme následující hodnocení tíže LSS a z tohoto vyplývající volbu léčebného postupu [30 – 38]. Je nutné si uvědomit, že uvedené skutečnosti neplatí absolutně, je důležité přihlédnout i k individuálním faktorům, jako jsou věk pacienta, jeho celkový zdravotní stav a pacientovy preference při výběru terapeutického postupu.
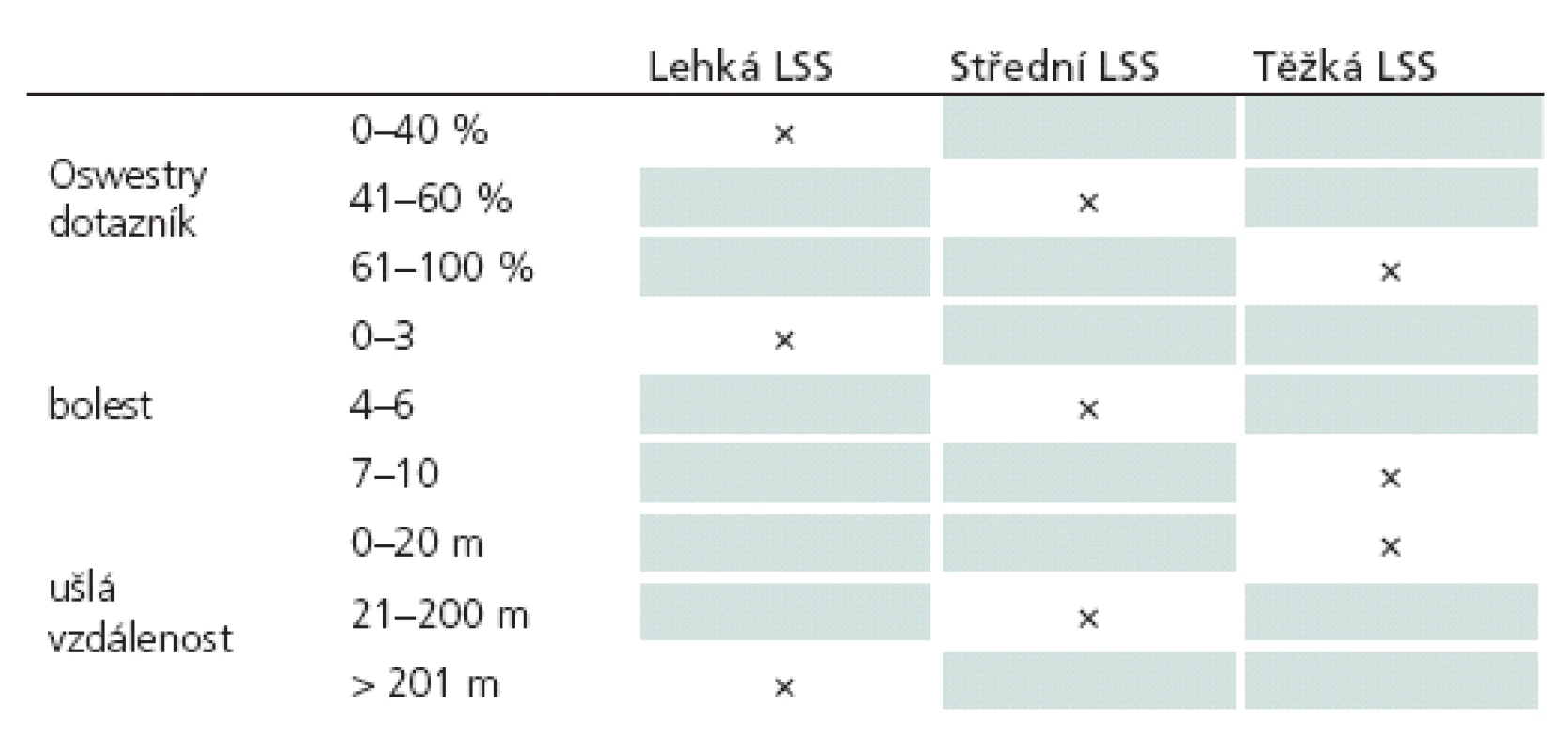
Tíži LSS navrhujeme hodnotit podle třech parametrů (tab. 3):
- intenzita bolesti stanovená pomocí numerické škály intenzity bolesti (lehká bolest: 1 – 3, střední bolest: 4 – 6, těžká bolest: 7 – 10),
- disabilita stanovená podle Oswestry dotazníku (lehké postižení: 0 – 40 %, střední postižení: 41 – 60 %, těžké postižení: 61 – 100 %),
- ušlá vzdálenost do vzniku NK hodnocená na mechanickém chodníku (těžké postižení: 0 – 20 m, střední postižení 21 – 200 m, lehké postižení nad 201 m).
Tyto tři parametry byly vybrány proto, že kvantifikují ty potíže, které mají pacienti s LSS nejčastěji a které jim vadí nejvíce. Skóre neurologického postižení u lumbální spinální stenózy (NIS ‑ LSS) nebylo do hodnocení tíže LSS zahrnuto ze tří důvodů – 1. v naší práci zabývající se tímto skóre jsme prokázali, že NIS ‑ LSS koreluje úzce s disabilitou, kterou považujeme za nadřazenou, 2. nemáme stanoveny jasné meze (cut‑off hodnoty) pro postižení lehké – střední – těžké u NIS ‑ LSS, 3. toto skóre je relativně nové a není tak rozšířené jako zvolené tři parametry.
Tíže LSS (lehká, střední, těžká) je následně odvozena podle převažující kategorizace jednotlivých parametrů (u každého parametru je kategorie lehká – střední – těžká). Pokud každý ze tří parametrů vykazuje jinou kategorii, řídíme se podle kategorie, do které spadá ušlá vzdálenost. Tento parametr lze dobře objektivizovat a neurogenní klaudikace jsou patognomický příznak pro LSS.
U pacientů s lehkou formou LSS volíme konzervativní postup, u pacientů s těžkou formou LSS zvažujeme na prvním místě operační řešení. U pacientů se střední formou LSS doporučujeme v první fázi konzervativní postup, při jeho neúspěchu (zhruba po době 3 – 6 měsíců) a progresi potíží pak zvažujeme operační léčbu. U pacientů, u nichž se rozvinul syndrom kaudy equiny, či u pacientů s progredujícími parézami je rovněž indikováno operační řešení. Naopak u pacientů vysokého věku s četnými komorbiditami se přikláníme ke konzervativnímu postupu. U této klasifikace a návrhu volby léčebného postupu zdůrazňujeme, že se jedná o doporučení orientační, které není všeobecně platné, i když při jeho sestavování jsme vycházeli z nejnovějších výsledků studií i analýz zabývajících se touto problematikou.
Závěr
Kvantifikace LSS by měla vycházet z klinického postižení, jeví se přínosná v běžné klinické praxi a napomáhá při volbě optimálního léčebného postupu.
Tíži LSS navrhujeme hodnotit podle tří parametrů – intenzity bolesti stanovené pomocí numerické škály intenzity bolesti, disability hodnocené pomocí Oswestry dotazníku a ušlé vzdálenosti na mechanickém chodníku do vzniku neurogenních klaudikací.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Blanka Mičánková Adamová, Ph.D.
Neurologická klinika
LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: badamova@fnbrno.cz
Přijato k recenzi: 12. 3. 2013
Přijato do tisku: 31. 5. 2013
Sources
1. Postacchini F. Management of lumbar spinal stenosis. J Bone Joint Surg Br 1996; 78(1): 154 – 164.
2. Epstein NE, Maldonado VC, Cusick JF. Symptomatic lumbar spinal stenosis. Surg Neurol 1998; 50(1): 3 – 10.
3. Jaeschke R, Singer J, Guyatt GH. Measurement of health status. Ascertaining the minimal clinically important difference. Control Clin Trials 1989; 10(4): 407 – 415.
4. Hägg O, Fritzell P, Nordwall A. The clinical importance of changes in outcome scores after treatment for chronic low back pain. Eur Spine J 2003; 12(1): 12 – 20.
5. Fritz JM, Delitto A, Welch WC, Erhard RE. Lumbar spinal stenosis: a review of current concepts in evaluation, management, and outcome measurements. Arch Phys Med Rehabil 1998; 79(6): 700 – 708.
6. Micankova Adamova B, Vohanka S, Hnojcikova M,Okacova I, Dusek L, Bednarik J. Neurological impairment score in lumbar spinal stenosis. Eur Spine J 2013; 22(8): 1897 – 1906.
7. Bergner M, Bobbitt RA, Carter WB, Gilson BS. The Sickness Impact Profile: development and final revision of a health status measure. Med Care 1981; 19(8): 787 – 805.
8. Ware JE jr, Sherbourne CD. The MOS 36 - item short ‑ form health survey (SF ‑ 36). I. Conceptual framework and item selection. Med Care 1992; 30(6): 473 – 483.
9. Fairbank JC, Couper J, Davies JB, O’Brien JP. The Oswestry low back pain disability questionnaire. Physiotherapy 1980; 66(8): 271 – 273.
10. Roland M, Morris R. A study of the natural history of back pain. Part I: development of a reliable and sensitive measure of disability in low ‑ back pain. Spine 1983; 8(2): 141 – 144.
11. Hägg O, Fritzell P, Romberg K, Nordwall A. The General Function Score: a useful tool for measurement of physical disability. Validity and reliability. Eur Spine J 2001; 10(3): 203 – 210.
12. Stucki G, Daltroy L, Liang MH, Lipson SJ, Fossel AH, Katz JN. Measurement properties of a self ‑ administered outcome measure in lumbar spinal stenosis. Spine 1996; 21(7): 796 – 803.
13. Lassale B, Bitan F, Bex M, Deburge A. Functional results and prognostic factors in the surgical treatment of degenerative lumbar stenosis. Rev Chir Orthop Reparatrice Appar Mot 1988; 74 (Suppl 2): 85 – 88.
14. Farrar JT, Young JP Jr, LaMoreaux L, Werth JL, Poole RM. Clinical importance of changes in chronic pain intensity measured on an 11 - point numerical pain rating scale. Pain 2001; 94(2): 149 – 158.
15. Paice JA, Cohen FL. Validity of a verbally administered numeric rating scale to measure cancer pain intensity. Cancer Nurs 1997; 20(2): 88 – 93.
16. Porter RW. Spinal stenosis and neurogenic claudication. Spine 1996; 21(17): 2046 – 2052.
17. Deen HG jr, Zimmerman RS, Lyons MK, McPhee MC, Verheijde JL, Lemens SM. Test ‑ retest reproducibility of the exercise treadmill examination in lumbar spinal stenosis. Mayo Clin Proc 2000; 75(10): 1002 – 1007.
18. Deen HG jr, Zimmerman RS, Lyons MK, McPhee MC, Verheijde JL, Lemens SM. Measurement of exercise tolerance on the treadmill in patients with symptomatic lumbar spinal stenosis: a useful indicator of functional status and surgical outcome. J Neurosurg 1995; 83(1): 27 – 30.
19. Deen HG, Zimmerman RS, Lyons MK, McPhee MC, Verheijde JL, Lemens SM. Use of the exercise treadmill to measure baseline functional status and surgical outcome in patients with severe lumbar spinal stenosis. Spine 1998; 23(2): 244 – 248.
20. Adamova B, Vohanka S, Dusek L. Differential diagnostics in patients with mild lumbar spinal stenosis: the contributions and limits of various tests. Eur Spine J 2003; 12(2): 190 – 196.
21. Nagler W, Hausen HS. Conservative management of lumbar spinal stenosis. Identifying patients likely to do well without surgery. Postgrad Med 1998; 103(4): 69 – 88.
22. Okoro T, Qureshi A, Sell B, Sell P. The accuracy of assessment of walking distance in the elective spinal outpatients setting. Eur Spine J 2010; 19(2): 279 – 282.
23. Schulte TL, Schubert T, Winter C, Brandes M, Hackenberg L, Wassmann H et al. Step activity monitoring in lumbar stenosis patients undergoing decompressive surgery. Eur Spine J 2010; 19(11): 1855 – 1864.
24. Baker D, Pynsent P, Fairbank J. The Oswestry Disability Index revisited. In: Roland J, Jenner J (eds). Back pain: New Approaches to Rehabilitation and Education. Manchester, UK: Manchester University Press 1989 : 174 – 186.
25. Suarez ‑ Almazor ME, Kendall C, Johnson JA, Skeith K, Vincent D. Use of health status measures in patients with low back pain in clinical settings. Comparison of specific, generic and preference‑based instruments. Rheumatology (Oxford) 2000; 39(7): 783 – 790.
26. Taylor SJ, Taylor AE, Foy MA, Fogg AJ. Responsiveness of common outcome measures for patients with low back pain. Spine 1999; 24(17): 1805 – 1812.
27. Fairbank JC, Pynsent PB. The Oswestry Disability Index. Spine 2000; 25(22): 2940 – 2953.
28. Mičánková Adamová B, Hnojčíková M, Voháňka S,Dušek L. Oswestry dotazník, verze 2.1a – výsledky u pacientů s lumbální spinální stenózou, srovnání se starší verzí dotazníku. Cesk Slov Neurol N 2012; 75/ 108(4): 460 – 467.
29. Mičánková Adamová B. Hodnotící škály a vyšetření na mechanickém chodníku. In: Mičánková Adamová B (ed). Lumbální spinální stenóza. 1st ed. Praha: Galén 2012 : 45 – 68.
30. North American Spine Society. Evidence Based Clinical Guidelines for Multidisciplinary Spine Care: Diagnosis and treatment of degenerative lumbar spinal stenosis (revised 2011) [on-line]. Available from URL: http:/ / www.spine.org/ Documents/ LumbarStenosis11.pdf.
31. Amundsen T, Weber H, Nordal HJ, Magnaes B, Abdelnoor M, Lilleas F. Lumbar spinal stenosis: conservative or surgical management? A prospective 10‑year study. Spine 2000; 25(11): 1424 – 1435.
32. Atlas SJ, Keller RB, Wu YA, Deyo RA, Singer DE. Long‑term outcomes of surgical and nonsurgical management of lumbar spinal stenosis: 8 to 10 year results from the maine lumbar spine study. Spine 2005; 30(8): 936 – 943.
33. Malmivaara A, Slätis P, Heliövaara M, Sainio P, Kinnunen H, Kankare J et al. Surgical or nonoperative treatment for lumbar spinal stenosis? A randomized controlled trial. Spine 2007; 32(1): 1 – 8.
34. Slätis P, Malmivaara A, Heliövaara M, Sainio P, Herno A, Kankare J et al. Long‑term results of surgery for lumbar spinal stenosis: a randomised controlled trial. Eur Spine J 2011; 20(7): 1174 – 1181.
35. Weinstein JN, Tosteson TD, Lurie JD, Tosteson AN, Blood E, Hanscom B et al. Surgical versus nonsurgical therapy for lumbar spinal stenosis. N Engl J Med 2008; 358(8): 794 – 810.
36. Weinstein JN, Tosteson TD, Lurie JD, Tosteson A, Blood E, Herkowitz H et al. Surgical versus nonoperative treatment for lumbar spinal stenosis four‑year results of the Spine Patient Outcomes Research Trial. Spine 2010; 35(14): 1329 – 1338.
37. Kovacs FM, Urrútia G, Alarcón JD. Surgery versus conservative treatment for symptomatic lumbar spinal stenosis: a systematic review of randomized controlled trials. Spine 2011; 36(20): E1335 – E1351.
38. Siebert E, Prüss H, Klingebiel R, Failli V, Einhäupl KM, Schwab JM. Lumbar spinal stenosis: syndrome, diagnostics and treatment. Nat Rev Neurol 2009; 5(7): 392 – 403.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2013 Issue 5
- Advances in the Treatment of Myasthenia Gravis on the Horizon
- Memantine in Dementia Therapy – Current Findings and Possible Future Applications
- Memantine Eases Daily Life for Patients and Caregivers
-
All articles in this issue
- Wilsonova nemoc
- Nová antikoagulancia v prevenci kardioembolických iktů u pacientů s nevalvulární fibrilací síní
- Homocysteín a sclerosis multiplex
- Kvantifikace postižení u pacientů s lumbální spinální stenózou
- Multiformní glioblastom – přehled nových poznatků o patogenezi, biomarkerech a perspektivách léčby
- Současné možnosti využití magnetické rezonance v diagnostice normotenzního hydrocefalu
- Neurologické komplikace dengue – možné nebezpečí pro střední Evropu
- Přesnost farmakogenetických algoritmů pro výpočet denní dávky warfarinu
- Interrater variabilita v hodnocení míry atrofie hipokampů pomocí Scheltensovy škály
- Porovnání peroperační radiační expozice při otevřené a miniinvazivní transpedikulární fixaci hrudní a bederní páteře
- Test 3F Dysartrický profil – normativní hodnoty řeči v češtině
- Operační léčba syndromu supinátorového kanálu
- Strategie diagnostiky, terapie a dispenzarizace pacientů s hemangioblastomy v CNS z pohledu neurochirurga
- Synkopy, hluchota a slepota u karcinomu prsu – kazuistika
- Gitelmanův syndrom provázený manifestní tetanií – kazuistika
- Konzumace marihuany jako rizikový faktor ischemické cévní mozkové příhody – kazuistika
- Tumoriformní varianta roztroušené sklerózy – dvě kazuistiky
- Souběžný výskyt mutace v genu ZNF9 (myotonická dystrofie typu 2) a v genu CLCN1 (myotonia congenita) v jedné rodině – kazuistika
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Wilsonova nemoc
- Multiformní glioblastom – přehled nových poznatků o patogenezi, biomarkerech a perspektivách léčby
- Tumoriformní varianta roztroušené sklerózy – dvě kazuistiky
- Test 3F Dysartrický profil – normativní hodnoty řeči v češtině