Vplyv druhu polyméru na liberáciu chlórhexidínu z hydrogélu
Influence of the kind of polymer on chlorhexidine liberation from hydrogel
The aim of this paper was to select the optimal polymer for the formulation of the model drug chlorhexidine dichloride into hydrogel. Two types of biopolymers were used, one of the modified polymers was of herbal origin taken from the group of cellulose derivates – methylcellulose, hydroxyethylcellulose and hydroxypropylcellulose, and the other was of animal origin – chitosan of a medium and a high molecular weight. The polymers were used in a concentration of 2.5% (m/m). Drug liberation was evaluated by the percentage of the drug released into the physiological solution. In addition, the rheological properties of hydrogels were evaluated. Judging the drug release from chitosan hydrogels, the one with the medium molecular weigh was found to be optimal. Contrary to that, from among the hydrogels prepared on the basis of cellulose derivatives, the optimal one was hydroxyethylcellulose hydrogel.
Key words:
chlorhexidinedichloride – polymers – hydrogel – liberation – rheological properties
:
Z. Vitková; M. Žabka; P. Herdová
:
Univerzita Komenského Bratislava, Farmaceutická fakulta, Katedra galenickej farmácie, Slovenská republika
:
Čes. slov. Farm., 2010; 59, 123-126
:
Original Articles
Predmetom tohto príspevku je určiť optimálny polymér pre formuláciu modelového liečiva chlórhexidíniumdichloridu do hydrogélu. Použili sa dva druhy biopolymérov, a to upravené polyméry rastlinného pôvodu zo skupiny derivátov celulózy – metylcelulóza, hydroxyetylcelulóza a hydroxypropylcelulóza – a živočíšneho pôvodu – chitosan o strednej a vysokej molekulovej hmotnosti. Polyméry sa použili v koncentrácii 2,5 % (m/m). Liberácia sa hodnotila percentom uvoľneného liečiva do fyziologického roztoku. Súčasne sa hodnotili aj tokové vlastnosti hydrogélov. Z hľadiska uvoľňovania liečiva z chitosanových hydrogélov sa ako najvhodnejší pre formuláciu hydrogélu ukázal chitosan o strednej molekulovej hmotnosti a z hydrogélov pripravených na báze derivátov celulózy bol to hydroxyetylcelulózový hydrogél.
Kľúčové slová:
chlórhexidíniumdichlorid – polyméry – hydrogél – liberácia – tokové vlastnosti
Úvod
Farmaceutické pomocné látky hrajú dominantnú úlohu pri formulácii liekovej formy. Pri príprave dermálnych polotuhých liekov – hydrogélov dominujú polyméry. Sú to tie pomocné látky, ktoré ovplyvňujú fyzikálno-chemické vlastnosti liekovej formy, vplývajú na uvoľňovanie liečiva, a tým môžu ovplyvniť aj terapeutický efekt. Medzi moderné polyméry patria polosyntetické (hlavne deriváty celulózy) a taktiež aj biodegradovateľné deacetylované deriváty chitínu – chitosan. Sú to pomocné látky, ktoré môžu vplývať na liberáciu liečiva, tokové vlastnosti, pH, stabilitu, rozdeľovací koeficient atď.
Hydrogély sú charakterizované ich schopnosťou absorbovať vodu alebo vodné roztoky. To závisí od viacerých faktorov, ako napr. teplota, pH prostredia a pod. Účinok liečiva závisí do veľkej miery od zvolenej liekovej formy a uvoľňovania liečiva z nej. Preto predmetom tohto príspevku je výber druhu polyméru na základe liberácie chlórhexidíniumdichloridu z hydrogélu. Kritériom pre hodnotenie bolo kumulované uvoľnené množstvo liečiva vyjadrené percentuálne v jednotlivých časových intervaloch.
Prvú skupinu upravených (polosyntetických) prírodných polymérov reprezentovali deriváty celulózy – metylcelulóza, hydroxyetylcelulóza a hydroxypropylcelulóza. Vlastnosti týchto éterov celulózy, najmä ich napučiavanie a rozpustnosť závisia od priemerného stupňa substitúcie. To znamená od počtu éterifikovaných OH skupín v glukopyrazónovej jednotke. Samozrejme, ich vlastnosti sú závislé aj od druhu substitúcie. Dôležitú úlohu hrá aj stupeň polymerizácie, ktorý udáva počet glukopyrazónových jednotiek v molekule.
Metylcelulóza je neiónový éter celulózy, ktorý sa dobre rozpúšťa v chladnej vode. Gély tvorí po zamiešaní v chladnej vode státím najmenej 30 minút. Postupne sa gél vyčíri. Metylcelulóza je kompatibilná s mnohými liečivami, je povrchovo aktívna, je dobrým spojivom pri výrobe granulátov a jej hydrogély sa používajú ako masťový základ.
Hydroxyetylcelulóza je hydrofilnejšia ako metylcelulóza, vlastnosti však má podobné. Pri vyšších teplotách koaguluje, rozpúšťa sa dobre v chladnej vode. Slizy hydroxyetylcelulózy sú vhodné na stabilizovanie heterogénnych disperzných systémov a využívajú sa aj pri obaľovaní tabliet. Gély sa používajú ako masťový základ.
Hydroxypropylcelulóza je tiež rozpustná v chladnej vode, jej hydrogély sú citlivé na teplotu, vyššie teploty môžu spôsobiť rozrušenie gélovej štruktúry 1). Zdanlivá viskozita hydroxypropylcelulózových gélov sa zvyšuje so zvyšujúcou sa molekulovou hmotnosťou a koncentráciou polyméru. Tento derivát sa používa aj ako spojivo v tabletách, alebo na vytvorenie rezervoáru v transdermálnych terapeutických systémoch 2, 3). Hydrogély pripravené z hydroxypropylcelulózy sú známe s rôznymi liečivami ako piroxikamom 4), dikolfenakom sodným 5) a indometacínom 6).
Uvedené deriváty celulózy majú vo farmaceutickej praxi široké použitie. Sú to spojivá, filmotvorné látky, zahusťovadlá adhezívnych gélov, uplatňujú sa pri príprave mikrokapsulí, sú stabilizátormi v emulziách a lociónoch, zvyšujú viskozitu očných liekov a v neposlednom rade pri formulácii dermálnych polotuhých liekov, v tomto prípade hydrogélov 7 – 9).
Druhou skupinou biopolymérov, ktorej vplyv na liberáciu sa hodnotí, je chitosan. Vyrába sa z odpadu pri spracovaní morských živočíchov, ich lastúr, pórovitých schránok tela bezstavovcov atď. Je to binárny polysacharid, ktorý obsahuje dve jednotky N-acetyl-D-glukosamínu a D-glukosamín, ktorý sa získava čiastočnou deacetyláciou chitínu. Ide o katiónový polymér. Tieto neúplne deacetylované frakcie chitosanu sa hodia na formuláciu hydrogélov. Prehľad vlastností a údajov o použití chitosanu vo farmácii je uvedený v práci 10). Vo farmácii má chitosan rozsiahle uplatnenie. Používa sa ako rozvoľňovadlo, enhancer, gélotvorná látka, filmotvorná látka, mukoadhezívny polymér, prostriedok na hojenie rán. Jednou z dôležitých jeho vlastností je aj možnosť optimalizácie disolučných profilov ťažko rozpustných liečiv 11–13).
Príspevok je zameraný na prípravu hydrogélov polotuhej konzistencie, ktoré majú vhodné reologické vlastnosti a použitie pri príprave dermálnych polotuhých liekov.
POKUSNÁ ČASŤ
Použité chemikálie
Chlórhexidíniumdichlorid SL1 (CHX) – (Imperial Chemical Industries, Geshire, GB); metylcelulóza (Methylcellulosum SL1 (MC), Hercules, USA), Natrosol® (Hydroxyethylcellulosum SL1 (HEC), Hercules, USA); Klucel® MCS (Hydroxypropylcellulosum SL1 (HPC), Hercules, USA); chitosan (CHIT) – stredná a vysoká molekulová hmotnosť (Sigma-Aldrich, USA); kyselina mliečna (Interpharm, SR); permeačná membrána (EKOZ s.r.o, SR); fyziologický roztok NaCl.
Použité prístroje
Permeačná aparatúra vyrobená na KGF, FaF, UK, Bratislava, SR; spektrofotometer – Philips Pyll Unicam 8625 Ltd., Cambridge, GB; termostat U 10 – Prüfgeräte-Werk Medingen, D; Viskotester VT 500, Haake Mess – Technik GmbH, Karlsruhe, D., pH meter Metrohm.
Zloženie hydrogélov
Liečivo chlórhexidíniumdichlorid bolo použité v 0,1% (m/m) koncentrácii. Polyméry – gélotvorné látky boli použité vždy v 2,5% (m/m) koncentrácii. Nakoľko chitosan sa rozpúšťa a tvorí gély len v kyslom pH prostredí, použila sa kyselina mliečna v 1% koncentrácii.
Liberácia liečiva chlórhexidíniumdichlorid z hydrogélov
Liberácia liečiva z hydrogélu sa sledovala a hodnotila podľa postupu uvedeného v práci 14) po 15, 30, 45, 60, 90 a 180 minút. Obsah liečiva – chlórhexidíniumdichloridu sa stanovil spektrofotometricky pri λ = 254 nm.
Stanovenie tokových vlastností
Reologické vlastnosti hydrogélov sa stanovili 48 hod. po príprave hydrogélov podľa práce 14).
Stanovenie pH gélov
pH sa meralo 48 hod. po príprave hydrogélov na pH – metri Metrohm, ktorý bol kalibrovaný dvoma referenčnými tlmivými roztokmi: ftalanovým o pH 4 ± 0,02 a boritanovým o pH 9 ± 0,02 pri 20 ± 0,2 °C.
VÝSLEDKY
Na obrázku 1 sú znázornené liberačné profily chlórhexidíniumdichloridu z gélov pripravených na báze derivátov celulózy – metylcelulózy, hydroxyetylcelulózy a hydroxypropylcelulózy. Tieto liberačné profily majú podobný priebeh. Významným výsledkom je, že sú štatisticky významné rozdiely v % uvoľneného liečiva. Najmenej liečiva sa uvoľnilo z gélu pripraveného z MC a najviac z HEC. V prípade MC gélu to bolo po 180 minútach 11 % (m/m) a v prípade HEC je to až 58,2 % (m/m). Je to dôsledok väčšej hydrofility HEC než MC. U obidvoch derivátov celulózy ide o étery celulózy. Liečivo chlórhexidíniumdichlorid je katiónové. V tomto prípade nedochádza k interakcii tohto liečiva s MC a HEC.
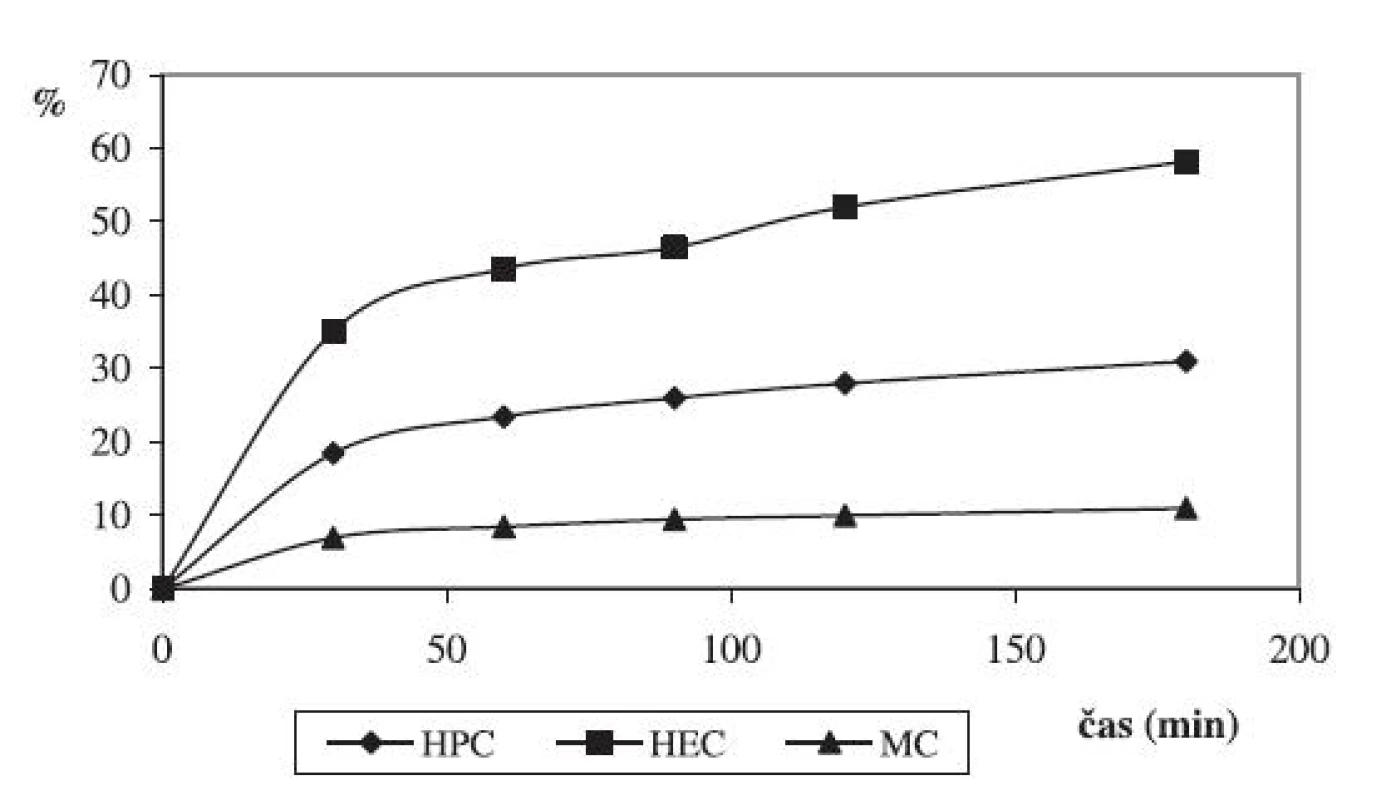
Ako z obrázku1 vidieť, liberačný profil chlórhexidíniumdichloridu z HPC gélov sa nachádza medzi liberačným profilom MC a HEC. Percento uvoľneného liečiva po 180 minútach z HPC gélu je 31 % (m/m).
Pri porovnaní tokových vlastností gélov z derivátov celulózy s liečivom vidieť, že gél MC s liečivom vykazuje plastický tok (obr. 2). Gély HEC a HPC sa reologickými vlastnosťami líšia od MC gélu. HEC (obr. 3) a aj HPC vykazujú časovo závislý tixotropný tok. Tieto reologické vlastnosti sú z hľadiska aplikácie dermálnych polotuhých liekov žiaduce.
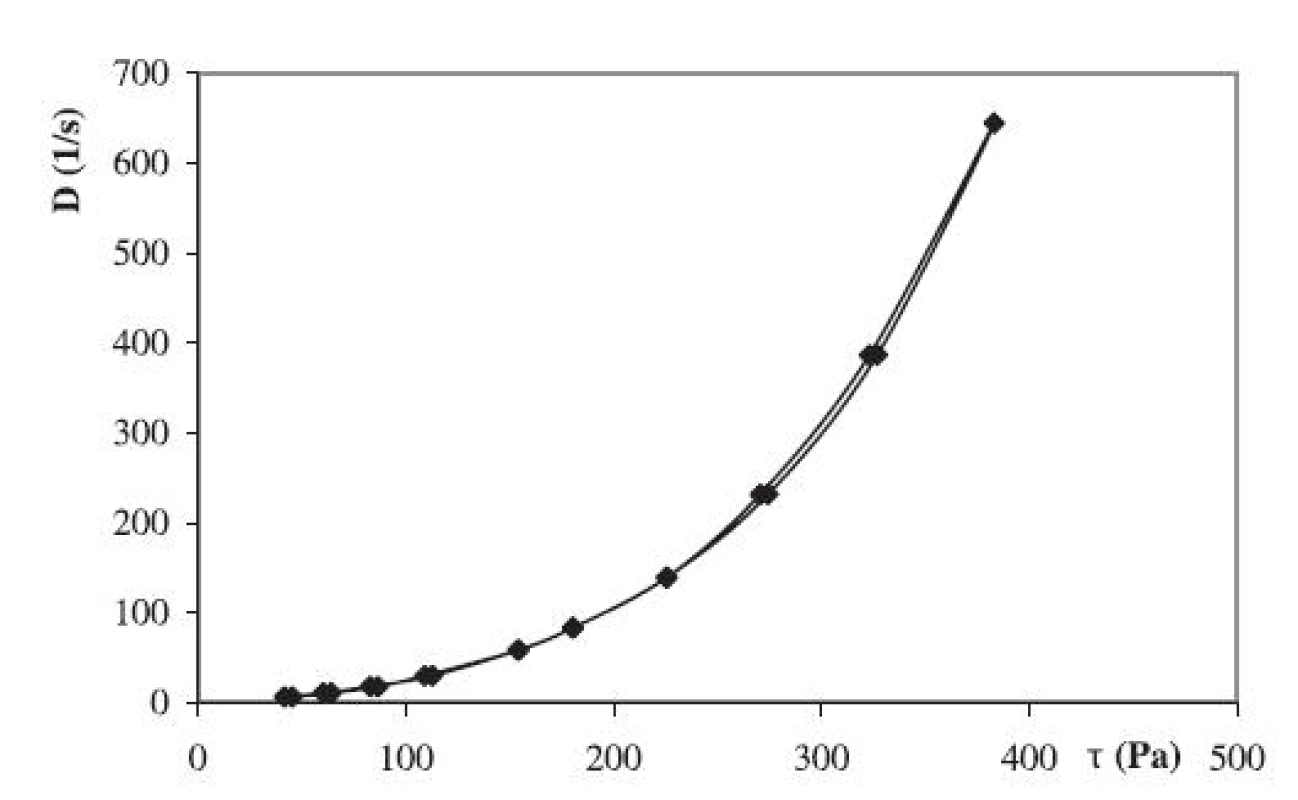
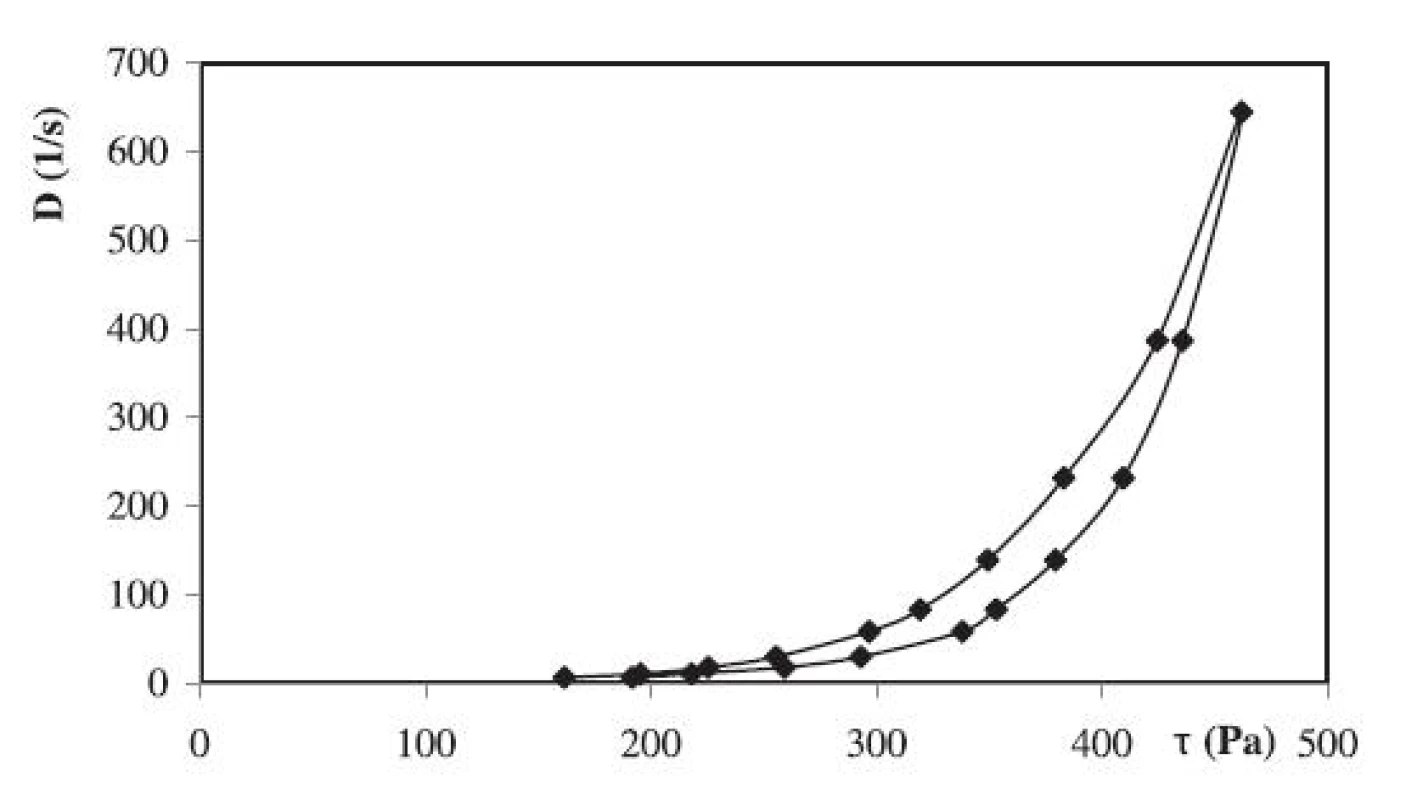
Na základe porovnania výsledkov z liberačných profilov a reologických vlastností v príspevku hodnotených hydrogélov možno konštatovať, že optimálnym polymérom spomedzi MC, HEC a HPC – pre formuláciu hydrogélu s chlórhexidíniumdichloridom je hydroxyetylcelulóza o 2,5 % koncentrácii.
Druhú skupinu biopolymérov, ktoré boli živočíšneho pôvodu, tvorí chitosan o strednej a vysokej molekulovej hmotnosti. Polymér – chitosan má zásaditý charakter, čím sa líši od celulózy a ďalších polysacharidov. Je schopný tvoriť gély pri nízkom pH. Tu dochádza k protonácii aminoskupiny, vlákna polyméru získavajú súhlasný náboj a v dôsledku toho sa odpudzujú a polymér napučiava.
Chitosan, ktorý bol v tejto práci použitý na prípravu gélov, disponuje radom cenných biologických vlastností. Spomenieme len tie vlastnosti, ktoré pre hydrogély s chlórhexidínom sú najdôležitejšie. Je to antimikrobiálny a antimykotický účinok. Ďalšou výhodou tohto polyméru je biokompatibilita a biodegradovaľnosť. Chitosan je vo forme soli s kyselinou chlorovodíkovou zaradený aj do Českého a Európskeho liekopisu.
Faktory, ktoré ovplyvňujú liberáciu liečiva zahŕňajú:
- vlastnosti liečiva (rozpustnosť, molekulová hmotnosť, elektrický náboj),
- vlastnosti a koncentrácia chitosanu (stupeň deacetylácie, molekulovú hmotnosť, pH).
Na obrázku 4 sú znázornené liberačné profily chlórhexidíniumdichloridu z chitosanových hydrogélov o dvoch molekulových hmotnostiach: strednej a vysokej. Ako z obrázku 4 vidieť, už po 30 minútach sa z gélu chitosanu o strednej molekulovej hmotnosti uvoľnilo viac liečiva než z gélu o vysokej molekulovej hmotnosti chitosanu. Rozdiely v uvoľnenom percente liečiva medzi dvomi hydrogélmi boli štatisticky vysoko významné. Po prvej hodine bol rozdiel medzi uvoľneným % chlórhexidíniumdichloridu z hydrogélu so strednou a vysokou molekulovou hmotnosťou chitosanu až 32 %. Pri vysokej molekulovej hmotnosti chitosanu bolo uvoľňovanie liečiva nižšie a pomalšie. Dôležitým výsledkom je, že koncentrácia uvoľneného liečiva v prípade chitosanových hydrogélov od prvej hodiny zostáva na rovnakej úrovni a dosahuje 50 % z celkovej dávky liečiva. V prípade derivátov celulózy 50 % liečiva sa uvoľnilo po 2 hodinách z hydroxyetylcelulózového hydrogélu a u ostatných dvoch derivátoch celulózy množstvo uvoľneného liečiva v porovnaní k hydroxyetylcelulózovému hydrogélu vykazovalo pokles – štatisticky významný rozdiel P > 0,01.
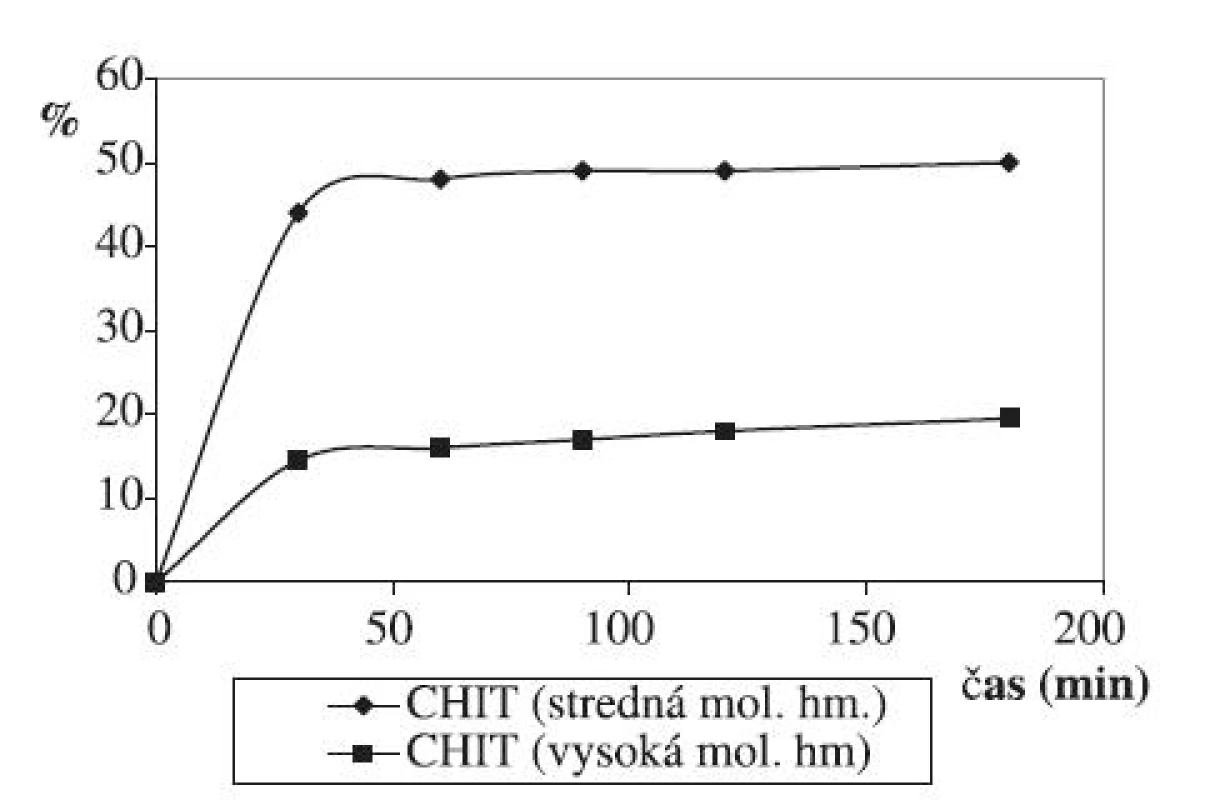
Pri porovnaní tokových vlastností hodnotených chitosanových gélov o rozdielnej molekulovej hmotnosti možno konštatovať, že gél pripravený z chitosanu o strednej aj vysokej molekulovej hmotnosti vykazuje pseudoplastický tok (obr. 5, 6). Výsledky možno zhrnúť nasledovne: Liberácia z gélov na báze derivátov celulózy stúpa v poradí: MC < HPC < HEC a na báze chitosanu vysoká < stredná molekulová hmotnosť.
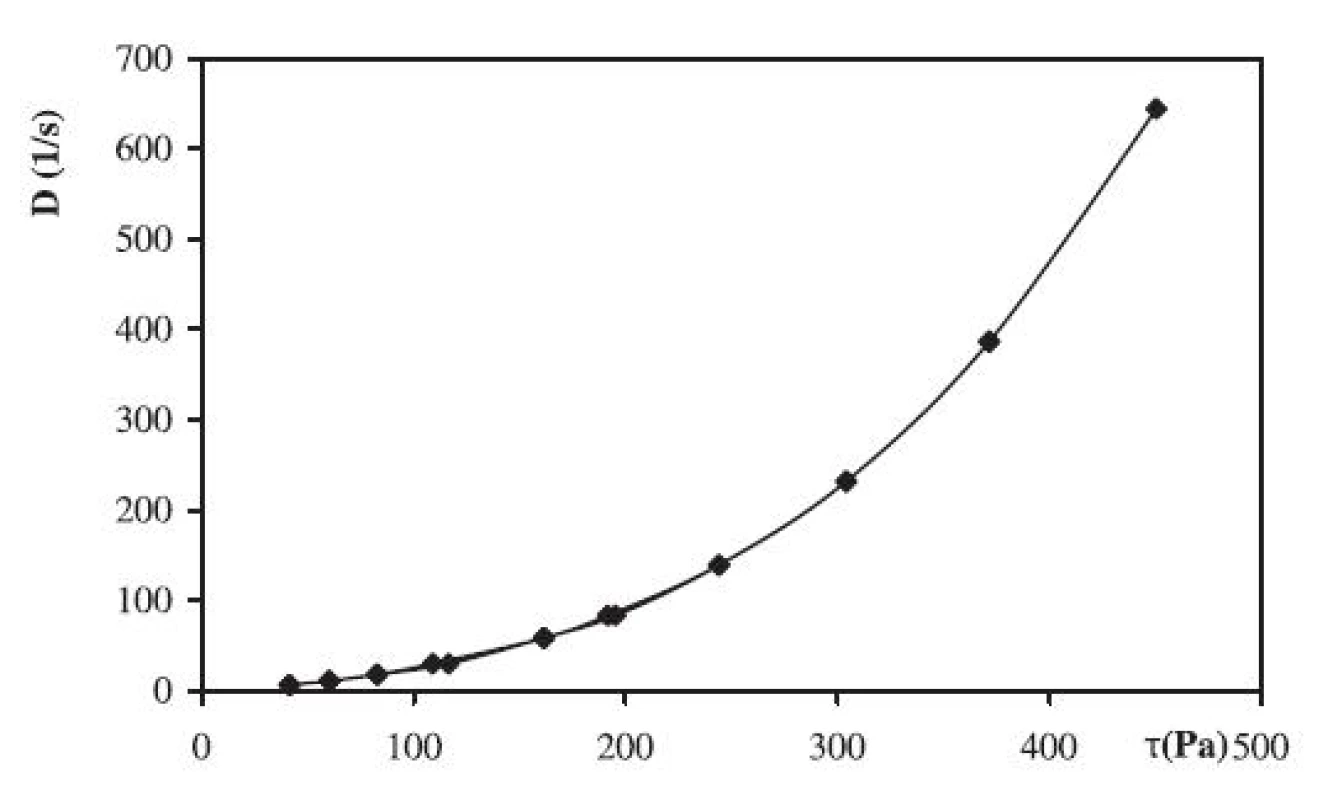
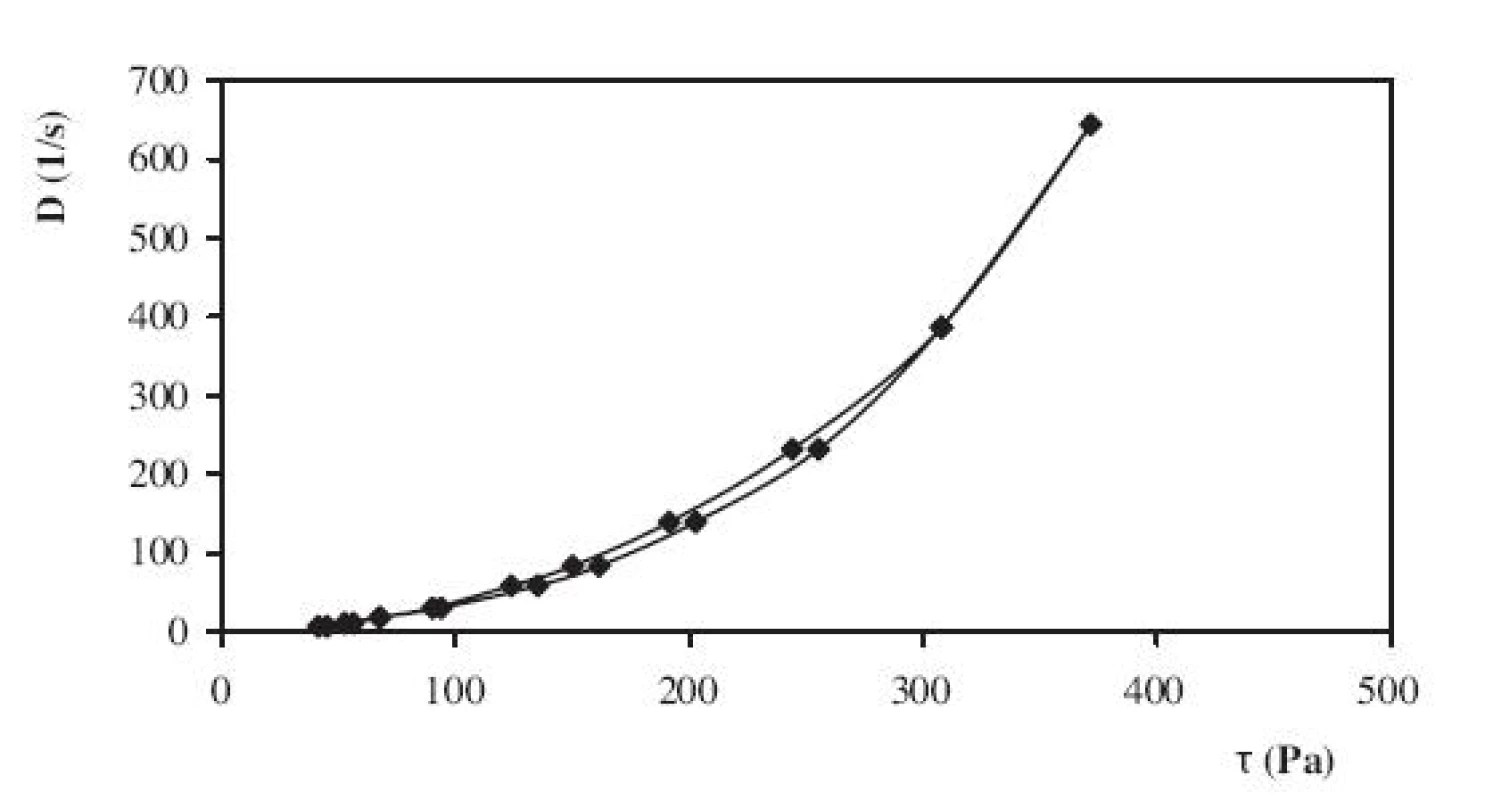
pH chitosanových hydrogélov sa pohybovalo v rozmedzí 5,5–6,2.
Hydrogély chlórhexidíndichloridu na báze MC a chitosanu o strednej a vysokej molekulovej hmotnosti vykazujú pseudoplastický tok a na báze HEC, HPC tixotropný tok.
Molekulová hmotnosť chitosanu sa pohybuje medzi 10–1400 kDA a ovplyvňuje liberáciu liečiva. Ako vidieť pri vyššej molekulovej hmotnosti chitosanu bolo uvoľňovanie chlórhexidíniumdichloridu nižšie, to znamená pomalšie.
Na základe získaných výsledkov možno konštatovať, že z hľadiska liberácie chlórhexidínu sa ako najvhodnejší polymér pre formuláciu hydrogélu javí chitosan o strednej molekulovej hmotnosti a hydroxyetylcelulóza.
Tento výskum bol podporený grantom VEGA č. 1/0320/08.
Adresa
pre korešpondenciu:
PharmDr.
Petra Herdová
Katedra
galenickej farmácie FaF UK
Odbojárov
10, 832 32 Bratislava, SR
e-mail:
herdova@fpharm.uniba.sk
Sources
1. Hirsh, S. G., Spontak, R. J.: Temperature – dependent property development in hydrogels derived from hydroxypropylcellulose. Polymer, 2002; 43, 123–129.
2. Ramachandran, S., Chen, S., Etzler, F.: Rheological charakterization of hydroxypropylcellulose gels. Drug Dev. Ind. Pharm., 1999; 25, 153–161.
3. Sinha, R. D., Rohera, B. D.: Comparative evaluation of rate of hydration and matrix erosion of HEC and HPC and study of drug release from their matrices. Eur. J. Pharm. Sci., 2002; 16, 193–199.
4. Rafiee-Tehrani, M., Mehramizi, A.: In vitro release studies of piroxicam from oil-in-water creams and hydroalcoholic gel topical formulations. Drug Dev. Ind. Pharm., 2000; 26, 409–414.
5. Vitková, Z., Šubová, M., Zbudilová, J., Cirbusová, E., Čižmárik, J.: Hodnotenie farmaceutickej dostupnosti nesteroidného antireumatika z hydrogélov. Farm. Obzor, 2003; 72, 197–200.
6. Fujii, M., Shiozawa, K., Watanabe, Y., Matsumoto, M.: Effect of phosphatidylcholine on skin permeation of indometacin from gel prepared with liquid paraffin and hydrogenated phospholipid. Int. J. Pharm., 2001; 222, 57–64.
7. Rabišková, M.: Moderní lékové formy pro orální a perorální aplikaci. Bratislava: Farmaceutická fakulta UK, 2009, 175.
8. Bajerová, M., Gajdziok, J., Dvořáčková, K., Masteiková, R., Kollár, P.: Polosyntetické deriváty celulosy jako základ hydrofilních gelových systémů. Čes. slov. Farm., 2008; 57, 63–69.
9. Donald L. Wise: Handbook of pharmaceutical controlled release technology. New York: Marcel Dekker Inc., 2000, 3–30.
10. Kopecký, F., Kopecká, B., Semjanová, O.: Vlastnosti chitosanu a sorpce měďnatých iontu z roztoku síranu měďnatého na chitosan. Čes. slov. Farm., 2002; 51, 134–139.
11. Varshosaz J., Jaffari F., Karimzadeh S.: Development of bioadhesive chitosan gels for topical delivery of lidocaine. Sci. Pharm., 2006; 74, 209–223.
12. Ammar, H.O., Salama, H.A., El-Nahhas, S.A., Elmotasen, H.: Design and evaluation of chitosan films for transdermal delivery of glimepiride. Curr. Drug Deliv., 2008; 5, 290–298.
13. Khoo, C. G., Frantzich, S., Rosinski, A., Sjöström, M., Hoogstraate, J.: Oral gingival delivery system from chitosan beds with hydrophilic polymers. Eur. J. Pharm. Biopharm., 2003; 55, 47–56.
14. Vitková, Z., Herdová, P., Šubová, M., Šimunková, V.: Formulácia chlórhexidínu do hydrogélov. Čes. slov. Farm., 2009; 58, 116–118.
Labels
Pharmacy Clinical pharmacologyArticle was published in
Czech and Slovak Pharmacy

2010 Issue 3
-
All articles in this issue
- Analytical methods for the determination of selected psychopharmaceuticals
- Pyrazinecarboxylic acid derivatives as effective abiotic elicitors of isoflavonoids production
- Influence of the kind of polymer on chlorhexidine liberation from hydrogel
- A comparison of the retardation effects of natural matrix-forming polymers and the synthetic polymers Kollicoat SR and Eudragit NE
- Effects of aluminium chloride on cell growth and production of coumarins in cell suspension cultures of Angelica archangelica L.
- Czech and Slovak Pharmacy
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Analytical methods for the determination of selected psychopharmaceuticals
- A comparison of the retardation effects of natural matrix-forming polymers and the synthetic polymers Kollicoat SR and Eudragit NE
- Influence of the kind of polymer on chlorhexidine liberation from hydrogel
- Pyrazinecarboxylic acid derivatives as effective abiotic elicitors of isoflavonoids production
