Úspěšná léčba krvácení z aortoezofageální píštěle metalickým samoexpandibilním stentem
Successful treatment of bleeding from aortoesophageal fistula with a metallic self-expandable stent
We present a case of a 70-year-old patient diagnosed with acute bleeding from an aortoesophageal fistula, which was treated by endoscopic insertion of a self-expandable stent. Although the haemostasis was successful, the patient died from complications. Aortoesophageal fistula is a rare cause of upper gastrointestinal bleeding with high mortality and morbidity. Thoracic aortic aneurysm is the most common aetiology among other causes such as oesophageal carcinoma, foreign body ingestion, trauma or iatrogenic causes. It is an urgent condition that has often lethal consequences, especially due to a symptoms-free period followed by a massive haemorrhage. Nowadays, the diagnostic standard is computed tomography with angiography. The therapeutic solution consists in either a one-step (surgery) or two-step approach (endovascular treatment). However, the mortality from of aortoesophageal fistula is still high and requires multidisciplinary team collaboration to ensure a well-chosen therapeutic approach, and management of septic complications.
Key words:
aortoesophageal fistula – endoscopy – self-expandable metallic stent – gastrointestinal bleeding
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Submitted: 13. 3. 2018
Accepted: 4. 6. 2018
Authors:
E. Evinová 1; O. Urban 2; D. Kučera 3; P. Fojtík 1; J. Krátký 4; T. Málek 5; Přemysl Falt 1
Authors‘ workplace:
Centrum péče o zažívací trakt, Vítkovická nemocnice a. s., Ostrava
1; II. interní klinika – gastroenterologie a geriatrie LF UP a FN Olomouc
2; Vaskulární centrum, Vítkovická nemocnice a. s., Ostrava
3; Radiologické oddělení, Vítkovická nemocnice a. s., Ostrava
4; Anesteziologicko-resuscitační oddělení, Vítkovická nemocnice a. s., Ostrava
5
Published in:
Gastroent Hepatol 2018; 72(3): 217-220
Category:
doi:
https://doi.org/10.14735/amgh2018217
Overview
Prezentujeme kazuistiku 70leté pacientky, u které bylo diagnostikováno akutní krvácení z aortoezofageální píštěle, které bylo řešeno zavedením samoexpandibilního metalického stentu a po stabilizaci následným zavedením stentgraftu do aortálnímu oblouku. I přes úspěšné dosažení hemostázy pacientka podlehla komplikacím. Aortoezofageální píštěl je jednou z vzácných příčin krvácení z horního gastrointestinálního traktu. Je zatížena vysokou mortalitou i morbiditou. Nejčastější etiologií je hrudní aneuryzma, mezi další patří nádory jícnu, cizí těleso v jícnu, trauma či iatrogenní důvod. Jedná se o urgentní stav, který má často letální následky, zejména pro různě dlouhé bezpříznakové období, po kterém následuje masivní krvácení. Zlatým diagnostickým standardem je dnes počítačová tomografie s angiografií. Terapeutické řešení zahrnuje jednostupňový (operační řešení) nebo dvoustupňový přístup (endovaskulární terapie). Mortalita aortoezofageální píštěle je však stále vysoká a vyžaduje multioborovou spolupráci, vhodně zvolený terapeutický přístup i zvládnutí septických komplikací.
Klíčová slova:
aortoezofageální píštěl – endoskopie – metalický samoexpandibilní stent – krvácení do gastrointestinálního traktu
Úvod
Aortoezofageální (AE) píštěl je vzácná příčina krvácení do horního gastrointestinálního traktu, s vysokou mortalitou a morbiditou [1]. I přes pokročilé diagnostické a léčebné možnosti je dopad píštěle často letální. Někteří pacienti se prezentují typickými symptomy, které byly popsány jako Chiariho triáda (dysfagie anebo bolest lokalizovaná uprostřed hrudníku, krvácení do trávicí trubice a následné masivní krvácení po bezpříznakovém období) [1–2]. Jedná se o urgentní stav, který vyžaduje okamžité řešení. Hrudní aneuryzma je nejčastější etiologií primární AE píštěle [3], další zahrnují vznik AE píštěle po požití cizího tělesa, penetrující karcinom jícnu, trauma nebo tuberkulózu [4–6]. Nicméně vzhledem k akutnímu průběhu je AE píštěl často diagnostikována až post mortem [1–2].
Popis případu
Žena, 70 let, léčena s arteriální hypertenzí, bez dalších sledovaných interních onemocnění či významných operací, byla přijata na jiné pracoviště pro komplikovaný průběh divertikulitidy s rozvojem septického stavu a ileu. Pacientka byla přijata na jednotku intenzivní péče, byla zahájena antibiotická a probiotická terapie, rehydratace. Nicméně stav progredoval do ileózního stavu, který si vyžádal operační řešení s ileostomií. Pacientka byla pro následný syndrom multiorgánové dysfunkce přeložena na anesteziologické a resuscitační oddělení (ARO), kde byla poskytnuta komplexní péče, vč. antibiotik a antimykotik a umělé plicní ventilace. Po stabilizaci stavu a přechodném zlepšení sepse byla pacientka přeložena k další léčbě na naše pracoviště. Průběh hospitalizace byl však 15. den komplikován hematemézou. Byla provedena akutní ezofagogastroduodenoskopie na lůžko ARO, která identifikovala zdroj masivního arteriálního krvácení v horním jícnu. Zdroj byl ošetřen naložením čtyř hemoklipů (Resolution® Clip, Boston Scientific). Po 8 hod došlo k recidivě. Druhá endoskopie byla provedena na endoskopickém sále za přítomnosti ARO týmu. Verifikovalo se masivní krvácení v horním jícnu v místě tlaku aortálního oblouku (obr. 1). V časové tísni u pacientky v hemoragickém šoku bylo rozhodnuto o zavedení celopotaženého metalického stentu (Boston Scientific Wallflex jícnový, délka do 120 mm, průměr 18/23) (obr. 2). K objasnění etiologie zdroje krvácení byla během hodiny urgentně v průběhu hodiny doplněna CT angiografie hrudníku, která zobrazila pseudoaneuryzma s AE píštělí (obr. 3) mezi atypicky pravostranně uloženou descendentní aortou a jícnem. Po konzultaci angiologického týmu byla provedena angiografie, a to přibližně 24 hod po druhé endoskopii, přístupem z levého třísla se zobrazením aortálního oblouku a potvrzením AE píštěle. Stav byl řešen zavedením stentgraftu (stentgraft Thoracit Variant 28/160 mm Captivia) do sestupného raménka aortálního oblouku s píštělí a překrytím ústí píštěle (obr. 4). Celkový časový odstup od počátků příznaků do zavedení stentgraftu do aortálního oblouku byl asi 36 hod. Prodloužení způsobila zejména nestabilita pacientky a snaha o maximální úpravu koagulačních parametrů.
Fig. 1. Emergency esophagogastroduodenoscopy – massive bleeding at the level of aortic arch, treated with hemoclips.
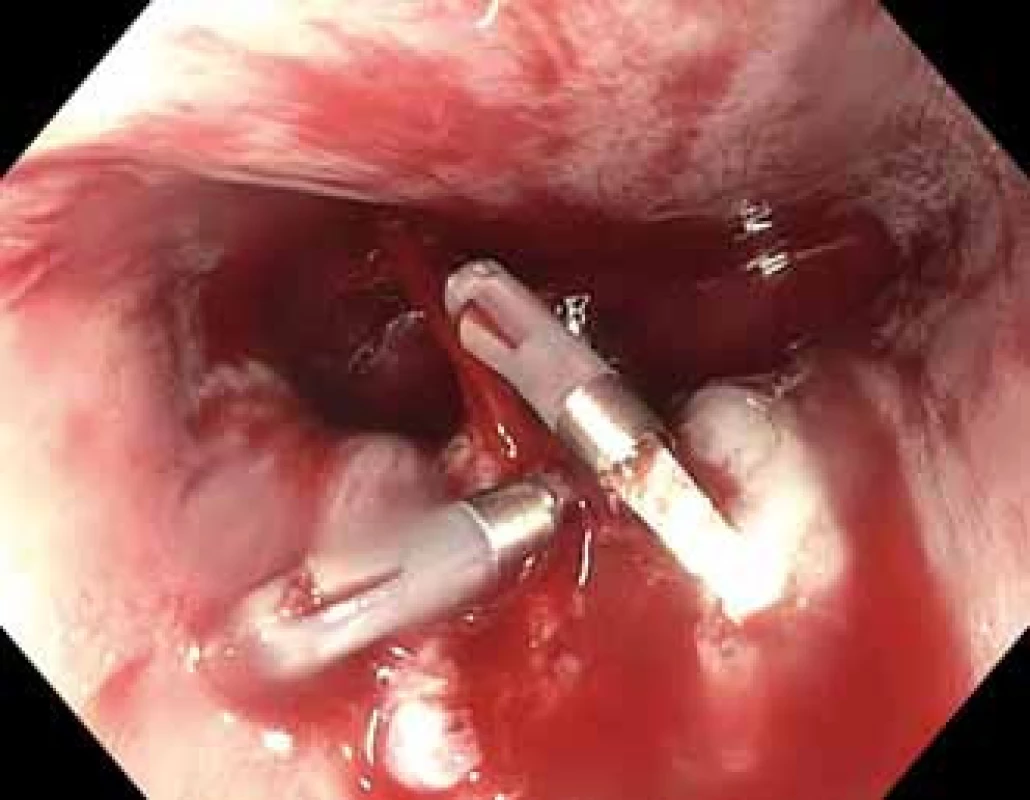
Fig. 2. Self-expandable metallic stent covering the source of bleeding.
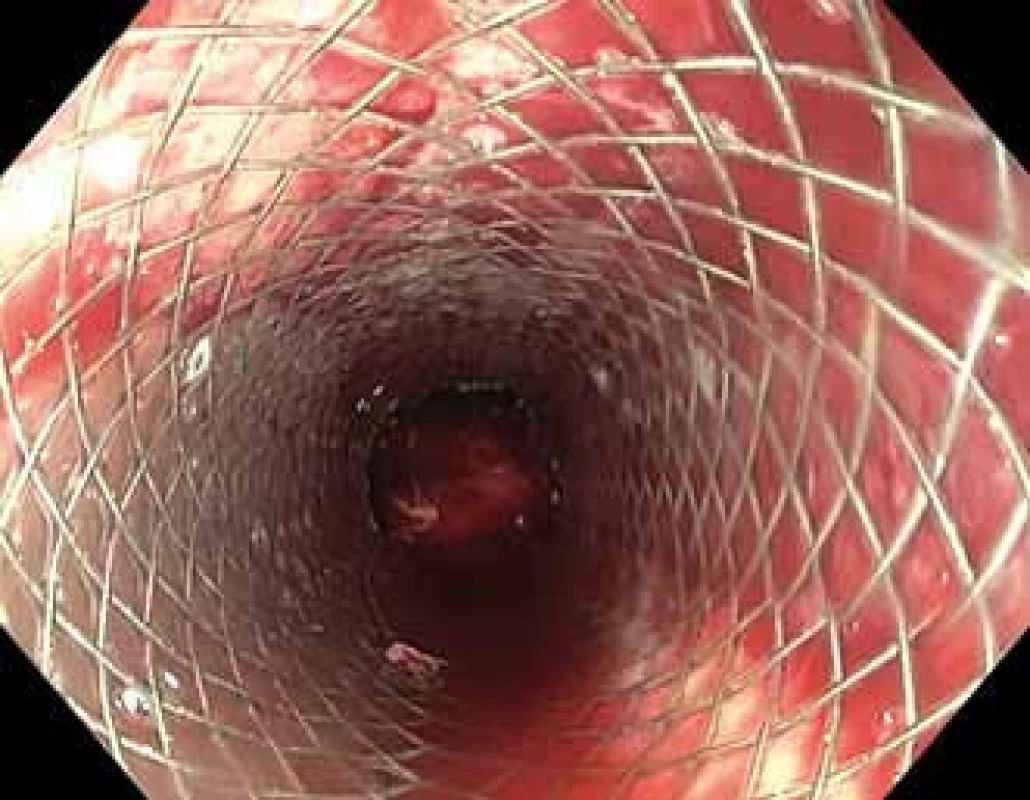
Fig. 3. Location of fistula at the level of the metallic stent (marked by an arrow).
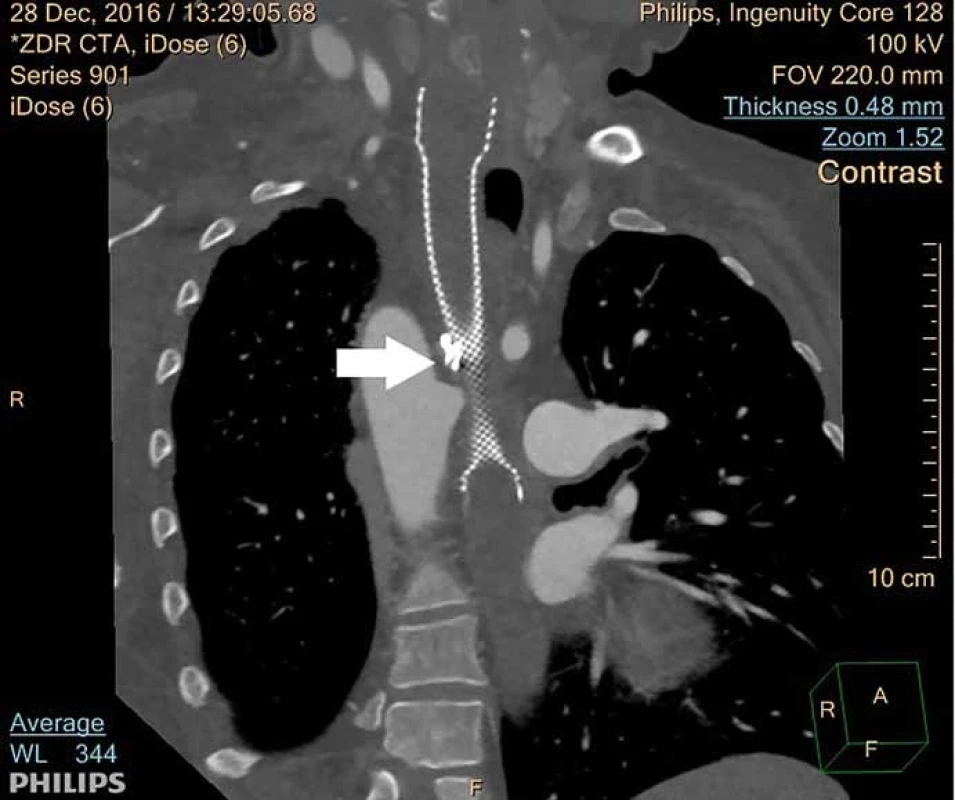
Fig. 4. Stent graft to the descending thoracic aorta.
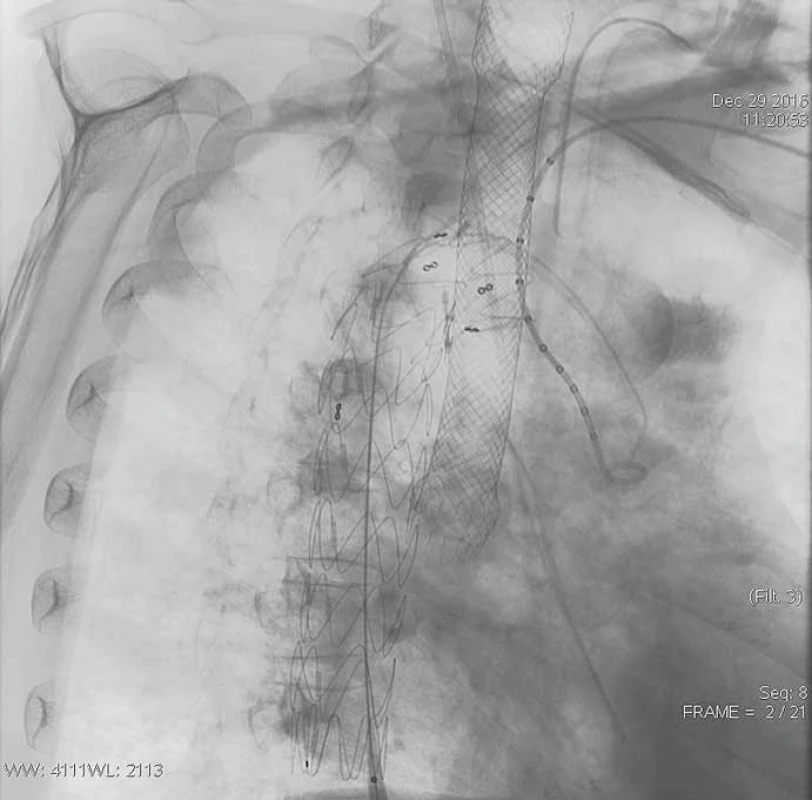
U naší pacientky se zvažovala zejména infekční etiologie při chronickém septickém stavu. Další léčba pokračovala na ARO, pacientka byla klinicky bez známek recidivy krvácení. Metalický jícnový stent byl endoskopicky extrahován 6. den od jeho zavedení. I přes dosažení hemostázy se stav pacientky nelepšil, přetrvávala nutnost umělé plicní ventilace. Septický stav progredoval, a to zejména při recidivě divertikulitidy, močové infekci a počínající plicní infekci – břišní intervence pro celkový stav pacientky a nestabilitu chirurgem tedy nebyla indikována. Po 25 dnech od první urgentní endoskopie a celkově 29. den hospitalizace byla pacientka akutně resuscitována pro asystolii a podlehla komplikacím. Septický stav byl také určen jako základní příčina smrti post mortem. Kauzální spojitost s předpokládanou infekční etiologií nebyla objasněna – potvrdila se však dextropozice aortálního oblouku s AE píštělí.
Diskuze
AE píštěl je vzácné, život ohrožující onemocnění, které tvoří méně než 10 % všech aortoenterických píštělí [4]. Je definována jako abnormální komunikace mezi jícnem a aortou. AE píštěl je způsobena vysokým tlakem aortální krve, což se projeví krvácením do jícnu anebo naopak – méně častěji – obsah jícnu pronikne do aorty [1]. Podle příčiny rozdělujeme AE píštěle na primární a sekundární. Hrudní aneuryzma je nejčastější etiologií primární AE píštěle [3]. Další příčiny jsou vznik AE píštěle po požití cizího tělesa, penetrující karcinom jícnu, trauma nebo tuberkulóza [4–6]. Sekundární etiologie AE píštěle zahrnuje iatrogenní etiologii, a to např. jako stav po předcházející operaci jícnu či aorty anebo jako komplikace aortální protézy [7,8]. AE píštěl, a to jak primární, tak sekundární, se může prezentovat rozmanitými symptomy. Jsou popsány klinické příznaky nazvané Chiariho triáda (dysfagie anebo bolest uprostřed hrudníku, krvácení do trávicí trubice, masivní krvácení po bezpříznakovém období) [8–10]. Ne u všech se ale tato triáda prezentuje v kompletní formě. Největším literárně popsaným souborem je Hollanderova studie z roku 1991, která popisuje více než 500 případů AE píštěle – je tak dosud nejcitovanějším zdrojem souhrnu literatury o této problematice. Autor popsal příznaky pacientů následovně: 59 % mělo bolesti na hrudi, 45 % dysfagii, 65 % krvácení, 45 % kompletní Chiariho triádu [3].
Vzhledem k dostupnosti a vysokému rozlišení je dnes zlatým diagnostickým standardem počítačová tomografie s angiografií [11]. V našem případě bylo první podezření vysloveno na základě endoskopického vyšetření u pacientky s hematemézou. Rozhodnutí o terapii je vždy nutné zvážit individuálně s přihlédnutím na průběh onemocnění.
Stran terapie je v současnosti při vhodných anatomických podmínkách preferována endovaskulární léčba pomocí stentgraftu, a to zejména díky menší invazivitě a menšímu riziku komplikací [12]. Další možností je chirurgická terapie, a to buď resekcí infikovaného segmentu aorty a rekonstrukcí cévní protézou [12–14], anebo extraanatomicky vedeným bypassem, pokud není přítomno masivní krvácení. Operační řešení však může mít také své komplikace, a to zejména infekční, např. mediastinitidu s eventuální následnou sepsí [12,14].
U naší nemocné nás průběh onemocnění vedl k dvoustupňovému řešení. Nejdříve byla v akutní fázi provedena ezofagogastroduodenoskopie se zavedením metalického stentu, kterým se překrylo ústí píštěle, a bylo tak dosaženo hemostázy. Po hemodynamické stabilizaci byl stav řešen zavedením stentgraftu do aortálního oblouku.
V literatuře se jednostupňový přístup, a tedy otevřená operace, považuje za standardní řešení [15]. Vzhledem k časté hemodynamické nestabilitě pacientů se však poslední dobou preferuje spíše dvoustupňový přístup, a to zejména u pacientů s vysokým rizikem komplikací při otevřené operaci [14]. Mortalita a morbidita AE píštěle je i v současné době vysoká, závisí zejména na zvolení terapeutického přístupu a na efektivním zvládnutí septických komplikací, dále samozřejmě na funkčním stavu pacienta a časnosti diagnostiky a v neposlední řadě na úspěšnosti stentování.
Jako lékaři tedy čelíme několika výzvám – primárně lokalizaci zdroje krvácení a identifikaci etiologie, a poté správné volbě terapie od endoskopické zástavy po až po arteriální a jícnovou rekonstrukci. Dalším problémem je zvládnutí sepse při infekci mediastina, která bývá druhou nejčastější příčinou úmrtí hned po krvácení.
Závěr
Kazuistika popisuje úspěšné řešení akutního krvácení způsobeného AE píštělí pomocí zavedení celopotaženého jícnového stentu. Zavedení stentu získalo čas pro hemodynamickou stabilizaci nemocné a následné endovaskulární řešení pomocí stentgraftu.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 13. 3. 2018
Přijato: 4. 6. 2018
MUDr. Eva Evinová
Centrum péče o zažívací trakt
Vítkovická nemocnice, a. s.
Zalužanského 1192/ 15 703 84 Ostrava
Sources
1. Heckstall RL, Hollander JE. Aortoesophageal fistula: recognition and diagnosis in the emergency department. Ann Emerg Med October 1998; 32 (4): 502–505. doi: 10.1016/s0196-0644 (98) 70182-9.
2. Gomes SI, Campos FP, Martines BM et al. Primary aortoesophageal fistula: a rare cause of acute upper gastrointestinal bleeding. Autops Case Rep 2011; 1 (4): 57–63. doi: 10.4322/acr.2011.018.
3. Hollander JE, Quick G. Aortoesophageal fistula: a comprehensive review of the literature. Am J Med 1991; 91 (3): 279–287. doi: 10.1016/0002-9343 (91) 90129-L.
4. Lam EC, Brown JA, Whittaker JS. Esophageal foreign body causing direct aortic injury. Can J Gastroenterol 2003; 17 (2): 115–117.
5. Cairols, MA, Izquirdo LM, Barjau E et al. Primary aorto-oesophageal fistula due to oesophageal carcinoma. Report of a successfully managed case. Int Angiol 2000; 19 (3): 290–293.
6. Robbs JV, Bhoola KD. Aorto-oesophageal fistula complicating tuberculous aortitis. A case report. S Afr Med J 1976; 50 (18), 702–704.
7. Hance KA, Hsu J, Eskew T et al. Secondary aortoesophageal fistula after endoluminal exclusion because of thoracic aortic transection. J Vasc Surg 2003; 37 (4): 886–888. doi: 10.1067/mva.2003.159.
8. Baron RL, Koehler RE, Gutierrez FR et al. Clinical and radiographic manifestations of aortoesophageal fistulas. Radiology 1981; 141 (3): 599–605. doi: 10.1148/radiology.141.3.7302210.
9. Lukáš K, Žák A. Chorobné znaky a příznaky. Praha: Grada 2010.
10. Krška Z, Zavoral M. Krvácení do gastrointestinálního traktu. Praha: Triton 2007.
11. Tozzi di Angelo I, Malý T, Neoral Č et al. Neobvyklý případ krvácení ze zažívacího traktu. Čes a Slov Gastroent a Hepatol 2009; 63 (4): 177–178
12. Krajíček M, Peregrin H, Roček M et al. Chirurgická a intervenční léčba cévních onemocnění. Praha: Grada 2007 : 149–152.
13. da Silva ES, Tozzi FL, Otochi JP et al. Aortoesophageal fistula caused by aneurysm of the thoracic aorta: successful surgical treatment, case report, and literature review. J Vasc Surg 1999; 30 (6): 1150–1157.
14. Omura A, Yoshida M, Koda Y et al. Surgical management without resection of the oesophagus for aorto-oesophageal fistula secondary to aortic arch aneurysm rupture. Interact Cardiovasc Thorac Surg 2016; 23 (6): 985–987. doi: 10.1093/icvts/ivw239.
15. da Silva ES, Tozzi FL, Otochi JP et al. Aortoesophageal fistula caused by aneurysm of the thoracic aorta: successful surgical treatment, case report, and literature review. J Vasc Surg 1999; 30 (6): 1150–1157.
Labels
Paediatric gastroenterology Gastroenterology and hepatology SurgeryArticle was published in
Gastroenterology and Hepatology
2018 Issue 3
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Spasmolytic Effect of Metamizole
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
- The Importance of Limosilactobacillus reuteri in Administration to Diabetics with Gingivitis
-
All articles in this issue
- Editorial šéfredaktora časopisu
- Digestivní endoskopie
- Cholangiopankreatoskopie – doporučený postup České gastroenterologické společnosti ČLS JEP
- Endoskopická transmurální resekce v léčbě lokálních reziduálních neoplazií tlustého střeva – analýza souboru 19 pacientů
- Případ maligního melanomu metastazujícího do pankreatu
- Úspěšná léčba krvácení z aortoezofageální píštěle metalickým samoexpandibilním stentem
- Migrace samoexpandibilního metalického stentu do drénované pseudocysty po endoskopické pseudocystogastrostomii a jeho endoskopická extrakce
- Adenóm Brunnerových žliaz – zriedkavá príčina krvácania z gastrointestinálneho traktu
- Příspěvek k problematice hepatorenálního poškození a selhání
- Naše zkušenosti s léčbou masivního krvácení u Crohnovy nemoci pomocí anti-TNF terapie
- Intoxikácia Amanita phalloides – stále aktuálny problém?
- Tumorózní atrioezofageální píštěl jako neobvyklý zdroj sepse
- Nový člen redakční rady časopisu
- 40th Czech and Slovak Endoscopic Days 19th Endoscopic Day IKEM
- Výběr z mezinárodních časopisů
- Vistaprep – standard přípravy střeva před koloskopickým vyšetřením
- Srovnání endoskopické slizniční resekce a endoskopické submukózní disekce při léčbě plochých neoplastických lézí konečníku
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Vistaprep – standard přípravy střeva před koloskopickým vyšetřením
- Tumorózní atrioezofageální píštěl jako neobvyklý zdroj sepse
- Intoxikácia Amanita phalloides – stále aktuálny problém?
- Naše zkušenosti s léčbou masivního krvácení u Crohnovy nemoci pomocí anti-TNF terapie
