Současné přístupy k očkování konjugovanou pneumokokovou vakcínou
Current strategy to pneumococcal conjugate vaccine immunization
Streptococcus pneumoniae causes diversiform scale of various diseases in childhood ranging from the most serious invasive like meningitis and septicemias (bacteriemias) through pneumonias up to life as a rule not threatening but all the more frequent acute otitis and sinusitis. Incidence of invasive pneumococcal diseases varies in different countries. Either the mass immunization strategy or risk group strategy are applied in the EU in current situation. However the risk group strategy is only an interlink in transition to the mass strategy. Among the mass European strategies schedules 2+1 or 3+1 are put on. The disadvantage of 2+1 strategy are regrettably in some degree lower antibody levels in sérotypes 6B a 23F, which massively appear in the Czech Republic and introduction of this schedule could limit its effectiveness. Administration of single or two-dose regimens, which are economically profitable, however they do not cover the major risks in categories of youngest kids, is not taken into consideration in children above 1 year of age in flat way as in meningococci. In spite of logically only one, recently registered 7-valent pneumoccocal conjugate vaccine asserts in current strategies, very soon we can probably expect conjugate vaccines containing more sérotypes and other protein carriers (10-valent GSK vaccine and 13-valent Wyeth vaccine). In far future are protein vaccines, which will not be type-specific or vaccines with intranasal or oral way of administration.
Key words:
Pneumococci, invasive pneumococcal diseases, acute otitis media, pneumococcal conjugate vaccine, immunogenicity, reactogenicity, mass immunization.
Authors:
R. Prymula 1; K. Pospíšilová 2
Authors‘ workplace:
Fakulta vojenského zdravotnictví UO, Hradec Králové
; Infekční klinika, FN L. Pasteura, Košice
2
Published in:
Prakt. Lék. 2008; 88(2): 104-107
Category:
Of different specialties
Overview
Streptococcus pneumoniae způsobuje v dětském věku pestrou škálu různých onemocnění. Od nejzávažnějších invazívních, jako jsou meningitídy a septikémie (bakteriemie), přes pneumonie až po život zpravidla neohrožující, avšak o to četnější akutní otitidy a sinusitidy. Incidence invazívních pneumokokových onemocnění se v různých zemích liší. V stávající situaci je aplikována v EU buď plošná strategie, nebo očkování rizikových skupin. Očkování rizikových skupin je však pouze mezičlánkem v přechodu na plošnou strategii. V plošných Evropských strategiích se uplatňují schémata 2+1 nebo 3+1. Nevýhodou schématu 2+1 je bohužel poněkud nižší hladina protilátek u sérotypů 6B a 23F, které se v ČR masivně vyskytují, a zavedení tohoto schématu by mohlo účinnost očkování limitovat. U pneumokokových onemocnění se zatím neuvažuje o aplikaci jednodávkových či dvoudávkových schémat plošně jako u meningokoků nad 1 rok věku, která jsou sice ekonomicky výhodná, ale hlavní rizika v kategoriích nejmladších dětí bohužel nekryjí. I když se ve stávajících strategiích uplatňuje logicky pouze jediná, toho času registrovaná 7-valentní konjugovaná vakcína, velmi brzy se pravděpodobně dočkáme konjugovaných očkovacích látek obsahujících vyšší počet sérotypů a jiné proteinové nosiče (vakcíny 10-valentní GlaxoSmithKline a 13-valentní Wyeth). Ve vzdálenější budoucnosti jsou proteinové vakcíny, které nebudou typově specifické, nebo vakcíny s intranazální či orální cestou aplikace.
Klíčová slova:
pneumokoky, invazívní pneumokoková onemocnění, akutní zánět středního ucha, pneumokoková konjugovaná vakcína, imunogenita, reaktogenita, plošné očkování.
Incidence pneumokokových onemocnění
Pneumokoková onemocnění patří k nejvýznamějším původcům morbidity a mortality celosvětově. Jejich původce – S. pneumoniae – byl objeven již v roce 1881. Jedná se o gram-pozitivní bakterii, která se vyskytuje v párech jako diplokok buď samostatně, nebo v krátkých řetízcích. Pneumokoky jsou fakultativně anaerobní a většina je kryta povrchovým polysacharidem. Právě ten umožňuje jejich typizaci. Dnes je popsáno na 40 skupin a identifikováno přes 90 různých sérotypů pneumokoků. Pouhých 6 skupin z nich odpovídá za přibližně 70 % všech invazívních onemocnění. Invazívní onemocnění jsou ta onemocnění, kde je pneumokok izolován z pů-vodně sterilního prostředí, tedy hlavně meningitidy a bakteriémie. Standardně mezi invazívní onemocnění nepatří pneumonie. Ovšem tam, kde je při pneumonii pozitivní hemokultura, již o invazívním onemocnění hovoříme. Definice pneumokokových onemocnění je stále ještě diskutována a v určitých detailech může doznat ještě drobných změn.
Incidence invazívních pneumokokových onemocnění (IPO) je v Evropských zemích různá. Nejvyšší výskyt je u dětí pod 2 roky věku v regionech Španělska, kde dosahuje hodnoty 174/100 000. Následuje Belgie 104/100 000, Finsko 40/100 000, Dánsko 35/100 000, Německo 19/100 000. Meningitida se vyskytuje přibližně v 0,5 až 2,0 případech na 100 000 dětí v Evropě i USA s mortalitou kolem 23 %. Výskyt pneumokokové bakteriémie kolísá v závislosti na sezóně s maximem v zimních měsících. I když neexistují reprezentativní evropská data o incidenci, na základě studií v Anglii, Švédsku a Dánsku je tuto možno odhadovat mezi 10 až 20 případy na 100 000 dětí mladších 5 let s mortalitou přibližně 20 %.
Incidence pneumonií je ještě vyšší. Finská data hovoří o 5,7 na 1 000 dětí ženského pohlaví pod 5 let věku, respektive 11,2 u mužského pohlaví. Nad 5 let věku klesá na hodnoty kolem 5,4 na 1 000 bez rozdílu pohlaví. V přenosu onemocnění se uplatňuje zejména nosičství pneumokoků v nosohltanu, jehož význam s věkem ale postupně klesá. Tento fenomén potvrzují výrazně vyšší hodnoty nosičství u dospělých v rodinách s dětmi ve srovnání s bezdětnými rodinami. Jakmile dojde k narušení slizniční bariéry dochází k výskytu otitíd či sinusitid, v případě průniku do krevního řečiště dojde k vývoji již zmíněných nepříliš častých, o to však závažnějších invazívních forem onemocnění (1, 2, 3).
Naopak akutní otitída je jedním z nejčastějších dětských onemocnění. Existují práce, které udávají výskyt až u 100 % dětí do 2 let věku, jiní autoři hovoří o 30–60 %. My jsme takto vysoké hodnoty v podmínkách ČR na souboru 5 000 dětí nepotvrdili, avšak i naše hodnota prokazující výskyt klinicky závažných otitid, které vedly k návštěvě pediatra či otorinolaryngologa u 20 % dětí, představuje enormní medicínské a zejmé-na ekonomické břemeno (4).
Zajímavá práce byla publikována belgickými autory v roce 2006. Ukazuje výrazný vliv podhlášenosti na publikovaná epidemiologická data. Naprostá většina údajů pochází totiž z pasívní surveillance a řada případů se do statistik nedostává. Belgická studie dokazuje dvakrát vyšší výsledky, když byla použita metoda aktivní (5). Výrazným způsobem také ovlivňuje výsledky místo, kde se data sbírají. Na příkladu USA je patrna podstatně vyšší záchytnost v hemokulturách ve srovnání s Evropou. Důvodem je odebírání hemokultury již u praktického lékaře narozdíl od nemocničního přístupu v Evropě. V České republice je počet odebíráných hemokultur obecně nízký, což se přímo promítá do nízkých hodnot vykazovaných pneumokokových bakteriemií.
Pneumokokové sérotypy
Pouzdro (kapsula) bakterie S. pneumonie sestává z polysacharidů a vytváří hlavní faktor virulence. Protilátky cílené proti polysacharidům pouzdra chrání proti infekci; typově specifické protilátky se vážou na antigeny pouzdra a opsonizace facilituje fagocytózu.
Většina sérotypů způsobuje závažná onemocnění, ačkoliv relativně omezený počet sérotypů vyvolává většinu invazívních pneumokokových infekcí. Deset nejběžnějších sérotypů odpovídá za přibližně 62 % invazívních onemocnění v celosvětovém měřítku, ačkoliv prevalence jednotlivých sérotypů kolísá v závislosti na lokalitě a věkové kohortě.
V USA sedm nejběžnějších sérotypů izolovaných z krve či cerebrospinálního moku od dětí ve věku <6 let (14, 6B, 19F, 18C, 23F, 4, a 9V) odpovídá za 80 % infekcí, a jsou proto sérotypy v licencované sedmivalentní pneumokokové konjugované vakcíně. Těchto sedm sérotypů však pokrývá v USA pouze 50 % izolátů u osob ve věku >6 let. Sérotypy 1 a 5 tvoří v USA pouze limitované procento invazívních izolátů, avšak v západní Evropě a některých rozvojových zemích jsou mnohem četnější. V USA ve všech věkových skupinách byly sérotypy 1 a14 nejčastěji izolovány z krve, sérotypy 6, 10 a 23 z mozkomíšního moku a sérotypy 3, 19 a23 ze středouší. (6, 7) Sérotyp 1 odpovídá za 7,2–9,5 % invazívních izolátů z Německa, Švédska, Itálie, Řecka a Slovinska. Tento fenomén je relativně nový, ačkoliv Dánsko, Španělsko aVelká Británie ho pozoruje již od 80tých let (1, 2, 6).
Během let 1981–1999 10 sérotypů (1, 4, 6A, 6B, 7F, 9V, 14, 18C, 19F, 23F) způsobilo 82 % invazívních infekcí udánských dětí. Nebyly pozorovány rozdíly v distribuci sérotypů ani v čase, ani podle pohlaví. Je odhadováno, že 7-, 9-, a11-valentní pneumokokové konjugované vakcíny pokryjí pravděpodobně kolem 60 %, 70 %, respektive 80 % všech invazívních infekcí udánských dětí ve věku 0–6 let. (3). Ve Švýcarsku bylo ve studii z let 2001 až 2004 analyzováno celkem 2 388 izolátů z IPO. Dominovaly sérotypy 1, 4, 5, 7F, 8, 9V a14 (8).
V České republice bylo v letech 1996–2003 analyzováno 1 553 vzorků od pacientů sIPO. V klinických vzorcích (krev, likvor, sekční materiál, punktát aaspirát dolních dýchacích cest, bronchoalveolární laváž, sputum) patřily knejčastějším kmeny sérotypů 3, 19F, 9V, 23F, 1, 14 a 4. Mimo typy společné pro kmeny izolované od pacientů všech věkových kategorií (1, 3, 6A, 9V, 14, 19F a23F) patřily navíc mezi nejčastější u pacientů 0–2 roky sérotyp 6B, u pacientů >2–5 let sérotypy 4, 6B, 7F a 18C a u pacientů >5 let typy 4, 7F, 8, 9N, 10A a11A.
Pneumokoková konjugovaná 7valentní vakcína pokrývá 63,1 %, 62,3 % a34,3 % sérotypů identifikovaných u 152 pacientů 0–2 roky, respektive 168 pacientů >2–5 let, respektive 1 233 pacientů >5 let věku. Zahrnuje 38,3 % sérotypů zjištěných u 1 055 kmenů izolovaných z krve, likvoru a sekčního materiálu od pacientů bez rozdílu věku. Ve sledovaném období vzrostlo procento kmenů obsahujících některý ze sérotypů zahrnutých ve vakcíně ze 45,5 % na 70,6 % u pacientů 0–2 roky, z 54,3 % na 73,0 % u pacientů >2–5 let az21,8 % na 38,7 % u pacientů starších 5 let; z30,0 % na 39,4 % u kmenů izolovaných z krve, likvoru a sekčního materiálu. Analogický trend byl zjištěn i při sledování prevalence séroskupin. Na tomto posunu má podíl i plynulý nárůst kmenů sérotypů 4 (z 1,0 % na 8,9 %) a 9N (z 0,0 % na 5,9 %) (9).
Na základě výše uvedené distribuce sérotypů byla hodnocena potenciální účinnost vakcíny proti invazívním onemocněním. Nejvyšší byla v USA, kde vakcína pokrývala 89–93 % séroskupin. Epidemiologické údaje z let 1988–2003 svědčí otom, že v Evropě se pokrytí liší v jednotlivých zemích. V severní části Evropy je pokrytí, stanovené u dětí pod 2 roky věku nižší, v jižní části Evropy je pokrytí vyšší. V důsledku toho sedmivalentní vakcína bude pokrývat 60 % až 86 % kmenů izolovaných z IPO u evropských dětí ve věku pod 2 roky. U evropských dětí ve věku 2–5 let by měl Prevenar pokrývat 50 % až 75 % izolovaných kmenů odpovědných za invazívní pneumokoková onemocnění. Snížení incidence IPO pozorované u starších dětí může být částečně důsledkem přirozeně získané imunity (1, 2, 10).
Možnosti aplikace různých strategií očkování pneumokokovou vakcínou
Přes poměrně širokou škálu terapeutických možností se ukazuje, že budoucnost celosvětového boje s pneumokokovými nákazami je jednoznačně v prevenci. Donedávna sice dominovaly terapeutické postupy pomocí antibiotik uinvazívních onemocnění aparacentézy a/nebo opět antibiotika uakutních otitíd, narůstající rezistence ve světě však vede k silnému tlaku na úpravu terapeutických přístupů zejména učetně se vyskytujících aklinicky ne tolik závažných jednotek, jako je klasická akutní otitída.
Polyvalentní polysacharidové vakcíny doporučované pro starší a chronicky nemocné však nejsou účinné u dětí do dvou let věku. Toto omezení může být překonáno nakonjugováním polysacharidů na proteinový nosič, který obsahuje T-buněčné epitopy.
První konjugovaná pneumokoková vakcína byla licensována v USA jako 7-valentní vakcína konjugovaná na protein CRM197. V roce 2000 byla zavedena do plošného schématu v USA. Efekt dlouhodobého používání konjugovaných pneumokokových vakcín je zcela nepopiratelný. V USA došlo k poklesu rizika inavazivního pneumokokového onemocnění o79 %, návštěvy ul ékaře s diagnózou otitis media poklesly o 118 na 1 000. Výskyt otitis media se pak snížil o10 % u dětí pod 2 roky věku a o 4 % u dětí v kohortě 2–5 let. Došlo k výrazné redukci výskytu a cirkulace sérotypů krytých vakcínou, a tedy zejména rezistentních sérotypů.
Déledobější zkušenosti však přinášejí iněkteré negativní poznatky, které je potřebné v dlouhodobém horizontu vyřešit. Spektrum pokrytí jednotlivých sérotypů není optimální. Zejména je vsoučasnosti zdůrazňována role sérotypů 1 a 5, které se v řadě zemí výrazně podílejí na incidenci invazivních pneumokokových onemocnění. Problémem se jeví i fenomén replacementu (kompetitivní náhrady sérotypů krytých vakcínou jinými pneumokokovými sérotypy, kompenzačním nárůstem netypovatelných hemofilů či případně jiných patogenů). Tento efekt zatím není výrazný a neohrožuje podstatu vakcinace, neboť nové pneumokokové sérotypy nejsou výrazně patogenní a i jejich rezistence je omezená. Jedinou výjimkou je sérotyp 19A. Jeho prudký nárůst v USA ukazuje, že pro příští generace vakcín je potřeba pokrýt i tento sérotyp společně s již zmíněnými sérotypy 1 a 5. U indikace proti akutní otitidě je třeba pokrýt i netypovatelné hemofily jako druhý nejčastější vyvolávající patogen (11, 12).
Odpůrci plošného očkování tvrdí, že vakcína chrání pouze proti omezenému počtu pneumokokových sérotypů běžných v USA, avšak dle šetření, které probíhalo v ČR v letech 1996–2003, pokrývá sedmivalentní vakcína v ČR 63,1 % sérotypů zjištěných u dětí do 2 let věku, 62,3 % dětí ve věku 2–5 let a 34,3 % u osob starších 5 let (9). Současná data SZÚ (Motlová J., 2007) z let 2000–2006 pro věk 0–1 let hovoří o pokrytí 66 % v kategorii 1–4 roky 65,1 %. Je známo, že pokud je pokrytí nad 60 %, je použití vakcíny indikováno. Rovněž argumentují rovnováhou mezi úbytkem počtu onemocnění vyvolaných sérotypy, proti kterým se očkuje, a nárůstem počtu onemocnění vyvolaných sérotypy, které ve vakcíně zahrnuté nejsou. Tento fakt je velmi účelově prezentován. Náhrada některých sérotypů zejména 19A nemusí být vůbec problémem vakcinace. Zdá se, že tento sérotyp narůstá i tam, kde se vůbec neočkovalo, a není vysvětlitelné ani zavlečením z jiných oblastí. Například nárůst sérotypu 19A v Izraeli a Jižní Korei, kde se konjugovaná pneumokoková vakcína doposud nepoužívala.
Náhrada sérotypem 19A se rozhodně nevyskytuje plošně ani v USA a v Evropě je naprosto minimální. I případná náhrada, která sice může znamenat výrazný procentuální nárůst, je z hlediska absolutních počtů s pozitivním efektem na vakcínou pokryté sérotypy naprosto nesrovnatelná, neboť sérotyp 19A se vyskytoval před nárůstem velmi omezeně. Přesto stávající vakcína není určitě konečným řešením. Průlomové, zejména v indikaci akutních zánětů středního ucha, jsou výsledky českých aslovenských autorů publikované v březnu 2006 v Lancetu. Dvojitě slepá, randomizovaná, multicentrická studie zahrnovala na 5 000 subjektů. Ve sledované skupině byla aplikována kandidátní 11-valentní pneumokoková konjugovaná vakcína (GSK), která využívá tzv. D-protein připravený z povrchových proteinů typovatelných i netypovatelných hemofilů, v tradičním schématu 3, 4, 5 měsíců s booster dávkou mezi 12 až 15 měsícem. V kontrolní skupině byla aplikována vakcína proti virové hepatitidě A.Konkomitantně byla vobou skupinách aplikována vakcína InfanrixHexa. Vakcína prokázala srovnatelnou účinnost proti vakcínou pokrytým sérotypům pnemokoků s vakcínou stávající, ale navíc přibližně 33% účinnost vůči akutnímu zánětu středního ucha bez ohledu na vyvolávající patogen. Tento efekt je 5–6x vyšší než u doposud registrované vakcíny. Jedním z hlavních důvodů je poprvé prokázaná účinnost (35,6 %) proti netypovatelným hemofilům, jakožto druhému nejčastějšímu původci otitid (4). Naopak připravovaná 13-valentní vakcína (Wyeth) má rozšířené spektrum, které pokrývá i problematický sérotyp 19A.
Ve stávající situaci je aplikována v EU buď strategie plošná, nebo očkování rizikových skupin, podobně jako v ČR (tab. 1). Očkování rizikových skupin je však pouze mezičlánkem v přechodu na plošnou strategii nebo, jako v případě Slovenska, nadefinováním velmi širokých skupin pokusem pokrýt velkou část populace, aniž by formálně bylo plošné očkování zavedeno.

Rizikové skupiny vyjmenovává v ČR vyhláška č.537/2006 Sb. O plošném očkování v ČR se uvažuje nejdříve od 1. 1. 2009. Na Slovensku vypadá situace příznivěji a je zde snaha zavést plošné očkování v průběhu roku 2008. V plošných Evropských strategiích se uplatňují schémata 2+1 nebo 3+1. Nevýhodou schématu 2+1 je bohužel poněkud nižší hladina protilátek u sérotypů 6B a 23F, které se v ČR masivně vyskytují, a zavedení tohoto schématu by mohlo účinnost očkování výrazně limitovat. Poslední zprávy však svědčí o tom, že po booster dávce je efekt obdobný u obou schémat. Problém tedy nastává pouze v době mezi termínem aplikace třetí dávky a booster dávkou, kdy u výše zmíněných sérotypů dochází k reálnému poklesu. Tento efekt by se zřejmě neměl projevit uinvazívních onemocnění, ale zdá se, že hladiny protilátek hrají svoji úlohu u pneumonií či jiných neinvazívních pneumokokových onemocnění.
U pneumokokových onemocnění se zatím neuvažuje o aplikací jednodávkových či dvoudávkových schémat plošně jako u meningokoků nad 1 rok věku, která jsou sice ekonomicky výhodná, ale hlavní rizika v kategoriích nejmladších dětí bohužel nekryjí.
Závěr
Očkování proti pneumokokovým nákazám je nepochybně jedním z mála, kde se naprosto reálně zvažuje plošný přístup díky bezpečnosti, snášenlivosti a vysoké účinnosti konjugované vakcíny, nejen na úrovni jednotlivých zemí, kde již v řadě z nich bylo plošně zavedeno, (obr. 1), ale i celosvětově. Hlavním limitujícím faktorem je zatím cena a dostatek vakcíny.
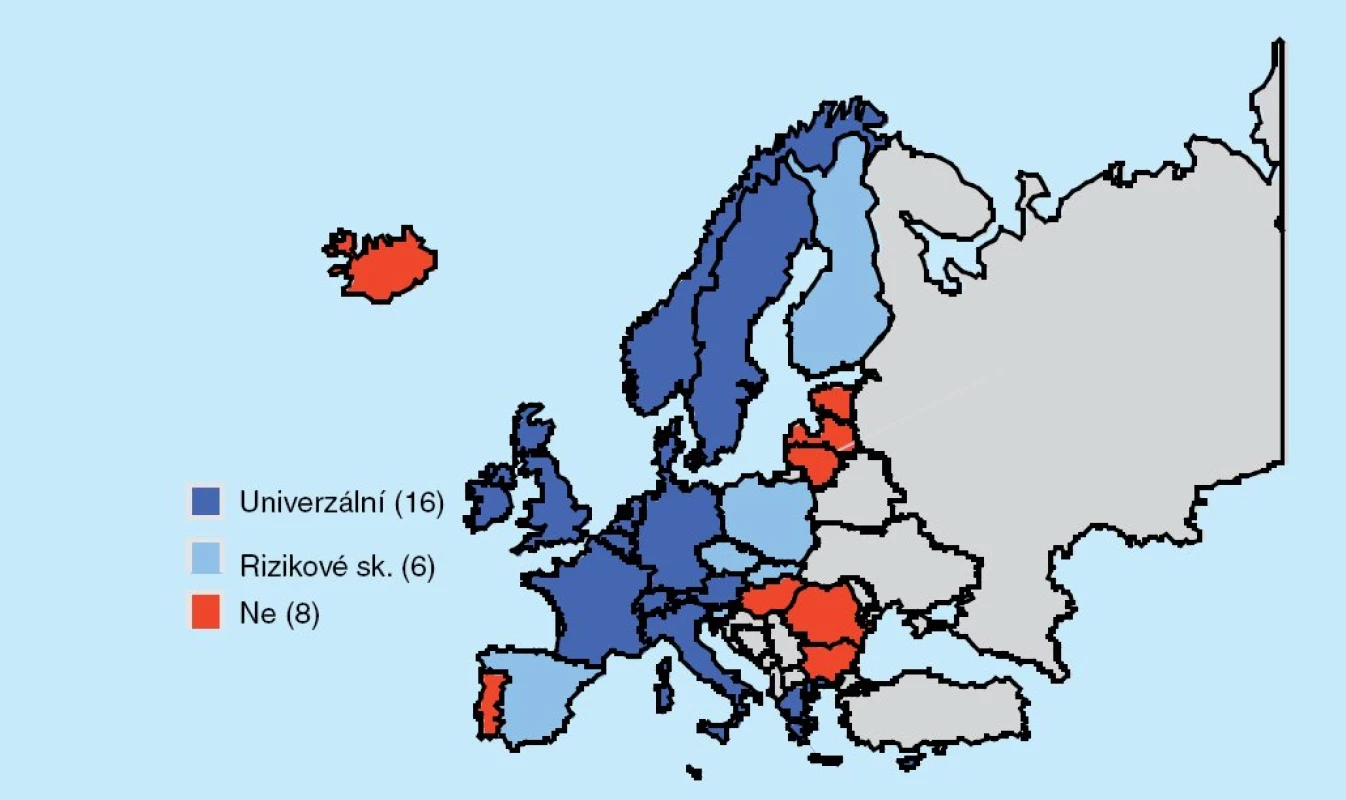
Zkušenosti zemí, kde plošné očkování již bylo zavedeno, ukazují, jak velký dopad má zejména na snížení výskytu invazívních pneumokokových onemocnění, pneumonií, akutních zánětů středního ucha, pozoruhodný je i nepřímý efekt na cirkulaci vakcíně specifických typů pneumokoků u starších věkových skupin díky eliminaci primárních zdrojů. Ve svém důsledku tak dochází k významnému snížení incidence i udospělé populace, která vakcinována není. V EU se diskutuje, zda aplikovat schéma 2+1 nebo 3+1. Řada studií v tuto chvíli ještě probíhá a definitivní doporučení v tomto ohledu není zatím možno vydat.
Prof.MUDr.Roman Prymula, CSc., Ph.D.
Fakulta vojenského zdravotnictví,
Katedra epidemiologie,
Třebešská 1575,
500 01 Hradec Králové,
fax: +495 513 018,
e.mail: prymula @pmfhk.cz
Sources
1. Hausdorff, W.P., Siber, G., Paradiso, P.R. Geographic differences in invasive pneumococcal disease rates and sérotype frequency in young children. Lancet 2001, 357, p. 950-952.
2. Hausdorff, W.P. Invasive pneumococcal disease in children: geographic and temporal variations in incidence and sérotype distribution. Eur. J. Ped. 2002, 161, (Suppl. 2), p. 135-139.
3. Konradsen, H.B., Kaltoft, M.S. Invasive Pneumococcal Infections in Denmark from 1995 to 1999: Epidemiology, Sérotypes, and Resistence. Clinical and Vaccine Imunology 2002, 9, 2, 358-365.
4. Prymula, R., Peeters, P., Chrobok, V. et al. Pneumococcal capsular polysaccharides conjugated to protein D for prevention of acute otitis media caused by both Streptococcus pneumoniae and non-typable Haemophilus influenzae: a randomized double-blind efficacy study. Lancet 2006, 367, p. 740-748.
5. Vergison, A., Tuerlinckx, D., Verhaegen, J., Malfroot, A. For the Belgian Invasive Pneumococcal Disease Study Group: Epidemiologic Features of Invasive Pneumococcal Disease in Belgian Children: Passive Surveillance Is Not Enough. Pediatrics 118, 3, September 2006.
6. Hausdorff, W.P., Bryant, J., Paradiso, P.R., Siber, G.R. Which Pneumococcal Serogroups Cause the Most Invasive Disease: Implications for Conjugate Vaccine Formulation and Use, Part I. Clinical Infectious Diseases, 2000, 30 p. 100-121.
7. Hausdorff, W.P., Bryant, J., Kloek, C., Paradiso, P.R., Siber, G.R. The Contribution of Specific Pneumococcal Serogroups to Different Disease Manifestations: Implications for Conjugate Vaccine Formulation and Use, Part II. Clinical Infectious Diseases 2000, 30, p. 122-140.
8. Kronenberg, A., Zucs, Droz, S., Muhlemann, K. Distribution and Invasiveness of Streptococcus pneumoniae Sérotypes in Switzerland, a Country with Low Antibiotic Selection Pressure,from 2001 to 2004. J. Clin. Microbiol 2006, 44, 6, p. 2032-2038.
9. Motlová J. Distribuce sérotypů a séroskupin Streptococcus pneumoniae u pacientů s invazívními pneumokokovými onemocněními v České republice v letech 1996–2003: podklady pro vakcinační strategii. Epidemiol. Mikrobiol. Imunol. 2005, 1 (54), p. 3-10.
10. Rendi-Wagner, P., Georgopoulos, A., Kundi M., Mutz I., Mattauch M., Nowak, J., Mikolášek A., Vecsei, A., Kollaritsch H. Prospective surveillance of incidence, sérotypes and antimicrobial susceptibility of invasive Streptococcus pneumoniae among hospitalized children in Austria. J. of Antimicrob. Chemoter. 2004, 53, 5, p. 826-831.
11. Eskola, J., Kilpi, T., Palmu, A., Jokinen, J., Haapakoski, J., Herva, E., Takala, A., Kayhty, H., Karma, P., Kohberger, R., Siber, G., Makela, P.H., Lockhart, S., Ecrola, M. Efficacy of a pneumococcal conjugate vaccine against acute otitis media. New Engl J. Med. 2001; 344 (6), p. 403-409.
12. Fireman, B., Black, S., Shinefield, H., Lee, J., Lewis, E., Ray, P. Impact of the pneumococcal conjugate vaccine on otitis media. Pediatr. Infect. Dis. J. 2003, 22 (1), p. 10-16.
Labels
General practitioner for children and adolescents General practitioner for adultsArticle was published in
General Practitioner

2008 Issue 2
- Hope Awakens with Early Diagnosis of Parkinson's Disease Based on Skin Odor
- Memantine Eases Daily Life for Patients and Caregivers
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Advances in the Treatment of Myasthenia Gravis on the Horizon
- Metamizole vs. Tramadol in Postoperative Analgesia
-
All articles in this issue
- Transparentní zodpovědnost (accountability) v medicíně a zodpovědnost etických komisí
- Současné možnosti a problémy antiretrovirové terapie
- Etiopatogeneze autismu z pohledu buněčné a molekulární biologie
- Paměť a její poruchy
- Metalothionein a jeho vztah k protinádorové léčbě na bázi platinových komplexů
- Hodnocení dynamiky transportní funkce a remodelace levé srdeční síně po úspěšné endoskopické mikrovlnné epikardiální izolaci plicních žil. Pilotní studie.
- O lidech, kteří hromadí věci a zvířata
- Současné přístupy k očkování konjugovanou pneumokokovou vakcínou
- Akutní toxická hepatitida po bylinném přípravku
- General Practitioner
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Paměť a její poruchy
- Současné možnosti a problémy antiretrovirové terapie
- O lidech, kteří hromadí věci a zvířata
- Akutní toxická hepatitida po bylinném přípravku
