TRUS/MRI fúzní biopsie prostaty u pacientů nad 65 let – analýza výsledků a komplikací
TRUS/MRI fusion prostate biopsy in patient over 65 years – results and complication rate analysis.
In the recent few years, multiparametric MRI of prostate is used in diagnostics, local staging and in follow-up after radical treatment of prostate cancer. This study presents single-institution results of TRUS/MRI fusion prostate biopsy performed at the department of urology, Oblastní nemocnice Kolín a.s., Czech Republic. Aim of this study is to evaluate the detection rate of prostate cancer using this method and comparison with standard TRUS-guided random prostate biopsy. The secondary aim of this study is complication rate analysis of TRUS/MRI prostate biopsy.
Keywords:
prostate cancer – TRUS-guided prostate biopsy – mpMRI of prostate – PI-RADS v2 – TRUS/MRI fusion biopsy
:
MUDr. Jakub Musil 1; MUDr. Jan Jandejsek; Mba Mba 1; prof. MUDr. Miloš Bro Ák, Ph.D. 2
:
Urologické oddělení Oblastní nemocnice Kolín, a. s.
1; Urologická klinika Fakultní nemocnice Hradec Králové
2
:
Geriatrie a Gerontologie 2019, 8, č. 2: 48-52
:
Original Article
Posledních několik let se v diagnostice karcinomu prostaty uplatňuje multiparametrická MRI prostaty. Její využití je v primární diagnostice, stagingu onemocnění i ve follow-up po radikální léčbě. Tato práce předkládá výsledky cílené TRUS/MRI biopsie prostaty u pacientů nad 65 let věku provedené na urologickém oddělení Oblastní nemocnice Kolín. V práci je zhodnocen záchyt karcinomu touto metodou a porovnání se systematickou biopsií prostaty. Druhým cílem práce je analýza komplikací TRUS/MRI fúzní biopsie.
Klíčová slova:
karcinom prostaty – TRUS biopsie prostaty – mpMRI prostaty – PI-RADS v2 – TRUS/MRI fúzní biopsie
Úvod
Karcinom prostaty je v současné době nejčastějším maligním onemocněním dospělých mužů. Zatímco incidence karcinomu prostaty za posledních 30 let stoupla z 20,89/100 000 obyvatel v roce 1986 na 71,06/100 000 obyvatel v roce 2016, mortalita zůstává po dobu sledování prakticky stejná(12,4 vs. 13,2). Incidence karcinomu prostaty roste s věkem, cca 74 % pacientů s nově diagnostikovaným karcinomem prostaty je starší 65 let (zdroj www.svod.cz). To činí z karcinomu prostaty významný problém jak medicínský, tak i socioekonomický.
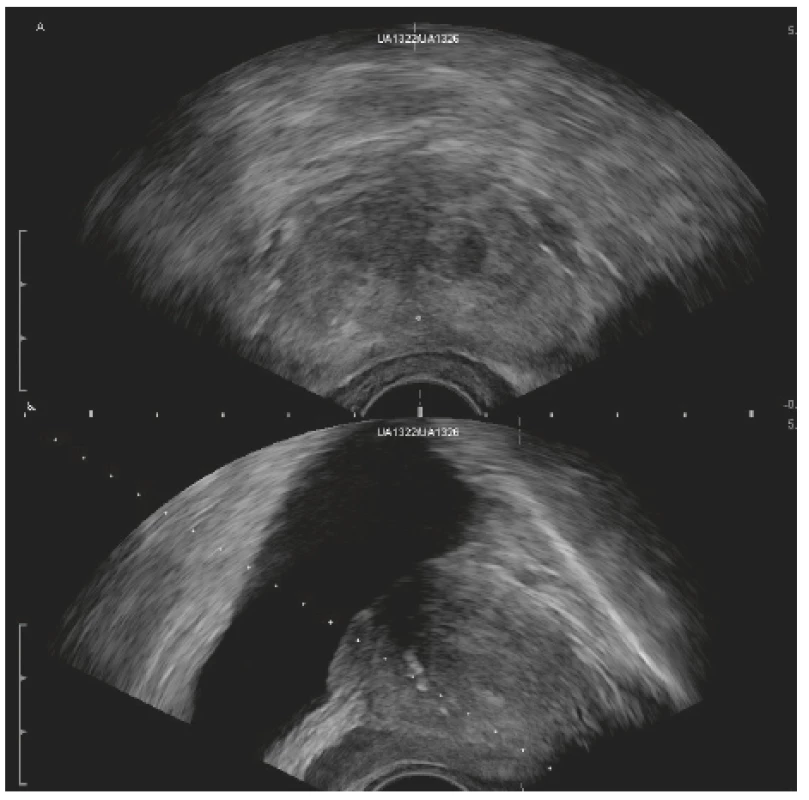
Současná diagnostika karcinomu prostaty je založena na palpačním vyšetření prostaty, hladině prostatického specifického antigenu (PSA) a systematické transrektální biopsii prostaty. Bez histologické verifikace není možné diagnózu karcinomu prostaty stanovit, a tedy ani zahájit odpovídající léčbu. Tento diagnostický algoritmus je však zatížen několika limity. Většina lokalizovaných karcinomů prostaty je nehmatných, tudíž nejsou palpačně zjistitelné. PSA vykazuje vysokou senzitivitu, ale poměrně nízkou specificitu. Pouze okolo 35 % pacientů s hladinou PSA 4–10 ng/ml má v rámci primobiopsie verifikovaný karcinom prostaty, u rebiopsií toto procento ještě dále klesá. Třetím limitem je sama systematická biopsie prostaty. Ta se standardně provádí pod transrektální ultrazvukovou kontrolou (TRUS). Ultrazvuk má pro diagnostiku karcinomu prostaty velmi nízkou senzitivitu a specificitu, umožňuje však detailně zhodnotit anatomii prostaty (obr. 1). Biopsie probíhá „naslepo“ podle předem stanoveného schématu, na základě doporučení zahrnuje 10–12 vzorků. Schémata biopsie prostaty zahrnující odběr většího počtu vzorků (více než 12) pouze nevýznamně zvyšují záchyt karcinomu (1). Vzorky jsou preferenčně odebírány z periferní zóny prostaty. Část karcinomů (zejména z předního fibromuskulárního stromatu, tranzitorní zóny a apexu) tak diagnostice uniká, menší ložiska mohou být bioptickou jehlou minuta, nebo je naopak zachyceno drobné ložisko nesignifikantního karcinomu. Nesignifikantní karcinom je definován Gleasonovým skóre 6, PSA < 10 ng/ml a maximálně 2 pozitivními vzorky v méně než 50 % objemu vzorku. Tyto karcinomy jsou zpravidla neagresivní, navíc jejich případná léčba zvyšuje morbiditu, představuje fyzickou i psychickou zátěž pro pacienty a nevede ke zlepšení prognózy pacientů.
Při snaze o zpřesnění diagnostiky karcinomu prostaty a redukci nadbytečných biopsií lze využít dvou přístupů. Prvním z nich je použití markeru s vyšší specificitou, než je samotné PSA, druhým přístupem je poté využití zobrazovací metody s vyšší senzitivitou a specificitou než samotná transrektální sonografie. V této indikaci se nejčastěji využívá multiparametrické magnetické rezonance prostaty (mpMRI).
Multiparametrická magnetická rezonance prostaty
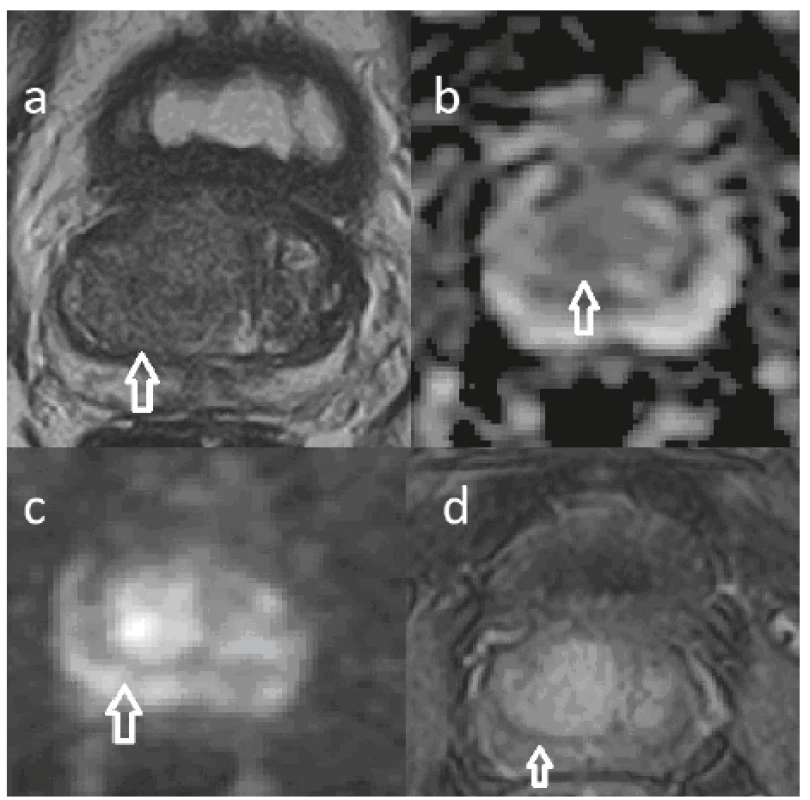
Multiparametrická magnetická rezonance prostaty se skládá z anatomického zobrazení na T2 vážených obrazech a 2, resp. 3 funkčních sekvencí (DWI+ADC mapování, DCE a spektroskopie). Senzitivita vyšetření pro karcinom prostaty v periferní zóně činí 80 %, pro karcinomy v tranzitorní zóně 81 % (2).
T2 vážené zobrazení je základní anatomická sekvence. Je založena na měření obsahu vody v tkáních. Periferní zóna zde vykazuje typicky vysoký signál, centrální zóna a přední fibromuskulární stroma nízký signál a transitorní zóna vykazuje nehomogenní signál smíšené intenzity. Ložiska karcinomu jsou typická sníženým signálem, intenzita signálu koreluje s Gleason skóre (nižší signál u vyšších Gleason skóre).
Difúzně vážené zobrazení (DWI – Diffusion Weighted Imaging) hodnotí difúzi molekul vody v tkáních na základě Brownova pohybu. Ve tkáních s vyšší buněčnou denzitou dochází k restrikci difúze. Na základě měření DWI sekvencí při různých b-hodnotách se vypočítává ADC (Apparent Diffusion Coefficient). Ložiska s restrikcí difúze mají na DWI typicky vysoký signál s korelujícím poklesem signálu na ADC mapě.
Dynamické kontrastní zobrazení (DCE – Dynamic Contrast Enhancement) hodnotí perfúzi tkání. Skládá se z několika po sobě jdoucích T1 vážených zobrazení po podání gadoliniové kontrastní látky. Sleduje se kinetika distribuce kontrastní látky v prostatě, optimálně se subtrakcí pozadí. Karcinom prostaty zde vykazuje časné vychytávání (wash-in) a rychlé vyplavování (wash-out) kontrastu.
Spektroskopie poskytuje informace o metabolickém stavu tkání. Registruje hladiny citrátu a cholinu. Citrát je syntetizován normálním žlázovým epitelem prostaty. Cholin je markerem buněčné proliferace. V normální tkáni nacházíme při spektroskopii vysoké hladiny citrátu a nízké hladiny cholinu. V maligních tkáních se tento poměr mění ve prospěch cholinu, což odráží zvýšený buněčný obrat a ztrátu normální buněčné funkce a struktury tkáně. Spektroskopie je momentálně metodou doplňkovou, v PI-RADS klasifikaci v2 již není zařazena.
V roce 2012 vydala Evropská společnost urogenitální radiologie (ESUR) první guidelines pro MRI prostaty známé jako PI-RADS version 1 (Prostate Imaging And Reporting Data System). PI-RADS v1 byla poté validována v řadě klinických studií. Na základě zkušeností se ukázaly některé limity této klasifikace, což vedlo v roce 2015 k vydání aktualizované klasifikace PI-RADS v2 (3).
PI-RADS hodnocení využívá 5stupňovou škálu, která je založená na hodnocení ložisek v T2WI, DWI a DCE. Výsledná kategorie koreluje s pravděpodobností výskytu signifikantního karcinomu.
Kategorie:
PI-RADS 1 – Velmi nízká (klinicky významný karcinom prostaty je velmi nepravděpodobný)
PI-RADS 2 – Nízká (klinicky významný karcinom je nepravděpodobný)
PI-RADS 3 – Střední (riziko signifikantního karcinomu prostaty je nejasné)
PI-RADS 4 - Vysoká (klinicky významný karcinom je pravděpodobný)
PI-RADS 5 – Velmi vysoká (klinicky významný karcinom je vysoce pravděpodobný)
Techniky cílené biopsie prostaty
Kognitivní TRUS/MRI fúzní biopsie prostaty představuje technicky nejjednodušší formu cílené biopsie prostaty. Nevyžaduje žádné speciální vybavení, díky čemuž je zároveň i nejlevnější a široce použitelnou alternativou k softwarové fúzní biopsii. Na druhou stranu klade největší nároky na zkušenosti a prostorovou orientaci vyšetřujícího. Na základě obrazové dokumentace radiolog zakreslí suspektní ložiska do sektorové mapy dle PI-RADS v2, vyšetřující urolog poté na základě znalosti umístění ložiska odebírá vzorky z popisované oblasti (4).
Softwarová TRUS/MRI fúzní biopsie prostaty představuje technicky sofistikovanější metodu navigované biopsie. Je založena na softwarovém spojení obrazové dokumentace MRI s transrektální sonografií v reálném čase. Umožňuje aplikaci jak transrektálního, tak i transperineálního přístupu.
In-bore MRI biopsie je nejstarší a zároveň nejsložitější systém cílené biopsie. Po vstupním diagnostickém vyšetření mpMRI prostaty postupuje pacient cílenou biopsii prostaty přímo pod MRI kontrolou. K tomu se využívají rychlé sekvence MR fluoroskopie, nejčastěji při transrektálním či transperineálním přístupu. Vyšetření je časově náročné (cca 60–90 minut), probíhá zpravidla v celkové anestezii a je náročné na technické a personální vyšetření. Dalšími nevýhodami jsou náklady spojené s dvěma MRI vyšetřeními a nemožnost provést v rámci vyšetření i systematickou biopsii prostaty. V současné době se in-bore MRI biopsie v České republice neprovádí.
V této práci předkládáme výsledky softwarové TRUS/MRI biopsie prostaty u pacientů starších 65 let provedené na Urologickém oddělení Oblastní nemocnice Kolín, a. s.
Soubor
Od září 2017 do března 2019 jsme na urologickém oddělení Oblastní nemocnice Kolín, a. s., provedli softwarovou TRUS/MRI fúzní biopsii u 145 pacientů, z toho 80 pacientů bylo starších 65 let. V souboru pacientů starších 65 let byla průměrná hodnota PSA 9,96 (0,48–37) ng/ml. U 80 bioptovaných pacientů se ve 20 případech jednalo o primobiopsie, u ostatních 60 se jednalo o rebiopsie (1–6 předchozích biopsií). Průměrný objem prostaty byl 65,5 ml (16–223 ml). Celkem bylo bioptováno 118 ložisek, z toho 44 ložisek PI-RADS 3, 53 ložisek PI-RADS 4 a 21 ložisek PI-RADS 5.
Metody
U všech pacientů byla před biopsií provedena mpMRI prostaty. Většina vyšetření byla provedena na 1,5T přístroji Toshiba Excelart Vantage, menší část vyšetření byla externích, provedených na 1,5T a 3T přístrojích. Všechna vyšetření zahrnovala T1 a T2 vážené sekvence, DWI + ADC a DCE, hodnocena byla dle klasifikačního systému PI-RADS v2. Jako pozitivní nález byla hodnocena ložiska PI-RADS kategorie 3–5. U externích vyšetření bylo provedeno druhé čtení naším radiologem.
Před biopsií byla vyžadována negativní kultivace moči, příprava rekta zahrnovala zavedení glycerinových čípků před vyšetřením. U všech pacientů byla podána antibiotická profylaxe sulfamethoxazolem/trimetoprimem 960 mg po 12 hodinách po dobu 3 dnů, v případě alergie byl podán cefuroxim 500 mg po 12 hodinách po dobu 3dnů. Před biopsií byla vysazena antiagregační a antikoagulační terapie, tolerována byla aplikace LMWH.
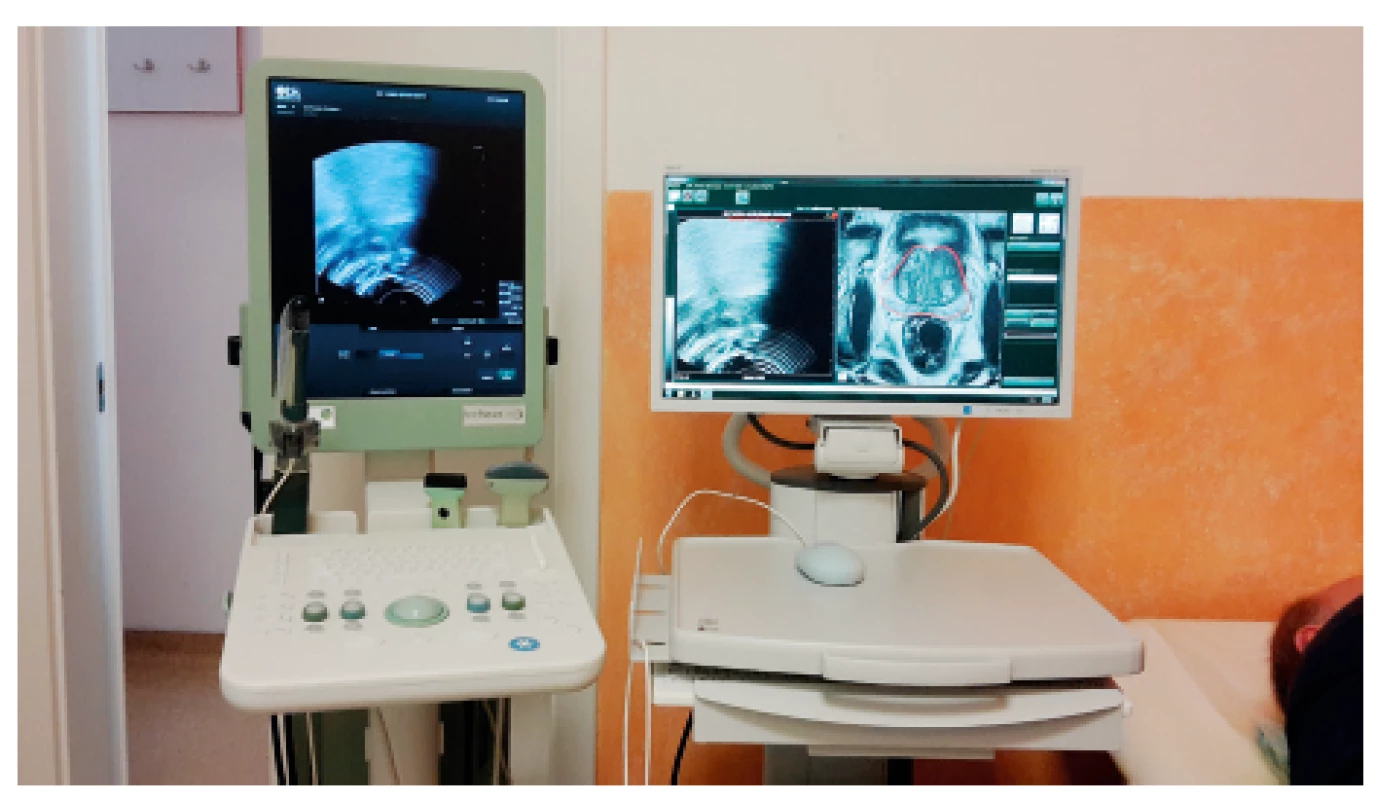
Fúzní TRUS/MRI biopsie byla provedena na přístroji BiopSee od firmy Medcom GmbH. Jedná se o externí modul k ultrazvukovému přístroji FlexFocus 400 od firmy BK Medical (obr. 3). Přístroj využívá standardní transrektální biplane sondu se side-fire pracovním kanálem 8808e. Po nahrání obrazové dokumentace z MR do fúzní jednotky byla provedena konturace prostaty a ložiska, resp. ložisek. Softwarově byl vypočítán objem prostaty a ložisek v ml. V další fázi došlo ke spojení kontur a real-time obrazu TRUS (registrace) a následně odebrány cílené vzorky z prostaty. Poloha bioptických vzorků byla zanesena do obrazové dokumentace. Výstupem TRUS/MRI biopsie je report (obr. 4), který je možno využít pro staging, plánování léčby nebo k plánování případné rebiopsie.
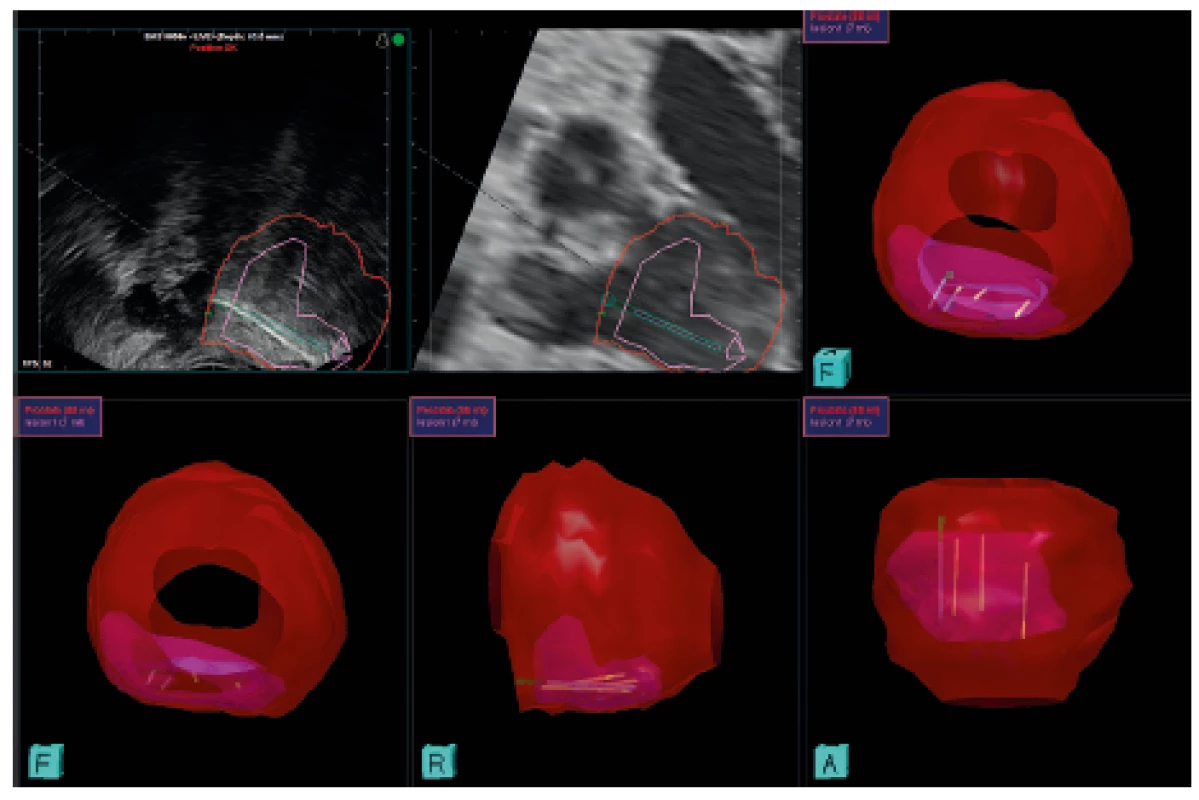
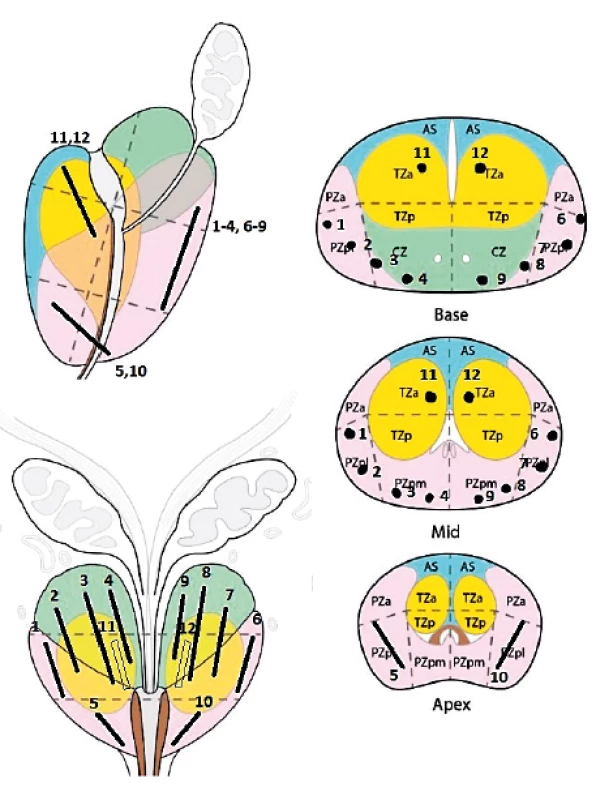
Bioptické schéma zahrnuje odběr 2–4 vzorků z každého ložiska (maximálně bioptovány 3 ložiska nejvyšší PIRADS kategorie) a následně systematickou biopsii 10–12 vzorků. V rámci systematické biopsie byly odebrány 4 vzorky z pravé i levé periferní zóny, 1 vzorek z obou stran apexu a 1 z pravé i levé transitorní zóny (obr. 5). Každý vzorek byl patologovi referován samostatně s informací o lokalizaci vzorku.
Hodnocen byl záchyt karcinomu prostaty v jednotlivých ložiscích a v systematické biopsii, porovnán byl záchyt karcinomu pro jednotlivé PI-RADS kategorie. Výsledky byly zpracovány standardními statistickými metodami.
Výsledky
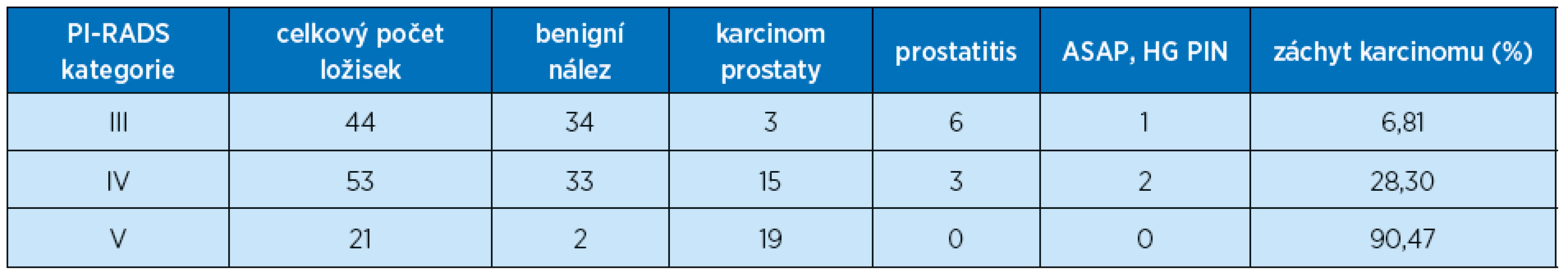
Karcinom prostaty byl v našem souboru diagnostikován u 38 pacientů (47,5 %), v podskupině primobiopsií byl karcinom prostaty zjištěn u 16 pacientů (80 %), u rebiopsií jsme zjistili karcinom prostaty u 22 pacientů (36,7 %). U 44 ložisek PIRADS 3 byl záchyt karcinomu prostaty ve 3 případech (6,81 %), ve 34 případech se jednalo o adenomyomatózní hyperplazii, v 6 případech o prostatitis a v 1 případě jsme zachytili premaligní lézi (ASAP, HG PIN). Pro skupinu ložisek PI-RADS 4 činil záchyt karcinomu prostaty 28,3 % (15/53), ve 33 ložiscích byla popsána adenomyomatózní hyperplazie, ve 3 ložiscích prostatitida a ve 2 případech premaligní léze. Nejvyšší záchyt karcinomu byl u ložisek PI-RADS 5 – 90,47 % (19/21), ve 2 ložiscích se jednalo o adenomyomatózní hyperplazii. Z 38 biopticky verifikovaných karcinomů bylo 28 zachyceno zároveň v systematické i cílené biopsii. V 5 případech se jednalo o záchyt jen v systematických vzorcích a u dalších 5 pacientů jen v cílené biopsii. Shrnutí výsledků ukazuje tabulka 1.
Analýza komplikací
Po biopsii prostaty bývá běžně přítomná přechodná hematurie, hemospermie či krvácení z rekta. Mezi nejčastější komplikace patří epididymitida, močová retence, prostatitida, méně často potom masivní hematurie či urosepse. Ostatní komplikace jsou vzácné (5).
V našem souboru jsme zaznamenali 4 případy močové retence, z toho 1 byla řešená za hospitalizace, ostatní 3 ambulantně. Epididymitida byla přítomná u 2 pacientů, jeden byl léčen ambulantně, jeden byl hospitalizován. Nezaznamenali jsme žádnou ze závažných komplikací jako např. urosepse či závažné krvácení. Žádná z výše uvedených komplikací si nevyžádala akutní chirurgickou intervenci (Clavien-Dindo 1-2).
Vyšší procento močových retencí lze u pacientů nad 65 let vysvětlit vyšší incidencí hyperplazie prostaty a s ní související subvezikální obstrukce. Ta může být dosud kompenzovaná a otok prostaty či hemorrhagie po biopsii mohou tuto rovnováhu narušit a vést k močové retenci. V práci Medeje (6) nebylo pozorováno vyšší riziko komplikací v souvislosti s počtem odebraných vzorků.
Diskuse
Multiparametrická MRI prostaty je užitečný diagnostický nástroj pro detekci i staging karcinomu prostaty. V současné době se její indikace rozšiřují a stává se tak široce využívanou metodou v klinické praxi. Na druhou stranu je velmi závislá na schopnostech a zkušenostech popisujícího radiologa (7).
V klinické praxi je možné využít dva základní principy TRUS/MRI fúzní biopsie – kognitivní a softwarovou. Zatím nebyla prokázána superiorita ani jedné z těchto dvou metod. Nicméně se ukazuje, že softwarová fúzní biopsie vykazuje lepší výsledky u drobných a ventrálně uložených ložisek (8).TRUS/MRI fúzní biopsie umožňuje zachytit i ložiska karcinomu atypicky uložená, a tudíž nedostupná pro standardní systematickou TRUS biopsii. Na druhou stranu část pacientů má negativní cílenou biopsii a pozitivní záchyt karcinomu v biopsii systematické. To je důvodem, proč stále zůstává systematická biopsie součástí diagnostického protokolu.
MUDr. Jakub Musil
e-mail: jakub.musil@nemocnicekolin.cz
Promoval v roce 2013 na 3. LF UK v Praze. Od roku 2013 pracuje na Urologickém oddělení Oblastní nemocnice Kolín, a. s. V roce 2015 absolvoval základní urologický kmen, v roce 2018 atestoval v oboru urologie. Od roku 2016 studuje doktorandský studijní program chirurgie na Lékařské fakultě UK v Hradci Králové. Jeho hlavním odborným zájmem je diagnostika karcinomu prostaty a endoskopická léčba urolitiázy.
Sources
1. Bjurlin MA, Taneja SS. Standarts for Prostate Biopsy. Curr Opin Urol 2014; 24(2): 155–161.
2. Bjurlin MA, et al. Optimization of prostate biopsy: the Role of Magnetic Resonance Imaging Targeted Biopsy in Detection, localization and Risc Assessment, J Urol 2014; 192 (3): 648–658.
3. PI-RADS v2, www.esur.org/esur-guidelines/prostate-mri
4. Rothwax JT, Georgie AK, et al. Multiparametric MRI in Biopsy Guidance for Prostate cancer: Fusion-Guided. Biomed Res Int 2014; 439171.
5. Stejskal J, et al. Diagnostika karcinomu prostaty pomocí fúzní biopsie. Ces Urol; 22(2): 87–98.
6. Madej A, Wilkosz J, et al. Complication rates after prostate biopsy according to the number of sampled cores. Cent European J Urol 2012, 65 : 16–118.
7. Šobrová A, Eret V, et al. Komparace multiparametrické magnetické rezonance se siloumagnetického pole 3 Tesla s transrektální monografií naváděnou biopsií prostaty. Ces Urol 2014; 18(3): 225–233.
8. Záleský M, Stejskal J, et al. Porovnání detekce signifikantního karcinomu prostaty pomocí systematické a cílené fúzní MRI/TRUS biopsie prostaty, Ces Urol; 22(2): 115–121.
9. Young JK, Jung SH, et al. Effectiveness of Bi-Parametric MR/US Fusion Biopsy for Detecting Clinically Significant Prostate Cancer in Prostate Biopsy Naive Men. Yonsei Med J 2019; 60(4), 346–351.
Labels
Geriatrics General practitioner for adults Orthopaedic prostheticsArticle was published in
Geriatrics and Gerontology

2019 Issue 2
- Advances in the Treatment of Myasthenia Gravis on the Horizon
- Memantine in Dementia Therapy – Current Findings and Possible Future Applications
- Memantine Eases Daily Life for Patients and Caregivers
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
-
All articles in this issue
- Editorial
- Specifics of acute urological care in elderly patients
- TRUS/MRI fusion prostate biopsy in patient over 65 years – results and complication rate analysis.
- Are robot-assisted radical prostatectomies safe in patients over 65?
- Risk and complications of the robotic partial nephrectomy in patients in age over 65 years
- The treatment of the water and electrolyte disturbances in geriatric patients.
- A Geriatrician in a General Practitioner´s Shoes
- Ohlédnutí za Celostátním gerontologickým kongresem
- DIABETES MELLITUS LÉČBA U STARŠÍCH PACIENTŮ V ČR. Doporučený diagnostický a terapeutický postup pro všeobecné praktické lékaře
- Geriatrics and Gerontology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Risk and complications of the robotic partial nephrectomy in patients in age over 65 years
- The treatment of the water and electrolyte disturbances in geriatric patients.
- TRUS/MRI fusion prostate biopsy in patient over 65 years – results and complication rate analysis.
- Are robot-assisted radical prostatectomies safe in patients over 65?
