Adiponektín vo vzťahu k obličkovej dysfunkcii u chorých s diabetes mellitus 2. typu
An association between adiponectin and renal dysfunction in patients with type 2 diabetes mellitus
Introduction:
Adiponectin is a hormone of adipose tissue produced exlusively by adipocytes. According to recent studies its serum concentrations are negatively associated with obesity and diabetes mellitus type 2 (DM).
The aim of the study was to clarify the relationship between renal functions and serum adiponectin in patients suffering from diabetic nephropathy.
Patients and methods:
The serum adiponectin levels were investigated in 120 patients and 40 controls. Patients in the diabetic group were divided according to albumin excretion rate into three groups – with normoalbuminuria (AER – albumin excretion rate/24 hod < 30 mg/24 h), with microalbuminuria (AER 30 ≤ 300 mg/24 h) and with macroalbuminuria (AER > 300 mg/24 h).
Results:
Serum adiponectin levels in diabetic group did not show any significant difference as compared with the control group. The highest concentrations of adiponectin were observed in patients with macroalbuminuria 24.22 ± 10.37 µg/ml (p < 0.0001) compared to those with normoalbuminuria and microalbuminuria, or control group, which was significant. Patients with normoalbuminuria 12.16 ± 5.3 µg/ml had the lowest concentrations of adiponectin. The univariate linear regression analysis revealed the negative correlation with BMI (r = –0.4, p < 0.0001) and glomerular filtration (r = –0.2, p < 0.05) and positive correlation with albuminuria (r = 0.5, p < 0.0001). Multiple linear regression confirmed that BMI and AER are independent predictive factors of adiponectin levels as well as that adiponectin and glomerular filtration are independent predictors of albuminuria.
Conclusion:
The beginning and progress of diabetic nephropathy play probably one of the most important roles in increased synthesis and excretion of adiponectin to blood circulation by diabetic patients with overt diabetic nephropathy.
Key words:
diabetes mellitus type 2 – adiponectin – obesity – diabetic nephropathy
Authors:
A. Galovičová 1; I. Lazúrová 1; D. Petrášová 2
Authors‘ workplace:
I. interná klinika Lekárskej fakulty UPJŠ a UN L. Pasteura Košice, Slovenská republika, prednostka prof. MUDr. Ivica Lazúrová, CSc.
1; Ústav experimentálnej medicíny Lekárskej fakulty UPJŠ Košice, Slovenská republika, prednosta MVDr. Alojz Bomba, DrSc.
2
Published in:
Vnitř Lék 2012; 58(11): 825-829
Category:
Original Contributions
Overview
Úvod:
Adiponektín je hormón tukového tkaniva produkovaný výlučne adipocytmi a podľa dostupných štúdií jeho sérové koncentrácie vykazujú negatívnu asociáciu s obezitou a ochoreniami spájanými s obezitou, ako sú diabetes mellitus 2. typu (DM). Cieľom práce bolo objasniť vzťah medzi renálnymi funkciami a sérovým adiponektínom u pacientov s diabetes mellitus 2. typu.
Súbory a metódy:
Sérové koncentrácie adiponektínu boli vyšetrené celkovo u 160 ľudí rozdelených do 2 skupín podľa prítomnosti diabetes mellitus. Diabetes mellitus malo 120 pacientov, 40 zdravých probandov tvorilo kontrolný súbor. Pacienti v diabetickej skupine boli rozdelení podľa albuminúrie do 3 súborov – s normoalbuminúriou [(AER – albumin excretion rate/24 hod) < 30 mg/24 hod], s mikroalbuminúriou (AER 30 ≤ 300 mg/24 hod) a s makroalbuminúriou (AER > 300 mg/24 hod).
Výsledky:
Sérový adiponektín v skupine s diabetes mellitus nevykazoval signifikantné rozdiely v porovnaní s kontrolnou skupinou. Signifikantne najvyššie koncentrácie adiponektínu (p < 0,0001) boli zistené u pacientov s makroalbuminúriou 24,22 ± 10,37 µg/ml v porovnaní s ostatnými 2 súbormi diabetikov i kontrolným súborom, a najnižšie v súbore s normoalbuminúriou 12,16 ± 5,3 µg/ml. Z univariantnej lineárnej regresnej analýzy vyplynula negatívna korelácia sérových hladín adiponektínu s BMI (r = –0,4, p < 0,0001), negatívna korelácia s glomerulovou filtráciou (r = –0,2, p < 0,05) a pozitívna korelácia s albuminúriou (r = 0,5, p < 0,0001). Viacnásobnou lineárnou regresiou sme potvrdili, že BMI a albuminúria sú významné nezávislé prediktory hladín adiponektínu a zároveň že adiponektín a glomerulová filtrácia sú prediktormi albuminúrie.
Záver:
V súhrne zistené údaje naznačujú, že vznik a vývoj diabetickej nefropatie zohráva pravdepodobne jednu z kľúčových úloh na zvýšenej syntéze a vylučovaní adiponektínu do krvného obehu potvrdenom u pacientov s manifestnou diabetickou nefropatiou.
Kľúčové slová:
diabetes mellitus 2. typu – adiponektín – obezita – diabetická nefropatia
Úvod
Objavenie leptínu v polovici 90. rokov 20. storočia znamenalo revolúciu vo vnímaní fyziologickej funkcie tukového tkaniva. Skončila sa éra, počas ktorej sa tukové tkanivo pokladalo za pasívne depo energie, a začal sa formovať koncept tukového tkaniva ako endokrinne aktívneho orgánu, ktorý je zdrojom bioaktívnych látok – adipokínov. Adipokíny ovplyvňujú široké spektrum fyziologických funkcií. Výsledky mnohých štúdií potvrdili význam adipokínov v regulácii fyziologických funkcií, čo viedlo k vzniku hypotézy, že zmeny v syntéze, sekrécii a/alebo účinku týchto látok u obéznych jedincov prispievajú k patogenéze obezity a sprievodných ochorení [1].
Adiponektín, 30 kDa proteín, inzulín senzitivizujúci hormón s antiaterogénnym a protizápalovým účinkom, je jedným z množstva adipocytokínov produkovaných v tukovom tkanive [2]. Aktívne vplýva na metabolizmus glukózy a lipidov a ovplyvňuje inzulínovú rezistenciu. Deficit adiponektínu je dôležitý v rozvoji inzulínovej rezistencie, sérové hladiny adiponektínu pozitívne korelujú s inzulínovou senzitivitou [3]. Zvýšené hladiny adiponektínu chránia pred rozvojom DM 2. typu, zatiaľ čo znížené hladiny môžu viesť k jeho predispozícii nezávisle od obezity [4]. Dostupné literárne zdroje uvádzajú, že znížené hodnoty plazmatickej koncentrácie adiponektínu sú zároveň asociované s vyšším výskytom a rozvojom mikrovaskulárnych i makrovaskulárnych komplikácií, diabetickej nefropatie, retinopatie, kardiovaskulárnych ochorení zastúpených ischemickou chorobou srdca a dolných končatín [5–10]. Kým hypoadiponektinémia je prediktorom uvedených ochorení a predpokladá sa, že renálna funkcia je dôležitým regulátorom hladín adiponektínu, zvýšená exkrécia albumínu sa v súčasnosti považuje za renálny prejav generalizovanej endoteliálnej dysfunkcie [11]. V dostupných štúdiách zaoberajúcich sa tématikou vzťahu adiponektínu a renálneho poškodenia sa závery rôznia. Vo väčšine sa však zhodujú, že renálne ochorenie je v pokročilých štádiách asociované so vzostupom hladín adiponektínu [12–16]. Cieľom práce bolo objasniť vzťah medzi renálnymi funkciami vyjadrenými albuminúriou a sérovým adiponektínom u pacientov s diabetes mellitus 2. typu a diabetickou nefropatiou v rôznych štádiách.
Metodika práce
Súbory
Sérové koncentrácie adiponektínu boli vyšetrené u 120 pacientov s diabetes mellitus 2. typu, 40 zdravých probandov tvorilo kontrolný súbor. Vstupným kritériom pre zaradenie do štúdie bola diagnóza diabetes mellitus 2. typu a vek nad 30 rokov. Vylučovacím kritériom pre zaradenie bol diabetes mellitus 1. typu, prítomnosť nediabetického obličkového ochorenia (určené na základe klinických kritérií), liečba diabetes mellitus tiazolidindiónmi a vek nad 70 rokov. Pacienti s DM 2. typu boli následne rozdelení na základe albuminúrie do 3 súborov: súbor 1 – pacienti s normoalbuminúriou < 30 mg/24 hod, súbor 2 – pacienti s mikroalbuminúriou 30–300 mg/24 hod, súbor 3 – pacienti s makroalbuminúriou > 300 mg/24 hod (tab. 1).

Antropometrické a biochemické parametre
U každého pacienta vo všetkých súboroch ako aj kontrolnej osoby boli stanovené antropometrické parametre – výška, váha, body mass index a tlak krvi.
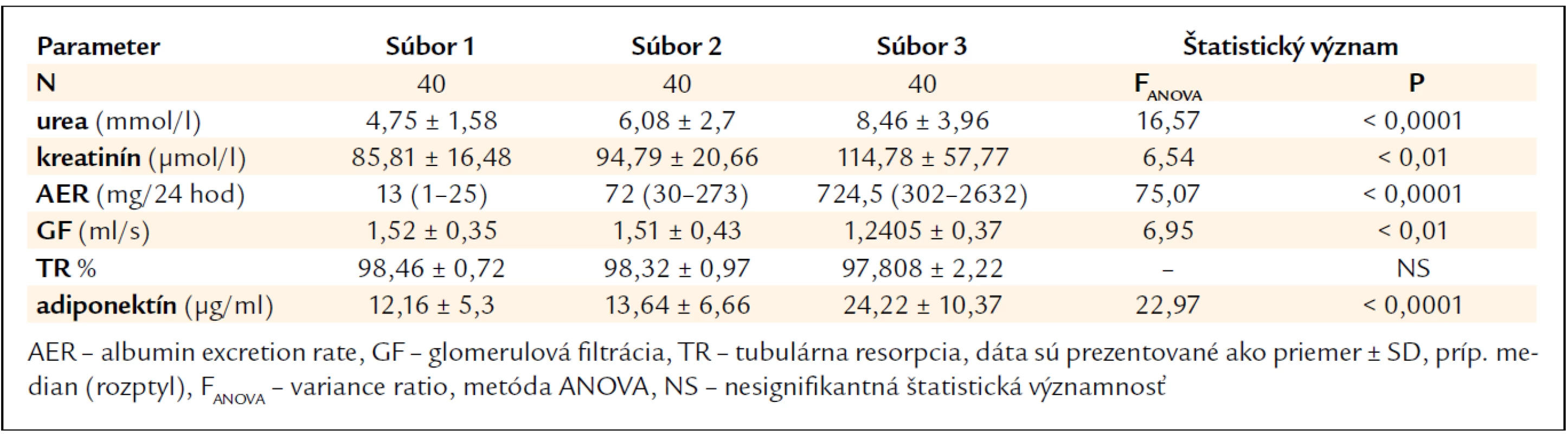
U pacientov s DM 2. typu sme sledovali vybrané biochemické parametre: glukózu, ureu, kreatinín a adiponektín. Funkčným vyšetrením obličiek boli vo všetkých 3 súboroch stanovené diuréza za 24 hod, glomerulová filtrácia, tubulárna resorpcia, mikroalbuminúria (za 24 hod, mg/l). Stupeň diabetickej nefropatie bol stanovený na základe hodnôt albuminúrie v minimálne 2 vzorkách moču vyšetrených v priebehu 3–6-mesačnej periódy za štandardných podmienok. Základné klinické parametre a vybrané biochemické parametre sú uvedené v tab. 1 a 2.
Analýza séra a moču
Vzorky krvi a moču boli odobrané za štandardných podmienok, nalačno, ráno do 8 hod. Sérum pacientov na vyšetrenie adiponektínu bolo až do doby vyšetrenia uskladnené pri teplote –80 °C. Biochemické parametre boli stanovené použitím rutinných metód. Adiponektín bol vyšetrovaný komerčne dostupnými ELISA (Enzyme-linked immunosorbent assay) setmi firmy BioVendor.
Štatistická analýza
Štatistické hodnotenie bolo vykonávané pomocou štatistického softwaru StatsDirect statistical software 2,7,2. Intervalové premenné sú prezentované ako aritmetický priemer ± smerodajná odchýlka (x ± SD), príp. medián a rozsah. Zhodnotenie významnosti rozdielov kvantitatívnych a kvalitatívnych parametrov v 3 a viacerých skupinách bolo realizované analýzou rozptylu (ANOVA – analysis of variance). Korelácie premenných v jednotlivých súboroch (súbory 1, 2, 3, kontrolný súbor) boli vyhodnotené lineárnou regresnou analýzou. Na zhodnotenie vzájomného vplyvu viacerých nezávislých premenných na závislú premennú bola použitá viacnásobná lineárna regresia. Pri všetkých uvedených štatistických analýzach bola signifikancia akceptovaná, ak hodnota P < 0,05.
Výsledky
Funkčným vyšetrením obličiek sme u všetkých pacientov stanovili glomerulovú filtráciu a albuminúriu. Porovnaním hodnôt GF medzi jednotlivými súbormi pacientov rozdelených podľa albuminúrie sme zistili jej signifikantný pokles v súbore s makroalbuminúriou (p < 0,01), teda v štádiu manifestnej diabetickej nefropatie, a očakávaný signifikantný vzostup kreatinínu (p < 0,01) a urey (p < 0,001) (tab. 2). Sérový adiponektín v skupine s diabetes mellitus nevykazoval signifikantné rozdiely v porovnaní s kontrolnou skupinou. Porovnali sme sérové koncentrácie adiponektínu u pacientov s DM medzi jednotlivými súbormi podľa albuminúrie a kontrolným súborom (tab. 3, graf 1). Signifikantne najvyššie koncentrácie adiponektínu (p < 0,0001) boli zistené u pacientov s makroalbuminúriou 24,22 ± 10,37 µg/ml v porovnaní s ostatnými 2 súbormi diabetikov a kontrolným súborom. Najnižšie hladiny boli namerané v súbore s normoalbuminúriou 12,16 ± 5,3 µg/ml. Z univariantnej lineárnej regresnej analýzy vyplynula pozitívna korelácia s albuminúriou (r = 0,5, p < 0,0001) (graf 2) a negatívna korelácia sérových hladín adiponektínu s glomerulovou filtráciou (r = –0,2, p < 0,05) a BMI (r = –0,4, p < 0,0001). Viacnásobnou lineárnou regresiou sme potvrdili, že BMI a albuminúria sú významné nezávislé prediktory hladín adiponektínu (pre BMI r = –0,31, p < 0,001, pre AER r = 0,53, p < 0,0001) a zároveň že adiponektín a glomerulová filtrácia sú prediktormi albuminúrie (pre GF r = –0,24, p < 0,01 a pre adiponektín r = 0,55, p < 0,0001).



Diskusia
Diabetická nefropatia je ochorenie obličiek rezultujúce zo základného ochorenia diabetes mellitus. Sérové markery, glomerulová filtrácia a mikroalbuminúria identifikujú renálne poškodenie v populácii diabetikov a mali by byť využívané v skríningu nefropatie [17]. Jednoduché a pacienta nezaťažujúce vyšetrenie by malo byť u diabetikov realizované včas a opakovane, pretože nízke hodnoty mikroalbuminúrie sú ovplyvniteľné liečbou [11].
Analyzovali sme vzťah sérových koncentrácií adiponektínu a vybraných renálnych laboratórnych parametrov u celkovo 120 diabetikov 2. typu. Po rozdelení pacientov s DM podľa štádia diabetickej nefropatie vyjadrenej albuminúriou, porovnanie hodnôt adiponektínu medzi súbormi s normoalbuminúriou a mikroalbuminúriou, teda bez nefropatie, resp. s incipientnou diabetickou nefropatiou, nepreukázalo signifikantné rozdiely. Signifikantne vyššie hladiny vyšetrovaného adiponektínu sme však potvrdili v súbore s makroalbuminúriou, a to ako pri porovnaní s koncentráciami adiponektínu u pacientov v úvodných štádiách diabetickej nefropatie, tak aj s kontrolným súborom.
Závery v súčasnosti dostupných štúdií zaoberajúcich sa tématikou vzťahu adiponektínu a renálneho poškodenia sa do istej miery rôznia. Väčšina uvádza, že akékoľvek renálne ochorenie, nielen diabetická nefropatia, je v pokročilých štádiách asociované so vzostupom hladín adiponektínu [12–16]. Saito et al zhodne s našími výsledkami konštatovali, že pacienti v IV. a V. štádiu diabetickej nefropatie mali signifikantne zvýšené koncentrácie adiponektínu v porovnaní zo zdravými kontrolami [18]. Podobne autori Koshimura et al uvádzajú, že sérové koncentrácie adiponektínu u pacientov s manifestnou diabetickou nefropatiou sú elevované v porovnaní s chorými bez nej. Nepotvrdili signifikantné rozdiely v hladinách adiponektínu medzi skupinami vyšetrovaných bez diabetickej nefropatie a štádiom incipientnej diabetickej nefropatie [12].
Elevácia sérového adiponektínu v súvislosti s manifestnou diabetickou nefropatiou už bola potvrdená aj u pacientov s diabetes mellitus 1. typu, aj na väčšej vzorke obéznych diabetikov 2. typu z kmeňa Pima indiánov [13,19]. Uvažuje sa, že zvýšenie koncentrácie adiponektínu môže byť spôsobené vlastnou zvýšenou syntézou, alebo redukciou klírensu adiponektínu pri porušenej funkcii obličiek, alebo kombináciou oboch. Fujita et al vo svojej práci analyzovali vzťah sérového adiponektínu a exkréciu adiponektínu močom u pacientov v rôznych štádiách diabetickej nefropatie, ale aj u diabetikov bez obličkového ochorenia. Hladiny oboch adiponektínov, sérového ako aj vylučovaného močom, boli signifikantne zvýšené u pacientov s manifestnou diabetickou nefropatiou, a naviac, sérové koncentrácie pozitívne korelovali s koncentráciami adiponektínu v moči u všetkých vyšetrených pacientov s diabetes mellitus 2. typu bez ohľadu na stupeň diabetickej nefropatie. Podľa autorov je preto pravdepodobnejšia teória, že zvýšené hodnoty sérového adiponektínu sú spôsobené jeho zvýšenou syntézou v tukovom tkanive a zvýšenou sekréciou do obehu skôr ako teória o redukovanom klírense adiponektínu v dôsledku porušenej renálnej funkcie [14].
Univariantnou regresnou analýzou sme potvrdili negatívnu koreláciu adiponektínu a GF a pozitívnu koreláciu adiponektínu s mikroalbuminúriou. Použitím viacnásobnej lineárnej regresie sme zistili, že albuminúria spolu s BMI sú významnými nezávislými prediktormi adiponektinémie a zároveň že adiponektín a glomerulová filtrácia sú nezávislými prediktormi albuminúrie.
Vyššie citovaní autori Koshimura et al [12], Looker et al [13], Fujita et al [14] aj Komaba et al [15] zhodne uvádzajú pozitívnu koreláciu adiponektínu a albuminúrie a negatívnu koreláciu s glomerulovou filtráciou obličiek. Podobne Saraheimo et al vo svojej štúdii pacientov s DM 1. typu dokumentovali pozitívnu koreláciu adiponektínu so sérovým kreatinínom a albuminúriou a negatívnu koreláciu s GF [19]. Egziabher et al sa zaoberali vzťahom skorých štádií nediabetického renálneho ochorenia a adiponektínu. Rovnako potvrdili negatívnu koreláciu GF s adiponektínom a zároveň pozitívnu koreláciu adiponektínu a albuminúrie [20]. Štúdia Lin et al dokumentovala znížené riziko vzniku alebo rozvoja renálnej dysfunkcie u diabetikov s vyššími hodnotami adiponektínu. Zároveň však potvrdila pozitívnu asociáciu adiponektínu a proteinúrie [21]. Závery väčšiny dostupných literárnych zdrojov sa zhodujú s nami zistenými nálezmi.
Odlišné výsledky uvádzajú Yenisecu et al [22,23]. Vo svojich prácach rozoberali opakovane asociáciu plazmatických hladín adiponektínu a proteinúrie u pacientov s diabetes mellitus 2. typu s diabetickou nefropatiou a následne v ďalšej práci vplyv podávania ACE inhibítora na plazmatické koncentrácie adiponektínu a proteinúriu. V oboch prácach zhodne došli k záveru, že plazmatické hladiny adiponektínu vykazujú negatívnu koreláciu s proteinúriou a jej závažnosťou. Popísali tiež pozitívny vplyv podávania ACE inhibítorov (ramiprilu) na koncentráciu adiponektínu a zároveň zmiernenie už existujúcej proteinúrie u týchto pacientov [22,23]. K prekvapivým záverom v porovnaní s väčšinovými závermi ostatných štúdii dospeli aj autori, ktorí sa vo svojej 6-ročnej prospektívnej observačnej štúdii zaoberali vzťahom medzi adiponektínom a renálnymi a retinálnymi chronickými komplikáciami diabetes mellitus 1. typu. Porovnanie koncentrácií adiponektínu u chorých s DM vs zdraví probandi preukázalo signifikantne vyššie koncentrácie adiponektínu v skupine diabetikov. U pacientov s perzistujúcou mikroalbuminúriou boli koncentrácie adiponektínu vyššie v porovnaní s pacientmi bez nefropatie [24]. Väčšina dostupných štúdii zameraných na vzťah albuminúrie a adiponektínu u pacientov s DM nepopisuje signifikantné rozdiely v koncentráciách tohto adiponektínu v štádiu normoalbuminúrie a mikroalbuminúrie. Štatistická významnosť v zmysle vzostupu koncentrácii adiponektínu sa objavuje až v štádiách makroalbuminúrie, resp. v pokročilých štádiách obličkového zlyhávania.
Záver
Pôsobenie tohto hormónu tukového tkaniva má pomerne široký záber a jeho komplexná úloha v patogenéze uvádzaných chorobných stavov nie je ani v súčasnosti aj napriek pomerne veľkému počtu štúdií dostatočne vysvetlená. V súlade s uvádzanými závermi aj naša práca poukazuje na to, že adiponektín sa zvyšuje až pri pokročilom poškodení obličiek u diabetikov. Nie je možné vylúčiť kachektizujúci vplyv chronického ochorenia obličiek, avšak je možné, že príčina je komplexnejšia, a jej objasnenie si vyžaduje realizáciu ďalších štúdií.
MUDr. Andrea Galovičová
www.lf.upjs.sk
e-mail: andrea.galovicova@zoznam.sk
Doručeno do redakce: 11. 6. 2012
Přijato po recenzi: 27. 8. 2012
Sources
1. Ukropcová B, Ukropec J, Klimeš I et al. Endokrinná funkcia tukového tkaniva. Via pract 2008; 5 : 115–121.
2. Zoccali C, Mallamaci F. Obesity, diabetes, adiponectin and the kidney: a podocyte affair. Nephrol Dial Transplant 2008; 23 : 3767–3770.
3. Tajtáková M, Petrášová D, Pidaniová A et al. Serum levels of leptin, adiponectin, retinol binding protein 4 and leptin/adiponectin molar ratio as another possible marker of insulin resistance in obese. Bratisl Lek Listy 2010; 111 : 212–215.
4. Monzillo LU, Hamdy O, Horton ES et al. Effect of lifestyle modification on adipokine levels in obese subjects with insulin resistance. Obes Res 2003; 11 : 1048–1054.
5. Kumada M, Kihara S, Sumitsuji S et al. Association of hypoadiponectinemia with coronary artery disease in men. Arteriosler Thromb Vasc Biol 2003; 23 : 85–89.
6. Pischon T, Girman CJ, Hotamisligil GS et al. Plasma adiponectin level and risk of myocardial infarction in men. JAMA 2004; 291 : 1730–1737.
7. Schulze MB, Shai I, Rimm EB et al. Adiponectin and future coronary heart disease events among men with type 2 diabetes. Diabetes 2005; 54 : 534–539.
8. Hotta K, Funahashi T, Arita Y. Plasma concentrations of a novel, adipose specific protein, adiponectin in type 2 diabetic patients. Arterioscler Thromb Vasc Biol 2000; 20 : 1595–1599.
9. Im JA, Kim SH, Lee JW et al. Association between hypoadiponectinemia and cardiovascular risk factors in nonobese healthly adults. Metabolism 2006; 55 : 1546–1550.
10. Koenig W, Khuseyinova N, Baumert J et al. Serum concentrations of adiponectin and risk of type 2 diabetes mellitus and coronary heart disease in apparently healthly middle-aged men: results from the 18-year follow-up of large cohort from southern Germany. J Am Coll Cardiol 2006; 48 : 1369–1377.
11. Monhart V. Mikroalbuminurie. Od diabetu ke kardiovaskulárnímu riziku. Vnitř Lék 2011; 57 : 293–298.
12. Koshimura J, Fujita H, Narita T et al. Urinary adiponectin excretion is increased in patient with overt diabetic nephrophaty. Bioch Biophys Res Commun 2004; 316 : 165–169.
13. Looker HC, Krakoff J, Funahashi Y et al. Adiponectin concentrations are influenced by renal function and diabetes duration in Pima Indians with type 2 diabetes. J Clin Endocrinol Metab 2004; 89 : 4010–4017.
14. Fujita H, Morii T, Koshimura J et al. Possible relationship between adiponectin and tubular injury in diabetic nephropathy. Endocrin Journal 2006; 53 : 745–752.
15. Komaba H, Igaki N, Goto S et al. Increased serum high molecular weight complex of adiponectin in type 2 diabetic patients with impaired renal function. Am J Nephrol 2006; 26 : 476–482.
16. Iwashima Y, Horio T, Kumada M et al. Adiponectin and renal function, and implication as risk of cardiovascular disease. Am J Cardiol 2006; 98 : 1603–1608.
17. Dabla PK. Renal function in diabetic nephropathy. World J Diabetes 2010; 1 : 48–56.
18. Saito T, Saito O, Kawano T et al. Elevation of serum adiponectin and CD 146 levels in diabetic nephropathy. Diabetes Res Clin Pract 2007; 78 : 85–92.
19. Saraheimo M, Forsblom C, Fagerudd J et al. Serum adiponectin is increased in type 1 diabetic patient with nephropathy. Diabetes Care 2005; 28 : 1410–1414.
20. Guebre-Egziabher F, Bernhard J, Funahashi T et al. Adiponectin in chronic kidney disease is related more to metabolic disturbances than to decline in renal function. Nephrol Dial Transplant 2005; 20 : 129–134.
21. Lin J, Hu FB, Curhan G et al. Serum adiponectin and renal dysfunction in men with type 2 diabetes. Diabetes Care 2007; 30 : 239–244.
22. Yenicesu M, Yilmaz MI, Caglar K et al. Adiponectin level is reduced and inversly correlated with degree of proteinuria in type 2 diabetic patients. Clin Nephrol 2005; 64 : 9–12.
23. Yenicesu M, Yilmaz MI, Caglar K et al. Blockade of the renin-angiotensin system increased plasma adiponectin levels in type 2 diabetic patients with proteinuria. Nephron Clin Pract 2005; 99 : 115–121.
24. Hadjadj S, Aubert R, Fumeron F et al. Increased plasma adiponectin concentrations are associated with microangiopathy in type 1 diabetic subjects. Diabetologia 2005; 48 : 1088–1092.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2012 Issue 11
-
All articles in this issue
- Účinnost lenalidomidu u vzácných krevních chorob: u histiocytózy z Langerhansových buněk, multicentrické Castlemanovy choroby, POEMS syndromu, Erdheimovy-Chesterovy choroby a angiomatózy. Popis případů a přehled literatury
- Metabolizmus vitaminu D a současné možnosti terapeutické aktivace receptoru pro vitamin D při chronickém onemocnění a selhání ledvin
- Kombinovaná kinezio-flebotromboemboloprofylaxia, mechano-flebotromboemboloprofylaxia a farmako-flebotromboemboloprofylaxia vénovej tromboembólie v internej medicíne
- Koronární-subklaviální steal syndrom, komplikace po chirurgické revaskularizaci myokardu
- Je syndróm polycystických ovárií asociovaný s autoimunitnou tyreoiditídou?
- Myxom levé síně – nečekaná příčina dušnosti a teplot mladého pacienta
- Karcinoid a jeho kardiální manifestace
- Neobvyklá příčina defektu nohy u nemocného s diabetes mellitus
- Kostní minerální denzita u nemocných s chronickým selháním ledvin při zahájení hemodialyzační léčby
- Revmatoidní artritida – nezávislý rizikový faktor kardiovaskulárních onemocnění
- Adiponektín vo vzťahu k obličkovej dysfunkcii u chorých s diabetes mellitus 2. typu
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Koronární-subklaviální steal syndrom, komplikace po chirurgické revaskularizaci myokardu
- Metabolizmus vitaminu D a současné možnosti terapeutické aktivace receptoru pro vitamin D při chronickém onemocnění a selhání ledvin
- Myxom levé síně – nečekaná příčina dušnosti a teplot mladého pacienta
- Karcinoid a jeho kardiální manifestace
