Léčba obrovskobuněčné arteriitidy – současnost a otevírající se možnosti
Treatment of giant cell arteritis – current approach and new possibilities
Giant Cell Arteritis (GCA) is an autoimmune mediated systemic vasculitis affecting large arteries – the aorta and its branches. It has the highest incidence of all systemic vasculitides and manifests nearly exclusively in patients aged 50 or older. Amongst its non-specific and specific symptoms are headaches, mastication claudication or signs of rheumatic polymyalgia, a relatively common and immediate treatment requiring condition being acute vision loss due to optic ischemia. A GCA diagnosis is based on clinical and paraclinical findings and imaging techniques including PET/CT; with an important role still being played by histological verification from temporal artery biopsy. Treatment is based on immunosuppressive agents – systemic glucocorticoids, with adjunct therapy options being methotrexate and tocilizumab. Currently, there are also several clinical trials examining the efficacy of other modern biological agents in GCA.
Keywords:
Methotrexate – glucocorticoids – giant cell arteritis – tocilizumab
Authors:
Jakub Videman; Martina Skácelová; Pavel Horák; Adéla Skoumalová; Dominik Hraboš
Authors‘ workplace:
III. interní klinika – nefrologická, revmatologická a endokrinologická, FN a LF UP Olomouc
Published in:
Vnitř Lék 2022; 68(5): 266-272
Category:
Main Topic
doi:
https://doi.org/10.36290/vnl.2022.058
Overview
Obrovskobuněčná arteriitida (GCA – Giant Cell Arteritis) je autoimunitně podmíněné systémové vaskulitické onemocnění postihující velké tepny – aortu a její větve. Je to nejčastěji se vyskytující systémová vaskulitida, manifestuje se prakticky pouze v populaci starší 50 let. Má řadu nespecifických i specifických příznaků, mezi něž se řadí bolesti hlavy, žvýkací klaudikace či příznaky revmatické polymyalgie, nezřídka se vyskytující závažnou komplikací vyžadující rychlý diagnosticko‑terapeutický zásah je pak ischemicky podmíněná porucha zraku. V diagnostice onemocnění se kromě klinického a laboratorního nálezu uplatňuje celá škála zobrazovacích vyšetření vč. PET/CT a též histologické vyšetření biopsie temporální arterie. Terapie onemocnění je založena na podávání imunosupresivní medikace – základem terapie jsou glukokortikoidy, doplňkově se uplatňuje methotrexát a tocilizumab. V současnosti též probíhá pro tuto indikaci řada prospektivních klinických hodnocení moderních biologických léčiv.
Klíčová slova:
glukokortikoidy – metotrexát – obrovskobuněčná arteriitida – tocilizumab
Úvod
Obrovskobuněčná arteriitida, také známá jako Hortonova nemoc či temporální arteriitida, v anglofonní literatuře pak Giant Cell Arteritis (GCA), je imunitně mediované systémové zánětlivé onemocnění – vaskulitida postihující cévní stěnu velkých a středně velkých tepen, tedy zejména aorty a jejích větví. GCA je nejčastěji se vyskytující idiopatickou vaskulitidou, přičemž se manifestuje prakticky pouze u osob nad 50 let věku. Incidence onemocnění je geograficky nejvyšší v severoamerických a severských evropských zemích – prokázaná incidence v Olmstead County v Minnesotě je 17 případů na 100 000 obyvatel nad 50 let věku, přičemž ženská populace je postižena častěji v poměru 3 : 1 (1). Epidemiologicky i klinicky významná je asociace GCA s revmatickou polymyalgií (PMR), kdy téměř 50 % pacientů s GCA manifestuje též příznaky PMR, a téměř 10 % pacientů s PMR rozvine onemocnění GCA.
Klinická manifestace choroby
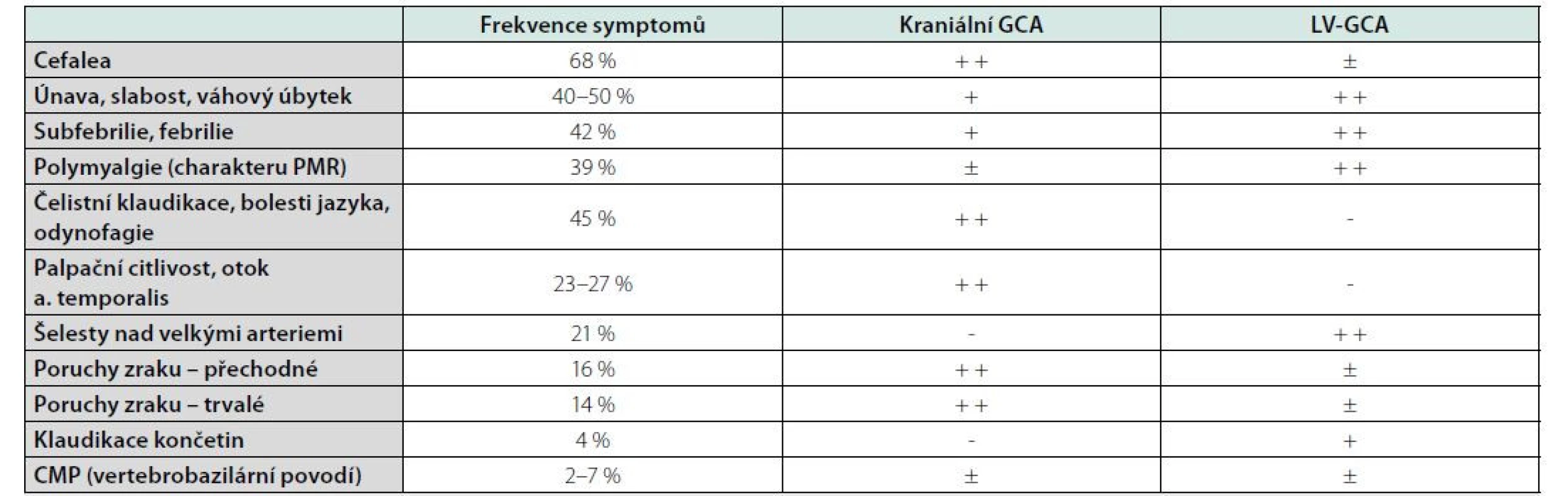
Obrovskobuněčná arteriitida se projevuje celou řadou nespecifických i specifických klinických symptomů zahrnujících recidivující subfebrilie až febrilie, zvýšenou únavnost a váhový úbytek. Mezi specifičtější symptomy se poté řadí bolesti hlavy, přičemž v tomto ohledu jsou typické zejména temporálně lokalizované bolesti, přítomnost zduřelé temporální arterie či absence pulzu temporální arterie, palpační bolestivost kůže skalpu, frekventní rekurence bolestí a nepříliš dobrá odezva na analgetickou farmakoterapii. Dalšími specifickými příznaky jsou čelistní neboli mastikační klaudikace, tedy ischemické bolesti žvýkacích svalů vyvolané námahou při žvýkání, a též příznaky přidružené revmatické polymyalgie, tedy pletencová svalově‑kloubní bolest a ranní ztuhlost. Vzácnějším, ale zcela klíčovým příznakem jsou pak poruchy zraku – diplopie, výpadky zorného pole či přechodná ztráta zraku (amaurosis fugax). Tyto příznaky jsou obvykle zprvu unilaterální, a jsou výrazným rizikovým faktorem možného rozvoje nejobávanější komplikace obrovskobuněčné arteriitidy, kterou je nevratná ztráta zraku patofyziologicky podmíněná několika možnými mechanismy, z nichž nejčastější je ischemické postižení n. opticus – AION (Anterior Ischemic Optic Neuropathy). Přítomnost těchto symptomů tedy vyžaduje promptní a razantní terapeutický přístup k minimalizaci rizika rozvoje nevratných změn. V moderním pojetí choroby se rozlišují dva více či méně se překrývající fenotypické formy choroby – kraniální forma vyznačující se spíše specifickými příznaky vyplývajícími z postižení karotid a jejich bezprostředních větví, a forma systémová postihující aortu a velké tepny (LV‑GCA – Large Vessels Giant Cell Arteritis) doprovázená dominantně celkovými nespecifickými příznaky (Tab. 1).
Diagnostika
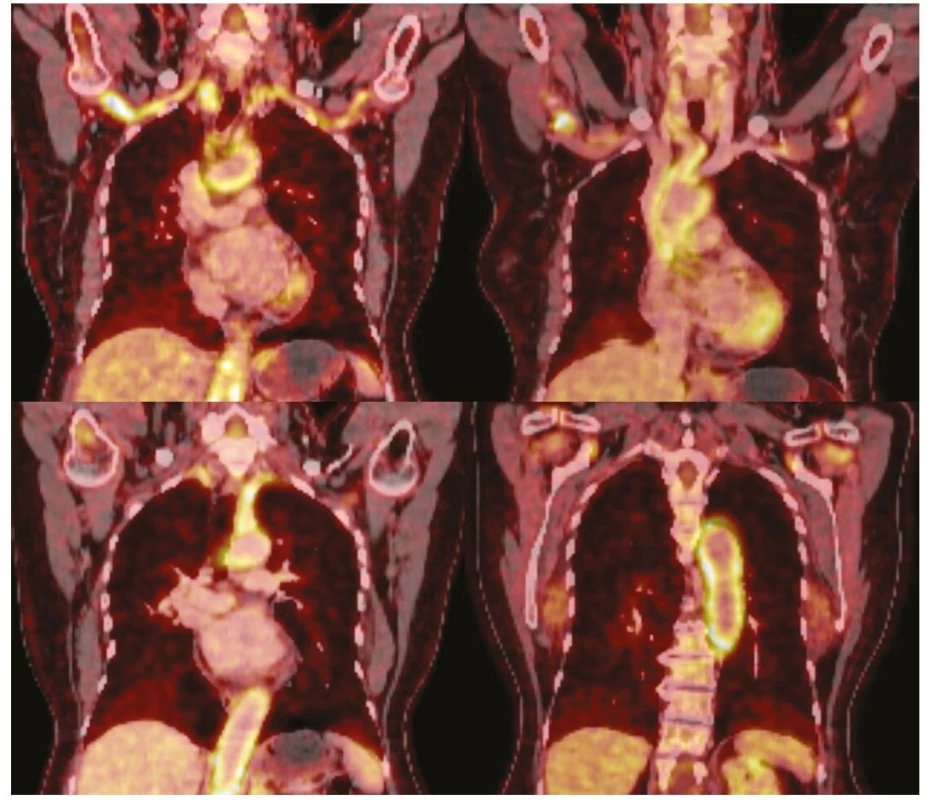
Laboratorními známkami aktivního onemocnění jsou nespecifické nálezy odpovídající systémovému zánětlivému procesu – elevace CRP a zejména sedimentace erytrocytů (FW), která může dosahovat či přesahovat hodnotu 100 mm/h, před zahájením terapie má pouze 5 % pacientů hodnotu FW nepřekračující 40 mm/h (2). Specifičtějším ukazatelem zánětlivé aktivity onemocnění se jeví IL6 (3), přičemž receptor pro IL6 je též jedním z terapeutických cílů, rutinní laboratorní testování sérových hladin IL6 však zatím není široce dostupné. Přítomna může být též chronická anemie a/nebo trombocytóza. Z dalších paraklinických modalit zlatým standardem v diagnostice GCA zůstává histologické vyšetření biopsie temporální arterie (Obr. 1 a 2), z neinvazivních zobrazovacích metod se uplatňuje zejména 18FDG‑PET/ CT vyšetření (Obr. 3), které v rámci studie GAPS prokázalo v porovnání s biopsií temporální arterie 92% senzitivitu a 85% specificitu (4), mezi výhody tohoto vyšetření mimo neinvazivitu patří též zobrazení rozsahu zánětlivého postižení – 42 % pacientů s pozitivním nálezem na biopsii temporální arterie mělo pomocí 18FDG‑PET/ CT prokázáno zánětlivé postižení aorty; u 7 % vyšetřených pacientů byla pak jako incidentální nález odhalena malignita.
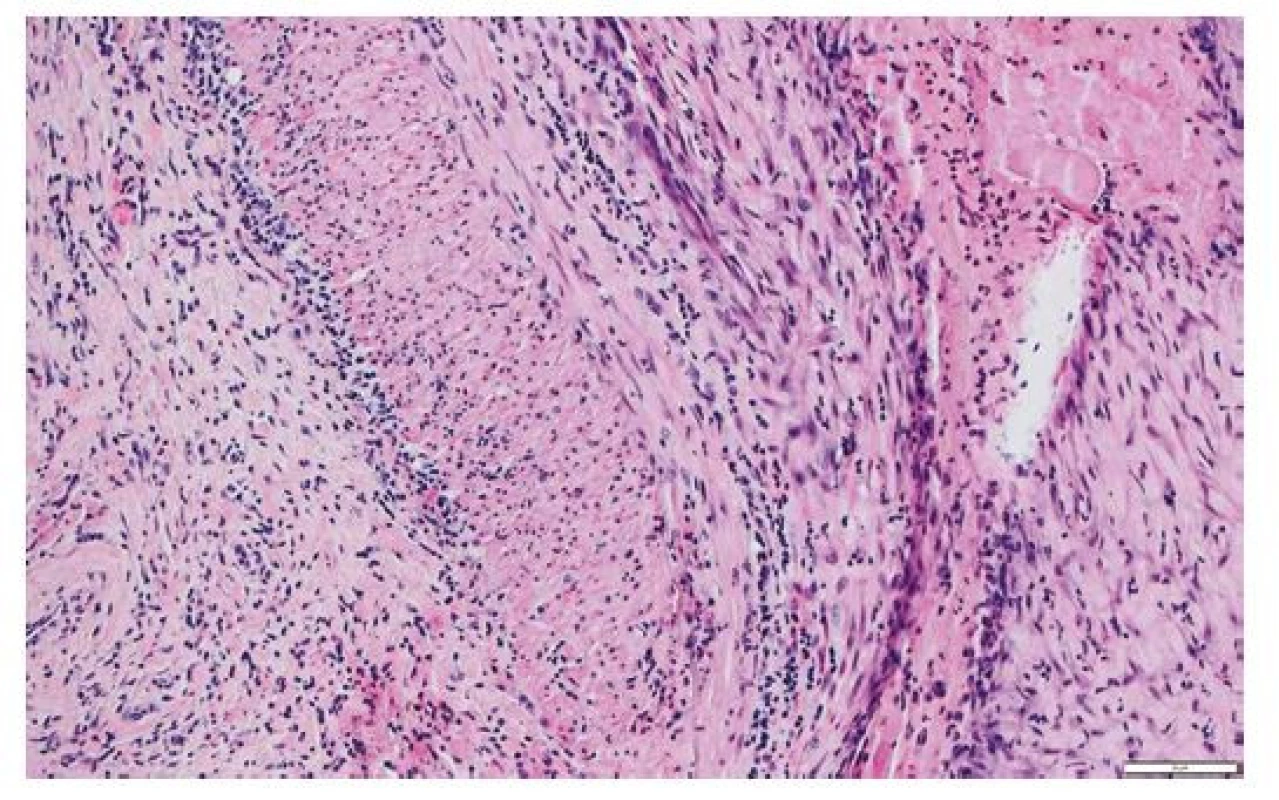

Z archivu Ústavu klinické a molekulární patologie Fakultní nemocnice Olomouc.
Významu nabývá též ultrasonografické vyšetření vč. Dopplerovské ultrasonografie, které umožňuje v rukou zkušeného sonografisty vysoce specifické posouzení zánětlivé afekce nejen kraniálních, ale též některých extrakraniálních arterií, například tepny podklíčkové či podpažní (5). Z dalších neinvazivních zobrazovacích vyšetření mají své místo v diagnostickém procesu též MR angiografie aa. temporalis a ultrasonografické vyšetření či CT nebo MR angiografie aorty.
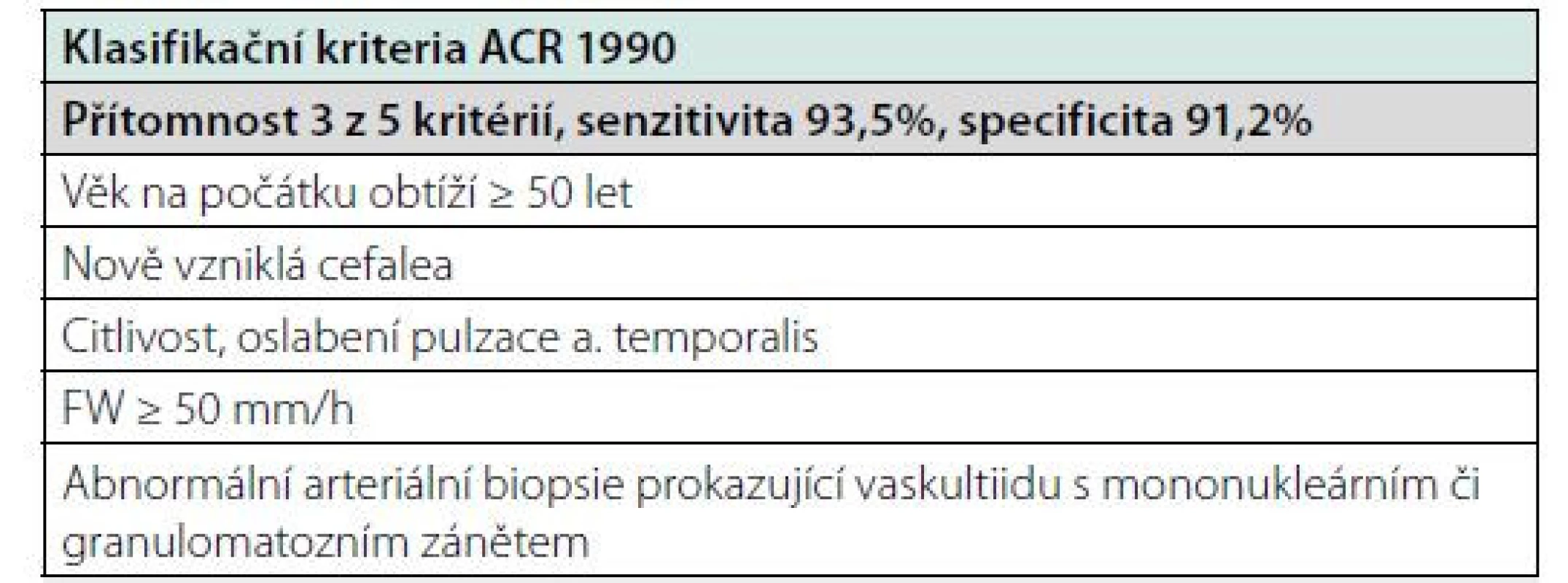
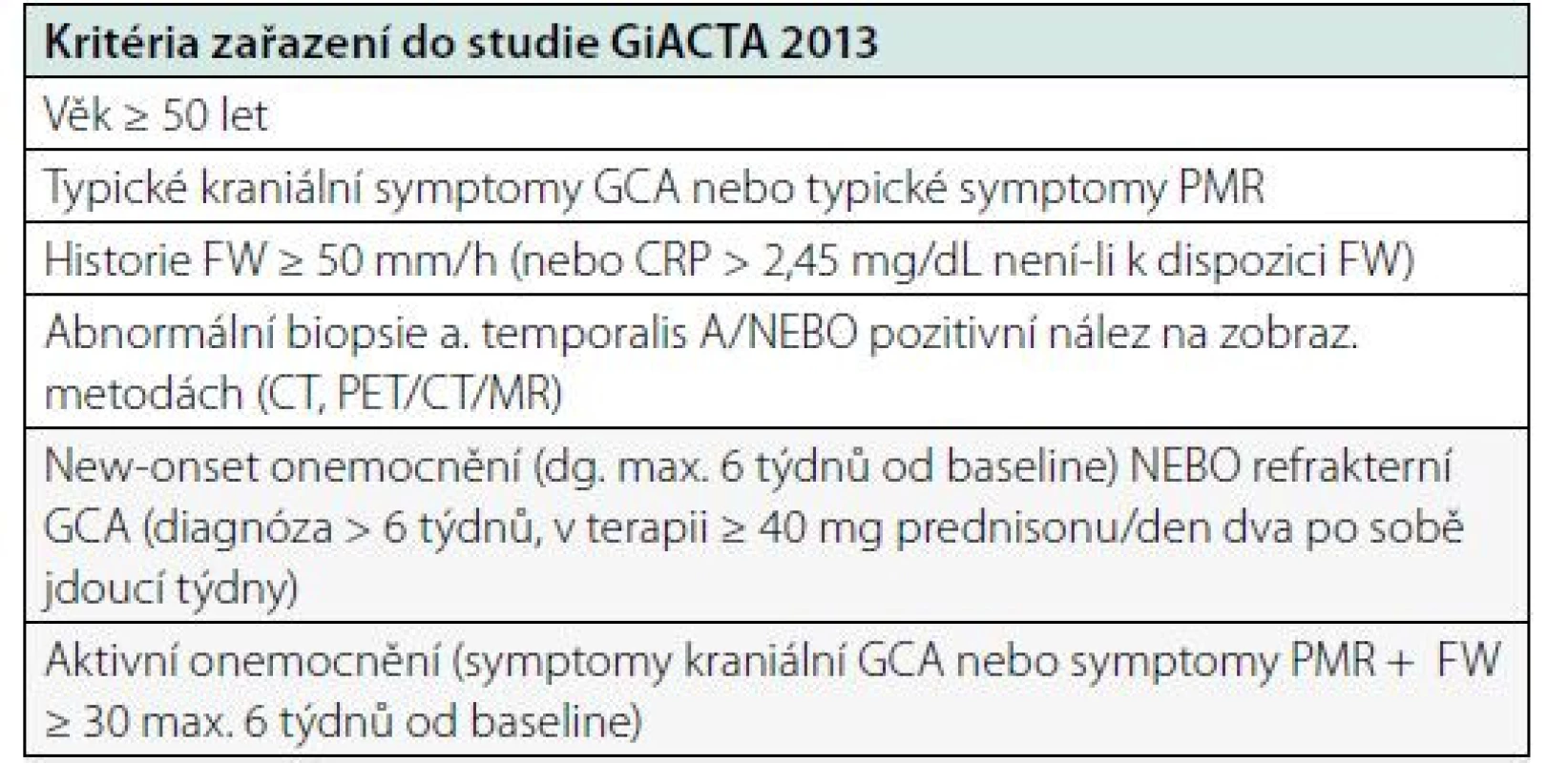
Stávajícími platnými klasifikačními kritérii GCA jsou nicméně klasifikační kritéria Americké revmatologické společnosti (ACR – American College of Rheumatology) z roku 1990 (Tab. 2), která ze zobrazovacích vyšetření berou v potaz pouze pozitivní histologický nález biopsie temporální arterie. Pro účely klinických hodnocení jsou proto často sestavována vstupní kritéria, která připouští též jiné radiologické známky aktivního onemocnění, jako například vstupní kritéria pro studii GiACTA (Tab. 3). V současnosti probíhá též projekt spolupráce ACR s Evropskou aliancí revmatologických asociací / Evropskou ligou proti revmatismu (EULAR – European League Against Rheumatism) s cílem sestavit nová klasifikační kritéria GCA reflektující lépe nové poznatky ohledně onemocnění a pokrok v oblasti zobrazovacích vyšetření.
Terapeutická doporučení
Terapeutický přístup k pacientům s GCA se řídí aktualizovanými doporučeními EULAR pro management vaskulitid velkých cév (LVV – Large Vessel Vasculitis), kam se GCA spolu s Takayasuovou arteriitidou řadí. Tato doporučení byla poprvé vydána v roce 2009, v roce 2018 byla poté aktualizována s přihlédnutím právě k novým poznatkům a diagnosticko‑terapeutickým možnostem. Na této aktualizaci se podílelo 20 odborníků napříč obory (revmatologie, interna, imunologie, neurologie, neurooftalmologie, epidemiologie) a v rámci pracovní skupiny se metodologicky pomocí Delfské metody stanovilo 8 otázek klíčových pro management pacientů s LVV, k těmto otázkám poté proběhla systematická literární rešerše (SLR) vycházející z databází MEDLINE, EMBASE a Cochrane CENTRAL. Výstupem byly 3 zastřešující principy a 10 konkrétních doporučení pro terapii (6).
Glukokortikoidy
Základním prvkem medikamentózní terapie GCA zůstávají nadále glukokortikoidy, jejichž efektivita v léčbě této diagnózy je potvrzena léty klinické praxe. Ačkoli není k dispozici žádná studie přímo potvrzující jejich efektivitu, existují studie prokazující preventivní efekt stran rozvoje výše zmíněných závažných komplikací, zejména nevratného poškození zraku. Retrospektivní studie zahrnující 245 pacientů s GCA, z nichž 34 manifestovalo nevratné poškození zraku, popisuje u 32 ze 34 těchto pacientů ztrátu zraku již před iniciací kortikoterapie, jeden případ pak do osmi dnů od zahájení terapie a jeden až rok po ukončení terapie systémovými kortikosteroidy v rámci normalizace klinických a laboratorních známek aktivity onemocnění (7).
Stran dávkování je pro rozhodnutí klíčová právě přítomnost klinických příznaků týkajících se zraku – udává‑li pacient nově manifestní poškození zraku charakteru diplopie, výpadků zorného pole či přechodné nebo perzistentní ztráty zraku, je třeba zahájit kortikoterapii promptně intravenózními pulzy, zvykle 500–1000 mg methylprednisolonu denně po dobu tří dnů. V případě absence těchto zrakových symptomů je terapie zahajována perorálně dávkami prednisolonu 1 mg/kg/den (či kortikosteroidního ekvivalentu, při maximální doporučované dávce prednisolonu 60 mg/den), obdobnými dávkami je též vhodno navázat na případnou předchozí intravenózní kortikoterapii. Při takto adekvátně zahájené terapii v řádu dnů dochází k citelnému subjektivnímu ústupu symptomů a též laboratorních známek zánětu, kdy CRP poklesá výrazně rychleji než ESR. Nedochází‑li k tomuto klinickému zlepšení, a zejména v kontextu případů, kdy je diagnóza GCA primárně na těchto klinických symptomech založena a není podepřena adekvátním bioptickým či radiologickým nálezem, měla by tato diagnóza být znovu zvážena či přehodnocena.
Při dobrém terapeutickém efektu je vhodno s redukcí dávek započít dva až čtyři týdny po zahájení terapie a redukce by měla být velmi pozvolná, tedy zpočátku o 10 mg/den každé dva týdny k dávkám okolo 0,5 mg/kg/den, poté dále redukce o 5 mg/den každé dva týdny podmíněná laboratorními kontrolami prokazujícími normalizaci zánětlivých parametrů a též adekvátní klinickou monitorací zajišťující včasné rozpoznání navracejících se symptomů. Dlouhodobá udržovací dávka je obvykle 10–20 mg prednisolonu denně, nicméně redukce dávek pod 10 mg/den je možná, stejně jako rozhodnutí o ukončení kortikoterapie při dlouhodobé kompletní remisi choroby.
Chorobu modifikující léky syntetické
V terapii GCA mají dle současných poznatků jakožto kortikoidy‑šetřící medikace místo dva preparáty – methotrexát a tocilizumab, přičemž tento fakt zohledňují též výše zmiňovaná doporučení EULAR pro terapii GCA z roku 2018. Methotrexát (MTX) je zástupcem konvenčních syntetických léčiv (csDMARDs). Ačkoliv tři randomizované studie zkoumající efekt MTX v terapii GCA dosáhly rozdílných, a ne vždy jednoznačných výstupů, meta‑analýza těchto studií na vzorku 161 pacientů prokázala statisticky signifikantní redukci kumulativní dávky glukokortikoidů, snížené riziko prvního i druhého relapsu onemocnění a pravděpodobnosti dosažení remise onemocnění (8). Zahajovací dávkou MTX je zpravidla 10–15 mg jedenkrát týdně, dostupná je jak perorální, tak subkutánní injekční forma preparátu. Pro minimalizaci nežádoucích účinků je třeba den po podání MTX suplementovat folát.
V terapii GCA byla zvažována též řada dalších preparátů – z konvenčních imunosupresiv byl logickou volbou cyklofosfamid (CFA), který se s úspěchem využívá v první linii indukční terapie jiných systémových vaskulitid. K dispozici je nicméně pouze několik menších studií naznačujících benefit u pacientů s vysokým rizikem glukokortikoidové toxicity, u kterých zároveň nedošlo k adekvátní terapeutické odpovědi na jinou imunosupresivní terapii či se nedaří adekvátně redukovat dávky glukokortikoidů. Systematická review 103 publikovaných případů sice ukázala v 86 % případů terapeutický efekt, nicméně ve 22 % případů došlo k relapsu onemocnění i přes udržovací imunosupresivní terapii, a zjištěno bylo též relativně vysoké riziko nežádoucích účinků – až v jedné třetině případů, přičemž 12 % pacientů muselo terapii ukončit pro infekt či hematologické změny charakteru cytopenií (9). Vzhledem k tomuto nepříznivému bezpečnostnímu profilu a nedostatku přesvědčivých důkazů o jeho efektu není v současných terapeutických doporučeních pro obrovskobuněčnou arteriitidu CFA uváděn a jediným zmiňovaným zástupcem skupiny csDMARDs tak zůstává MTX.
Chorobu modifikující léky biologické
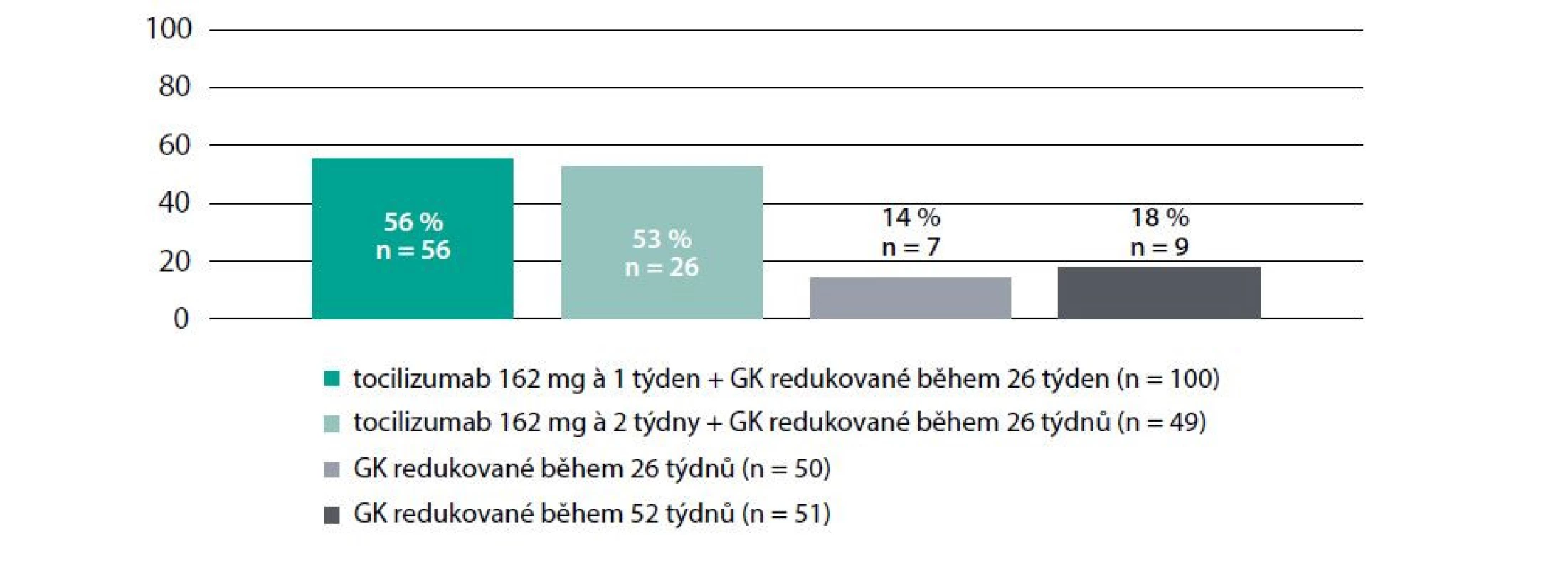
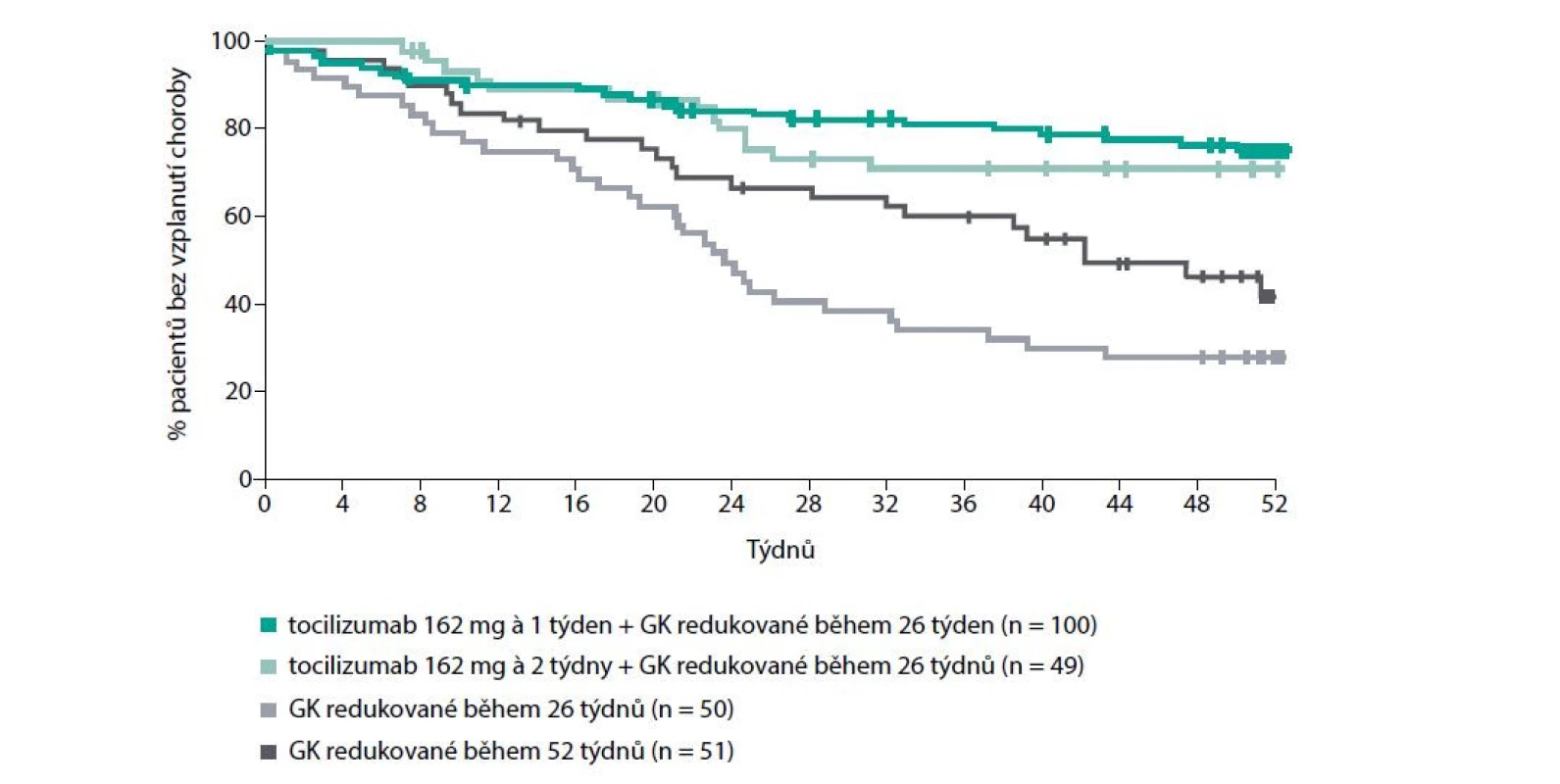
Druhým doporučovaným farmakem, které je nicméně v terapii GCA rezervováno pro pacienty ve vysokém riziku toxicity kortikoidů a jehož rutinní užívání je prozatím otázkou ne zcela vyjasněnou, je zástupce moderních biologických preparátů (bDMARDs) antagonista IL-6R tocilizumab (TCZ). Studie GiACTA byla multicetrickou, randomizovanou, dvojitě zaslepenou, placebem kontrolovanou studií zkoumající účinnost a bezpečnostní profil tocilizumabu. Ve studii bylo zařazeno 251 pacientů, kteří byli rozděleni v poměru 2 : 1 : 1 : 1 do skupin léčených subkutánní aplikací tocilizumabu v dávce 162 mg jednou týdně, resp. dvakrát týdně v kombinaci s dávkou kortikoidů postupně redukovanou do 26. týdne versus placebem s kortikoidy redukovanými během 26, resp. 52 týdnů. Primárním cílem studie bylo udržení remise v 52. týdnu, čehož bylo dosaženo u 56 % pacientů a 53 % pacientů ve skupinách léčených tocilizumabem, kdežto ve skupinách placebových pouze ve 14 %, resp. 18 % případů (p < 0,001). Prokázána byla též výrazně nižší kumulativní dávka kortikoidů potřebná k udržení remise ve skupině léčené tocilizumabem (10) (Obr. 4 a 5). Vyvstává nicméně otázka, zda mechanismus účinku tocilizumabu, tedy inhibice IL-6R, má skutečně plně protizánětlivý efekt, nebo zda dochází pouze k přechodnému potlačení korespondujících klinických projevů. Tato obava vyplývá ze zkušenosti s incidentálním sekčním nálezem pacienta s GCA, který byl hodnocen jako v klinické remisi při terapii kortikoidy + TCZ, nicméně post mortem byla prokázána aktivní vaskulitida aorty, podklíčkových arterií a pravé spánkové tepny (11).
Dalšími z preparátů, které by se mechanismem účinku jevily vzhledem k patofyziologii GCA jako vhodná volba, jsou inhibitory TNF – infliximab, adalimumab, etanercept. Řada menších, nicméně často multicentrických, dvojitě zaslepených placebem kontrolovaných skupin však jejich efekt neprokázala. Například studie 44 pacientů v remisi indukované glukokortikoidy byla rozdělena do dvou skupin v poměru 2 : 1 do skupin užívajících infliximab 5 mg/kg a placebo. Již ve 22. týdnu studie předběžné zhodnocení neukázalo oproti placebu pokles relativního rizika relapsu (43 % vs. 50 %), podíl pacientů jejichž kortikoterapie mohla být redukována k 10 mg/den prednisolonu, též nepoukazoval na benefit léčby (61 % vs. 75 %) a studie byla předčasně ukončena (12). Předčasně ukončená a přínos neprokazující byla též multicentrická placebem kontrolovaná studie jiného inhibitoru IL-6, sirukumabu (13).
Experimentální léčba
V terapii GCA se tedy jeví prostor a příležitost pro rozšíření stávajících možností terapie a probíhá řada klinických hodnocení preparátů jak zcela nových, tak preparátů již schválených a s úspěchem využívaných v terapii jiných systémových zánětlivých onemocnění. Jedním z vhodných adeptů se jeví například blokátor kostimulačního systému aktivace T‑lymfocytů CD28-CD80/86 abatacept, který je FDA schválen pro terapii revmatoidní artritidy. Již proběhla menší dvojitě zaslepená studie 2. fáze, v níž 49 pacientů s nově diagnostikovanou či relabující GCA bylo léčeno prednisolonem a i.v. abataceptem v dávce 10 mg/kg v 1., 15, 29. dni a 8. týdnu. Ve 12. týdnu byli poté pacienti v remisi rozděleni do skupiny užívající abatacept jedenkrát měsíčně a skupiny placebové, následné hodnocení ve 12. měsíci ukázalo relapse‑free survival ve 48 % pacientů léčených abataceptem oproti pouze 30 % pacientů léčených placebem (14). Potenciální místo abataceptu v terapii GCA by tedy mohla potvrdit právě probíhající multicentrická randomizovaná, dvojitě zaslepená studie ABAGART.
Mezi řadu dalších terapeutických kandidátů, u kterých nyní probíhají 3. fáze klinického hodnocení, patří například inhibitor IL-17 A secukinumab nebo zástupce relativně nové terapeutické skupiny inhibitorů Janusových kináz (JAKi) upadacitinib v rámci probíhající multicentrické dvojitě zaslepené studie SELECT‑GCA. Dalším zkoumaným zástupcem této skupiny je pak baricitinib, prozatím v rámci prospektivní otevřené studie u relabující GCA. V déledobém horizontu se jako další vhodní adepti k provedení plnohodnotné 3. fáze klinického hodnocení jeví též duální inhibitor IL-12/IL-23 ustekinumab, který vykázal příznivý efekt v malé otevřené studii u pacientů vyžadujících setrvalé vyšší dávky kortikoidů (15) či inhibitor kolonie stimulujícího faktoru granulocytů a makrofágů (GM‑CSF) mavrilimumab, který již prokázal v kombinaci s glukokortikoidy superioritu vůči placebu v dosažení remise aktivní GCA v rámci multicentrické, dvojitě zaslepené placebem kontrolované 2. fáze klinického hodnocení (16).
Závěrečné shrnutí
Závěrem je třeba zdůraznit, že diagnóza obrovskobuněčné arteriitidy by měla být zvažována v diferenciální diagnostice zánětlivých stavů a horečnatých onemocnění nejasného původu, zejména u pacientů starších 50 let věku. V rámci diagnosticko‑terapeutického postupu je poté vhodno mít na paměti následující doporučení (5) (Obr. 6):
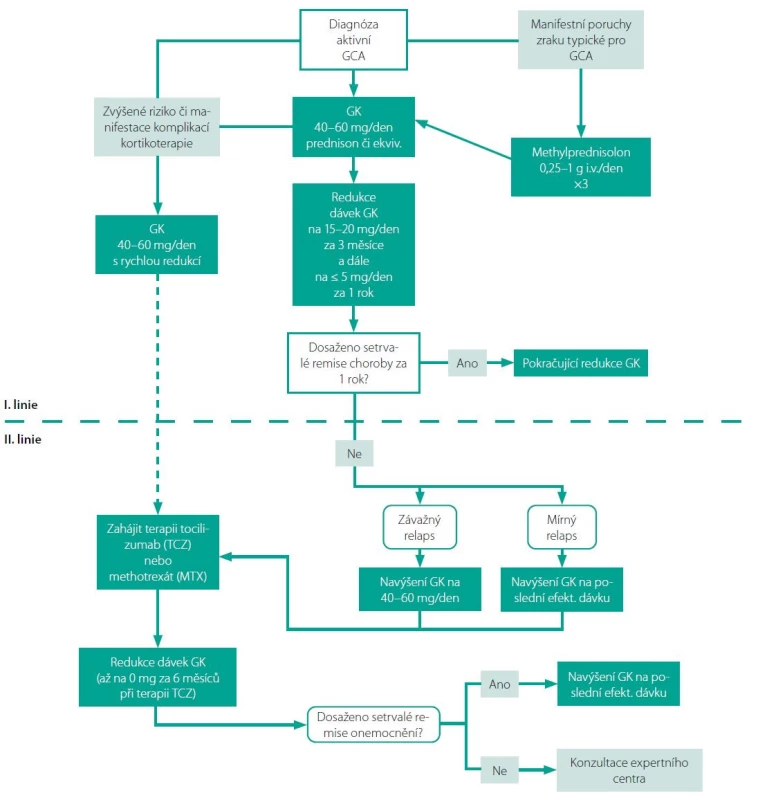
• Všichni pacienti s manifestními symptomy či nálezy svědčícími pro GCA by měli být okamžitě odesláni na specializované pracoviště umožňující multidisciplinární diagnostiku.
• Podezření na vaskulitidu velkých tepen je třeba potvrdit vhodnou zobrazovací metodou – pro aortu či jiné extrakraniální arterie jsou metodou volby USG, CT, PET/CT či MRI. Pro kraniální arterie jsou metodou volby USG či MRI, případně histopatologické vyšetření biopsie temporální arterie.
• U aktivní GCA je třeba zahájit kortikoterapii dávkami nejméně 40–60 mg prednisolonu denně. Jakmile je onemocnění pod kontrolou, cílem je postupné snížení dávek na 15–20 mg/den v průběhu 2–3 měsíců a na ≤ 5 mg/den během 1 roku.
• Doplňující kortikoidy‑šetřící medikace by měla být využívána v případě refrakterního či relabujícího onemocnění nebo při zvýšeném riziku nežádoucích účinků kortikoterapie, lékem volby je tocilizumab, alternativou methotrexát.
• Při závažnějším relapsu choroby (známky ischemie či progredující vaskulitidy) je doporučeno navýšení dávek kortikoterapie odpovídající indukčním dávkám. Při menším relapsu je vhodno navýšit dávku na poslední účinnou.
• Antiagregační a antikoagulační léčba není v rutinní terapii GCA indikována. Ve specifických situacích – ischemické komplikace, vysoké kardiovaskulární riziko – je jejich podávání na individuálním posouzení.
• Je doporučeno dlouhodobé pravidelné klinické sledování pacientů s GCA zahrnující monitoraci subjektivních i objektivních příznaků a zánětlivých parametrů (CRP, FW).
V současnosti probíhá řada klinických hodnocení zkoumajících účinnost široké palety moderních léčiv v terapii GCA. Co se týče rozšíření farmakoterapeutického armamentária a nadějí na zlepšení péče o pacienty s GCA, jeví se budoucnost optimisticky.
Podpořeno granty IGA LF_2022_003 a MZ ČR ‑ RVO FNOL-00098892.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Jakub Videman
3. interní klinika FN Olomouc
I. P. Pavlova 6, 725 00 Olomouc
Cit. zkr: Vnitř Lék. 2022;68(5):266-272
Článek přijat redakcí: 31. 5. 2022
Článek přijat po recenzích: 26. 7. 2022
Sources
1. Gonzalez‑Gay MA, Vazquez‑Rodriguez TR, Lopez‑Diaz MJ et al. Epidemiology of giant cell arteritis and polymyalgia rheumatica. Arthritis Rheum. 2009;61(10):1454.
2. Salvarani C, Hunder GG. Giant cell arteritis with low erythrocyte sedimentation rate: frequency of occurence in a population‑based study. Arthritis Rheum. 2001;45(2):140.
3. Roche NE, Fulbright JW, Wagner AD et al. Correlation of interleukin-6 production and disease activity in polymyalgia rheumatica and giant cell arteritis. Arthritis Rheum. 1993;36(9):1286.
4. Sammel AM, Hsiao E, Schembri G et al. Diagnostic Accuracy of Positron Emission Tomography/ Computed Tomography of the Head, Neck, and Chest for Giant Cell Arteritis: A Prospective, Double‑Blind, Cross‑Sectional Study. Arthritis Rheumatol. 2019 Aug;71(8):1319-1328.
5. Schmidt WA. Ultrasound in the diagnosis and management of giant cell arteritis. Rheumatology (Oxford). 2018 Feb 1;57(suppl_2):ii22-ii31.
6. Hellmich B, Agueda A, Monti S, et al. 2018 Update of the EULAR recommendations for the management of large vessel vasculitis. Ann. Rheum. 2020;79 : 19-30.
7. Aiello PD, Trautmann JC, McPhee TJ et al. Visual prognosis in giant cell arteritis. Ophthalmology. 1993;100(4):550.
8. Mahr AD, Jover JA, Spiera RF et al. Adjunctive methotrexate for treatment of giant cell arteritis: an individual patient data meta‑analysis. Arthritis Rheum. 2007 Aug;56(8):2789-97.
9. De Boysson H, Boutemy J, Creveuil C et al. Is there a place for cyclophosphamide in the treatment of giant ‑ cell arteritis? A case series and systematic review. Semin Arthritis Rheum. 2013;43(1):105.
10. Villiger PM, Adler S, Kuchen S et al. Tocilizumab for induction and maintenance of remission in giant cell arteritis: A phase 2, randomised, double‑blind, placebo ‑ controlled trial. Lancet. 2016;387(10031):1921.
11. Unizony S, Arias‑Urdaneta L, Miloslavsky E et al. Tocilizumab for the treatment of large‑vessel vasculitis (giant cell arteritis, Takayasu arteritis) and polymyalgia rheumatica. Arthritis Care Res (Hoboken). 2012 Nov;64(11):1720-9.
12. Hoffman GS, Cid MC, Rendt‑Zagar KE et al. Infliximab for maintenance of glucocorticosteroid ‑ induced remission of giant cell arteritis: a randomized trial. Ann Intern Med. 2007;146(9):621.
13. Schmidt WA, Dasgupta B, Luqmani R et al. A Multicentre, Randomised, Double‑Blind, Placebo‑Controlled, Parallel‑Group Study to Evaluate the Efficacy and Safety of Sirukumab in the Treatment of Giant Cell Arteritis. Rheumatol Ther. 2020 Dec;7(4):793-810.
14. Langford CA, Cuthbertson D, Ytterberg SR et al. A Randomized, Double‑Blind Trial of Abatacept (CTLA-4Ig) for the Treatment of Giant Cell Arteritis. Arthritis Rheumatol. 2017;69(4):837.
15. Conway R, O‘Neill L, Gallagher P et al. Ustekinumab for refractory giant cell arteritis: A prospective 52-week trial. Semin Arthritis Rheum. 2018 Dec;48(3):523-528.
16. Cid MC, Unizony SH, Blockmans D et al. Efficacy and safety of mavrilimumab in giant cell arteritis: a phase 2, randomised, double‑blind, placebo ‑ controlled trial. Ann Rheum, DiS. 2022 May;81(5):653-661.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2022 Issue 5
-
All articles in this issue
- Hlavní téma – Aktuality v revmatologii
- Léčba obrovskobuněčné arteriitidy – současnost a otevírající se možnosti
- Co nového v léčbě systémového lupus erytematodes?
- Novinky v léčbě axiálních spondyloartritid
- Časná diagnostika systémové sklerodermie
- Difuzní alveolární hemoragie jako život ohrožující manifestace nově diagnostikované granulomatózy s polyangiitidou navazující na infekci covid-19 – kazuistika
- Co je nového v doporučeních ESC 2021 pro kardiovaskulární prevenci?
- Proč brát vážně orgánové poškození u hypertenze?
- Zánět a vaskulární onemocnění
- Time in range: nový parametr v diabetologii
- Co je nového v Doporučených postupech ESC 2020 pro diagnostiku a léčbu akutních koronárních syndromů bez ST elevací?
- Diferenciální diagnostika bolestí zad
- Entresto (sakubitril-valsartan) získalo prestižní mezinárodní Galénovu cenu za nejlepší farmaceutický produkt pro rok 2022
- XXXIX. dny mladých internistů v Martině
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Diferenciální diagnostika bolestí zad
- Časná diagnostika systémové sklerodermie
- Co je nového v doporučeních ESC 2021 pro kardiovaskulární prevenci?
- Co nového v léčbě systémového lupus erytematodes?
