Diferenciální diagnostika urychlení sedimentace erytrocytů
Differential diagnosis of increased Erythrocyte Sedimentation rate
The paper is aimed at differential diagnosis of increased sedimentation rate (ESR) from the point of internal medicine. After the interpretation of the term we describe the technique of the examination and possible errors in pre-analytical as well as analytical phase. The paper includes ranges for conventional FW assessment (analysis of ESR based on Fahraeus-Westergren) and the characteristics of newer methods. We list the overview of the most common causes that affect faster or slower ESR. The stress is put on the assessment of the causes of increased ESR and its persistence from the perspective of clinical practice, we also describe diseases with slower ESR.
Attention is drawn to the comparison of the results of the most common acute phase reactants, especially to discordant results of ESR, CRP and procalcitonin in the serum, and to the contribution of the analysis of ESR and CRP in selected diseases. The final part is aimed at the correct diagnostic approach when assessing increased ESR of unknown etiology, underlining the significance of the patient´s history, physical examination and the position of basic as well as complementary laboratory methods and examinations including imaging techniques.
Keywords:
procalcitonin – diagnostic approach – C‑reactive protein – differential diagnosis of increased and decreased erythrocyte sedimentation rate – normal ESR ranges – ESR of unknown etiology – Fahreus‑Westergren method
Authors:
Vlastimil Ščudla; Pavel Horák
Authors‘ workplace:
III. interní klinika – nefrologická, revmatologická a endokrinologická LF UP a FN, Olomouc
Published in:
Vnitř Lék 2023; 69(1): 48-56
Category:
Differential Diagnosis Column or What You Can Be Asked at a Postgraduate Certification Exam
doi:
https://doi.org/10.36290/vnl.2023.007
Overview
Náplní sdělení je problematika diferenciální diagnostiky urychlení sedimentace erytrocytů (SE) z pohledu interní medicíny. Vedle vymezení pojmu jsou popsány technika vyšetření, chyby v preanalytické i analytické fázi, referenční hodnoty klasického FW vyšetření (podle Fahraeuse‑Westergrena), charakteristika novějších metod a zejména je rozveden přehled základních příčin vedoucích k urychlení, případně ke zpomalení rychlosti SE. Stěžejní náplní článku je rozbor příčin urychlení SE a její případné perzistence z pohledu klinické praxe, popsány jsou i chorobné stavy, vyznačující se zpomalením SE. Zvláštní pozornost je věnována srovnání výsledků vyšetření vybraných reaktantů akutní fáze, a to zejména z pohledu nesouladu výsledků vyšetření SE, CRP a prokalcitoninu v séru, samostatně je uveden přínos analýzy SE a CRP u vybraných chorobných stavů. Sdělení uzavírá diagnostický postup při řešení SE nejasné etiologie (SENE) se zhodnocením významu anamnézy, fyzikálního vyšetření a postavení základních i výběrových laboratorních metod a pomocných vyšetření včetně metod zobrazovacích.
Klíčová slova:
prokalcitonin – diagnostický postup – C‑reaktivní protein – diferenciální diagnostika zvýšené hodnoty sedimentace erytrocytů – diferenciální diagnostika snížené hodnoty sedimentace erytrocytů – referenční hodnoty sedimentace erytrocytů – sedimentace erytrocytů nejasné etiologie – Fahreusova‑Westergrenova metoda
Úvod
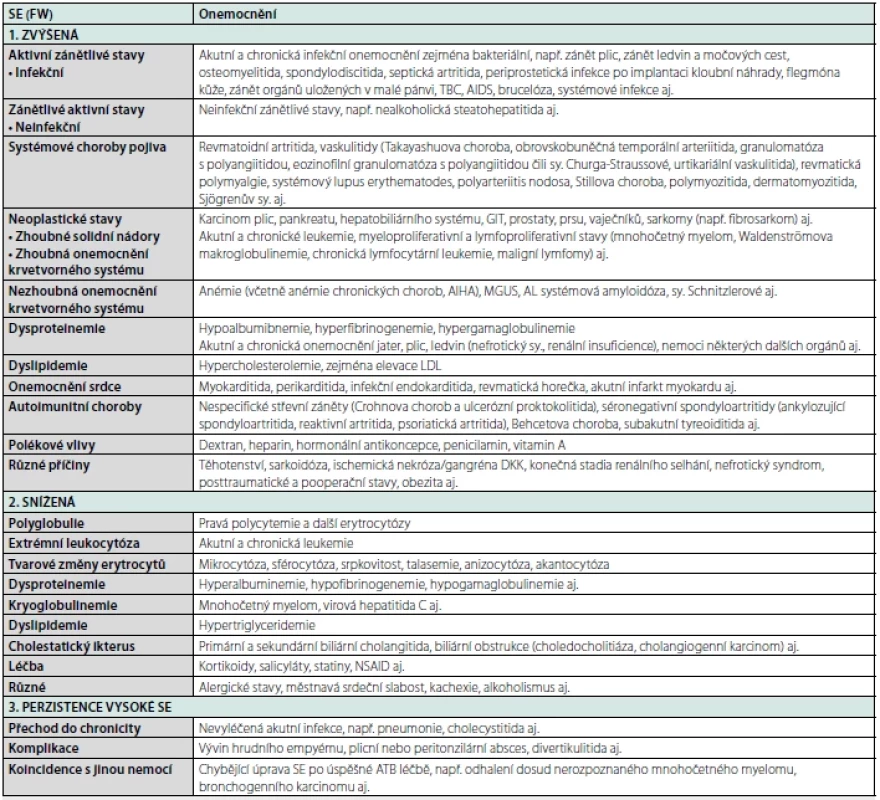
Sedimentace erytrocytů (SE, resp. FW podle průkopníků testu dle Fahraeuse‑Westergrena) je nepřímý ukazatel reakce akutní fáze (RAF) hodnotící rychlost samovolného poklesu a usazování erytrocytů vyjádřený v mm/1 hod. ve vzorku nesrážlivé citrátové krve umístěné v kalibrované, svisle uložené sedimentační trubici (1). Jde o jednu z nejstarších, stále však používanou laboratorní metodou v lékařské praxi jako součásti dalších vyšetření indikovaných k objasnění přítomných projevů nemoci (2). Toto senzitivní, ale nespecifické vyšetření krve, objevené již v roce 1897 polským lékařem E. Biernackim, se vyznačuje jednoduchostí, rychlostí, snadnou proveditelností a nízkými náklady, obvykle upozorňující s výjimkou gravidity na přítomnost chorobného stavu (potenciální „indikátor nemoci“). Zjištěné urychlení SE bývá nezřídka významným impulzem k zahájení pátrání po chorobného dění v organismu. V klinické praxi je zjištění zrychlené SE považováno za „signální“ ukazatel, využívaný v případě nespecifických příznaků nebo asymptomatického stavu při podezření na přítomnost nemoci. Abnormální výsledek vyšetření SE neumožňuje sám o sobě stanovení diagnózy či příčiny nemoci a není ani automatickou výzvou k zahájení terapie (3). V klinické praxi je urychlení SE obvykle svědectvím systémové infekce, neinfekčního zánětu, nádorové, autoimunitní či metabolické nemoci, případně řady dalších, méně často se vyskytujících chorobných stavů (Tab. 1) (4, 5). Výše hodnoty SE odráží širokou plejádu změn v organismu navozených nemocí. Její provedení je indikováno zejména v případě horečky nejasné etiologie, bolestí svalů, kloubů, nejasných bolestí hlavy, zad či bolestivé ztuhlosti pažních a kyčelních pletenců, ale i nechutenství se ztrátou hmotnosti, zjištěné chudokrevnosti a případně dalších významných příznaků nemoci (3, 6). S určitou interpretační obezřetností se uplatňuje zejména v diagnostickém screeningu, neboť normální hodnota SE až na výjimky prakticky vylučuje např. diagnózu revmatické polymyalgie (RP) a obrovskobuněčné (temporální) arteriitidy (giant cell arteritis – GCA). K hodnocení výsledku SE je nutno vždy přistupovat v kontextu klinického obrazu a výsledků specifických laboratorních testů včetně zohlednění vlivů, na nichž je rychlost SE závislá. Vždy je nutno brát v potaz, že k jejímu urychlení dochází s nejméně 1–2denním zpožděním od počátku nemoci, např. u bakteriálního zánětu až po vzestupu teploty a/nebo počtu leukocytů. Opakované vyšetření SE přispívá k hodnocení vývoje již dříve rozpoznaného stavu, tj. příznivé léčebné reakce, nebo naopak její absence či progrese nemoci (7, 8). Normální hodnota SE není sama o sobě indikátorem zdraví a přítomnost nemoci zcela nevylučuje, není proto vhodným a spolehlivým screeningovým testem u klinicky bezpříznakových jedinců. Potřebnost SE v současné klinické praxi byla některými autory pro relativní necitlivost a nespecificitu opakovaně zpochybněna a do značné míry nahrazena vyšetřením hladiny CRP, případně prokalcitoninu (PCT) v séru. Přes uvedené výhrady a dobrou dostupnost přesnějších a specifičtějších laboratorních testů je vyšetření SE i v současnosti přínosnou součástí diagnostické praxe.
Způsob vyšetření
Standardní klasická metoda: Odběr krve na vyšetření SE ze žíly nevyžaduje zvláštní přípravu a provádí se vždy nalačno, neboť zejména po tučném jídle může dojít k urychlení sedimentační rychlosti. Odebírá se 1,6 ml krve do suché zkumavky s 0,4 ml Na‑citrátu a následně nasaje při pokojové teplotě ~ 20 °C do skleněné, kalibrované, 20 cm dlouhé a 2,5 mm široké sedimentační pipety (Westergrenova pipeta) svisle umístěné ve stojanu. Po 1 hod. (historicky i po 2 hod.) se provádí odečet rychlosti SE podle úrovně horní hranice sloupce erytrocytů oddělených v důsledku gravitace proti plazmě (1, 3, 9). V procesu SE lze rozpoznat 3 fáze: v 1. penízkovatění (tvorba „rouleaux“), v 2. usazování agregátů červených krvinek a v konečné, tj. ve 3. fázi zpomalení rychlosti sedimentace v důsledku natlačení agregátů erytrocytů na dno sedimentační trubice („packing stage“). Přesnost určení horní hranice sloupce usazených erytrocytů může znesnadnit příliš ikterický a/nebo růžový vzorek v důsledku ikteru nebo přítomnosti volného hemoglobinu v rámci význačné intravaskulární hemolýzy (7). V případě pochybnosti o správnosti prvního měření je možno celé vyšetření zopakovat. Tato zavedená, referenční metoda měření rychlosti SE a její validace přijatá za „zlatý standard“ ICSH (International Committee for Standardization in Haematology) vychází z postupu popsaného již v roce 1921 Westergrenem (9, 10, 11). V případě použití modifikované metody založené na sklonu trubice 45O se provádí odečet již za 7 minut, případně i za další 3 minuty.
Chyby v preanalytické a analytické fázi vyšetření SE: Při měření je nutná prevence interferujících faktorů vedoucích k urychlení SE, tj. sezónně vyšší pokojová teplota, ostrý sluneční svit, přítomnost okolní vibrace, šikmá poloha a neúplná náplň sedimentační kapiláry, vadná diluce aj. Ke zpomalení SE dochází naopak v důsledku nízké pokojové teploty, vzduchových bublin v kapiláře a více nežli 2 hod. časového odstupu mezi odběrem a instalací krve do sedimentační trubice vedoucí k vývinu sféroidních erytrocytů a částečnému srážení krve omezujícímu vývin „rouleaux“ erytrocytů aj. (12, 13).
Novější metody: Jsou založeny na centrifugaci a použití specializovaných automatických zařízení (7). V některých laboratořích je preferován automatizovaný sterilní bezpečnostní vakuový systém, používající uzavřenou vakuovou pipetu s preparační dávkou citrátu zkracující vyšetření a snižující biologické riziko pro vyšetřující (14, 15). Některé laboratoře používají metodu „stopped flow“ („zastavení průtoku“), při níž se v nesrážlivé venózní krvi s EDTA měří kinetika první fáze sedimentace erytrocytů, tj. jejich agregace („rouleaux“) v prvních 20 sekundách, a s pomocí matematického modelu je vypočtena rychlost SE v mm/1 hod. (16). Použití automatizovaných technik vede ke zrychlení vyšetření, vyšší laboratorní bezpečnosti a ke zlepšení reproduktibility výsledků, referenční hodnoty SE se ovšem od zavedené klasické FW metody podstatně liší (17). Z dříve vypracovaných metod se v současnosti ve velmi omezené míře používá pouze méně citlivá metoda dle Wintrobea, používající užší, 100 mm dlouhou sedimentační kapiláru (18), nikoliv ale již např. metoda Linzenmeierova a Cutlerova.
Referenční hodnoty klasického FW testu (podle R. S. Fahraeuse a A. V. Westergrena): U zdravého člověka je rychlost sedimentace erytrocytů v nesrážlivé krvi pozvolná a konstantní. Ve věku < 50 let: muži 3–8 (≤ 15); ženy 6–11 (≤ 20) mm/hod.; > 50 let: za ještě normální je u mužů považována hodnota SE ≤ 20 a u žen ≤ 30 mm/hod. (2, 19).
K výpočtu horní hranice normálního rozmezí SE lze použít vzorec respektující vyšší SE u žen a v seniorském věku: muži = věk : 2; ženy = (věk + 10) : 2 (1, 19, 20). Příčinou rychlejší SE u žen je přirozeně nižší počet červených krvinek a vyšší koncentrace fibrinogenu v krvi, což ale platí především pro těhotenství. Lehké urychlení SE je fyziologicky přítomno v premenstruu, v případě hormonální antikoncepce a od 4. týdne gravidity. Rychlost SE < 3 mm/hod. je abnormální, zatímco hodnota SE > 100 mm/hod. je obvykle podmíněna přítomností aktivní, závažné nemoci.
Příčiny vedoucí ke změně rychlosti SE
Rychlost SE není důsledkem změny jednoho markeru, ale komplexní ukazatel shrnující uplatnění a vzájemnou interakci stále se měnících „humorálních“ faktorů a „korpuskulárních“ komponent v důsledku nemoci (7).
Urychlení sedimentace erytrocytů
„Humorální“ složka urychlení SE: Na změně viskozity krve se stěžejním způsobem podílí zvýšená koncentrace fibrinogenu v krvi, změna hladiny imunoglobulinů (více IgM nežli IgG) a přítomnost monoklonálního imunoglobulinu (MIg) v séru. K participujícím faktorům patří vzestup hladiny CRP (syntéza v játrech závisí na reakci interferonu, IL-6, IL-1 a TNF-α, tumory‑α nekrotizujícího faktoru), RAF, např. haptoglobinu, protrombinu, plazminogenu, α1-antitrypsinu, antagonisty IL-1R, hepcidinu, feritinu, PCT a dílčích složek komplementu v séru, k nimž dochází v průběhu různých chorobných, zejména zánětlivých stavů (1, 7).
„Korpuskulární“ komponenty urychlení SE: sedimentační rychlost závisí především na velikosti sedimentujících částic. Tato „nezánětlivá“ příčina urychlené SE zahrnuje snížení počtu (anémie) a změnu velikosti erytrocytů (makrocytóza), zejména ale jejich sklon ke shlukování, neboť válcovité aglomeráty červených krvinek se v procesu „rouleaux“ stávají těžšími a sedimentují rychleji nežli samotné erytrocyty (1, 3, 7, 8, 12). U zdravého člověka je SE stálá a pomalá, neboť erytrocyty se spojují v pouze malé shluky, zatímco u chorobných stavů dochází k urychlení SE v důsledku tvorby větších a početných, rychle sedimentujících agregátů.
Souhrnné faktory urychlující SE: Na urychlení SE se podílí zejména změna složení plazmy vedoucí ke změně agregability erytrocytů, a to především hyperfibrinogenemie (např. těhotenství, infekce, diabetes mellitus, nádorové choroby a onemocnění srdce), přítomnost MIg v séru (zejména mnohočetný myelom–MM a Waldenströmova makroglobulinemie–WM), vysoká hladina cirkulujících imunokomplexů a imunoglobulinů (systémová onemocnění pojiva, vaskulitidy a autoimunitní nemoci), ale i elevace dusíkatých katabolitů (renální insuficience), hypoalbuminemie (zánětlivé a nádorové stavy), acidóza, dyslipidemie (zejména zvýšení „low density lipoproteinu“ – LDL), zvýšená hladina haptoglobinu (hemolytická anémie), přítomnost anti‑erytrocytárních protilátek (Coombs‑pozitivní hemolýza), ale i léčba dextranem, heparinem, penicilaminem, vitaminem A aj. (1, 3, 7).
Zpomalení rychlosti sedimentace erytrocytů
Existuje řada faktorů vedoucích k podstatnému zpomalení přirozené rychlosti SE nebo k nálezu nižší nežli očekávané hodnoty, např. nízká SE v případě systémového zánětu.
Faktory zpomalující rychlost SE: Podstatně zvýšená viskozita krve (např. vysoký počet erytrocytů u pravé polycytemie či jiných erytrocytóz a extrémně vysoký počet leukocytů u leukemie), ale i zpomalení v rámci nápadné mikrocytózy, anisocytózy, akantocytózy, přítomnosti srpkovitosti a sférocytózy, tj. okolností omezujících tvorbu „rouleaux“ (1, 7, 8, 12). K dalším příčinám patří dysproteinemie, např. hyperalbuminemie, hypofibrinogenemie a hypogamaglobulinemie, alkalóza a význačná hyperbilirubinemie s vysokou hladinou žlučových kyselin, k určitému zpomalení vede i chronická fyzická zátěž (7) a pravidelný abúzus alkoholu (7, 8) (Tab. 1). Zajímavým zjištěním je odhalení inverzního vztahu mezi výší SE a mutací HBB genu (p. Gln40stop) u obyvatel Sardinie trpících beta‑talasemií (21).
DD rozvaha
Odhalení příčiny výrazného urychlení SE je nezřídka svízelný úkol a vyžaduje soustředěné myšlenkové nasazení zkušeného a erudovaného lékaře s dobrými analytickými schopnostmi.
Zvýšená hodnota SE
S různě zvýšenou hodnotou SE se setkáváme u široké plejády akutních i chronických chorobných stavů, zejména ale v případě aktivních zánětů infekční etiologie i neinfekčního původu, systémových chorob pojiva a dalších autoimunitních onemocnění, nádorových stavů (včetně zhoubných onemocnění krvetvorného systému), nezhoubných onemocnění hematopoézy, dysproteinemie, dyslipidemie (zejména hypercholesterolemie s elevací LDL frakce) a u široké škály dalších onemocnění různé etiologie, podrobněji rozvedených v tabelárním přehledu (Tab. 1) (1, 4, 5, 7). Z míry urychlení SE lze do jisté míry usuzovat na závažnost chorobného stavu, nicméně sedimentační rychlost nemusí vždy spolehlivě odrážet aktuální klinickou situaci.
Urychlená SE zánětlivého původu: I v současnosti zaujímá vyšetření SE významné postavení v řešení „horečky nejasné etiologie-HNE“, neboť může pomoci v nasměrování diagnostického procesu, např. v případě obrovskobuněčné (temporální) arteriitidy (GCA), PR, Kawasakiho nemoci či Takayashuovy arteriitidy (1, 3, 7). V případě osteomyelitidy existuje na rozdíl od septické artritidy a periprostetického zánětu kyčelního nebo kolenního kloubu dobrá korelace výše SE a CRP s tíží zánětu a s reakcí na efektivní léčbu (7, 12, 22, 23). S obvyklou elevací SE, CRP, případně dalších RAF přispívajících k hodnocení tíže, aktivity a účinnosti léčby se setkáváme vedle RA rovněž v případě Stillovy nemoci v dospělosti („adult‑onset Sill’s disease“ – AOSD) (24, 25) a v menší míře i u granulomatózy s polyangiitidou, ankylozující spondyloartritidy, smíšené nemoci pojiva a Behcetově syndromu (1, 6). Přes výše uvedené výhrady poskytuje vyšetření SE významnou informaci přispívající v případě příznačné anamnézy (např. u PR) a fyzikálního nálezu (např. u GCA) k dosažení správného diagnostického závěru (26).
Výše hodnoty SE: K diferenciálně‑diagnostickému významu zvýšené hodnoty SE přispívá stupeň urychlení, tj. lehký (< 50), střední (50–100) a velmi urychlený stupeň (> 100 mm/hod.) (Tab. 2).
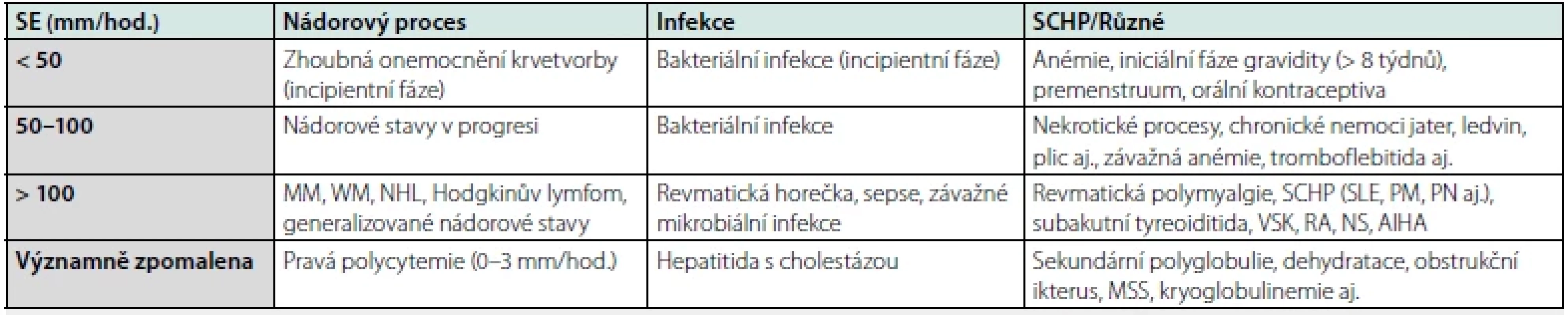
Vysoce urychlená SE: Extrémně vysoká hodnota SE (> 100 mm/ hod.) se vyskytuje s pouze nízkou falešnou pozitivitou u velmi závažných chorobných stavů (27, 28), např. v případě velmi závažné infekce, pokročilého mnohočetného myelomu (MM), Waldenströmovy makroglobulinemie (WM), generalizovaného/metastatického zhoubného procesu, systémové choroby pojiva včetně vaskulitid, maligního lymfomu s vysokým stupněm zhoubnosti, častou příčinou vysoce urychlené SE je rovněž PR a GCA, u níž se považuje spolu s CRP vysoká hodnota SE za relativně specifický biomarker (Tab. 2) (12, 29).
Urychlení SE nezánětlivého původu: K lehkému urychlení sedimentační rychlosti dochází v pokročilém věku a u žen (viz vzorec výpočtu SE) (10, 12), u významnější anémie, v konečné fázi renálního selhání (20 % > 100 mm/hod.) a u nefrotického syndromu (existence pozitivní korelace tíže proteinurie s rychlostí SE). Urychlení SE může provázet taktéž akutní infarkt myokardu (30) a ischemickou akutní cévní mozkovou příhodu (31). V klinické praxi přispívá zvýšená hodnota SE k odlišení zánětlivé od nezánětlivé artritidy (26). Nutno ale zohlednit, že k elevaci hodnoty SE může dojít i u nezánětlivé artritidy v případě koincidence se situacemi, vyznačujícími se urychlením SE, např. při současné renální insuficienci, dysproteinemii, hyperlipoproteinemii a/ nebo doposud nerozpoznané iniciální fázi zhoubného onemocnění, zatímco v případě osteoartrózy v důsledku obvykle vysokého věku (26). Zvýšená hodnota SE navozená vysokou hodnotou fibrinogenu a/ nebo haptoglobinu v séru bez souběžné elevace ostatních RAF, a vysoká hodnota CRP v důsledku zvýšené produkce IL-6 tukovou tkání se vyskytuje v případě obezity. U nádorových stavů, např. u Hodgkinova lymfomu, melanomu, karcinomu ledviny, prsu, prostaty, a zhoubného tumoru kolorektální oblasti, představuje často vyšetření RAF včetně SE přínosný ukazatel nádorové rekurence a prognózy. Jde rovněž o ukazatele, přispívající k odlišení zhoubného, tj. klonálního vs. reaktivního, tj. polyklonálního procesu (12).
Výskyt výrazně zvýšené hodnoty SE (> 100 mm/hod.): V jedné z předchozích studií byla příčinou enormního urychlení sedimentační rychlosti erytrocytů v 33 % infekce, v 17 % nádorové onemocnění, v 17 % nemoci ledvin a 14 % neinfekční zánětlivé stavy (1).
Monitorace zvýšené hodnoty SE: Umožňuje sledování průběhu nemoci včetně hodnocení léčebné odezvy, detekci přechodu nemoci do chronické fáze nebo odhalení komplikace, např. peritonzilárního abscesu po akutní tonzilitidě. Nezřídka může perzistence vysoké hodnoty SE upozornit na přítomnost jiného, doposud neodhaleného onemocnění, např. perzistence značně vysoké SE po úspěšné léčbě zánětu plic by měla vést k pomyšlení na možnost skrytého zhoubného nádorového stavu nebo jiné závažné nemoci.
Perzistence vysoké hodnoty SE: Přetrvávání zvýšené hodnoty SE po prodělání akutního chorobného stavu obvykle signalizuje přechod nemoci přes podanou léčbu do chronické fáze, vývin komplikace, případně koincidenci s jinou závažnou nemocí, např. perzistence vysoké SE po vyléčení zánětu plic v případě doposud nerozpoznaného MM (Tab. 1). U 6 % jedinců v populaci se vyskytuje středně zvýšená hodnota SE, kterou se nepodařilo přes předchozí vyšetřovací úsilí objasnit a jejíž příčina zůstává dlouhodobě nejasná jako tzv. vysoká „SE nejasné etiologie“ (SENE).
Snížená hodnota SE
S velmi sníženou hodnotou SE (1–3 mm/hod.) je nutno počítat v důsledku vysoké viskozity krve např. u pravé polycytemie (PV) a dalších erytrocytóz, s méně nápadným zpomalením se lze setkat u cholestatického ikteru, kryoglobulinemie (chladová gelifikace kryoglobulinu při poklesu teploty vzorku krve v sedimentační trubici pod hodnotu teploty těla), u hyperalbuminemie, hypertriglyceridemie, hypofibrinogenemie, hypogamaglobulinemie, alkalózy, u extrémní leukocytózy, mikrocytární anémie, hereditární sférocytózy, talasemie, srpkovité anémie (Tab. 1) (1, 3). Z klinického pohledu je nutno počítat se zpomalením SE u alergických stavů, městnavé srdeční slabosti, kachexii a s „falešně“ nižší hodnotou SE při léčbě kortikoidy, salicyláty, statiny a nesteroidními antirevmatiky (1, 2, 20, 32, 33). Se zpomalením SE se rovněž setkáváme u chronického alkoholismu a vysoké fyzické zátěže (7, 8, 32). Nezohlednění výše uvedených vlivů při klinické interpretaci zpomalené rychlosti SE může vést k narušení diagnostické rozvahy (7).
Normální hodnota SE
Zjištění normální hodnoty SE přítomnost závažné choroby zásadně nevylučuje, neboť může jít např. o počáteční, ohraničenou fázi nemoci, virové onemocnění bez bakteriální superinfekce, degenerativní onemocnění bez zánětlivé komponenty (např. osteoartróza), překvapivě někdy i u nádorových stavů, především ale v důsledku přítomnosti faktorů zpomalujících SE.
Srovnání výsledků vyšetření vybraných reaktantů akutní fáze
Nesoulad mezi výsledkem SE a koncentrace CRP: Je vyvolán odlišnou výpovědní schopností SE a CRP vyplývající z odlišné podstaty a reaktibility obou metod. Hodnota SE odpovídá rychlosti sedimentace červených krvinek v sedimentační trubici, zatímco hodnota CRP koncentraci tohoto specifického proteinu v séru (8, 10, 12). Na jejich odlišné výpovědní schopnosti se mj. uplatňuje odlišná produkce zánětlivých cytokinů (IL-6, IL-1, TNF‑α aj.) a jejich modulátorů u různých chorob, v případě SE uplatnění „korpuskulární“ složky, tj. tvorby „rouleaux“ s případnou přítomností dalších faktorů ovlivňujících reologické vlastnosti a viskozitu krve (20).
CRP v séru
Jde o tzv. pravý RAF, vyznačující se vysokou kinetikou s rychlou syntézou a katabolismem. Při jeho hodnocení je důležité zohlednění okolnosti, že jeho hladina stoupá s věkem, je vyšší u žen (muži: věk/5, ženy: věk/5 + 0,6 mg/l), v případě obezity, abúzu nikotinu a zejména v případě horečnatého stavu. Dynamika změn koncentrace CRP v séru je rychlá a v souladu s progresí nebo ústupem zánětu, jde tedy o vhodný a pružný ukazatel pro monitoraci zánětlivé reakce, tj. aktuální aktivity, závažnosti, progrese, regrese a rekurence nemoci nebo naopak jejího ústupu či vymizení. V průběhu bakteriální infekce se CRP vyznačuje okamžitým (do 4–6 hod.) vzestupem syntézy s dosažením nejvyšší hodnoty v průběhu ~ 36 hod. a s rychlou úpravou po odeznění akutního zánětu ~ po 24–48 hod. Příčinou vzestupu CRP je infekční zánět (bakteriální, nikoliv virový), z neinfekčních zánětlivých stavů autoimunitní nemoci (např. Crohnova choroba, vaskulitidy, RA, GCA a PR), nádorové stavy (některé maligní solidní tumory a zhoubná onemocnění krvetvorby), určité metabolické dysbalance (např. renální insuficience), závažné posttraumatické stavy a syndrom ARDS (acute respiratory distress syndrome, akutní respirační tíseň dospělých) aj. Mimořádně vysoké hodnoty CRP v séru se vyskytují spíše u infekčního, resp. i nádorového stavu, nežli u onemocnění revmatického charakteru (6). U některých chronických infekcí, např. TBC, kapavky, lues či Lymeské boreliózy, k elevaci CRP obvykle nedochází, neboť imunitní systém je stimulován jiným způsobem (34). S nezvýšenou koncentrací CRP v krvi je nutno rovněž počítat v případě sklerodermie a systémového lupusu erythematodes (SLE), i když v případě SLE může provázet elevace CRP přítomnou aktivní lupusovou serositidu, chronickou synovitidu a/nebo současnou bakteriální infekci (12).
Vztah rychlosti SE a koncentrace CRP v séru
Zatímco SE reaguje na průběh nemoci zvolna, koncentrace CRP v séru stoupá velmi rychle a je proto citlivějším i přesnějším ukazatelem reakce akutní fáze nežli SE. K diskrepanci výsledků SE a CRP se setkáváme především v situaci, kdy k urychlení SE dochází na podkladě změny složení krve, tj. dysimunoglobulinemii, paraproteinemii, zejména ale v důsledku změny počtu, velikosti a tvaru erytrocytů (35). K objasnění rozdílného výsledku těchto parametrů je nezbytné vyšetření hemogramu a biochemické vyšetření séra včetně elektroforézy bílkovin.
Normální hodnota CRP v séru prakticky vylučuje závažné akutní bakteriální zánětlivé onemocnění. Na rozdíl od SE slouží nález vysoké hodnoty CRP v séru k rozlišení bakteriální (≥ 40 mg/l) a virové infekce, zatímco k vzestupu SE dochází obvykle u bakteriální i virové infekce. K nárůstu hodnoty SE dochází vždy až po zvýšení koncentrace CRP v séru, a to podstatně pomaleji, obvykle až v odstupu > 48 hod. od začátku zánětu. Rovněž k úpravě rychlosti SE dochází na rozdíl od CRP (již po 24–48 hod.) mnohem pomaleji, nezřídka i v několikatýdenním odstupu (~ 3–4 týdny) od vymizení ostatních projevů nemoci.
Hodnoty SE a CRP často odrážejí intenzitu zánětlivého procesu obdobně, v řadě situací však reagují rozdílně, např. v případě infarktu myokardu a tromboembolické nemoci, u nichž zánětlivá složka nemusí vždy vést k urychlení SE, takže vysoká hladina CRP je provázena normální hodnotou SE (1). Na rozdíl od SE je CRP u mnoha autoimunitních onemocnění, např. u PR, GCA a RA vhodnějším ukazatelem monitorace aktivity nemoci, neboť k jeho vzestupu dochází dříve nežli v případě SE a vesměs souběžně s tíží zánětlivého stavu (6, 29, 35). Vyšetření koncentrace CRP v séru vyznívá rovněž spolehlivěji nežli hodnota SE v případě akutního zánětu u imunitně kompromitovaných jedinců (34). V případě „low grade“ bakteriální infekce kosti a kloubů může být SE vhodnějším ukazatelem intenzity zánětlivého procesu než CRP. Rovněž v případě SLE nedochází na rozdíl od SE obvykle k elevaci CRP (12, 36). U nemocných s MM a WM, vyznačující se většinou významně zrychlenou SE, je vždy účelné současné vyšetření CRP, neboť na jeho koncentraci v séru nemá MIg (M‑protein) bezprostřední vliv (29). Z výše uvedených důvodů se doporučuje v řadě klinických situací provádět vyšetření obou ukazatelů současně a nespoléhat se pouze na výsledek jednoho z nich (8). Srovnání odlišných výsledků vyšetření SE a CRP v séru je podrobněji rozvedeno v tabulce 3.

Prokalcitonin v séru
Tento solubilní prohormon kalcitoninu (PCT) je nespecifický biomarker, uvolňovaný do oběhu především z jater pod patronací zvýšené produkce zánětlivých cytokinů a aktivace monocyto‑makrofágového (Mo–Ma) systému v případě závažného systémového bakteriálního zánětu (34). PCT se vyznačuje velmi rychlou reaktivitou a z klinického pohledu vysokou přesností v rozpoznání bakteriální infekce a septického stavu. K vzestupu hladiny v séru dochází v průběhu 2–4 hod. od stimulace, k 50% poklesu z nejvyšší hodnoty již v průběhu 1–1,5 dne. Tento významný ukazatel bakteriální infekce se vyznačuje lehce vyšší senzitivitou nežli vyšetření CRP, ale mnohem vyšší specificitou, jde proto o vhodnější ukazatel pro rozpoznání sepse nežli CRP (12, 37). Standardní indikací vyšetření PCT v séru v diagnostické praxi je potvrzení, resp. vyloučení bakteriemie, sepse a/nebo septického šoku, zhodnocení jejich závažnosti (vztah výše PCT k závažnosti systémového bakteriálního zánětu) a sledování průběhu mikrobiálního a mykotického systémového zánětu včetně reakce na antibiotickou terapii. Normální hodnoty PCT vylučují systémový bakteriální zánět. Virová infekce stejně jako lokální bakteriální infekce, např. absces či akutní tonzilitida, k vzestupu PCT v séru nevede. Prokalcitonin je na rozdíl od ostatních zánětlivých markerů rovněž vysoce specifickým ukazatelem přítomnosti komplikující bakteriální infekce u autoimunitních nemocí (12).
Vztah hodnot CRP a PCT v séru
Zvýšená hladina PCT v séru je vysoce specifická v detekci bakteriální infekce a ve srovnání s CRP i poněkud citlivější. Vyšetření PCT se proto ve srovnání s CRP vyznačuje v rozpoznání bakteriální infekce, sepse a septického šoku podstatně vyšší diagnostickou přesností a ve srovnání s ostatními RAF i vyšším diferenciálně‑diagnostickým (DD) potenciálem v odlišení virové infekce, zánětů neinfekčního původu a nádorových stavů od zánětu bakteriální etiologie (38).
Ostatní RAF
K „pozitivním“ RAF, reagujícím v průběhu zánětu vzestupem jejich sérové hladiny, patří vedle CRP a prokalcitoninu rovněž ceruloplazmin, dílčí komponenty komplementové kaskády, sérová hladina amyloidové komponenty A (SAA), fibrinogen, alfa-1 antitrypsin, haptoglobin, hemopexin, antagonisté receptoru IL-1 (IL-1R), hepcidin, feritin aj. Je známo, že sérové hladiny SAA a CRP se mění paralelně a podle některých studií je SAA ve srovnání s CRP v detekci zánětlivé reakce dokonce citlivější (12). K hyperferetinickým zánětlivým stavům vyznačující se excesivně vysokou hladinou feritinu v séru patří např. Stillova choroba (systémová forma juvenilní idiopatické artritidy i adultní forma Stillovy choroby), katastrofický antifosfolipidový syndrom, syndrom aktivovaných makrofágů (MAS), těžká sepse a závažná forma infekce SARS‑Cov - 2 provázená cytokinovou bouří. Stanovení IL-6 v séru není v rozpoznání sepse oproti PCT vhodnější, neboť postrádá specificitu (34). Mezi „negativní“ RAF, reagující na přítomnost zánětu poklesem jejich sérové koncentrace patří např. albumin, transferin, transtyretin aj. (12). V průběhu reakce akutní fáze dochází rovněž k poklesu koncentrace železa a zinku v séru, zatímco hladina mědi stoupá (12).
Specifické využití RAF u vybraných chorobných stavů
Revmatoidní artritida: SE a CRP jsou citlivé indikátory aktivity u cca 40 % nemocných a jsou využívány v monitoraci průběhu nemoci a odezvy k léčbě. Vzhledem k tomu, že rychlost SE závisí u RA vedle koncentrace fibrinogenu a imunoglobulinů na mnoha dalších humorálních a korpuskulárních faktorech, nemusí vždy výše SE vystihovat její aktivitu, takže za vhodnější biomarker je považován CRP, k jehož vzestupu dochází dříve a souběžně s tíží zánětlivého procesu (6, 24, 35). Podstatně citlivějším indikátorem aktivity, predikce progrese a detekce subklinické formy RA je přes jisté indikační pochybnosti vyšetření tzv. „multi‑biomarker disease aktivity“ (MBDA), zahrnující vedle SE, CRP a SAA hladiny dalších markerů v séru, např. molekul adheze, růstových faktorů, „cytokine - related“ proteinů, matrix metaloproteinázy aj. (12, 24), tento komplexní parametr si však zatím cestu do praktického použití neproklestil pro svou metodologickou a ekonomickou náročnost. V případě RA je vyšetření SE rovněž součástí hodnocení aktivity dle indexu DAS 28 (Disease Activity Score) hodnotící 28 kloubů.
Revmatická polymyalgie: Je častou příčinou zvýšené hodnoty SE a CRP, vysoká hodnota SE > 100 mm/hod. se vyskytuje u ~ 20 % nemocných. Vyšetření SE a CRP je proto považováno za vhodný přístup v diagnostice a monitorování průběhu a aktivity nemoci s tím, že hladina CRP v séru reaguje ve srovnání se SE dříve a zpravidla odpovídá tíži zánětlivého procesu (6, 12, 29, 35).
Obrovskobuněčná (temporální) arteriitida (GCA): SE a CRP jsou vhodnými biomarkery v diagnostice a monitorování průběhu a aktivity této nemoci. Jejich vysoká hodnota se považuje za relativně specifický biomarker, i když u ~ 1/10 nemocných, především s absencí systémových projevů bývá hodnota SE < 40 mm/hod. (12).
SLE: Na rozdíl od SE jsou hodnoty CRP zpravidla nízké, a to i u aktivní formy nemoci v důsledku inhibice syntézy CRP v játrech v rámci vysoké exprese interferonu I (12, 36). Výjimkou je SLE s přítomností přidružené bakteriální infekce nebo vyjádřené lupusové serositidy a/nebo synovitidy.
Kardiovaskulární nemoci: CRP, především jeho hypersenzitivní forma (HS‑CRP), je považována za biomarker zvýšeného kardiovaskulárního rizika. Vzhledem k překrývání s jinými příčinami se jeho sledování v klinické praxi příliš neosvědčilo.
Infekce: Představuje důležitou příčinu elevace RAF, monitorace jejich hladin umožňuje pružné sledování kinetiky a hloubky léčebné odezvy, např. rychlá úprava CRP a podstatně pozvolnější pokles SE při úspěšné antibiotické léčbě bakteriálních zánětů.
Zhoubná onemocnění: Vyšetření RAF přispívá k vyloučení přítomnosti nebo rekurence některých maligních nádorů a případně i k předpovědi prognózy nemoci. Vyšetření indikátorů zánětlivé reakce neslouží pouze k diagnostice a monitoraci zánětlivého stavu, ale u některých chorobných stavů má i prognostický potenciál, např. u diabetu mellitu II. typu, uremie, akutní cévní mozkové příhody. Zvýšená hodnota rovněž signalizuje „pokročilejší biologický věk“ spojený s nebezpečím vyšší mortality (12).
Diagnostický postup
Odhalení příčiny zrychlené „SE nejasné etiologie“ (SENE) vyžaduje vedle důkladné anamnézy a fyzikálního vyšetření vhodně zvolené spektrum laboratorních a pomocných vyšetření, vycházející z DD rozboru stavu a z pracovní diagnózy. Vysoká hodnota SENE vyžaduje komplexní rozbor s pátráním především po skrytém zánětlivém nebo nádorovém onemocnění, případně i po možnosti méně obvyklé příčiny, a to i mimo sféru interní medicíny, např. gynekologie, urologie, ORL aj. (4, 5) (tab. 1). Nutno připustit, že v ~ 5 %, a to především u bezpříznakových jedinců, se přes podrobné vyšetření nepodaří příčinu zrychlené SE objasnit a nemocného je nutno v několikaměsíčních intervalech sledovat, neboť zjištění navyšování hodnoty SE může přispět k odhalení původně skrytého onemocnění až v různě dlouhém časovém odstupu.
1. Cílená anamnéza
V anamnéze nynějšího onemocnění je nutné zaměření na odhalení celkových nespecifických příznaků nemoci, tj. slabosti, malátnosti, únavnosti, snížené chuti k jídlu s poklesem hmotnosti aj., a příznačných subjektivních stesků upozorňujících na postižení určitého orgánového systému, např. bolestivá ranní ztuhlost drobných ručních kloubů trvající > 30 minut na RA, bolest ramenních a/nebo pánevních pletenců s šířením na šíji a/nebo do hýžďové krajiny na PR, bolest hlavy s případnou poruchou prokrvení HKK a tranzitorním výpadkem zraku („amaurosis fugax“) na GCA, občasná dysurie na exacerbaci chronické pyelonefritidy, projevy postižení zažívacího traktu, tj. neurčité bolesti břicha, průjem, horečka, krev ve stolici aj. na zánětlivé nebo nádorové postižení zažívací trubice, nebo narůstající bolesti páteře nereagující na analgetickou léčbu u jedince v seniorském věku na MM aj. (34).
Osobní anamnéza je zacílena především na podchycení všech předchozích nemocí, jejichž případná reaktivace může vysvětlit opětovný vzestup SE (např. reaktivace TBC plic, infekční endokarditidy, maligního lymfomu aj.).
Rozbor farmakologické anamnézy vede obvykle k ozřejmění charakteru a závažnosti předchozího nebo nynějšího onemocnění, např. léčba kortikoidy u systémové nemoci pojiva, chemoterapie a/ nebo radioterapie či biologická léčba v případě nádorového stavu aj. Rozbor medikace může vysvětlit v některých případech zjištěný nesoulad mezi očekávanou a zjištěnou hodnotou SE v důsledku určité léčby (Tab. 1).
2. Fyzikální vyšetření
Fyzikální vyšetření je v řešení zejména SENE velmi důležité, neboť může vést k nasměrování diferenciálně diagnostické rozvahy, např. lokalizované nebo generalizované zvětšení lymfatických uzlin (infekční, zánětlivá či nádorová lymfadenopatie), splenomegalie (zhoubné onemocnění krvetvorného systému, systémová infekce nebo onemocnění pojivové tkáně aj.), chlopňová srdeční vada (možnost infekční endokarditidy), abnormální auskultační nález na plicích (např. zánět plic, bronchiektázie aj.), bolestivá ranní ztuhlost, prosáknutí a typická deformace metakarpofalangeálních kloubů (RA), ranní ztuhlost s palpační bolestivostí svalstva a omezením rozsahu hybnosti pažních a kyčelních pletenců (PR), palpačně citlivé uzlovité zduření spánkové tepny (GCA), motýlovitý heliotropní exantém tváří (SLE nebo dermatomyozitida), hmatná rezistence v abdominální oblasti (Crohnova choroba, karcinom tlustého střeva, karcinom žlučníku aj.), případně další, nezřídka potenciálně patognomonické nálezy zjištěné při objektivním vyšetření (34).
3. Základní a výběrová laboratorní nebo pomocná vyšetření
Hematologie
KO kompletní: detekce „korpuskulární příčiny“ zvýšené SE, např. anémie, penízkovatění erytrocytů („rouleaux“ u MM a WM), sférocytóza (hereditární sférocytóza), přítomnost schistocytů a přilbovitých fragmentů erytrocytů (mikroangiopatická hemolytická anémie a diseminovaná intravaskulární koagulopatie), leukocytóza s případným posunem doleva (systémový zánět a infekce) či leukemoidní reakce (závažná infekce, septický stav), „hiatus leucaemicus“ (dominance blastů bez granulocytárních prekurzorů v periferní krvi u akutní leukemie), leukoerytroblastické reakce (infiltrace kostní dřeně, např. při zhoubném onemocnění krvetvorby nebo metastatickém postižení kostní dřeně v rámci generalizace zhoubného nádoru aj.), eozinofilie (např. eozinofilní granulomatóza s polyangiitidou čili syndrom Churga‑Straussové aj.), leukopenie (např. febrilní neutropenie) aj. (34).
Výběrově
Biopsie kostní dřeně (KD): vysoká „SE nejasné etiologie“ s abnormálním nálezem v hemogramu je obvykle indikací k biopsii KD (aspirační a/nebo trepanobiopsie) včetně histologie a imunohistologie, případně vícebarevné průtokové cytometrie.
Biochemie
Základní biochemický panel v krevním séru: včetně CRP a fibrinogenu.
Patologické nálezy mohou přispět k odhalení doposud skrytého onemocnění, projevujícího se urychlenou SENE (Tab. 1), např. průkaz monoklonálního imunoglobulinu (paraproteinu) u mnohočetného myelomu, u Waldenströmovy makroglobulinemie či jiné monoklonální gamapatie, ale i dysimunoglobulinemie (např. jaterní cirhóza, vaskulitida), hypoalbuminemie (např. nefrotický syndrom nebo pokročilé zhoubné onemocnění), zvýšené hladiny volných lehkých řetězců imunoglobulinu (VLŘ) κ nebo λ v séru (Freelite test, zejména MM, MW či jiná MG).
Moč: výrazná proteinurie ≥ 3,5 g/24 hod. (nefrotický syndrom u „glomerulopatií“, AL‑amyloidózy aj.), vysoký odbyt VLŘ močí (MM, MW nebo „monoclonal gammopathy of renal significance“–MGRS). Leukocyturie s významnou bakteriurií > 10 × 10/5 (infekce močových cest nebo ledvin), mikroskopická, případně makroskopická hematurie (glomerulopatie, karcinom ledviny nebo vývodných močových cest, TBC ledvin) (34).
Výběrově
Prokalcitonin: případně i některé z ostatních RAF.
Mikrobiologie
Mikrobiologická vyšetření: mikroskopické, kultivační (včetně hemokultury) a sérologické testy jsou většinou klíčovými postupy v rozpoznání a diferenciální diagnostice bakteriální, virové a mykotické infekce provázené zvýšenou SE, CRP a/nebo ostatních RAF.
Výběrově
PCR (polymerázová řetězová reakce) a cíleně zvolené specifické testy zaměřené na méně obvyklá infekční onemocnění, např. TBC.
Imunologie
Vyšetření: revmatoidní faktory, anticitrulinové protilátky, ASLO, ANA (antinukleární protilátky), anti‑dsDNA, Coombsův test a další testy přispívají k rozpoznání zánětlivé revmatické choroby, autoimunitní hemolytické anémie aj.
Výběrově
Speciální vyšetření: elektroforéza Hb (hemoglobinopatie), průkaz kryoglobulinu (kryoglobulinemie I. a II. typu), ANCA (protilátky proti cytoplazmatickému antigenu neutrofilů, u mikroskopické polyangiitidy p‑ANCA, v případně granulomatózy s polyangiitidou c‑ANCA), HLA B27 (Bechtěrevova choroba a další spondyloartritidy), vícebarevná průtoková cytometrie (subklasifikace leukemie, maligního lymfomu aj.).
Zobrazovací metody
RTG vyšetření: radiografie srdce a plic, skeletu na podkladě výsledku diferenciálně-diagnostického rozboru a pracovní diagnózy.
Ultrasonografie: ultrazvukové vyšetření břicha a výběrově dalších orgánů velmi často přispívá k rychlému objasnění vysoké hodnoty SENE.
Výběrově
WB‑CT (celotělová výpočetní tomografie), WB‑MRI (celotělová magnetická rezonance) a zejména FDG‑PET/ CT (fluorodeoxyglukózová‑pozitronová emisní tomografie/výpočetní tomografie): zejména celotělové zobrazovací metody se často rozhodujícím způsobem podílejí na objasnění příčiny vysoké SENE detekcí ložiskového či difuzního zánětlivého nebo nádorového procesu, včetně rozpoznání jeho rozsahu.
Endoskopie: vyšetření GIT nebo průdušek (detekce nádorového nebo zánětlivého postižení trávicí trubice nebo bronchiálního stromu).
Závěr
Ačkoliv zvýšená sedimentace erytrocytů nedefinuje sama o sobě žádnou nemoc, má stále své místo jako pomocný test v diferenciální diagnostice chorobných stavů a v monitoraci aktivity některých nemocí. SE musí být kombinována s jinými vyšetřovacími metodami. Pokud je hladina SE extrémně zvýšená (> 100 mm/hod.), je obvykle přítomna závažná příčina (malignita, infekce, vaskulitida). Pokud je hladina mírně až středně zvýšená bez zjevných příčin a bez dalších alarmujících anamnestických údajů, fyzikálních, laboratorních či zobrazovacích nálezů, může být indikováno pouhé opakování testu, a to u asymptomatického nemocného po několika měsících. Trvale zvýšená SE může vyžadovat extenzivnější pátrání po skryté nemoci.
prof. MUDr. Vlastimil Ščudla, CSc.
III. interní klinika – nefrologická, revmatologická a endokrinologická LF UP a FN, Olomouc
Vlastimil.Scudla@fnol.cz
Cit. zkr: Vnitř Lék. 2023;69(1):48-56
Článek přijat redakcí: 14. 5. 2022
Článek přijat po recenzích: 15. 10. 2022
Sources
1. Wikipedia. Erythrocyte sedimentation rate. Available from: www:en.wikipedia.org/wiki/ erythrocyte_sedimentation rate
2. Cherney K, Goodwin M. Erythrocyte sedimentation rate test (ESR test).Available from: www:healthline.com/health/esr
3. MedlinePlus. Erythrocyte sedimentation rate (ESR). Available from: www:medlineplus. gov/lab‑tests/ erythrocyte‑sedimentation‑rate‑esr/
4. Lukáš K, Žák A. Chorobné znaky a příznaky, diferenciální diagnostika. 1. vyd. Grada: Praha 2014. ISBN 978-80-247-5067-5.
5. Bobek K et al. Základy diferenciální diagnostiky vnitřních nemocí. 1. vyd. Státní zdravotnické nakladatelství: Praha 1963. ISBN 08-061-63.
6. Bitik B, Mercan R, Tufan A, et al. Differential diagnosis of elevated erythrocyte sedimentation rate and C‑reactive protein levels: a rheumatology perspective. Eur J Rheumatol. 2015; 2 : 131-134.
7. Tishkowski K, Gupta V. Erythrocyte sedimentation rate. Available from: www:ncbi.nlm. nih.gov/books/NBK557485/
8. Testing. Com. Erythrocyte sedimentation rate (ESR). Available from: www:testing.com/ tests/erythrocyte‑sedimentation‑rate‑esr/
9. Reference method for the erythrocyte sedimentation rate (ESR) test on human blood. Br J Haematol. 1973;24 : 671-673. Available from: PubMed 4732536.
10. Harrison M. Erythrocyte sedimentation rate and C‑reactive protein. Aust Prescr. 2015;38 : 93-94. Available from: PubMed: 26648629.
11. Kratz A, Plebani M, Peng M et al. International Council for standardization in haematology (ICSH). ICSH reccomendations for modified and alternate methods measuring the erythrocyte sedimentation rate. Int J Lab Hematol. 2017;39 : 448-457. Available from: PubMed: 28497537.
12. Kushner I. Acute phase reactants Available from: www: uptodate.com. UpToDate 2022.
13. Lawrence JS. Sources of error in the erythrocyte sedimentation rate. Ann Rheum Dis. 1953;12 : 206-211. Available from: PubMed:13105212.
14. Plebani M, De Toni S, Sanzari MC, et al. The TEST 1 automated system: a new method for measuring the erythrocyte sedimentation rate. Am J Clin Pathol 1998;110 : 334-340. Available from: PubMed: 9728608.
15. Valkus M, Straňáková L. Stanovení rychlosti sedimentace erytrocytů na analyzátoru ALCOR iSED. Bulliten FONS, 4/2020.
16. Lapić I, Piva E, Spolaore F, et al. Automated measurement of the erythrocyte sedimentation rate: method validation and comparison. Clin Chem Lab Med. 2019;57 : 1364-1373. Available from: PubMed: 30939112.
17. Zlonis M. The mystique of the erythrocyte sedimentation rate. A reappraisal of one of the oldest laboratory tests still in use. Clin Lab Med. 1993;13 : 787-800. Available from: PubMed:8313681.
18. Gilmour D, Sykes AJ. Westergren and Wintrobe methods of estimating ESR compared. Brit Med J. 1951;2 : 1496-1497. Available from: PubMed: 14886634.
19. Miller A, Green M, Robinson D. Simple rule for calculation normal erythrocyte sedimentation rate. Brit Med J 1983; 286 (6361):266, doi:10.1136/bmj.286.6361.266
20. Bray C, Bell LN, Liang H, et al. Erythrocyte sedimentation rate and C‑reactive protein measurements and their relevance in clinical medicine. WMJ 2016;115 : 317-321. www.wisonsinmedicalsociety. org/_WMS/publications/wmj/pdf/115/6/317.pdf).
21. Sidore C, Busonero F, Maschio A, et al. Genome sequencing elucidates Sardinian genetic architecture and augments association analyses for lipid and blood inflammatory markers. Nature Genetics. 2015;47 : 1272-1281. doi:10.1038/ng.3368
22. Orr CK, Najm A, Young F, et al. The utility and limitations of CRP, ESR and DAS28-CRP in appraising disease activity in rheumatoid arthritis. Front Med (Lausanne) 2018;5 : 185. Available from: PubMed 30123796.
23. Saleh A, George J, Faour M, et al. Serum biomarkers in periprosthetic joint infections. Bone Joint Res. 2018;7 : 85-93. Available from: PubMed:29363518.
24. Taylor PC, Deleuran B. Biologic markers in the diagnosis and assessment of rheumatoid arthritis. Available from: www. uptodate.com, UpToDate 2022.
25. Mandl LA. Clinical manifestations and diagnosis of adult‑onset Still’s disease. Available from: www.uptodate.com, UpToDate 2022.
26. Shmerling RH. Evaluation of the adult with polyarticular pain. Available from: www. uptodate.com, UpToDate 2022.
27. Fincher RM, Page MI. Clinical significance of extreme elevation of the erythrocyte sedimentation rate. Arch Intern Med. 1986;146 : 1581-1583. Available from: PubMed: 3729639.
28. Lluberas‑Acosta G, Schumacher HR. Markedly elevated erythrocyte sedimentation rates: consideration of clinical implications in a hospital population. Brit J Clin Pract. 1996;50 : 138-142. Available from: PubMed: 8733332.
29. Salvarani C, Muratore F. Clinical manifestations and diagnosis of polymyalgia rheumatica. Available from: www.uptodate.com, UpToDate 2022.
30. Yayan J. Erythrocyte sedimentation rate as a marker for coronary disease. Vasc Health Risk Manag. 2012;8 : 219-223. Available from: PubMed: 22536077.
31. Chamorro A, Vila N, Ascaso C, et al. Early prediction of stroke severity. Role of the erythrocyte sedimentation rate. Stroke 1995;26 : 573-576. Available from: Pub Med: 7709399.
32. Alende‑Castro V, Alonso‑Sampedro M, Vasquez‑Temprano N, et al. Factors influencing erythrocyte sedimentation rate in adults: New evidence for an old test. Medicine (Baltimore) 2019;98:e16816. Available from: PubMed: 31441853.
33. Hegg R, Lee AG, Tagg NT, et al. Statin or nonsteroidal anti‑inflammatory drug use is associated with lower erythrocyte sedimentation rate in patients with giant cell arteritis. J Neuroophtalmol. 2011;31 : 135-138. Available from: PubMed:21358421.
34. Ščudla V, Horák P, Karásek D, et al. Základy diferenciální diagnostiky ve vnitřním lékařství. 1. vyd. Univerzita Palackého: Olomouc 2022, ISBN – 978-80-244-5957-8.
35. Litao MK, Kamat D. Erythrocyte sedimentation rate and C‑reactive protein: how best to use them in clinical practice. Pediatr Ann, 2014;43 : 417-420.
36. Enochsson H, Sjawal Ch, Skogh T, et al. Interferon I + - mediates supression of C‑reactive protein: explanation for muted C‑reactive protein response in lupus flares? Arthr Rheum. 2009;60 : 3755-3760.
37. Meisner M. Update on procalcitonin measurements. Ann Lab Med. 2014;34 : 263-273. doi:103343/alm.2014. 34. 4263. Available from: www.ncbi.nlm.nih.gov/pmg/articles/ PMC4071182/.
38. Simon L, Gauvin F, Amre DK, et al. Serum procalcitonin and C‑reactive protein levels as markers of bacterial infection: A systematic review and meta‑analysis. Clin Inf Disease 2004;39 : 206-217. Available from: https://doi.org/10.1086/421997.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2023 Issue 1
-
All articles in this issue
- Jistoty a nejistoty na křižovatkách současné medicíny
- Izolovaná plicní embolie – specifická klinická jednotka?
- Co je nového v doporučeních ESC 2022 pro předoperační vyšetření a perioperační péči
- Infekční komplikace syndromu diabetické nohy – diagnostika a léčba
- Dentálne výkony pri perorálnej antitrombotickej liečbe
- Histaminová intolerance
- Črevný mikrobióm a transplantácia obličky
- Diferenciální diagnostika urychlení sedimentace erytrocytů
- Novinky v kardiologii 2022
- ESC 2022 a studie DELIVER
- Zprávy o knihách
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Histaminová intolerance
- Diferenciální diagnostika urychlení sedimentace erytrocytů
- Dentálne výkony pri perorálnej antitrombotickej liečbe
- Co je nového v doporučeních ESC 2022 pro předoperační vyšetření a perioperační péči
