Dárci ledvin po nezvratné zástavě oběhu (DCD) – zkušenosti jednoho centra
Kidney donors after circulatory death (DCD) – single centre experience
Introduction:
Kidney procurement from donors after circulatory death (DCD) is an important part of worldwide transplantation programmes. The first kidney transplantation from DCD was successfully performed in the Czech Republic in 2002.
Method:
Forty four kidneys from DCD were procured in the Transplant Centre of Pilsen between 2002 and 2015. We used the technique of “in situ“ procurement with the double balloon triple lumen catheter and 5−10 minutes of the no-touch interval. The method of pulsatile hypothermic perfusion was used to test the viability of the kidneys. Twenty eight recipients with mean age 51.1 (26−73) years were transplanted. Sixteen (57.1%) kidneys were from the 2nd, 8 (28.6%) from the 3rd and 4 (14.3%) from the 4th category according to the Maastricht criteria.
Results:
30-day mortality and morbidity rates were 0 and 10.7% i. e.14.3% respectively (N=4). Primary non-function was presented in 2 (7.1%), and delayed graft function in 5 (17.9%) cases. One, five and ten years of recipient and graft survival rates were 100%, 86.4% and 76.7%; and 92.9%, 69.6% and 61.9%, respectively. The long-term results are fully comparable with kidneys transplanted from donors after brain death.
Conclusion:
DCD are an important source for kidney transplantation. Kidney transplantation from DCD is a logistically, economically and personally demanding method with very good long-term results.
Key words:
donors after circulatory death – kidney transplantation – results
Authors:
V. Třeška; T. Reischig; D. Hasman; B. Čertík; J. Moláček; R. Šulc; M. Čechura; L. Kielberger; K. Houdek; V. Opatrný
Authors‘ workplace:
Transplantační centrum LF Univerzity Karlovy a FN v Plzni
přednosta: prof. MUDr. V. Třeška, DrSc.
Published in:
Rozhl. Chir., 2016, roč. 95, č. 4, s. 147-150.
Category:
Original articles
Overview
Úvod:
Odběr ledvin z dárce s nezvratnou zástavou oběhu (DCD – donor after circulatory death) je důležitou součástí transplantačních programů v celosvětovém měřítku. V České republice byla první transplantace ledvin z DCD úspěšně provedena v roce 2002. Autoři diskutují vlastní a literární zkušenosti s tímto programem. Snahou je zvýšit potenciál odběru ledvin z DCD v České republice.
Metoda:
Od roku 2002 do roku 2015 bylo v plzeňském Transplantačním centru odebráno celkem 44 ledvin z DCD. Technikou byl „in situ“ odběr pomocí „double baloon triple lumen“ katetru při zachování 5–10 min. „no-touch“ intervalu. Metoda hypotermické pulzatilní perfuze byla použita k testování viability odebraných ledvin. Transplantováno bylo celkem 28 ledvin příjemcům o průměrném věku 51,1 roku (26–73 let). Dle maastrichtských kritérií bylo 16 (57,1 %) ledvin ve skupině II, 8 (28,6 %) ve skupině III a 4 (14,3 %) ve skupině IV.
Výsledky:
30denní pooperační mortalita byla 0 a morbidita 10,7 tj. 14,3 % (N=4). Primární afunkce ledviny byla přítomna u 2 (7,1 %), opožděný nástup funkce pak u 5 (17,9 %) nemocných. Jeden rok, 5 a 10 let po transplantaci žije 100 %; resp. 86,4 % a 76,7% nemocných a ve stejných intervalech je funkčních 92,9; 69,6 a 61,9 % transplantovaných ledvin. Dlouhodobé výsledky jsou plně srovnatelné s transplantacemi ledvin od dárců se smrtí mozku.
Závěr:
DCD jsou významným zdrojem ledvin pro transplantace. Transplantace ledvin z DCD je metodou logisticky, ekonomicky a personálně náročnou s velmi dobrými dlouhodobými výsledky.
Klíčová slova:
dárci s nezvratnou zástavou oběhu – transplantace ledvin – výsledky
Úvod
Odběry ledvin z dárců s nebijícím srdcem (NHBD – non-heart beating donor) nebo nověji z dárců po nezvratné zástavě oběhu (DCD – donors after circulatory death) patří k historicky nejstarším zdrojům ledvin pro transplantační účely. V 50.–60. letech minulého století to byly nejčastější odběry vůbec. Teprve s definicí kritérií smrti mozku v roce 1968 (Harvardská kritéria) se dárci se smrtí mozku (DBD – donors after brain death) stali hlavními zdroji orgánů pro transplantace. V České republice byl první odběr a transplantace ledvin z DCD uskutečněny v roce 2002 v plzeňském Transplantačním centru [1].
Cílem našeho sdělení je podat vlastní dosavadní zkušenosti s transplantací ledvin z DCD, diskutovat současný stav ve světě a zamyslet se nad budoucími trendy vývoje transplantací z DCD.
Metoda
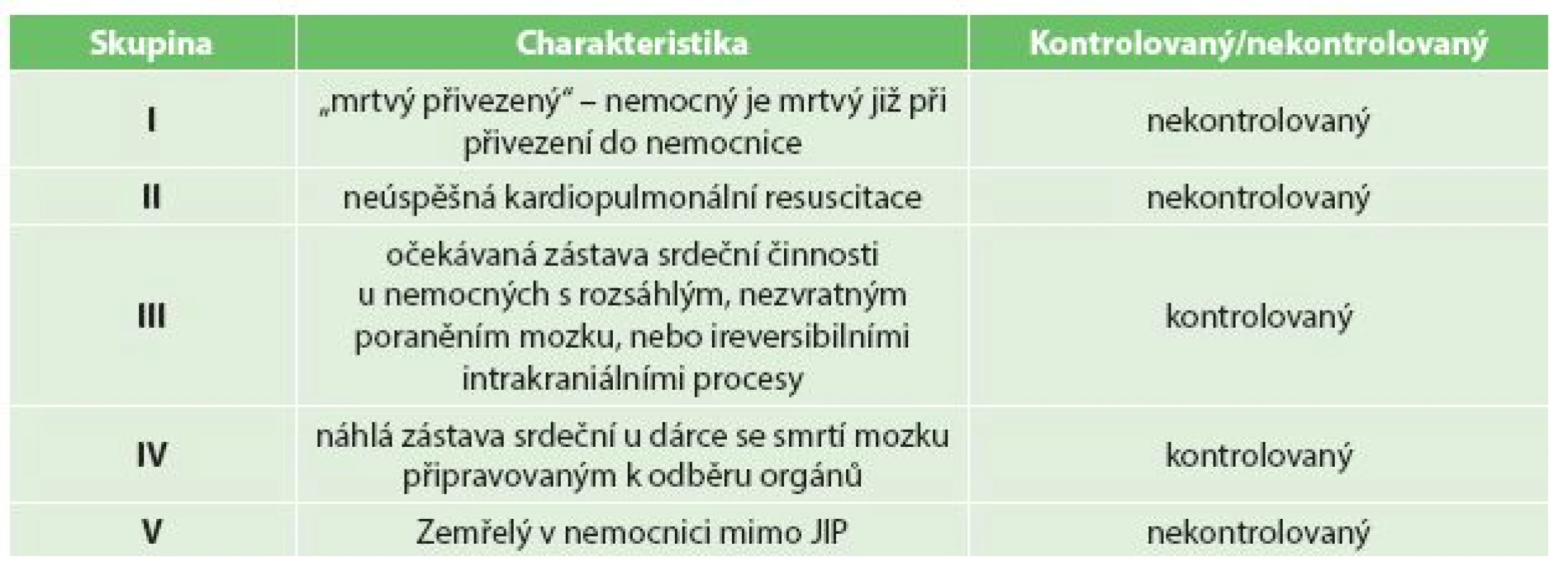
V roce 2002 byl v plzeňském transplantačním centru zahájen program transplantací ledvin z DCD, kterému předcházel experimentální program transplantací ledvin z NHBD na selatech. Vše bylo důkladně konzultováno s transplantačními centry v Barceloně a Maastrichtu, kde byl tento program dobře zaveden. Do roku 2015 jsme odebrali celkem 44 ledvin z 22 DCD. Technika odběru byla popsána v předchozích sděleních [2]. Ve stručnosti se jednalo o techniku s využitím speciálního perfuzního katétru (DBTL – double balloon triple lumen) zavedeného do společné femorální tepny. Sběrný katétr byl zaveden do společné femorální žíly. Katétry byly zavedeny až po jednoznačném stanovení nezvratné zástavy oběhu po vyčerpání všech současných možností kardiopulmonální resuscitace – chybění periferních pulzů, elektrické aktivity na elektrokardiogramu nebo chybění pulzové křivky při invazivní monitoraci krevního tlaku. Dodrželi jsme tzv. „no-touch“ interval (5−10 min.). Ledviny byly perfundovány 15 litry konzervačního roztoku (Custodiol, 4 °C), provedena laparotomie s aplikací ledové tříště do dutiny břišní a následný odběr ledvin. Ledviny byly poté bioptovány, perfundovány metodou pulzatilní perfuze a jejich kvalita byla hodnocena pomocí renální rezistence, hladinou glutathion S transferázy (GST) a rozdílem v hmotnosti štěpu před a na konci perfuze. Transplantovali jsme 28 ledvin 28 příjemcům, 9 ženám a 19 mužům průměrného věku 51,1 roku (26–73 let). Dle maastrichtských kritérií bylo 16 (57,1 %) ledvin ve skupině II, 8 (28,6 %) ve skupině III a 4 (14,3 %) ve skupině IV – Tab. 1. Jako imunosupresivní schéma jsme použili trojkombinaci (tacrolimus, kortikoidy, mykofenolát mofetil) s indukcí basiliximabem. K transplantaci jsme nepoužili 16 ledvin (36,4 %). Nejčastějším důvodem byla špatná makroskopická kvalita ledviny nebo ověřená biopsií a perfuzními parametry při pulzatilní perfuzi, chybění příjemce zejména v počátečních letech programu, kdy naše centrum bylo v ČR jediné zabývající se transplantacemi ledvin z DCD.
Výsledky
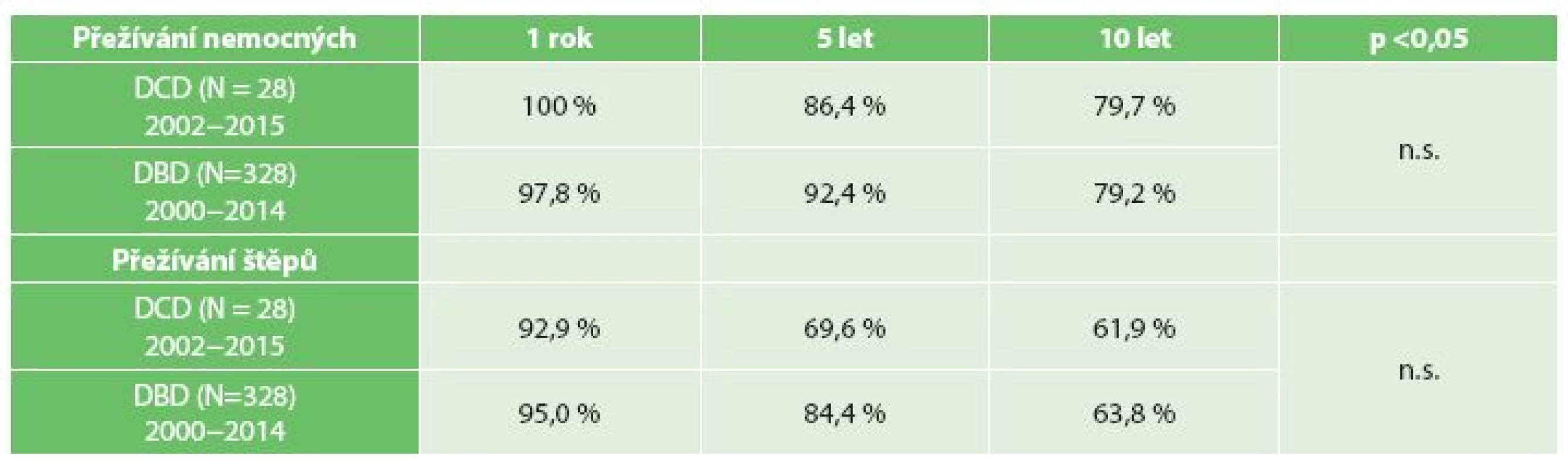
Do 30 dní po transplantaci nezemřel žádný nemocný. 30denní pooperační morbidita byla 14,3 %. Revidovali jsme 2 nemocné pro krvácení, u jednoho nemocného proběhla krátkodobá psychická alterace a u našeho posledního nemocného (současná hospitalizace) probíhá těžká nekrotizující pankreatitida. Primární afunkce (PNF – primary non-function) ledviny byla přítomna u 2 (7,1 %), opožděný nástup funkce (DGF – delayed graft function) pak u 5 (17,9 %) nemocných – Tab. 2. Dlouhodobé výsledky jsou uvedeny v Grafu 1. Jeden rok, 5 a 10 let po transplantaci žije 100 %; resp. 86,4 % a 76,7 % nemocných a ve stejných intervalech je funkčních 92,9 %; 69,6 % a 61,9 % transplantovaných ledvin. V průběhu sledování zemřelo 5 nemocných (dva na kardiální selhání, dva na generalizaci malignity a jeden na chřipku H1N1), z toho 3 s funkčním štěpem. Srovnáním skupin transplantovaných z DCD a DBD získáváme naprosto srovnatelné dlouhodobé výsledky (Tab. 3).


Diskuze
DCD jsou definováni jako dárci, u kterých došlo mechanismem smrti k nezvratné zástavě krevního oběhu, který se nepodařilo účinně vedenou kardiopulmonální resuscitací po dobu minimálně 30 minut obnovit. Typickými dárci této kategorie jsou nemocní s devastujícím postižením mozku, které nesplňuje kritéria smrti mozku (posthypoxické – neresuscitabilní, akutní infarkt myokardu, intracerebrální ischemie, hemorrhagie, devastující poranění). Diagnostika smrti na podkladě zástavy oběhu musí splňovat 2 ze 3 následujících kritérií: chybění periferního pulzu (absence pulzové vlny při invazivní monitoraci krevního tlaku), vymizení elektrické aktivity na elektrokardiogramu nebo vymizení mechanické aktivity srdeční na ultrasonografii [3,4]. Po stanovení definice smrti mozku v roce 1968 se změnila odběrová aktivita ve prospěch DBD. Nicméně v důsledku trvajícího nedostatku dárců při zvyšujícím se počtu čekatelů na transplantaci ledvin došlo k jakési renesanci odběrů ledvin z DCD po roce 1990, kdy byly v Maastrichtu definovány IV základní kategorie DCD, ke kterým se v roce 2000 přidala V. kategorie. V současnosti jsou transplantace ledvin z DCD prováděny v 10 zemích Evropské unie a řadě dalších států (např. v USA, Kanadě, Japonsku). V řadě vyspělých evropských zemí se tak po roce 1990 velmi výrazně zvýšila díky DCD odběrová aktivita (Španělsko, Velká Británie, Holandsko, Belgie) a v řadě zemí pak DCD tvoří hlavní zdroj ledvin pro transplantace. V České republice byl zahájen program transplantací ledvin z DCD v roce 2002, kdy byly úspěšně transplantovány první dvě ledviny z DCD v našem transplantačním centru.
Vzhledem k delšímu intervalu teplé ischemie (WIT – warm ischemia time) a následnému ischemicko-reperfuznímu poranění ledvinné tkáně po obnovení průtoku krve štěpem je funkce transplantovaných ledvin z DCD zatížena vyšší PNF (5−22 %) a DGF (20−70 %) ve srovnání s ledvinami od DBD. Nicméně dlouhodobé výsledky transplantací jsou u obou skupin naprosto srovnatelné [5,6], což potvrzuje i náš soubor nemocných. K rizikovým faktorům funkce transplantovaných ledvin z DCD kromě délky WIT patří i délka studené ischemie (delší 12 hodin), věk dárce nad 50 let, retransplantace a doba tzv. agonální fáze (začíná při SpO2 pod 70 % nebo středním arteriálním tlaku pod 50 mmHg), pokud je delší 4 hodin po ukončení podpory kardiopulmonálních funkcí [7,8]. Obecně by mělo platit pravidlo, že délka WIT pro transplantovanou ledvinu z DCD by neměla být delší 120 min. [9].
Technika odběrů ledvin z DCD je předmětem diskuzí. Existují fakticky tři možné způsoby odběru ledvin: „in situ“ perfuze konzervačním roztokem pomocí DBTL katétru, nebo okamžitá laparotomie a odběr prakticky shodný s odběrem z DBD, nebo využití mimotělní normotermní či hypotermní membránové oxygenace (ECMO). Na našem pracovišti využíváme metodu „in situ“ perfuze pomocí DBTL katétru, která se postupem času stala standardem s velmi dobrými výsledky. Metodu okamžité laparotomie a odběru lze prakticky využít u kontrolovaného dárce III. skupiny a její výhodou je maximální zkrácení WIT. ECMO metoda s normotermní perfuzí ledvin oxygenovanou krví je nepochybně velmi zajímavá. První zkušenosti ukazují na výrazné snížení výskytu DGF z 55 na 21 % [10] a navíc nově se zkouší pomocí této metody i možnost odstranění leukocytů z periferní krve, což může vést k dalšímu zlepšení transplantačních výsledků [11].
Otázka zda použít či nikoli metodu pulzatilní perfuze před vlastní transplantací je řešena řadou autorů. Někteří nenacházejí rozdíl v dlouhodobé funkci štěpů [12], jiní [13] včetně našeho pracoviště ji považuji za důležitou pro snížení výskytu DGF (až o 38 %). Velmi důležitý je fakt, že metoda umožňuje již před operací vyřadit ledviny, které by s vysokou pravděpodobností po operaci nefungovaly (pomocí renální rezistence, hladiny tubulárního markeru tGST a hmotnosti štěpu na konci perfuze). Důkazem toho jsou i naše výsledky s poměrně nízkým (17,9 %) výskytem DGF v porovnání s jinými pracovišti. Tato metoda byla také v našem souboru hlavním vyřazovacím kritériem řady sporně viabilních ledvin. Negativní stránkou pulzatilní perfuze jsou její poměrně vysoké ekonomické náklady.
Odběr ledvin z DCD má však stále řadu otázek, které v nejbližší budoucnosti bude nutno řešit obecnou dohodou napříč transplantačními centry. Jedná se o etické otázky smrti dárce související s určením okamžiku smrti po zástavě srdeční, kdy není šance na reparaci vitálních funkcí, resp. kdy ukončit podporu vitálních funkcí [14,15]. Rovněž různá transplantační centra mají stanovený různě dlouhý „no-touch“ interval (5–20 min.), kdy v jeho průběhu dochází v jedněch centrech k zavádění perfuzního katétru, jiná zavádějí katétr až po uplynutí příslušné doby. Jsou rovněž různá doporučení na maximální délku agonální fáze, která u maastrichtské kategorie III je rovněž různá v závislosti na centru (60 min. až 4 hod.). Dále se dle center různí i časové limity jednotlivých technických kroků, kdy je ještě možné použít ledviny z DCD. Jedná se o interval zástavy oběhu do KPR, který by měl být kratší 15−30 min., o interval od ukončení KPR do zavedení perfuzního katetru (kratší 90−120 min.) a interval od zahájení in situ perfuze do začátku odběru ledvin (kratší 120−270 min.). Jak je patrné, časové limity jednotlivých kroků se velmi různí a je pak velmi těžké porovnávat výsledky jednotlivých pracovišť. Nedořešenou otázkou zůstává i odběr ledvin z dětských DCD [16].
Závěr
Odběr ledvin z DCD je logistiky, ekonomicky i personálně náročný program, který má své pevné místo v transplantační medicíně. Jedná se o program, který má v České republice stále skrytý potenciál a lze si jen přát, aby tento potenciál byl v nejbližší době využit.
Podpořeno Výzkumným záměrem UK v Praze – PRVOUK – P36
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
Vladislav Třeška
U Českého dvora 11
326 00 Plzeň
e-mail: treska@fnplzen.cz
Sources
1. Třeška V, Hasman D, Čechura M, et al. Naše první zkušenosti s transplantacemi ledvin z dárců s nebijícím srdcem. Rozhl Chir 2002;81 : 582−6.
2. Třeška V, Hasman D, Hes O, et al. Dárce s nebijícím srdcem – nová možnost rozšíření dárcovského programu ledvin. Rozhl Chir 2000;79 : 613–8.
3. Kieslichová E. a kol. Dárci orgánů. Praha, Maxdorf 2015.
4. Třeška V. a kol. Transplantologie pro mediky. Praha, Karolinum 2002.
5. Ortega-Deballon I, Homby L, Shemie SD. Protocols for uncontrolled donation after circulatory death: a systematic review of international guidelines, practices and transplant outcomes. Crit Care 2015;19 : 268−80.
6. Koostra G, van Heurn E. Non-heartbeating donation of kidneys for transplantation. Nature Clinical Practice Nephrology 2007;3 : 154–63.
7. Algahim MF, Love RB. Donation after circulatory death: the current state and technical approaches to organ procurement. Curr Opin Organ Transplant 2015;20 : 127−32.
8. Akoh JA. Kidney donation after cardiac death. WJN 2012;1 : 79−91.
9. Detry O, Le Dinh H, Noterdaeme T, et al. Categories of donation after cardiocirculatory death. Transplant Proc 2012;44 : 1189−95.
10. Hosgood SA, Nicholson ML. The first clinical case of intermediate ex vivo normothermic perfusion in renal transplantation. Am J Transpl 2014;14 : 1690−2.
11. Hoogland ER, Snoeijs MG, van Heurn LW. DCD kidney transplantation: results and measures to improve outcome. Curr Opin Organ Transplant 2010;15 : 177−82.
12. Moers C, Smits JM, Maathuis MH, et al. Machine perfusion or cold storage in deceased-donor kidney transplantation. N Engl J Med 2009;360 : 7−19.
13. Watson CJ, Wells AC, Roberts RJ, et al. Cold machine perfusion versus static cold storage of kidneys donated after cardiac death: a UK multicenter randomized controlled trial. Am J Transplant 2010;10 : 1991−9.
14. Bruzzone P. Ethical and legal issues in donation after cardiac death in Italy. Transplant Proc 2010;42 : 1046−47.
15. Gardiner D, Shemie S, Manara A, et al. International perspective on the diagnosis of death. Brit J Anestesth 2012;108 : 14−28.
16. Ribalta A, Gallardo J, Ruiz A, et al. Donation after cardiac arrest program in Catalonia (Spain). Med Clin 2009;10 : 18−21.
Labels
Surgery Orthopaedics Trauma surgeryArticle was published in
Perspectives in Surgery

2016 Issue 4
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
- Metamizole vs. Tramadol in Postoperative Analgesia
-
All articles in this issue
- Infekce kůže a měkkých tkání
- Dárci ledvin po nezvratné zástavě oběhu (DCD) – zkušenosti jednoho centra
- Aktuální stav chirurgické léčby karcinomu pankreatu v České republice
- Prediktivní a prognostické faktory karcinomu žaludku
- Pedální bypass s použitím allogenní žilní náhrady
- Bouveretův syndrom – kazuistika a přehled literatury
- Splenóza ako zriedkavá príčina bolestí brucha
- Perspectives in Surgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Infekce kůže a měkkých tkání
- Splenóza ako zriedkavá príčina bolestí brucha
- Dárci ledvin po nezvratné zástavě oběhu (DCD) – zkušenosti jednoho centra
- Bouveretův syndrom – kazuistika a přehled literatury
