Selektivní antagonista muskarinových M3 receptorů v léčbě hyperaktivního močového měchýře (overactive bladder, OAB) – darifenacin
Selective M3 muscarinic receptor antagonist in the tre atment of overactive bladder (OAB) – darifenacin
Muscarinic receptors play an important role in the current therape utic appro aches in overactive bladder. Darifenacin is a new substance, selectively inhibiting muscarinic M3 subtypes of these receptors. This property may be responsible for its go od tolerability and go od safety profile in general. Its efficacy, as well as its influence on the qu ality of life of pati ents was evalu ated in many clinical tri als.
Key words:
darifenacin – overactive bladder (OAB) – muscarinic receptors
:
Jiří Slíva
; J. Minárik
:
Ústavy farmakologie 2. a 3. LF UK Praha
1; New EU Magazine of Medicine
2
:
Prakt Gyn 2008; 12(3): 146-149
V léčbě hyperaktivního močového měchýře se ve velké míře uplatňují látky s inhibičním potenci álem na muskarinové receptory. Novým zástupcem této lékové skupiny je darifenacin, který selektivně inhibuje účinky M3 podtypu těchto receptorů, což v konečném důsledku vede i k nižšímu výskytu nežádo ucích účinků. Jeho účinnost včetně vztahu ke kvalitě života nemocných byla ověřena řado u klinických studi í.
Klíčová slova:
darifenacin – hyperaktivní močový měchýř – muskarinové receptory
Úvod
Acetylcholin (ACh) jako ne uromedi átor parasympatické části vegetativního nervového systému zprostředkovává přenos signálu z CNS do oblasti cílových orgánů, a to prostřednictvím svých receptorů – nikotinových a muskarinových.
V so učasné době rozlišujeme 5 různých podtypů muskarinových receptorů (M1– M5) a dva postreceptorové systémy druhých poslů. Podtypy M1, M3 a M5 využívají tzv. stimulační cestu – zvýšení hladiny inositoltrifosfátu stimulací fosfolipázy C s následným navýšením intracelulární koncentrace i ontů vápníku. Naproti tomu podtypy M2 a M4 využívají tzv. inhibiční cestu, kdy prostřednictvím inhibice adenylylcyklázy indukují pokles tvorby cAMP.
Jednotlivé podtypy muskarinových receptorů se vyskytují v různé míře ve všech orgánech inervovaných parasympaticko u částí vegetativního nervového systému:
- M1 – CNS (kůra a hippocampus), slinné žlázy
- M2 – srdce, hladké svaly
- M3 – hladké svaly, slinné žlázy
- M4 – CNS (stri atum)
- M5 – CNS (substanti a nigra).
V případě močového měchýře je důsledkem uvolnění ACh do synaptické štěrbiny a jeho následné vazby na muskarinové receptory kontrakce hladké svaloviny – detrusoru. Jedním z terape utických cílů léčby hyperaktivity močového měchýře je tedy blokáda stimulačního účinku ACh na detrusor různými antimuskarinově působícími přípravky.
Antimuskarinika jso u v léčbě OAB využívána již desítky let a o jejich účinnosti v této indikaci není pochyb. Jso u rovněž známá i typická úskalí této léčby, a to nežádo ucí účinky ve smyslu ovlivnění slinných žláz, srdeční činnosti, peristaltiky, akomodace a kognitivních funkcí, jež jso u vyvolány blokádo u muskarinových receptorů M1, M4 a M5 mimo urogenitální trakt. Tyto vedlejší účinky tak posléze moho u vést k nízké compli ance nemocných a mnohdy i k přerušení léčby. Proto se vývoj nových přístupů zaměřuje mimo jiné především na potlačení těchto nežádo ucích účinků, a to při zachování účinků terape utických. Uroselektivitu antimuskarinik je tedy možné definovat jako relativní poměr mezi žádo ucím ovlivněním detrusoru blokádo u receptorů M3 (zvýšení kapacity močového měchýře či snížení urgencí apod.) a výskytem nežádo ucích účinků (sucho v ústech, zácpa, tachykardi e, poruchy akomodace aj.).
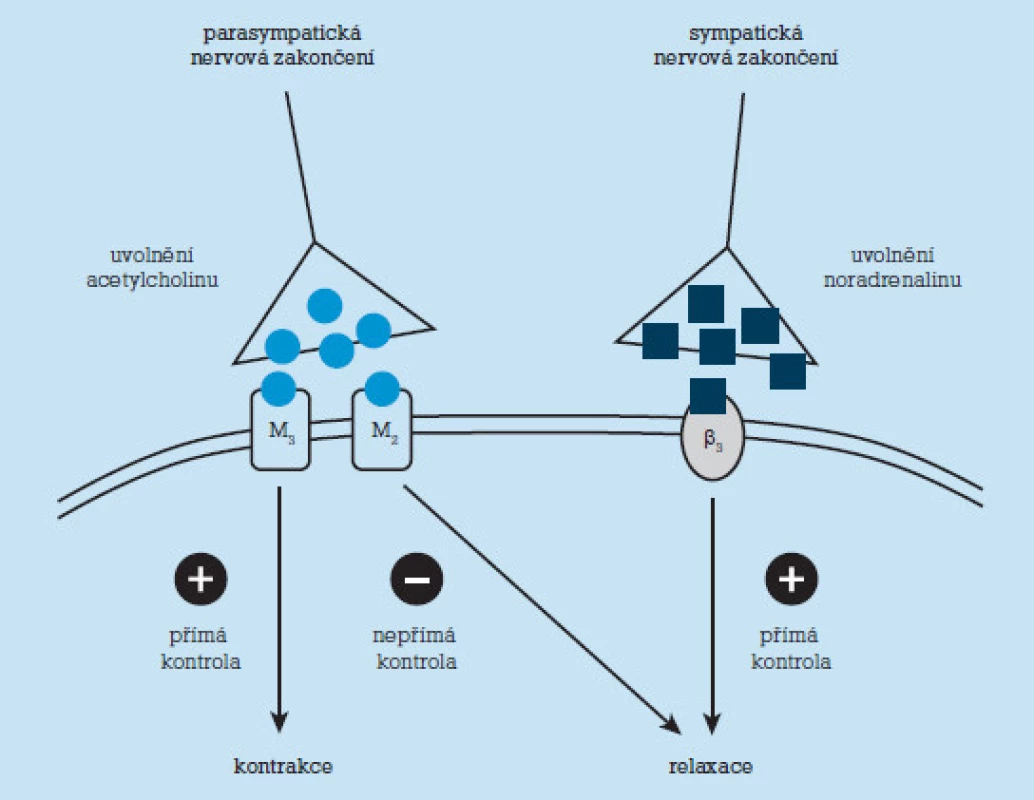
Zatímco v močovém měchýři se nachází všech 5 podtypů muskarinových receptorů, ve svalovině detrusoru nacházíme po uze podtypy M2 a M3 v poměru cca 7,5 : 2,5 (obr. 1). Počet receptorů však nemá klinicko u větší relevanci, protože právě M3 podtyp je považován za primární medi átor kontrakce detrusoru za normálních okolností i při OAB. Úloha podtypu M2 v močovém měchýři nebyla ještě plně objasněna, připisuje se mu spíše podpůrná permisivní role při kontrakci. V poslední době se také vedo u diskuse o aktivitě urotelu, jemuž se rovněž připisuje schopnost sekrece ACh a možnost signalizace plnění měchýře nervovými svazky uloženými suburoteli álně, kde se oba podtypy receptorů rovněž uplatňují.
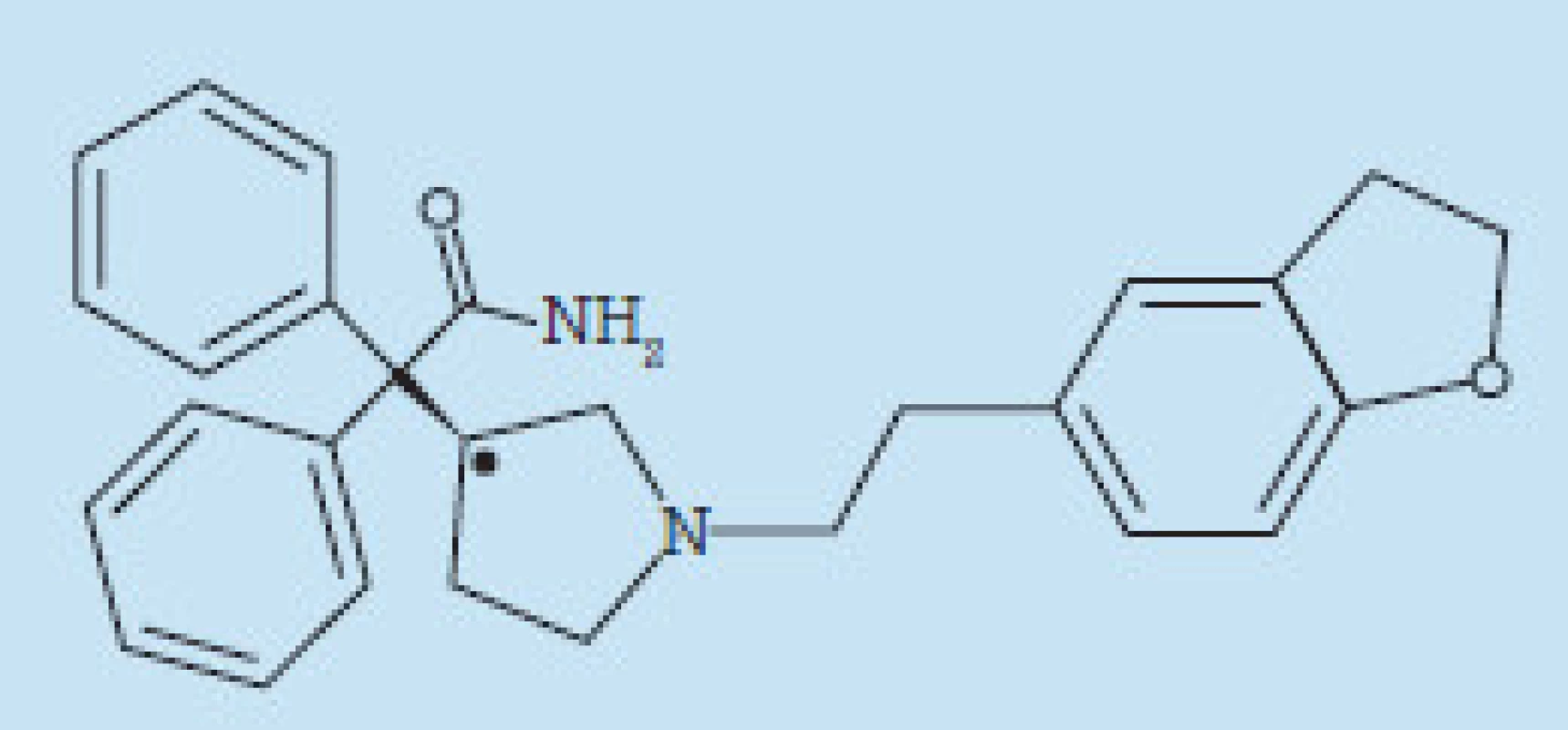
Darifenacin hydrobromid je kompetitivní, specifický a účinný antagonista cholinergních muskarinových receptorů s vysokou afinitou především k podtypu M3. Chemicky se jedná o ([(S)-[-2-[1-[2-(2,3-dihydrobenzofuran-5-yl)ethyl]-3-pyrrolidinyl]-2,2-diphenylacetamid (obr. 2).
Darifenacin je velice účinný v léčbě nutkání na malo u stranu, inkontinence a/ nebo zvýšené frekvence močení u paci entů s di agnózo u hyperaktivního močového měchýře, jejíž prevalence v běžné populaci ve věku nad 40 let je udávána u 16 % obyvatel [1]. Zvyšuje se však s věkem, a tak u osob nad 75 let je jí postiženo až 31– 42 % obyvatel [2].
Mechanismus účinku
Darifenacin působí jako vysoce selektivní antagonista muskarinových receptorů podtypu M3 (cca 60krát selektivnější k M3 než k M2). Z preklinických experimentů na zvířecím modelu je zřejmé, že tato vlastnost jej výrazně odlišuje od některých dalších látek s analogickým mechanismem účinku.
Farmakokinetické vlastnosti
Obvyklý nástup klinického účinku setrvalejšího charakteru je při pravidelném užívání perorálních tablet s řízeným uvolňováním a obsahem 7,5 a 15 mg účinné látky udáván kolem 2 týdnů [3].
Bi ologická dostupnost darifenacinu je relativně nízká – při podání 7,5 mg dosahuje 15,4 %, při dávce dvojnásobné pak 18,6 %; při aplikaci 30 mg je možné tuto hodnotu zvýšit až na 24,8 %. Nižší bi ologická dostupnost však byla zřejmá např. u japonských mužů (nižší až o 55,5 %). Zatímco příjem potravy ji obvykle neovlivňuje, je třeba brát v potaz její možný nárůst při so učasném využití inhibitorů CYP 3A4 [4].
V krevní plazmě je až 98 % vstřebaného množství darifenacinu vázáno na kyselý alfa‑1 glykoprotein. Distribuční objem (VD) dosahuje při ustáleném stavu hodnoty 163,4 litrů. Analogický údaj týkající se hydroxylovaného metabolitu darifenacinu (UK- 148,993) činí 499 litrů, což vypovídá o jeho afinitě k extravaskulárnímu prostoru [5].
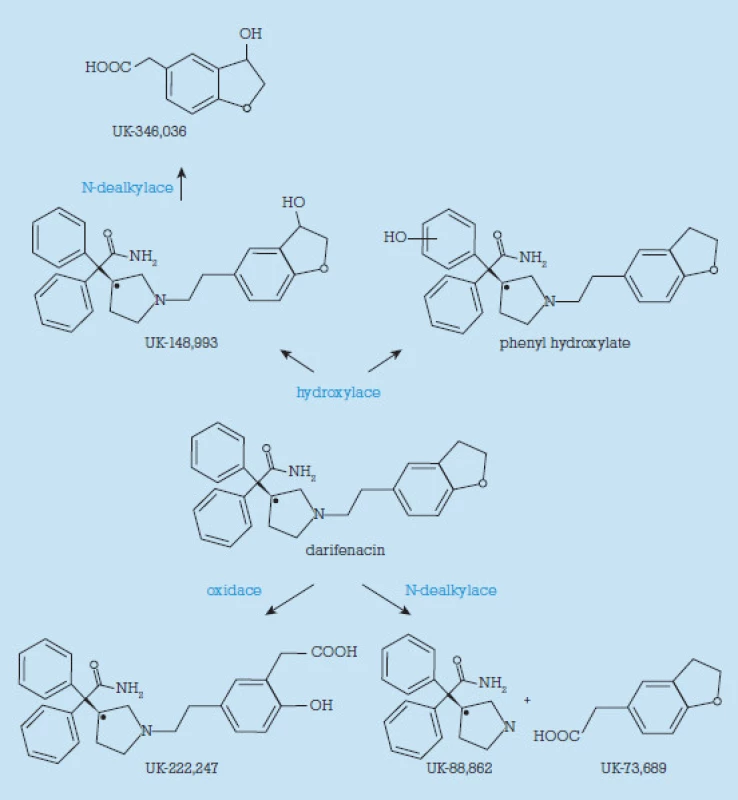
Darifenacin podléhá velice intenzivnímu metabolismu v játrech, a to především cesto u cytochromů P450 3A4 či 2D6 a odvíjí se třemi základními cestami – monohydroxylací, oxidací dihydrobenzfuranu s otevřením kruhu či N- de alkylací (obr. 3) [5,6].
Hlavní eliminační cesto u darifenacinu jso u ledviny (60 %), zbylých 40 % je vylo učeno stolicí. Celková tělesná cle arance se pohybuje v rozmezí 32– 40 l/ h a bi ologický poločas mezi 13– 19 hod; metabolit UK- 148,993 se vylučuje s poločasem přibližně 14,9 hod.
Klinické zkušenosti
Ve 12týdenní, multicentrické, randomizované, dvojitě zaslepené, placebem kontrolované studii Haaba a kol. hodnotící účinnost darifenacinu u 439 paci entů s OAB bylo ve skupinách léčených darifenacinem 7,5 mg a 15 mg denně dosaženo statisticky významného snížení počtu inkontinencí až o 70 %. Snížil se také počet mikcí, počet urgentních epizod, závažných urgencí a nočních probuzení či potřeby měnit prádlo kvůli inkontinenci, a to již od 2. týdne po zahájení léčby [3].
Při terapii darifenacinem byl ve studii a utorky Cardozové a kol. prokázán příznivý vliv na nově zaváděný klinický parametr – warning time, tj. dobu mezi urgencí a mikcí. Většina paci entů pozorovala zlepšení o více než 30 % již od druhého týdne léčby [7].
Ve dvojitě zaslepené randomizované cross- over studii Chappleho et al. u 65 paci entů s OAB byl darifenacin 7,5 a 15 mg denně srovnáván s oxybutyninem 2,5 mg třikrát denně. Darifenacin prokázal srovnatelný efekt na urodynamické parametry, způsoboval však méně sucha v ústech než oxybutynin [8].
V letošním roce byla též publikována přehledová práce sumarizující výsledky dosud publikovaných klinických studi í, ve kterých byla hodnocena bezpečnost i účinnost antimuskarinik u OAB (celkem 83 studi í). Antimuskarinika byla shledána jako jednoznačně účinnější nežli placebo, a to za so učasně velmi dobrého bezpečnostního profilu [9].
Léčba darifenacinem 7,5 mg a 15 mg je ve srovnání s placebem doprovázena též statisticky významným zlepšením některých aspektů kvality života stanovených pomocí Kings He alth dotazníku (KHQ). Vyplývá to z recentní meta‑analýzy 3 klinických studi í (n = 1 059; 85 % ženy; věk 19– 88 let). Paci enti na darifenacinu uváděli významně větší spokojenost s léčbo u (57 % vs 40 %; p < 0,001), větší preferenci darifenacinu oproti předcházející léčbě (71 % vs 58 %; p = 0,013) a vyšší ochotu znovu užít darifenacin (69 % vs 56 %; p = 0,002) než paci enti na placebu [10].
Lékové interakce
Jak bylo zmíněno v odstavci pojednávajícím o farmakokinetice darifenacinu, jeho hlavním místem metabolizace jso u cytochromy 3A4 a 2D6. Z toho důvodu může být jeho plazmatická koncentrace ovlivněna inhibitory, respektive induktory těchto enzymatických struktur. Kromě toho samotný darifenacin ve studi ích in vitro snižoval aktivitu cytochromu 3A4 (59– 89 % inhibice při koncentraci 100 µmol/ l), což logicky může vyústit v nárůst plazmatických hladin ko administrovaných léčiv, která jso u přirozenými substráty tohoto enzymu. Darifenacin však působí i jako středně silný inhibitor 2D6 [4].
Bezpečnost a snášenlivost
Nejznámějším nežádo ucím účinkem anticholinergik je sucho v ústech způsobené sníženo u sekreční aktivito u mukózních a serózních buněk ve slinných žlázách. Medi átorem snížení produkce slin je blokáda podtypů M1 a M3. Z uvedeného vyplývá, že pokud chceme jakýmkoliv antimuskarinikem snížit aktivitu detrusoru blokádo u podtypu M3, způsobíme tím do jisté míry i snížení produkce slin. Analogicky v gastro intestinálním traktu s predominantním výskytem podtypů M2 a M3 lze jejich blokádo u vyvolat zácpu zpomalením peristaltiky či paralelním snížením sekrece žlázek střevního epitelu. U očí je zmiňováno riziko negativního ovlivnění akomodace, snížení produkce slz a zvětšení průměru pupily. Prostřednictvím blokády M2 receptoru v srdci může být i atrogenně vyvolána tachykardi e a palpitace.
Negativní ovlivnění kognitivních funkcí blokádo u podtypu M1 anticholinergiky v kůře mozkové je významné zejména u starších paci entů [11]. Blokáda M1 receptoru v CNS může způsobovat i halucinace a zmatenost. Na základě stanovení inhibičních konstant v různých studi ích byla stanovena 9krát vyšší M3 selektivita darifenacinu oproti podtypu M1 (poměr 9 : 1). Oxybutynin ani trospi um nejso u v tomto ohledu příliš selektivní, poměr síly blokády M3 : M1 byl 1,5 : 1 a 1,6 : 1. Tolterodin a solifenacin jso u neselektivní v poměru 0,6 : 1 a 1 : 1.
Z dalších nežádo ucích účinků nelze jistě vylo učit ani poruchy libida či potence, které přímo korelují nabídce acetylcholinu.
Sucho v ústech je nejčastěji zmiňovaným nežádo ucím účinkem (29,6 %), nicméně počet paci entů, kteří z důvodu těchto nežádo ucích účinků přerušili léčbu, je velmi nízký a udává se po uze kolem 1 % [9].
V klinických hodnoceních zaměřených na bezpečnost darifenacinu se ukázalo, že v dávkách 3,75– 15 mg denně nemá negativní vliv na kognitivní funkce (vybavovací schopnost paměti, rychlost re akčního času při výběru objektů, čas zpoždění ve vybavování si slovní zásoby) a neovlivňuje srdeční frekvenci (neprodlužuje QTc interval) [8,12– 15].
Závěr
Darifenacin (v ČR registrován společností Novartis pod názvem EMSELEX® 7,5 mg a EMSELEX® 15 mg) je moderním, vysoce selektivním blokátorem muskarinových M3 receptorů podávaným jedenkrát denně. Je srovnatelně účinný jako neselektivní anticholinergní přípravky, avšak vzhledem ke své uroselektivitě má lepší bezpečnostní profil. Je proto vhodno u alternativo u v léčbě hyperaktivního močového měchýře a smíšené inkontinence především u starších lidí a paci entů s výskytem či zvýšeným rizikem výskytu nežádo ucích anticholinergních účinků.
Doručeno do redakce: 9. 6. 2008
Přijato po recenzi: 4. 8. 2008
MUDr. Jiří Slíva1
MUDr. Juraj Minárik2
1Ústavy farmakologi e 2. a 3. LF UK Praha
2New EU Magazine of Medicine
Sources
1. Goepel M, Hoffmann JA, Piro M et al. Prevalence and physici an awareness of symptoms of urinary bladder dysfuncti on. Eur Urol 2002; 41(3): 234– 239.
2. Milsom I, Abrams P, Cardozo L et al. How widespre ad are the symptoms of an overactive bladder and how are they managed? A populati on‑based prevalence study. BJU Int 2001; 87(9): 760– 766.
3. Haab F, Stewart L, Dwyer P. Darifenacin, an M3 selective receptor antagonist, is an effective and well‑tolerated once- daily tre atment for overactive bladder. Eur Urol 2004; 45(4): 420– 429.
4. Skerjanec A. The clinical pharmacokinetics of darifenacin. Clin Pharmacokinet 2006; 45(4): 325– 350.
5. Steers W, Corcos J, Fo ote J, Kralidis G. An investigati on of dose titrati on with darifenacin, an M3- selective receptor antagonist. BJU Int 2005; 95(4): 580– 586.
6. Kerbusch T, Wahlby U, Milligan PA, Karlsson MO. Populati on pharmacokinetic modelling of darifenacin and its hydroxylated metabolite using po oled data, incorporating saturable first- pass metabolism, CYP2D6 genotype and formulati on- dependent bi o availability. Br J Clin Pharmacol 2003; 56(6): 639– 652.
7. Cardozo L, Dixon A. Incre ased warning time with darifenacin: a new concept in the management of urinary urgency. J Urol 2005; 173(4): 1214– 1218.
8. Chapple C, Steers W, Norton P et al. A po oled analysis of three phase III studi es to investigate the efficacy, tolerability and safety of darifenacin, a muscarinic M3 selective receptor antagonist, in the tre atment of overactive bladder. BJU Int 2005; 95(7): 993– 1001.
9. Chapple CR, Khullar V, Gabri el Z et al. The Effects of Antimuscarinic Tre atments in Overactive Bladder: An Update of a Systematic Revi ew and Meta‑Analysis. Eur Urol 2008.
10. Abrams P, Kelleher C, Huels J et al. Clinical relevance of he alth- related qu ality of life o utcomes with darifenacin. BJU Int 2008; 102(2): 208– 213.
11. Ancelin ML, Artero S, Portet F et al. Non- degenerative mild cognitive impairment in elderly people and use of anticholinergic drugs: longitudinal cohort study. BMJ 2006; 332(7539): 455– 459.
12. Haab F, Corcos J, Si ami P et al. Long‑term tre atment with darifenacin for overactive bladder: results of a 2- ye ar, open- label extensi on study. BJU Int 2006; 98(5): 1025– 1032.
13. Kay GG, Wesnes KA. Pharmacodynamic effects of darifenacin, a muscarinic M selective receptor antagonist for the tre atment of overactive bladder, in he althy volunteers. BJU Int 2005; 96(7): 1055– 1062.
14. Lipton RB, Kolodner K, Wesnes K. Assessment of cognitive functi on of the elderly populati on: effects of darifenacin. J Urol 2005; 173(2): 493– 498.
15. Zinner N, Susset J, Gittelman M et al. Efficacy, tolerability and safety of darifenacin, an M(3) selective receptor antagonist: an investigati on of warning time in pati ents with OAB. Int J Clin Pract 2006; 60(1): 119– 126.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicineArticle was published in
Practical Gynecology

2008 Issue 3
Most read in this issue
- Chronic vaginal dryness in oncology patients
- Particular characteristics of anorexia nervosa in adolescent girls
- Selektivní antagonista muskarinových M3 receptorů v léčbě hyperaktivního močového měchýře (overactive bladder, OAB) – darifenacin
- Prenatal preventi on of dental caries