Bolest nenádorového původu v gynekologii a možnosti její léčby
Non-tumour pain in gynaecology and options for its treatment
The review discusses pathophysiology and treatment options for acute and chronic pain in gynaecology. Pharmacotherapy should reflect the newest scientific findings with an emphasis on long-term safety. Chronic pain requires multidisciplinary approach with an optimal use of pharmacotherapy, psychotherapy, invasive methods and physiotherapy provided through cooperation between gynaecologist and algesiologist.
Key words:
acute pain – chronic pain – analgesics – adjuvant analgesics – invasive procedures
Authors:
P. Nosková
Authors‘ workplace:
Centrum léčby bolesti KARIM, VFN v Praze
Published in:
Prakt Gyn 2011; 15(2): 87-92
Category:
Review Article
Overview
Článek pojednává obecně o patofyziologii a možnostech léčby akutní a chronické bolesti zaměřených na oblast gynekologie. Farmakoterapie by měla být vedena podle nejnovějších doporučení s důrazem na bezpečnost při dlouhodobém podávání. Chronické bolestivé stavy vyžadují multidisciplinární přístup s využitím dostupných možností farmakoterapie, psychoterapie, invazivních metod a rehabilitace, který je zajištěn spoluprací gynekologa a algeziologa.
Klíčová slova:
akutní bolest – chronická bolest – analgetika – adjuvantní léčiva – invazivní metody
Úvod
Bolest definujeme (IASP – International Association for Study of Pain) jako nepříjemný senzorický a emocionální prožitek spojený se skutečným nebo potenciálním poškozením tkáně nebo popisovaný výrazy pro takové poškození. Bolest je vždy subjektivní.
Gynekolog je nucen bolest řešit ve své každodenní praxi. Patologické i fyziologické stavy ženských pohlavních orgánů vyvolávají bolest akutní (AB) i chronickou (CHB).
CHB, nazývaná také jako syndrom chronické nenádorové bolesti, se vyznačuje stížností pacientů na bolest tělesnou nebo útrobní, trvající déle než 3–6 měsíců. Za chronickou je třeba považovat i bolest kratšího trvání, pokud přesahuje dobu obvyklou pro dané onemocnění či poruchu.
CHB vyžaduje odlišný lékařský přístup než AB a je třeba si uvědomit základní rozdíly (tab. 1), které vedou k nastavení účelné terapie.
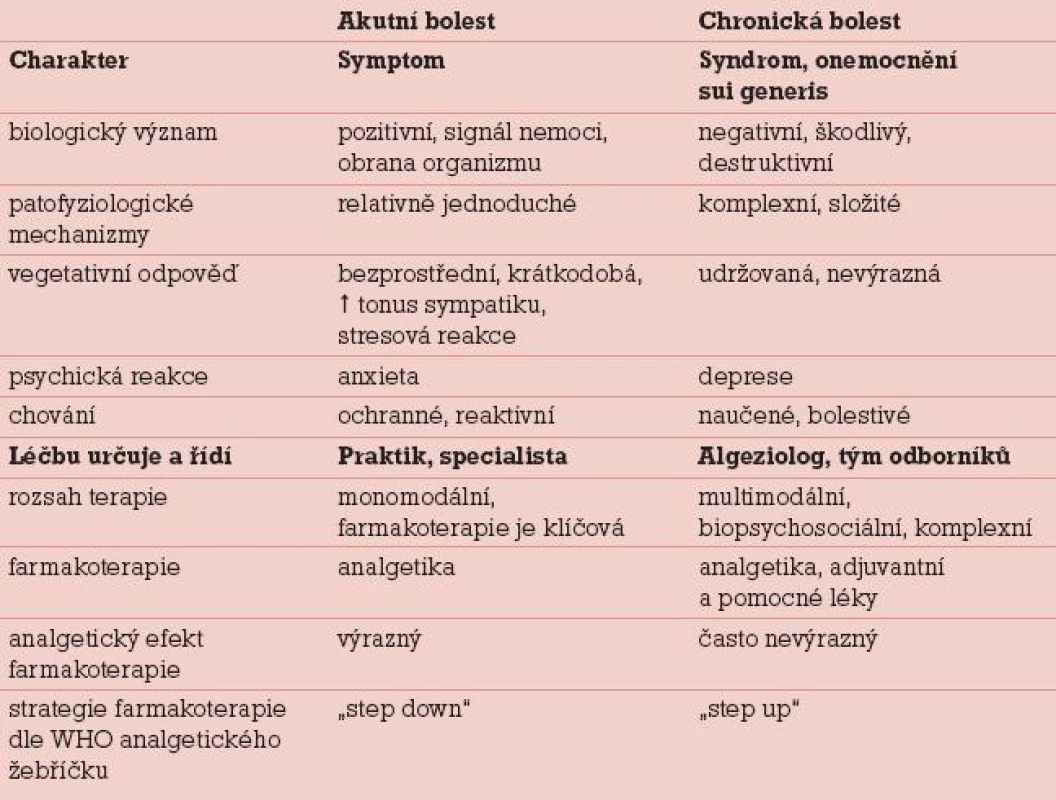
Příčiny bolestí v gynekologii
V oblasti gynekologie se setkáváme s bolestí z nejrůznějších příčin. Nejčastější klinické stavy nenádorového původu uvádí následující přehled [1]:
- příčiny akutní bolesti: ruptura cysty ovaria, torze adnex, akutní nekróza myomu, pánevní zánětlivá nemoc, ovariální hyperstimulační syndrom, spontánní potrat, mimoděložní těhotenství;
- příčiny chronické bolesti: pánevní adheze, endometrióza, pelipatie, vulvodynie, pruritus vulvae, vestibulitis, postmastektomický syndrom (onkologie);
- příčiny intermitentní bolesti: ovulační bolest, primární dysmenorea, sekundární dysmenorea.
Lokalizace gynekologické bolesti nepřesahuje ventrálně spina iliaca anterior superior a dorzálně je soustředěna nad os sacrum s možností propagace do gluteální oblasti. Výjimečně přechází až na přední stranu stehna. V diferenciální diagnostice je třeba odlišit nemoci gastrointestinálního systému, urogenitální etiologie (zejména intersticiální cystitidu), postižení periferních nervů (plexus lumbalis a n. pudendus), patologie pohybového aparátu (degenerativní změny, traumata a anomálie lumbosakrální páteře, fibromyalgie, spazmus svalů dna pánevního) a systémová onemocnění.
Patofyziologie
Vnímání bolesti u žen je ovlivněno ženskými pohlavními hormony. Předpokládalo se, že estrogeny mohou zesílit přenos bolestivých vjemů, naopak progesteron vykazuje opačný efekt. V dnešní době však výsledky popisující vliv ženských pohlavních hormonů na vnímání bolesti nejsou jednotné [2] a v klinických studiích bylo prokázáno, že ženy ve folikulární i luteální části menstruačního cyklu mají vyšší práh bolesti než muži. Kontroverzní nálezy však mohou být důsledkem rozdílných metod zkoumání bolesti a vyžadují další studie.
Pro správnou diagnostiku a léčbu pánevních bolestí je zásadní i znalost inervace příslušných orgánů. Děloha: plexus uterovaginalis (sympatikus Th12–L1, parasympatikus S2–S4); vagina: plexus uterovaginalis + n. pudendus dolní část orgánu; zevní rodidla: n. ilioinguinalis, n. genitofemoralis, n. pudendus; svaly hráze: n. pudendus.
Patofyziologickým podkladem pro vznik CHB jsou změny CNS ve smyslu neuroplasticity, periferní a centrální senzitizace a sekundární hyperalgezie. Nemalý vliv na vznik bolestivého prožitku mají také paměť a emoce. Z toho vyplývá základní pravidlo algeziologie: racionální a efektivní řešení AB znamená prevenci vzniku CHB.
Na základě patofyziologických mechanizmů CHB se v gynekologii uplatňují následující typy:
- nociceptivní,
- neuropatická,
- psychogenní a
- smíšená.
Pochopení typu bolesti hraje důležitou roli ve výběru farmak.
1. Nociceptivní bolest
Vzniká podrážděním nociceptorů [3], zahrnujícím nocisenzory (volná nervová zakončení v tkáních, aktivují se pouze při bolestivé stimulaci), mechanosenzory (Vater–Paciniho tělíska) a polymodální receptory (reagují na teplo a chlad). Podle umístění receptorů se rozlišuje bolest somatická a viscerální. Z nejčastějších klinických jednotek patří do této skupiny bolesti pohybového aparátu a bolesti vnitřních orgánů. V diagnostice se využívají dostupné zobrazovací metody (rtg, ultrazvuk, CT, NMR), laboratorní parametry a vyšetření rehabilitačního lékaře. Farmakoterapie uplatňuje analgetický žebříček WHO dle stupně bolesti (tab. 2).
![Analgetický žebříček WHO [11].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/b3148908f7591745f332f332830e173c.jpg)
2. Neuropatická bolest
Tato bolest je generována nervovým systémem. Rozlišuje se mezi periferní neuropatickou bolestí s asymetrickými lokalizovanými neuropatiemi (postherpetická neuralgie, úžinové syndromy, plexopatie, iatrogenní postižení nervů po operaci) a systémovými polyneuropatiemi (diabetická, toxická: alkohol, chemoterapie) a centrální neurogenní bolestí (tumory CNS, míšní léze). Z anamnézy vyplývá typický charakter bolesti: píchavá, bodavá, pálivá, šlehavá, zhoršující se v klidu a v noci. Je doprovázena alodynií, při které nebolestivý vjem vyvolá bolestivou stimulaci. S tímto jevem se můžeme setkat u vulvodynie. Lékem první volby jsou koanalgetika (adjuvantní léčiva). Klasická analgetika nedosahují běžného účinku. Součást diagnostického postupu tvoří i neurologické vyšetření a EMG.
3. Psychogenní bolest
U této bolesti převažuje nebo dominuje psychická komponenta. Především u depresivních poruch a některých neuróz je bolest somatickou projekcí primárních obtíží. Nejčastěji si pacienti stěžují na bolesti břicha a zad. V gynekologii je tento typ velmi častý, zejména v kombinaci s problémy v oblasti sexuálního života, a nejdůležitějším krokem ke správné léčbě je získat si důvěru pacientky. Základ terapie tvoří psychologické postupy (autogenní trénink, kognitivně behaviorální metody) a psychofarmaka (po podrobném vyšetření psychiatrem).
4. Smíšená bolest
Zahrnuje stavy, na kterých se podílí více předchozích typů bolesti. V praxi se nejčastěji setkáváme s kombinací nociceptivní a neuropatické etiologie. Farmakoterapie se odvíjí od klinického stavu a typu bolesti, na který si pacient stěžuje.
Hodnocení bolesti
Pro správně vedenou léčbu CHB je základním vodítkem pečlivě odebraná anamnéza. Obvyklé otázky se zaměřují na dobu trvání, charakter příznaků, lokalizaci a propagaci bolesti, faktory ovlivňující bolest, kvalitu spánku, intenzitu bolesti a změny v čase. Významnou roli hraje i rozpoznání psychosociálního stavu pacienta, zejména rodinného zázemí a vztahu k práci. K objektivizaci symptomů slouží různé škály: vizuální analogová (VAS – Visual Analogical Scale), numerická (0 – žádná bolest až 10 – nejvyšší intenzita) nebo obličejová (tzv. smajlíci, využitelná hlavně u dětí). Velmi užitečnou pomůckou při vyhodnocování je deník bolesti, kam si pacient zapisuje hodnoty VAS během dne, užitá analgetika a veškeré nežádoucí účinky léčby. V oblasti gynekologie má význam zejména u diagnózy intermitentní bolesti. Důležitá je také informace o výskytu průlomové bolesti (PB). PB je definována jako přechodné vzplanutí bolesti silné intenzity při stabilně kontrolované základní bolesti analgetickou léčbou. Nejčastějšími příčinami jejího vzniku jsou: pohybová aktivita, kašel a zvýšení břišního lisu. Proto je třeba pacienta vybavit i analgetiky s rychlým nástupem účinku pro případ řešení této situace. Častější výskyt průlomové bolesti většinou vede k přehodnocení léčby a její úpravě ve smyslu navýšení dávky retardované formy nebo změny analgetika.
Farmakoterapie – obecný postup
Základ léčby CHB tvoří farmakoterapie, v případě AB doprovázená zákrokem vedoucím k odstranění příčiny bolesti. Klasickým a vžitým vodítkem je analgetický žebříček WHO (tab. 2), původně koncipovaný pro bolest nádorovou. V obecném schématu se také počítá s podáváním adjuvantních analgetik (koanalgetik), která příznivě ovlivňují některé typy bolesti, a pomocných léků určených k léčbě nežádoucích účinků farmak. Volba a vedení terapie vychází z údajů o intenzitě a charakteru bolesti, konkrétního klinického stavu a přidružených chorob.
Akutní bolest je ovlivňována silnými analgetiky s rychlým nástupem účinku, retardované formy se většinou neužívají. K výběru vhodného farmaka podle analgetické potence slouží Oxfordská liga analgetik (tab. 3). Jde o žebříček analgetik sestavený podle jejich NNT hodnot určených na základě výsledků nezávislých metaanalýz četných klinických studií (randomizovaných, kontrolovaných, dvojitě slepých) týkajících se působení analgetik u akutních bolestí u dospělých. Tyto studie, prováděné z pozice medicíny založené na důkazech, jsou komerčně nezávislé. Podle Oxfordské ligy analgetik mají u akutní bolesti nejvyšší pravděpodobnost analgetického účinku (nejnižší NNT) nejen silné opioidy, ale i nesteroidní antirevmatika (NSA), kombinace paracetamolu s opioidy podané ve vysokých (ale ještě přípustných) dávkách a metamizol. I když je třeba u Oxfordské ligy analgetik počítat s určitými omezeními (měří pravděpodobnost spíše než vlastní intenzitu analgetického účinku, vychází z akutní bolesti a jednorázové aplikace), získala si mezi lékaři rychle velkou autoritu. Podle posledních výsledků klinického testování dochází k její průběžné aktualizaci a je přístupná na internetu v lékovém bulletinu „Bandolier“ (www.pain.cz; www.jr2.ox.ac.uk).
![Oxfordská liga analgetik [12].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/85320a157805e475b5959f9c103a0008.jpg)
Podle nejnovějších postupů a zásad se zcela upouští od intramuskulární aplikace farmak a doporučuje se podání subkutánní [4].
U chronické bolesti se jednoznačně upřednostňuje neinvazivní podávání léků (perorálně, rektálně, transdermálně), s výjimkou onkologických pacientů v terminálním stavu. Analgetika se podávají pravidelně podle časového plánu s preferencí retardovaných forem. Vždy se titruje od nejnižších dávek k analgeticky účinné a pacientem dobře tolerované hladině léku. V případě výskytu průlomových bolestí je nemocný vybaven i farmaky s rychle nastupujícím účinkem. Kombinací opioidních a neopioidních analgetik lze dosáhnout aditivního účinku.
Při dlouhodobém podávání je třeba brát v úvahu nežádoucí účinky léků na jednotlivé systémy, pouze v případě nádorové bolesti v konečném stadiu není jejich eventuální toxicita překážkou.
1. Analgetika 1. stupně WHO
Analgetika – antipyretika
Mechanizmus analgetického působení paracetamolu (PCT) není přesně znám. Předpokládá se, že v CNS inhibuje COX3 (cyklooxygenáza) a zasahuje do dalších neurohumorálních mechanizmů. Analgeticky účinná dávka je 750–1 000 mg, maximálně 4g/den, v intervalech po 4–6 hod. Má příznivý bezpečnostní profil, a proto představuje lék první volby u geriatrických pacientů. Svým rychlým nástupem je vhodný k řešení PB. Racionální je ho podat asi 30 min před plánovanou pohybovou aktivitou. Je lékem první volby během gravidity a laktace (FDA). Velkou výhodou paracetamolu, ve srovnání se salicyláty a jinými NSA, je absence gastrointestinální toxicity, která zvyšuje riziko GIT krvácení. Proto se stává neopioidním analgetikem první volby také u chronicky antikoagulovaných pacientů. Jen v případě dlouhodobého užívání vyšších dávek paracetamolu (více než 2g denně) je doporučeno přísněji monitorovat INR a případně snížit dávku warfarinu. Poškození jater po terapeutických dávkách paracetamolu je výjimečné a přichází v úvahu spíše při stavech s nízkými hladinami glutathionu, jako jsou kachexie při anorexii, hepatitida C a cirhóza jater [5]. O rektálním podání paracetamolu a nástupu účinku jsou stále vedeny diskuze vzhledem k rozdílné absorpci z rektálních venózních pletení a k formulaci jednoznačných závěrů je třeba dalších studií. Injekční forma (Perfalgan 500–1 000 mg) se používá ke krátkodobé léčbě středně silných bolestí po chirurgických výkonech, zejména v porodnictví, a má své místo v léčbě PB u hospitalizovaných pacientů. Rychlost nástupu analgetického účinku Perfalganu se udává 5–10 min, v praxi je zaznamenávána i doba delší (až 30–45 min).
Z nežádoucích účinků metamizolu (Novalgin, Algifen), který je oblíben i v geriatrii, je znám jeho negativní vliv na krvetvorbu. Poslední epidemiologické studie ukazují, že toto riziko je velmi nízké (1 : 1 000 000). Agranulocytóza bývá reverzibilní a jejími klinickými projevy jsou horečka a pharyngitis [6]. Je třeba však počítat s vzácnou, ale těžkou anafylaktoidní reakcí, kterou tento lék může vyvolat. Proto by neměl být podáván u asthma bronchiale a polyvalentních alergiků. Intravenózní forma je běžnou součástí řešení PB u hospitalizovaných pacientů a metamizol v kombinaci se spasmolytikem (Algifen) představuje účinnou léčbu PB u bolestí břicha. Maximální dávka je až 216 kapek rozdělená do 4 denních dávek (20–54 kapek).
Nesteroidní antirevmatika (NSA)
Představují silná analgetika a pro svůj volný prodej také velmi oblíbená, zároveň vyžadují opatrnost z důvodů závažných nežádoucích účinků. Podle jejich působení na cyklooxygenázu 1(COX1 – konstituční) a cyklooxygenázu 2 (COX2 – indukovatelná) je dělíme na:
- specifické COX 1 inhibitory (KAS),
- neselektivní COX inhibitory – klasická NSA (ibuprofen, diclofenak, naproxen, piroxicam),
- preferenční COX 2 inhibitory (nimesulid, meloxicam) a
- COX2 selektivní inhibitory = koxiby (parekoxib, etorikoxib, celekoxib).
Pro svůj vysoký analgetický potenciál mají své místo při řešení AB, ale je třeba zdůraznit, že klasická NSA jsou farmaka naprosto nevhodná pro dlouhodobé podávání. Důvodem jsou jejich závažné nežádoucí účinky na GIT, kardiovaskulární systém, trombocyty a ledviny. Nadužívání klasických NSA vede ke klinickým jednotkám známým jako NSA indukovaná gastropatie, NSA enteropatie a kolopatie. Rizikovou skupinu představují pacienti nad 65 let věku, s chronickou kortikoterapií, warfarinizací a pozitivní GIT anamnézou. Pokud je nezbytné jejich dlouhodobé pravidelné podávání (revmatologie, onkologie), je vhodné zároveň nasadit inhibitory protonové pumpy. H2 blokátory se jeví v tomto případě jako neúčinné. Nedávno dlouhodobě užívaný nimesulid (Coxtral, Aulin, Nimesil) s rychlým nástupem účinku je od září 2007 schválen společností SÚKL v dávkování 200 mg denně (2 tablety) pouze po dobu dvou týdnů. Při dlouhodobějším podávání se může projevit jeho hepatotoxicita. Své místo mají díky inhibici syntézy prostaglandinů při řešení primární dysmenorey (NSA).
2. Analgetika II. stupně WHO – slabé opioidy
Užívání tramadolu (slabý µ-agonista) je rozšířeno pro jeho rozmanitou škálu lékových forem vhodných k řešení akutní i chronické bolesti. Toho času je v České republice registrováno asi 400 různých balení a forem přípravků s obsahem tramadolu. V léčbě AB se uplatňuje tramadol ve formě kapek, effervescentní tableta Tradef (50 mg) a během hospitalizace intravenózní podání. V chronické terapii je dostupný velký výběr retardovaných forem. Nejčastějšími nežádoucími účinky jsou nauzea a zvracení na počátku léčby a výskyt zácpy při dlouhodobém podávání. K řešení těchto problémů se využívá kombinace s antiemetiky (Degan, Torecan) a laxativy. Maximální denní dávka je 400 mg.
Často se v praxi setkáváme s pacienty, kteří mají popsanou alergii na tramadol a to ve formě nauzey a zvracení. Je nutno zdůraznit, že se jedná o běžný nežádoucí účinek všech opioidů.
Kombinovaná analgetika
Oxfordská liga analgetik přinesla přesvědčivý doklad o tom, že kombinace slabých opioidních analgetik (kodeinu, tramadolu) s paracetamolem má výhodný aditivní až synergický efekt a významně vyšší analgetickou účinnost, než když jsou tyto látky podány samostatně [7].
Za zmínku stojí Panadol ultra rapid (paracetamol + kofein + kodein) s rychlým nástupem účinku a Zaldiar (paracetamol + tramadol). Tato kombinace zaručuje vyšší analgetické působení a zároveň snížení toxicity a výskytu nežádoucích účinků tramadolu. Nevýhodou těchto preparátů z pohledu pacienta je jejich vyšší cena.
3. Analgetika 3. stupně WHO
Při velmi silné, neztišitelné bolesti se využívají silné opioidy. Opioidy mají na lidský organizmus komplexní vliv. V dnešní době již zaznamenáváme ústup od tzv. opiofobie, kdy byly tyto léky určeny pouze k řešení terminálních stavů v oblasti onkologie. Opioidy mohou mít sice různé nežádoucí účinky (nevolnost, zvracení, dezorientace, zácpa), ale téměř žádný z nich neohrožuje při adekvátním terapeutickém postupu pacientův život.
K řešení AB lze po určení diagnózy užít morfin nebo piritramid (Dipidolor) podle aktuálních poznatků subkutánně. Dříve běžně užívaný pethidin je již dnes v managementu léčby bolesti pokládán za obsolentní z důvodu krátké doby působení (2 hod) a vzniku toxického metabolitu norpethidinu.
Intravenózní aplikace silných opioidů je vyhrazena pouze pro pacienty, kteří jsou trvale monitorováni, a přísluší anesteziologovi nebo intenzivistovi.
Také některé chronické nenádorové bolestivé stavy v gynekologii, které jsou opioid senzitivní, mohou vyžadovat dlouhodobou aplikaci silných opioidů. Riziko vzniku psychické závislosti u pacientů bez anamnézy abúzu je nízké. Každý nemocný dlouhodobě léčený opioidy však musí být považován za fyzicky závislého a při náhlém vysazení je nutno počítat s rizikem vzniku abstinenčního syndromu. Nejčastěji používaná farmaka jsou dostupná v perorálních retardovaných formách: morfin (Vendal, MST – ukončena registrace v ČR), oxykodon (Oxycontin) a hydromorfon (Palladone), která se podávají 2krát denně, novější preparát hydromorfonu (Jurnista) působící 24 hod. Velkým pokrokem jsou transdermální formy v matrixových systémech: buprenorfin a fentanyl, které zajišťují 72–84 hod působení a vysoký komfort pro pacienta.
Při této léčbě je třeba dodržovatdůsledně pravidla pro léčbu silnými opioidy dle Metodických doporučení pro léčbu chronické nenádorové bolesti (2009) Společnosti pro studium a léčbu bolesti (SSLB). Důležitá je správná indikace a znalost psychosociálního prostředí nemocného. Pacient podepisuje před zahájením léčby tzv. informovaný souhlas a je vybaven průkazem pacienta léčeného silnými opioidy. Tyto léky je nutno předepisovat na recepty s modrým pruhem a je třeba zdůraznit, že neexistuje preskripční omezení!
Léčba je zahajována co nejnižšími dávkami, a to z důvodu zachycení nežádoucích účinků, a pacient je na toto období vždy vybaven pomocnými léky.
4. Adjuvantní léčiva
Koanalgetika primárně nepatří mezi analgetika, ale svými účinky příznivě ovlivňují vedení bolesti nervovými vlákny. Bývají také označována jako modulátory bolesti. Pokud je na základě anamnézy a charakteru bolesti uvažováno o neuropatické bolesti, jsou tato farmaka běžnou součástí léčby. Uplatňují se i v potlačování šlehavých, bodavých nebo vystřelujících pocitů bolesti, které mohou být zaměňovány za PB a jsou tlumeny užíváním koanalgetik v pravidelných intervalech.
Antiepileptika snižují spontánní neuronální výboje účinkem na iontové kanály nebo neurotransmitery, a mohou tak mít obdobný efekt na abnormální výboje bolestivých vláken. V poslední době byl prokázán i příznivý efekt některých antiepileptik III. generace a ta se stala běžnou součástí léčby neuropatické bolesti. Gabapentin (Neurontin, Gabator, Gabalept) inhibuje napěťově řízené vápníkové kanály a zesiluje GABAergní tlumivé účinky. Začíná se dávkou 300 mg na noc (v geriatrii 100 mg) a opatrně se v průběhu několika dnů až týdnů, podle snášenlivosti, titruje do analgeticky účinné dávky (900–3600 mg). Gabapentin je velmi dobře tolerován, mezi nejčastější nežádoucí účinky patří somnolence, závratě a někdy ataxie. Pregabalin (Lyrica) je nově vyvinutý nástupce gabapentinu se silnější afinitou k podjednotce Ca kanálu. Jednou z výhod oproti gabapentinu je jeho výborná biologická dostupnost (bioavailability), takže nevyžaduje delší titrační období. Příznivě ovlivňuje i poruchy spánku a deprese. V psychiatrii je indikován k terapii afektivně úzkostné poruchy. Podle efektu a tolerance se užívá 75–600 mg/den, ve dvou denních dávkách. Má poměrně hodně nežádoucích účinků, z nichž jsou nejčastější: sucho v ústech, poruchy vidění, ospalost, otoky (zejména periferní), přírůstek hmotnosti.
Hlavní skupinou psychofarmak, která příznivě působí na bolest, zůstávají tricyklická antidepresiva. Mechanizmus jejich analgetického účinku spočívá v potenciaci noradrenergní a serotoninergní neurotransmise na úrovni descendentního tlumivého systému míšního. Lékem první volby, schváleným i Neurologickou společností, je amitriptylin. Začíná se opět malými dávkami 25 mg na noc, pro jeho tlumivý účinek, a pokračuje se až do maximální analgetické dávky 150 mg/den. Jeho podání je kontraindikováno u pacientů s kardiologickou anamnézou (arytmogenní účinek), s glaukomem a v kombinaci s IMAO (inhibitory monoamonioxidázy). Indikací pro jeho podání je také pálivý charakter bolesti. U pacientů s onemocněním kardiovaskulárního aparátu bývá lépe tolerován nortriptylin. Ostatní moderní antidepresiva, zejména skupiny SSRI, se většinou jako koanalgetika v léčbě bolesti neuplatňují, ale mají své významné místo v léčbě doprovodné deprese. Pro minimální množství lékových interakcí a dobrou snášenlivost se nejčastěji používá citalopram.
Myorelaxancia jsou indikována u bolestí doprovázených svalovými spasmy. Nejčastěji užíváme baclofen, tetrazepam (Myolastan), mefenoxalon (Dorsiflex) a tolperizon (Mydocalm). Je třeba zdůraznit, že u chronických bolestivých vertebrogenních stavů, u hypotonických jedinců a osob s ochablým svalovým korzetem, je léčba myorelaxancii naprosto nevhodná. Hlavní léčebný efekt má v takových případech fyzioterapie [8].
Lokální anestetika mají své místo zejména v léčbě neuropatické bolesti k lokální aplikaci. V praxi se nejčastěji používá mesocain gel a lidocain spray vhodný i na oblast vulvy při pruritu.
5. Pomocná léčiva
Pomocná léčiva představují skupinu léků, která se používají k prevenci a terapii nežádoucích účinků analgetik. Na počátku léčby opioidy se zařazují antiemetika. Častou stížností pacientů při dlouhodobé léčbě je výskyt zácpy. Doporučuje se úprava diety, dostatek tekutin a laxativa s preferencí přírodních látek. Vhodné je střídání různých projímadel.
Gastroprotektiva, a to pouze inhibitory protonové pumpy, mají své uplatnění při dlouhodobém podávání NSA a kortikoidů.
Psychoterapie
Bolesti v oblasti pánve jsou častou příčinou problémů v sexuálním životě žen. Častý stud při prvním kontaktu s lékařem zamezuje důkladnému odběru anamnézy a určení správné diagnózy. Proto patří vytvoření důvěry mezi základní uplatňované principy a usnadňuje další postupy v terapii. U CHB je namístě spolupráce s psychologem nebo psychiatrem a v případě potřeby zahájení léčby psychofarmaky.
Velice dobrou podpůrnou funkci plní i jako doplněk metody alternativní medicíny.
Rehabilitace
Patofyziologickým podkladem pro bolesti podbřišku nebo dysmenorey jsou u mladých žen často patologie myoskeletálního aparátu. Mezi nejčastější patří blokáda sakroiliakálního skloubení, poruchy thorakolumbálního přechodu a spazmusm.iliopsoas [9]. Pomůckou v diagnostice může být i palpace trigger pointů (spouštěče bolesti) v oblasti břišních, gluteálních svalů a m. piriformis [10]. Proto, po vyloučení ostatních příčin, patří spolupráce s rehabilitačním lékařem mezi důležité postupy v léčbě bolestivého stavu.
Invazivní postupy
Po vyčerpání všech možností farmakoterapie bez dosažení efektivní analgezie se přistupuje k invazivním technikám. Nejrozšířenější metodou jsou nervové blokády na úrovni míšní (epidurální, spinální, kaudální), blokády nervových pletení či vegetativních ganglií.
Z farmak k nervovým strukturám nejčastěji aplikujeme směs lokálního anestetika a opioidu, v případě periferních nervů lze použít i depotní kortikoidy. Nejčastějšími místy zásahu v gynekologické problematice jsou n. genitofemoralis, n. ilioinguinalis, a zejména n. pudendus. V případech silné onkologické bolesti nereagující na systémovou léčbu opioidy jsou u nádorů v oblasti pánve a vulvy prováděny ireverzibilní neurolytické blokády ganglion impar alkoholem a fenolem.
Závěr
Léčba akutní bolesti v gynekologické oblasti patří plně do rukou gynekologa. Pokud se však jedná o bolest chronickou, své uplatnění nachází multidisciplinární přístup, který zahrnuje spolupráci algeziologa, gynekologa, neurologa, rehabilitačního lékaře, psychologa a psychiatra. Tím je vytvořena příležitost využít všechny dostupné metody k řešení bolestivého stavu a zlepšit kvalitu života pacientek.
MUDr.
Pavlína Nosková
Centrum
léčby bolesti KARIM, VFN
v Praze
pavlina.noskova@vfn.cz
Sources
1. Čepický P, Líbalová Z. Bolest v gynekologii. In: Rokyta R (ed). Bolest. Praha: Tigis 2006: 446–452.
2. Yamamotová A, Papežová H. Význam estrogenů ve vnímání bolesti u zdravých žen a pacientek s poruchou příjmu potravy. Psychiatrie 2010; 14 (Suppl 1): 30.
3. Rokyta R. Patofyziologie bolesti. Postgrad Med 2003; 5(1): 51–54.
4. Ševčík P, Málek J et al. Léčba akutní pooperační bolesti. Doporučení ČSARIM 2008.
5. Lauterburg BH. Analgesics and glutathione. Am J Ther 2002; 9(3): 225–233.
6. Kršiak M. Farmakoterapie bolestí zad. Bolest 2007; 10(1): 11–16.
7. Kršiak M. Analgetická kombinace paracetamolu s tramadolem. Farmakoterapie 2005; 1(3): 208–211.
8. Mečíř P. Neurologové se ptají. Neurol Praxi 2008; 9(2): 119.
9. Jandová J. Vertebroviscerální stavy. Doporučené postupy pro praktické lékaře ČLS JEP 2001.
10. Fall M, Baranowski AP, Elneil S et al. EAU guidelines on chronic pelvic pain. Eur Urol 2010; 57(1): 35–48.
11. Doležal T, Hakl M, Kozák J et al. Metodické pokyny pro farmakoterapii akutní a chronické nenádorové bolesti. Praha: SSLB 2009.
12. Doležal T, Hakl M, Kozák J et al. Metodické pokyny pro farmakoterapii nádorové bolesti. Praha: SSLB 2009.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicineArticle was published in
Practical Gynecology

2011 Issue 2
Most read in this issue
- GyneFix – nitroděložní tělísko bez pevného těla a ramének
- Farmakoterapie endometriózy v reprodukční gynekologii
- Prognostický význam tumor markeru SCCA u pacientek s operabilními stadii dlaždicobuněčného karcinomu děložního hrdla
- Probiotika v gynekologické praxi
