SEXUÁLNĚ PŘENOSNÁ ONEMOCNĚNÍ Z POHLEDU UROLOGA
Sexually transmitted disease from the urologist's point of view
The author offers information and review about important sexual transmitted diseases (STD). He is engaged in etiology, diagnosis and therapy of STD and options of prevention of their spread.
KEY WORDS:
sexual transmitted diseases, Chlamydia trachomatis, Candida, Neisseria gonorrhoeae, Treponema pallium, Herpes genitalis virus, Human Papilloma Virus, Human Immunodeficiency Virus
Authors:
R. Staněk
Authors‘ workplace:
Urologické oddělení, Slezská nemocnice Opava
Published in:
Urol List 2005; 3(2): 56-64
Overview
Autor podává informace a přehled o významných sexuálně přenosných onemocněních (sexual transmitted diseases - STD). V textu se zabývá etiologií, diagnostikou a terapií STD a možnostmi prevence jejich šíření.
KLÍČOVÁ SLOVA:
sexuálně přenosná onemocnění, Chlamydia trachomatis, Candida, Neisseria gonorrhoeae, Treponema pallium, Herpes genitalis virus, Human Papilloma Virus, Human Immunodeficiency Virus
ÚVOD
STD (sexually transmitted disease) - sexuálně přenosná onemocnění jsou infekční onemocnění přenosná sexuálním stykem. Jedná se o onemocnění, jejichž hlavním vektorem šíření je sexuální styk, případně přímý kontakt.
Rozlišujeme 5 základních - klasických sexuálně přenosných onemocnění a další onemocnění, která jsou sexuálním stykem přenositelná. Mezi 5 základních onemocnění patří syfilis, gonorrhoea, granuloma inguinale, lymfogranuloma venerum a chankroid. Další heterogenní skupinou jsou onemocnění typu chlamydie, AIDS/HIV, poševní vaginóza, kvasinkové infekce, herpes genitalis, mykoplazmata, ureaplazmata a také pneumonie novorozenců a virová hepatitida B (VHB). Jako urologové se nejčastěji setkáváme se zánětlivými projevy infekčních onemocnění v uropoetickém systému a na zevním genitálu. V uropoetickém systému jsou to především uretritida, prostatitida, epididymitida a balanitida (tedy onemocnění převážně mužské populace). Symptomatologie u žen je predispozičně lokalizována do oblasti zevních genitálií, případně vnitřních genitálií (kolpitis, vulvovaginitis, cervicitis, endometritis, salpingitis, pánevní zánětlivé onemocnění). Samozřejmě že ani ženám se nevyhýbá onemocnění uretritis, cystitis. Žádné z pohlaví není ušetřeno kožních projevů STD.
Klasická sexuálně přenosná onemocnění se vyskytují především u skupin s rizikovým chováním v rámci sexuální hygieny. Toto chování je charakterizováno promiskuitou a častým nezodpovědným střídáním sexuálních partnerů. Ve druhé skupině onemocnění představují podobné riziko onemocnění AIDS/HIV a v současnosti asi nejrozšířenější sexuálně přenosné onemocnění - chlamydie. Chlamydie je také nejčastějším původcem příznaků, se kterými pacienti do ambulance urologa přicházejí. Šíření STD umožňuje také jejich častý asymptomatický průběh, který ještě více uvolňuje rizikové nezodpovědné chování. Obecně lze říci, že se klasická sexuálně přenosná onemocnění dostávají do ústraní vlivem nárůstu frekvence výskytu chlamydií a virových onemocnění.
Úlohou urologa a jiných odborností, které se zabývají STD, je:
- diagnostika a terapie symptomatických pacientů
- efektivní vyhledání sexuálních partnerů, jejich diagnostika a terapie
- vyhledávání asymptomatických nemocných a jejich terapie
- efektivní poučení obyvatelstva o sexuální hygieně.
CHLAMYDIA TRACHOMATIS
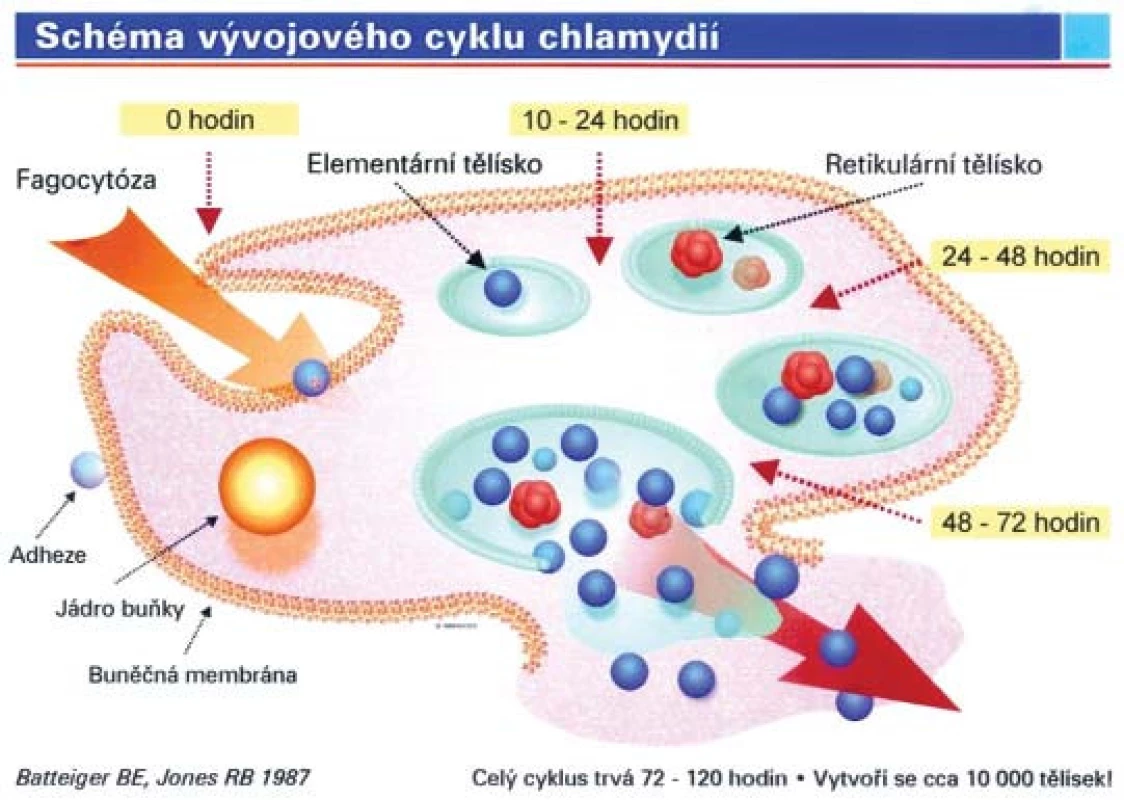
Infekce způsobené chlamydií trachomatis je v západním světě nejrozšířenější onemocnění patřící do skupiny STD. V MEDLINu získáme zadáním hesla chlamydie 17 551 odkazů. Vzhledem k tomuto faktu by měl být každý urolog dobře informován o tomto onemocnění a měl by být schopen jej dobře diagnostikovat a především dobře léčit. Chlamydie jsou gramnegativní intracelulární bakterie - kokobacily. Urology zajímají chlamydie trachomatis, a to především sérotypy D - K. Jsou závislé na metabolizmu hostitelské buňky, a tato vlastnost jim dává určité specifikum, které je důležité respektovat právě s ohledem na diagnostiku a terapii intracelulárních infekcí. Vyskytují se ve 2 vývojových fázích [1]. Jedná se o metabolicky aktivní neinfekční a infekční metabolicky inaktivní stadium vývoje (retikulární RB a elementární tělísko EB). Vývojový cyklus chlamydií trvá asi 48-72 hodin. Začíná endocytózou elementárního tělíska do buňky a změnou na metabolicky aktivní retikulární tělíska, která se začnou dělit. Cyklus obvykle končí rozpadem buňky a uvolněním množství elementárních tělísek, která napadají další buňky a již zmíněnou endocytózou jsou inkorporována do dalších buněk. Vývojový cyklus může probíhat i bez rozpadu buňky - elementární tělíska se uvolňují exocytózou. Průběh chlamydiové infekce je ve většině případů asymptomatický (u 50 % mužů a 70 % žen)! Toto chování infekce je rizikovým faktorem pro další šíření onemocnění.
Ve Velké Británii stanovila skupina zabývající se prevencí STD rizikové faktory pro získání chlamydiové infekce [2]:
- mladší věk (pod 25 let)
- tzv. „singles“
- užívání perorálních kontraceptiv
- nový sexuální partner v průběhu posledních 3–12 měsíců
- etnikum
- nižší stupeň vzdělání
- nulipara.
Centrum pro kontrolu nemocí v USA provedlo v letech 1999–2001 skríningovou studii, jejíž výsledky byly publikovány v říjnu 2004:
5–14 % žen ve věku 16–20 let a 3–12 % žen mezi 20–24 lety mělo pozitivní testy na chlamydie [3]. Přítomnost chlamydiové infekce zvyšuje riziko vzniku PID (pánevní zánětlivá nemoc - Pelvic Inflammatory Disease). Toto onemocnění v akutní formě ohrožuje ženu na životě pod obrazem sterilní peritonitis, chronická forma je velmi diskomfortním onemocněním probíhajícím pod obrazem pánevní bolesti, dyspareunie, mikčních potíží, subfebrilní, rezultující v infertilitu. U 5–50 % žen s PID byly izolovány chlamydie.
17 % žen s PID je infertilních a 10 % žen je postiženo ektopickým těhotenstvím [4]. Z vyhodnocení rizikových faktorů a incidence vyplynula doporučení pro skríningové programy:
- skríning je doporučen u sexuálně aktivních žen pod 25 let (vzhledem k maximu prevalence), cílený skríning u žen nad 25 let se provádí:
- v případě změny sexuálního partnera během posledních 12 měsíců
- u všech žen, které se chystají k endoinstrumentaci v pochvě.
Z uvedeného je zřetelné, že se cílený skríning zaměřuje především na ženy. Existují 3 důvody, proč tomu tak je:
- ženy onemocní vysoce rizikovým onemocněním PID
- vyšší spolupráce žen než mužů při užití detekčních metod
- počítačové analytické modely prokázaly vyšší „cost-effectiveness“ (poměr cena/ /efektivita) při skríningu žen než při skríningu mužů [2].
Skríningové programy jako v USA jsou v současnosti v ČR hudbou budoucnosti, ale neměli bychom se vyhýbat jiným formám depistáže.
Kdy chlamydie vyšetřovat a jak?
Chlamydie atakují vícevrstevnatý přechodní epitel uretry, čípku děložního a spojivkového vaku. Z toho vyplývá také symptomatologie. U žen je na chlamydiovou infekci nutno myslet v případě recidivujících infekcí močových cest pod obrazem uretritidy nebo cystitidy. Chlamydie může být podkladem pro adhezi dalších patogenních kmenů. Dále je nutno na chlamydie myslet v případě protrahovaného mikčního diskomfortu: strangurie, nucení na mikci, polakisurie, urgence, tlaky v hypogastriu. Močový a kultivační nález je často chudý nebo se vyskytuje hraniční množství leukocytů v močené moči s negativním kultivačním nálezem. Reiterův syndrom se symptomatologií uretritidy, polyartritidy a konjunktivitidy je velmi pravděpodobně způsoben chlamydiemi. V gynekologii se chlamydie projevují mukopurulentní cervicitidou. U mužů bývá nejčastějším projevem infekce uretritida se stranguriemi, nucením na mikci, případným sklovitým výtokem. U symptomů chronické prostatitidy, bolestí perigea a bolestí v hypogastriu nejasné etiologie je nutno provést vyšetření na chlamydie před a po masáži prostaty. U mladých mužů jsou chlamydie nejčastější příčinou akutní epididymitidy, s možností negativního ovlivnění fertility jedince. Toto jsou indikace klinické, vycházející z pohledu symptomatologie. Při indikaci k vyšetření chlamydiové infekce je nutno brát v úvahu i doporučení v rámci rizikových faktorů a skríningových programů (viz výše). U novorozenců, kteří se narodí matkám s pozitivní infekcí, je 60-70% riziko vzniku konjunktivitidy, nebo chlamydiové pneumonie. Je třeba doplnit, že chlamydie se mohou přenášet i orálním stykem a mohou vést ke vzniku atypických chlamydiových onemocnění: proktitis a tonsilitis.
Jaké jsou možnosti diagnostiky Chlamydia trachomatis?
K diagnostice chlamydiových infekci používáme několik metod: kultivační metody, přímý průkaz, imunofluorescenci ELISA testy, amplifikační metody LCR (ligase chain reaction), PCR (polymerase chain reaction) a také genové hybridizační testy. Tyto testy se liší svou invazivitou, specificitou, senzitivitou a v neposlední řadě i cenou. Pouze u amplifikačních metod můžeme použít přímo moč nebo sekret, v ostatních případech je nutno provádět invazivní stěry na štětičku. Kultivační metoda vyžaduje přísné dodržení parametrů odběru a dopravy, které lze víceméně zajistit jen při těsném sepjetí mikrobiologické laboratoře s klinickým pracovištěm. Specificita kultivačních metod je 100 %, senzitivita okolo 60–80 %. Výhodou imunoflurescenčního průkazu chlamydií je jejich možnost užití i při větší vzdálenosti mezi klinickým pracovištěm a mikrobiologem. Interval mezi odběrem a zpracováním materiálu na sklíčku je až 48 hod. Tato metoda je ale zatížena subjektivní chybou hodnotitele. V případě zkušených mikrobiologů ale dosahuje specificita až 99 % a senzitivita 60–75 %. Amplifikační metody jsou výhodné u asymptomatických jedinců a zajišují dobrou spolupráci s diagnostickým centrem. Jejich výhodou je vysoká specificita pohybující se kolem 98–99 % a senzitivita kolem 70 %, možnost neinvazivního odběru moči a doprava i na větší vzdálenosti v transportním médiu. Jejich nevýhodou je vysoká cena.
![Srovnání senzitivity a specificity jednotlivých testů [5].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/21e078d4fdce012ab2e7cb3cf4356147.png)
Terapie chlamydiových infekcí vyžaduje dlouhodobější podávání antibiotik, než je obvyklé u jiných infekčních onemocnění. Obvyklá doba podávání je 10–14 dní, není výjimkou aplikace 21 a více dní. Doporučuje se použití antibiotik patřících do tetracyklinové, makrolidové, azalidové a fluorochinolonové řady. Doxycyklin je základním antibiotikem, podává se v dávce 200 mg na den, obvykle 10–21 dní. Průnik do buněk je pasivní a pomalý. Na druhou stranu je to nejlevnější terapie. Dále pak se doporučuje terapie erytromycinem 500 mg 3krát denně po dobu 14–21 dní. Erytromycin lze užít u těhotných žen, stejně tak roxitromycin 2krát 300 mg per os denně 3 dny, poté 2krát 150 mg denně 10 dnů. Pro terapii chlamydiových infekcí užíváme také klaritromycin v dávce 500 mg 1krát denně v SR formě 10–14 dní. Flurochinolony jsou v terapii chlamydiových infekcí velmi účinné, výhodou je jejich rychlý průnik do buněk a dlouhodobá účinnost. Nejčastěji využíváme ciprofloxacin 500 mg 2krát denně 10–14 dní [6]. Azitromycin je velmi vhodný pro rizikové skupiny, svou farmakokinetikou zajišuje dobrou spolupráci pacientů. Dobře proniká do buněk. Jeho výhodou je dlouhá doba působení po jednorázovém podání. Proto se v USA doporučuje terapie Azitromycinem v jednorázové dávce 1000 mg, případně jeho podávání 3–5 dní v dávce 500 mg na den. Azitromycin je možno použít v těhotenství. V případě těhotenství a alergií na výše jmenované léky je možno použít i amoxycilin 3krát 500 mg po dobu 10–14 dní, s vědomím nižší efektivity tohoto léku. V terapii je nutno dodržovat následující doporučení [5]:
- vždy léčit i sexuální partnery nemocného a následně provést kontrolu terapie diagnostickými testy
- v průběhu terapie je vhodné dodržovat sexuální abstinenci
- do doby potvrzené negativity všech sexuálních partnerů používat bariérovou ochranu - kondom
- kontrolní testy chlamydií fluroescenční metodou provádět 3 týdny po ukončení terapie (k vyloučení falešně pozitivních nálezů)
- doporučuje se kontrolní skríningový test 3–4 měsíce po terapii, vzhledem k časté recidivě chlamydií.
Chlamydie nepodléhají povinnému epidemiologickému hlášení.
KANDIDA - KVASINKY
Dalším onemocněním, se kterým se často setkáváme, je poševní kandidóza a vaginóza. Frekvence tohoto onemocnění je výrazně vyšší než u chlamydií.
Dle komparativní studie Arzouniho byl výskyt chlamydií 10% a kandidózy 45% při symptomatologii pálení zevního genitálu a bolestech pánve [7]. Vaginální kandidóza se obvykle projevuje jako vulvovaginitis, s příznaky pálení, svědění zevního genitálu, zarudnutí a vytváření pustul na kůži a sliznici pochvy s bělavým výtokem. Doprovodným příznakem bývá nucení na mikci, polakisurie, strangurie imitující infekci dolních močových cest. Podobně může být postižen glans a vnitřní list prepucia, kandidová balanitida se může projevit až ulceracemi a následně fimózou. Zdrojem této infekce jsou kvasinky, nejčastěji Candida albicans. Je zajímavé že kvasinky se vyskytují až u 13 % zdravých asymptomatických žen. V ústech se vyskytují kvasinky v 50–60 %. Kandidóza vzniká především u žen v aktivním věku, u postmenopauzálních žen je kandidóza nepravděpodobná, vzhledem k poklesu hladiny estrogenů, poklesu hladiny glykogenu v buňkách pochvy a atrofizaci poševní sliznice. Při symptomatologii vaginální kandidózy se v tomto případě jedná spíše o vaginózu - poševní dysmikrobii. Dalším zdrojem kandidózy je superinfekce při medikaci širokospektrými antibiotiky, imunosuprese při cukrovce, hypotyreóze, Cushingově syndromu a jiných imunitních a endokrinologických onemocněních, nádorová onemocnění, medikace cytostatiky, AIDS, hypovitaminóza B1, B2, B6, C8.
Diagnóza spočívá v klinickém vyšetření, kultivaci a mikroskopickém vyšetření stěrů, ve kterých nalézáme hyfy.
Terapie je především topická. Užíváme klotrimazol, mikonazol a nystatin 7–14 dní ve formě masti, případně intravaginálních tablet. Mikonazol ve formě 200mg intravaginální tablety je možno užít jen 3 dny. U těžších případů používáme orální jednorázovou medikaci flukonazolem 150 mg nebo itrokonazolem 600 mg [9]. V případě topické aplikace antimykotik by měla terapie pokračovat ještě 48 dní po vymizení syndromů. Jako prevence kandidózy se doporučuje terapie laktobacilem, studie však prokázaly, že tato prevence není efektivní [10].
NEISSERIA GONORRHOEAE - KAPAVKA
Trend ve výskytu gonokokové infekce je pro společnost uspokojivý, protože v posledních letech docházelo k postupnému snižování incidence [11] (graf 1). Tento trend nadále pokračuje. Při záchytu onemocnění je nutno provést povinné epidemiologické hlášení.
![Vývoj počtu hlášených případů gonokokové infekce v ČR [12].](https://pl-master.mdcdn.cz/media/image/809753b07951c657342274b1fc9205c2.jpg?version=1537794888)
Prevalence se dnes pohybuje na úrovni 22 případů na 100 000 obyvatel, data ÚZIS za rok 2002 a 2003. Výskyt onemocnění se liší také podle lokality (graf 2).
![Gonokoková infekce - podíl počtu případů v krajích ČR v roce 2000 [11].](https://pl-master.mdcdn.cz/media/image/e796c69f3af36b6f32bd14d1e6e89175.jpg?version=1537797408)
Gonokoková infekce je způsobena diplokokem Neisseria gonorrhoeae. Jedná se o sexuálně přenosné onemocnění, které probíhá nejčastěji jako uretritida. V jiných případech jsou postiženy další orgány urogenitálního systému. Často dochází k asymptomatickému průběhu, obvykle u žen, které se tak stávají přenašečkami onemocnění. Toto onemocnění se šíří prakticky výhradně sexuálním stykem a je typickým onemocněním rizikových promiskuitních skupin. Inkubační doba je 3–6 dní od nakažení, maximálně 14 dní. Probíhá jako akutní či chronické onemocnění. U mužů je typickým projevem urethritis acuta se žlutavým hnisavým výtokem s projevy pálení a řezání uretry při i mimo mikci. Chronická infekce se projevuje spíše jako drobný výtok, resp. jako kapka na spodním prádle, a dysurie. Častěji se vyskytuje jako chronická prostatitis, případně epididymitis, která následně může vést ke sterilitě.
U žen je akutní uretritida vzácnější. Gonokoková infekce se spíše projevuje hlenohnisavou cervicitis, případně vulvovaginitis s otokem a zarudnutím sliznic.
Základem diagnostiky neisseria gonorrhoeae je mikroskopické vyšetření a kultivace. Nejlépe je provádět odběr z typických lokalit (uretrální ústí, cervix, pochva) přímo na kultivační půdy (čokoládový agar), nebo do transportních půd. Neisserie jsou poměrně citlivé organizmy, proto by jejich kultivace měla být zahájena co nejdříve. Odběr by měl být proveden cca 2–5 hodin po mikci, abychom dosáhli maximální koncentrace patogenů. Iniciálně se gonokoky nacházejí extracelulárně, v průběhu onemocnění se fagocytózou postupně lokalizují do leukocytů, tedy intracelulárně.
V terapii podáváme především penicilinová antibiotika. V České republice jsou neisserie dobře citlivé na fluorochinolonová antibiotika. V západní Evropě a USA se doporučuje jednorázová terapie levofloxacinem 250 mg p. o., alternativně je možno použít cefixim per os a ceftriaxon jednorázově v intramuskulární aplikaci, což zajišuje dobrou spolupráci pacienta. Často dochází k současnému výskytu chlamydií a gonokoků, proto je vhodné provádět vyšetření na oba organizmy současně a nezapomínat na zopakování obou vyšetření po terapii s odstupem času cca 3 měsíců. Nedílnou součástí terapie je depistáž sexuálních partnerů, jejich vyšetření a terapie, podobně jako to bylo popsáno v oddíle chlamydií.
TREPONEMA PALLIDUM - SYFILIS
Incidence syfilis se na rozdíl od kapavky zvyšuje [12]. Je k nám často importována z východních zemí bývalého Sovětského svazu, kde je její výskyt velmi vysoký. Bohužel v těchto případech je pozitivita syfilis také spjata s vyšším rizikem HIV-pozitivity. Zvyšuje se incidence časných onemocnění (graf 3) s latentním či atypickým průběhem.

Treponema pallidum patří mezi spirochety. Zdrojem infektu je v 95 % rizikový sexuální styk. Může se jednat i o jiný kontaktní způsob přenosu. Typický průběh získaného onemocnění je charakterizován tvorbou kožních eflorescencí (na rozdíl od gonorey a chlamydiových infekcí, které probíhají pod obrazem iritačních příznaků). Treponemová infekce probíhá ve 3 stadiích. Urolog se nejčastěji setká s primárním stadiem.
Inkubační doba je okolo 3 týdnů (ale i 90 dní). Po uplynutí inkubační doby je 1. stadium charakteristické tvorbou tzv. ulcus durum, tvrdého vředu. Začíná zarudnutím se sekrecí (ta obsahuje obvykle značné množství treponem). Později po 2 dnech se tato léze mění na indukovanou tuhou papulu s plochým šedavým lesklým středem - syfilitická skleróza. Celý proces může probíhat atypicky vznikem edému, erozivních změn, může vzniknout purulentní balanitida s fimózou. V 6. týdnu od nákazy vzniká unilaterální lymfadenopatie (indolentní bubo). V tomto období se také syfilis stává séropozitivní, tedy sérologicky diagnostikovatelným onemocněním. S 2. stadiem onemocnění, které se projevuje především kožním exantémem, se již urologové obvykle nesetkávají. 3. stadium je typické systémovými změnami, tzn. specifickým granulomem - gumou, aortitis, neurosyfilis.
V případě podezření na onemocnění syfilis se používá několik metod k diagnostice. Základní metodou je přímý mikroskopický průkaz treponem v sekretu za použití fázového kontrastu. Daleko častěji se používají sérologické metody. Nejstarší metodou je průkaz protilátek proti fosfolipidovým antigenům: BWR - Bordet-Wassermanova reakce. V poslední době se spíše používá VDRL - general disease research laboratories a RRR - rychlá reaginová reakce. Tyto 3 diagnostické postupy jsou založeny na nespecifickém průkazu treponem. Přímý průkaz protilátek proti treponemám je představován metodou TPHA - treponema pallidum haemaglutination assay (lyzát z treponemat adsorbovaný na kuřecí krvinky), TPI - treponema pallidum immobilisation (ztráta pohyblivosti treponemat při styku s krví nemocného člověka) a FTA - ABS (absorpce a eliminace protilátek proti saprofytickým treponematům) [14].
V terapii je stále velmi účinný penicilin. Dochází však často ke vzniku alergických reakcí, případně toxoalergické Jarisch-Herxheimerově reakci vlivem rozpadu treponemat. Doba podávání antibiotik je 15–21 dní. Další možností terapie je podání azitromycinu 2 g perorálně v jednorázové dávce, ceftriaxonu 1 g intramuskulárně denně cca 10 dní nebo doxycyklinu 100 mg 2krát denně po dobu 14 dní [15].
HSV2T - HERPES GENITALIS VIRUS
V diferenciální diagnostice syfilitických lézí primárního stadia je třeba brát v úvahu i vezikulární léze při herpes genitalis. Nejedná se o časté onemocnění, ale vzhledem k promořenosti populace herpetickými viry je nutno se o tomto onemocnění zmínit.
Onemocnění se přenáší přímým kontaktem, inokulací. Jednou nakažený pacient se stává doživotním nosičem viru. Viry se nacházejí v lokálních nervových gangliích. V novorozeneckém věku převažuje infekce HSV2T herpes genitalis, později dominuje HSV1T herpes zoster (50–90 %). Prevalence HSV2T herpes genitalis se potom opět zvyšuje po 15. roce v souvislosti se zvýšenou sexuální aktivitou.
Typickým projevem herpetické infekce je zarudnutí, lokální bolestivost a následný výsev vezikul. Symptomatická infekce HSV se vyskytuje jako projev imunosuprese na podkladě onkologických onemocnění, stresu, virových onemocnění nebo chemoterapie. HSV se projevují především lokálně, mohou však mít také celkové projevy: subfebrilie, febrilie, nevolnost, projevy meningitidy a encefalitidy. HSV2T herpes genitalis probíhá spíše pod obrazem lokální symptomatologie.
Symptomatologie, anamnéza a přímý průkaz viru se sérologickou diagnostikou umožňují detekci viru.
V terapii používáme virostatika: aciklovir, valaciklovir a famciklovir v lokální celkové nebo celkové perorální a injekční formě. U těžkých infekcí virostatika redukují symptomatologii, při dlouhodobém podávání snižují počet recidiv. Diaz Mitoma prokázal ve skupině pacientů léčených famciklovirem 72% reccurence free rate během 12 měsíců oproti placebu reccurence free rate 22 % [16].
HPV - HUMAN PAPILLOMA VIRUS
Dalším onemocněním, se kterým se jako urologové často setkáváme, jsou HPV: human papilloma virus. Onemocnění vyvolává DNA virus [17]. Projevuje se intraepiteliálními lézemi, condylomata accuminata, nádory čípku, penisu a perianálními karcinomy. V histologickém obraze se projevuje zvětšením jádra, hyperchromazií a specificky perinukleárními kavitacemi - koilocytózou [18]. Je jedním z nejčastěji se vyskytujících onemocnění a riziko nákazy je až 70 %. V USA je prevalence 10–46 % u sexuálně aktivních žen a odhadem 10–20 % mužů [19]. U 5–40 % žen probíhá onemocnění symptomaticky [20].
Riziko nákazy je nejvyšší ve věkovém intervalu 20–25 let. Typicky se projevuje výrůstky na sliznici a kůži. Celkově tvoří toto onemocnění poměrně vysoké 10% zastoupení všech genitálních infekcí. Význam této virové infekce spočívá především v riziku vzniku nádorového onemocnění čípku, podíl má i na vzniku penilního a anorektálního karcinomu [21,22,23]. Význam tohoto onemocnění potvrzuje skutečnost, že karcinom čípku tvoří 10 % všech karcinomů u žen. Existuje okolo 100 sérotypů HPV, ne všechny jsou však onkogenní [24]. Mezi sérotypy s potvrzenou onkogenitou patří HPV 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, z nichž nejvýznamnější jsou 16, 18, 31, 45. Nízká onkogenní aktivita se nalézá u sérotypů 6, 11, 42, 43, 44 [25]. Shepherd [26] provedl revizi Cochrane-databáze, kde hodnotil souvislost mezi HPV a karcinomem čípku. Z výsledků studie bylo možno doporučit prevenci nádorového onemocnění čípku cestou dodržování pravidel bezpečného sexu. Zajímavým zjištěním je studie Ramirezova, která poukazuje na to, že v současnosti má populace dost informací o HIV, ale o ostatních sexuálně přenosných onemocněních je informovanost nedostatečná, ačkoliv rizika spojená s jejich nákazou jsou mnohdy epidemiologicky a zdravotně stejně závažná jako u HIV infekce [27].
Diagnostika spočívá na odhalení lézí, tedy klinickém nálezu v oblasti čípku, předkožky, případě perianální oblasti. Typickým projevem HPV-infekce jsou condylomata accuminata, nejčastěji vyvolaná nízkorizikovými sérotypy HPV 6, 11 [24]. V současnosti existují DNA testy, které stanoví i onkogenní riziko, určením sérotypů a rozdělením na vysokorizikové a nízkorizikové HPV. Dříve se používalo barvení dle Papanicolau. V USA se doporučuje k diagnostice jako dostačující pouze cervikální cytologie [28].
V terapii se doporučuje především lokální řešení chirurgické, případně topická aplikace cytostatik, vaporizace CO2 laserem nebo aplikace interferonu v nízké dávce. Studie Cardamakisova [29] prokázala vysokou schopnost trojkombinace v eradikaci HPV-infekce a vzniklých intraepiteliálních lézí: 5-FU a CO2 laserová vaporizace s IFN-a-2a (vysoké dávkování) mělo 96,15% úspěšnost. Kombinace 5-FU a CO2 laserová vaporizace měla 87,09% a kombinace CO2 laserová vaporizace s IFN-a-2a 80% úspěšnost.
Významnou úlohu by měla plnit primární prevence, tedy vzdělávání a informovanost populace o rizicích onemocnění a možnostech prevence při dodržení pravidel sexuální hygieny a bezpečného sexu. V současnosti se také rozvíjejí metody vakcinace proti HPV, a to jak profylaktické, které mají zabránit vzniku infekce, tak terapeutické, které způsobují regresi prekanceróz. Jedná se o DNA-free virus like particles, s navázáním kapsulárního antigenu L130. Metody vakcinace jsou v současnosti v poslední fázi klinických studií [33]. Vakcinace se ukazuje jako účinný způsob sekundární prevence vedoucí ke snížení prevalence onemocněni. Efektivita se netýká jen žen, ale i mužů, první studie ukazují, že lze vakcinací mužů snížit riziko vzniku karcinomu cervixu u žen o 2,2 %. Použitím vakcinace HPV u žen lze snížit riziko karcinomu čípku až o 61 % [34]. Je to cesta, jak se i urologie může zapojit do prevence nádorových onemocnění u žen, tedy diagnostikou rizikových sérotypů HPV, informováním pacientů a pro futuro použitím budoucích vakcinací.
HIV - HUMAN IMMUNODEFICIENCY VIRUS
Není možné se nezmínit o HIV-infekci a jejím vztahu k uropoetickému systému. V současnosti v ČR není její výskyt vysoký, nicméně je nutné se připravit na její vyšší výskyt vzhledem k migraci obyvatelstva, hlavně z východní Evropy, kde se epidemie AIDS zatím šíří velmi rychle a je spojena s koexistencí dalších STD. HIV, AIDS je virové onemocnění způsobené virem HIV - human immunodeficiency virus, v terminálním symptomatickém stadiu vyvolává onemocnění AIDS - Acquired Immunodeficiency Disease Syndrome.
Vir HIV se vyskytuje ve 2 sérotypech, HIV-1 a 2. Nejčastějším zdrojem infekce pro člověka je HIV-1. HIV postihuje lymfocyty CD4+, svou replikací způsobuje jejich pokles a následně pokles imunity vedoucí k manifestaci oportunních onemocnění s protrahovaným, recidivujícím průběhem, v terminální fázi onemocnění s fatálním koncem. Virus se nachází v krvi, moči, preejakulatorní tekutině, vaginálním sekretu a také v mateřském mléce.
Přenos se uskutečňuje především sexuálním stykem (vaginálním, orálním i análním). Další možnou cestou přenosu jsou infikované jehly, domácí piercing, transfuze, porody. Dle dat WHO v roce 2003 bylo na světě nakaženo celkem 37,8 milionu lidí. V roce 2003 bylo nově infikováno 4,8 miliónu lidí a ve stejném roce zemřelo 2,9 miliónu lidí [31,32].
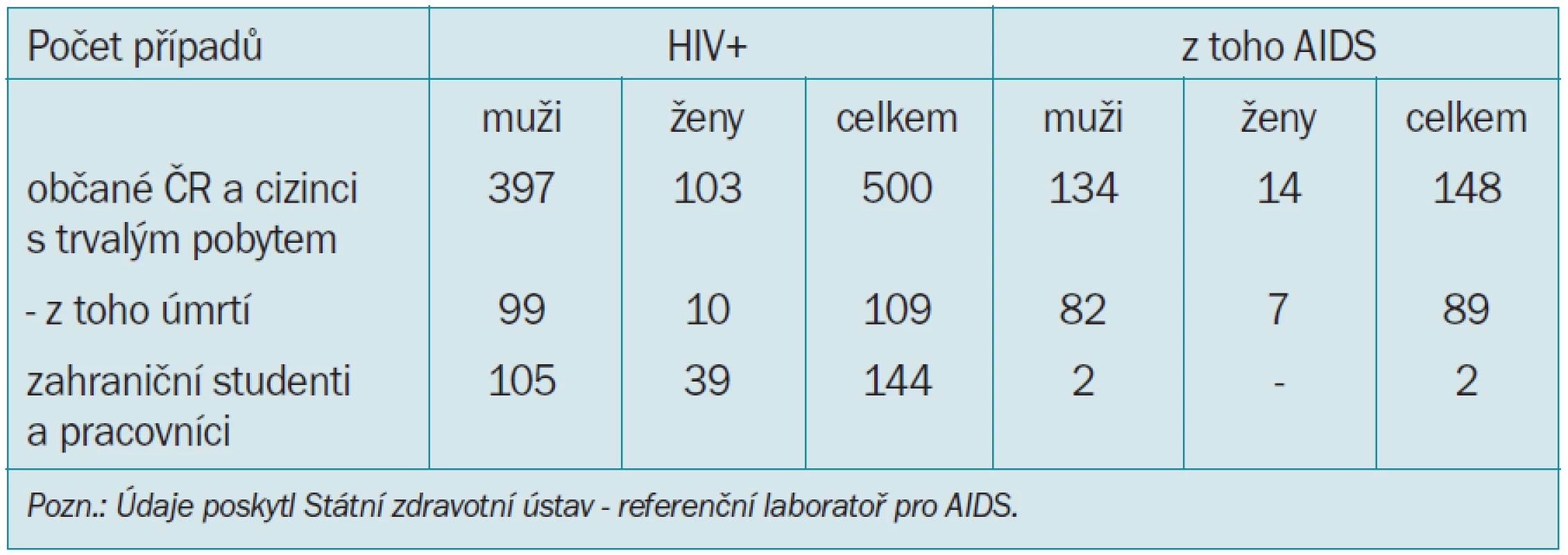
V České republice jsou dostupná data z roku 2000 [35] (tab. 2).
Infekce probíhá v několika fázích. Po expozici virem se do 1–2 měsíců projeví 1. stadium - primární infekce - primoinfekce. Ta se projevuje symptomy podobnými chřipce (flu-like syndrome, subfebrilie, teploty, bolesti hlavy, lymfadenopatie, únavnost). Toto období spontánně vymizí po 1 týdnu až 1 měsíci. Vysoká koncentrace virů v urogenitálních sekretech je pro tento interval typická. Další období je obdobím symptomatickým, probíhá různě dlouhou dobu od několika měsíců až po 10 a více let. V tomto období se může objevit také generalizovaná lymfadenopatie, s projevy lymfopenie, anémie, trombocytopenie a především postupný pokles CD4+. Klinickým projevem je ztráta váhy, pokles aktivity, kožní eflorescence, opakované subfebrilie, poruchy krátkodobé paměti, opakované kvasinkové infekce. AIDS - 3. symptomatické období dělíme na časné a pozdní. V časném období se projevuje AIDS (acquired immunodeficiency syndrome) tzv. malými oportunními infekcemi, jako jsou herpes zoster, kandidózy, leukoplakie, neuropatie. CD4+ poklesne na 100–500/µl. V rozvinutém stadiu jsou CD4+ jsou pod 50/µl. U postižených se projevuje CMV-infekce, atypické mykobakterie, kachektizace, nádorová onemocnění, hematologické neoplazie.
Jaké jsou projevy AIDS v uropoetickému systému?
Poškození ledvin až do terminálního stadia se u AIDS pacientů vyskytuje v 5–10 % [36]. Porucha ledvin se projevuje především hyponatremií a hyperkalemií. Na vzniku hyponatremie se podílí také porucha sekrece adiuretinu vlivem neuropatologie CNS [37]. Případně addisonská krize vlivem CMV infekce nadledvin [37]. Akutní renální insuficience se vyskytuje u 20–40 % pacientů s rozvinutým AIDS na podkladě tubulární nekrózy, hypovolemie, glomerulosklérozy a hyperurikemie při rozpadu nádorových onemocnění. Při vzniku retroperitoneálního Burkitova lymfomu [39], případně non-Hodgkinova lymfomu, dochází k renální obstrukční uropatii s nutností drenáže JJ-stentem nebo nefrostomií. Transplantace ledvin je v případě nedodržení preventivních vyšetření vysoce rizikovým faktorem přenosu HIV [41].
Prostata bývá nejčastěji postižena infekčními atypickými chorobami bakteriální, kvasinkové i virové povahy (tab. 3).

Infekce prostaty často probíhají pod obrazem abscedující prostatitidy s nutností dlouhodobé 6týdenní antibiotické terapie a transuretrální, transperineální nebo transrektální drenáže [42,43,44,45]. Případný adenokarcinom prostaty obvykle probíhá pod obrazem rychle progredujícího onemocnění.
Na penisu se až ve 20 % objevuje Kaposiho sarkom charakterizovaný tvorbou mnohočetných zarudlých indurací a bolestivostí [46]. Vyšší frekvence je zaznamenána u homosexuálních mužů, často se zachytí koexistence s CMV a HSV viry. V terapii lokální solitární léze se používá chirurgická excize, CO2 laser, případně radioterapie, která dosahuje při aplikaci 18–30 Gy v průběhu 10 dní 100% odpovědi a v 54–85 % dlouhodobé remise [47]. Při multilokulární lézi a její generalizaci se pak využívá trojkombinační chemoterapie ABV: adriamycin, bleomycin a vinkristins 88% odpovědí [48].
Varle a nadvarle jsou obvykle postiženy atypickými infekcemi podobně jako prostata [49]. Zvyšuje se výskyt nongerminativních i germinativních nádorů testes. V případě symptomatické fáze se v terapii postupuje dle zavedených standardů terapie [50,51].
AIDS uretry se projevuje frekvenčně urgentním syndromem, také v rámci Reiterova syndromu, s nálezem negativní kultivace. Může docházet k obstrukci uretry vlivem rozvoje B a T-lymfomů [52].
Postižení močového měchýře se projevuje u 36 % AIDS pacientů. Typickým projevem je obraz neurogenního měchýře [53]. Retence se vyskytuje v 54 %, areflexie v 36 %, hyperreflexie ve 27 %, subvezikální obstrukce a hyporeflexie obě v 18 %. Komplikací enterálního non-Hodgkinova lymfomu může být enterovezikální píštěl s pneumaturií.
![Přípravky a lékové formy antiretrovirotik [54].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/f62dd9721687af6368b8ab09d42df766.png)
Při pohledu na AIDS je zřejmé, že se toto onemocnění v uropoetickém systému může projevit v celé šíři různých symptomů a klinických jednotek. Pro diagnózu AIDS je důležitá anamnéza rizikového sexuálního chování, poranění infikovanou jehlou, či jiný rizikový kontakt s infikovanou osobou. Klinický průběh byl popsán výše, v laboratorním panelu jsou pouze nespecifické změny: vysoká sedimentace erytrocytů, leukopenie, lymfopenie, mírná anémie a trombocytopenie. Základem diagnostiky AIDS je průkaz protilátek anti-AIDS, který je při pozitivitě následně kontrolován a referován Národní referenční laboratoří pro AIDS Státního zdravotního ústavu. Terapie pak probíhá v centrech pro AIDS. Je založena na antiretrovirální terapii a terapii oportunních infekcí a symptomatické terapii.
Problematiku STD lze shrnout do několika bodů:
- STD jsou onemocnění, která postihují nejčastěji věkovou skupinu kolem 20 let a skupiny lidí s rizikovým sexuálním chováním.
- STD probíhají často synchronně, tedy u jednoho pacienta je přítomno více infekcí.
- Při užití antibiotik je nutná dokonalá diagnostika všech agens a jejich specifická terapie s následnými kontrolami pro riziko recidiv.
- K zamezení dalšího šíření diagnostikovaného onemocnění je nutná depistáž sexuálních partnerů a hlášení epidemiologických dat.
- Důležitá je primární prevence, informovanost, poučení populace o možnostech bariérové ochrany a sexuální hygieny.
MUDr. Roman Staněk
Urologické oddělení, Slezská nemocnice Opava
Sources
1. Toriová V. Mykoplazmatické a chlamydiové respirační infekce ve vztahu k ATB léčbě. Přednáška.
2. CMO's Expert Advisory Group on Chlamyda trachomatis in UK, 2004.
3. Chlamydia screening among sexually active young female enrolles of health plans - United States, 1999-2001 MWR. Morb Mortal Wkly Rep 2004; 53(42): 983-985.
4. Westrom L. Incidence, prevalence, and trend of acute pelvic inflammatory disease and its consequences in industrialized Countries. Am J Obstet Gynecol 1980; 138 : 880-892.
5. California Chlamydia Action Coalition. Chlamydia Screening and Treatment Practice Guidelines 2002.
6. Grella M. Chlamydial infections. eMedicine Journal 2001; 2(10).
7. Arzouni JP, Bouilloux JP, de Mouy D, Bicart-See A, Charbit C, Doeschler T, Fleutiaux S, Galinier JL, Gontier P, Lacharme H, Larribet G, Berges JL, Lepargneur JP, Armengaud A. Genital infections in women, in community practice. Comparison of two studies, 1987 and 2002. Med Mal Infect 2004; 34(2): 92-96.
8. Lambiase MC, Vaughan TK. eMedicine Journal 2002; 3(1).
9. Owen MK, Clenney TL. Management of vaginitis. Am Fam Physician 2004;70(11): 2125-2132.
10. Pirotta M, Gunn J, Chondros P et al. Effect of lactobacillus in preventing post-antibiotic vulvovaginal candidiasis: a randomised controlled trial. BMJ 2004; 329 : 548-551.
11. Hlášená onemocnění pohlavními nemocemi v ČR v roce 2000, aktuální informace č. 38/2001, ÚZIS ČR.
12. Hlášená onemocnění pohlavními nemocemi v ČR v roce 1999, aktuální informace č. 22/2000, ÚZIS ČR.
14. Resl V. Doporučené postupy pro praktické lékaře, grant a/004/233, Sexuálně přenosné nemoci II, 2002.
15. Byron EB. STDs, Progress! International Congress of Sexually Transmitted Infections: 2nd Joint Meeting of the International Society for Sexually Transmitted Diseases Research (ISSTDR) and the International Union against Sexually Transmitted Infections (IUSTI) June 24-27, 2000, Berlin.
16. Diaz-Mitoma F, Sibbald G, Shafran SD, Boon R, Saltzman RL. Oral Famciclovir for the Suppression of Recurrent Genital HerpesTrial: A Randomized Controlled for the Collaborative Famciclovir Genital Herpes Research Group. JAMA 1998; 280 : 887-892.
17. Franco EL, Duarte-Franco E, Ferenczy A. Cervical cancer: epidemiology, prevention and the role of human papillomavirus infection Review. CMAJ 2001; 164(7); 1017-1025.
18. Brett C. Mellinger, Human Papillomavirus in the Male: An Overview, AUA Lesson 13 Volume 8, 1994.
19. Koutsky L. Epidemiology of genital human papillomavirus infection. Am J Med 1997; 102 : 3-8.
20. Franco EL, Villa LL, Richardson H, Rohan T, Ferenczy A. Epidemiology of cervical human papillomavirus infection. In: Franco EL, Monsonégo J (eds). New developments in cervical cancer screening and prevention. Oxford: Blackwell Science 1997 : 14-22.
21. National Institutes of Health Consensus Conference on Cervical Cancer. Bethesda, Maryland, April 1-3, 1996. J Natl Cancer Inst Monogr 1996; 21 : 1-148.
22. Munoz N, Bosch FX. The causal link between HPV and cervical cancer and its implications for prevention of cervical cancer. Bull Pan Am Health Organ 1996; 30 : 362-377.
23. Schiffman MH, Bauer HM, Hoover RN, Glass AG, Cadell DM, Rush BB et al. Epidemiologic evidence showing that human papillomavirus infection causes most cervical intraepithelial neoplasia. J Natl Cancer Inst 1993; 85 : 958-964.
24. Dupin N. Genital warts. Clin Dermatol 2004; 22(6): 481-486.
25. IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. Human papillomaviruses. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. Lyon: International Agency for Research on Cancer, World Health Organization 1995; 64. vol.
26. Shepherd J, Weston R, Peersman G, Napuli IZ. Interventions for encouraging sexual lifestyles and behaviours intended to prevent cervical cancer (Cochrane Review). In: The Cochrane Library. Oxford: Update software 2000; 1. vol.
27. Ramirez JE, Ramos DM, Clayton L, Kanowitz S, Moscicki AB. Genital human papillomavirus infections: knowledge, perception of risk, and actual risk in a nonclinic population of young women. J Womens Health 1997; 6 : 113-121.
28. Franco EL, Syrjänen K, De Wolf C, Patnick J, Ferenczy A, McGoogan E et al. Meeting report: new developments in cervical cancer screening and prevention. Cancer Epidemiol Biomarkers Prev 1996; 5 : 853-856.
29. Cardamakis E, Relakis K, Ginopoulos P, Korantzis A, Metalinos K, Stathopoulos E, Papathanasiou Z, Michopoulos J, Mantouvalos H, Kotoulas IG, Tzingounis V. Treatment of penile intraepithelial neoplasia (PIN) with interferon alpha-2a, CO2 laser (vaporization) and 5-fluorouracil 5% (5-FU). Eur J Gynaecol Oncol. 1997; 18(5): 410-413.
30. Harper DM, Franco EL, Wheeler C, Ferris DG, Jenkins D, Schuind A, Zahaf T, Innis B, Naud P, De Carvalho NS, Roteli-Martins CM, Teixeira J, Blatter MM, Korn AP, Quint W, Dubin G. GlaxoSmithKline HPV Vaccine Study Group.Efficacy of a bivalent L1 virus-like particle vaccine in prevention of infection with human papillomavirus types 16 and 18 in young women: a randomised controlled trial. Lancet 2004; 364(9447):1757-1765.
31. Garnett GP. Role of Herd Immunity in Determining the Effect of Vaccines against Sexually Transmitted, Disease. J Infect Dis 2005; 191(Suppl 1): S97-S106.
32. Taira AV. Evaluating human papillomavirus vaccination programs. Emerg Infect Dis 2004; 10(11): 1915-1923.
33. http://hivinsite.ucsf.edu
34. Treat 3 by 5: Scaling up antiretroviral therapy in ressource limited settings: treatment guidelaines for a public health approach, 2003 revision of World Health Organization, Geneve 2004.
35. Hlášená onemocnění pohlavními nemocemi v ČR v roce 2000, aktuální informace 38/2001 ÚZIS.
36. Frassetto L, Schoenfeld PY, Humphreys MI. Increasing incidence of human immunodeficiency viruse associated nephropathy at San Francisco General Hospital. Amer J Kidney Dis 1991; 18 : 655-659.
37. Vitting KE, Gardenswartz MI-I, Zabetakis PM et al. Frequency of hyponatremia and nonosmolar vasopressin release in the acquired immunodeficiency syndrome. JAMA 1990; 263 : 973-978.
38. Guerra I, Kimmel PL. Hypokalemic adrenal crisis in a patient with AIDS. South Med J 1991; 84 : 1265-1267.
39. Comiter S, Glasser J, Al-Askari S. Ureteral obstruction in a patient with Burkitt's lymphoma and AIDS. Urology 1992; 39 : 277-280.
40. Mohler JL, Jarow JP, Marshall FF. Unusual urological presentations of acquired immune dificiency syndrome: Large cell lymphoma. J Urol 1987; 138 : 627-629.
41. Zaleski C, Burke G, Nery J et al. Risk of AIDS (HIV) transmission in 581 renal transplants. Transplant Proc 1993; 25 : 1483-1484.
42. Leport C, Rousseau F, Perronne C et al. Bacterial prostatitis in patiens infected with the human immunodeficiency virus. J Ural 1989; 141 : 334-336.
43. Zighelboim J, Goldfarb RA, Mody D et al. Prostatic abscess due to Histoplasma Capsulatum in a patient with the acquired immunodeficiency syndrome. I Ural 1992; 1473 : 166-168.
44. Adams JR, Mata JA, Culkin DJ et al. Acquired immunodeficiency syndrome manifesting as prostatic nodule secondary to cryptococcal infection. Urology 1992; 39 : 289-291.
45. Mamo GJ, River MA, Jacobs SC. Cryptococcal prostatic abscess associated with the acquired immunodeficiency syndrome. J Ural 1992; 148 : 889-890.
46. Lowe FC, LattimerDG, Metroka CE. Kaposi´s sarcina of the penis in patiens with AIDS. J Urology 1989; 142 : 1475-1477.
47. Vapnem JM, Quivey JM, Carroll PR. AIDS - related Kaposi´s sarcoma of the male genitalia: management with radiation therapy. J Urol 1991; 1145 : 333-336.
48. Safai B, Schwartz JJ. Kaposi's sarcoma and the acquired immunodeficiency syndrome. In Devita VT Jr, Hellman S, and Rosenberg SA (eds). AIDS: Etiology, Diagnosis, Treatment and Prevention. 3rd ed Philadelphia: JB Lippincott 1992 : 209-223.
49. Kwan DJ, Lowe FC. Acquired immunodeficiency syndrome A venereal disease. Ural Clin North Am 1992; 19 : 13-24.
50. Leibovitch I, Goldwasser B. The spectrum of acquired immune deficienty syndrome-associated testicular disorders. Urology 1994; 443 : 818-824.
51. Wilson TW, Frenkel E, Vuitch F et al. Testicular tumors in men with human immunodeficiency virus. I Urol 1992; 147 : 1038-1040.
52. Lopez AE, Latiff AG, Ciancio G et al. Lymphoma of urethra in patient with acquired immune deficiency syndrome. Urology 1993; 42 : 596-598.
53. Snider WD, Simpson DM, Nielsen S et al. Neurological complications of acquired immunodeficiency syndrome: analysis of 50 patients. Ann Neural 1983; 14 : 403-418.
54. Staňková M, Rozsypal H. Doporučené postupy pro praktické lékaře. Reg. č.o/020/249, HIV infekce, 2002.
Labels
Paediatric urologist UrologyArticle was published in
Urological Journal

2005 Issue 2
-
All articles in this issue
- NEKOMPLIKOVANÉ UROINFEKCE: CO JE NOVÉHO A CO SE ZMĚNILO
- KOMPLIKOVANÉ UROINFEKCE: CO JE NOVÉHO A CO SE ZMĚNILO
- INFEKCIE MOČOVÝCH CIEST U DETÍ A V TEHOTENSTVE
- MYKOTICKÉ INFEKCE
- UROGENITÁLNÍ TUBERKULÓZA NA POČÁTKU 3. TISÍCILETÍ
- SEXUÁLNĚ PŘENOSNÁ ONEMOCNĚNÍ Z POHLEDU UROLOGA
- CHRONICKÉ PÁNEVNÍ BOLESTI
- SEPTICKÝ ŠOK U UROINFEKCÍ
- PRINCIPY ANTIMIKROBIÁLNÍ LÉČBY U UROINFEKCÍ
- Urological Journal
- Journal archive
- Current issue
- About the journal
Most read in this issue
- MYKOTICKÉ INFEKCE
- INFEKCIE MOČOVÝCH CIEST U DETÍ A V TEHOTENSTVE
- SEPTICKÝ ŠOK U UROINFEKCÍ
- NEKOMPLIKOVANÉ UROINFEKCE: CO JE NOVÉHO A CO SE ZMĚNILO
