Chronické pánevní bolesti a sexuální funkce pohledem urologa a anatoma
CHRONIC PELVIC PAIN AND SEXUAL FUNCTIONS AS SEEN BY UROLOGIST AND ANATOMIST
The treatment of pelvic pains is a complex issue due to low success rate in determining their pathophysiological causes. These difficulties are most often classified as interstitial cystitis (IC) or chronic prostatitis (CP). In addition to painful symptoms in pelvic organs, also present are functional difficulties enhanced by psychological strain which eventually assumes a dominant role as a consequence of prolonged and not always efficient therapy. Sexual functions of men irrespective of age can be easily affected. The combination of chronic pain and psychical alteration is a nurturing ground for sexual dysfunction in general. Based on a joint urologist and anatomist view and detailed insight into the nervous supply of the pelvic organ area, the authors have tried to identify the hypothetical links explaining the causes of sexual dysfunction in men.
Key words:
chronic pelvic pain, chronic prostatitis, sexual dysfunction, nervus pudendus
:
doc. MUDr. Michael Urban 1,2; MUDr. Jiří Heráček 1,2; MUDr. Václav Báča 3
:
Urologická klinika 3. LF UK a FN Královské Vinohrady Šrobárova 50, 0 4 Praha
urbanm@fnkv. cz
1; Androgeos - soukromé urologické a andrologické centrum, Centrum pro léčbu chronické pánevní bolesti, Praha
2; Anatomický ústav 3. LF UK, Centrum pro integrované studium pánve, Praha
3
:
Urol List 2007; 5(2): 28-37
Léčba pánevních bolestí je problém komplikovaný vzhledem k málo úspěšnému určování jejich patofyziologických příčin. Potíže se nejčastěji označují jako intersticiální cystitis (IC) či chronická prostatitis (CP). Kromě bolestivých příznaků v orgánech pánve jde o postižení funkčního charakteru umocněné psychickou složkou, která s protrahovaným průběhem a ne vždy efektní terapií získává určitou dominanci. Oblast, která je snadno zranitelná, jsou sexuální funkce u muže bez rozdílu věku. Kombinace chronické bolesti s psychickou alterací je dobrou živnou půdou pro sexuální dysfunkci obecně. Společným pohledem urologa a anatoma a detailním dešifrováním nervového zásobení oblasti pánevních orgánů se pokusíme najít hypotetické souvislosti objasňující původ sexuální dysfunkce u muže.
Klíčová slova:
chronická pánevní bolest, chronická prostatitis, sexuální dysfunkce, nervus pudendus
DEFINICE CHRONICKÝCH PÁNEVNÍCH BOLESTÍ (CPP) A TERMINOLOGIE
Chronické pánevní bolesti
Chronické pánevní bolesti jsou nemaligní bolesti pociované ve strukturách spojených s pánví u mužů i žen. V případě dokumentovaných nociceptivních bolestí, které přecházejí v chronické, musí být bolesti trvalé či opakující se po dobu nejméně 6 měsíců. Pokud jsou zaznamenány neakutní bolestivé mechanizmy, bolesti lze považovat za chronické nezávisle na době jejich trvání. Ve všech případech mohou být spojeny s negativními kognitivními, behaviorálními či sociálními důsledky (nová definice).
Přípony -algie a -dynie se často používají jako prostředek k získání hmatatelné diagnózy pro pacienta, což samo o sobě může znamenat příspěvek k léčbě. V těchto pravidlech jsme však z důvodu jasnosti od těchto termínů upustili. Současné definice odpovídají nejnovějším doporučením pro terminologii určené International Continence Society (ICS) [1] a využívají osovou strukturu klasifikace International Association for the Study of Pain (IASP), tab. 1, [2].
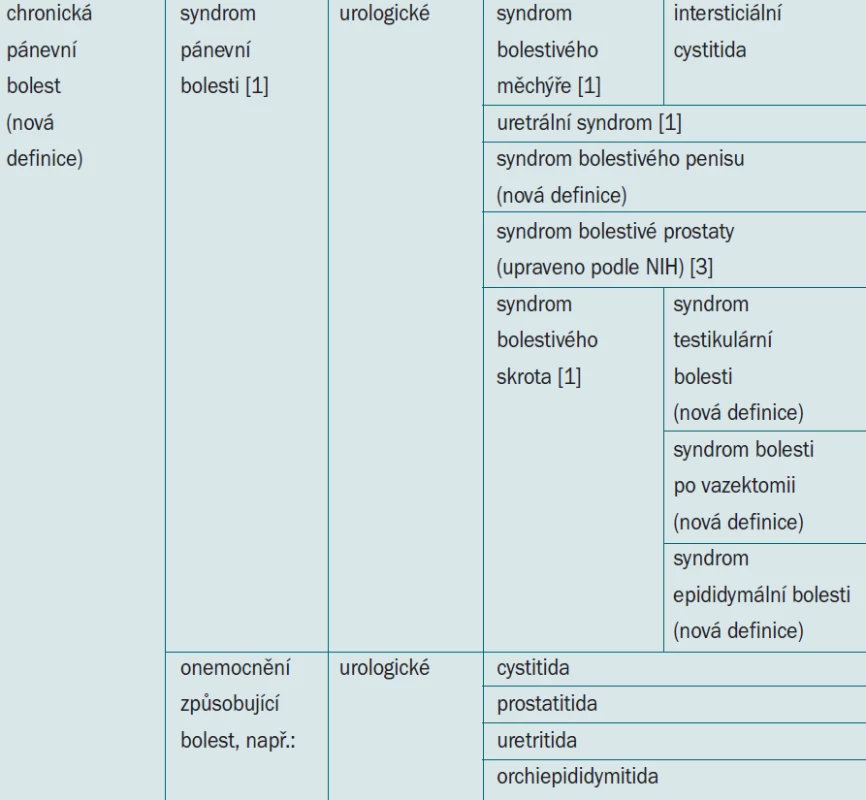
Syndrom pánevních bolestí (CPPS) je výskyt přetrvávajících či opakujících se epizod pánevních bolestí spojených se symptomy, které naznačují špatnou funkci dolních cest močových, problémy sexuální, střevní či gynekologické. Není prokázána žádná infekce nebo jiná zřejmá patologie (převzato z ICS 2002) [1].
Syndrom bolestí močového měchýře jsou suprapubické bolesti související s plněním močového měchýře a spojené s dalšími symptomy jako jsou zvýšená frekvence denního a nočního močení, bez prokázané infekce močových cest či jiné zřejmé patologie (ICS 2002) [1].
Syndrom bolestí močové trubice je výskyt opakujících se epizod bolestí močové trubice, obvykle při močení, při zvýšené denní frekvenci a nykturii, bez prokázané infekce či jiné zřejmé patologie (ICS 2002) [1].
Syndrom bolestí penisu je výskyt bolestí penisu, které nejsou primárně spojeny s močovou trubicí, bez prokázané infekce či jiné zřejmé patologie (nová definice).
Syndrom bolestí prostaty je výskyt přetrvávajících či opakujících se epizod bolestí spojených se symptomy, které signalizují špatnou funkci močového ústrojí a/nebo sexuální problémy. Není prokázána žádná infekce či jiná zřejmá patologie (nová definice). Definice syndromu bolestí prostaty byla převzata z dohodnuté definice a klasifikace prostatitis Národního ústavu zdraví (National Institutes of Health - NIH) [3] a zahrnuje stavy, které jsou označovány jako syndrom chronických pánevních bolestí. Podle klasifikačního systému lze syndrom bolestí prostaty dále rozdělit na typ A – zánětlivý a B – nezánětlivý (tab. 2).

Syndrom bolestí šourku je výskyt přetrvávajících či opakujících se epizod bolestí spojených se symptomy naznačujícími špatnou funkci močového ústrojí či sexuální problémy. Není prokázána epididymoorchitis nebo jiná zřejmá patologie (ICS 2002) [1].
Syndrom bolestí varlat je výskyt přetrvávajících či opakujících se epizod bolestí lokalizovaných při vyšetření ve varlatech a spojených se symptomy naznačujícími špatnou funkci močového ústrojí či pohlavní problémy. Není prokázána epididymoorchitis či jiná zřejmá patologie (nová a specifičtější definice než syndrom bolestí šourku - obr. 1).
Syndrom bolestí nadvarlat je výskyt přetrvávajících či opakujících se epizod bolestí lokalizovaných při vyšetření v nadvarlatech a spojených se symptomy naznačujícími špatnou funkci močového ústrojí či sexuální problémy. Není prokázána epididymoorchitis či jiná zřejmá patologie (nová a specifičtější definice než syndrom bolestí šourku obr. 1).
Syndrom bolestí po vazektomii je syndrom bolestí šourku, které následují po vazektomii (nová definice).
Syndrom bolestí spojených s endometriem jsou chronické či opakující se pánevní bolesti - je přítomna endometriosis, avšak plně nevysvětluje všechny symptomy (nová definice).
Syndrom bolestí pochvy je výskyt přetrvávajících nebo opakujících se epizod bolestí spojených se symptomy naznačujícími špatnou funkci močového ústrojí nebo pohlavní problémy. Není prokázána infekce pochvy ani jiná zřejmá patologie (ICS 2002).
Syndrom bolestí vulvy je výskyt přetrvávajících či opakujících se epizod bolestí vulvy spojených buï s mikčním cyklem či se symptomy naznačujícími špatnou funkci močového ústrojí či pohlavní problémy. Není prokázána žádná infekce či jiná zřejmá patologie (ICS 2002) [1].
Symptom generalizovaných bolestí vulvy (formálně dysestetická vulvodynie) označuje pálení či bolesti vulvy, jež nelze spolehlivě a přesně lokalizovat mapováním bodovým tlakem pomocí aplikátoru s vatovým koncem či podobným nástrojem. Může být postižena poševní předsíň, ale obtíže nejsou omezeny pouze na tuto oblast. Klinicky se mohou bolesti vyskytovat s provokací i bez ní - dotek, tlak nebo tření (International Society for the Study of Vulvovaginal Disease (ISSVD 1999).
Syndrom lokalizovaných bolestí vulvy označuje bolesti, jež nelze spolehlivě a přesně lokalizovat mapováním bodovým tlakem na jednu či více částí vulvy. Klinicky se bolest vyskytuje jako výsledek provokace - dotek, tlak či tření (ISSVD 1999).
Syndrom vestibulárních bolestí (dříve vulvární vestibulitida) označuje bolesti, které mohou být lokalizovány mapováním bodovým tlakem v jedné či více částech předsíně pochvy.
Syndrom bolestí klitorisu označuje bolesti, které mohou být lokalizovány mapováním bodovým tlakem v klitorisu.
Proctalgia fugax označuje silné a krátké epizody bolestí, které jakoby vycházely z konečníku a které vznikají v nepravidelných intervalech (IASP 1994) [2].
Syndrom anorektálních bolestí je výskyt přetrvávajících či opakujících se epizod bolestí konečníku, které jsou spojeny s určitými spouštěcími oblastmi konečníku/citlivostí a související se symptomy špatné funkce střev. Není prokázána žádná infekce nebo jiná zřejmá patologie (nová definice).
Anizmus je výskyt análních bolestí souvisejících s procesem defekace, které vznikají tím, že příčně pruhované svalstvo pánevního dna není schopno se uvolnit, včetně zevního análního svěrače (nová definice).
Syndrom pudendálních bolestí jsou bolesti neuropatického typu, které vznikají v oblasti inervace pudendálního nervu a příznaky špatné funkce konečníku, močového ústrojí nebo sexuálních problémů. Není prokázána žádná zřejmá patologie.
Syndrom perineálních bolestí je výskyt přetrvávajících či opakujících se epizod perineálních bolestí, které souvisejí buï s mikčním cyklem, nebo jsou spojeny se symptomy naznačujícími špatnou funkci močového ústrojí nebo sexuální problémy. Není prokázána žádná infekce či jiná zřejmá patologie (ICS 2002) [1].
Syndrom bolestí svalstva pánevního dna je výskyt přetrvávajících či opakujících se epizod bolestí pánevního dna spojených se spouštěcími body, které souvisejí buï s mikčním cyklem nebo se symptomy naznačujícími špatnou funkci močového ústrojí nebo sexuální problémy. Není prokázána žádná infekce či jiná zřejmá patologie (nová definice), obr. 2, 3.
V současnosti neexistuje ideální klasifikace stavů, které lze považovat za syndromy chronických bolestí. Výše uvedené rozdělení je založeno na klasifikaci IASP [2]. Většina terminologie vychází z klasifikace chronických bolestí ICS [1] se vstupy z ISSVD a speciální zájmové skupiny IASP, z Bolestí urogenitálního původu (PUGO) a Mezinárodní sítě specialistů pro bolest (SPIN). Hlavní rozpory v této oblasti se týkají toho, že bolesti mohou zahrnovat mnoho zdrojů, etiologií a mechanizmů.
člověk využívající výše uvedenou klasifikaci by měl začít vlevo v tabulce a postupovat doprava pouze tehdy, pokud je schopen skutečně a spolehlivě potvrdit patologii odpovídajícího systému a orgánu. V mnoha případech se může dostat pouze k označení stavu jako syndromu pánevních bolestí. Např. v mnoha případech, kdy byla v minulosti porucha pacientů označena jako prostatodynie, není možné kategoricky stanovit, že bolest vychází z prostaty a nikoliv z jiných zdrojů jako jsou např. svaly pánevního dna. Intersticiální cystitis (IC) lze dobře definovat. Mnoho pacientů, u kterých byly obtíže dříve označovány jako IC, však neodpovídá výzkumným kritériím, a v důsledku toho je musíme označit jako pacienty se syndromem bolesti močového měchýře.
Termín syndrom bolestí se používá tehdy, pokud lze dobře definovat primární patologii s 1 počátečním zdrojem. Pokud však stav pokračuje, jeho obraz se může komplikovat a zahrnovat více zdrojů a mechanizmů. Stav se pak stává syndromem – komplexem symptomů a příznaků. Osová klasifikace IASP se rozšiřuje nad a pod systém použitý zde a zahrnuje časové a etiologické charakteristiky a charakteristiky intenzity. Tyto parametry by také měly být zaznamenány pro kontrolu pacientů a výzkum. Podle požadavku ISSVD by mělo být zaznamenáno, zda bolesti vznikají provokací či nikoliv. Tento systém klasifikace by měl spojit zkušenosti specializovaných skupin. Ale bude třeba jej během několika příštích let výrazně upravit.
CHRONICKÁ PROSTATITIS
Úvod
Prostatitis představuje nejasnou a špatně pochopenou chorobu, vzhledem k tomu, že její výzkum komplikuje omezený fyzický přístup ke žláze. Žádná jistota o její etiologii, nedostatek odlišujících klinických charakteristik a nejednotná diagnostická kritéria spolu se zdlouhavým průběhem léčby způsobují, že uspokojivé vysvětlení této choroby je daleko před námi. U cca 5–10 % případů je u klinické prostatitis prokázána bakteriální etiologie. Tam, kde laboratorní metody u zbylých 90 % případů neprokázaly, že je způsobena bakteriemi, je choroba klasifikována jako chronická nebakteriální prostatitis či prostatodynie [4,5,6]. Fakt, že její symptomy nutně neukazují na izolovanou chorobu prostaty, vedl k jejímu přejmenování na chronickou prostatitis spojenou se syndromem chronických pánevních bolestí (CPPS), což je nový termín používaný u pacientů se symptomatickou prostatitis nebakteriálního původu (tab. 2) [7]. Pro větší jasnost a srozumitelnost bude v tomto pojednání používána starší terminologie.
Definice
Chronická prostatitis spojená se syndromem chronických pánevních bolestí je definována jako potíže či bolesti v pánevní oblasti se sterilními kulturami vzorků a nevýznamnými počty bílých krvinek ve vzorcích specifických pro prostatu, zejména v semeni, vyloučených sekrecích prostaty (EPS) a moči odebrané po masáži prostaty (VB) [7] (tab. 2). Podle nové klasifikace Národního ústavu pro diabetes a choroby trávení a ledvin (NIDDK) je chronická prostatitis spojená se syndromem chronických pánevních bolestí definována jako kategorie IIIB [8] (tab. 2).
Patogeneze
Etiologie a patofyziologie chronické prostatitis zůstává záhadou. Akutní bakteriální prostatitis je jiný chorobný proces než syndromy chronické prostatitis. Jak tomu často bývá u syndromu chronických pánevních bolestí, i zde převládají hypotézy nepodložené podstatnými důkazy.
Pacienti se syndromem chronických pánevních bolestí nevykazují žádné projevy zánětu. Netrpí uretritis, urogenitální rakovinou, zúžením uretry či neurologickou chorobou postihující močový měchýř. Skutečně nevykazují zřejmé onemocnění ledvinového ústrojí [7].
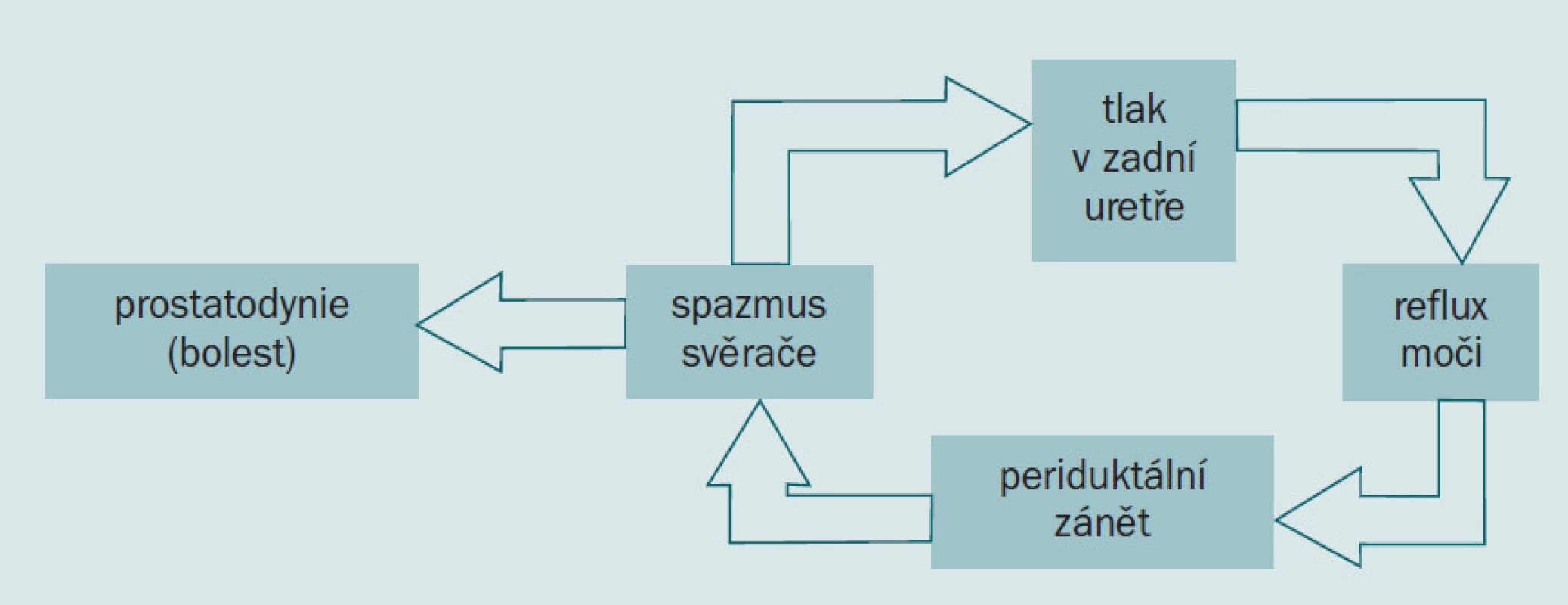
K popisu etiologie chronické prostatitis bylo navrženo několik hypotéz. Někdo tvrdí, že bolesti a následné symptomy podrážděného a ztíženého močení mohou být vyvolány obstrukcí dolních cest močových v souvislosti s problémy hrdla močového měchýře, špatnou funkcí svěrače nebo detruzoru, zúžením močové trubice či poruchou močení ve smyslu obstrukce [9,10,11]. Jiní popsali, že reflux moči do ductus deferens uvnitř prostaty byl způsoben vysokým tlakem, turbulentním močením v kombinaci s anatomickou abnormalitou (obr. 1) [12,13].
Mikrobiologická etiologie je považována za rozumný předpoklad. U některých komenzálů dolních cest močových, kteří byli považování za neškodné, bude možná zjištěno, že jsou patogeničtí. Citlivější izolační metody možná odhalí zatím nezachycené původce infekcí [7].
Někteří autoři označují za původce nebakteriální prostatitis imunologické procesy, precipitaci nerozpoznaným antigenem či autoimunitní proces [14,15]. Reflux moči do vývodu ductus deferens v prostatické části močové trubice by mohl stimulovat sterilní zánětlivou odpověï [13].
Také nervosvalová etiologie našla názorovou podporu [16,17]. Tyto symptomy mohou představovat typ reflexivní sympatické dystrofie perinea a pánevního dna.
Symptomatologie a její inervace
Subjektivní stížnosti při chronické, ale i akutní prostatitidě a bolestech pánevního dna. U akutní formy jsou výraznější.
Gastroenetrologická:
- bolesti v oblasti vesica fellea - senzitivní kořenová oblast Th7-Th9
- bolesti v gastrické oblasti - senzitivní kořenová oblast Th 6-Th10
- poruchy peristaltiky, nadýmání, zácpa - pro tlusté střevo senzitivní kořenové oblasti Th11-L1
V řadě případů byl operován žlučník, appendix nebo žaludek bez zlepšení a s minimálním patologickým nálezem nebo spíše negativním nálezem na preparátu. Operace byla indikována spíše z rozpaků diagnostických.
Urologická:
- bolesti vyzařují do bederních krajin buï oboustranně, nebo také pouze jednostranně. Jsou popisovány příznaky zánětu sedacího nervu při prostatitidách, což se uvádí jako typický příklad významu znalostí útrobních kořenových okrsků (areae radiculares viscerales).
- bolesti nad sponou stydkou
- bolesti v tříslech s vyzařováním do podbřišku rovněž jedno nebo oboustranně inervační oblast n. ilioinguinalis a r. genitalis n. genitofemoralis na povrchové inervaci – v hluboké jsou to autonomní vlákna z plexus deferentialis podél průběhu funiculus spermaticus tříselným kanálem (stejně jako orgánové dráždění)
- bolesti vystřelující do varlat buï jednostranně, nebo oboustranně – vzhledem k senzitivním vláknům varlat jdoucím do segmentů Th10-Th11 může jít také o přenesené dráždění oblasti žaludku, jícnu, dvanáctníku. Může jít však i o reakci na změny a dráždění funkční.
- různé tlaky, pálení, šimrání, nepříjemný pocit v trubici močové bez pozitivního mikrobiologického nálezu
- bolest při kořeni penisu s vyzařováním do celého penisu, poruchy ejakulace, snížení libida, zhoršení erekce, změna citlivosti penisu až přecitlivělost s bolestí dotyku s prádlem atd. Původ této symptomatologie je pravděpodobný z iritace nervus pudendus.
- tlak nebo bolest na hrázi s iradiací do vnitřních ploch stehen nebo jen na hrázi je v oblasti kořenové inervace L2, L3, S2 a můžeme usuzovat i na iradiační bolesti ze senzitivní inervační oblasti n. pudendus na penisu (S2-S4) nebo jeho dráždění v průběhu
- tlak v konečníku může být symptomem dráždění rr. rectales inferiores, které jako větve n. pudendus probíhají transverzálně skrze fossa ischiorectalisi
Vzhledem k senzitivní kořenové oblasti varlat (Th10-11), prostaty (Th11-L1), močového měchýře a penisu (Th12-L2) a inervační oblasti n. pudendus (S2-S4) můžeme při komplexním pohledu vidět souvislost a možnosti iradiace symptomů při onemocnění organických či funkčních močopohlavního ústrojí s dalšími orgánovými systémy.
Sexuální odpověï může být rozdělena do 4 stadií - vzrušení, plateau, orgazmus a remise (obr. 4).
![Schéma sexuální odpovědi u muže [47] .](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/709d3f1d43e4a0c03fe01a9567f7b660.jpg)
Vzrušení – taktilní či vizuální podněty nebo psychické stimuly vedou k ohromnému množství aferentních impulzů do CNS. Eferentní vlákna odsud vedou míchou impulzy k parasympatickému výstupu na úrovni segmentů S2-S4 (nn. splanchnici pelvici), kde je sídlo sexuálních reflexů [18-20]. Pregangliová vlákna vstupují do plexus hypogastricus inferior, kde jsou synapticky přepojena na vlákna postgangliová. Tyto postgangliové neurony procházející přes plexus prostaticus se připojují k arteria pudenda interna a probíhají s jejími větvemi až do úrovně arteriol do topořivých těles penisu. Klinicky důležitý je průběh těchto vláken podél prostaty, které popsal Walsh [22]. V dalších pracích např. Lue et al nacházíme detailní popis průběhu tohoto neurovaskulárního svazku tak, že dorzálně se nachází po stranách prostaty na hodinovém ciferníku v pozici 5 a 7, ventrálněji se poté přesouvá do pozice 3 a 9, aby se přiložil k močové trubici v pozicích 11 a 1. Na toto uložení je třeba dbát při operacích prostaty pro zachování erektilních funkcí [23].
Za normálních okolností udržuje sympatikus stálý tonus hladké svaloviny arteriol, což umožňuje stálý průtok krve orgánem. Při sexuální stimulaci, která nemusí být vědomá, ale může být reflexní, dojde k vazodilataci arteriol a zvýšení krevního proudu do prostorů kavernózních těles. Přeplněné sinusy tlačí vény proti tunica albuginea, čímž společně s kontrakcí m. bulbospongiosus a ischiocavernosus, dochází ke snížení odtoku krve, a tím ke zvětšování objemu a obvodu penisu včetně jeho napřimování. Kromě erekce dochází k sekreční činnosti bulbouretrálních a uretrálních žláz, což je odpověï na sekreční parasympatickou stimulaci. činnost žláz je důležitá pro lubrikaci uretry. Z uvedeného vyplývá, že pro 1. stadium sexuální odpovědi včetně erekce je nejdůležitější parasympatické centrum v míšních segmentech S2-S4. Ovšem v případě úrazů s přerušením míchy mohou ale tuto funkci převzít sympatická centra Th1-L2 [19,21].
Plateau – k udržování sexuálního vzrušení je nezbytná kontinuální senzitivní stimulace, přicházející z glans penis a kůže penisu do míchy konečnými větvemi nervus pudendus (nn. dorsales penis). Rytmické pohyby podporují kontinuální přenos impulzů do centrálního nervového systému.
Orgazmus – na rozdíl od erekce se na této fází podílí převážně sympatická inervace pohlavního systému. U mužského pohlaví ji můžeme rozdělit do 2 stadií:
1. EMISE - transport spermií z epididymis do dustus ejaculatorius a uretry a sekrece žláz k vytvoření ejakulátu. Tření na glans penis společně s ostatními aferentními impulzy zvyšují sexuální tenzi a vedou k vybití sympatickými vlákny segmentů L1-L2 inervujícími hladké svalstvo vývodných cest (epididymis, ductus deferens, vesiculae seminales, ductus ejaculatorius a prostatu). Kontrakcí této hladké svaloviny jsou spermie se sekretem žláz vypuzeny do prostatické části uretry. Sekret bulbouretrálních a uretrálních žláz se přidává těsně před ejakulací v proximální části spongiózní uretry k vytvoření definitivního ejakulátu. Informace o hromadění ejakulátu je opět senzitivní inervací skrze větve nervus pudendus vedena do míchy a spolupodílí se na koordinaci motorické a autonomní odpovědi.
2. EJAKULACE - neprodleně následuje emise spermií a stává se pohonem k evakuaci ejakulátu ven z uretry při orgazmu. Ejakulát je poháněn rázným stahem hladké svaloviny uretry a perineálních svalů (m. bulbospongiosus, ischiocavernosus). Hladká svalovina uretry je inervována parasympaticky ze segmentů S2-S4, kdežto svalovina perinea je inervována motorickými větvemi n. pudendus. Během ejakulace dochází ve shodě s převahou sympatiku ke kontrakci m. sphincter urethrae internus v hrdle měchýře, který znemožňuje průnik spermatu do močového měchýře a zároveň znemožňuje průnik moči do uretry.
Remise – po ejakulaci či ukončení sexuální stimulace způsobí sympatická inervace arteriol v kavernózních tělesech kontrakci, a tím se omezí krevní přítok. V návaznosti na to klesne tlak, uvolní se stěny venul, čímž se normalizuje krevní odtok a penis ochabne. Po ejakulaci nastává latentní perioda, než se vegetativní centra opět připraví na novou sexuální odpověď.
Diagnóza
Navzdory tomu, co naznačuje název, je chronická prostatitis symptomatickou diagnózou. Může být diagnostikována na základě 3měsíčního trvání genitourinárních bolestí a absence dalších patologií dolních cest močových popsaných výše. Závažnost této choroby, jejího průběhu a odpovědi na léčbu můžeme určit pouze ověřeným postupem hodnocení symptomů [24,25]. Kromě toho může být užitečné zhodnocení kvality života. Bylo zjištěno, že chronická prostatitis zasahuje do kvality života podobně jako akutní infarkt myokardu, nestabilní angina pectoris či Crohnova choroba [26,27]. Spolehlivými a platnými indexy symptomů a kvality života jsou Index symptomů prostatitis NIH (CPSI – tab. 3) a Mezinárodní hodnocení prostatických symptomů (IPSS) [28].

Urodynamické studie ukazují u chronické prostatitis sníženou rychlost průtoku moči, neúplné uvolnění hrdla močového měchýře a prostatické močové trubice a také abnormálně vysoký tlak uzavírání močové trubice v klidovém stavu. Uvolnění zevního svěrače močové trubice při močení je normální [29]. Laboratorní diagnóza je založena na testu 4 skel pro lokalizaci bakterií (zlatý standard). Tento test je však příliš složitý na to, aby jej mohla využívat většina praktických urologů [7]. Mikroskopické nálezy vyloučených sekretů prostaty vykazují množství leukocytů a makrofágů obalených lipidy. Mikroskopií či kultivací však nebyl odhalen žádný organizmus a vzorek měchýře je sterilní. Účinnost diagnostiky lze úsporně zvýšit jednoduchou procedurou (test 2 skel) [30].
Příznaky spojené s chronickou prostatitis (tab. 3) a přehled diagnostického hodnocení chronické prostatitis je uveden na obr. 5.
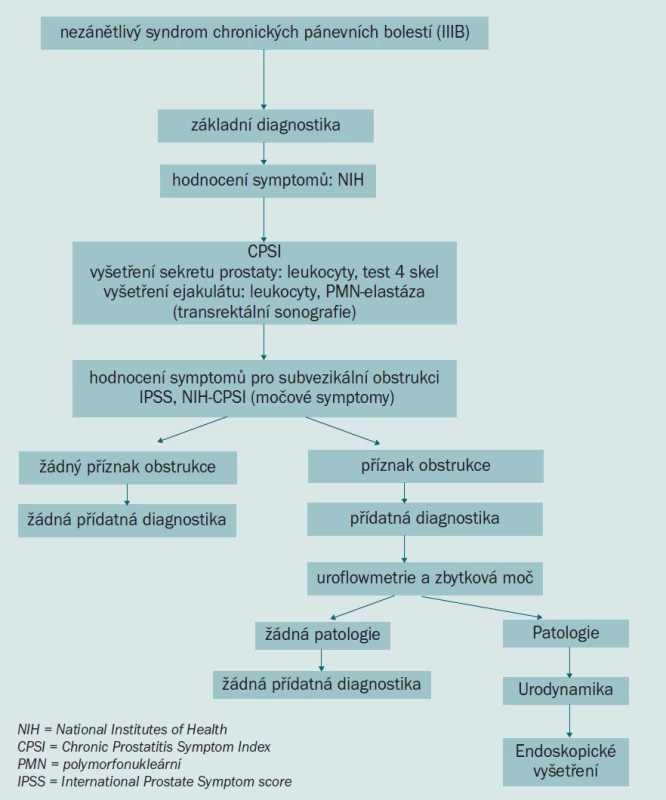
Léčba
Příčina chronické prostatitis (syndrom kategorie IIIB) není známa, takže příčinná léčba představuje problém a mnoho léčebných postupů je založeno pouze na empirii. Vyléčení je často nereálné, takže jedinou cestou ke zlepšení kvality života je zmírnění symptomů [31].
Přehled literatury ukazuje, že symptomy zlepšují blokátory alfa, svalové relaxanty a různé fyzikální terapie [31].
Uvádí se, že svalové relaxanty (diazepam, baklofen) pomáhají tehdy, je-li špatná funkce svěrače či vznikají-li křeče svalů pánevního dna/perinea, ale nebyly provedeny žádné prospektivní klinické testy k potvrzení této teorie.
Omezené studie s blokátory alfa ukazují, že klinické zlepšení je patrné u 48–80 % případů [32,33]. Zlepšený výkon močení blokováním receptorů alfa v hrdle močového měchýře a prostatě může zmírnit některé ze symptomů.
Uvádí se, že tyto symptomy zlepšuje také podpůrná léčba jako např. biofeedback, relaxační cvičení, změna životního stylu (tj. diety, přerušovaná jízda na kole), akupunktura, masážní léčba, chiropraktická léčba či meditace [7,31].
U některých pacientů bylo pozorováno zlepšení při antimikrobiální léčbě [3], doporučuje se proto pokusná léčba antibiotiky [34,40]. Pacienti, kteří reagují na antibiotika, by měli být léčeni 4–6 týdnů nebo dokonce i déle. Pokud po ukončení léčby vznikne recidiva, měla by být znovu zavedena antimikrobiální léčba nízkými dávkami a mělo by se v ní pokračovat, dokud je účinná. Dlouhodobé výsledky s trimetoprim-sulfametoxazolem byly slabé [34]. Výsledky léčby chinolonem, včetně norfloxacinu, ciprofloxacinu a ofloxacinu jsou zřejmě nadějnější [35, 36,37].
U většiny pacientů s prostatitis se podávají analgetika, ale údaje o jejich dlouhodobé účinnosti jsou omezené [31].
U některých pacientů může mít léčba nesteroidními protizánětlivými medikamenty příznivé účinky. Imunitní modulace inhibitory cytokinů či jiné postupy mohou být prospěšné. Před doporučením takové léčby je však třeba provést odpovídající testy [38].
Některé omezené pilotní studie s inhibitory 5alfa-reduktázy nasvědčují tomu, že finasterid by mohl příznivě ovlivňovat močení a bolesti [39,40].
Anticholinergní látky jsou prospěšné při snižování dráždivých symptomů při močení a napomáhají normální sexuální aktivitě [41].
Byly popsány pozitivní účinky fytoterapie [42] a pentosanpolysulfátu (PPS). Tyto možnosti léčby je třeba však prozkoumat v prospektivních studiích, než je bude možno doporučit.
Uvádí se, že léčba teplem, jako např. transrektální hypertermie [43] a transuretrální termoterapie vyvolává u některých pacientů příznivé účinky [44].
Chirurgické zákroky jako např. transuretrální incize hrdla močového měchýře [10], radikální transuretrální resekce prostaty [45] či zejména radikální prostatektomie hrají velmi omezenou roli a vyžadují další specifické indikace [31].
V poslední době se zaznamenávají dobré výsledky po obstřiku oblasti nervus pudendus v oblasti Alcockova kanálu, kde se předpokládá, že dochází k útisku průchodu tohoto nervu, a tím k neuralgickým projevům v oblasti jeho inervace – oblasti perinea, konečníku, skrota, penisu, u ženy labia majora a klitoris (obr. 6–8) [46]. Pokud je náš předpoklad o iritaci n. pudendus v oblasti Alcockova kanálu podobným mechanizmem jako karpální syndrom na ruce pravdivý, lze uvažovat o dekompresi n. pudendus. Dekomprese spočívá v endoskopické mikrochirurgické technice v oblasti fossa ischiorectalis s uvolněním vazivové struktury v Alcockově kanálu (obr. 9).
![Průběh nervus pudendus v pánvi - transverzální pohled [47] .](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/aab83f89014d026cbd5b45765b16756c.jpg)
![Nervus pudendus a Alcockův kanál [47].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/876e36b844dc2019f4f928a2b920cd5d.jpg)
![Průběh nervus pudendus v pánvi - sagitální pohled [47] .](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/0c2bde99412f8f4d8792bafe5f9e4d45.jpg)
![Fossa ischiorectalis a nervus pudendus [47].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/73daaefa7dbb99879da4160bb9bcb85d.jpg)
V indikovaných případech navazujeme na léčbu pánevní bolesti specifickou terapií poruchy erekce. Lékem první volby erektilní dysfunkce jsou inhibitory PDE-5 (sildenafil, tadalafil, vardenafil), které uvolňováním NO v kavernózních tělesech a zvýšenou hladinou cyklického guanosinmonofosfátu (cGMP) způsobují relaxaci hladké svaloviny kavernózních těles a zvyšují tak přítok krve do penisu a vyvolávají erekci. Mechanizmus účinku inhibitorů PDE-5 spočívá v zabránění degradace cGMP, takže dochází k jeho nadbytku a prodloužení proerektilního působení. Léčba je jednoduchá a při dodržení kontraindikací bezpečná. Léčiva neovlivňují libido, průběh ejakulace či orgazmu. Absolutní kontraindikace je léčba nitráty nebo donory NO, jelikož inhibitory PDE-5 potencují jejich vazodilatační, hypotenzivní a antikoagulační účinky. Relativní kontraindikace jsou nestabilní nebo těžká kardiovaskulární onemocnění, zvýšené opatrnosti je třeba u pacientů s poškozením jaterních nebo renálních funkcí a u pacientů nad 65 roků, kde je snížena clearance léku.
Přehled léčebných možností CHPPS je uveden na obr. 10.
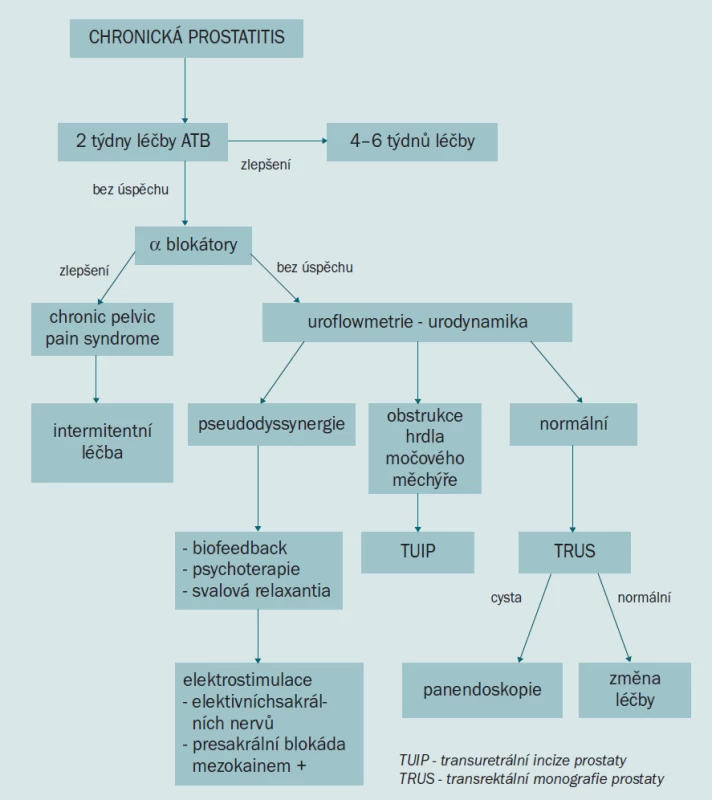
ZÁVĚR
Vzhledem ke všem složitostem diagnostiky příčin a léčby nepatří problematika erektilní dysfunkce jen do péče sexuologů, i když je jim obvykle přenechávána. Problematika je tak složitá, že léčba musí být mezioborová a musejí se na ní podílet specialisté různého zaměření (internisté, GIT, chirurgové, endokrinologové, fyzioterapeuti, psychologové, lázeňští specialisté a sexuologové). Urolog je však jednoznačně koordinujícím článkem a lékařem, který individuálně modeluje léčbu pacientů, protože každý pacient má naprosto specifickou symptomatologii. Při hodnocení společného pohledu urologa a anatoma se souvislost n. pudendus a všech jeho větví se sexuálními dysfunkcemi a CHPPS jeví jako zřejmá. Připravujeme prospektivní studii, jejímž cílem je prokázat souvislost n. pudendus a klinických obtíží pacientů s CHPPS. Principem je ovlivnění klinických obtíží pacientů po uvolnění n. pudendus v případě pozitivní odpovědi na obstřik Alcockova kanálu mezokainem.
doc. MUDr. Michael Urban1,2
MUDr. Jiří Heráček1,2
MUDr. Václav Báča3
1Urologická klinika 3. LF UK a FN Královské Vinohrady Šrobárova 50, 100 34 Praha 10
urbanm@fnkv.cz
2Androgeos - soukromé urologické a andrologické centrum, Centrum pro léčbu chronické pánevní bolesti, Praha
3Anatomický ústav 3. LF UK, Centrum pro integrované studium pánve, Praha
Sources
1. Abrams P, Cardozo L, Fall M et al. The standardisation of terminology of lower urinary tract function: report from the Standardisation Subcommittee of the International Continence Society. Am J Obstet Gynecol 2002; 187 : 116-26.
2. Merskey H, Bogduk N. Classification of Chronic Pain. Descriptions of Chronic Pain Syndromes and Definitions of Pain Terms. Seattle: IASP Press 2002.
3. Krieger JN, Nyberg L Jr, Nickel JC. NIH consensus definition and classification of prostatitis. JAMA 1999; 282 : 236-237.
4. de la Rosette JJ, Hubregtse MR, Meuleman EJ et al. Diagnosis and treatment of 409 patients with prostatitis syndromes. Urology 1993; 41 : 301-307.
5. Meares EM jr. Prostatitis. Med Clin North Am 1991; 75 : 405-24.
6. Brunner H, Weidner W, Schiefer HG. Studies on the role of Ureaplasma urealyticum and Mycoplasma hominis in prostatitis. J Infect Dis 1983; 147 : 807-813.
7. Nickel JC, Weidner W. Chronic prostatitis: Current Concepts and antimicrobial therapy. Infect Urol 2000; 13 : 22.
8. Nickel JC. Prostatitis: myths and realities. Urology 1998; 51 : 362-366.
9. Barbalias GA, Meares EM Jr, Sant GR. Prostatodynia: clinical and urodynamic characteristics. J Urol 1983; 130 : 514-517.
10. Kaplan SA, Te AE, Jacobs BZ. Urodynamic evidence of vesical neck obstruction in men with misdiagnosed chronic nonbacterial prostatitis and the therapeutic role of endoscopic incision of the bladder neck. J Urol 1994; 152 : 2063-2065.
11. Murnaghan GF, Millard RJ. Urodynamic evaluation of bladder neck obstruction in chronic prostatitis. Br J Urol 1984; 56 : 713-716.
12. Blacklock NJ. Anatomical factors in prostatitis. Br J Urol 1974; 46 : 47-54.
13. Kirby RS, Lowe D, Bultitude MI, Shuttleworth KE. Intra-prostatic urinary reflux: an aetiological factor in abacterial prostatitis. Br J Urol 1982; 54 : 729-731.
14. Doble A, Walker MM, Harris JR et al. Intraprostatic antibody deposition in chronic abacterial prostatitis. Br J Urol 1990; 65 : 598-605.
15. Shortliffe LM, Wehner N. The characterization of bacterial and nonbacterial prostatitis by prostatic immunoglobulins. Medicine 1986; 65 : 399-414.
16. Andersen JT. Treatment of prostatodynia. In: Nickel JC (ed). Textbook of Prostatitis. London: ISIS 1999.
17. Egan KJ, Krieger JL. Chronic abacterial prostatitis a urological chronic pain syndrome? Pain 1997; 69(3): 213-218.
18. Williams PL et al. Gray´s Anatomy. 38. ed. Edinburgh: Churchill-Livingstone 1999 : 1848-1861.
19. Snell RS. Clinical Anatomy for Medical Students. 7. ed. Philadelphia: Lippincott Williams – Wilkins 1995 : 436-437.
20. Moore KL, Dalley AF. Clinically Oriented Anatomy. 5. ed. Philadelphia: Lippincott Williams–Wilkins 2006 : 459.
21. Pansky B. Review of Gross Anatomy. 6. ed. New York: McGraw-Hill 1996 : 488-489.
22. Walsh PC, Lepor H, Eggleston JC. Radical prostatectomy with preservation of sexual function: anatomical and pathological considerations. Prostate 1983; 34 : 473.
23. Lue TF, Zeineh SJ, Schmidt RA, Tanagho EA. Neuroanatomy of Penile Erection: Its Relevance to Iatrogenic Impotence. J Urol 1984; 131 : 273-280.
24. Barry MJ, Fowler FJ Jr, O'Leary MP et al. The American Urological Association symptom index for benign prostatic hyperplasia. The Measurement Committee of the American Urological Association. J Urol 1992; 148 : 1549-1557.
25. Nickel JC. Effective office management of chronic prostatitis. Urol Clin North Am 1998; 25 : 677-684.
26. Wenninger K, Heiman JR, Rothman I et al. Sickness impact of chronic nonbacterial prostatitis and its correlates. J Urol 1996; 155 : 965-968.
27. Mc Naughton-Collins M, O'Leary MP, Litwin MS. Quality of life is impaired in men with chronic prostatitis results from the NIH Cohort study (abstract). J Urol 2000; 163 (suppl): 23.
28. Mebust WK, Bosch R, Donovan J et al. Symptom evaluation, quality of life and sexuality. In: Cockett ATK, Khoury S, Aso Y et al (eds). Proceedings, The 2nd consultation on benign prostatic hyperplasia (BPH). Paris: Scientific Communication International Ltd. 1993 : 129.
29. Meares EMJ, Minich W. Prostatodynia: clinical findings and rationale for treatment. In: Weidner W, Brunner H, Krause W, Rothauge CJ (eds). Therapy of Prostatitis. München: Zuckschwerdt Verlag 1986 : 207.
30. Nickel JC. The Pre and Post Massage Test (PPMT): a simple screen for prostatitis. Tech Urol 1997; 3 : 38-43.
31. Nickel JC. Prostatitis: evolving management strategies. Urol Clin North Am 1999; 26 : 737-751.
32. de la Rosette JJ, Karthaus HF, van Kerrebroeck PE et al. Research in 'prostatitis syndromes': the use of alfuzosin (a new alpha 1-receptor-blocking agent) in patients mainly presenting with micturition complaints of an irritative nature and confirmed urodynamic abnormalities. Eur Urol 1992; 22 : 222-227.
33. Neal DE Jr, Moon TD. Use of terazosin in prostatodynia and validation of a symptom score questionnaire. Urology 1994; 43 : 460-465.
34. Drach GW. Trimethoprim sulfamethoxazole therapy of chronic bacterial prostatitis. J Urol 1974; 111 : 637-639.
35. Meares EM. Long-term therapy of chronic bacterial prostatitis with trimethoprim - sulfamethoxazole. Can Med Assoc J 1975; 112 : 22-25.
36. Schaeffer AJ, Darras FS. The efficacy of norfloxacin in the treatment of chronic bacterial prostatitis refractory to trimethoprimsulfamethoxazole and/or carbenicillin. J Urol 1990; 144 : 690-693.
37. Childs SJ. Ciprofloxacin in treatment of chronic bacterial prostatitis. Urology 1990; 35 : 15-18.
38. Canale D, Scaricabarozzi I, Giorgi P et al. Use of a novel non-steroidal anti-inflammatory drug, nimesulide, in the treatment of abacterial prostatovesiculitis. Andrologia 1993; 25 : 163-166.
39. Golio G. The use of finasteride in the treatment to chronic nonbacterial prostatitis. Abstacts of the 49th Annual Meeting of the Northeastern Section of the American Urological Association. Phoenix: AZ 1997 : 128.
40. Holm M, Meyhoff HH. Chronic prostatic pain. A new treatment option with finasteride? Scand J Urol Nephrol 1997; 31 : 213-215.
41. Meares EJ. Prostatitis and related disorders. In: Walsh PC, Retik AB, Stamey TA, Vaughan EDJ (eds). Campbell's Urology. Philadelphia: WV Saunders 1992 : 807.
42. Buck AC, Rees RW, Ebeling L. Treatment of chronic prostatitis and prostatodynia with pollen extract. Br J Urol 1989; 64 : 496-499.
43. Kamihira O, Sahashi M, Yamada S et al. Transrectal hyperthermia for chronic prostatitis. Nippon Hinyokika Gakkai Zasshi 1993; 84 : 1095-1098.
44. Choi NG, Soh SH, Yoon TH, Song MH. Clinical experience with transurethral microwave thermotherapy for chronic nonbacterial prostatitis and prostatodynia. J Endourol 1994; 8 : 61-64.
45. Barnes RW, Hadley HL, O'Donoghue EP. Transurethral resection of the prostate for chronic bacterial prostatitis. Prostate 1982; 3 : 215-219.
46. Robert R, Labat JJ, Bensignor M et al. Decompression and transposition of the pudendal nerve in pudendal neuralgia:A randomized contolled trial and long-term evaluation. Eur Urol 2005; 47 : 403-408.
47. Netter FH. Anatomický atlas člověka. 3. vyd. Praha: Galén 2005.
Labels
Paediatric urologist UrologyArticle was published in
Urological Journal

2007 Issue 2
-
All articles in this issue
- CANCER PAIN AND OPTIONS FOR ITS TREATMENT
- PATHOPHYSIOLOGY OF PELVIC PAIN
- CHRONIC PELVIC PAIN AND SEXUAL FUNCTIONS AS SEEN BY UROLOGIST AND ANATOMIST
- Chronic pain in interstitial cystitis
- CHRONIC PAIN AND SEXUAL DYSFUNCTION IN PATIENTS WITH CHRONIC PROSTATITIS/CHRONIC PELVIC PAIN SYNDROME
- POSTOPERATIVE PAIN
- Urological Journal
- Journal archive
- Current issue
- About the journal
Most read in this issue
- CHRONIC PELVIC PAIN AND SEXUAL FUNCTIONS AS SEEN BY UROLOGIST AND ANATOMIST
- Chronic pain in interstitial cystitis
- PATHOPHYSIOLOGY OF PELVIC PAIN
- POSTOPERATIVE PAIN

![Svaly dna pánevního [47].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/8c4076d5d924eab227c76d01de62af85.jpg)
![Svaly dna pánevního [47].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/764f2d82c8a2e731b3a901e0514546bb.jpg)
