-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Efekt časného nasazení vysokofrekvenční oscilace v léčbě dětí s respiračním selháním
Effect of early use of high frequency oscillation in children with respiratory failure
Objective:
To demonstrate the effect of high frequency oscillation (HFOV) on gas exchange in children with ARDS. To compare the groups with early and late application of HFOV for different variables.Design:
Retrospective analysis of the group of patients hospitalized from January 1994 to December 2006.Setting:
Department of Paediatric Anaesthesiology and Resuscitation, University Hospital.Materials and methods:
Fifty patients with severe hypoxaemic respiratory failure were included. The patients were included in the „early“ group (n = 30, 60%) if commenced on HFOV within 24 hours of initiating mechanical ventilation, or in the „late“ group if HFOV was commenced later than that. We studied the demographic data, PRISM score, primary diagnosis, time of ventilation, variables of acid-base balance, indexed variables (AaDO2, OI, PaO2/FiO2) and the oscilator settings (Paw, FiO2). Evaluation of the group mortality was performed.Results:
In both the groups pH and PaCO2 values improved achieving normal values. The early commencement group showed significant improvement in the values of AaDO2, PaO2/FiO2 and OI. The late commencement group did not show significant difference compared with baseline. Significant differences in the values of Paw were observed between the groups and a necessity for higher Paw setting in the late commencement group was evident. It was possible to decrease FiO2 faster in the early commencement group compared with the late commencement group. The mortality was 53 % in the early commencement group compared with 75 % in the late commencement group.Conclusion:
Early switch to HFOV had a positive influence on ventilation and oxygenation. Significant beneficial difference between the groups was observed mainly in AaDO2, PaO2/FiO2 and OI. The observed difference in mortality was not statistically significant but it could point to the ideal timing of commencing the patient on HFOV.Keywords:
respiratory failure – ARDS – children – high frequency oscillatory ventilation
Autori: Koudelková Ludmila; Košut Peter; Žurek Jiří; Marek Lukáš; Fedora Michal
Pôsobisko autorov: Klinika dětské anesteziologie a resuscitace, Pracoviště dětské medicíny, Fakultní nemocnice Brno
Vyšlo v časopise: Anest. intenziv. Med., 21, 2010, č. 5, s. 245-250
Kategória: Intenzivní medicína - Původní práce
Súhrn
Cíl studie:
Demonstrovat efekt vysokofrekvenční oscilace (HFOV) na výměnu plynů u dětí s ARDS. Porovnat v jednotlivých parametrech skupinu časného a pozdního nasazení HFOV.Typ studie:
Retrospektivní analýza souboru pacientů v období leden 1994 až prosinec 2006.Název a sídlo pracoviště:
Klinika dětské anesteziologie a resuscitace fakultní nemocnice.Materiál a metoda:
Do souboru bylo zařazeno 50 pacientů se závažným hypoxemickým respiračním selháním. Pacienti byl zařazeni do skupiny „časné“, pokud byli napojen na HFOV do 24 hodin po napojení na konvenční UPV (n = 30, 60 %); pokud byli napojen později, byli zařazeni do skupiny „pozdní“. Sledovali jsme demografické údaje, PRISM skóre, primární diagnózu, dobu ventilace, hodnoty ABR, indexované parametry (AaDO2, OI, PaO2/FiO2) a hodnoty nastavení oscilátoru (Paw, FiO2). Byla srovnána mortalita skupin.Výsledky:
V obou skupinách se normalizovaly hodnoty pH i PaCO2. U časně napojených pacientů se signifikantně zlepšily hodnoty AaDO2, PaO2/FiO2 i OI. U pozdně napojených pacientů nebyly signifikantní rozdíly proti hodině 0 pozorovány. Mezi skupinami byly signifikantní rozdíly v hodnotách Paw a nutnost vyššího nastavení Paw u pozdně napojených. FiO2 je možno snižovat u časně napojených oproti skupině pozdního nasazení rychleji. Časně napojení vykazují mortalitu 53%, pozdně napojení 75%.Závěr:
Časné napojení na HFOV mělo pozitivní vliv na ventilační i oxygenační parametry. Signifikantní rozdíly ve prospěch časně napojených byly sledovány zejména u parametrů AaDO2, PaO2/FiO2 a OI. Velký rozdíl v mortalitě nebyl statisticky významný, přesto by mohl poukázat na ideální načasování napojení pacienta na HFOV.Klíčová slova:
respirační selhání – ARDS – děti – vysokofrekvenční oscilační ventilaceÚvod
HFOV je v poslední době studována jako „rescue“ terapie u pacientů s ARDS, u kterých selhala konvenční mechanická ventilace a kde lze jen s obtížemi zajistit adekvátní ventilaci a oxygenaci v mezích protektivní ventilace. Refrakterní hypoxémie může být velkým problémem v péči o pacienty s ARDS, velmi často je příčinou úmrtí multiorgánové selhání, kdy jako jeho spouštěč může působit biotrauma [6].
HFOV produkuje velmi malé dechové objemy (nejedná se o skutečné dechové objemy, ale o amplitudu – obvykle označujeme jako ΔP) v rychlé frekvenci. Frekvence se pohybuje od 3 Hz u dospělých až po 25 Hz u novorozenců. Nízké objemy ve velmi rychlé frekvenci tak zajišťují minutový dechový objem [1]. Alveoly jsou udržovány otevřené za pomoci konstantního tlaku v plicích, který nemá velkých výchylek. HFOV účinně odděluje oxygenaci a ventilaci, což umožňuje klinikovi manipulovat s výhodou zvlášť s oxygenací a zvlášť s ventilací. Další odlišností od konvenční ventilace je to, že i exspirium je u HFOV aktivním procesem, což je za použití již zmíněných vysokých frekvencí v podstatě nutností [1, 3].
Cílem naší práce bylo podpořit předpoklad, že jakákoliv ventilační strategie, která může být efektivní v ovlivnění mortality, musí být aplikována časně v průběhu nemoci a předtím než je způsobeno biotrauma.
Soubor pacientů a metoda
Do souboru bylo zařazeno 50 pacientů, kteří byli na naši kliniku přijati se závažným hypoxemickým respiračním selháním a splňovali kritéria ARDS podle ACCP Consensus Conference z roku 1994 [4].
Od roku 1997 jsou všichni pacienti léčeni podle protokolu ALI/ARDS používaného na našem pracovišti. Protokol zahrnuje protektivní konvenční mechanickou ventilaci (tlakově řízenou CMV s PEEP a recruitment manévry) s permisivní hyperkapnií, sigh ventilaci, polohování pacienta do pronační polohy, aplikaci inhalovaného oxidu dusnatého, tracheální insuflaci plynu (TGI), vysokofrekvenční oscilační ventilaci, parciální kapalinovou ventilaci a extrakorporální membranózní oxygenaci [5]. Strategie konvenční ventilace je založena na principech protektivní plicní ventilace a vychází z doporučení ACCP (American College of Chest Physicians) z roku 1994 [4].
Indikací pro přepojení pacienta z konvenční UPV na HFOV byla nutnost použití FiO2 > 0,6 a středního tlaku v dýchacích cestách (Paw) > 15 cm H2O pro SpO2 minimálně 90 % nebo přetrvávající hyperkapnie a/nebo acidóza při konvenční UPV s TGI.
Základní strategií HFOV je „High Volume Strategy“ – recruitment alveolů a dosažení optimálního plicního objemu (nad alveolárním zavíracím objemem). Po přepojení z konvenční UPV na HFOV bylo základní nastavení středního tlaku v dýchacích cestách (Paw) o 2–5 cm H2O vyšší než Paw na UPV bezprostředně před HFOV. Dalším krokem bylo zvyšování Paw o 1–2 cm H2O do okamžiku, kdy se výrazně zlepšila SpO2 (> 97 %) a bylo možné snížit FiO2 z úvodní hodnoty 1,0 na 0,6 a méně při SpO2 > 90 % nebo do známek hyperinflace plic (deprese kardiovaskulárního systému nebo rozepnutí plic nad 9. žebro podle RTG obrazu). Pokud byl přítomen air-leak syndrom (pneumotorax, pneumomediastinum, pneumoperikard, intersticiální plicní emfyzém), byla manipulace s Paw mírně odlišná: po dosažení optimálního plicního objemu jsme snížili o 1–2 cm H2O Paw a tolerovali zvýšení FiO2 nad 0,6 pro SpO2 periferní krve > 85 % po přechodnou dobu (12–24 hodin), eventuálně do resorpce air-leak [2, 5].
Frekvence (f) je nepřímo úměrná hmotnosti pacienta, proto u malých kojenců bylo nastavení blízké neonatální aplikaci (10 Hz), u batolat a větších dětí byla frekvence nastavena mezi 10 a 5 Hz, pacienty s tělesnou hmotností nad 30 kg jsme ventilovali frekvencí pod 5 Hz [2, 5].
Amplituda tlaku (ΔP) byla při napojení na HFOV nastavena empiricky a upravena podle PaCO2 s maximem 7 kPa. Pokud nebyla ΔP dostatečná, zvyšovali jsme ji o 2–5 cm H2O, dalším krokem bylo snižování f o 1–2 Hz. U žádného pacienta nebylo nutné prodloužení inspiračního času (Tinsp) z 33 % na 50 % [2, 5].
Po úvodním zvýšení Paw, a tím nitrohrudního tlaku, byla u všech pacientů nutná expanze intravaskulárního objemu k zajištění adekvátního předtížení (preloadu). Po stabilizaci HFOV nebyli pacienti relaxováni, odsávání z dýchacích cest v prvních hodinách HFOV nebylo nutné (dokonce není doporučováno, protože náhlý pokles Paw při rozpojení okruhu vede k rychlé ztrátě plicního objemu [5] ).
Pokud bylo nutné pacienty odsávat, byl použit zavřený systém TrachCare®. V případech, kde to bylo možné a indikované, jsme použili pronační polohu i na HFOV. Ostatní péče a léčba se nelišily od postupů používaných při konvenční ventilaci.
Odpojování od HFOV probíhalo standardně – postupně jsme snižovali Paw o 1–2 cm H2O podle SpO2 nebo PaO2 a ΔP o 2–5 cm H2O podle PaCO2. Přepojení zpět na CMV jsme zvažovali u pacienta, který splňoval následující kritéria: Paw 15–20 cm H2O, FiO2 < 0,6, bez air-leak a/nebo zlepšení RTG nálezu, bez desaturace při odsávání dýchacích cest. Pokud při Paw 15 ± 2 cm H2O toleroval pacient odsávání z dýchacích cest bez poklesu saturace, byl přepojen na konvenční ventilátor (Siemens Servo 300), Volume Support, FiO2 a Paw stejné jako poslední na HFOV. Pacient byl považován za odpojeného při splnění těchto kritérií: SpO2 > 90 %, FiO2 < 0,4, Paw < 15 cm H2O, normální pH při počtu dechů (RR) < 30/min a PIP < 35 cm H2O [5].
Pacienti byli rozděleni do skupin „časného“ (E – early) a „pozdního“ (L – late) nasazení HFOV. Časnost nasazení HFOV jsme rozdělili intervalem 24 hodin, pokud byl pacient napojen na HFOV do 24 hodin po konvenční UPV (umělá plicní ventilace), řadili jsme jej do skupiny „časné“, pokud později, řadili jsme jej do skupiny „pozdní“. U každého pacienta jsme sledovali: demografické údaje (věk, hmotnost, pohlaví, PRISM skóre), primární diagnózu (interní, chirurgická, traumatologická, onkologická), dobu ventilace (dobu konvenční UPV před napojením na HFOV (preCMV), dobu HFOV, dobu konvenční UPV po odpojení z HFOV (postCMV), celkovou dobu UPV, hodnoty acidobazické rovnováhy (pH, PaO2 (kPa), PaCO2 (kPa)), indexované parametry: AaDO2 (alveolo-arteriální diference parciální tenze kyslíku, kPa), oxygenační index (OI = Paw . FiO2 . 100/PaO2), hypoxemia skóre PaO2/FiO2 (mm Hg), hodnoty nastavení oscilátoru: Paw (pressure airways – střední tlak v dýchacích cestách), FiO2 (inspirační frakce kyslíku). Hodnoty ABR a indexované parametry jsme hodnotili v 0. hodině (tzn. čase napojení na HFOV) a dále v 1., 2., 3., 6., 12., 18., 24., 30., 36., 42. a 48. hodině.
Ke statistickému zhodnocení rozdílů mezi skupinami pacientů i uvnitř nich jsme použili Fisherův přesný test k hodnocení pohlaví, primární diagnózy a mortality, Mannův-Whitneyův U test k hodnocení věku, hmotnosti a PRISM skóre a Wilcoxonův párový test k hodnocení ABR, AaDO2, indexovaných parametrů a nastavení oscilátoru. Za statisticky významnou byla považována hodnota p ≤ 0,05.
Výsledky
Celý soubor tvořilo 50 pacientů s průměrným věkem 46 měsíců a průměrnou hmotností 15 kg. Průměrné příjmové PRISM skóre bylo 18. Průměrná délka preCMV byla 64 hodin, průměrná délka HFOV 111 hodin, průměrná délka postCMV 86 hodin. Průměrná délka celkové doby UPV byla 260 hodin.
V souboru pacientů bylo více pacientek ženského pohlaví (63 %), 38 % pacientů přežilo, nejvíce pacientů mělo primární diagnózu interní povahy (68 %).
Ve skupině časného nasazení HFOV bylo 30 pacientů, ve skupině pozdního nasazení 20 pacientů. Základní údaje celého souboru pacientů i obou skupin ukazuje tabulka 1.
Tab. 1. Časná/pozdní HFOV – demografická data, délky ventilací, PRISM 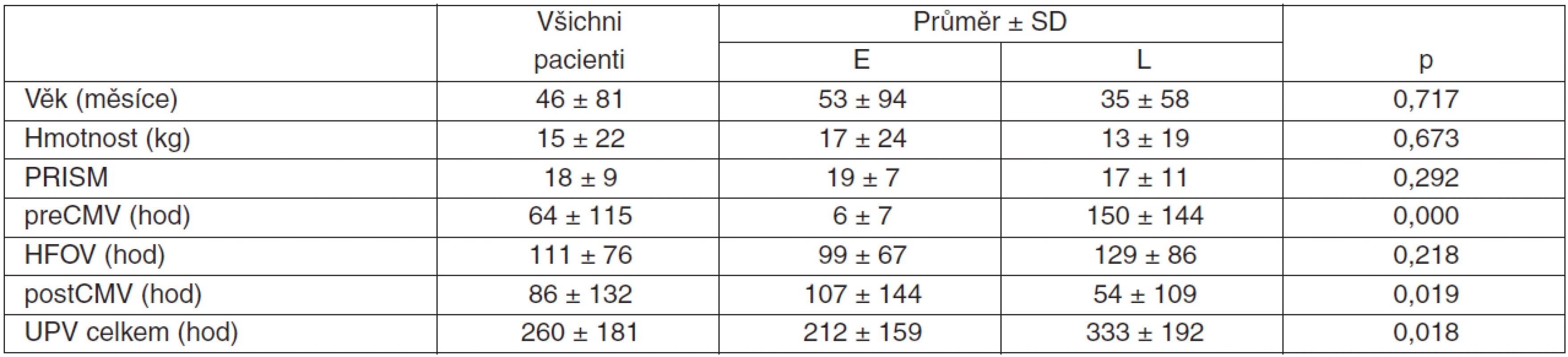
PRISM – Pediatric Risk of Mortality Score, preCMV – doba konvenční ventilace před napojením na HFOV, HFOV – vysokofrekvenční oscilační ventilace, postCMV – doba konvenční UPV po odpojení z HFOV, UPV – umělá plicní ventilace, SD – směrodatná odchylka (standard deviation), p – hladina statistické významnosti, E – časné (early), L – pozdní (late) Vstupní hodnoty u obou skupin pacientů ABR, indexovaných parametrů, Paw a FiO2 ukazuje tabulka 2.
Tab. 2. Časná/pozdní HFOV – vstupní hodnoty ABR, indexovaných parametrů, Paw a FiO2 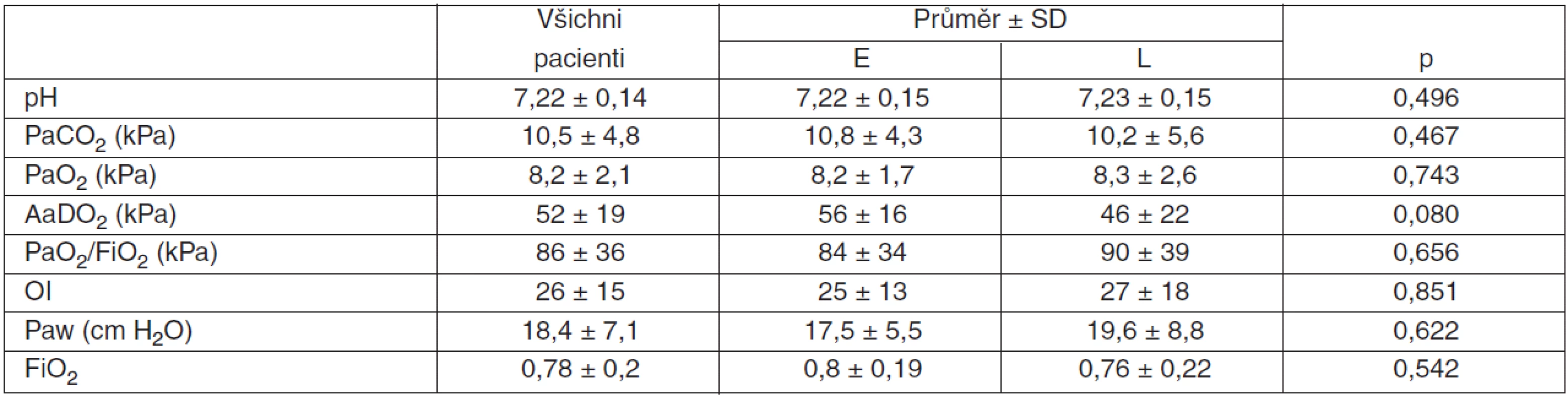
pH – záporný dekadický logaritmus koncentrace vodíkových iontů, PaCO2 – parciální tlak oxidu uhličitého v arteriální krvi, paO2 – parciální tlak kyslíku v arteriální krvi, AaDO2 – alveolo arteriální diference parciální tenze kyslíku, FiO2 – inspirační frakce kyslíku, PaO2/FiO2 – hypoxémie skóre, OI – oxygenační index, Paw – pressure airways (střední tlak v dýchacích cestách), FiO2 – inspirační frakce kyslíku, SD – směrodatná odchylka (standard deviation), E – časné (early), L – pozdní (late) Graf 1 ukazuje, že pH se ve skupině časného nasazení HFOV signifikantně zlepšovalo po celých 48 hodin. Obdobně ve skupině pozdního nasazení byly významné rozdíly ve všech časech kromě 2. hodiny. Rozdíly mezi skupinami nejsou. V obou skupinách dochází k normalizaci hodnot pH velmi rychle po napojení na HFOV.
Graf 1. Srovnání průběhu pH skupin časné/pozdní HFOV 
Graf 2 ukazuje, že hodnoty PaCO2 ve skupině časného nasazení HFOV dosahují statisticky významných rozdílů oproti 0. hodině od 1. do 48. hodiny. Skupina pozdního nasazení od 3. do 48. hodiny. Rozdíly mezi skupinami nejsou. V obou skupinách se hladina PaCO2 rychle normalizuje.
Graf 2. Srovnání průběhu PaCO<sub>2</sub> skupin časné/pozdní HFOV 
Graf 3 ukazuje, že v hodnocení paO2 nejsou v žádné ze skupin statisticky významné rozdíly vůči 0. hodině, zároveň nejsou ani rozdíly mezi skupinami. Ve 3. hodině se oxygenace zlepšuje v obou skupinách.
Graf 3. Srovnání průběhu PaO<sub>2</sub> skupin časné/pozdní HFOV PaO<sub>2</sub> – parciální tlak oxidu uhličitého v arteriální krvi 
Graf 4 ukazuje, že v průběhu AaDO2 jsou ve skupině časného nasazení HFOV statisticky významné rozdíly oproti 0. hodině od 3. do 48. hodiny, kdy hodnota AaDO2 postupně klesá. Ve skupině pozdního nasazení je statisticky významný rozdíl pouze v hodině 1., kdy se hodnota AaDO2 zvyšuje a od 2. hodiny se postupně snižuje. Téměř celých 48 hodin jsou hodnoty AaDO2 ve skupině pozdního nasazení vyšší než ve skupině časného nasazení, ačkoliv v 0. hodině je tomu naopak. Rozdíly mezi skupinami nejsou.
Graf 4. Srovnání průběhu AaDO<sub>2</sub> skupin časné/pozdní HFOV 
Graf 5 ukazuje, že v průběhu PaO2/FiO2 byly ve skupině časného nasazení statisticky významné rozdíly oproti 0. hodině v 6., 12., 30., 42. a 48. hodině. Ačkoliv je ve skupině časného nasazení výchozí hodnota PaO2/FiO2 nižší než u skupiny pozdního nasazení, postupně dochází k jejímu zvyšování a tedy ke zlepšení oxygenace a možnosti snížení FiO2. Ve skupině pozdního nasazení je výchozí hodnota PaO2/FiO2 vyšší, a přesto dochází nejprve k jejímu snížení a teprve od hodiny 3. k postupnému zvyšování bez statisticky významných rozdílů. Mezi skupinami se žádné rozdíly neprokázaly.
Graf 5. Srovnání průběhu PaO<sub>2</sub>/FiO<sub>2</sub> skupin časné/pozdní HFOV 
Graf 6 ukazuje v průběhu OI ve skupině časného nasazení signifikantní rozdíly mezi 30.–48. hodinou proti 0. hodině. Skupina pozdního nasazení žádné rozdíly nevykazuje. Mezi skupinami jsou rozdíly v 18. a 42. hodině. Ve skupině časného napojení HFOV bylo možno tedy dříve snižovat razantnost nastavení oscilátoru při zároveň zlepšující se oxygenaci.
Graf 6. Srovnání průběhu OI skupin časné/pozdní HFOV 
Z průběhu křivek grafu 7 je zřejmé vyšší nastavení Paw ve skupině pozdního nasazení HFOV. Statisticky významné rozdíly proti 0. hodině nejsou v žádné ze skupin. Rozdíly mezi skupinami jsou ve 2. a 24.–48. hodině.
Graf 7. Srovnání průběhu Paw skupin časné/pozdní HFOV 
Graf 8 ukazuje, že od 12. hodiny je ve skupině časného nasazení HFOV potřeba nižšího FiO2 než ve skupině pozdního nasazení. Mezi skupinami však statisticky významné rozdíly nejsou. Ve skupině časného nasazení jsou statisticky významné rozdíly proti 0. hodině ve 2., 6., 12., 18., 24., 30., 36., 42. a 48. hodině. Ve skupině pozdního nasazení je pouze jeden významný rozdíl proti 0. hodině, a to ve 12. hodině.
Graf 8. Srovnání průběhu FiO<sub>2</sub> skupin časné/pozdní HFOV 
Výsledná mortalita ve skupině časného nasazení HFOV je 53% a ve skupině pozdního nasazení HFOV 75%. Rozdíl mezi mortalitami není statisticky významný.
Diskuse
Hlavním zjištěním studie bylo, že časné napojení pacientů na HFOV má pozitivní účinek jak na ventilační, tak na oxygenační parametry. Hlavní rozdíly ve prospěch časně napojených byly v parametrech PaO2/FiO2, AaDO2 a OI. Dalším zjištěním byla nutnost vyššího nastavení Paw a FiO2 ve skupině pozdně napojených. Předpokládané ovlivnění mortality ve prospěch skupiny časně napojených nebylo statisticky prokázáno, přesto bylo pozorováno nesignifikantní snížení mortality v této skupině.
Naše závěry jsou obdobné závěrům 2 prospektivních observačních studií, které ukázaly, že HFOV je bezpečným a efektivním způsobem ventilace v léčbě dospělých [7, 8]. Tyto studie referovaly o zlepšení oxygenace i ventilace u dospělých s těžkým ARDS léčených HFOV. Taktéž obě studie poukázaly na fakt, že vyšší počet dnů na konvenční UPV před napojením na HFOV je signifikantně spojen s vyšší mortalitou. Mortalita v obou studiích byla poměrně vysoká (Fort et al. 53% [7], Mehta et al. 67% [8]), podobně jako v naší práci (62%). HFOV však byla aplikována jako rescue terapie u pacientů v závažném stavu a příčinou jejich úmrtí bylo většinou multiorgánové selhání, nikoliv selhání respirační (Fort et al. 33% exitus na podkladě respiračního selhání [7], Mehta et al. 6% [8], v naší práci nehodnoceno vzhledem k tomu, že většina pacientů se nacházela ve vážném stavu komplikovaném multiorgánovým selháním a nebylo možné odlišit jednoznačnou příčinu úmrtí.
V randomizované studii Derdaka et al. bylo zahrnuto 148 dospělých s ARDS [9]. Byli randomizováni do skupiny konvenční UPV nebo do skupiny HFOV. Skupina HFOV vykazovala rychlé zlepšení PaO2/FiO2 v porovnání se skupinou na konvenční UPV, ale tento rozdíl netrval déle než 24 hodin. V naší studii tento rozdíl přetrvával ve skupině časně napojených i po 24. hodině. Přesto byla mortalita v Derdakově studii ve skupině HFOV 37%, kdežto v naší studii 62%. Jelikož se v naší studii jedná o dětské pacienty, u nichž byl použit jiný skórovací systém než u dospělých, nelze přesně porovnat, v kterých parametrech se pacienti lišili a jejichž závažnost by mohla být příčinou rozdílných mortalit. V Derdakově studii rovněž identifikovali multivariantní analýzou 4 parametry, které signifikantně predikovaly 30denní mortalitu. Kromě APACHE II skóre, výchozího pH a OI v 16. hodině to také bylo více než 5 dnů na konvenční ventilaci před napojením na HFOV. To je shodné i s naším závěrem, že více dnů na konvenční UPV před napojením na HFOV je spojeno s vyšší mortalitou.
Do prospektivní tuniské studie z roku 2005 bylo zařazeno 10 pediatrických pacientů, u kterých byla HFOV užita jako časná „rescue“ terapie [10]. Průměrná délka konvenční ventilace byla pouhé 4 hodiny. Bylo prokázáno signifikantní zlepšení průběhu PaCO2, signifikantní pokles OI a AaDO2 a vzestup PaO2/FiO2 a těchto výsledků bylo dosaženo v průběhu 4 hodin po napojení na HFOV. Osm pacientů přežilo. Užití HFOV jako časné „rescue“ terapie zde prokázalo rychlé a trvalé zlepšení výměny plynů a nízkou mortalitu. Obdobné výsledky měla i naše studie ve skupině časně napojených, ale mortalita byla vyšší. Počet pacientů v tuniské studii je však nízký.
Závěr
Z naší studie je zřejmé, že časné napojení na HFOV má pozitivní vliv jak na ventilační, tak i na oxygenační parametry. Signifikantní rozdíly ve prospěch skupiny časného nasazení HFOV byly sledovány zejména v hodnocení parametrů AaDO2, paO2/FiO2 a OI.
Zajímavý je velký rozdíl v mortalitách obou skupin. Ačkoliv rozdíl mezi mortalitami nebyl statisticky významný, přesto by mohl poukázat na ideální načasování, kdy napojit pacienta na HFOV.
Došlo dne 4. 3. 2010.
Přijato dne 14. 7. 2010.
Adresa pro korespondenci:
MUDr. Ludmila Koudelková
Palackého 19
678 01 Blansko
e-mail: lkoudelkova@fnbrno.cz
Zdroje
1. Roubík, K. Vysokofrekvenční oscilační ventilace. Medical Tribune, 2007, III, 4, p. B5.
2. Null, D.,Perlmann, N. High Frequency Oscillatory Ventilation: Disease Specific Clinical Management. Strategie [online], c2008 [cit. 2008-06-26]. Dostupný na www: http:www.sensormedics.com.
3. Dostál, P. et al. Základy umělé plicní ventilace. Maxdorf-Jesenius: Praha, 2005.
4. Slutsky, A. S. et al. ACCP Consensus Conference: mechanical ventilation. Intensive Care Med., 1994, 20, p. 64–79.
5. Fedora, M. Vliv terapeutického protokolu na mortalitu syndromu akutní respirační tísně v dětském věku. Habilitační práce, LF MU Brno 2005.
6. Ritacca F. V., Stewart, T. E. Clinical review: High-frequency oscillatory ventilation in adults-a review of the literature and practical applications. Crit. Care, 2003, 7, p. 385–390.
7. Fort, P., Farmer, C. , Westerman, J. et al. High-frequency oscillatory ventilation for adult respiratory distress syndrome:a pilot study. Crit. Care Med., 1997, 25, p. 937–947.
8. Mehta, S., Lapinsky, S. E. , Hallett, D. C. et al. Prospective trial of high-frequency oscillation in adults with acute respiratory distress syndrome. Crit. Care Med., 2001, 29, p. 1360–1369.
9. Derdak, S., Mehta, S., Stewart, T. E. et al. High-Frequency Oscillatory Ventilation for Acute Respiratory Distress Syndrome in Adults. Am. J. Respir. Crit. Care Med., 2002, 166, p. 801–808.
10. Ben Jaballah, N. et al. High-frequency oscillatory ventilation in paediatric patiens with acute respiratory distress syndrome-early rescue use. Eur. J. Pediatr., 2005, 164, 1, p. 17–21.
Štítky
Anestéziológia a resuscitácia Intenzívna medicína
Článok vyšiel v časopiseAnesteziologie a intenzivní medicína
Najčítanejšie tento týždeň
2010 Číslo 5- DESATORO PRE PRAX: Aktuálne odporúčanie ESPEN pre nutričný manažment u pacientov s COVID-19
- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
- Metamizol v liečbe pooperačnej bolesti u opioid-tolerantnej pacientky – kazuistika
- e-Konzilium.cz — Masivní plicní embolie při tromboembolické nemoci
-
Všetky články tohto čísla
- Rekombinantní aktivovaný faktor VII v léčbě závažného krvácení u nehemofiliků – „vyšetřování (s využitím klinických randomizovných studií) skončilo, zapomeňte?“
- Rekombinantní aktivovaný faktor VII (rFVIIa) v léčbě závažného poporodního krvácení – data z registru UniSeven v České republice
- Aktivovaný rekombinantní faktor VII u závažného krvácení při těžkém poranění jater – kazuistiky
- Efekt časného nasazení vysokofrekvenční oscilace v léčbě dětí s respiračním selháním
- Pacienti s pandemickou chřipkou A (H1N1) 2009 v intenzivní péči
- Spontánní porod během ECMO podpory zahájené pro ARDS u nemocné s H1N1 pneumonií – kazuistika
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- Konference a kongresy
- Výborová schůze ČSARIM
- ZPRÁVY ČSIM
- Za profesorem MUDr. Zdeňkem Kalendou
- Anesteziologie a intenzivní medicína
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- Rekombinantní aktivovaný faktor VII (rFVIIa) v léčbě závažného poporodního krvácení – data z registru UniSeven v České republice
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- Aktivovaný rekombinantní faktor VII u závažného krvácení při těžkém poranění jater – kazuistiky
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



