-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Pacienti s pandemickou chřipkou A (H1N1) 2009 v intenzivní péči
Patients with pandemic influenza A (H1N1) 2009 in intensive care
Objective:
To describe the epidemiological and clinical characteristics, treatment and clinical outcome of patients with severe pandemic influenza.Design:
Retrospective observational study.Setting:
Department of Infectious Diseases, University Hospital.Materials and methods:
This is a retrospective study of patients hospitalized on the ICU from August 1, 2009, to January 31, 2010, with influenza symptoms and Pandemic A (H1N1) 2009 virus infection confirmed by rtPCR or specific antibody detection.Results:
Sixteen patients fulfilled the inclusion criteria (9 men and 7 women, aged 21–65 years, median 40). Median time from symptom onset to hospital admission was 5 days; from admission to transfer to the ICU 11 hours; from symptom onset to the start of antiviral therapy 5 days. Eight patients had a chronic underlying condition, 4 of them combined with obesity. Seven patients were obese with BMI > 30. Fever, cough and dyspnoea were the most frequent influenza symptoms. Median APACHE II score was 9.5. The reasons for ICU admission were bilateral pneumonia with acute respiratory failure (13 patients) and acute haemodynamic collapse (3 patients). Conventional mechanical ventilation was required in 9 patients. Two patients with acute renal failure were treated with continuous renal replacement therapy. The mean hospital stay was 25 days, median stay was 19 days. Twelve patients recovered and four died (25%).Conclusion:
The results confirmed the findings of previous studies: lower age of the patients with severe Pandemic A (H1N1) 2009 virus infection, common absence of comorbid conditions and a high rate of obesity. Primary influenza pneumonia was the prominent cause of the critical condition. A rational choice of antibiotic and antiviral treatment is discussed. The authors conclude that daily dosage of oseltamivir in severe influenza pneumonia should be increased to 300-600 mg.Keywords:
influenza, Pandemic A (H1N1) 2009, primary influenza pneumonia, respiratory failure
Autoři: Džupová Olga 1; Havlíčková Martina 2; Helcl Miroslav 3; Kabelková Maria 3; Kulichová Jana 3; Roháčová Hana 3; Beneš Jiří 1
Působiště autorů: Univerzita Karlova, 3. lékařská fakulta, Klinika infekčních nemocí, Praha 1; Národní referenční laboratoř pro chřipku, Státní zdravotní ústav, Praha 2; Klinika infekčních nemocí, Fakultní nemocnice Na Bulovce, Praha 3
Vyšlo v časopise: Anest. intenziv. Med., 21, 2010, č. 5, s. 251-257
Kategorie: Intenzivní medicína - Původní práce
Souhrn
Cíl práce:
Popsat epidemiologické a klinické charakteristiky pacientů s komplikovaným průběhem pandemické chřipky, jejich léčbu a léčebný výsledek.Typ studie:
Retrospektivní observační studie.Typ pracoviště:
Klinika infekčních nemocí fakultní nemocnice.Materiál a metoda:
Retrospektivní studie pacientů hospitalizovaných na JIP od 1. 8. 2009 do 31. 1. 2010, kteří měli klinické příznaky chřipky a byla u nich potvrzena infekce virem Pandemic A (H1N1) 2009 detekcí virové RNA pomocí rtPCR nebo průkazem specifických protilátek.Výsledky:
Vstupní kritéria splnilo 16 pacientů, 7 žen a 9 mužů ve věku 21–65 let, medián 40 let. Medián doby od začátku příznaků do hospitalizace byl 5 dnů, čas od přijetí do překladu na intenzivní lůžko 11 hodin, od začátku příznaků do zahájení léčby oseltamivirem 5 dnů. Základní chronické onemocnění mělo 8 pacientů, 4 v kombinaci s obezitou. Obézních pacientů s BMI > 30 bylo celkem 7. Nejčastějšími příznaky chřipky byly horečka, kašel a dušnost. Medián APACHE II skóre byl 9,5 bodů. Důvodem hospitalizace na JIP byla bilaterální pneumonie s akutní respirační insuficiencí (13 pacientů) a akutní oběhová insuficience při kardiální dekompenzaci (3 pacienti). Devět pacientů bylo uměle ventilováno konvenční ventilací. Dva nemocní s akutním renálním selháním byli léčeni eliminační technikou. Průměrná doba hospitalizace činila 25 dnů, medián 19 dní. Dvanáct pacientů se uzdravilo, čtyři zemřeli (25 %).Závěr:
Studie potvrdila výsledky prací zahraničních autorů, především nižší věk pacientů s komplikovaným průběhem chřipky A (H1N1) 2009, častou absenci interní komorbidity a vysoký výskyt obezity. Nejčastější příčinou těžkého až kritického stavu byla primární chřipková pneumonie. V práci je diskutována volba antibiotické a antivirové terapie při tomto onemocnění. Autoři považují za vhodné zvýšit dávkování oseltamiviru u těžké chřipkové pneumonie na 300–600 mg/den.Klíčová slova:
chřipka – Pandemic A (H1N1) 2009 – komplikace – primární chřipková pneumonie – respirační selháníÚvod
Počet osob postižených v průběhu loňského roku novým subtypem viru chřipky A označovaným Pandemic A (H1N1) 2009 není znám, pohybuje se celosvětově v řádu milionů. Počet úmrtí, které evidovala Světová zdravotnická organizace (WHO) v polovině května 2010, přesáhl 18 000 [1]. Příčinou závažného průběhu nebo úmrtí byla zejména těžká pneumonie s následným kardiorespiračním selháním.
Popisem a analýzou možných příčin těžkého průběhu pandemické chřipky se zabývala řada týmů v různých zemích [2–11]. Počty pacientů v jednotlivých publikovaných studiích jsou poměrně nízké a pohybují se obvykle kolem 20–40 osob. Skupina australských autorů popsala dosud největší soubor 722 pacientů léčených na jednotkách intenzivní péče v Austrálii a na Novém Zélandu [12].
V České republice byl pandemický virus poprvé identifikován u nemocných osob v 21. kalendářním týdnu roku 2009, vlna onemocnění kulminovala v průběhu října až prosince, s maximem ve 49. kalendářním týdnu. Ke dni 3. 3. 2010 bylo v ČR evidováno 2453 laboratorně potvrzených případů [13]. Domníváme se, že skutečný počet onemocnění lze odhadovat na desítky až stovky tisíc. Počet evidovaných úmrtí na chřipku ke stejnému datu činil 101 případů.
V komplexu klinik infekčních nemocí ve FN na Bulovce bylo v průběhu epidemie vyšetřeno a léčeno několik set pacientů s chřipkou. Cílem práce bylo popsat epidemiologické a klinické charakteristiky pacientů léčených na JIP, jejich léčbu a léčebný výsledek.
Metodika
Retrospektivní studie, zahrnující pacienty hospitalizované na Jednotce intenzivní péče (JIP) Kliniky infekčních nemocí 3. LF UK a FN Na Bulovce, probíhala v období od 1. 8. 2009 do 31. 1. 2010. Do studie byli zařazeni pacienti s klinickými příznaky chřipky a současně s laboratorně potvrzenou infekcí virem Pandemic A (H1N1) 2009. Splnění klinických kritérií znamenalo přítomnost alespoň dvou ze čtyř obvyklých příznaků chřipky: horečka nad 38 °C, celková zchvácenost, bolesti hlavy, svalů nebo kloubů, kašel a dušnost. Za laboratorní průkaz chřipkové infekce jsme považovali nález virové RNA pomocí polymerázové řetězové reakce (rtPCR, reverse transcription PCR) ve výtěru z nazofaryngu nebo aspirátu z dýchacích cest, nebo zjištění specifických protilátek hemaglutinačně inhibičním testem. Protilátky byly u většiny pacientů se sérologicky potvrzenou infekcí stanoveny pouze v jednom vzorku séra odebraného v akutní fázi nemoci; titr vyšší než 1 : 10 byl hodnocen jako pozitivní. PCR a sérologická vyšetření u studovaných pacientů zajišťovala Národní referenční laboratoř pro chřipku ve Státním zdravotním ústavu v Praze.
U většiny pacientů byla současně provedena mikrobiologická vyšetření zaměřená na průkaz bakteriálních původců respiračních infekcí: hemokultura, kultivační vyšetření sputa nebo endotracheálního aspirátu a PCR diagnostika hlavních respiračních patogenů ze stejných materiálů (Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Mycoplasma pneumoniae, Chlamydophila pneumoniae, Legionella pneumophila,Bordetella pertussis).
Zaznamenali jsme demografická data pacientů, jejich chronická onemocnění, stav výživy, dobu od začátku příznaků do přijetí do nemocnice, od přijetí do nemocnice do umístění na JIP, dobu do zahájení léčby antivirotikem a délku jeho podávání, klinické příznaky a vybrané laboratorní hodnoty při přijetí do nemocnice, vstupní rentgenový plicní nález, komplikace chřipky vedoucí k potřebě intenzivní péče, komplikace vzniklé během intenzivní péče, výsledek léčby a příčiny úmrtí. Stav výživy jsme hodnotili pomocí body mass index (BMI), závažnost celkového stavu pomocí Acute Physiology and Chronic Health Evaluation II (APACHE II) skóre a závažnost pneumonie pomocí Pneumonia Severity Index (PSI).
Studie byla provedena v souhlase se závěry Helsinské deklarace (revize 1996). Etická komise FN Na Bulovce byla o studii informována. Od pacientů nebo jejich příbuzných nebyl požadován podpis informovaného souhlasu, protože studie byla retrospektivní a nebyla spojena s žádnými vyšetřovacími ani léčebnými intervencemi nad rámec standardních vyšetření a léčby. Data pacientů byla přísně anonymní.
Výsledky
V uvedeném období bylo na JIP hospitalizováno celkem 20 pacientů s klinickým obrazem komplikované chřipky. Do souboru jsme zařadili pouze 16 z nich, u nichž byla laboratorně potvrzena infekce virem Pandemic A (H1N1) 2009. Průkaz infekce spočíval v nálezu virové RNA ve výtěru z nazofaryngu u 11 pacientů, v endotracheálním aspirátu u 1 pacienta a v pozitivní sérologické odpovědi u dalších 4 pacientů.
Tři pacienti byli přeloženi na naši kliniku po krátké hospitalizaci na jiném oddělení naší nebo jiné nemocnice, ostatní byli přijati primárně na naše pracoviště.
Průměrná doba hospitalizace činila 25 dní (medián 19). Uzdravilo se 12 pacientů, kteří byli všichni po doléčení na standardních odděleních propuštěni domů. Čtyři pacienti zemřeli, což odpovídá letalitě 25 %. U 2 žen bylo příčinou úmrtí nezvladatelné respirační selhání, u 2 mužů kardiální selhání.
Základní demografická data souboru a vybrané klinické a laboratorní charakteristiky jsou uvedeny v tabulce 1. Ani jeden pacient nebyl očkován proti sezonní chřipce, jedna pacientka byla očkována proti pandemické chřipce jeden den před začátkem příznaků.
Tab. 1. Demografické, klinické a laboratorní charakteristiky pacientů s komplikovaným průběhem pandemické chřipky A (H1N1) 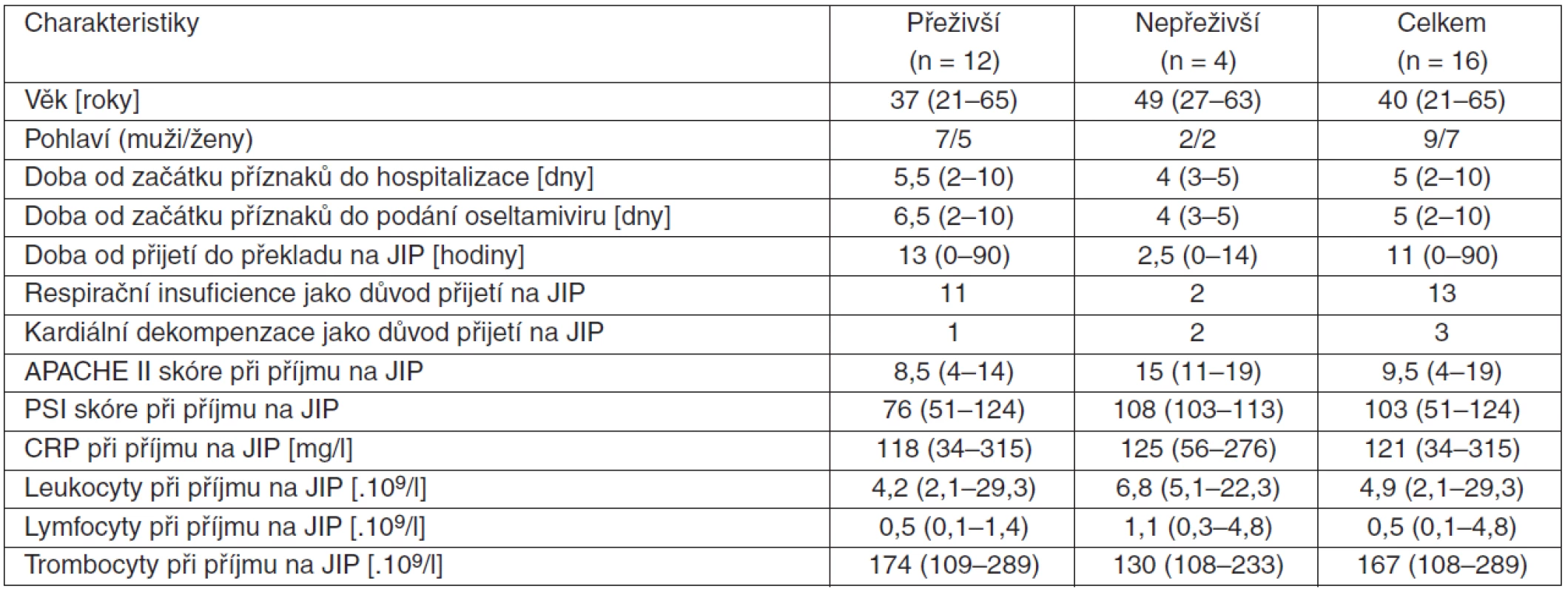
Hodnoty v tabulce udávají medián a rozptyl. Chronická interní choroba jako možná predispozice ke komplikovanému průběhu chřipky byla zjištěna u 8 nemocných, z toho čtyřikrát v kombinaci s obezitou. Spektrum komorbidit bylo následující: hypertenzní choroba u 4 nemocných, poruchy srdečního rytmu u 2 pacientů (fibrilace síní; ataky blíže nespecifikované tachykardie léčené amiodaronem) a dále u jednotlivých pacientů chronická kardiální insuficience na podkladě vrozené srdeční vady (viz níže); plicní fibróza; chronická obstrukční plicní nemoc (CHOPN); B non-hodgkinský lymfom po chemoterapii a biologické léčbě s přetrvávajícím imunodeficitem; diabetes mellitus léčený perorálními antidiabetiky. Tři pacienti měli dvě různé chronické choroby. Ze zbývajících 8 pacientů byli 3 obézní, u 2 mladých žen jsme obezitu hodnotili jako extrémní, s hmotností 120 a 140 kg při výšce 155 a 175 cm. Odpovídající hodnoty BMI činily 50 a 52.
Tabulka 2 ukazuje klinické příznaky pozorované v našem souboru, ve srovnání s příznaky u 552 nemocných s pandemickou chřipkou, které byly hlášeny epidemiologickému oddělení Hygienické stanice hl. m. Prahy.
Tab. 2. Četnost klinických příznaků pandemické chřipky A (H1N1) u pacientů hospitalizovaných na JIP a u pacientů registrovaných na území Prahy [23] ![Četnost klinických příznaků pandemické chřipky A (H1N1) u pacientů hospitalizovaných na JIP a u pacientů registrovaných na území Prahy [23]](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/cf10eea0256670458dd0af9713f9d8c9.png)
nz = nezjištěno Všichni naši pacienti s pneumonií měli na rentgenovém snímku hrudníku obraz bilaterálních nehomogenních více či méně splývajících infiltrátů převážně v dolních a středních plicních polích. V některých případech rentgenolog popsal jasný obraz intersticiální pneumonie (obr. 1 a 2). U nemocných s kardiální dekompenzací byla obvykle konstatována dilatace srdce a hyperémie plicních hilů jako projev městnání v malém oběhu. Laktátdehydrogenáza (LD) byla vyšetřena jen u 3 pacientů s rozmezím hodnot 7,9 až 13,6 μkat . l-1 a hladina kreatinkinázy (CK) u 4 pacientů s rozmezím hodnot 1,2-22,3 μkat . l-1. Dvanáct pacientů (75 %) mělo lymfopenii pod 1000 . 109/l.
Obr. 1. RTG snímek plic 56leté pacientky 1. den hospitalizace Nález popsán jako obraz oboustranného městnání v malém oběhu až charakteru kardiálního edému, při popisu kontrolního snímku po 2 dnech přehodnocen na oboustranné difuzní plicní infiltráty. 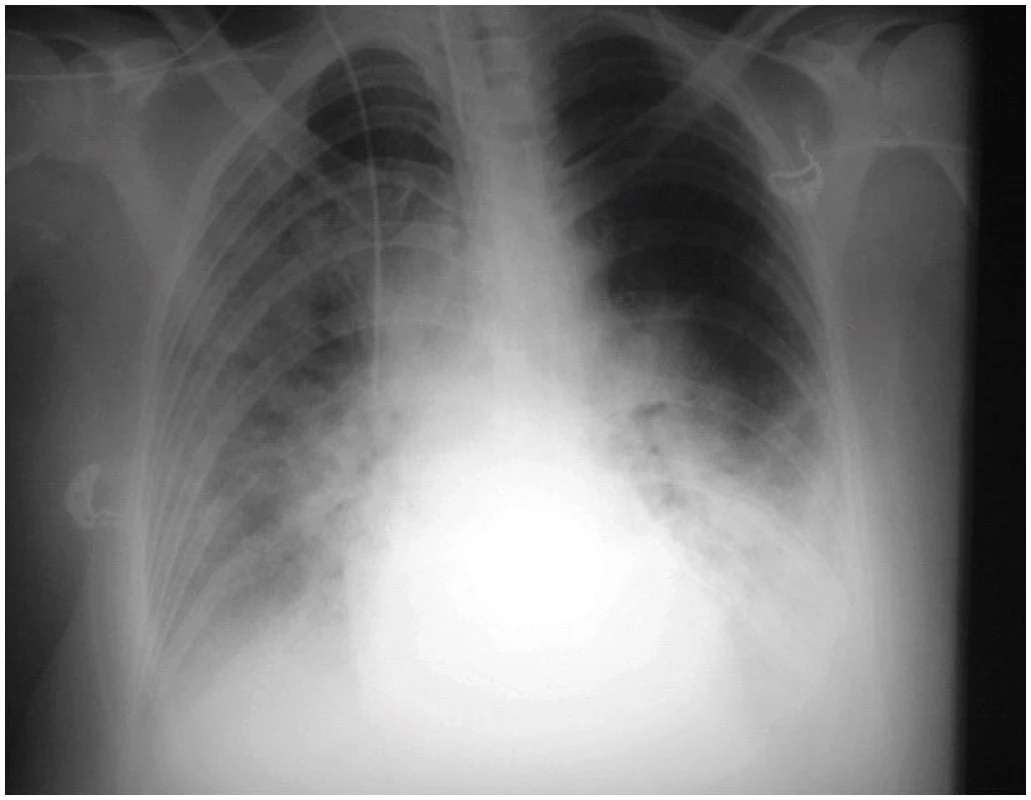
Obr. 2. CT scan plic stejné pacientky 35. den hospitalizace Výrazně difuzně snížená transparence plicního parenchymu, vakovité bronchiektázie v obou plicních křídlech. Obraz odpovídá proliferativní fázi ARDS. 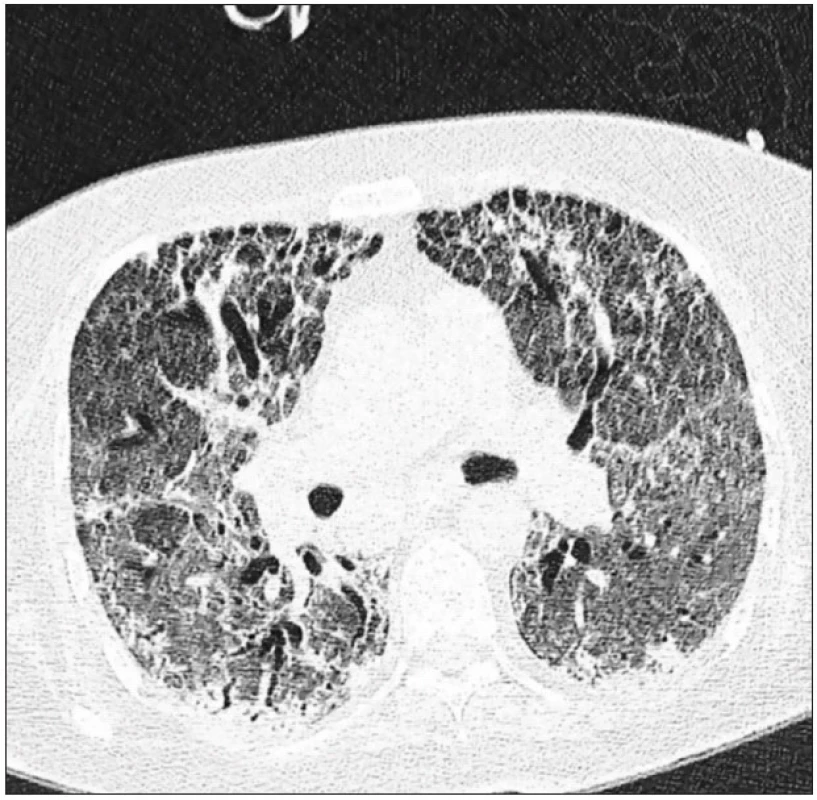
Akutní respirační insuficience si vynutila zahájení umělé plicní ventilace u 9 pacientů. Charakteristiky této podskupiny udává tabulka 3. U 2 pacientů s akutním renálním selháním bylo nutné nahradit renální funkce eliminační technikou.
Tab. 3. Další charakteristiky pacientů s komplikovanou chřipkou a nutností umělé plicní ventilace 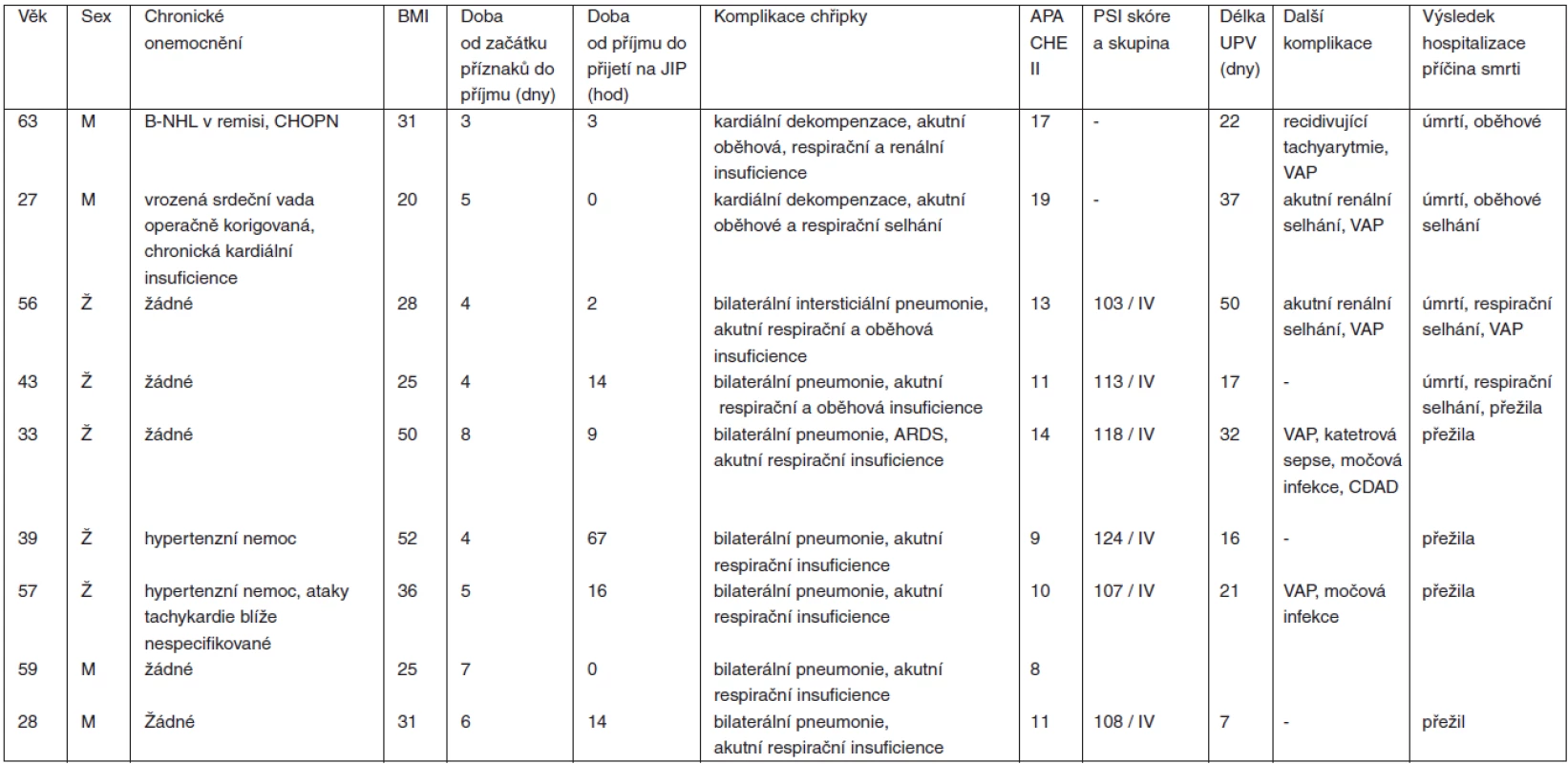
BMI = body mass index, PSI = pneumonia severity index, UPV = umělá plicní ventilace, VAP = ventilátorová pneumonie, CDAD = post-antibiotická kolitida vyvolaná Clostridium difficile, B-NHL = B-nonhodgkinský lymfom, CHOPN = chronická obstrukční plicní nemoc Při umělé plicní ventilaci jsme se maximálně snažili o protektivní ventilaci podle současných doporučení pro ARDS, avšak vzhledem k tíži primárního ARDS u našich pacientů nebylo praktické provedení vždy možné. Na úvod bylo nutné u většiny nemocných aplikovat FiO2 1,0; PEEP 10–15 cm H2O; režim tlakové ventilace; poměr inspiria k exspiriu 1 : 1 a často přechodně i inverzní poměr. V prvních hodinách až několika dnech jsme museli přistoupit k intermitentní nebo kontinuální svalové relaxaci. Ani tak jsme se u některých pacientů nevyhnuli plató tlakům kolem 40 cm H2O. Jednalo se zejména o obézní pacientky s BMI ≥ 50, kdy se jistě uplatňoval i vliv snížené poddajnosti hrudní stěny. Ke zlepšování ventilačních parametrů a tedy k ústupu od agresivního ventilačního režimu došlo u přeživších pacientů zpravidla během prvního týdne, u dvou z nich však až ve 2. a 3. týdnu umělé ventilace. Pronační polohu jsme nepoužívali vzhledem k obezitě a/nebo probíhající kontinuální eliminační technice. Podávání inhalačního oxidu dusného není na JIP dostupné. Barotrauma se vyskytlo až preterminálně u 2 pacientek s nezvladatelnou respirační insuficiencí. Žádný z pacientů nebyl léčen pomocí mimotělní membránové oxygenace (ECMO), protože jejich těžký stav znemožňoval transport do jiného zdravotnického zařízení.
Tři ze čtyř zemřelých pacientů byli pitváni. Při pitvě bylo jako příčina smrti u obou žen zjištěno těžké difuzní alveolární postižení s fibroproliferací v alveolech, aktivací pneumocytů, překrvením intersticia a reaktivní mediastinální lymfadenitidou. Mladší muž zemřel na následky kardiální dekompenzace při chronické dysfunkci pravé komory na podkladě vrozené srdeční vady (transpozice velkých arterií korigované Mustardovou operací; ejekční frakce pravé komory, která dodávala krev do aortálního řečiště, činila pouhých 20 %).
Ventilátorová pneumonie, respektive sekundární bakteriální plicní infekce způsobená nozokomiální flórou, se vyskytla v průběhu hospitalizace u šesti nemocných. U pitvaných osob však podle patologického nálezu nebyla hodnocena jako příčina smrti.
Diskuse
Práce zahraničních autorů monitorují většinou období 2–3 měsíců, kdy v jejich lokalitě pandemie chřipky probíhala. Většina našich pacientů byla na JIP léčena v době vrcholící epidemie v naší republice, tedy v listopadu a prosinci 2009. Od února do vzniku článku v květnu 2010 nebyl na klinice hospitalizován žádný další pacient s potvrzenou infekcí virem Pandemic (H1N1) 2009.
Komplikovaný průběh infekce pandemickým virem je v literatuře popisován především u mladších pacientů; medián se pohybuje od 27 do 46 let [2, 5, 7–10, 12, 14,15], průměr od 32 do 38 let [3, 6, 11]. S tím patrně souvisí i nízká četnost základních nemocí, hlavně plicních a kardiálních, které jsou známé jako predisponující faktory komplikovaného průběhu sezonní chřipky [16]. V našem souboru pouze polovina pacientů měla nějakou základní chronickou chorobu a při přísnějším hodnocení bychom mohli za vážně predisponované považovat jen tři pacienty: pacienta s CHOPN a non-hodgkinským lymfomem v remisi, pacienta s těžkou vrozenou srdeční vadou a pacientku s plicní fibrózou a restrikční poruchou ventilace.
Pacienti bez chronické komorbidity byli významně častěji obézní a celkový podíl obezity v našem souboru dosahoval 44 %. V zahraničních publikovaných souborech kriticky nemocných byl výskyt obezity 28 až 62 %, autoři z Michiganu uvádějí obezitu dokonce u devíti z deseti nemocných [14]. Většina autorů hodnotí obezitu jako významný rizikový faktor primární chřipkové pneumonie s nepříznivým průběhem a vysokou letalitou [2–3, 9, 11, 12].
Dominantní klinické příznaky u našich nemocných byly horečka, kašel a dušnost. U pacientů evidovaných Hygienickou stanicí hl. m. Prahy rovněž převažuje horečka a kašel, ale další hlavní příznaky byly bolesti svalů, kloubů a hlavy. Tyto symptomy zřejmě v subjektivním vnímání u pacientů s chřipkovou pneumonií nejsou tak zřetelné.
Medián doby trvání příznaků nemoci do přijetí v nemocnici, do zahájení intenzivní péče nebo do podání oseltamiviru se v zahraničních studiích pohyboval v rozmezí 3–8 dnů [3–6, 8, 11, 12, 14]. S ohledem na malý počet pacientů nelze provést statistické zhodnocení časových rozdílů ani klinických a laboratorních ukazatelů mezi skupinou přeživších a zemřelých, proto jsou rozdíly popsány jen v absolutních číslech. Na rozdíl od jiných studií jsou v našem souboru časové intervaly u pacientů zemřelých kratší než u pacientů, kteří přežili. Tento jev lze vysvětlit tím, že jejich stav byl již od přijetí závažnější a vedl tedy bez odkladů k přijetí přímo na JIP a okamžitému podání antivirotika.
Při příjmu na JIP měli pacienti s pneumonií SpO2 50–70 % na vzduchu a přesto jen někteří udávali těžší dušnost. Je zřejmé, že u tohoto typu pneumonie (intersticiální pneumonie postihující mladší jedince) nemusí postižený člověk subjektivně vnímat významnou dušnost, přestože je již přítomna značná porucha oxygenace krve. Velmi proto doporučujeme, aby všechny příjmové ambulance v nemocnicích i ambulance praktických lékařů byly vybaveny oxymetry. Jen pomocí nich je možné v ambulantních podmínkách rychle a objektivně určit závažnost nemoci a správně rozhodnout o postupu léčby.
Další zajímavou skutečností je poměrně dlouhá doba od začátku obtíží do rozvoje závažné pneumonie – průměrně 5,7 dne. Srovnejme tuto dobu s oficiálním doporučením podat nemocným antivirotika (oseltamivir, Tamiflu®) do 48 hodin od začátku nemoci [17]. Je zřejmé, že při komplikovaném průběhu chřipky je možné zahájit antivirovou léčbu i týden od začátku nemoci.
Otázkou zůstává, jak dlouho se antivirotika na JIP mají podávat. Závazné doporučení obsažené v Souhrnu údajů o přípravku (SPC) stanoví 5 dnů [17]. V prestižní přednášce prof. Petersena na letošním Evropském kongresu klinické mikrobiologie a infekčních nemocí byl prezentován soubor 20 nemocných s komplikovaným průběhem chřipky, u nichž byla zjišťována doba vylučování viru. Pacienti vylučovali životaschopné viry po dobu 3–25 dní od přijetí do nemocnice, průměrně 12 dní; 75 % z nich vylučovalo virus déle než 7 dní. Všichni přitom byli léčeni oseltamivirem 4krát 75 mg podávaným sondou, případně zanamivirem (Relenza®) v dávce 4krát 25 mg inhalačně [18]. Prokázali jsme přítomnost virové RNA v tracheálním aspirátu u pacientky s těžkou chřipkovou pneumonií ještě 6. den podávání oseltamiviru (14. den od začátku příznaků chřipky). Tento nález sám o sobě sice ještě nedokazuje životaschopnost viru, přesto však považujeme za vhodné ponechat u pacientů s rozvíjející se chřipkovou pneumonií antivirovou léčbu do stabilizace stavu, minimálně po dobu 10 dnů.
Není uspokojivě vyřešeno ani správné dávkování oseltamiviru u pacientů na JIP. Podle SPC je oseltamivir u dospělých osob registrován jen pro dávkování 2krát 75 mg [17]. Žádnou jinou možnost tato závazná právní norma neuvádí. Doporučení celosvětově uznávaných autorit typu WHO a CDC (Centers for disease control and prevention) však výslovně konstatuje, že správné dávkování u komplikované chřipky má být 2krát 150 mg a stejný názor sdílejí jednotliví další autoři [19, 20].
I když zdůvodnění dvojnásobného dávkovacího schématu není nikde jasně formulováno, lze předpokládat, že hlavním důvodem je snížená kvalita imunitní odpovědi u nemocných, např. v souvislosti s nedostatečnou tvorbou interferonu. Je však potřeba brát v úvahu i farmakokinetické aspekty. Oseltamivir je v organismu rychle metabolizován na aktivní látku (oseltamivir-karboxylát), která se distribuuje v objemu odpovídajícím extracelulární tělesné tekutině (cca 23 litrů u dospělého člověka). Vylučuje se ledvinami, a to glomerulární filtrací i tubulární sekrecí [17].
Uvedené základní údaje jsou získávány studiemi na zdravých dobrovolnících, kteří mají standardní farmakokinetické parametry. U pacientů v intenzivní péči se však farmakokinetika léků mění. Většinou se zvětšuje množství extracelulární tekutiny, zatímco rozsah glomerulární filtrace se může významně zmenšit i zvětšit, v závislosti na stavu cirkulace, funkční schopnosti ledvin a poskytované léčbě. U mladých osob bez preexistující kardiální a renální insuficience lze očekávat spíše hyperkinetickou cirkulaci a zvýšený rozsah vylučování. Je tedy možné, že dávkování oseltamiviru u našich nemocných bylo nedostačující a dobrého účinku by bylo dosaženo teprve při dávkách kolem 450–600 mg/den. Bohužel zatím neexistují dostatečně rozsáhlé prospektivní studie, které by odpovídaly požadavkům medicíny založené na důkazech (EBM). Ostatně, tento problém se projevil již při léčbě pacientů s těžkými formami ptačí chřipky (H5N1) před několika lety.
Situaci dále komplikuje skutečnost, že oseltamivir je k dispozici pouze v tabletové formě. U ventilovaných nemocných s projevy multiorgánového selhávání nemáme při podávání oseltamiviru do žaludeční nebo duodenální sondy jistotu o biologické dostupnosti léku. V září 2009 proběhla tiskem zpráva o úspěšné léčbě 22leté ženy, jejíž imunitní systém byl podstatně oslaben v důsledku prodělané chemoterapie a oseltamivir i zanamivir ve standardním podávání neměly žádoucí efekt. Ženu se podařilo vyléčit intravenózní aplikací zanamiviru [21]. Zanamivir však není registrován pro nitrožilní podání. Větší naději v současné době skýtá nový antivirový přípravek peramivir, který je určen k parenterální terapii a prochází klinickým zkoušením. Dosud není v žádném státě registrován k léčebnému použití.
Pokud se týká antibakteriální léčby, naši nemocní byli zpravidla po přijetí na JIP léčeni kombinací cefalosporinu 3. generace (cefotaxim, ceftriaxon) s makrolidem (klaritromycin). Tuto léčbu odpovídající doporučeným postupům České pneumologické společnosti [22] jsme podávali i při vysokém podezření na chřipkovou pneumonii, protože pacienti splňovali kritéria těžké pneumonie a při vysoké hodnotě C-reaktivního proteinu (CRP) nebylo možné vyloučit bakteriální nebo duální etiologii. Antibiotika jsme vysazovali až poté, kdy byla potvrzena diagnóza chřipky a zároveň vyšetření tracheálního aspirátu neprokázalo bakteriální infekci dolních dýchacích cest.
Na základě rentgenového obrazu a klinických projevů jsme nakonec hodnotili téměř u všech našich pacientů pneumonii jako primární virovou. U žádného pacienta v tomto souboru jsme neprokázali nasedající stafylokokovou nebo pneumokokovou pneumonii. Velmi nízký výskyt sekundárních bakteriálních pneumonií popisují i další autoři [3, 7, 8, 14].
Závěr
Primární chřipková pneumonie je nejčastější komplikací při infekci novým pandemickým chřipkovým virem A(H1N1). Tato intersticiální pneumonie může způsobit těžký až kritický stav pacientů s nutností intenzivní péče. Postiženi bývají především jedinci mladšího a středního věku bez vážnější interní komorbidity, častěji obézní jedinci. U některých pacientů neodpovídá relativně dobrý klinický stav významné poruše oxygenace přítomné již v době přijetí do nemocnice. Léčba antivirotikem by měla být zahájena co nejdříve při podezření na plicní komplikace chřipky a u pacientů s komorbiditou již při samotném podezření na chřipku. Dávka antivirotika doporučená v SPC a příbalovém letáku je pravděpodobně pro některé nemocné nedostatečná a měla by být zvýšena alespoň na dvojnásobek, jak doporučuje WHO. U některých nemocných lze zdůvodnit i podání čtyřnásobku doporučovaného dávkování.
Došlo dne 1. 6. 2010.
Přijato dne 10. 7. 2010.
Adresa pro korespondenci:
MUDr. Olga Džupová, Ph.D.
Nám. Jiřího z Lobkovic 2
130 00 Praha 3
e-mail: olga.dzupova@lf3.cuni.cz,
olga.dzupova@post.lf3.cuni.cz
Zdroje
1. WHO Pandemic (H1N1) 2009 – update 101. Dostupné na www: http://www.who.int/csr/don/2010_05_21/en/index.html
2. Dominguez-Cherit, G., Lapinsky, S. E., Macias, A. E., Pinto, R., Espinosa-Perez, L., de la Torre, A. et al. Critically Ill Patients With 2009 Influenza A(H1N1) in Mexico. JAMA 2009, 302, p. 1880–1887.
3. Gomez-Gomez, A., Magana-Aquino, M., Garcia-Sepulveda, C. A., Ochoa-Perez, U. R., Falcon-Escobedo, R., Comas-Garcia, A. et al. Severe pneumonia associated with pandemic (H1N1) 2009 outbreak, San LuisPotosí, Mexico. Emerg. Infect Dis., 2010, 16, p. 27–34.
4. Jain, S., Kamimoto, L., Bramley, A. M., Schmitz, A. M., Benoit, S. R., Louie, J. et al. Hospitalized Patients with 2009 H1N1 Influenza in the United States, April–June 2009. N. Engl. J. Med., 2009, 361, p. 1935–1944.
5. Kopel, E., Amitai, Z., Grotto, I., Kaliner, E., Volovik, I. Patients with Pandemic (H1N1) 2009 in intensive care units, Israel. Emerg. Inf. Dis., 2010, 16, p. 720–721.
6. Kumar, A., Zarychanski, R., Pinto, R., Cook, D. J., Marshall, J., Lacroix, J., Stelfox, T. et al. Critically ill patients with 2009 influenza A(H1N1) infection in Canada. JAMA, 2009, 302, p. 1872–1879.
7. Louie, J. K., Acosta, M., Winter, K., Jean, C., Gavali, S., Schechter, R. et al. Factors associated with death or hospitalization due to pandemic 2009 influenza A(H1N1) infection in California. JAMA, 2009, 302, p. 1896–1902.
8. Perez-Padilla, R., de la Rosa-Zamboni, D., Ponce de Leon, S., Hernandez, M., Quinones-Falconi, F., Bautista, E. et al. Pneumonia and respiratory failure from swine-origin influenza A(H1N1) in Mexico. N. Engl. J. Med., 2009, 361, p. 680–689.
9. Rello, J., Rodriguez, A., Ibanez, P., Socias, L., Cebrian, J., Marques, A. et al. Intensive care adult patients with severe respiratory failure caused by Influena A(H1N1)v in Spain. Crit. Care, 2009, 13, p. R148.
10. Yeung, J. H. Y., Bailey, M., Perkins, G. D., Smith, F. G. Presentation and management of critically ill patients with influenza A(H1N1): a UK perspective. Crit. Care, 2009, 13, p. 426.
11. Zarychanski, R., Stuart, T. L., Kumar, A., Doucette, S., Elliott, L., Kettner, J. et al. Correlates of severe disease in patients with 2009 pandemic influenza (H1N1) virus infection. Canad. Med. Assoc. J., 2010,182, p. 257–264.
12. Webb, S. A., Pettila, V., Seppelt, I., Bellomo, R., Bailey, M., Cooper, D. J. et al. Critical care services and 2009 H1N1 influenza in Australia and New Zealand. N. Engl. J. Med., 2009, 361, p. 1925–1934.
13. SZÚ Aktualizované informace – potvrzené případy onemocnění virem “Pandemic (H1N1) 2009” ke dni 3.3. 2010. Dostupné na www: http://www.szu.cz/tema/prevence/aktualizovane-informace-o-potvrzenych-pripadech-onemocneni-2
14. CDC Intensive-care patients with severe novel influenza A (H1N1) virus infection – Michigan, June 2009. MMWR Morb. Mortal Wkly. Rep., 2009, 58, p. 749–752.
15. Mauad, T., Hajjar, L. A., Callegari, G. D., da Silva, L. F., Schout, D., Galas, F. R. et al. Lung pathology in fatal novel human influenza A (H1N1) infection. Am. J. Respir. Crit. Care Med., 2010, 181, p. 72–79.
16. CDC Prevention and control of influenza: recommendations of the advisory committee on immunization practices (ACIP). 2008, MMWR Morb. Mortal. Wkly. Rep., 57 (No.RR-7).
17. Tamiflu – Souhrn údajů o přípravku. Dostupné na www: http://www.leky.sukl.cz/informace-o-pripravku-tamiflu
18. Petersen, E. Optimal management of severe H1N1. European Congress on Clinical Microbiology and Infectious Diseases, Vienna, 10.–13.4.2010.
19. WHO Guidelines for pharmacological management of pandemic influenza A(H1N1) 2009 and other influenza viruses. Dostupné na www: http://www.who.int/csr/resources/ publications/swineflu/h1n1_guidelines_pharmaceutical_mngt.pdf
20. Rello, J., Pop-Vicas, A. Clinical review: Primary influenza viral pneumonia. Critical Care, 2009, 13, p. 235.
21. Intravenous relenza saves swine flu woman. Dostupné na www: http://www.reuters.com/article/idUSL310017920090903
22. Kolek, V. et al. Diagnostika a léčba komunitně získané pneumonie dospělých. Aktualizace 11.4.2007. Dostupné na www: http://www.pneumologie.cz/odborne/doporucene-postupy.php
23. Webové stránky Hygienické stanice hl.m. Prahy; údaje k 4.3.2010. Dostupné na www: http://hygpraha.cz
Štítky
Anestéziológia a resuscitácia Intenzívna medicína
Článok vyšiel v časopiseAnesteziologie a intenzivní medicína
Najčítanejšie tento týždeň
2010 Číslo 5- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
- Metamizol v liečbe pooperačnej bolesti u opioid-tolerantnej pacientky – kazuistika
- e-Konzilium.cz — Masivní plicní embolie při tromboembolické nemoci
- DESATORO PRE PRAX: Aktuálne odporúčanie ESPEN pre nutričný manažment u pacientov s COVID-19
-
Všetky články tohto čísla
- Rekombinantní aktivovaný faktor VII v léčbě závažného krvácení u nehemofiliků – „vyšetřování (s využitím klinických randomizovných studií) skončilo, zapomeňte?“
- Rekombinantní aktivovaný faktor VII (rFVIIa) v léčbě závažného poporodního krvácení – data z registru UniSeven v České republice
- Aktivovaný rekombinantní faktor VII u závažného krvácení při těžkém poranění jater – kazuistiky
- Efekt časného nasazení vysokofrekvenční oscilace v léčbě dětí s respiračním selháním
- Pacienti s pandemickou chřipkou A (H1N1) 2009 v intenzivní péči
- Spontánní porod během ECMO podpory zahájené pro ARDS u nemocné s H1N1 pneumonií – kazuistika
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- Konference a kongresy
- Výborová schůze ČSARIM
- ZPRÁVY ČSIM
- Za profesorem MUDr. Zdeňkem Kalendou
- Anesteziologie a intenzivní medicína
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- Rekombinantní aktivovaný faktor VII (rFVIIa) v léčbě závažného poporodního krvácení – data z registru UniSeven v České republice
- 6. CELOSTÁTNÍ KONFERENCE UMĚLÁ PLICNÍ VENTILACE 2010
- Aktivovaný rekombinantní faktor VII u závažného krvácení při těžkém poranění jater – kazuistiky
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



