-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Rituximab v rukou nefrologa – první zkušenosti
Rituximab in nephrologist’s hands – first experience
In nephrologic patients refractory to standard combined immunosuppressive therapy, or in those not tolerating it, biological therapy, including rituximab, has recently become a possible alternative. Rituximab (RTX) is a chimeric monoclonal antibody against the antigen CD20. Administration of RTX causes a selective transient depletion of B lymphocytes. In this article, our present experience with the use of RTX is summarized and commented. In our department, RTX has been so far administered to 17 patients with various nephrologic diagnoses (7x ANCA associated vasculitis - AAV, 5x systemic lupus erythematosus - SLE, 2x cryoglobulinaemia associated with hepatitis C virus infection - KG, 2x membranous nephropathy - MGN, 1x thrombotic thrombocytopenic purpura – TTP). In 7 patients, 4x375 g/m2 of rituximab was administered weekly. In 10 patients, the dose used was 1 g each separated by 2 weeks. Out of 15 patients with a follow-up longer than 1 year, at least partial remission has been achieved in all treated patients with SLE, KG and TTP, and also in some patients with AAV. In AAV patients with predominant granulomatous involvement, and in patients with MGN, the treatment with RTX was not successful. RTX was well tolerated in most patients; mild adverse events (fever, chills) were observed in 3 out of 17 patients (18%). Thus, rituximab seems to be a safe and effective drug in the therapy of some nephrologic diseases, even though the results of larger trials, which would unambiguously answer the questions of proper indications, the best administration strategy, possibility of repeated treatment and long-term safety, are still missing.
Key words:
biological therapy, glomerulonephritis, monoclonal antibody, refractory disease, rituximab
Autoři: Z. Hrušková 1,2; H. Marečková 2; E. Jančová 1; R. Ryšavá 1; V. Tesař 1
Působiště autorů: Klinika nefrologie VFN a 1. LF UK v Praze, 2Ústav imunologie a mikrobiologie VFN a 1. LF UK v Praze 1
Vyšlo v časopise: Čes. Revmatol., 17, 2009, No. 3, p. 127-133.
Kategorie: Původní práce
Souhrn
U nefrologických pacientů refrakterních na standardní kombinovanou imunosupresivní terapii, či u pacientů ji netolerujících, se v poslední době stala možnou alternativou biologická terapie včetně rituximabu. Rituximab (RTX) je chimérická monoklonální protilátka proti antigenu CD20, jejíž podání vede k přechodné selektivní depleci B lymfocytů. V tomto článku shrnujeme a komentujeme naše dosavadní zkušenosti s využitím RTX, který byl na našem pracovišti zatím podán u 17 pacientů s různými nefrologickými diagnózami (7x ANCA asociovaná vaskulitida – AAV, 5x systémový lupus erythematodes – SLE, 2x kryoglobulinemie asociovaná s HCV infekcí – KG, 2x membranózní nefropatie – MGN, 1x trombotická trombocytopenická purpura – TTP). U 7 pacientů bylo podáno 4 x 375 g/m2 rituximabu po týdnu, u 10 pacientů 2 x 1g po 14 dnech. Z 15 pacientů se sledováním delším než 1 rok se léčbou podařilo dosáhnout alespoň parciální remise u všech pacientů se SLE, KG a TTP a také u některých pacientů s AAV. U pacientů s AAV s převážně granulomatózním postižením a u pacientů s MGN terapie rituximabem úspěšná nebyla. Tolerance terapie byla velmi dobrá, mírné nežádoucí účinky (horečka, třesavka) byly pozorovány u 3 ze 17 pacientů (18 %). Rituximab se tak zdá být bezpečným a účinným lékem v terapii některých nefrologických onemocnění, i když zatím stále chybí větší studie, které by jednoznačně zodpověděly otázky vhodných indikací, nejlepší strategie podání, možnosti opakované léčby i dlouhodobé bezpečnosti.
Klíčová slova:
biologická terapie, glomerulonefritida, monoklonální protilátka, refrakterní onemocnění, rituximabÚvod
Standardní (často kombinovanou) imunosupresivní terapií se dnes podaří navodit remisi u většiny pacientů s glomerulonefritidami (ať už primárními s izolovaným postižením ledvin, či sekundárními s postižením ledvin v rámci systémového onemocnění), u kterých je tato léčba indikována. Někteří pacienti jsou však i přes vysoké dávky na terapii refrakterní. Běžně používané imunosupresivní režimy navíc často zahrnují cytotoxické preparáty (např. cyklofosfamid, chlorambucil), vysoké dávky kortikosteroidů, nebo jsou spojeny s jinými riziky, zejména při dlouhodobém užívání (např. cyklosporin – nefrotoxicita). S postupem doby a zlepšením celkové prognózy pacientů se systémovým onemocněním také přibývá těch, kteří sice na standardní terapii odpovídají dobře, ale při pokusu o snížení dávek či vysazení terapie rychle relabují, a tak je u nich kumulativní dávka podaných preparátů neúnosně vysoká.
Možnou alternativou v léčbě pacientů refrakterních na léčbu, či pacientů z různých důvodů netolerujících standardní terapii, se v posledních letech stala biologická terapie. Ta spočívá v podání látek biologické povahy, které zasahují do patofyziologického mechanismu zánětu ve prospěch léčeného organismu (1). Biologická terapie je obecně spojena s relativně malými nežádoucími účinky a je většinou dobře tolerována. V nefrologii je zatím asi nejvíce využívána u pacientů po transplantaci ledviny, ale postupně nachází své uplatnění i u pacientů s glomerulonefritidami, zejména u systémových onemocnění typu ANCA-asociované vaskulitidy (AAV) či systémového lupus erythematodes (SLE). Mezi biologické preparáty, jejichž podání je v těchto indikacích v různých fázích klinického výzkumu, patří vysokodávkované intravenózní imunoglobuliny (IVIg), antithymocytární globulin (ATG) a dále pak různé monoklonální protilátky namířené proti molekulám hrajícím roli v patofyziologii zánětu: protilátky či látky blokující tumor-nekrotizující faktor alfa (TNFα) – infliximab, etanercept, adalimumab; protilátky proti molekule CD20 – rituximab, ocrelizumab; protilátky proti molekule CD52 – alemtuzumab; a komplex CTLA-4-imunoglobulin – abatacept.
Rituximab (RTX) je chimérická monoklonální protilátka skládající se z myší variabilní oblasti namířené proti molekule (antigenu) CD20 a lidské IgG1 konstantní oblasti (2). CD20 je membránový fosfoprotein, který je exprimován pouze na B lymfocytech, a to na všech vývojových stadiích B lymfocytů s výjimkou kmenových a plazmatických buněk (3). Podání RTX tak navodí přechodnou selektivní depleci CD20 pozitivní (CD20+) B buněčné subpopulace lymfocytů trvající většinou nejméně 6 měsíců, s následnou postupnou rekonstitucí počtu B buněk (4). Mechanismy, kterými RTX vede k depleci B buněk, pravděpodobně zahrnují na protilátkách závislou buňkami zprostředkovanou cytotoxicitu (antibody-dependent cell-mediated cytotoxicity, ADCC), cytotoxicitu zprostředkovanou aktivací komplementu a navození apoptózy přímou signalizací (5). Teoreticky způsobí RTX eliminaci všech CD20+ B buněk, tedy i těch s abnormální tolerancí, čímž je zabráněno vzniku a/nebo expanzi autoreaktivních buněk produkujících autoprotilátky (3). Navíc naruší i interakci mezi B a T lymfocyty, a tak ovlivní také funkci T lymfocytů (6).
Od roku 1997 je rituximab využíván v léčbě hematologických malignit jako bezpečný a relativně dobře tolerovaný lék (2). V posledních letech se indikace k jeho podání rozšířily i na autoimunitní onemocnění. Byly publikovány práce referující o úspěšném podání RTX u pacientů se SLE, AAV nebo kryoglobulinemií asociovanou s HCV infekcí (7–11) a ačkoli např. u AAV právě probíhá kontrolovaná randomizovaná studie (12), revmatoidní artritida zůstává jedinou autoimunitní chorobou, u níž již výsledky velké studie prokázaly účinnost podání RTX (13) a pro jejíž léčbu je RTX v České republice od r. 2007 registrován.
Na Klinice nefrologie VFN a 1. LF UK v Praze jsme rituximab v off-label indikaci poprvé použili u pacientky se SLE v prosinci 2004. Od té doby bylo na našem pracovišti rituximabem léčeno dalších 16 pacientů s různými diagnózami. Cílem tohoto článku bylo shrnout a zhodnotit naše dosavadní zkušenosti s podáním tohoto léku.
Charakteristika pacientů
Od prosince 2004 do března 2009 bylo na naší klinice léčeno rituximabem 17 pacientů (8 žen, 9 mužů; medián věku 38 let; 7 pacientů s AAV, 5 pacientů se SLE, 2 pacientky s membranózní nefropatií (MGN), 2 pacienti s kryoglobulinemií (KG) asociovanou s HCV infekcí a non-Hodgkinským lymfomem (NHL) a 1 pacient s trombotickou trombocytopenickou purpurou (TTP) refrakterní na terapii plazmaferézami), jejichž základní charakteristiky ukazuje tabulka 1. Všichni tito pacienti jsou nadále ve sledování naší kliniky, průměrná doba sledování od podání rituximabu je nyní 32 měsíců. V rámci pravidelných kontrol na klinice byly u pacientů monitorovány hematologické, biochemické a imunologické parametry, včetně hladiny lymfocytů. V článku se dále podrobněji zmíníme o 15 z těchto pacientů, jejichž doba sledování činí alespoň 1 rok.
Tab. 1. Základní charakteristika 17 pacientů léčených rituximabem. 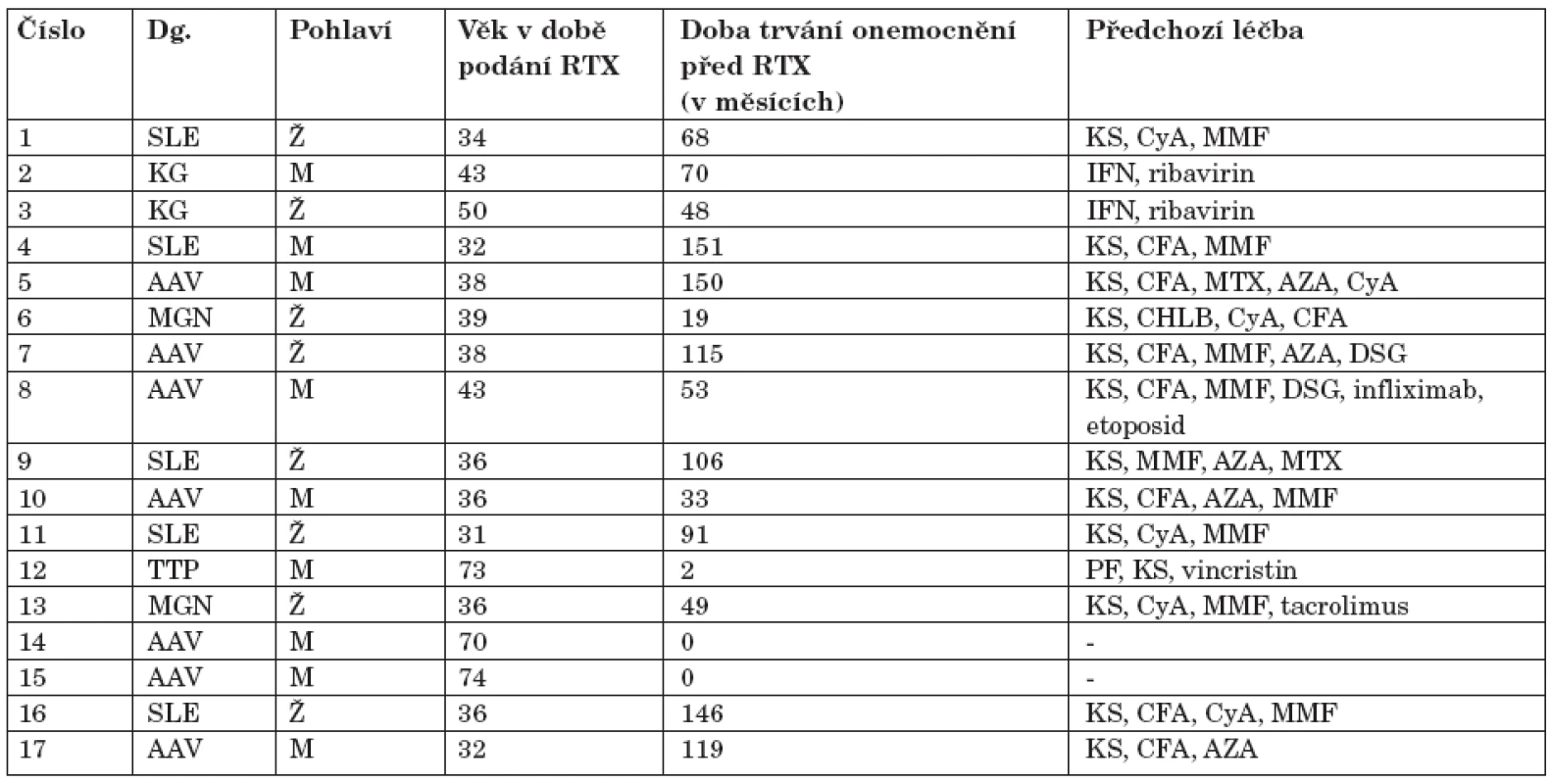
Dg. = diagnóza, AAV = ANCA asociovaná vaskulitida, SLE = systémový lupus erythematodes, KG = kryoglobulinemie, MGN = membranózní neuropatie, TTP = trombotická trombocytopenická purpura. Ž = žena, M = muž. RTX = rituximab. KS = kortikosteroidy, CFA = cyklofosfamid, AZA = azathioprin, CyA = cyklosporin A, MMF = mykofenolát-mofetil, PF = plazmaferézy, IFN = interferon, DSG = desoxyspergualin, CHLB = chlorambucil, MTX = metotrexát. U pacientů s kryoglobulinemií při HCV infekci s následným vznikem B-NHL bylo podání RTX primárně indikováno hematology. Dva pacienti s AAV byli RTX léčeni v rámci mezinárodní randomizované studie, kde byl RTX zkoušen jako indukční terapie. U všech ostatních pacientů byl RTX podán pro refrakterní onemocnění, po vyčerpání/selhání či intoleranci standardní, a v několika případech i jiné alternativní, terapie. Před aplikací RTX byli všichni pacienti o možném přínosu i rizicích léčby řádně poučeni a podepsali informovaný souhlas.
Dávka a způsob podání rituximabu
V původních studiích byl rituximab „standardně“ podáván ve 4 dávkách po 375 mg/m2v jednotýdenních intervalech. Toto dávkování jsme také využili u 7 našich pacientů (tab. 2), u pacienta s KG byly indikovány 2 cykly po 4 dávkách. Dávkovací protokol byl později v různých studiích mírně upravován, přičemž zejména v terapii SLE a AAV se často používal tzv. modifikovaný zkrácený režim podání 2 dávek rituximabu á 1 g po 14 dnech (2), který byl dodržen u zbývajících 10 našich pacientů. Podání rituximabu bylo většinou doplněno standardní imunosupresivní terapií (tab. 2), která byla (pokud to stav pacienta umožňoval) následně redukována či vysazena.
Tab. 2. Detaily podání rituximabu u 17 léčených pacientů. 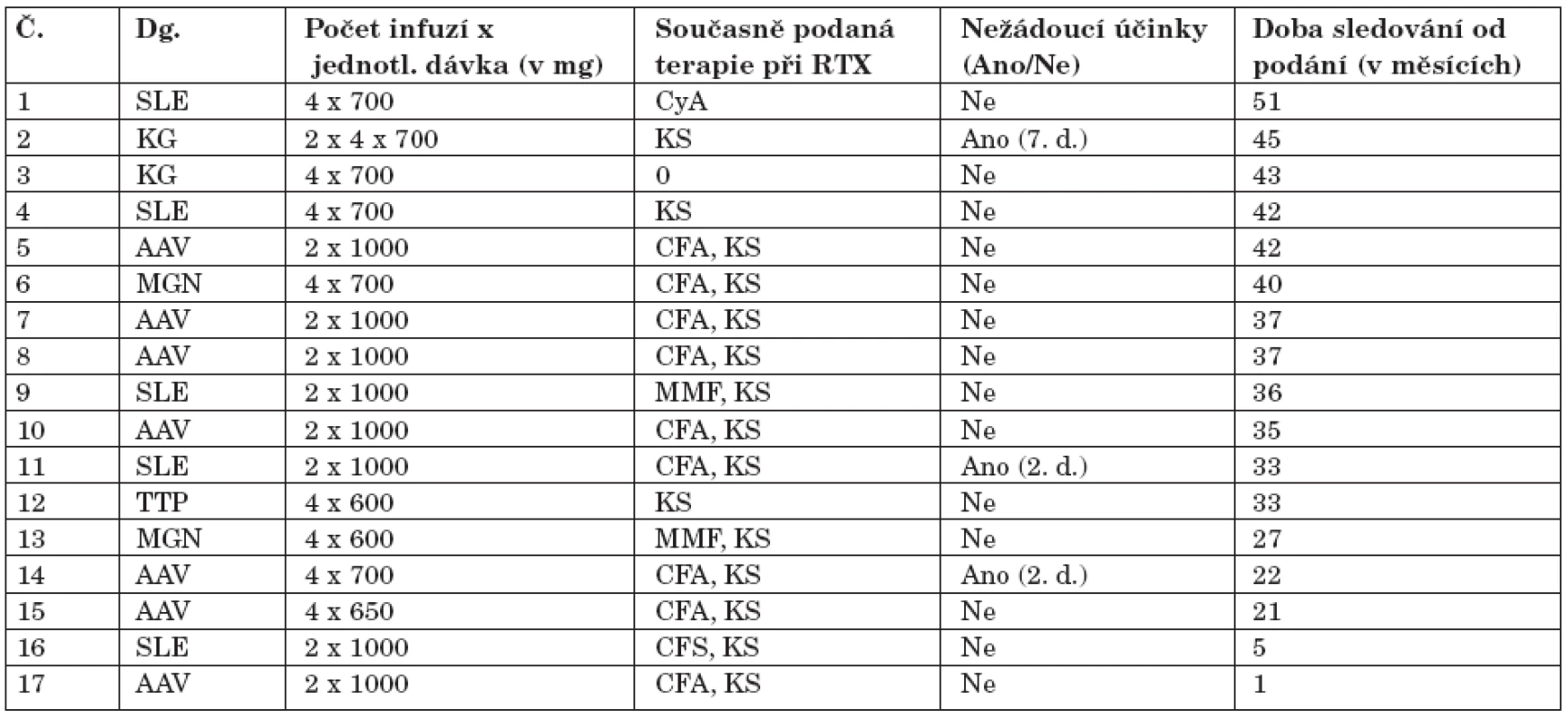
Č. = číslo. Dg. = diagnóza, AAV = ANCA asociovaná vaskulitida, SLE = systémový lupus erythematodes, KG = kryoglobulinemie, MGN = membranózní neuropatie, TTP = trombotická trombocytopenická purpura. RTX = rituximab. KS = kortikosteroidy, CFA = cyklofosfamid, MMF = mykofenolát-mofetil, CyA = cyklosporin A. d = dávka. Bezprostředně před vlastním podáním rituximabu byla aplikována všem pacientům premedikace (kortikosteroidy i.v., Dithiaden tbl., Paralen tbl.). Po celou dobu podání infuze byl u pacientů pravidelně monitorován celkový klinický stav, krevní tlak a tělesná teplota a zaznamenávány event. nežádoucí účinky.
Výsledky léčby
Výsledky léčby RTX orientačně shrnuje tabulka 3. Za kompletní remisi bylo považováno úplné vymizení známek aktivity onemocnění, parciální remise byla definována jako významné klinické zlepšení (o ≥ 50 % v měřitelných parametrech). Dlouhodobou úplnou depleci cirkulujících B lymfocytů se podařilo dosáhnout u všech pacientů s výjimkou jedné ženy (tab. 3). Podrobnější výsledky budou zmíněny a diskutovány v následujících odstavcích samostatně u jednotlivých diagnóz.
Tab. 3. Účinnost rituximabu u 15 léčených pacientů. 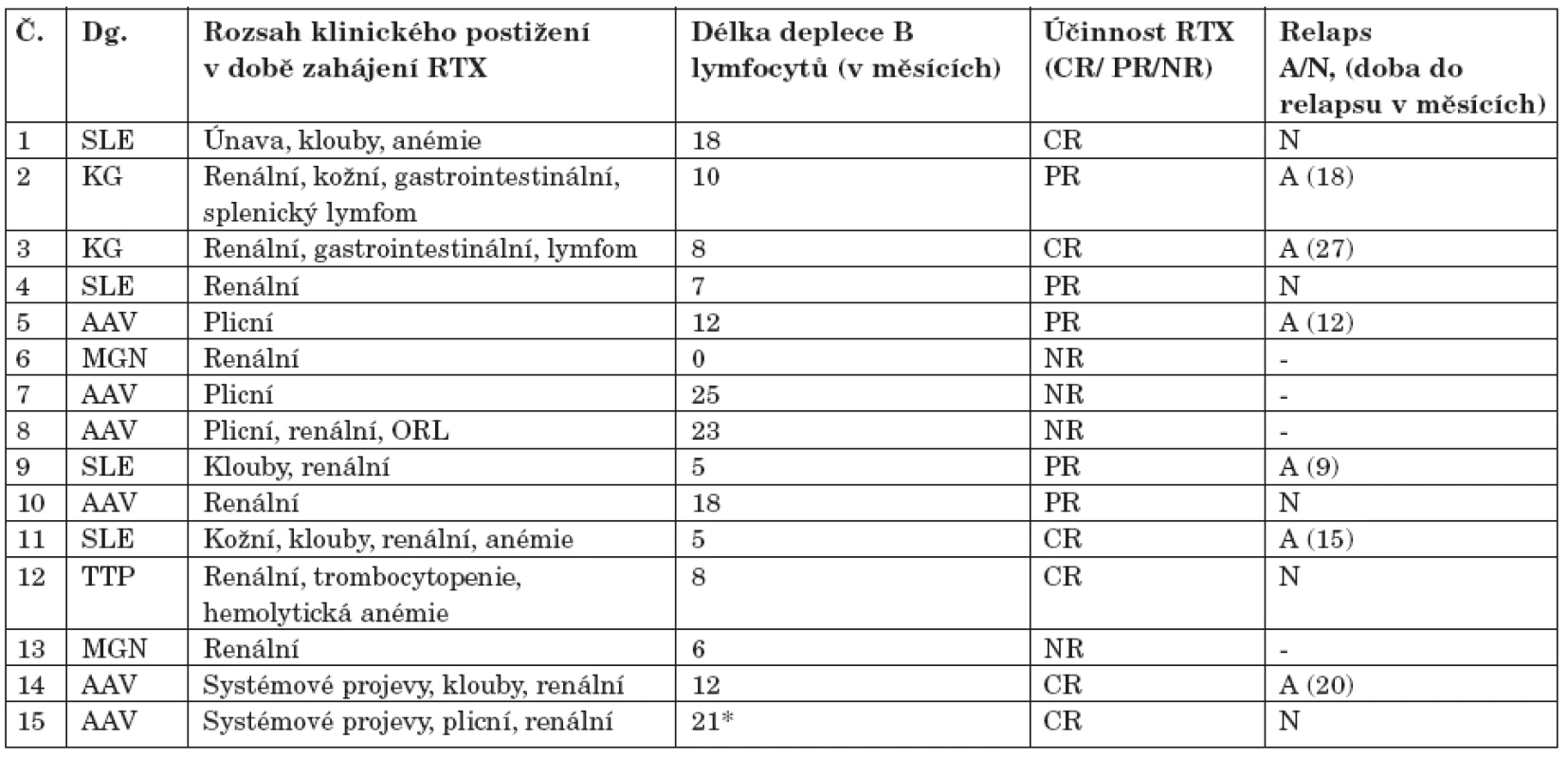
* deplece ještě trvá Č. = číslo. Dg. = diagnóza, AAV = ANCA asociovaná vaskulitida, SLE = systémový lupus erythematodes, KG = kryoglobulinemie, MGN = membranózní neuropatie, TTP = trombotická trombocytopenická purpura. RTX = rituximab. CR = kompletní remise, PR = paciální remise, NR = bez odpovědi na léčbu. A = ano, N = ne. ANCA-asociovaná vaskulitida
Rituximab byl v rámci mezinárodní studie RITUXVAS (12) organizované Evropskou skupinou pro studium vaskulitid (European Vasculitis Study Group, EUVAS), se kterou dlouhodobě spolupracujeme, podán dvěma našim pacientům s generalizovanou AAV (mikroskopickou polyarteritidou) jako indukční terapie. U obou pacientů bylo dosaženo kompletní remise onemocnění, včetně normalizace původně zvýšených ANCA protilátek. Studie nezahrnovala žádnou udržovací imunosupresivní léčbu kromě malé dávky kortikosteroidů a záhy po znovuobjevení B lymfocytů v periferní krvi (po 12 měsících od léčby) u jednoho pacienta začaly narůstat ANCA protilátky a po dalších 8 měsících jsme u něj pozorovali malý relaps, který dobře zareagoval na navýšení dávky kortikosteroidů.
U ostatních pacientů s AAV, kde jsme RTX podali pro refrakterní charakter onemocnění, vyčerpání celého spektra terapeutických možností a vysokou kumulativní dávku cyklofosfamidu (tab. 1), již výsledky terapie RTX tolik přesvědčivé nebyly. U dvou pacientů bylo léčbou dosaženo alespoň parciální remise (u pacienta s převážně renální aktivitou) či přechodné stabilizace onemocnění (u pacienta s plicním postižením), u zbylých dvou pacientů s plicním postižením s rozsáhlými granulomy, z nichž 1 byl v pravidelném dialyzačním programu, onemocnění (Wegenerova granulomatóza) i přes léčbu RTX dále progredovalo (tab. 3).
Indikaci k podání RTX (tedy terapie cílené primárně na B lymfocyty) u AAV podpořily důkazy o přímé úloze ANCA protilátek v patogenezi onemocnění (14). V několika menších zahraničních studiích se u pacientů s AAV refrakterních na běžnou terapii podařilo eliminací B lymfocytů rituximabem úspěšně navodit kompletní, ale většinou dočasnou remisi onemocnění (10, 15 ). V souladu s naším pozorováním se i u jiných autorů později ukázalo, že léčba RTX je více účinná u pacientů s tzv. vaskulitickou formou AAV, zatímco u pacientů s dominujícím granulomatózním postižením nedochází k výraznějšímu zlepšení (16). Přes některé slibné výsledky je zřejmé, že jasné indikace pro podání RTX v léčbě AAV bude teprve třeba stanovit, stejně jako vyřešit otázku indikace a bezpečnosti event. opakovaného podání RTX či doplnění udržovací imunosupresivní terapie.
Systémový lupus erythematodes
V léčbě SLE jsme RTX použili u 4 mladých pacientů s mnohaletým trváním tohoto onemocnění a také mnohaletou závislostí na užívání kombinované imunosupresivní terapie, z nichž 3 měli v době podání také aktivní lupusovou nefritidu. U 2 pacientek se podařilo navodit kompletní remisi onemocnění, u dalších 2 pacientů došlo k parciálnímu zlepšení. U naší nejdéle léčené pacientky remise onemocnění nadále trvá a po mnoha letech nutnosti užívání cyklosporinu A je tak nyní pacientka již přes 3 roky léčena pouze menší dávkou kortikosteroidů. I když u 2 pacientek došlo po 9, resp. 15 měsících, k relapsu onemocnění, podařilo se aspoň na přechodnou dobu vysadit či snížit dávku standardních imunosupresiv.
SLE je doslova prototypem imunokomplexového onemocnění, a tak nepřekvapí časté využití RTX v této indikaci. Zkušenosti s podáním rituximabu u refrakterních pacientů s lupusem, včetně aktivní lupusové nefritidy, byly v menších studiích zatím, stejně jako u nás, převážně pozitivní, a to i u několika pediatrických pacientů (shrnuto v 2). Selhání léčby, včetně nenavození deplece B lymfocytů, bylo pozorováno častěji u černošské populace (8). Nejnovější větší retrospektivní studie britských autorů se 7letým sledováním 50 léčených pacientů (17), jejíž výsledky byly nyní zveřejněny, uvádí dosažení kompletní remise u 42 % a parciální remise u 47 % po podání 1 cyklu této biologické terapie. Autoři většinou používali dávkování 2 x 1 g a léčbu doplňovali o 2 pulzy CFA a metylprednisolonu. Přestože se i v této práci rituximab jeví jako bezpečný lék, autoři také zdůrazňují trvající nutnost opatrnosti. Výsledky probíhajících větších randomizovaných studií (např. 18) by mohly napovědět více. Právě u SLE, který postihuje převážně mladé ženy, se ale RTX zdá nadějí pro refrakterní pacienty a pacienty s komplikacemi běžné terapie či její vysokou kumulativní dávkou.
Membranózní nefropatie
Rituximab byl také podán u dvou mladých pacientek s idiopatickou membranózní nefropatií a refrakterním nefrotickým syndromem. U první pacientky po vyčerpání všech standardních možností přetrvával těžký nefrotický syndrom, zejména hluboká hypalbuminemie s hladinou albuminu pod 10 g/l. Pro sklon k symptomatické hypotenzi pacientka netolerovala ani malou dávku blokátorů renin-angiotenzinového systému. U druhé pacientky jsme při volbě RTX mj. přihlíželi k přání pacientky v budoucnu otěhotnět, a proto jsme se chtěli vyhnout cytostatickým preparátům. Podání RTX však ani u jedné pacientky nevedlo ke zlepšení stavu, nedošlo k významnějšímu poklesu proteinurie ani vzestupu hladiny albuminu.
Podkladem pro myšlenku podání RTX u idiopatické MGN je charakteristický nález subepiteliálních depozit IgG v glomerulární bazální membráně a také průkaz CD20+ buněk v renálních biopsiích (2, 19). Nedávno bylo publikováno systematické zhodnocení účinnosti RTX v terapii MGN (20), ve kterém Bomback et al. shrnují výsledky 21 článků o celkem 85 pacientech s MGN léčených RTX. Podle této práce vede RTX k navození kompletní remise u 15–20 % pacientů a parciální remise u 35–40 % pacientů s MGN a jeho účinnost je tak zřejmě podobná jako u standardně používaných postupů (CyA, CFA či chlorambucil), při potenciálně lepší toleranci. Jak ale sami autoři upozorňují, více než polovina pacientů pochází z 1 centra (Remuzzi et al., např. 21, 22), kde je RTX používán jako primární terapie, a vliv na celkovém výsledku může mít i snaha pracovišť více publikovat pozitivní výsledky. Pro potvrzení účinnosti RTX u MGN tak bude zapotřebí doplnit větší kontrolované studie. Naše zkušenosti jsou zatím spíše negativní, ale na neúspěchu léčby u první pacientky se mohl podílet i fakt, že se přes standardní dávkování nepodařilo navodit úplnou depleci periferních B lymfocytů, došlo pouze k poklesu jejich hladiny.
Kryoglobulinemie
U obou našich pacientů s kryoglobulinemií asociovanou s infekcí virem hepatitidy C a s biopticky verifikovanou membranoproliferativní glomerulonefritidou byla zjištěna tzv. benigní adenomegalie, která vyústila v B-non-Hodgkinský lymfom (splenický lymfom u 1 pacienta a susp. B-lymfom marginální zóny u druhé pacientky). Pacienti byli indikováni hematologem k terapii RTX. V době jejího zahájení byly u obou pacientů dále patrny známky renální aktivity (zhoršení renálních funkcí, erytrocyturie, proteinurie) i další projevy systémové vaskulitidy (kožní, event. gastrointestinální – enterorhagie). Terapie RTX byla u obou pacientů velmi úspěšná, vedla ke klinickému i laboratornímu zlepšení a remisi lymfomu, po přechodném očekávaném zvýšení došlo i k přechodnému snížení virové nálože HCV. Po 18, resp. 27 měsících se u obou pacientů objevily známky relapsu, a proto bylo rozhodnuto o opakování terapie se znovu dobrým efektem i tolerancí. Opakování léčby již probíhalo na hematologickém pracovišti, a proto zde není podrobněji zmíněno.
Asociace chronické HCV infekce, KG a B-NHL lymfomu je dobře známa. O dobrých výsledcích léčby RTX u těchto pacientů byla opakovaně publikována kazuistická sdělení (23). Dle jiných autorů je RTX možné úspěšně využít i v léčbě refrakterní KG bez lymfomu (24).
Trombotická trombocytopenická purpura
U našeho pacienta s TTP s renálním postižením byl RTX podán pro perzistující závažnou trombocytopenii po selhání terapie plazmaferézami i vinkristinem. Terapie RTX byla u tohoto pacienta velmi úspěšná, záhy po jejím ukončení došlo k úplné normalizaci hladiny trombocytů, došlo i ke zlepšení červeného krevního obrazu a zlepšení renálních funkcí. V anamnéze pacienta byl 3 roky před výskytem TTP diagnostikován a chirurgicky a radioterapií léčen karcinom prostaty, stav pacienta byl poté ošetřujícími urology dlouhodobě hodnocen jako kompletní remise. Před podáním poslední dávky rituximabu byl pacient vyšetřen pro bolesti páteře zobrazovacími metodami (rtg a CT) a zde byly překvapivě zjištěny 2 kostní metastázy pravděpodobně karcinomu prostaty, pro které byla indikována hormonální terapie. Zpětně tak nelze vyloučit, že se jednalo o paraneoplastickou TTP.
TTP je asociována se snížením aktivity metaloproteinázy ADAMTS13, která štěpí vonWillebrandův faktor, působením autoprotilátek. V literatuře byly opakovaně popsány případy úspěšné léčby rekurentní nebo refrakterní TTP rituximabem. V relativně větší publikované skupině 11 pacientů se podařilo dosáhnout remise či zabránit relapsu u všech pacientů a u všech také došlo k nárůstu plazmatické aktivity ADAMTS13 (25). I tato vzácnější diagnóza je tedy jednou z možných indikací pro RTX.
Nežádoucí účinky
Terapie RTX je obecně dobře tolerována a nežádoucí účinky jsou většinou mírné. Nejčastěji se jedná o horečku se zimnicí a třesavkou, kterou jsme také pozorovali u 3 ze 17 našich pacientů (18 %). Závažnější nežádoucí účinky, jako těžší alergické reakce (dyspnoe, hypotenze, bronchospazmus, angioedém) či infekční komplikace jsou poměrně vzácné (2) a nebyly u našich pacientů zaznamenány. Zejména při opakovaném podání RTX může docházet k tvorbě antichimérických protilátek s možnou sérovou reakcí, ale přesná incidence výskytu těchto protilátek není známa. Ojediněle byly publikovány zprávy o výskytu tumoru po léčbě rituximabem (shrnuty v 2), u našeho pacienta s TTP se však vzhledem k velmi krátkému časovému intervalu od léčby a rozsahu metastatického postižení karcinomem domníváme, že metastázy pouze nebyly v době ataky TTP diagnostikovány. I do budoucna je však namístě jistá ostražitost, protože zkušenosti s dlouhodobým nebo opakovaným podáním RTX u autoimunitních chorob zatím chybějí.
Závěr
Naše zkušenosti s podáním RTX byly pozitivní zejména u pacientů se SLE, KG, TTP a některých pacientů s AAV. Oproti literárním údajům jsme nezaznamenali příznivý efekt u pacientek s MGN a také se zdá, že RTX není vhodným lékem pro pacienty s AAV s dominujícím granulomatózním postižením, i když naopak může být velmi výhodný u pacientů s „vaskulitickou“ formou onemocnění. Tolerance léčby byla u většiny pacientů velmi dobrá a nepozorovali jsme větší nežádoucí účinky. I když se u řady pacientů objevil s odstupem relaps onemocnění, přihlédneme-li k faktu, že k léčbě byli indikováni zejména pacienti s opravdu refrakterním onemocněním či komplikacemi standardní terapie, jsou výsledky terapie povzbudivé. Rituximab se tak zdá být bezpečným a účinným lékem v terapii některých nefrologických onemocnění, i když zatím stále chybí větší studie, které by jednoznačně zodpověděly otázky vhodných indikací, nejlepší strategie podání a možnosti opakované léčby nebo dlouhodobé bezpečnosti.
MUDr. Zdenka Hrušková
Klinika nefrologie
Všeobecná fakultní nemocnice v Praze
U Nemocnice 2
128 08 Praha 2
e-mail: zd.hruskova@seznam.cz
Zdroje
1. Zbořil V. Biologická terapie v gastroenterologii. Čes a Slov Gastroent a Hepatol 2007; 61(6): 287–292.
2. Salama AD, Pusey CD. Drug Insight: rituximab in renal disease and transplantation. Nat Clin Pract Nephrol 2006; 2 : 221–30.
3. Thatayatikom A, White AJ. Rituximab: A promising therapy in systemic lupus erythematosus. Autoimmun Rev 2006; 5 : 18–24.
4. Flossmann O, Jones RB, Jayne DRW, Luqmani RA. Should rituximab be used to treat antineutrophil cytoplasmic antibody associated vasculitis? Ann Rheum Dis 2006; 65 : 841–4.
5. Anolik JH, Campbell D, Felgar RE, Young F, Sanz I, Rosenblatt J, et al. The relationship of FcgammaRIIIa genotype to degree of B cell depletion by rituximab in the treatment of systemic lupus erythematosus. Arthritis Rheum 2003; 48 : 455–9.
6. Sfikakis PP, Boletis JN, Lionaki S, Vigklis V, Fragiadaki KG, Iniotaki A, et al. Remission of proliferative lupus nephritis following B cell depletion therapy is preceded by down/regulation of the T cell costimulatory molecule CD40 Ligand. Arthritis Rheum 2005; 52 : 501–513.
7. Gottenberg JE, Guillevin L, Lambotte O, Combe B, Allanore Y, Cantagrel A, et al. Club Rheumatismes et Inflammation (CRI). Tolerance and short term efficacy of rituximab in 43 patients with systemic autoimmune diseases. Ann Rheum Dis 2005; 64 : 913–20.
8. Looney RJ, Anolik JH, Campbell D, Felgar RE, Young F, Arend LJ, et al. B cell depletion as a novel treatment for systemic lupus erythematosus: a phase I/II dose-escalation trial of rituximab. Arthritis Rheum 2004; 50 : 2580–9.
9. Leandro MJ, Cambridge G, Edwards JC, Ehrenstein MR, Isenberg DA. B-cell depletion in the treatment of patients with systemic lupus erythematosus: a longitudinal analysis of 24 patients. Rheumatology 2005; 44 : 1542–5.
10. Keogh KA, Ytterberg SR, Fervenza FC, Carlson KA, Schroeder DR, Specks U. Rituximab for refractory Wegener’s granulomatosis: report of a prospective, open-label pilot trial. Am J Respir Crit Care Med. 2006; 173 : 180–7.
11. Roccatello D, Baldovino S, Rossi D, Mansouri M, Naretto C, Gennaro M, et al. Long-term effects of anti-CD20 monoclonal antibody treatment of cryoglobulinaemic glomerulonephritis. Nephrol Dial Transplant 2004; 19 : 3054–61.
12. Jones R, Savage C, Peh CA. Rituximab: A novel remission induction agent in ANCA associated vasculitis. The design of an international, randomised trial (RITUXVAS). J Am Soc Nephrol 2007;18 : 972A.
13. Edwards JC, Szczepanski L, Szechinski J, Filipowicz-Sosnowska A, Emery P, Close DR, et al. Efficacy of B-cell-targeted therapy with rituximab in patients with rheumatoid arthritis. N Engl J Med 2004; 350 : 2572–81.
14. Morgan MD, Harper L, Williams J, Savage C. Anti-neutrophil cytoplasm-associated glomerulonephritis. J Am Soc Nephrol 2006; 17 : 1224–1234.
15. Stasi R, Stipa E, Del Poeta G, Amadori S, Newland AC, Provan D. Long-term observation of patients with anti-neutrophil cytoplasmic antibody-associated vasculitis treated with rituximab. Rheumatology 2006; 45 : 1432–36
16. Aries PM, Hellmich B, Voswinkel J, Both M, Nölle B, Holl-Ulrich K, et al. Lack of efficacy of rituximab in Wegener’s granulomatosis with refractory granulomatous manifestations. Ann Rheum Dis 2006; 65 : 853–58.
17. Lu TY, Ng KP, Cambridge G, Leandro MJ, Edwards JC, Ehrenstein M, et al. A retrospective seven-year analysis of the use of B cell depletion therapy in systemic lupus erythematosus at university college london hospital: The first fifty patients. Arthritis Rheum 2009; 61 : 482–7.
18. A Study to Evaluate the Efficacy and Safety of Rituximab in Patients With Severe Systemic Lupus Erythematosus (EXPLORER) (online). Citováno 13.05.2009. Dostupné z: http://clinicaltrials.gov/ct2/show/NCT00137969.
19. Cohen CD, Calvaresi N, Armelloni S, Schmid H, Henger A, Ott U, et al. CD20-positive infiltrates in human membranous glomerulonephritis. J Nephrol 2005; 18 : 328–333.
20. Bomback AS, Derebail VK, McGregor JG, Kshirsagar AV, Falk RJ, Nachman PH. Rituximab therapy for membranous nephropathy: a systematic review. Clin J Am Soc Nephrol 2009; 4 : 734–44.
21. Remuzzi G, Chiurchiu C, Abbate M, Brusegan V, Bontempelli M, Ruggenenti P. Rituximab for idiopathic membranous nephropathy. Lancet 2002; 360 : 923–924.
22. Ruggenenti P, Chiurchiu C, Brusegan V, Abbate M, Perna A, Filippi C, et al. Rituximab in idiopathic membranous nephropathy: A one-year prospective study. J Am Soc Nephrol 2003; 14 : 1851–1857.
23. Lamprecht P, Lerin-Lozano C, Merz H, Dennin RH, Gause A, Voswinkel J, et al. Rituximab induces remission in refractory HCV associated cryoglobulinaemic vasculitis. Ann Rheum Dis 2003; 62 : 1230–3.
24. Zaja F, De Vita S, Mazzaro C, Sacco S, Damiani D, De Marchi G, et al. Efficacy and safety of rituximab in type II mixed cryoglobulinemia. Blood 2003; 101 : 3827–34.
25. Fakhouri F, Vernant JP, Veyradier A, Wolf M, Kaplanski G, Binaut R, et al. Efficiency of curative and prophylactic treatment with rituximab in ADAMTS13-deficient thrombotic thrombocytopenic purpura: a study of 11 cases. Blood 2005;106 : 1932–7.
Štítky
Dermatológia Detská reumatológia Reumatológia
Článek Vzdělávací akce IPVZ
Článok vyšiel v časopiseČeská revmatologie
Najčítanejšie tento týždeň
2009 Číslo 3- První zkušenosti s léčbou psoriázy bimekizumabem v české reálné praxi – kazuistika z FNUSA
- Na český trh přichází biosimilar adalimumabu s prokázanou terapeutickou ekvivalencí
- Nehoňte nemocné s mMCC od čerta k ďáblu!
-
Všetky články tohto čísla
- Konkomitující fibromyalgie u pacientů s revmatoidní artritidou
- Rituximab v rukou nefrologa – první zkušenosti
- Péče o pacienty se zlomeninou horního konce stehenní kosti. I. Ortopedická péče. Doporučené postupy České revmatologické společnosti a Společnosti pro metabolická onemocnění skeletu
- Bezpečnost biologické léčby – doporučení České revmatologické společnosti
- Současný pohled na etiopatogenezi fibromyalgie
- Vaskulární endotelový růstový faktor u zánětlivých revmatických nemocí
- Akcelerovaná ateroskleróza u systémového lupus erythematodes
- Vzdělávací akce IPVZ
- Informace České revmatologické společnosti ČLS JEP
- VIII. Slapské symposium Měřín
- Česká revmatologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Péče o pacienty se zlomeninou horního konce stehenní kosti. I. Ortopedická péče. Doporučené postupy České revmatologické společnosti a Společnosti pro metabolická onemocnění skeletu
- Vaskulární endotelový růstový faktor u zánětlivých revmatických nemocí
- Konkomitující fibromyalgie u pacientů s revmatoidní artritidou
- Bezpečnost biologické léčby – doporučení České revmatologické společnosti
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



