-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Využití ultrazvuku v diagnostice onemocnění střev
The role of ultrasound in diagnostics of bowel disease
This article summarises the possibilities of ultrasound imaging of the small and large bowel. Bowel ultrasound plays an important role above all in patients with Crohn’s disease, but it could be used in other bowel pathological conditions as well. Due to its non-invasiveness, availability and imaging efficiency, it is a suitable imaging modality both in first line diagnostics and in long-term follow-up in patients with chronic diseases such as IBD. Ultrasound is able to image not only the bowel wall and to separate bowel wall layers, but also the changes in the surroundings tissue or organs such as mesentery, which is able to increase the sensitivity of the method for disease activity assessment. Recently, there has been a tendency to use ultrasound contrast agents, which should allow a more precise assessment of activity of inflammatory processes.
Key words:
imaging methods – ultrasound – diagnostics – follow up – small bowel – large bowel
Autori: D. Bartušek; M. Vavříková; V. Válek; J. Hustý
Pôsobisko autorov: Radiologická klinika FN Brno-Bohunice a LF MU Brno
Vyšlo v časopise: Gastroent Hepatol 2010; 64(4): 18-24
Kategória: IBD: Aktuální přehled
Súhrn
Článek přináší přehled možností využití transabdominální ultrasonografie v zobrazení tenkého i tlustého střeva. Ultrazvuk je v poslední době velice přínosnou metodou nejen u pacientů s Crohnovou chorobou, ale i u ostatních střevních onemocnění. Zvláště pro svou neinvazivnost, dostupnost a výpovědní hodnotu je velice pohotovou metodou jak v první linii diagnostiky, tak i v rámci dlouhodobého sledování pacientů s chronickým onemocněním, jakým je např. Crohnova choroba či ulcerózní kolitida aj. Ultrazvuk umožňuje posoudit nejenom samotnou stěnu střevní a její jednotlivé vrstvy, ale i změny v okolí střeva, např. mesenterium, což zvyšuje senzitivitu metody v posouzení aktivity. V poslední době je snaha o širší využití kontrastních látek při sonografii, což by mělo zpřesňovat a objektivizovat aktivitu zánětlivých procesů.
Klíčová slova:
zobrazovací metody – ultrazvuk – diagnostika – sledování – tenké střevo – tlusté střevoÚvod
Sonografie je v řadě klinických oborů již řadu let hojně využívanou metodou. Zvláště zobrazení dutiny břišní patří neodmyslitelně do racionálního algoritmu vyšetřovacích metod. V dnešní době, i přes prudký technický rozvoj endoskopických metod, je zobrazení tenkého střeva doménou radiologických metod. Stojí tedy na jedné straně enteroskopie a videokapsle a na straně druhé ultrazvuk, konvenční enteroklýza, CT či MR střev. Každá z těchto metod má své výhody, ale i svá omezení, které je třeba zvážit při indikaci jednotlivých vyšetření. Situace v zobrazení tlustého střeva je poněkud odlišná. Kolonoskopie je suverénní metodou v zobrazení a posouzení patologických změn a umožňuje současně provádět biopsii a některé terapeutické zákroky. Při obecných limitacích kolonoskopického vyšetření se zde nabízí i prostor pro zobrazovací metody, jako jsou ultrazvuk, RTG irrigografie, CT či MR irrigografie, včetně speciálních zobrazení v rámci virtuální kolonoskopie.
Technika vyšetření, výhody a limitace sonografie
Ultrazvukové vyšetření tenkého střeva je dnes široce využívané v diagnostice postižení trávicí trubice, především u nemocných s Crohnovou chorobou. Sledování dynamiky procesu a opakované kontroly přitom pacienta nepoškozují radiační zátěží, pacient nemusí být k vyšetření připravován, nemusí lačnět. Ultrazvuk je tedy poměrně levné, rychlé a dnes již plně dostupné vyšetření.
Vyšetřování se provádí transabdominálními sondami. Nízkofrekvenční konvexní sonda s frekvencí cca 3,5–5 MHz slouží k přehlédnutí celé peritoneální dutiny s možností posouzení i parenchymatózních orgánů a malé pánve v jedné době. Detailní posouzení střeva, zvláště posouzení jednotlivých vrstev stěny střevní, okolního mesenteria, včetně lymfatických uzlin, umožňuje vysokofrekvenční lineární sonda s frekvencí 7,5–17 MHz. Samozřejmostí je možnost využití PD-modu (Power Doppler) ke zhodnocení míry a charakteru vaskularizace postižených úseků či zhodnocení průtoku v mesenterických tepnách. Velký rozvoj zaznamenalo v posledních letech i využití kontrastních látek v ultrazvukovém zobrazení, které je výhodné především pro zpřesnění hodnocení aktivity choroby.
Ultrazvuk, podobně jako jiné metody, má však určité limitace, mezi něž patří: určitá subjektivita v hodnocení patologických změn, obtížné vyšetření u obézních pacientů, plynová náplň tlustého střeva, která dovoluje posouzení většinou jen její ventrální stěny. Nevýhodou je i nestandardizovaná obrazová dokumentace. Jedná se o dynamické vyšetření, kdy archivace záznamu vyšetření je sice možná, ale hodnocení druhou osobou, tzv. druhé čtení, které je běžně využíváno u ostatních zobrazovacích metod, zde prakticky není možné. Obtížněji se vyšetřují pacienti po složitějších či opakovaných resekčních výkonech pro atypické anatomické poměry v dutině břišní. U nemocných s atypickým průběhem střeva je topografická orientace a lokalizace patologického postižení rovněž obtížná. Otevřena zůstává otázka senzitivity a specificity vyšetření pro jednotlivé choroby, kde se literární údaje různí.
Zánětlivé postižení střev
Využití ultrazvuku v diagnostice akutní apendicitidy dnes nikoho nepřekvapí. Toto vyšetření je prováděno prakticky na všech pracovištích. Senzitivita ultrazvuku v diagnostice akutní apendicitidy je udávána mezi 80–93 % a specificita dosahuje až 94 %. Ultrazvukem můžeme posoudit jak samotný apendix, jeho délku a uložení, šířku stěny, echogenitu jednotlivých vrstev stěny, vaskularizaci, celkovou šíři apendixu, přítomnost koprolitu aj., ale též změny v okolí, jako je přítomnost volné tekutiny, uzliny, absces, píštěle, periapendikulární infiltrát, posouzení oblasti terminálního ilea a céka. Při absenci zánětlivého postižení apendixu můžeme posoudit i ostatní orgány dutiny břišní, jako jsou žlučové cesty, ledviny, střevní kličky aj. ve snaze o stanovení event. alternativní diagnózy. Za hraniční hodnoty jsou v ultrazvukovém obraze považovány šíře stěny apendixu do 3 mm a celková šíře červa do 7 mm. Pokud je schopen ultrazvuk posoudit takto malou strukturu v dutině břišní, pak posuzování ostatních kliček střevních ultrazvukem se přímo nabízí (obr. 1).
Obr. 1. Akutní apendicitida – zesílení stěny a průsvitu lumen. Fig. 1. Acute appendicitis – thickening of the appendix walls and of the lumen. 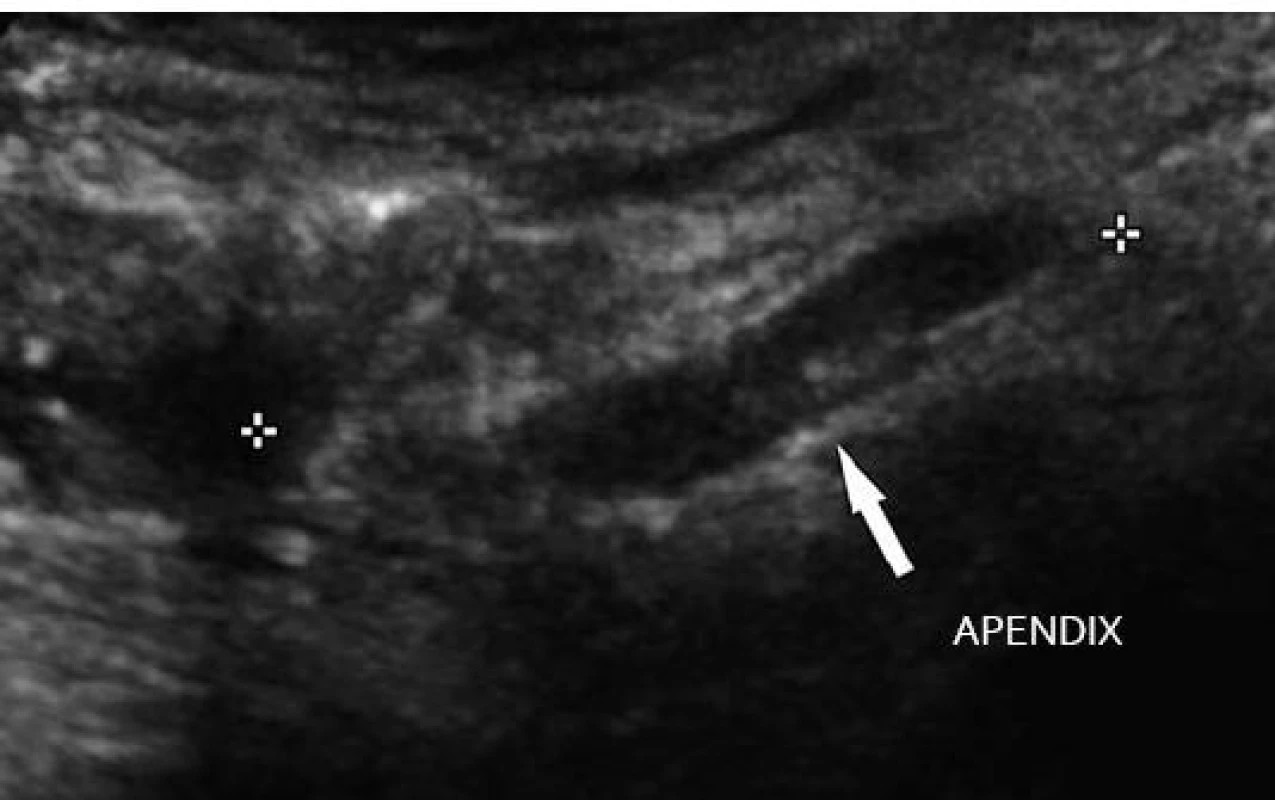
V diagnostice zánětlivých onemocnění střev lze dosáhnout již dnes podobných výsledků a v literatuře uváděná senzitivita ultrazvuku se pohybuje od 67–96 % a specificita od 79–97 %. Toto poněkud širší rozmezí uvedených hodnot lze mimo jiné odůvodnit rozdíly mezi jednotlivými pracovišti, resp. zkušenostmi v diagnostice postižení střev ultrazvukem.
Ultrazvukové vyšetření střev nám umožňuje posoudit:
- stěnu střevní (její celkovou šířku, rozlišení jednotlivých vrstev – zesílení, echogenitu)
- Kerkringovy řasy (tvar, velikost, počet, šířku, uspořádání)
- vaskularizaci stěny střevní (Power Doppler)
- lumen kliček (spasmus, stenózy, charakter stenóz, rigiditu, edém, prestenotickou dilataci)
- vedlejší známky zánětu (hypersekreci a motilitu kliček střevních)
- komplikace (zánětlivý pseudotumor, přítomnost abscesu a píštělí, postižení mesenteria)
- mesenteriální uzliny (velikost, echogenitu, vaskularizaci)
- průtok v arteria mesenterica superior (RI = rezistentní index, maximální rychlosti)
Na jedné straně jsou tedy široké možnosti ultrazvuku, na druhé straně jsou limitace, které je nutné mít na zřeteli. Využití se však přímo nabízí zvláště u idiopatických střevních zánětů, malabsorbčních stavů, také však v diagnostice akutních stavů (divertikulitida, ileózní stavy aj.). Klasifikace změn zachycených při ultrazvukovém vyšetření střev nemocných s Crohnovou chorobou není tak podrobná jako při endoskopickém vyšetření nebo u konvenční enteroklýzy, nicméně možnosti posuzovat echogenitu, šíři střevní stěny a jejích jednotlivých vrstev dává velký prostor diferenciálně diagnostické rozvaze [1]. K tomu přistupuje spektrum obrazů při postižení okolí trávicí trubice (uzliny, mesenterium) a hodnocení prokrvení stěny tenkého střeva. V časné fázi onemocnění Crohnovou chorobou detekujeme hypersekreci a hypermotilitu, zvláště jejunálních kliček patřících k obrazu sekundárních malabsorbčních změn. Samotné postižené úseky mají vzhledem k charakteru zánětu (transmurální) zesílený celý průsvit stěny střevní, především však mukózy a submukózy. Stěna je nehomogenní, hranice jednotlivých vrstev jsou setřelé, v rámci edému (obr. 2). V barevném záznamu (Power Doppler) je patrné překrvení zesílené stěny tenkého střeva. V okolí postiženého úseku střeva a na mesenteriu vidíme zvětšené lymfatické uzliny. Velikost uzlin nepřesahuje obvykle 10 mm.
Obr. 2. Crohn – aktivní zánět v oblasti ilea. Fig. 2. M. Crohn – active inflammation of the ileum. 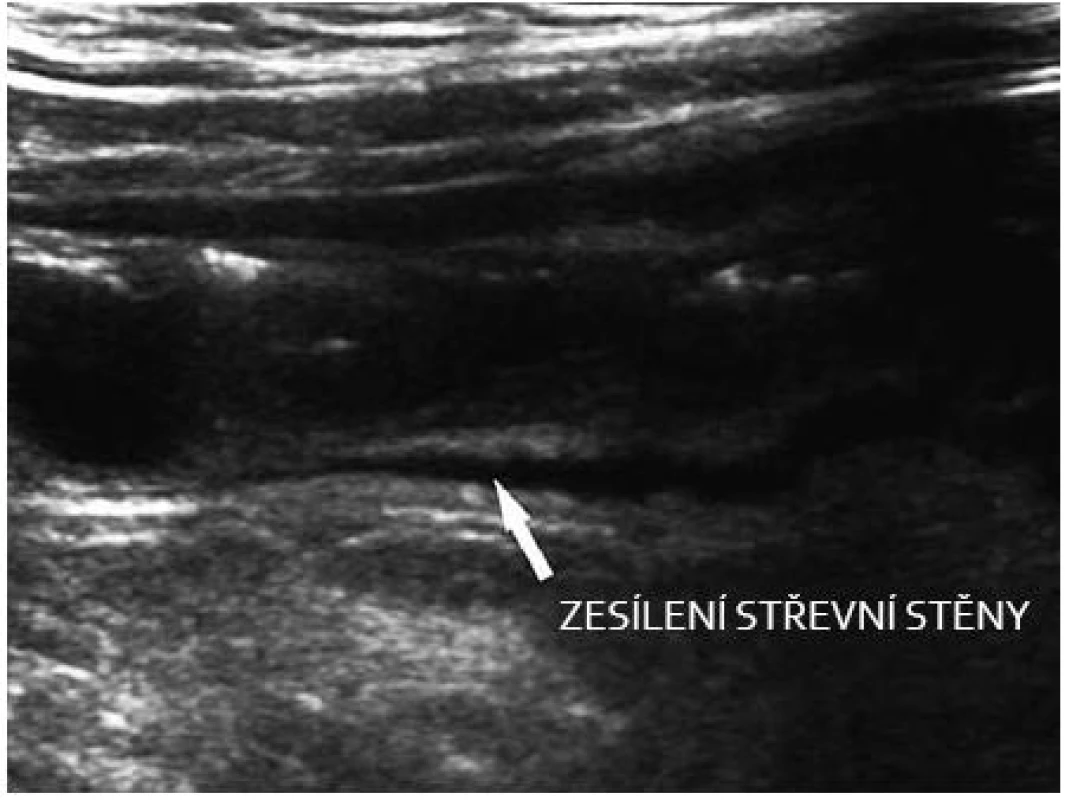
V pokročilé fázi zánětu detekuje sonografie často homogenně hypoechogenní, překrvenou, zesílenou stěnu. Submukóza většinou splývá s mukózou. Stěna může být i hyperechogenní a dokonce mohou být patrné i jednotlivé, dobře ohraničené vrstvy, které mají normální echogenitu. Tento obraz podle našich zkušeností odpovídá "dlaždicovému reliéfu" (což je termín známý a patognomický z dvojkontrastního vyšetření). Ulcerace se však daří zobrazit na rozdíl od zánětlivého, překrveného pseudotumoru jen výjimečně. Na možné ulcerace nepřímo poukazují nerovnosti sliznice a celkové známky zesílené stěny a edému. Průtok v a.mesenterica superior je u akutního zánětu zrychlený a ve srovnání se zdravou populací je výraznější index rezistence. V objektivizaci aktivity zánětu se jeví slibně využití kontrastního ultrazvuku (CEUS).
Významné je posouzení přítomnosti komplikací akutního zánětu, jako jsou píštěle nebo abscesy [2]. Můžeme detekovat jak píštěle do okolního mesenteria, tak pseudotumoru či entero-enterální a entro-kolické píštěle (obr. 3). Zobrazují se jako hypoechogenní pruhy s návazností na lumen kličky a mohou obsahovat i drobné kolekce plynu. Abscesy jsou hypoechogenní formace v okolí postiženého úseku, často v pseudotumoru, a obvykle se k nim táhne vlastní píštěl či je detekována jen desmoplastická reakce v podobě jemných hypoechogenních pruhů [3]. Dle našich zkušeností by při záchytu píštělí či abscesů v rámci komplikací Crohnovy choroby mělo následovat CT vyšetření střev k určení rozsahu samotného postižení střeva a míry komplikací s možností intervence pod CT kontrolou (punkce, drenáž).
Obr. 3. Crohn, komplikace – suprapubický absces, aktivní zánětlivé postižení ilea a sigmoidea, entero sigmoideální fistulace. Fig. 3. M. Crohn, complications – suprapubic abscess, acute inflammation of the ileum and sigmoid, entero-sigmoid fistulation. 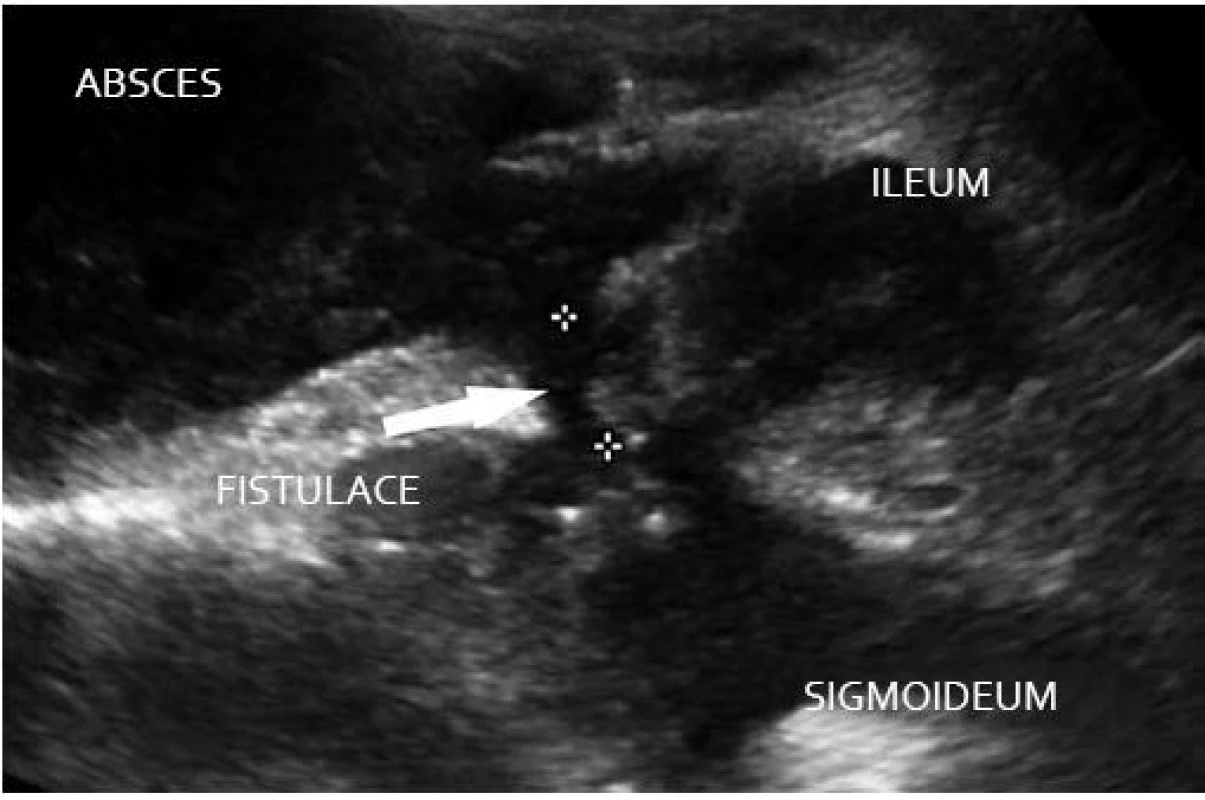
V chronické fázi onemocnění, zvláště pokud v akutní fázi byl zánět i v okolí postiženého segmentu, můžeme detekovat obraz pseudotumoru. S postupující fibrózou se zvyšuje echogenita střevní stěny. Zesílená je především submukóza. Prokrvení střevní stěny je minimální (obr. 4). Zobrazit můžeme i atrofii sliznice, vazivovou stenózu a prestenotickou dilataci.
Obr. 4. M. Crohn – chronické změny v oblasti ileocaeka. Fig. 4. M. Crohn – chronic changes in the ileo-caecal region. 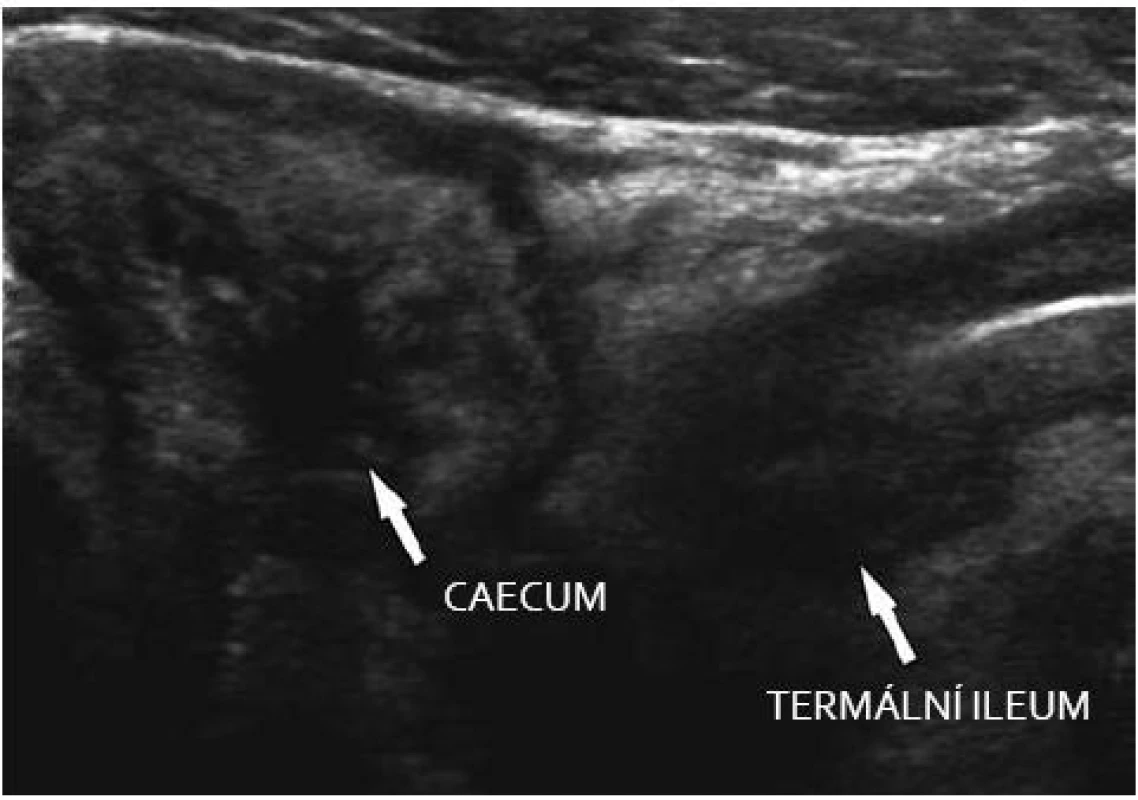
U funkční stenózy je při ultrazvukovém vyšetření zesílená především mukóza a muscularis propria. Komprese stěny je možná a peristaltika po uvolnění komprese postiženým úsekem střeva prochází. Stěna střevní je často překrvená. U fibrózní stenózy je střevní stěna málo prokrvená a většinou hyperechogenní. Zřejmá je prestenotická dilatace a komprese lumen není možná. Peristaltika postiženým úsekem tenkého střeva neprochází. Obtížné je detekovat krátké, cirkulární stenózy, často v podobě skip lézí orálních úseků tenkého střeva, kdy mnohdy detekujeme segmentální dilatace, ale samotný postižený úsek není jednoznačný. Zde je dále prostor pro některou z forem enteroklýzy či enteroskopie.
V posouzení rigidity stenóz je ultrazvuk velice vhodnou metodou. Protože se jedná o dynamické vyšetření, postižený úsek můžeme nejenom komprimovat, ale i sledovat v peristaltické vlně, a tím se vyjádřit o elasticitě stěny střevní.
Výhodnou modifikací v posuzování charakteru stenóz je metoda sono enteroklýzy. Při aplikaci kontrastní látky nasojejunální sondou (metylcelulóza) dochází k optimální distenzi kliček. Dobře je patrná hranice mukóza/lumen a lepší posouzení elasticity či rigidity postiženého úseku. Sono enteroklýza má vyšší senzitivitu, ale stejnou specificitu jako nativní ultrazvukové vyšetření, a může tedy být jeho doplňkovou metodou.
Celiakie
Ultrazvukové vyšetření střev u pacientů s celiakální sprue je prozatím nedoceněnou metodou. Diagnostika celiakie se opírá především o stanovení protilátek a enterobiopsii.
S ultrazvukovým obrazem malabsorbce se u pacientů s dyspeptickými obtížemi můžeme setkat poměrně často. Při vyloučení sekundárních příčin malabsorbce a při typickém ultrazvukovém obraze je nutné uvažovat o primární formě malabsorbce [4]. Vyšetření ultrazvukem lze provádět opakovaně, nevyžaduje zvláštní přípravu a nezatěžuje pacienta, lze tak porovnávat výsledky vyšetření před stanovením diagnózy a následně také efekt bezlepkové diety na morfologické změny střeva.
Vzhledem k různým formám celiakie je i ultrazvukový obraz přítomných změn velice různorodý. Je třeba si též uvědomit, že se jedná o velice dynamické onemocnění. V typickém případě se setkáváme s obrazem úbytku řas v orální části tenkého střeva, tzv. „kolonizace jejuna“, vedoucí někdy až k úplnému vyhlazení řas, atrofii (obr. 5). Naopak zmnožené řasy nacházíme v aborální části tenkého střeva, tzv. „jejunizace ilea“ (obr. 6). Navíc jsou tyto řasy nepravidelné a zesílené. Velmi častý je obraz dysmotility, chaotické peristaltiky tenkého střeva, vystupňované až do obrazu intermitentních invaginací (obr. 7), které mohou být v klinickém obraze zodpovědné za kolikovité bolesti břicha v okolí pupku [5]. Ultrazvuk, jako dynamické vyšetření, je v diagnostice tohoto funkčního příznaku suverénní metodou. Dále je sledovatelná hypersekrece ve střevě podmíněná špatnou vstřebávací schopností střeva. Pro celiakii je typická přítomnost zvětšených, ovoidních a hyperechogenních mesenteriálních uzlin. S přítomností typických mesenteriálních uzlin se setkáváme i u pacientů v klidovém stavu, tedy s dobře kompenzovanou celiakií (obr. 8). Často u pacientů, kde je celiakie diagnostikována v pozdějším věku, detekujeme zmenšenou slezinu, která zřejmě souvisí s funkčním hyposplenismem popisovaným u autoimunních chorob. Benefitem užití sonografie v iniciální fázi vyšetřování je i možnost „vyloučení“ jiných příčin obtíží, např. IBD aj. Ultrazvukové vyšetření nenahrazuje enterobiopsii. Je to však metoda velice vhodná v iniciálních fázích diagnostiky „střevních, resp. zažívacích obtíží“. Na základě jejího výsledku může být již v počátku nastaven další racionální diagnostický algoritmus (endoskopie horní části trávicího ústrojí, enteroskopie, biopsie, kolonoskopie aj.).
Obr. 5. Celiakiální sprue – atrofie řas jejuna – „kolonizace jejuna“ – úbytek a ztluštění řas. Fig. 5. Celiac sprue – villous atrophy – „jejunal colonization” – the loss and thickening of villi. 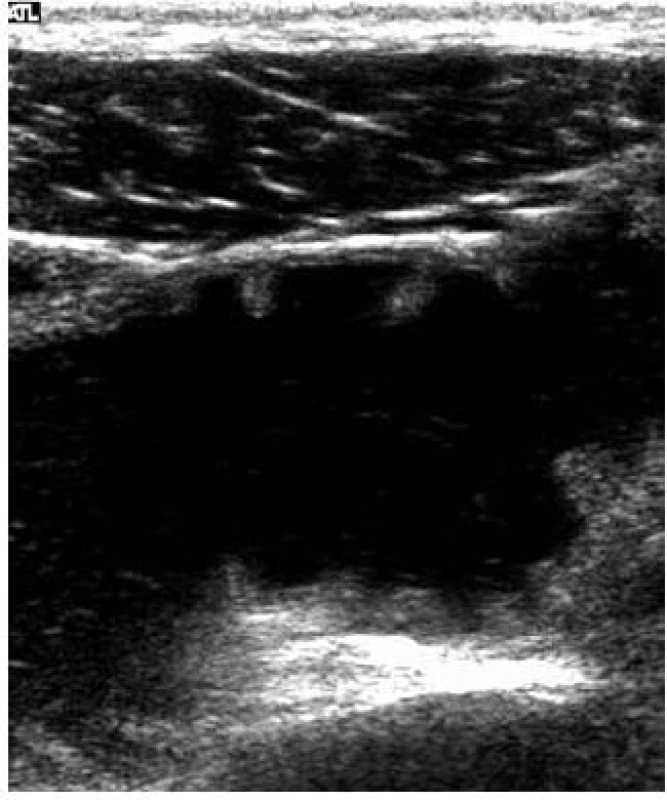
Obr. 6. Celiakální sprue – zmnožení řas na ileu – „jejunizace ilea“. Fig. 6. Celiac sprue – plethora of villi on the ileum – „jejunization of the ileum”. 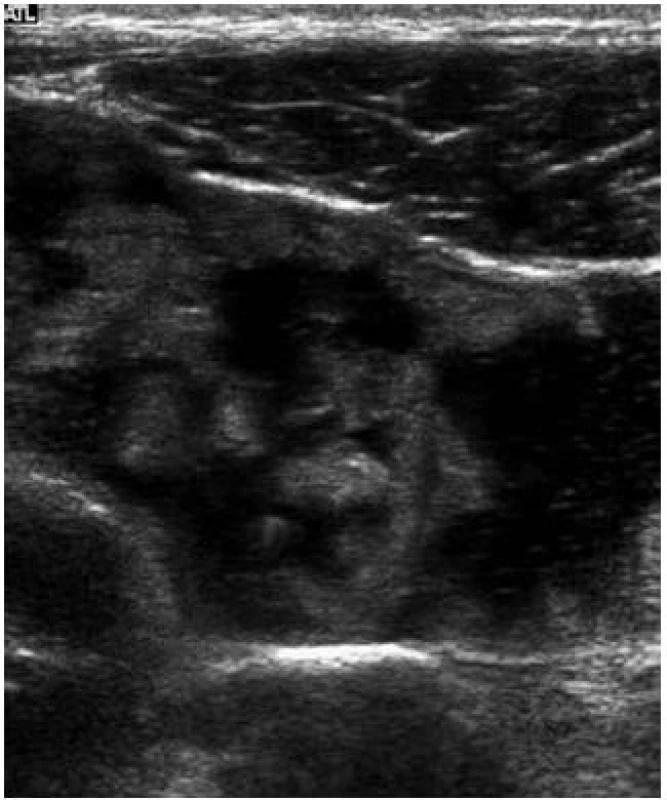
Obr. 7. Celiakální sprue – intermitentní invaginace. Fig. 7. Celiac sprue – intermittent invagination. 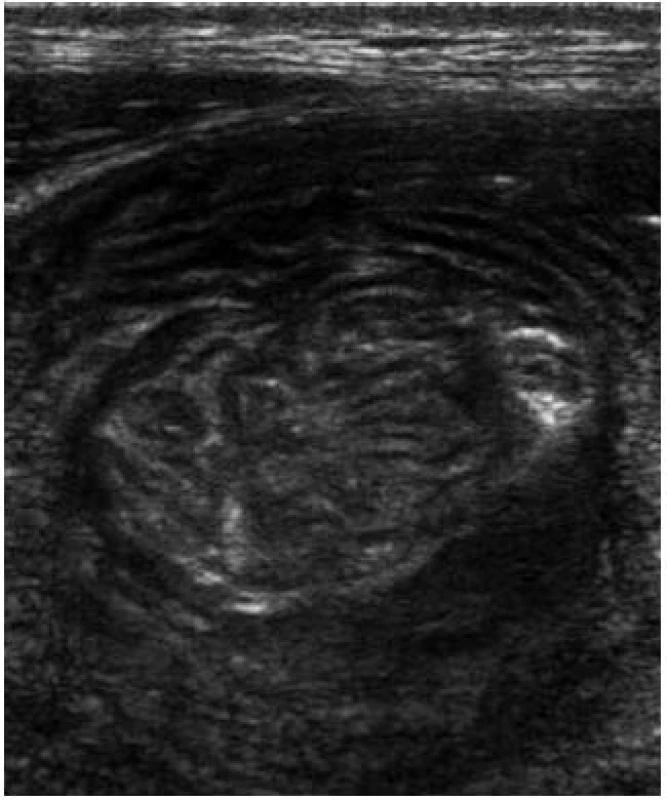
Obr. 8. Celiakální sprue – mesenteriální lymfadenopatie. Fig. 8. Celiac sprue – mesenterial lymphadenopathy. 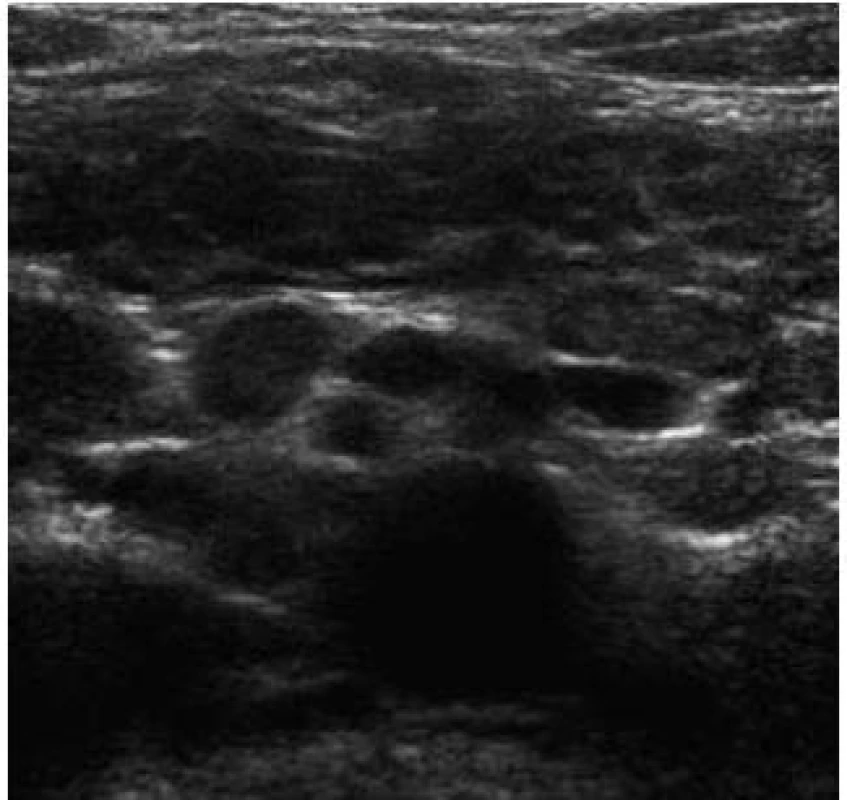
Tumory tenkého střeva
Nádorová postižení tenkého střeva diagnostikuje ultrazvuk většinou náhodně, v rámci sledování pacientů s Crohnovou chorobou či celiakií (adenokarcinom, lymfom), či u akutních pacientů s poruchami pasáže (leiomyom aj.). Poměrně typický obraz má karcinoid v podobě hypoechogenní submukózní léze, která je vaskularizovaná. Často vidíme i hypervaskularizované metastázy karcinoidu jater. U onkologických pacientů se můžeme setkat s metastázami na tenkých kličkách. U hematogenních metastáz detekujeme excentricky uložené hypoechogenní až cystické ložisko, kdy stěna střevní je zesílená jen v místě metastázy, tedy semicirkulárně. Ložisko je zvýšeně prokrvené. Obecně jsou metastázy tenkého střeva častější než primární nádory tenkého střeva (obr. 9).
Obr. 9. Nádorové postižení tenkého střeva – metastáza adenokarcinomu caeka na kličce ilea. Fig. 9. Small intestine tumour – metastatic adenocarcinoma of the caecum on the ileum loop. 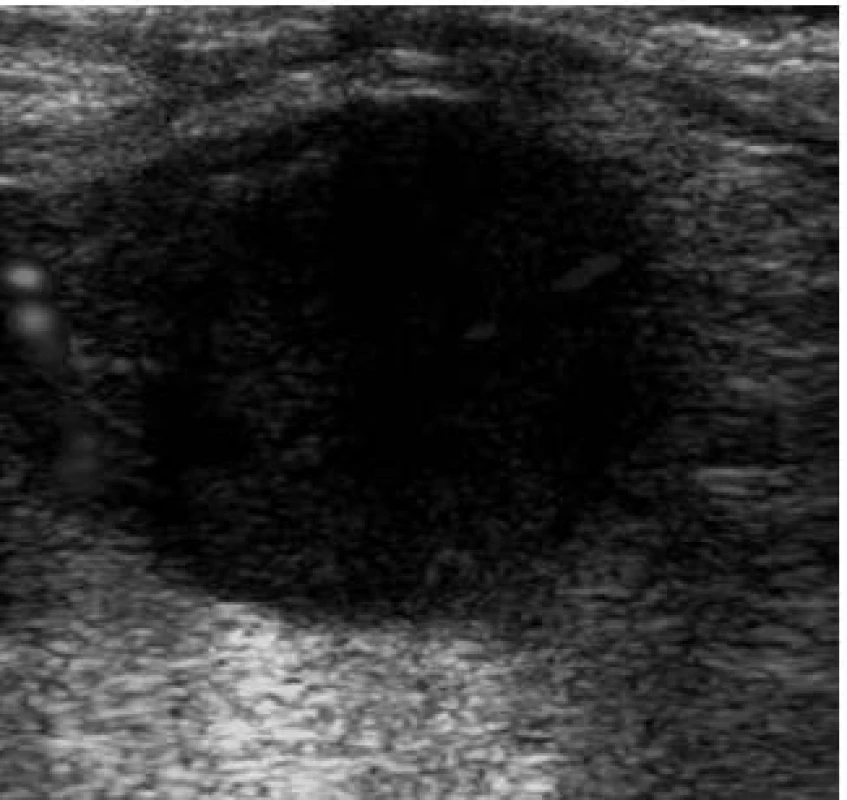
Tlusté střevo
Na rozdíl od tenkého střeva je vzhledem k možnostem endoskopie situace v diagnostice postižení tlustého střeva poněkud odlišná. Nicméně i zde se širokou měrou uplatňují zobrazovací metody. Zvláště výhodnou metodou je pak využití ultrazvuku v diagnostice a sledování pacientů s postižením tlustého střeva u Crohnovy choroby tračníku i ulcerózní kolitidy. Stanovení rozsahu a charakteru změn, posouzení aktivity a komplikací je výhodné nejen v iniciálním stadiu vyšetřování, ale i při dlouhodobém sledování [6]. Sonografická kritéria patologických změn na tlustém střevě jsou prakticky obdobná jako na střevě tenkém (zesílení stěny, charakter jednotlivých vrstev stěny střevní, vaskularizace, změny okolí atd.) (obr. 10).
Obr. 10. M. Crohn – postižení tlustého střeva v oblasti lienální flexury s aktivitou, fistulacemi a zánětlivým pseudotumorem v okolí. Fig. 10. M. Crohn – large intestine involvement in the lienal flexure with activity, fistulation and inflammatory pseudotumour in the surroundings. 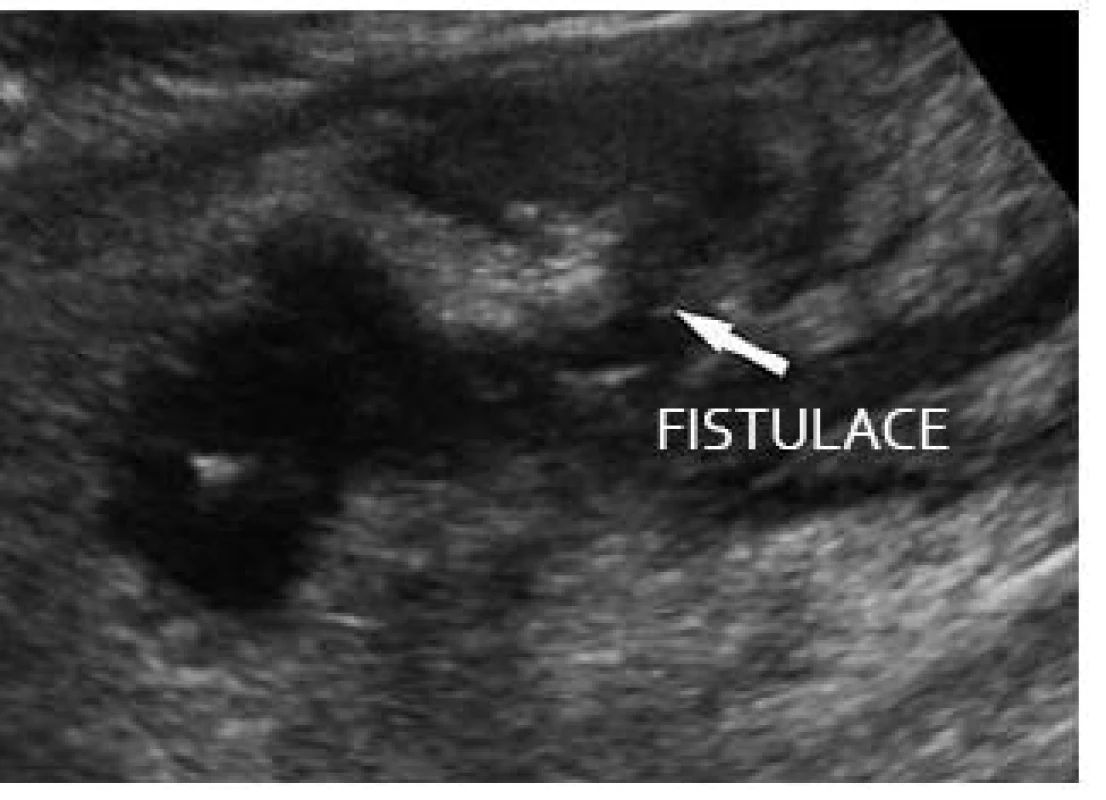
V poslední době se setkáváme se zvýšeným počtem pacientů se zánětlivým postižením tlustého střeva po léčbě širokospektrými antibiotiky. Roste počet onemocnění vyvolaných C. difficile (CDAD). V posledních letech stoupá nejen incidence, ale i závažnost onemocnění. Jedná se zvláště o starší pacienty, polymorbidní a imunokompromitované. U těchto pacientů je většinou kolonoskopie velice zatěžujícím vyšetřením. Ultrazvuk je metodou velice vhodnou k posouzení rozsahu a charakteru změn, a zvláště pak ke sledování těchto pacientů (obr. 11). Selhání léčby v některých případech vede až k rozsáhlým chirurgickým výkonům s celkově těžkým průběhem.
Obr. 11. CDAC – aktivní pankolitida s výrazným edémem stěny. Fig. 11. CDAC – active pancolitis with distinctive wall oedema. 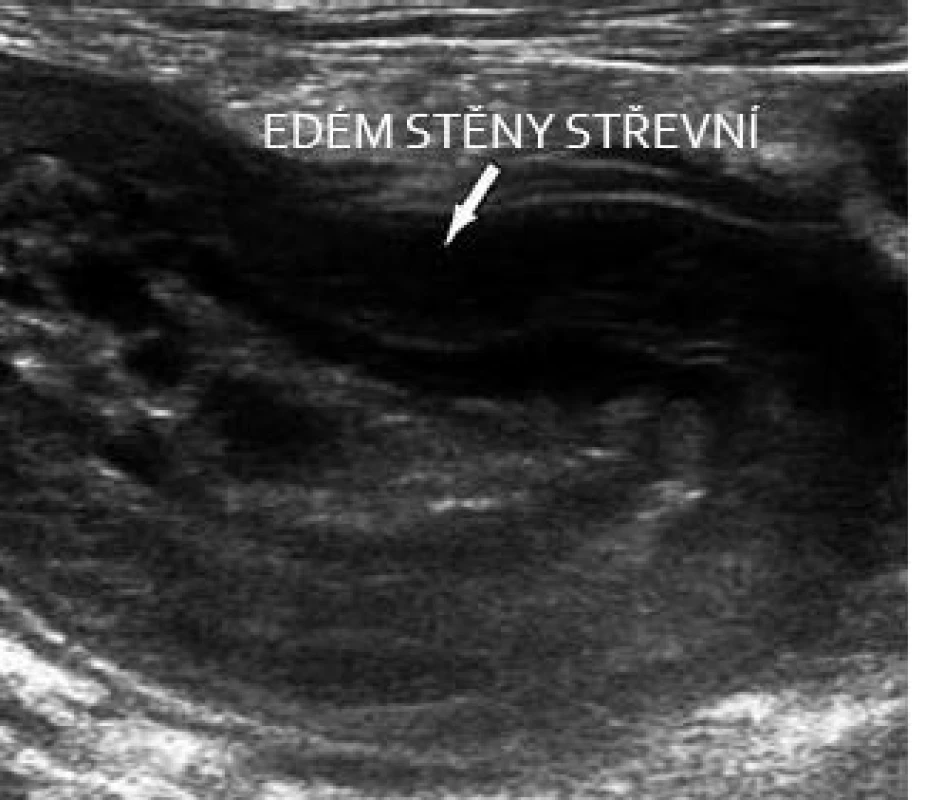
Velký význam a citlivost má sonografie v diagnostice divertikulitidy (obr. 12). Při klinickém podezření je ultrazvukové vyšetření v tomto akutním stavu pro klinika nesmírně cenné. Ultrazvukem je možné určit rozsah změn a komplikací (divertikly, zesílení stěny, edém, prosáknutí okolí, píštěle, kolekce, abscesy) (obr. 13). Neinvazivnost vyšetření a možnost sledování dalšího vývoje jsou velkým potenciálem ultrazvuku. Při větším rozsahu změn či limitacích ultrazvuku je metodou volby CT vyšetření s možností intervenčního výkonu (punkce, drenáž).
Obr. 12. Divertikulitida sigmoidea. Fig. 12. Sigmoid diverticulitis. 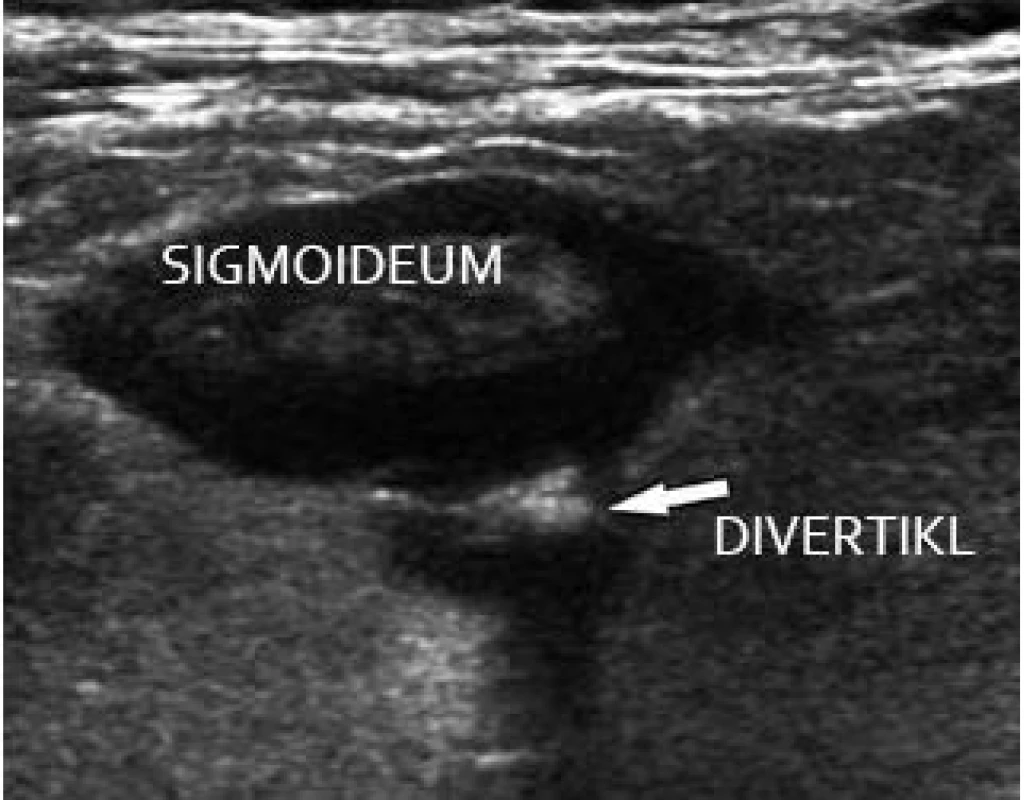
Obr. 13. Komplikace divertikulitidy – mezikličkový absces. Fig. 13. Complications of diverticulitis – interloop abscess. 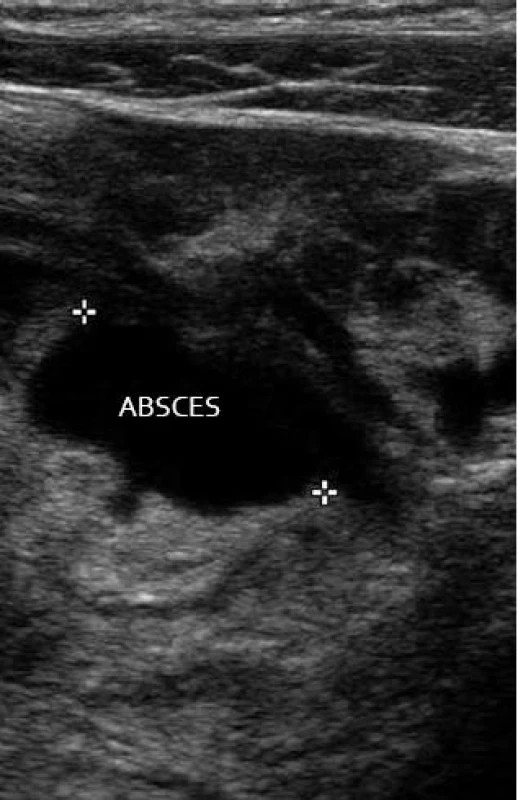
S maligními tumory tlustého střeva se většinou setkáváme až v pokročilejších stadiích či jako náhodný nález, obvykle již při hmatné rezistenci. Ultrazvuk následně detekuje cirkulární infiltraci stěny tlustého střeva (hypoechogenita, zesílená stěna s destrukcí jednotlivých vrstev, zvýšená vaskularizace). Avšak hodnocení oblasti rekta do 20 cm distálního úseku tlustého střeva není transabdominálním ultrazvukem možné. Tuto oblast je možné posoudit pouze konvexní, nízkofrekvenční sondou, která však neumožňuje detailní posouzení stěny střevní. Lze tak detekovat jen těžké aktivní záněty či velké tumory, a to ještě jen při příznivých akustických poměrech v malé pánvi. Malá pánev je však doménou rektoskopie, endosonografie či MR vyšetření.
CEUS střev (Contrast enhanced ultrasound, ultrazvukové vyšetření střev s aplikací kontrastní látky nitrožilně)
V poslední době zaznamenává tato vyšetřovací metoda poměrně velký rozmach. Uplatňuje se nejen při vyšetření solidních ložiskových lézí jater či ledvin, ale také u vyšetření malých útvarů, jako jsou lymfatické uzliny či právě střevní kličky. Jde o miniinvazivní, relativně levnou a rychlou metodu, která pacienta nijak nezatěžuje.
Principiálně je technika založena na metodě tzv. pulzní inverze, kdy při potlačení základní frekvence zůstávají pouze frekvence harmonické. Bubliny kontrastní látky rezonují s ultrazvukovými vlnami, při srážce ultrazvukové vlny s mikrobublinou plynu dochází k nelineární oscilaci, a tím pádem k produkci vyšších harmonických frekvencí.
Využívá se vhodných kontrastních látek, které jsou schopny zobrazit mikrocirkulaci a nepronikají do extravaskulárního řečiště, nemetabolizují se. Tyto vlastnosti splňuje např. kontrastní látka SonoVue firmy Bracco. Částice plynu jsou menší než plicní kapiláry (1–10 μm), a tudíž schopné proniknout i do levostranného řečiště, kde přežívají až 10 min. Nosičem bublin je v tomto případě sulfur hexafluorid, mikrobubliny jsou stabilizovány kapsulou tvořenou perfluorokarbony [7].
Vyšetření vyžaduje kvalitní ultrazvukový přístroj dovolující specifické kontrastní zobrazení. Důležité je také nastavení nízkého mechanického indexu („low MI imaging“), protože toto působí protektivně vůči destrukci mikrobublin. Při vyšetření střev by měl být index nižší než 0,1. Vyšetřujeme lineárními sondami o frekvencích 9 a 12 MHz, v závislosti na použité sondě aplikujeme také množství kontrastní látky. V případě 9 MHz sondy je to 1,5–2,5 ml, u 12 MHz sondy až 4 ml kontrastní látky intravenózně. Výhodou je, že s odstupem několika minut lze kontrastní látku po manuálním rozbití mikrobublin v oběhu použít u téhož pacienta znovu, třeba na jiném patologicky změněném úseku střeva. Po aplikaci kontrastní látky sledujeme při duálním zobrazení sycení postiženého úseku střeva. V pravé polovině displeje máme nativní obraz v ultrazvukovém B modu, kde si můžeme v průběhu vyšetření ověřovat polohu na postižené oblasti, na levé straně displeje je obraz postkontrastní [8]. Jde o dynamické vyšetření, během něhož pořizujeme videozáznam, který je potřeba poté odeslat do počítače s vyhodnocovacím softwarem (např. Qlab). Zde probíhá tzv. postprocessing, jímž získáváme křivku sycení patognomickou pro danou patologii.
Tuto metodu lze s úspěchem využít u pacientů s nespecifickými střevními záněty, jako je Crohnova choroba a ulcerózní kolitida. Díky ní můžeme odlišit zánět aktivní od chronického. Nabízí se také využití u tumorózních expanzí, infiltrátů či abscesových formací.
U aktivního zánětu dochází k sycení celého průsvitu stěny střevní v časné arteriální fázi a později k postupnému vymývání z okrajů. Při chronických změnách se zpravidla sytí celý průsvit stěny. U pokročilých fibrózních změn se sytí nejprve zevní části stěny a periviscerální cévy a poté celý průsvit stěny. Abscesová formace obsahuje hypoechogenní až anechogenní nesytící se centrální areu a intenzivně se sytí její stěna. U zánětlivých rezistencí a infiltrátů se výrazně sytí vnitřní část a periferně měkké tkáně.
Ultrazvukové vyšetření střev s kontrastní látkou zvyšuje jednoznačně senzitivitu v detekci střevních zánětů u zesílené střevní stěny a umožňuje podobně jako vyšetření počítačovou tomografií (CT) či magnetickou rezonancí (MR) posoudit sycení střevní stěny. Je tedy přínosné v managementu pacientů s Crohnovou chorobou, zejména při monitoraci klinického průběhu a hodnocení odezvy na terapii.
Závěr
Ultrazvukové vyšetření střev je vzhledem ke své neinvazivnosti a výše uvedeným možnostem velice perspektivní metodou pro diagnostiku a zejména sledování pacientů.
V rukou zkušeného sonografisty může být důležitým nástrojem vedoucím k redukci počtu jiných, náročnějších, zejména radiací zatěžujících vyšetření. Ultrazvuk je dostačující v případě některých diagnóz a často již jen vyslovení podezření na určitou patologii určuje následný racionální algoritmus vyšetřovacích metod. Proto by sonografie měla být metodou první volby u pacientů s podezřením na střevní patologii a standardně by měla být využívána ke sledování pacientů s Crohnovou chorobou, kde má své výsadní postavení.
Jsou určité limitace, pro které ultrazvuk samozřejmě nemůže ve specifických indikacích nahradit ostatní zobrazovací (CT či MR) nebo endoskopické metody. Další možnosti jeho využití se otevírají zvláště v kombinaci s využitím kontrastních látek především u nespecifických střevních zánětů.
MUDr. Daniel Bartušek, Ph.D.
Radiologická klinika FN Brno-Bohunice a LF MU Brno Jihlavská 20, 634 00 Brno
d.bartusek@seznam.cz
Zdroje
1. Válek V. Tenké střevo, radiologicko-patologické stavy. Brno 2003.
2. Maconi G, Sampietro GM, Satani A et al. Bowel ultrasound in Crohn's disease: surgical perspective. Int J Colorectal Dis 2008; 23(4): 339–347.
3. Tarján Z, Tóth G, Györke T et al. Ultrasound in Crohn's disease of the small bowel. Eur J Radiol 2000; 35(3): 176–182.
4. Castiglione R, Rispo A, Cozzolino A et al. Bowel sonography in adult celiac disease: diagnostic accuracy and ultrasonographic features. Abdom Imaging 2007; 32(1): 73–77.
5. Rettenbacher T, Hollerweger A, Macheiner P et al. Adult Celiac Disease: US Signs. Radiology 1999; 211(2): 389–394.
6. Parente F, Greco S, Molteni M et al. Modern imaging of Crohn's disease using bowel ultrasound, Inflamm Bowel Dis 2004; 10(4): 452–461.
7. Serra C, Menozzi G, Labate AM. Ultrasound assessment of vascularization of the thickened terminal ileum wall in Crohn's disease patients using a low-mechanical index real-time scanning technique with a second generation ultrasound contrast agent. Eur J Radiol 2008; 65(2): 242–243.
8. Schreyer AG, Finkenzeller T, Gössmann H et al. Microcirculation and perfusion with contrast enhanced ultrasound (CEUS) in Crohn's disease: first results with linear contrast harmonic imaging (CHI). Clin Hemorheol Microcirc 2008; 40(2): 143–155.
Štítky
Detská gastroenterológia Gastroenterológia a hepatológia Chirurgia všeobecná
Článek Zpráva o CEURGEM 2010
Článok vyšiel v časopiseGastroenterologie a hepatologie
Najčítanejšie tento týždeň
2010 Číslo 4- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Když se ve střevech děje něco nepatřičného...
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- V 21. století budeme bez zácpy(Zácpa je syndrom nízkého serotoninu)
- Využití ultrazvuku v diagnostice onemocnění střev
- Riziko kombinace klopidogrelu s inhibitory protonové pumpy – význam a možnosti řešení
- Nevyšetřená dyspepsie – nový pojem, užitečný termín?
- Zpráva o CEURGEM 2010
- České a Slovenské endoskopické dny, Praha, 24.–25. 6. 2010
- Petr Anděl. Manuál transanální endoskopické mikrochirurgie. Praha: Galén 2010. 90 stran
- Eosinofilní gastroenteritida jako vzácná příčina ascitu
- Gastroenterologie a hepatologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Využití ultrazvuku v diagnostice onemocnění střev
- Riziko kombinace klopidogrelu s inhibitory protonové pumpy – význam a možnosti řešení
- Eosinofilní gastroenteritida jako vzácná příčina ascitu
- V 21. století budeme bez zácpy(Zácpa je syndrom nízkého serotoninu)
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



