-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Anderson-Fabryho choroba a postižení gastrointestinálního traktu
Anderson-Fabry disease and gastrointestinal tract involvement
Anderson-Fabry disease (AFD) is a relatively rare X-linked hereditary storage disorder, caused by mutation of the gene for α-galaktosidase A (α-Gal A). Low or even zero level activity of the enzyme α-Gal A caused accumulation of glycosphingolipids in lysosomes. This lysosomal storage causes cell dysfunction and subsequent organ malfunction. AFD patients suffer from renal, cardiac, vessel and neurological symptoms, last but not least from skin and gastrointestinal involvement. Enzyme replacement therapy has been shown effective, with earlier diagnosis resulting in better outcomes in patients with AFD.
Keywords:
Anderson-Fabry disease – lysosomal storage – diarrhoea – Electron microscopy
Autori: Dostálová G. 1; Roblová L. 1; Reková P. 2; Rob D. 1; Marek J. 1; Kodet O. 3; Dubská Z. 4; Linhart A. 1
Pôsobisko autorov: II. interní klinika – klinika kardiologie a angiologie 1. LF UK a VFN, Praha 1; Neurologická klinika 1. LF UK a VFN v Praze 2; Dermatovenerologická klinika 1. LF UK a VFN v Praze 3; Oční klinika 1. LF UK a VFN v Praze 4
Vyšlo v časopise: Gastroent Hepatol 2020; 74(2): 158-162
Kategória: Vybrané kapitoly z vnitřního lékařství: kazuistika
doi: https://doi.org/10.14735/amgh2020158Súhrn
Anderson-Fabryho choroba (AFD – Anderson-Fabry disease) je dědičné, na X-chromozom vázané onemocnění, jehož podkladem je mutace genu kódujícího enzym α-galaktosidázu A (α-Gal A). Nulová anebo nízká enzymová aktivita α-Gal A vede ke kumulaci glykosfingolipidů v lyzozomech a následné dysfunkci na orgánové úrovni. Pacienti s AFD mají kombinaci postižení ledvin, srdce, cév, neurologických obtíží a dále projevů postižení trávicího traktu a kůže. Správná diagnostika AFD umožní zahájit časnou specifickou terapii, která může onemocnění zastavit anebo alespoň výrazně zpomalit.
Klíčová slova:
Anderson-Fabryho choroba – lyzozomální střádání – průjmovitá stolice – elektronová mikroskopie
Úvod
Anderson-Fabryho choroba (AFD – Anderson-Fabry disease; OMIM 301500) nebo také jen Fabryho choroba je dědičné, na X chromozom vázané onemocnění patřící do skupiny vzácných chorob. Jedná se o progresivní metabolické onemocnění ze skupiny sfingolipidóz, charakterizované akumulací neutrálních glykosfingolipidů (zejména globotriaosylceramidu Gb3, ale i dalších izoforem Gb3 metabolitů) intralyzozomálně. Podkladem je mutace v GLA genu kódujícím enzym α-galaktosidázu A (α-Gal A). Snížená nebo až nulová aktivita enzymu α-Gal A, který za normálního stavu Gb3 degraduje, vede k akumulaci právě glykosfingolipidů v různých tkáních organizmu, a tím k progredujícímu multiorgánovému postižení a následným symptomům postižených pacientů [1,2]. Klinicky závažné a život zkracující je především postižení ledvin, s postupnou progresí proteinurie a renální insuficience až do stadia renálního selhání s nutností dialýzy a/ nebo transplantace. Závažná jsou postižení myokardu, projevující se hypertrofickou kardiomyopatií, velmi často i s obstrukcí výtokového traktu levé komory a arytmiemi, ústící do implantace kardiostimulátoru a defibrilátoru. Třetím, neméně závažným je postižení centrálního nervového systému s časnými a opakujícími se tranzitorními ischemickými atakami a cévními mozkovými příhodami v poměrně časném věku (od 20. roku věku u mužů, u žen o 5–10 let později).
Prevalence AFD je ve světě udávaná v rozmezí 1 : 40 000–1 : 60 000 [3]. V ČR máme v Centru pro Fabryho chorobu ve sledování přes 200 pacientů. V rizikových populacích pro AFD jsou prováděna nejrůznější screeningová vyšetření (dialyzovaní pacienti bez bioptické verifikace selhání ledvin, mladí pacienti s časnou cévní mozkovou příhodou, pacienti s hypertrofií levé komory), v těchto vyhledávacích studiích je výskyt AFD mezi 0,3 a 1 % z vyšetřené populace. AFD byla popsána roku 1898 téměř současně dokonce dvěma autory ve dvou zemích, v Německu dermatologem Johannesem Fabrym a v Anglii chirurgem William Andersonem [4,5]. Jako první popsali u mladých pacientů postižení kůže typické, a právě pro AFD, angiokeratomy kůže a postižení termoregulační funkce kůže s hypo - až anhidrózou.
Dalším přidruženým příznakem, výrazně snižujícím kvalitu života, je i postižení smyslových orgánů jako např. vestibulokochleárního aparátu. Pacienti mají porušenou stabilitu, vertigo komplikující chůzi, zhoršení sluchu s nutností nošení naslouchátek apod. [2]. S postupným střádáním i ve tkáních střeva dochází k poruchám pasáže jak ve smyslu průjmovitých stolic, tak zácpy. Časté jsou bolesti břicha bez vazby na specifické jídlo nebo dietní opatření.
Onemocnění se může manifestovat ve velmi širokém věkovém rozmezí od raného dětství až po pozdní dospělost a tíže fenotypu často koreluje s charakteristickými mutacemi [2,6]. Škála postižení je ale různá i u nemocných se stejnou mutací v GLA genu, i v jedné rodině mohou být pacienti s AFD s rozdílnou manifestací (jako příklad může sloužit rodina sledovaná v našem Centru pro Fabryho nemoc, kdy jeden z nemocných bratrů má zejména postižení kardiální – hypertrofická kardiomyopatie s těžkou obstrukcí výtokového traktu levé komory, druhý bratr je kvůli selhání ledvin závislý již ve věku 35 let na dialýze a následně absolvoval transplantaci ledviny; vlastní zkušenost autora).
Protože se jedná o onemocnění vázané na X chromozom, Fabryho nemoc rozdílnou klinickou manifestaci u mužů a u žen. U žen nastupují stejné symptomy a orgánová postižení průměrně o 5–10 let později než u mužů. Nicméně kvůli fenoménu lyonizace neboli X inaktivace, kdy se v každé jaderné buňce jeden z páru chromozomu inaktivuje, nejsou výjimkou i ženy zcela asymptomatické (pokud je inaktivován postižený X chromozom a funkční zůstává zdravý X bez GLA mutace) anebo mohou být postiženy dívky a ženy stejně jako muži vzhledem k inaktivaci X chromozomu bez GLA mutace (pak je jediným aktivním X chromozomem právě ten s GLA mutací, a tedy nedostatečnou produkcí enzymu α-Gal A).
Prvním příznakem již v dětství, kolem 5.–10. roku u chlapců a 15. roku u dívek, je postižení kůže. Objevují se a postupně přibývají drobné kožní léze, tzv. angiokeratomy (angiokeratoma corporis diffusum) (obr. 1a a 1b). Angiokeratomy jsou benigní vaskulární kožní léze charakterizované dilatací cév v papilární dermis. Rozložení angiokeratomů je symetrické okolo pupku, postranních partií břicha, dále pak typicky v tříslech a v oblasti genitálu. Další časnou známkou je porucha termoregulační funkce kůže, většina pacientů se velmi málo potí nebo se u nich dokonce objeví anhidróza. Pacienti pak zpětně udávají, že měli v dětství velmi časté subfebrilie, horečky (mezi 37 a 38 °C), kvůli kterým byli velmi často vyšetřováni, bez jasného nálezu. Zvýšenou tělesnou teplotu navíc vyprovokovala fyzická námaha, sport, tělocvik ve škole, v některých případech dokonce i pouhý stres ve škole.
Obr. 1. a. Angiokeratomy kůže u pacienta s Anderson-Fabryho chorobou.
Fig. 1.a. Angiokeratomas of the skin in a patient with Anderson-Fabry disease.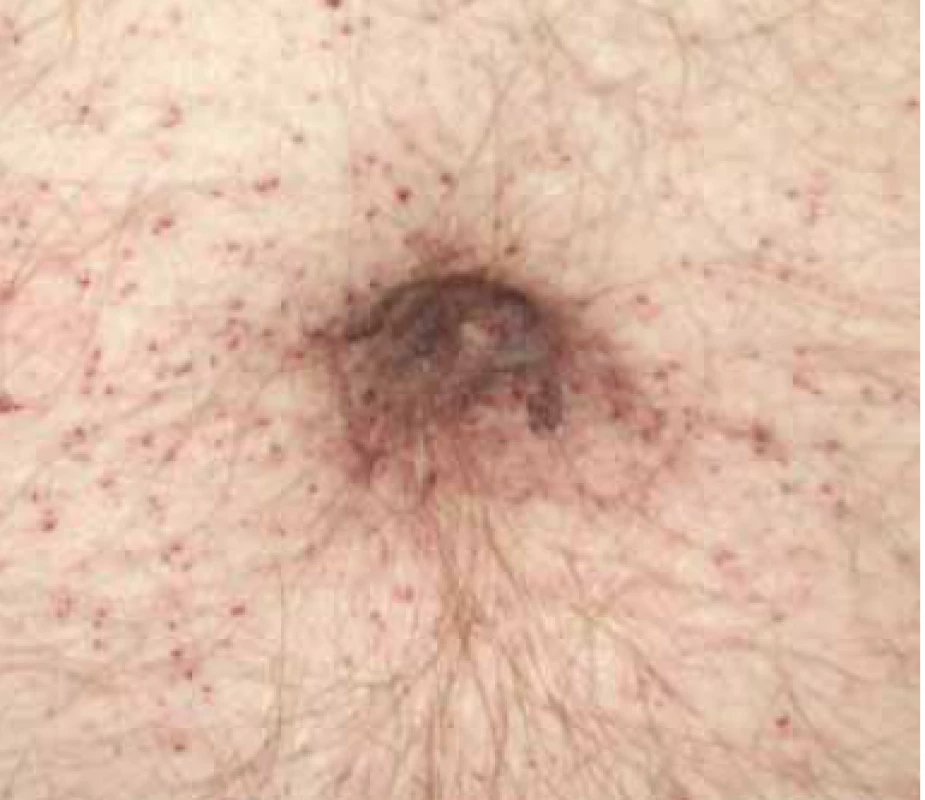
Obr. 1.b. Angiokeratomy mohou být i ojedinělé, jako v tomto případě.
Fig. 1.b. Angiokeratomas can be isolated, as in this case.
Puberta u chlapců je období prvních známek postižení ledvin, objevuje se mikroalbuminurie nebo i proteinurie a postupně se snižuje glomerulární filtrace. Muži, v případě nerozpoznané AFD, bez zahájené terapie, dospějí s klasickými projevy onemocnění k dialýze a/ nebo transplantaci mezi 25. a 40. rokem věku, ženy o 10 let později. U obou pohlaví se objevují bolesti hlavy, tranzitorní ischemické ataky nebo i cévní mozkové příhody v časném věku, kolem 25–50 let. Rovněž se v tomto období projeví i postižení myokardu. Na EKG je typické zkrácení PQ intervalu pod 120 ms (obr. 2), obraz hypertrofie levé komory se zatížením na EKG křivce je následně potvrzen echokardiografickým vyšetřením. Arytmie typické pro AFD jsou AV blokády vyššího stupně s nutností implantace kardiostimulátoru, komorové arytmie jako nesetrvalé komorové běhy nebo fibrilace komor jsou indikací k implantaci kardioverter-defibrilátoru.
Obr. 2. EKG křivka u pacienta s Anderson-Fabryho chorobou – nález hypertrofické kardiomyopatie, zkráceného PQ intervalu < 120 ms, známky hypertrofie a zatížení levé komory (voltáž QRS komplexů a změny ST úseků).
Fig. 2. ECG curve in an Anderson-Fabry disease patient with hypertrophic cardiomyopathy, shortened PQ interval < 120 ms, signs of hypertrophy and left ventricular load (QRS complex voltage and changes in ST segments).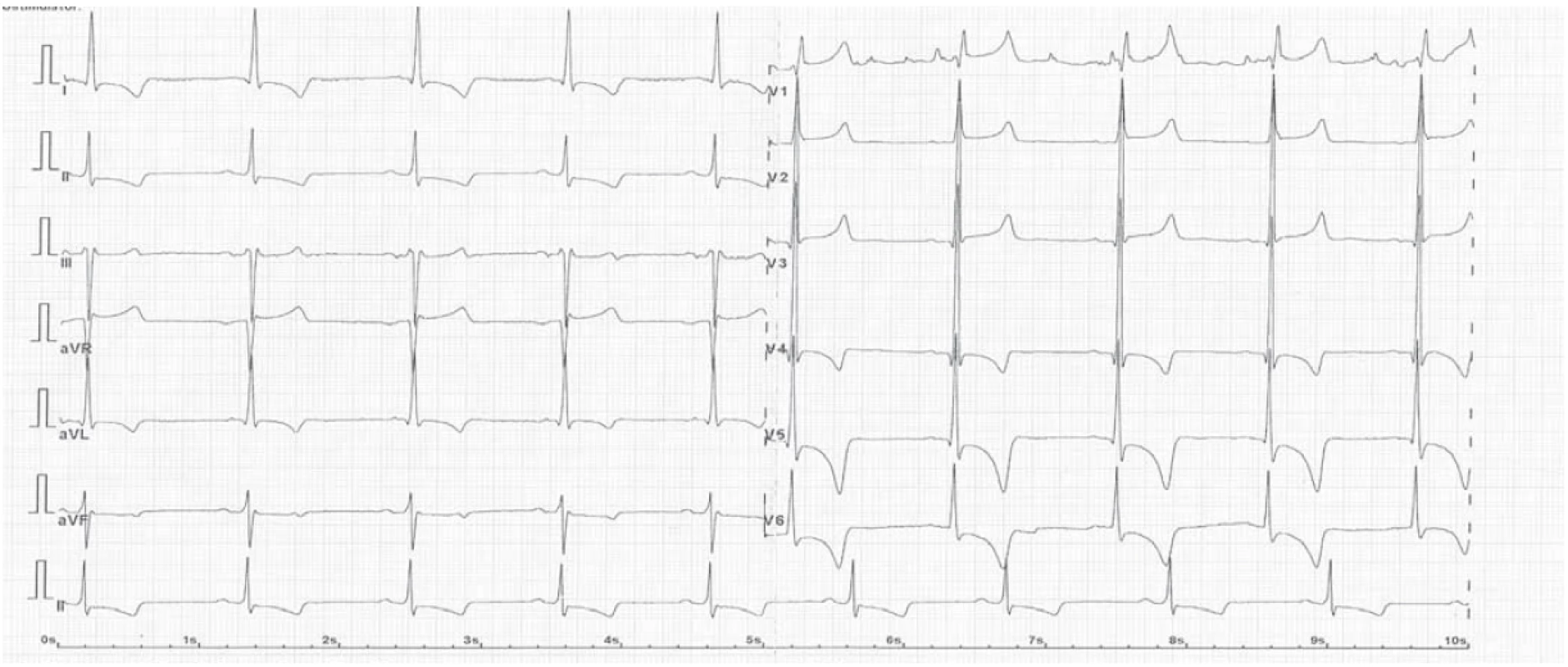
Téměř dvě třetiny pacientů udávají gastrointestinální obtíže. První symptomy zaznamenávají již od dětství a puberty. Velmi často jsou pro neprospívání a opakované průjmovité stolice (průměrně 3–5 stolic denně) vyšetřováni praktickými lékaři. Někteří jsou následně vyšetřeni i v ambulanci gastroenterologů, vč. fibroskopických vyšetření (gastrofibroskopie, koloskopie), která ale neprokáží žádnou obstrukci či jinou významnou patologii patrnou při pohledu na střevní stěnu. Nicméně v případě provedení biopsie mohou histopatologické nálezy navést na správnou diagnózu, pokud se na základě projasnění a vakuolizace cytoplazmy, bez známek zánětlivé celulizace nebo ložisek nekrózy doplní elektronová mikroskopie. Nález na elektronovém mikroskopu pak popíše velmi typické četné myelinové figury charakteristického vzhledu s koncentrickou lamelací. Inkluze jsou obklopeny jednoduchou membránou identifikující jejich lyzozomální původ (obr. 3).
Obr. 3. Elektronová mikroskopie – nález střádání v lysozomech, obraz typický pro Anderson-Fabryho chorobu, „zebra like bodies”. (Fotografie prof. Elleder, Ústav dědičných metabolických poruch 1. LF UK, Praha.)
Fig. 3. Electron microscopy – finding of accumulation in lysosomes, image typical for Anderson-Fabry disease, „zebra like bodies“. (Photo Prof. Elleder, Institute of Inherited Metabolic Disorders, 1st Faculty of Medicine, Charles University, Prague.)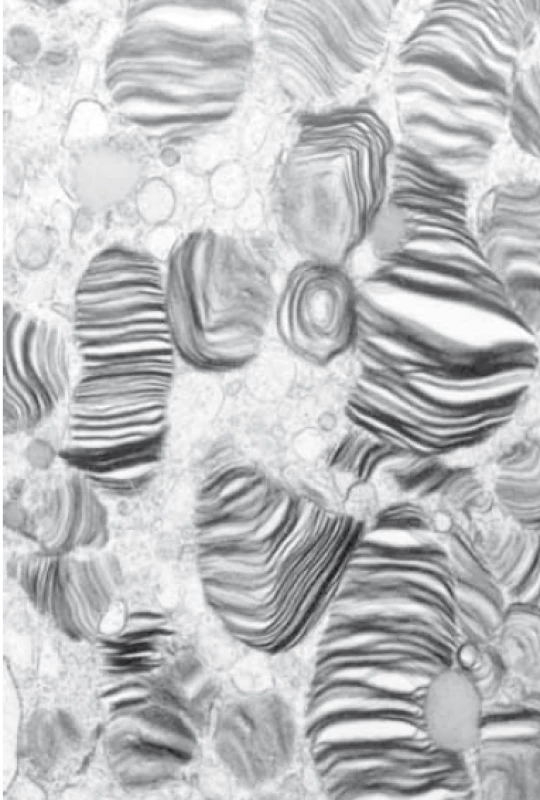
Stanovení správné diagnózy co nejčasněji je od roku 2004, od kdy je k dispozici specifická enzym-substituční terapie, velmi důležité, s obrovským dopadem na další rozvoj anebo zpomalení onemocnění, a tím i na prognózu pacienta. K dispozici jsou nyní v ČR dva intravenózně podávané léky (infuze léku pravidelně každých 14 dní) a jeden perorální preparát charakteru chaperonové léčby u nemocných, kteří jsou schopni v buňkách enzym vyrobit, ale problémem je jeho stabilita nebo prostorové uspořádání pro správnou funkci. Chaperon pak stabilizuje a umožní správnou funkci vlastního enzymu pacienta. Všechny tyto léky jsou plně hrazeny z prostředků veřejného zdravotního pojištění. V rámci studií a výzkumu budeme mít nejspíše další terapeutické možnosti (další typ infuzně podávaných léků, genové terapie apod.).
Kazuistika
Muž, narozen 1974, byl přijat pro těžké deprese na psychiatrickou kliniku. Během přijímacího rozhovoru byla zjištěna a zapsána anamnestická data pacienta týkající se nejen jeho psychiatrické diagnózy, ale i interních a dalších komorbidit.
V dětství prodělal běžné dětské infekční choroby, bez komplikací. Nicméně byl opakovaně hospitalizován na dětském oddělení a infekční klinice pro horečky nejasné etiologie. Tehdy byl vyšetřen ortopedem, revmatologem pro „růstové bolesti ve dne“ a při zátěži se objevující pálení dlaní, chodidel (akroparestetické bolesti), přehřívání se a výraznou fyzickou únavu i po malé fyzické aktivitě. Bolesti svalů a kloubů během teplotních špiček. Tehdy byl i poprvé vyšetřen psychiatrem, nález pacient nezná.
V období puberty trvají bolesti konečků prstů, zejména po námaze, při horečkách, stresu. Poprvé se objevuje depresivní ladění, bez intervence, bez medikace. Během preventivní prohlídky u pediatra poprvé zachycena proteinurie, další kontrola moči již bez významné přítomnosti bílkoviny v moči. Častější stolice, průměrně 3–4 denně, bez příměsi krve či hlenu. Dle pacienta „byl nejhubenější ve třídě“.
Studium vysoké školy bez psychiatrického sledování. Při preventivní kontrole opět záchyt proteinurie. Vyšetřen očním lékařem pro cizí předmět v oku, doporučeno další oční vyšetření pro časný zákal, kataraktu. Nebylo pacientem doplněno.
Po dokončení vysoké školy, mezi 25. a 42. rokem, opakovaně vyšetřen gastroenterology pro zažívací obtíže (průjmovitá stolice, bez příměsi 3–5× denně, hubnutí, nechutenství). Po opakovaném koloskopickém vyšetření uzavřeno jako suspektní dráždivý tračník, doporučena dietní opatření. Biopsie provedena nebyla. Ve 27 letech přechodně – několik hodin trvající porucha řeči, s následnou výraznou bolestí hlavy a únavou.
Od cca 35 let věku postupný rozvoj závislosti na alkoholu, progredující depresivní syndrom.
Ve 42 letech přijat k hospitalizaci na psychiatrické klinice a zvážení dalšího postupu. Konziliární vyšetření vedené psychiatrem doporučilo doplnit další vyšetření, zejména k vyšetření možného postižení ledvin a periferního nervového systému. Následně v rámci diferenciální diagnostiky otázka možného postižení u lyzozomální střádavé choroby, a to typu AFD. Doplněna vyšetření, v tab. 1 přehledně uvedeny nálezy u pacienta. Obtíže ORL nebo plicní se u tohoto pacienta nevyskytovaly.
Tab. 1. Souhrn postižených orgánů a symptomů pacienta.
Tab. 1. Summary of affected organs and symptoms.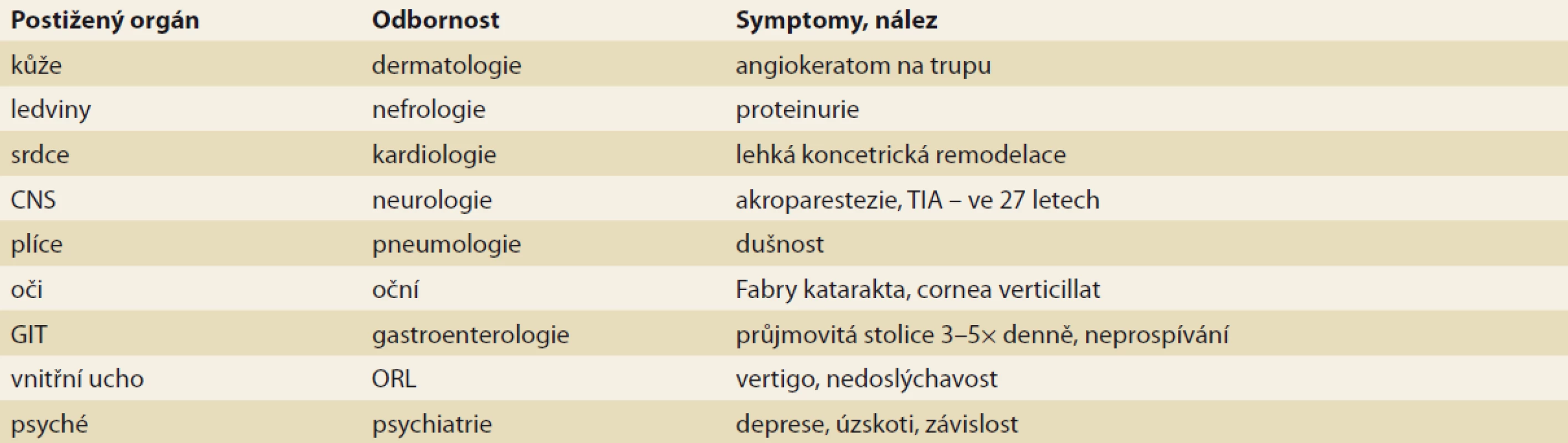
CNS – centrální nervový systém, GIT – gastrointestinální trakt, ORL – ortorhinolaryngologie, TIA – transitorní ischemická ataka Po vysvětlení a podpisu informovaného souhlasu byl pacientovi odebrán krevní vzorek a odeslán k vyšetření hladiny enzymu α-galaktosidázy. Vyšetření potvrdilo výrazně sníženou hladinu a bylo doplněno vyšetření genetické, které prokázalo patogenní mutaci v GLA genu c. (868A/ G), p. (Met290Val).
U pacienta byla zahájena enzym substituční terapie podávaná 1× za 14 dní intravenózní infuzí. Po více než ročním podávání došlo ke zlepšení symptomů a stabilizaci renálních funkcí. Zlepšila se i psychika pacienta, abstinuje.
Závěr
V kazuistice jsme popsali případ pacienta, u něhož byla správná diagnóza stanovena cca 36 let od prvních obtíží a klinických projevů AFD. Byl opakovaně vyšetřován pro jednotlivé symptomy mnoha odborníky (neurologie, oční, gastroenterologie, praktický lékař atd.). Rozpoznání, že tyto symptomy a orgánová postižení spolu může spojovat jediná diagnóza, např. lyzozomální střádavé onemocnění typu AFD, je klíčové. Následně je totiž možné zahájit specifickou terapii, která výrazně ovlivňuje nejen jednotlivé obtíže a symptomy pacienta, ale i jeho prognózu.
Časná diferenciální diagnostika v rámci postižení gastrointestinálního traktu u pacienta s dalšími interními diagnózami v relativně mladém věku může být učiněna právě gastroenterology. Bioptické vyšetření vč. doplnění elektronové mikroskopie by v takovém případě mělo být součástí komplexního vyšetření. Následné vyšetření hladiny α-Gal A a genetické vyšetření je možné doplnit přímo v gastroenterologické ambulanci (kity pro vyšetření lze zaslat poštou na pracoviště a následně opět poštou odeslat k vyšetření do laboratoře, objednání kitů je možné cestou Centra pro Fabryho nemoc, Praha).
Doručeno/ Submitted: 30. 3. 2020
Přijato/ Accepted: 1. 4 2020
MUDr. Gabriela Dostálová, Ph.D.
Centrum pro Fabryho chorobu
II. interní klinika – klinika kardiologie a angiologie 1. LF UK a VFN Praha
Karlovo náměstí 32
128 08 Praha 2
Konflikt zájmů: Autoři deklarují, že text článku odpovídá etickým standardům, byla dodržena anonymita pacientů a prohlašují, že v souvislosti s předmětem článku nemají finanční, poradenské ani jiné komerční zájmy.
Publikační etika: Příspěvek nebyl dosud publikován ani není v současnosti zaslán do jiného časopisu pro posouzení. Autoři souhlasí s uveřejněním svého jména a e-mailového kontaktu v publikovaném textu. Obr. 1 publikován se souhlasem pacienta.
Dedikace: Článek není podpořen grantem ani nevznikl za podpory žádné společnosti.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Conflict of Interest: The authors declare that the article/manuscript complies with ethical standards, patient anonymity has been respected, and they state that they have no financial, advisory or other commercial interests in relation to the subject matter.
Publication Ethics: This article/manuscript has not been published or is currently being submitted for another review. The authors agree to publish their name and e-mail in the published article/manuscript. Fig. 1 published with patient consent.
Dedication: The article/manuscript is not supported by a grant nor has it been created with the support of any company.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Zdroje
1. Mehta A, Ricci R, Widmer U et al. Fabry disease defined: baseline clinical manifestations of 366 patients in the Fabry Outcome Survey. Eur J Clin Invest 2004; 34(3): 236–242. doi: 10.1111/ j.1365-2362.2004.01309.x.
2. Meikle PJ, Hopwood JJ, Clauge AE et al. Prevalence of lysosomal storage disorders. JAMA 1999; 281(3): 249–254. doi: 10.1001/ jama.281.3.249.
3. Anderson W. A case of „angio-keratoma“. Br J Dermatol 1898; 10(4): 113–117.
4. Fabry J. Ein Beitrag zur Kenntnis der Purpura haemorrhagica nodularis (Purpura papulosa haemorrhagica Hebra). Arch Dermatol Syphilol (Berlin) 1898; 43 : 187–201.
5. Hopkin RJ, Bissler J, Banikazemi M et al. Characterization of Fabry disease in 352 pediatric patients in the Fabry Registry. Pediatr Res 2008; 64(5): 550–555. doi: 10.1203/ PDR.0b013e318183f132.
6. Kanda A, Nakao S, Tsuyama S et al. Fabry disease: ultrastructural lectin histochemical analyses of lysosomal deposits. Virchows Arch 2000; 436(1): 36–42. doi: 10.1007/ pl00008196.
Štítky
Detská gastroenterológia Gastroenterológia a hepatológia Chirurgia všeobecná
Článok vyšiel v časopiseGastroenterologie a hepatologie
Najčítanejšie tento týždeň
2020 Číslo 2- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
-
Všetky články tohto čísla
- Covid-19 a játra
- Editorial
- Doporučený postup České hepatologické společnosti ČLS JEP pro diagnostiku a léčbu nealkoholové tukové choroby jater
- Infection in patients hospitalised with advanced chronic liver disease (cirrhosis) – single-centre experience
- De novo non-alcoholic fatty liver disease after liver transplantation – as diagnosed by magnetic resonance
- Doporučení pro léčbu idiopatických střevních zánětů v době pandemie covid-19
- Odporúčania slovenskej Pracovnej skupiny pre IBD pri SGS pre liečbu biosimilárnymi anti-TNF biologikami u dospelých a detských pacientov
- Endoskopická drenáž infikované ohraničené pankreatické nekrózy s komplikovaným průběhem – kazuistika
- Čtyřleté zkušenosti s monitorováním farmakokinetiky infliximabu a adalimumabu u pacientů s idiopatickými střevními záněty
- Vedolizumab v léčbě Crohnovy choroby ve světle nových poznatků
- Laserová litotripse zaklíněného biliárního konkrementu v tlustém střevě
- Anderson-Fabryho choroba a postižení gastrointestinálního traktu
- Gastroenterologie a gastrointestinální endoskopie v podmínkách pandemie viru SARS-CoV-2
- Devadesátiny doc. MU Dr. Miloše Sedláčkové, CSc.
- Životní jubileum As. MU Dr. Hany Dvořákové, CSc.
- Komentář k článku: Caha M, Politová P, Vlk R et al. Překvapivá příčina úmrtí pacienta s krvácením do horního trávicího traktu. Gastroent Hepatol 2020; 74(1): 50–53. doi: 10.14735/ amgh202050.
-
Novel Pancreatic Developmentsprof. Peter Layer – Gastro Update Europe 2019, Budapest
Nové poznatky o pankreatu -
Biliopancreatic endoscopy
prof. Marco Bruno – Gastro Update Europe 2019, Budapest - Novel Developments In Intestinal Endoscopy<br> prof. Oliver Pech – Gastro Update Europe 2019, Budapest
- Výběr z mezinárodních časopisů
- Kreditovaný autodidaktický test
- Gastroenterologie a hepatologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Covid-19 a játra
- Endoskopická drenáž infikované ohraničené pankreatické nekrózy s komplikovaným průběhem – kazuistika
- Doporučený postup České hepatologické společnosti ČLS JEP pro diagnostiku a léčbu nealkoholové tukové choroby jater
- Doporučení pro léčbu idiopatických střevních zánětů v době pandemie covid-19
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



