-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Zhodnocení účinnosti extrakorporální litotrypse elektromagnetického generátoru EMSE 140f Dornier Compact Sigma a stanovení efektivní energetické dávky
Assessment of the efficacy of extracorporeal shock wave lithotripsy using a EMSE 140f Dornier Compact Sigma electromagnetic generator, and determination of the effective energy dose
Aim:
The aim of this study was to present the initial results of extracorporeal shock wave lithotripsy (ESWL) using a new mobile lithotripter machine – Dornier Compact Sigma, assess its electromagnetic generator efficacy, and determine the mean energy dose applied.Methods:
Efficacy of ESWL treatment with the use of the new mobile lithotripter machine Dornier Compact Sigma was prospectively assessed in the first 50 patients treated with the device from December 2012 to February 2013. Procedures were performed under analgosedation. Size of the stones was recorded before each procedure. Total energy dose was applied on the basis of the standardized protocol which was determined in advance, using the recommended dose range provided by the manufacturer of the lithotripter. The procedure was prematurely terminated in cases of early stone disintegration visualized using fluoroscopy. Success rate of stone disintegration, stone free rate (SFR), efficacy quotient (EQ) and mean applied energy dose (Edose) were evaluated.Results:
Native nephrogram and ultrasound were performed three months after the procedure to assess the treatment results. The primary effect of stone disintegration and SFR was achieved in 87.0% and 78.0% of the patients respectively. An auxiliary procedure was subsequently performed in 6 patients. The EQ was determined to be 61.6%, the mean energy dose applied during the LERV procedure was 70.4 J. Subcapsular renal hematoma complication was recorded in one patient.Conclusion:
Initial results of the LERV procedure in our group demonstrated high efficacy of the EMSE 140f generator with the EQ reaching 61.6%. The mean energy dose (Edose) applied in cases of nephrolithiasis and ureterolithiasis was 73.2 J and 58.0 J respectively. In conclusion, a lower mean effective energy dose proved to be sufficient in our study group when comparing our results to the current data in the lite-rature.Key words:
extracorporeal shock wave lithotripsy, disintegration, stone free rate, energy dose, efficacy quotient.
Autoři: Vít Paldus 1; Vladimír Šámal 1,2; Jan Mečl 1; Jiří Pírek 1
Působiště autorů: Urologické oddělení Krajské nemocnice Liberec, a. s. 1; Urologická klinika Fakultní nemocnice a Lékařské fakulty UK, Hradec Králové 2
Vyšlo v časopise: Ces Urol 2014; 18(4): 316-323
Kategorie: Původní práce
Souhrn
Cíl:
Cílem práce je prezentace prvních výsledků litotrypse extrakorporální rázovou vlnou (LERV) pomocí nového mobilního přístroje Dornier Compact Sigma, zhodnocení účinnosti jeho elektromagnetického zdroje EMSE 140f a stanovení průměrně aplikované energetické dávky.Metodika:
V období od prosince 2012 do února 2013 jsme prospektivně zhodnotili účinnost LERV u prvních 50 pacientů. Výkony jsme provedli v analgosedaci pomocí nového mobilního litotryptoru Dornier Compact Sigma. Před každým výkonem jsme zaznamenali velikost litiázy, celkovou energetickou dávku jsme aplikovali na základě předem určeného schématu, kdy podkladem pro dané aplikační schéma bylo doporučené dávkovací rozmezí dodané výrobcem litotryptoru. V případě časné dezintegrace patrné na skiaskopii jsme výkon předčasně ukončili. V souboru jsme následně hodnotili úspěšnost dezintegrace, stone free rate (SFR), koeficient účinnosti (EQ) a průměrně aplikovanou energetickou dávku (Edose).Výsledky:
Hodnocení v daném souboru jsme provedli za 3 měsíce od zákroku pomocí nativního nefrogramu a sonograficky. Primárního efektu dezintegrace litiázy jsme dosáhli u 87,0 % pacientů, SFR jsme zaznamenali u 78,0 % pacientů a auxiliární procedura byla následně provedena u šesti pacientů. Na základě daných výsledků jsme určili EQ 61,6 % a navíc jsme stanovili průměrnou energetickou dávku 70,4 J aplikovanou během LERV. U jednoho pacienta po výkonu vznikl subkapsulární hematom ledviny.Závěr:
Iniciální výsledky LERV v našem souboru prokázali vysokou efektivitu generátoru EMSE 140f, kdy EQ dosahuje v našem souboru 61,6 %. Průměrně užitá energetická dávka Edose byla pro nefrolitiázu 73,2 J a pro ureterolitiázu 58,0 J. Souhrnně jsme prokázali nižší průměrnou potřebu efektivní energetické dávky Edose v porovnání s literárně dostupnými údaji.Klíčová slova:
litotrypse extrakorporální rázovou vlnou, dezintegrace, stone free rate, energetická dávka, koeficient účinnosti.ÚVOD
Litotrypse extrakorporální rázovou vlnou (LERV) je neinvazivní metoda léčby urolitiázy využívající fyzikálních vlastností rázové vlny. První záznamy účinku rázové vlny pochází z období 2. světové války, kdy byla u utonulých námořníků při pitvě pozorována poškození plic a to v souvislosti s podmořskou explozí. Dalšího zájmu se rázové vlně dostalo až v osmdesátých letech 20. století, kdy německá firma Dornier ve spolupráci s mnichovskými urology dokončila vývoj prvního litotryptoru. První sdělení o nové úspěšné metodě bylo následně publikováno v časopisu Lancet (1). Z hlediska fyzikálních vlastností je rázová vlna akustickou vlnou a je charakterizována vysokou energií, tlakem, variabilní frekvencí a na rozdíl od běžné akustické vlny se šíří nelineárně. V klinickém využití je pak rázová vlna generována ze zdroje – elektrohydraulického, elektromagnetického nebo piezoelektrického. Pro šíření rázové vlny a zachování její energie je nezbytné vhodné materiálové médium. Optimálním médiem – prostředím pro přenos rázové vlny z generátoru do těla pacienta je voda bez bublinek vzduchu, kdy na rozhraní těchto dvou prostředí dochází ke ztrátě asi jen 1 % energie. Naopak v případě prostředí voda – konkrement činí ztráta energie 5–25 %, na rozhraní prostředí voda – kost činí ztráta energie 50–60 %, prakticky k úplné ztrátě energie až 99,9 % dochází na rozhraní prostředí voda – vzduch (2). Veličina, která definuje vlastnosti prostředí pro přenos rázové vlny je pak akustická impedance. Přenos rázové vlny od jejího zdroje do ohniska (coupling) musí tak probíhat v prostředí s minimálními rozdíly akustické impedance (3). Technologie LERV zaznamenala v tomto směru za posledních 30 let podstatných změn, kdy první způsob transportu rázové vlny ve vodní lázni (pacient ležel po dobu výkonu ve vaně s vodou) byl postupně nahrazen suchým konceptem, kdy je přenos mezi generátorem a pacientem zajištěn pomocí gelu nebo oleje. Další podmínkou účinnosti rázové vlny je její fokusace (koncentrace do určitého bodu – ohniska). Reálně není rázová vlna koncentrována do jednoho bodu, ale do prostoru definovaného jako fokální zóna. Fyzikálně se jedná o trojrozměrný prostor, ve kterém jsou naměřené hodnoty tlaku alespoň 50 % maximálního tlaku rázové vlny. Tvarově je fokální zóna elipsoid, kdy nejdelší rozměr odpovídá ose šíření rázové vlny. Různé typy přístrojů od různých výrobců mají odlišné velikosti fokálních zón. Obecně platí, že přístroje s úzkou fokální zónou mají vyšší cílové tlaky v ohnisku. Bylo však prokázáno, že úspěšnost fragmentace konkrementu nekoreluje s hodnotami tlaku v ohnisku (4). Naproti tomu schopnost fragmentace konkrementů úzce koresponduje s energií rázové vlny dodané do ohniskové zóny (5–7). Vlastní energie rázové vlny pak byla definována dle IEC (International Electrotechnical Commision) a standartu 61 846. Tato energie prochází skrze cirkulární oblast, a protože je zároveň určena pro cílovou oblast průměru 12 mm byla nazvána jako efektivní energie Eeff (12 mm) (8). Celková energetická dávka potřebná k dezintegraci litiázy je pak definována konceptem energetické dávky, de facto tato energie odpovídá počtu rázů násobených energií na jednotlivých energetických hladinách:
Edose = n * Eeff(12 mm), resp. Edose = n1 * Eeff1 + n2 * Eeff2 + n3 * Eeff3 …
Koncept energetické dávky umožňuje srovnání efektivity různých zdrojů rázových vln. Jinak porovnání mezi jednotlivými litotryptory zůstává obtížné (9). Ve snaze porovnat efektivitu terapie jednotlivými přístroji byl nakonec v klinické praxi zaveden parametr koeficient účinnosti (EQ – quotient efficacy). Nejčastěji užívanou rovnicí pro výpočet EQ je rovnice dle Denstedta a Claymana (10, 11), přestože tato rovnice nezahrnuje předchozí auxiliární procedury a konkrementy odstraněné následným kurativním auxiliárním výkonem, jsou zařazeny mezi úspěšné případy. Přesnější modifikací výpočtu EQ je rovnice dle Rassweilera (12), která dané nedostatky odstraňuje. Zohledňuje, jak zavedení stentu před vlastní LERV, tak následné auxiliární procedury po LERV.
Denstedt, Clayman:
EQ = (% SFR * 100%)/(100% + % Re-treatment + % Post-auxiliary treatment)
Rassweiller:
EQ = (% SFR – % Curative Auxiliary Measures) × 100%/(100% + % Re-treatment + % Pre-Auxiliary Proc. + % Post-Auxiliary Proc.)
METODIKA
V pilotní studii jsme prospektivně zhodnotili efektivitu extrakorporální litotrypse za pomoci elektromagnetického zdroje rázových EMSE vln 140f. Zároveň jsme stanovili průměrně aplikovanou energetickou dávku (Edose) na jeden výkon. Zhodnotili jsme 50 pacientů v období od prosince roku 2012 do února roku 2013, u pacientů jsme provedli celkem 60 výkonů. Periferní nefrolitiázu jsme řešili ve 26 případech, pyelolitiázu ve 23 případech a ureterolitiázu v 11 případech. Před každým výkonem jsme zaznamenali velikost konkrementu v nejdelším průměru pomocí spirálního CT nebo pomocí nativního nefrogramu.
Výkony jsme provedli v analgosedaci, k premedikaci jsme užili Indometacin 100 mg čípek a během výkonu jsme titrovaně podávali za současné monitorace tlaku, saturace a EKG Fentanyl intravenózně v dávce 1–2 ml (50–100 µg). K LERV jsme použili mobilní litotryptor Dornier Compact Sigma s elektromagnetickým zdrojem EMSE 140f. Velikost ohniska je u daného přístroje 5 × 15 mm, penetrační hloubka je 150 mm, ohniskový tlak od 6,7 MPa do 55MPa a rozsah nastavení umožňuje až devět energetických úrovní (a, b, c, 1–6), kdy doporučené nastavení výrobcem pro trypsi litiázy je na energetické hladině 2–6 a odpovídá rozsahu dávek od 22–60 mJ (energetická hladina 2–22 mJ, 3–30 mJ, 4–40 mJ, 5–50 mJ, 6–60 mJ). Náš přístroj je plně kompatibilní s ostatními dostupnými přístroji.
V daném souboru jsme sledovali primární efekt dezintegrace, stone free rate (SFR), auxiliární procedury a komplikace. V hodnoceném souboru jsme zohlednili habitus pacientů, kdy body mass index (BMI) pacientů byl v rozpětí 19,0–44,1. Podváhou netrpěl žádný pacient, normální váhu (BMI 18,5–24,9) jsme zaznamenali u 32,5 % pacientů, nadváhu (BMI 25–29,9) u 40 % pacientů a obezitu (BMI nad 30) u 27,5 % pacientů. Další faktory jako toleranci výkonu a složení litiázy jsme nezohlednili. Vlastní trypsi jsme provedli na základě předem určeného schématu aplikace postupného zvyšovaní energetické hladiny 2–5, kdy na energetické hladině 2 jsme aplikovali 200 rázů, na energetické hladině 3 celkem 1500 rázů, na energetické hladině 4 pak 800 rázů a na energetické hladině 5 maximálně 600 rázů. Během výkonů jsme užili frekvenci 80 rázů/minutu a coupling během výkonu byl optimálně na hodnotě 3 z možného rozsahu 0–5. Předčasný konec trypse jsme metodicky definovali jako časnou dezintegraci, kdy litiáza nebyla na skiaskopii dále patrna. Dalším důvodem předčasného ukončení výkonu mohla být špatná tolerance výkonu. Jinak v případě všech výkonů jsme nikdy nepřekročili maximální dávky doporučené výrobcem litotryptoru. Definitivní zhodnocení výsledků jsme provedli za 3 měsíce od zákroku pomocí nativního nefrogramu a sonograficky. Podmínkou provedení výkonu byla schopnost skiaskopického zaměření litiázy (fokusace), kdy jsme následně po celou dobu výkonu průběžně kontrolovali polohu konkrementu tak, aby hodnocení dávky pro dezintegraci bylo validní bez možných odchylek způsobených špatným zaměřením litiázy. Rovněž jsme kontrolovali kvalitu couplingu pro optimální přenos energie s minimalizací energetických ztrát.
Průměrnou energetickou dávku jednoho výkonu jsme stanovili na základě konceptu výpočtu celkové energetické dávky:
Edose = n1* Eeff1 + n2* Eeff2 + n3* Eeff3 + …
VÝSLEDKY
Primárního efektu dezintegrace litiázy jsme dosáhli u 87,0 % pacientů, SFR jsme do 3 měsíců zaznamenali u 78,0 % pacientů. Výkon jsme opakovali celkem 10krát a celkem v šesti případech jsme provedli ureterorenoskopii jako auxiliární proceduru. Pět pacientů z daného souboru je s reziduální litiázou v dolním kalichu dále sledováno (tab. 1).
Tab. 1. Výsledky dezintegrace a SFR Table 1. Results of disintegration and SFR 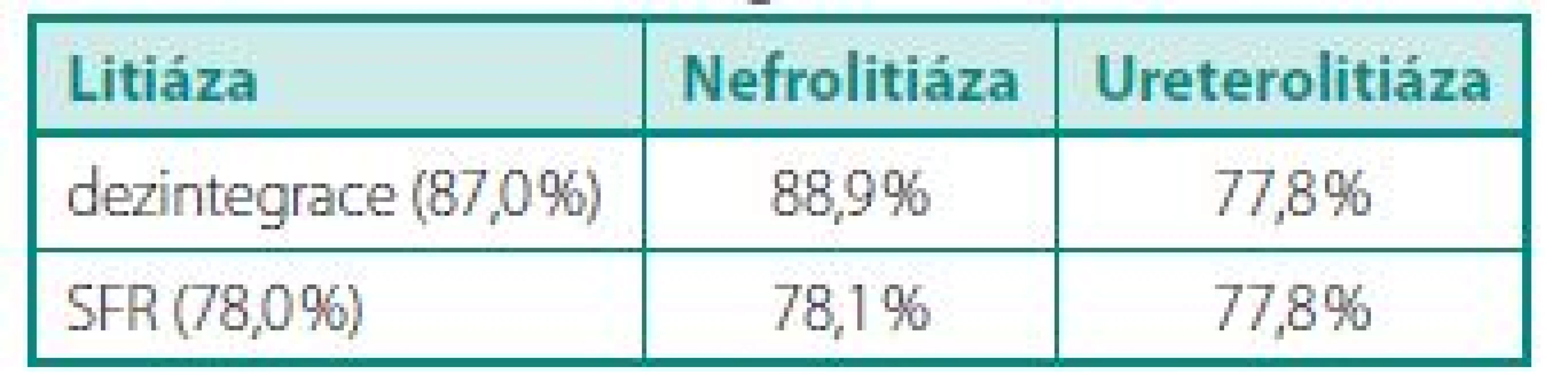
Koeficient účinnosti generátoru EMSE 140f dosáhl ve sledovaném souboru 61,6 % dle rovnice Denstedta a Claymana:
EQ = (78 % * 100 %)/(100 % + 16,7 % + 10 %) = 61,6 %
Průměrně jsme aplikovali 2226 rázů během jednoho výkonu, v rozmezí od 780 do 3085 rázů. Maximální aplikovaná energetická dávka tak byla dle daného schématu aplikace 110,6 J. Průměrně dodaná energetická dávka (Edose) byla 70,4 J, pro nefrolitiázu byla průměrná dávka 73,2 J a pro ureterolitiázu pak jen 58,0 J. Průměrná velikost nefrolitiázy byla 10,6 mm a průměrná velikost ureterolitiázy 7,2 mm (tab. 2).
Tab. 2. Výpočet E<sub>dose</sub> Table 2. Assessment of E<sub>dose</sub> 
Ve vztahu k velikosti byl nejvíce problematický spontánní odchod litiázy větších rozměrů, kdy tato skupina je zatížena větším počtem auxiliárních procedur nebo opakováním výkonu a to při realitě aplikace vyšších energetických dávek. V případě pyelolitiázy velikosti 5–10 mm jsme při průměrné velikosti 7,0 mm a průměrně aplikované energetické dávce 59,8 J dosáhli SFR u 100 % pacientů. Naopak v případě pyelolitiázy velikosti 10–15 mm a průměrně aplikované energetické dávce 89,9 J jsme zaznamenali SFR jen 66,7 %, a to při průměrné velikosti litiázy 13,6 mm. Ve vztahu k lokalizaci je pak nejvíce problematická pasáž litiázy z dolní kalichové skupiny a to zejména ve spojení s její velikostí, kdy při velikosti litiázy 10–15 mm jsme zaznamenali SFR pouze u 44,4 % pacientů při průměrné velikosti litiázy 12 mm a průměrně aplikované energetické dávce 79,5 J. Naopak v případě drobné litiázy dolního kalichu velikosti 5–8 mm jsme dosáhli SFR ve 100 % případů při průměrné velikosti litiázy 6,3 mm a průměrně aplikované energetické dávce 57,6 J. Ve vztahu k BMI jsme u pacientů s normální hmotností dosáhli 100% efektivity LERV, u pacientů s nadváhou v rozmezí BMI 25–30 jsme naopak zaznamenali SFR jen u 69 % pacientů a nakonec u pacientů s nadváhou a BMI nad 30 jsme dosáhli SFR jen u 55 % pacientů.
DISKUSE
Litotrypse extrakorporální rázovou vlnou je již 30 let nedílnou součástí komplexní léčby urolitiázy, trvale jsou studovány fyzikální principy rázové vlny a metoda je výrobci neustále zlepšována, přesto nebyla doposud zodpovězena řada otázek. Koncept energetické dávky umožňuje srovnání různých zdrojů rázových vln, jinak je reálné globální srovnání jednotlivých přístrojů dnes prakticky nemožné. Software pro zpracování dat není standardizován, chybí nezávislá instituce pro zpracování analýz, nejsou dokonce ani standardizovány jednotky, kdy někteří výrobci uvádí při aplikaci rázových vln užitou energii v jednotkách milivolt místo v jednotkách joule.
Graber et al. (13) v prospektivní randomizované studii porovnali výsledky užití elektrohydraulického litotryptoru (Dornier MH3) a elektromagnetického litotryptoru (Lithostar plus), kdy reziduální fragmenty < 2 mm mělo 91 %, resp. 65 %. Nicméně jiné studie ukazují nesignifikantní rozdíl mezi elektrohydraulickými a elektromagnetickými litotryptory (14) nebo mezi jednotlivými piezoelektrickými litotryptory (15). De Marco et al. dokonce prezentuje lepší dezintegrační schopnosti u artificiálního konkrementu in vitro při užití nových elektromagnetických zdrojů s technologií EMSE v porovnání s roky zlatým standardem elektrohydraulickým zdrojem HM3. Následně závěry dokládá klinickou studií na 197 pa-cientech, kdy v případě užití litotryptoru EMSE 220-XXP byl SFR dosažen u 86 % pacientů, časná dezintegrace zaznamená v 79 % a auxiliární výkony byly provedeny u 20 % pacientů. Naopak při užití litotryptoru HM3 byla časná dezintegrace dosažena jen v 66 %, SFR byl 76 % a auxiliární výkony byly provedeny u 28 % pacientů (16). Další porovnání účinnosti elektromagnetických a elektrohydraulických zdrojů prezentuje Tailly roku 2002, kdy výsledky účinku zdrojů jsou ekvivalentní, ale při užití nižších dávek energie u elektromagnetických zdrojů (17).
Naše první výsledky prokazují dobrou efektivitu dané metody a jsou dále srovnatelné s literárně dostupnými údaji. Překvapivým zjištěním bylo užití výrazně nižších energetických dávek aplikovaných během LERV v porovnání s literárně publikovanými údaji. Koser et al. (18) udávají energetické dávky 152–164 J pro ureterolitiázu a 138–164 J pro nefrolitiázu, Tailly (14) dokonce uvádí dávky 228 J (zdroj rázových vln EMSE 220 F) a 307 J (zdroj rázových vln EMSE 220 F-XP). Sorensen et al. (19) publikovali zkušenosti při užití zdroje rázových vln EMSE 140. V případě litiázy velikosti do 10 mm byla užita energie přibližně 110 J a v případě litiázy velikosti 10–20 mm energie 140 J. Dané výsledky zdůvodňují doporučení energetických dávek pro LERV, kdy pro nefrolitiázu je doporučená dávka Edose (12 mm) 100–130 J a pro ureterolitiázu pak dávka Edose (12 mm) = 150–200 J (20). V případě neúspěchu fragmentace může být eventuálně dávka překročena a pro nefrolitiázu lze užít dávky 150–200 J, pro ureterolitiázu dávku 220–270 J (9).
Tab. 3. Vztah lokalizace, velikosti, E<sub>dose</sub> a SFR Table 3. Relation of size, localization, E<sub>dose</sub>and SFR 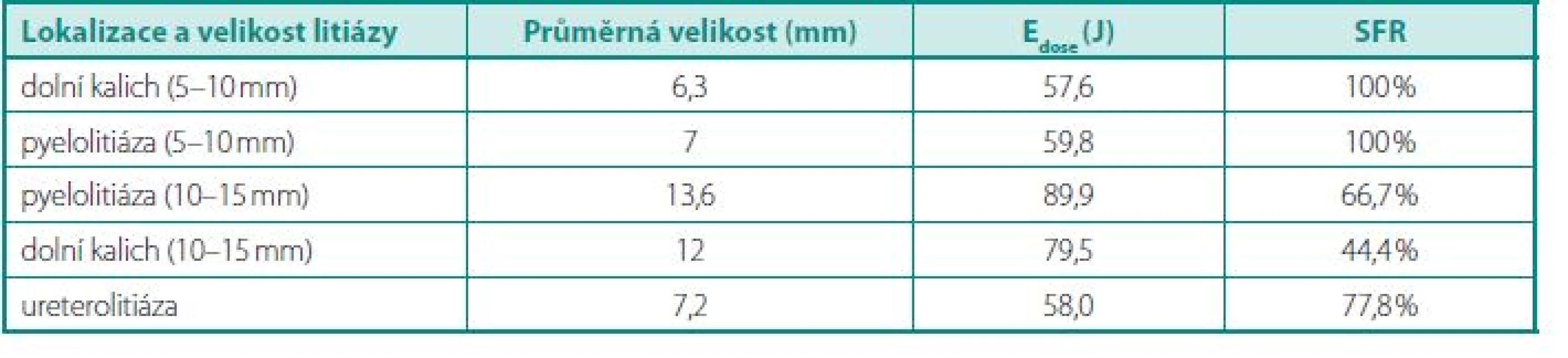
Tab. 4. BMI – SFR Table 4. BMI – SFR 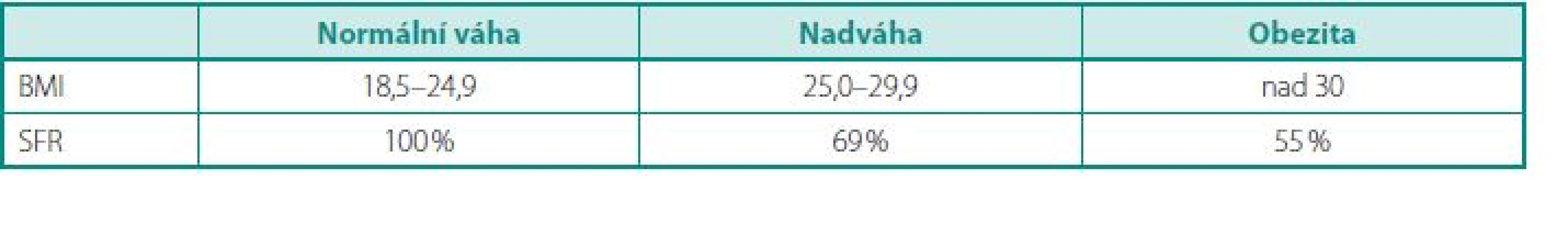
Absence relevantních údajů v literatuře nejednoznačně definované energetické dávky, doporučení výrobce, která nejsou prezentována jako oficiální dokument, nás vedli k nutnosti kontaktovat firmu Dornier – zakladatele extrakorporální litotrypse a dodavatele našeho přístroje. Následná korespondence včetně potvrzení užití širokého rozmezí energetických dávek danou realitu potvrdila. Doporučení EAU (21) vztahující se k počtu rázových vln, nastavení energie a opakování výkonu jsou obecná a v zásadě energetické dávky nedefinují. Obecně udávají, že počet rázových vln je závislý na typu litotryptoru a síle šokových vln, kdy ale není jasný konsenzus v maximálním počtu rázových vln. Bohužel tato obecná definice prakticky postrádá základní informaci doporučené energetické dávky pro LERV.
Zdůvodnění užití širokého rozsahu energetických dávek v klinické praxi může být obtížné. Jednou z možných odpovědí, proč je za určitých podmínek potřeba více a v jiném případě méně energie, dávají práce zabývající se vlivem couplingu na dezintegraci litiázy, kdy odstranění vzduchových bublin na rozhraní prostředí je nezbytné pro přenos a zachování energie rázových vln (22). Bohris et al. popisují měření couplingu pomocí integrované kamery, kdy pouze v 10 případech z 30 bylo ideální spojení pro transport rázové vlny. Současně udávají rozdílný počet rázových vln potřebný k úplné dezintegraci konkrementů v závislosti na optimálním couplingu (spojení bez bublin 100 ± 4 rázů, 5 % bublin 126 ± 3 rázů, 10 % bublin ve spojení 151 ± 8 rázů a v případě 20 % bublin ve spojení dokonce potřeba 287 ± 5 rázů) (23). Tailly et al. pak udávají, že při optimálním kontrolovaném couplingu lze snížit potřebnou energetickou dávku až o 38 % (24). Pishchalnikov et al. (25) na modelu in vitro zjistil, že 2% pokrytí vzduchovými kapsami při couplingu snižuje dezintegraci litiázy o 20–40 %. Mezi další faktory ovlivňující finální potřebu energetické dávky pro úspěšnou dezintegraci patří užití stentingu před LERV, kdy některé práce prokazují negativní vliv stentingu na dezintegraci litiázy při terapii (26, 27). Obecně dalšími predisponujícími faktory selhání LERV jsou složení, lokalizace, počet a velikost litiázy, stejně tak jako renální morfologie nebo poměr rázových vln a energie (28, 29).
Přestože jsme ve sledovaném souboru užili průměrně nižší energetické dávky, zaznamenali jsme jednu závažnou komplikaci poranění ledviny. Při zpětné analýze se jako zásadní jeví fakt, že v případě poškozené ledviny jsme užili energetickou dávku nad 100 J, přestože průměrně aplikovaná dávka pro nefrolitiázu byla jen 73,2 J. V žádném případě jsme i přes značně široké dávkovací rozpětí určené výrobcem nepřekročili doporučené maximální dávky.
Uvážíme-li, že energetickou dávku lze považovat za rozhodující parametr extrakorporální litotrypse z hlediska efektivity a bezpečnosti, pak se může zdát absence relevantních dat a jasných doporučení překvapivá.
ZÁVĚR
Iniciální výsledky LERV ve sledovaném souboru prokázali vysokou efektivitu nového přístroje Dornier Compact Sigma, kdy EQ generátoru EMSE 140f dosahuje v daném souboru 61,6 % a je srovnatelný s literárně dostupnými údaji EQ dnes nejvýkonnějších litotryptorů. Průměrně užitá energetická dávka Edose pro renální konkrementy byla 73,2 J a pro ureterální konkrementy pak 58,0 J. Souhrnně jsme prokázali nižší průměrnou potřebu efektivní energetické dávky Edose v porovnání s literárně dostupnými údaji. Zásadní pro dobrou efektivitu LERV (SFR, EQ) je nejen množství užité energie, ale zejména velikost litiázy, její lokalizace a BMI pacienta. Z našich výsledků dále vyplývá závislost mezi velikostí litiázy a množstvím aplikované energie ve vztahu k dosaženému SFR. Širší diskuse, analýzy dat a budoucí snaha přesněji definovat energetické dávky jako hlavního parametru efektivity a bezpečnosti extrakorporální litotrypse by měla mít význam pro následné zlepšení naší klinické praxe.
Došlo: 2. 7. 2014.
Přijato: 8. 10. 2014.
Kontaktní adresa
MUDr. Vít Paldus
Urologické oddělení, Krajská nemocnice Liberec, a.s.
Husova 10, 460 63 Liberec
e-mail: vit.paldus@nemlib.cz
Práce vznikla s finanční podporou Vědecké rady Krajské nemocnice Liberec, a.s.
Zdroje
1. Chaussy C, Brendel W, Schmiedt E. Extracorporeally induced destruction of kidney stones by shock wave. Lancet 1980; 2 : 165–168.
2. Cleveland RO, McAteer JA. The physics of Shock Wave Lithotripsy. In: Smith AD, Badlani G, Bagley D, Clayman R, other a eds, Smiths Textbook Of Endourology. Hamilton-London: BC Decker Inc 2006; 317–332.
3. Fógel K. Fyzikální základy extrakorporální litotrypse. Ces Urol 2010; 14(2): 73–80.
4. Kerbl K, Rehman J, Landman J, et al. Current management of urolithiasis: progress or regress? J Endourol 2002; 16 : 281–288.
5. Granz B, Köhler G. What makes a shock wave efficient in lithotripsy Stones Disease 1992; 4 : 123–128.
6. Rassweiler JJ, Bergsdorf T, Ginter S, Granz B, Häcker A, Lutz A, Wess O, Wilbert D. Progress in Lithotripter Technology. In: Chassy C, Haupt G, Jocham D, Köhrmann KU, Wilbert D (eds.) Therapeutic Energy Applications in Urology. Standards and recent developments. Stuttgart – New York: Thieme 2005; 3–15.
7. Rassweiler JJ, Tailly GG, Chaussy C. Progress in lithotriptor technology. EAU Update Series 2005; 17–36.
8. Chaussy C, Tailly G, Forssmann B, Bohris Ch, Lutz A, Tailly-Cusse M, Tailly T. Extracorporeal Shock Wave Lithotripsy in a Nutschell 2013; 3 : 13–22.
9. Chaussy C, Haupt G, Jocham D, Köhrmann KU. Consensus: Shock Wave Technology and Application – State of the Art in 2010. Therapeutic Energy Applications in Urology II 2010; 2 : 37–52.
10. Denstedt JD, Clayman RV, Preminger GM. Efficacy quotient as a means of comparing lithotripters. J Endourol 1990; 3 : 100.
11. Clayman RV, MCLennan BL, Garvin TJ, Denstedt JD, Andriole GL. Lithostar: An electromagnetic acoustic shock wave unit for extracorporeal lithotripsy. J Endourol 1989; 3 : 307–313.
12. Rassweiler J, Köhrmann J, Jünemann KP, Alken P. Use of electromagnetic technology. In Smith AD. Controversies in endourology. Philadelphia: WB Saunders Co 1995 : 95–106.
13. Graber SF, Danuser H, Hochreiter WW, Studer UE. A prospective randomized trial comparing two lithotriptors for stone disintegration and induced renal trauma. J Urol 2003; 169 : 54–57.
14. Sheir KZ, Madbouly K, Elsobky E. Prospective randomized comparative study of the effectiveness and safety of electrohydraulic and electromagnetic extracorporeal shock wave lithotripters. J Urol 2003; 170 : 389–392.
15. Ng CF, MacLornan L, Thompson TJ, Tolley D. Comparison of 2 generations of piezoeletric lithotriptors using matched pair analysis. J Urol 2004; 172 : 1887–1891.
16. De Marco F, et al. XVIIIth Congress of the European Association of Urology. Madrid, Spain, March 12–15, 2003.
17. Tailly GG. In situ SWL of ureteral stones: comparison between an electrohydraulic and electromagnetic shock wave source. J Endourol 2002; 16 : 209–214.
18. Koser M, Rhein A, Haecker M, Rabs U. Extracorporeal shock wave lithotripsy (ESWL) of urinary calculi – effect of shock wave frequency on fragmentation success: preliminary result of prospective study. Eur Urol 2001; 39(Suppl): 58.
19. Sorensen C, Chandhoke P, Moore M, Wolf C, Sarram A. Comparison of intravenous sedation versus general anesthesia on the efficacy of the Doli 50 lithotriptor. J Urol 2002; 168 : 35–37.
20. Rassweiler J, Knoll T, Köhrmann K, McAtter J, Lingeman J, Cleveland R, Bailey M, Chaussy Ch. Shock Wave Technology and Application: An Update. Eur Urol 2011; 59(5): 784–796.
21. Türk C, Knoll T, Petrik A, Sarica K, Skolarikos A, Straub M, Seitz C. Guidelines on urolithiasis 2013. EAU Clinical Guidelines 2013; 5 : 19–40.
22. Guanqyan Li, James C. Williams Jr, Yuri A. Pischalnikov, Ziyue Liu, McAteer JA. Size and Location of Defects at the Coupling Interface Affect Lithotripter Performance. BJU Int 2012; 110: E871–E877.
23. Bohris C, Roosen A, Dickmann M, Hocaoglu Y, Sandner S, Bader M, Stief CG, Walther S. Monitoring the coupling of the lithotripter therapy head with skin during routine shock wave lithotripsy with a surveillance camera. J Urol 2012; 187 : 157–163.
24. Tailly GG. Optical coupling control in ESWL: first clinical experience. Poster.
25. Pishchalnikov YA, Neucks JS, Von DerHaar RJ, Pishchalnikova IV, Williams Jr JC, McAteer JA. Air pockets trapped during routine coupling in dry head lithotripsy can significantly decrease the delivery of shock wave energy. J Urol 2006; 176 : 2706–2710.
26. Petřík A, Záťura F, Beneš J. Vliv stentingu na dezintegraci ureterolitiázy in vitro. Ces Urol 2004; 8(3): 46–48.
27. Petřík A, Alterová E, Fiala M, Novák J, Záťura F. Vliv stentingu na dezintegraci ureterolitázy in vivo. Ces Urol 2006; 10(1): 59–63.
28. Madlouby K, Sheir KZ, Elsobky E, Eraky I, Kenawy M. Risk factors for the formation of steinstrasse after extracorporeal shock wave lithotripsy: a statistical model. J Urol 2002; 167 : 12349–12442.
29. Abdel-Khalek M, Sheir KZ, Mokhtar AA, Eraky I, Kenawy M, Bazzed M. Prediction of success rate after extracorporeal shock wave lithotripsy of renal stones – a multivariate analysis model. Scan J Urol Nephrol 2004; 38 : 161–167.
Štítky
Detská urológia Nefrológia Urológia
Článek EditorialČlánek Primární amyloidóza ureteru
Článok vyšiel v časopiseČeská urologie
Najčítanejšie tento týždeň
2014 Číslo 4- Aktuálne európske odporúčania pre liečbu renálnej koliky v dôsledku urolitiázy
- MUDr. Šimon Kozák: V algeziológii nič nefunguje zázračne cez noc! Je dôležité nechať si poradiť od špecialistov
- Vyšetření T2:EGR a PCA3 v moči při záchytu agresivního karcinomu prostaty
- Lék v boji proti benigní hyperplazii prostaty nyní pod novým názvem Adafin
-
Všetky články tohto čísla
- Editorial
- Imunoterapie a karcinom prostaty
- Autonomní dysreflexie u pacientů po spinálním poranění
- Extrakorporální litotrypse rázovou vlnou v současné urologické praxi
- Využití multiparametrické magnetické rezonance a srovnání s ostatními moderními zobrazovacími metodami v předoperační diagnostice karcinomu prostaty
- Hodnocení absolutní indikace operační léčby BPH u pacientů s prokázanou cystolitiázou
- Zhodnocení účinnosti extrakorporální litotrypse elektromagnetického generátoru EMSE 140f Dornier Compact Sigma a stanovení efektivní energetické dávky
- Hodnocení erektilní dysfunkce po roboticky asistované radikální prostatektomii
- Primární amyloidóza ureteru
- Deset tipů pro začínající kongresové řečníky
- Soutěž ČUS o nejlepší vědeckou publikaci za rok 2013
- Central European Meeting v Krakově – vybrané přednášky
- Česká urologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Extrakorporální litotrypse rázovou vlnou v současné urologické praxi
- Využití multiparametrické magnetické rezonance a srovnání s ostatními moderními zobrazovacími metodami v předoperační diagnostice karcinomu prostaty
- Autonomní dysreflexie u pacientů po spinálním poranění
- Hodnocení erektilní dysfunkce po roboticky asistované radikální prostatektomii
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



