-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Diferenciální diagnostika granulomatózních procesů v plicích
Differential diagnosis of granulomatous lung diseases
Brief review of histopathology of non-tumor pulmonary diseases with nodular or granulomatous morphology. Differential diagnosis of infections, sarcoidosis, vasculitides with a granulomatous component and selected pneumoconioses is presented.
Keywords:
granuloma – mycobacterioses – mycosis – sarcoidosis – vasculitis – silicosis
Autori: Helena Hornychová 1; Markéta Nová 1; Radoslav Matěj 2,3
Pôsobisko autorov: Fingerlandův ústav patologie, Fakultní nemocnice a Lékařská fakulta Karlovy univerzity, Hradec Králové 1; Oddělení patologie a molekulární medicíny, Thomayerova nemocnice, Praha 2; Ústav patologie 1. LF UK a VFN, Praha 3
Vyšlo v časopise: Čes.-slov. Patol., 52, 2016, No. 2, p. 93-99
Kategória: Přehledové články - Interscitiální plicní procesy
Súhrn
Stručný přehled histopatologie nenádorových plicních onemocnění s nodulární nebo granulomatózní morfologií. Prezentována je zejména diferenciální diagnóza infekcí, sarkoidózy, vaskulitid s graulomatózní komponentou a některých pneumokonióz.
Klíčová slova:
granulom – mykobakteriózy – mykózy – sarkoidóza – vaskulitida – silikóza
Na většinu stavů v nenádorové pneumopatologii lze aplikovat základní poučku, že určitý typ morfologie může být vyvolán mnoha různými etiologickými faktory. U granulomů jsou těmi třemi základními infekce, sarkoidóza a vaskulitidy, ale i řada dalších. Následující text je pokusem o shrnutí základních diferenciálně diagnostických znaků, které by nás ke správné etiologii mohly nasměrovat. Nutnou poznámkou je, že všechny tyto diagnózy by měly být stanovovány v úzké spolupráci s klinickými lékaři a radiology v rámci multidisciplinárního přístupu.
INFEKCE
Granulomatózní zánět vyvolávají z infekčních agens nejčastěji mykobakteria (m. tuberculosis i atypická mykobakteria) a plísně. Tyto dvě skupiny infekčních organismů naopak zase nemusí vyvolávat pouze granulomatózní zánětlivou reakci – výsledný typ zánětu je kombinací aktuální imunitní kompetentnosti organismu a virulence infekčního agens. Pokud některou z těchto infekcí onemocní imunokompetentní hostitel, mívá obvykle anatomickou predispozici pro onemocnění – bronchiektazie nebo jizevnaté dutinovité změny, ve kterých pak vznikají mycetomy s jen minimální nespecifickou zánětlivou reakcí v okolí (obr. 1A). Dalším typem je alergická zánětlivá reakce na mykotické agens (nejčastěji na aspergila). Nacházíme zahuštěný hlen s Charcottovými-Leydenovými krystaly a eozinofilními granulacemi, výraznou hyperplázii pohárkových buněk a intenzivní zánětlivou infiltraci s eozinofily ve stěně bronchu. Mykotické elementy bývají zachyceny jen ve velmi malém množství, nemusí být v materiálu zachyceny vůbec (např. je tento typ reakce v plicích popisován u mycetomu ve vedlejších dutinách nosních).Za situace, kdy je agresivita agens v jisté křehké rovnováze s obrannými mechanismy částečně imunosuprimovaného pacienta, je typickou reakcí granulomatózní zánět (obr. 1B a 2). Oba výše zmiňované typy zánětlivé reakce mohou v případě imunosuprese pacienta progredovat do granulomatózní zánětlivé reakce. Rozsah nekrotizace často koreluje s větší agresivitou agens nebo těžší imunosupresí pacienta. Pokud se tato křehká rovnováha poruší (těžká imunosuprese, velmi agresivní agens) převažují nekrotické změny.
Obr. 1. Žena 48 let, resekce ložiska v plíci. Pacientka s periferním T lymfomem v léčbě, předoperačně z bronchoskopických a zobrazovacích metodik stanovena klinická diagnóza: aspergilom a atypická mykobakterióza. 
A. Bronchiektazie se strukturami mycetomu a nespecifickou smíšenou zánětlivou infiltrací ve stěně bronchu (hematoxylin-eozin, zvětšení 40x) B. Jiná oblast stěny bronchiektazie – nekróza sliznice bronchu s granulomatózní zánětlivou reakcí (hematoxylin-eozin, zvětšení 200x). V bronchiektazii v barvení dle Grocotta v povrchových oblastech nekrózy mykotické elementy vzhledu aspergila (Ziehl-Neelsen zde negativní). V dalších blocích mimo oblast bronchiektazie granulomy s klasickou popraškovou nekrózou a acidorezistentními tyčkami. V plicích nebyly známky infiltrace při základním hematologickém onemocnění. Obr. 2. Muž 52 let, rozpadový proces horním laloku levé plíce. 
A. Typická morfologie specifického granulomu s popraškovou nekrózou (hematoxylin-eozin, zvětšení 100x). B. Nekróza sliznice bronchu s granulomatózní zánětlivou reakcí (hematoxylin-eozin, zvětšení 40x). V barvení dle Ziehl-Neelsena vícečetné acidorezistentní tyčky, PCR vyšetření na m. tuberculosis negativní, na atypická mykobakteria sporné (menší citlivost metodiky), klinicky uzavíráno jako atypická mykobakterióza. Dobrým diferenciálně diagnostickým vodítkem může být charakter šíření. Nejcharakterističtější pro infekční etiologii je šíření aerogenní, jehož typickým projevem je bronchiolitida s nekrózou sliznice a granulomatózní zánětlivou reakcí v okolí (obr. 1B a 2B) (dif.dg. – nekrotizující bronchiolitida v rámci granulomatózy s polyangiitidou). Dalším typem šíření je šíření lymfogenní s granulomy v perilymfatické lokalizaci a postižením spádových lymfatických uzlin, je časté u mykobakterióz (dif.dg. – sarkoidóza, méně pneumokoniózy). Poslední je šíření hematogenní, typický je miliární rozsev u tuberkulózy a tvorba infarktů u některých mykóz, zejména u mukormykózy nebo aspergilózy (dif.dg. infarkt, nekrózy v rámci vaskulitid nebo systémových onemocnění pojiva – např. revmatoidní artritida).
Pro diagnostiku infekčních typů granulomatózních zánětů jsou naprosto stěžejní speciální barvení (Ziehl-Neelsen, Grocott, Gram, event. PAS, Giemsa, Warthin-Starry). Do výčtu barvení jsou kromě základních barvení na mykobakteria a mykotické elementy zařazena i speciální barvení na bakteriální elementy, protože podobné morfologické obrazy může mít například i chronická aktinomykóza nebo chronické abscesy jiné bakteriální etiologie. Všechny granulomatózní záněty i jiné léze s možnou infekční etiologií by měly být vyšetřeny speciálními barveními. Pokud jsou (imuno)histochemická vyšetření negativní a je klinická suspekce na infekční etiologii, nebo pokud potřebujeme blíže dozařadit infekční agens, lze provést PCR vyšetření i z parafinového bloku (s trochu nižší citlivostí než má tato metodika z nativního materiálu). U primodiagnóz mykobakterióz by to (pokud není k dispozici kultivační vyšetření) mělo být pravidlem, protože legislativně daný epidemiologický dohled je u tuberkulózy daleko striktnější než u ostatních mykobakterióz, a odlišení těchto dvou jednotek je tedy pro pacienty velmi důležité (1-6).
SARKOIDÓZA
Sarkoidóza je onemocnění charakterizované patologickou reakcí CD4 T lymfocytů (Th1 subsetu) a makrofágů tvorbou granulomatózní zánětlivé reakce. Makrofágy se postupně pod vlivem cytokinů mění na epiteloidní buňky s vystupňovanou sekreční aktivitou a ztrátou schopnosti fagocytózy. V dalším průběhu existence granulomu může dojít k obklopení imunokompetentních buněk fibroblasty a následné skleróze granulomů. Imunopatologická Th1 odpověď na specifické antigeny je charakterizována také produkcí cytokinů, a to hlavně IL-2 a IFN-gama, které vedou k proliferaci B buněk a ke zvýšené produkci imunoglobulinů. Tyto procesy jsou podkladem pro typický imunologický obraz u sarkoidózy, kdy v postižené tkáni nebo orgánu jsou nakupeny CD4+ T lymfocyty, ale naopak v periferní krvi je relativní lymfopenie s převahou CD8+ T lymfocytů a hypergamaglobulinemie. Typickým morfologickým znakem je výskyt specifických granulomů bez nekrotizace v perilymfatické lokalizaci, tj. v oblasti bronchovaskulárních struktur, plicních sept a pleury (obr. 3A). Granulomy jsou obvykle střední velikosti (větší mohou být u nodulární sarkoidózy), dobře formované s přítomností epiteloidních buněk a buněk mnohojaderných. Ve většině publikací je poměrně podrobný popis jednotlivých druhů inkluzí v mnohojaderných buňkách (netřeba uvádět, že asteroidní inkluze jsou opravdu krásné), bohužel inkluze nejsou znakem, který by byl pro sarkoidózu patognomický. Jediný podstatný moment je odlišit tyto inkluze od aspirovaného materiálu v granulomu z cizích těles nebo materiálu v granulomech u pneumokonióz. Schaumannovy konchoidní inkluze totiž také typicky stáčejí rovinu polarizovaného světla. Diferenciálně diagnosticky je dále důležité odlišit nekrózu (která by nás vedla spíše k infekční etiologii) a hyalinizaci, která může být zejména v uzlinách poměrně homogenního charakteru. Hyalinizace je typická pro centrum granulomu u nodulární sarkoidózy (obr. 3B) a pokročilé fáze sarkoidózy, kdy nález může nabývat až obrazu end-stage postižení plíce a jedinou známkou sarkoidózy mohou být jen zavzaté Schaumannovy inkluze. Naopak v časnějších fázích můžeme najít více lymfocytů, tehdy je pak v diferenciální diagnostice zejména hypersenzitivní pneumonie (ta má drobnější vágně formované granulomy tvořené aktivovanými makrofágy bez obrazu epiteloidního granulomu v peribronchiolární lokalitě a obvykle nemívá postižení spádových lymfatických uzlin). Vzhledem k distribuci podél lymfatik mohou být granulomy ve velmi těsné souvislosti s arteriemi a venami a v některých případech jsou dokonce granulomy v cévní stěně. Na rozdíl od vaskulitid s granulomatózní zánětlivou složkou jsou však postiženy cévní struktury všech kalibrů, navíc nedochází k destrukci cévní stěny s nekrózou. Granulomy vídáme také ve sliznici velkých bronchů, což umožňuje jejich zachycení v endobioptických bronchiálních odběrech.Naprostým pravidlem pro diagnostiku sarkoidózy by mělo být provedení speciálních barvení na infekční agens, zejména atypické mykobakteriózy či vzácné (cizokrajné) plísně mohou mít granulomatózní zánět bez nekrotizace. Zcela identickou morfologii mají některé pneumokoniózy (berrylióza), k diagnóze je tedy naprosto nezbytná korelace s klinikou, anamnézou expozice a případně analýzou prvků z bioptické tkáně (7-10).
Obr. 3. Muž 49 let, chirurgická biopsie plíce u pacienta, který měl dle zobrazovacích metodik vícečetné ložiskové změny v plicích i postižení plicního intersticia a mediastinální lymfadenopatii, z transbronchiální biopsie granulomatózní zánět bez nekrotizace, v bronchoalveolární laváži minimum lymfocytů. 
A. Dobře formované granulomy střední velikosti bez nekróz umístěné v oblasti bronchovaskulárního svazku, poměrně výrazné fibrózní změny (hematoxylin-eozin, zvětšení 40x). B. Nodulární sarkoidóza – hyalinizovace uvnitř většího ložiska granulomů (hematoxylin-eozin, zvětšení 40x). Konečná diagnóza v korelaci s klinikou: pokročilá sarkoidóza (u pacientů s velkými fibrózními změnami může chybět typický obraz v bronchoalveolární laváži). Zvláštní jednotkou na pomezí mezi sarkoidózou a vaskulitidami je nekrotizující sarkoidní granulomatóza. Jde o velmi vzácnou afekci, kdy převažují změny charakteru granulomatózního zánětu (jako u sarkoidózy) a nekróza má charakter ischemické koagulační nekrózy v důsledku postižení přívodných cévních struktur zánětem. Na rozdíl od klasických vaskulitid by nemělo docházet k destrukci architektoniky cévní stěny (tj. dobře zachovalá elastika v cévní stěně), ale pouze k uzávěru cévního lumen. Tato diagnóza by měla být stanovována s maximální opatrností a to zejména až po vyloučení infekční etiologie všemi dostupnými metodikami (10,11).
VASKULITIDY S GRANULOMATÓZNÍ ZÁNĚTLIVOU REAKCÍ
Do této skupiny onemocnění v plicích spadají zejména granulomatóza s polyangiitidou (dříve Wegenerova granulomatóza) a eozinofilní granulomatóza s polyangiitidou (dříve choroba Churgova-Straussové) (12). Druhá jmenovaná jednotka mívá poměrně charakteristickou kliniku (eozinofilie v periferní krvi u pacienta s astmatem), proto se s ní v praxi setkáváme málokdy a následující text věnujeme tedy převážně granulomatóze s polyangiitidou. Klasickým nálezem je uzlovitá konsolidace plicního parenchymu s různě rozsáhlými zónami nekrotizace až geografického charakteru. Základní diagnostická kritéria jsou shrnuta v tabulce 1, zahrnují typickou triádu projevů – nekrózu parenchymu, vaskulitidu a granulomatózní zánětlivou reakci.
Tab. 1. Histopatologické známky Granulomatózy s polyangiitidou (dle: Vašáková M, Polák J, Matěj R. Intersticiální plicní procesy. Praha: Maxdorf; 2011). 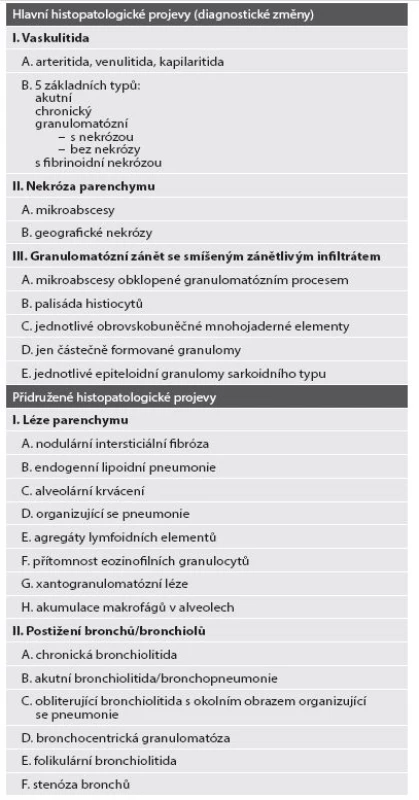
Onemocnění je charakterizováno zánětem postihujícím cévy kalibru od kapilár po středně velké cévy. Projevem kapilaritidy je alveolární krvácení s nekrózou alveolárních sept, změny po proběhlém krvácení jsou charakteristické přítomností siderofágů v alveolech i alveolárních septech. Po kapilaritidě je třeba cíleně pátrat, může být velmi diskrétní a v některých případech může být jediným vodítkem ke správné diagnóze.Postižení středně velkých cév (obr. 4A,B) může být u granulomatózy s polyangiitidou postižením jak muskulárních arterií, tak i žilních struktur. Postižení arterií je snáze hodnotitelné. V barvení na elastická vlákna je vidět destrukce cévní stěny a v povodí postižené tepny najdeme ložisko nekrózy. Intenzita průvodní zánětlivé reakce se liší dle stáří léze. V akutní fázi nacházíme destrukci s nekrózou a neutrofily ve stěně cévy. V pozdnějších fázích přibývá fibrózní a granulomatózní zánětlivé reakce a dochází k jizvení místy až s obliterací cévního lumen. V některých případech mohou být změny poměrně diskrétní, limitované na endotel (endotelitida) nebo subendoteliální úseky cévní stěny.Ložiska nekróz (obr. 4C) jsou charakterizována velkou přítomností neutrofilů, bývají velká, mapovitá, můžeme však najít i drobná okrouhlá ložiska s dobře patrným lemem granulomatózní zánětlivé reakce (tzv. neutrofilní mikroabscesy). Na rozdíl od níže popsaného revmatoidníhu uzlu je nekróza kompletní, bez zachování struktur původního plicního parenchymu v barvení na elastická vlákna. Nekrotizující zánětlivé změny mohou (stejně jako v horních dýchacích cestách) postihovat i sliznici bronchů (dif. dg. infekce). V okolním plicním parenchymu mohou být dle aktivity onemocnění různé reaktivní změny, zejména organizující se pneumonie, podrobně jsou uvedeny v tabulce 1. Eozinofilní granulomatóza s polyangiitidou má morfologický nález velmi podobný, navíc nacházíme typicky astmatické změny na bronších. V zánětlivém infiltrátu mají převahu eozinofilní granulocyty (v menší míře mohou být i u granulomatózy s polyangiitidou), charakteristické jsou mikroabscesy s četnými eozinofily a eozinofilním detritem, tyto formace jsou někdy označovány jako eozinofilní granulom. V okolí často nacházíme obraz eozinofilní pneumonie. Obecně u onemocnění, kde je pro diagnózu podstatná přítomnost eozinofilů, je třeba dát pozor na event. anamnézu aplikace kortikosteroidů před odběrem biopsie, následkem bývá dramatické snížení počtu eozinofilů v zánětlivém infiltrátu a výrazné ztížení našich diagnostických možností.Stran speciálních barvení je pro diagnostiku vaskulitidy nutné dobré barvení na elastická vlákna a speciální barvení na vyloučení infekční etiologie, vhodné je i barvení na železo za účelem ozřejmení oblastí proběhlé kapilaritidy (13-15).
Obr. 4. Žena 74 let, resekce části plíce pro infiltrativní plicní proces v bazálních segmentech vlevo. Pacientka vyšetřována jako suspekce na tumor, z předcházející jehlové biopsie pouze diagnóza zánětlivých změn. 
A, B. Vaskulitida (hematoxylin-eozin a van Gieson-elastika, zvětšení 100x). C. Menší granulom s palisádou epiteloidních buněk s neutrofily v centru (hematoxylin-eozin, zvětšení 100x). Pacientka v době biopsie bez klinické suspekce na vaskulitidu, proto histologie z tohoto materiálu uzavírána opatrně s navržením diagnózy granulomatózy s polyangiitidou na prvním místě. Následně klinicky pozitivita ANCA protilátek a v následné biopsii ledvin nález také kompatibilní s granulomatózou s polyangiitidou ASPIRACE
Aspirace je relativně častá a je velmi poddiagnostikovaná. Morfologické změny při aspiraci jsou charakteristické přítomností cizorodého materiálu a mnohojaderných buněk typu z cizích těles. V okolí bývají zánětlivé změny různého stáří často i ve formě abscesů s mikrobiálními elementy. Bývá patrna xantogranulomatózní zánětlivá reakce, organizující se pneumonie apod. Cizorodý materiál je dobré odlišit od konchoidních inkluzí u sarkoidózy; oxalátové krystaly, které bývají někdy přítomny u aspergilózy, mohou mít také reakci typu z cizích těles. Při opakovaných aspiracích mohou fibrózní změny v plíci připomínat až intersticiální plicní onemocnění (10,16,17).
REVMATOIDNÍ UZEL
Revmatoidní artritida je ze systémových onemocnění pojiva asi nejčastějším onemocněním s postižením plicního parenchymu, může být i prvním projevem onemocnění. Postižení může mít několik různých vidů, jednak difúzní postižení plicního parenchymu a/nebo přítomnost revmatoidních uzlů (kombinace těchto dvou nálezů je pro revmatoidní artritidu vysoce charakteristická). Revmatoidní artritida jako taková bývá častěji u žen, postižení plic však mívají častěji spíše muži.Co se týká postižení plicního parenchymu, poměrně charakteristickým znakem je přítomnost chronické zánětlivé infiltrace, nejtypičtěji ve formě lymfoidní hyperplázie (i s přítomností lymfatických foliklů) zejména ve sliznici bronchiolů (tzv. folikulární bronchiolitidy) a chronické zánětlivé infiltrace pleury. Vlastní plicní parenchym může mít změny charakteru jakéhokoliv plicního intersticiálního procesu, nejčastěji nespecifické intersticiální pneumonie – NSIP (spíše její celulární varianty), při větší lymfoidní infiltraci až lymfoidní intersticiální pneumonie – LIP, kdy je třeba diferenciálně diagnosticky zvažovat i MALT lymfom, do kterého onemocnění může progredovat. V některých případech můžeme najít i obraz běžné intersticiální pneumonie – UIP, obvykle nás ke správné etiologii dovede právě výše zmíněné chronické zánětlivé postižení pleury a míra zánětlivé celulizace.Revmatoidní uzel (obr. 5) je obvykle klínovité subpleurálně uložené ložisko nekrózy s jemně eozinofilním granulárním detritem, ve kterém bývá v barvení na elastická vlákna dobře patrná původní struktura plicního parenchymu. Na okraji léze bývá palisáda epiteloidních buněk. Ložiska se mohou vyskytovat vícečetně v různých lokalitách, obvykle však subpleurálně. I v případě zcela typického nálezu je třeba nález korelovat s klinikou a zejména pečlivě vylučovat možnost infekční etiologie (pacienti k ní mají predispozici v důsledku iatrogenní imunosuprese při terapii základního onemocnění). Z jiných postterapeutických změn je diferenciálně diagnosticky nutno pamatovat také na polékové postižení plic při léčbě metotrexátem, které se projevuje drobnými (sarcoid-like) granulomy. Nález může činit značné obtíže jak stran vyloučení infekční etiologie, tak i v diferenciální diagnóze s hypersenzitivní pneumonií případně sarcoid-like reakcí na MALT lymfom (18-22).
Obr. 5. Muž 53 let, konzultační případ, tři bloky z resekce ložiska v plíci. 
A, B. Ložisko tvořeno amorfně vyhlížejícím materiálem, v barvení na elastická vlákna zachována původní struktura plicního parenchymu (hematoxylin-eozin a van Gieson-elastika, zvětšení 20x). C. detail na epiteloidní histiocyty na okraji ložiska (hematoxylin-eozin, zvětšení 200x). Negativní speciální barvení na mykózy a mykobakteria, negativní PCR na mykobakteria, v přilehlé plicní tkáni četnější lymfocyty peribronchiolárně. Nález uzavírán s navržením diagnózy postižení plíce při revmatoidní artritidě (revmatoidní uzel), odpovídající kliniku se nepodařilo dozjistit. PNEUMOKONIÓZY
Z pneumokonióz nejčastěji tvoří nodulární formace chronická silikóza. Typicky jde o tzv. silikotické uzlíky (obr. 6) – tj. cirkulárně formovaná ložiska hyalinně fibrózních struktur v perilymfatické lokalizaci, v polarizovaném světle najdeme velmi drobné jehlicovité krystaly stáčející rovinu polarizovaného světla. Uzlíky mohou měřit od několika milimetrů až do 1 cm v průměru. V časných lézích nacházíme v hypocelulárním pojivu ještě zbytky makrofágů vytvářejících lem v okolí fibrotického centra. Starší léze jsou již prakticky bezbuněčné, často dystroficky kalcifikované či dokonce osifikované. V průběhu progrese onemocnění mají uzly tendenci splývat a tvořit objemnější masy. Pokud takto splývající fibrotická ložiska měří více než 2 cm v průměru, hovoříme o konglomerátech. Maximum změn bývá obvykle v horních plicních polích (i s fibrózou subpleurálně), typické je paralelní postižení silikotickými uzlíky v hilových a mediastinálních lymfatických uzlinách. Noduly by neměly obsahovat nekrózu. Pokud se tak stane, může jít o kombinaci silikózy s revmatoidní artritidou (tzv. Caplanův syndrom) nebo infekcí, proto by takováto ložiska měla být vyšetřována speciálními barveními (23-26).
Další pneumokoniózou s diferenciální diagnózou směrem ke granulomatózním zánětům je berrylióza, která má morfologii prakticky neodlišitelnou od sarkoidózy (27,28).
Obr. 6. Muž 87 let, pitevní nález rozsáhlého fibrózně nodulárního postižení plic převážně v horních lalocích u pacienta s karcinomem prostaty, trombo/embolickými komplikacemi (paraneoplastické etiologie?) a čerstvou malacií v mozku. Profesionální anamnézu se z dokumenace nepodařilo zjistit (nicméně bydliště v hornické lokalitě). Typická morfologie cirkulárně (cibulovitě) uspořádané fibrózy v silikotickém uzlíku při těžké antrakosilikóze. 
KLÍČ K URČOVÁNÍ ETIOLOGIE GRANULOMATÓZNÍCH FORMACÍ V PLICÍCH
převážně dle Hutton Klein JR (29)
NEKRÓZA
ano:
- infekce (pokud je nekróza popraškového typu je diferenciálně diagnosticky na prvním místě tuberkulóza)
- vaskulitidy (granulomatóza s polyangiitidou má typicky nekrózu s neutrofily, často jde o velké mapovité nekrózy; eozinofilní granulomatóza s polyangiitidou má nekrózu drobnější s eozinofily)
- revmatoidní uzel (palisáda epiteloidních histiocytů na okraji, v barvení na elastická vlákna zůstává zachována původní struktura plicního parenchymu)
ne:
- sarkoidóza, některé infekce (zejména atypická mykobakterióza), silikóza
MATERIÁL STÁČEJÍCÍ ROVINU POLARIZOVANÉHO SVĚTLA
- silikóza (jehlicovité krystaly)
- sarkoidóza (konchoidní inkluze)
- aspirovaný materiál
VELMI DROBNÁ VELIKOST GRANULOMŮ
- sarcoid-like reakce – reakce na cokoliv (často paraneoplastická reakce)
- hypersenzitivní pneumonie – drobné granulomy v okolí drobných bronchiolů, v akutní fázi s lymfocyty, v chronické fázi s fibrózní reakcí
LOKALIZACE GRANULOMŮ
- perilymfatická lokalita:
- sarkoidóza
- pneumokoniózy
- vztah k bronchu
- peribronchiolární granulomy:
- hypersenzitivní pneumonie
- postižení bronchu bez destrukce:
- sarkoidóza
- bronchiolitida s nekrózou epitelu:
- infekce
- velmi vzácně granulomatóza s polyangiitiou
- postižení cév
- bez destrukce:
- velmi časté (infekce, nekrotizující sarkoidní granulomatóza…)
- destrukce stěny cév:
- barvení na elastická vlákna vaskulitidy
ZÁVĚR
V problematice granulomatózních plicních lézí je asi nejdůležitějším faktorem určení etiologie: je buď infekční, nebo jde o nějaký projev patologické reakce imunitního systému pacienta; od toho se odvíjející terapie je buď na infekci (antibiotika, antituberkulotika, antimykotika), nebo imunosupresivní. Je zjevné, že tyto terapeutické modality jdou zásadně proti sobě, proto je naším hlavním úkolem vyloučit infekční etiologii. Kromě klasických speciálních metodik je vhodné používat molekulárně genetické metody, a pokud se dostaneme k nativnímu materiálu, je zásadní neopomenout zajistit materiál na kultivační vyšetření. Dále je nutné pamatovat na možnost, že pacienti chronicky léčení imunosupresí (např. pro granulomatózu s polyangiitidou, revmatoidní artritidu apod.) jsou náchylnější i infekcím a v průběhu onemocnění mohou mít kromě základní léze i infekční komplikaci, přičemž její morfologie může být kvůli léčbě atypická. Bohužel i ve velkých studiích z renomovaných pracovišť zůstává etiologie minimálně třetiny granulomatózních procesů nejasná (29,30).
PODĚKOVÁNÍ
Vřelé poděkování patří spolupracujícím klinikům (Plicní klinika, Radiologická klinika, oddělení hrudní chirurgie Kardiochirurgické kliniky, Ústav klinické mikrobiologie FN HK) i patologům obohacujícím naše zkušenosti dodáváním zajímavých konzultačních případů.
Práce vznikla za částečné podpory projektů PRVOUK P37/11 a P27/LF1/1, OPPK CZ.2.16/3.1.00/24509 a BBMRI LM2010004.
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Adresa pro korespondenci:
MUDr. Helena Hornychová, Ph.D.
Fingerlandův ústav patologie
Fakultní nemocnice Hradec Králové
Sokolská 581,
500 05 Hradec Králové
tel.: 495832238
e-mail: hornyhel@gmail.com
Zdroje
1. Rosati LA, Leslie KO. Lung infections. In: Leslie KO, Wick MR. Practical pulmonary pathology (2nd ed). Philadelphia: Elsevier; 2011 : 159-187.
2. Irion LD, Woodhead M. Pulmonary mycobacterial infections. In: Hasleton P, Flieder DB. Spencer´s Pathology of the lung (6th ed). Cambridge University Press; 2013 : 206-225.
3. Khayyata S, Moore CB, Richardson MD, Hasleton P, Farver C. Pulmonary mycotic infections. In: Hasleton P, Flieder DB. Spencer´s Pathology of the lung (6th ed). Cambridge university press; 2013 : 226-287.
4. Travis WD, Colby TV, Koss MN, Rosado-de-Christenson ML, Müller NL, King TE. Non-neoplastic disorders of lower respiratory tract. Washington: Armed Forces Institute of Pathology; 2002 : 579-592 a 616-632.
5. Tomashefski JF, Farver CF. Tuberculosis and nontuberculous mycobacterial infections. In: Tomashefski JF, Cagle PT, Farver CF, Fraire AE. Dail and Hammar´s Pulmonary pathology (3rd ed). New York: Springer; 2008 : 316-348.
6. Haque AK, McGinnis MR. Fungal infections. In: Tomashefski JF, Cagle PT, Farver CF, Fraire AE. Dail and Hammar´s Pulmonary pathology (3rd ed). New York: Springer; 2008 : 375-391.
7. Vašáková M, Polák J, Matěj R. Intersticiální plicní procesy. Praha: Maxdorf; 2011 : 201-221.
8. Farver CF. Sarcoidosis. In: Tomashefski JF, Cagle PT, Farver CF, Fraire AE. Dail and Hammar´s Pulmonary pathology (3rd ed). New York: Springer; 2008 : 668-694.
9. Fukuoka J, Leslie KO. Chronic diffuse lung disases. In: Leslie KO, Wick MR. Practical pulmonary pathology (2nd ed). Philadelphia: Elsevier; 2011 : 250-252.
10. Rossi G, Cavazza A, Colby TV. Pathology of Sarcoidosis. Clin Rev Allergy Immunol 2015; 49(1): 36-44.
11. Rosen Y. Four decades of necrotizing sarcoid granulomatosis: what do we know now? Arch Pathol Lab Med 2015; 139(2): 252-262.
12. Jennette JC, Falk RJ, Bacon PA, et al. 2012 revised International Chapel Hill Consensus Conference Nomenclature of Vasculitides. Arthritis Rheum 2013; 65(1): 1-11.
13. Vašáková M, Polák J, Matěj R. Intersticiální plicní procesy. Praha: Maxdorf; 2011 : 312-329.
14. Travis WD, Colby TV, Koss MN, Rosado-de-Christenson ML, Müller NL, King TE. Non-neoplastic disorders of lower respiratory tract. Washington: Armed Forces Institute of Pathology; 2002 : 233-248.
15. Travis WD, Leslie KO, Beasley MB. Pulmonary vasculitis and pulmonary hemorrhage. In: Leslie KO, Wick MR. Practical pulmonary pathology (2nd ed). Philadelphia: Elsevier; 2011 : 341-354.
16. Tomashefski JF, Dail DH. Aspiration, bronchial obstruction, bronchiectasis, and related disorders. In: Tomashefski JF, Cagle PT, Farver CF, Fraire AE. Dail and Hammar´s Pulmonary pathology (3rd ed). New York: Springer; 2008 : 84-94.
17. Mukhopadhyay S, Katzenstein AL. Pulmonary disease due to aspiration of food and other particulate matter: a clinicopathologic study of 59 cases diagnosed on biopsy or resection specimens. Am J Surg Pathol 2007; 31(5): 752-759.
18. Vašáková M, Polák J, Matěj R. Intersticiální plicní procesy. Praha: Maxdorf; 2011 : 293-298.
19. Travis WD, Colby TV, Koss MN, Rosado-de-Christenson ML, Müller NL, King TE. Non-neoplastic disorders of lower respiratory tract. Washington: Armed Forces Institute of Pathology; 2002 : 293-300.
20. Butnor KJ, Khoor A. Collagen vascular diseases and disorders of connective tissue. In: Tomashefski JF, Cagle PT, Farver CF, Fraire AE. Dail and Hammar´s Pulmonary pathology (3rd ed). New York: Springer; 2008 : 725-730.
21. Fukuoka J, Leslie KO. Chronic diffuse lung disases. In: Leslie KO, Wick MR. Practical pulmonary pathology (2nd ed). Philadelphia: Elsevier; 2011 : 231-233.
22. Schneider F, Gruden J, Tazelaar HD, Leslie KO. Pleuropulmonary pathology in patients with rheumatic disease. Arch Pathol Lab Med 2012; 136(10): 1242-1252.
23. Vašáková M, Polák J, Matěj R. Intersticiální plicní procesy. Praha: Maxdorf; 2011 : 243-268.
24. Travis WD, Colby TV, Koss MN, Rosado-de-Christenson ML, Müller NL, King TE. Non-neoplastic disorders of lower respiratory tract. Washington: Armed Forces Institute of Pathology; 2002 : 803-814.
25. Sporn T, Roggli VL. Pneumoconioses, mineral and vegetable. In: Tomashefski JF, Cagle PT, Farver CF, Fraire AE. Dail and Hammar´s Pulmonary pathology (3rd ed). New York: Springer; 2008 : 911-918.
26. Butnor KJ, Roggli VL. Pneumoconioses. In: Leslie KO, Wick MR. Practical pulmonary pathology (2nd ed). Philadelphia: Elsevier; 2011 : 311-317.
27. Sporn T, Roggli VL. Pneumoconioses, mineral and vegetable. In: Tomashefski JF, Cagle PT, Farver CF, Fraire AE. Dail and Hammar´s Pulmonary pathology (3rd ed). New York: Springer; 2008 : 923-924.
28. Butnor KJ, Roggli VL. Pneumoconioses. In: Leslie KO, Wick MR. Practical pulmonary pathology (2nd ed). Philadelphia: Elsevier; 2011 : 332-333.
29. Hutton Klein JR, Tazelaar HD, Leslie KO, Colby TV. One hundred consecutive granulomas in a pulmonary pathology consultation practice. Am J Surg Pathol 2010; 34(10): 1456-1464.
30. Mukhopadhyay S, Farver CF, Vaszar LT, et al. Causes of pulmonary granulomas: a retrospective study of 500 cases from seven countries. J Clin Pathol 2012; 65(1): 51-57.
Štítky
Patológia Súdne lekárstvo Toxikológia
Článek Jaká je Vaše diagnóza?
Článok vyšiel v časopiseČesko-slovenská patologie

2016 Číslo 2-
Všetky články tohto čísla
- Intersticiální plicní onemocnění asociovaná s kouřením
- Stručne o kongrese digitálnej patológie v Londýne
- Jaká je Vaše diagnóza?
- Non-traumatická arteriovenózna malformácia sleziny s fatálnym krvácaním
- Vzpomínka na prof. MUDr. Dagmar Kalouskovou, Ph.D.
- Jaká je Vaše diagnóza? Odpověď
- Meningoteliální hamartom měkkých tkání hlavy
- Prof. MUDr. Aleš Rejthar, CSc. (1938 – 2015)
- Intersticiální plicní procesy
- With the winner of the Bednář Award 2015
- MONITOR aneb nemělo by vám uniknout, že
- Histopatologické principy vyšetření intersticiálních plicních procesů
- Idiopatická plicní fibróza - problematika multidisciplinární diagnostiky a léčby ve světle nových poznatků
- Diferenciální diagnostika granulomatózních procesů v plicích
- Česko-slovenská patologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Diferenciální diagnostika granulomatózních procesů v plicích
- Intersticiální plicní onemocnění asociovaná s kouřením
- Idiopatická plicní fibróza - problematika multidisciplinární diagnostiky a léčby ve světle nových poznatků
- Histopatologické principy vyšetření intersticiálních plicních procesů
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy










