-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Prevence osteoporózya sarkopenie
Prevention of osteoporosis and sarcopenia
This review presents an overview of the available information concerning pathogenesis of osteoporosis, relationship between peak bone mass, bone remodelling and the loss of bone mass. Main risk factors are mentioned as well as additional potentiating factors. Special attention is paid to possible kinds of prevention. Sarcopenia is discussed as one of the main factors of loss of independency – its pathogenesis, potentiating factors, prevention and treatment.
Keywords:
osteoporosis – bone remodelation – risk factors – sarcopenia – independency
Autoři: H. Matějovská Kubešová
Působiště autorů: Klinika interní, geriatrie a praktického lékařství LF MU a FN Brno
Vyšlo v časopise: Geriatrie a Gerontologie 2013, 2, č. 4: 213-215
Kategorie: Přehledové články
Souhrn
Přehledový článek předkládá souhrnné informace o patogeneze osteoporózy, vztahu vrcholové kostní hmoty, kostní remodelace a rychlosti úbytku kostní hmoty. Jsou zmíněny hlavní rizikové faktory vzniku osteoporózy a další faktory toto riziko potencující. Zvláštní pozornost je věnována možným způsobům prevence osteoporózy. Dále je diskutována problematika sarkopenie jako jednoho z hlavních faktorů ztráty soběstačnosti – její patogeneze, potencující faktory a možnosti prevence a léčby.
Klíčová slova:
osteoporóza – kostní remodelace – rizikové faktory osteoporózy – sarkopenie – soběstačnostVznik osteoporózy
Pevnost a integrita skeletu závisí na procesu kostní remodelace, což je trvalá obměna kosti představovaná permanentní kontrolovanou resorpcí kosti osteoklasty s následnou náhradou kosti pomocí kostních buněk osteoblastů. K remodelaci dochází v diskrétních úsecích nazývaných kostní remodelační jednotky. Nerovnováha mezi kostní resorpcí a kostní formací vede k osteoporóze, pokud převáží osteoresorpce, nebo osteopetróze, pokud převáží osteoapozice. Na celé této přestavbě se účastní celá řada růstových faktorů, cytokinů, stejně jako systémových peptidů a steroidních hormonů, jež regulují diferenciaci nezralých prekurzorových buněk a aktivitu zralých buněk jak do osteoklastické, tak do osteoblastické řady. Celý remodelační cyklus trvá přibližně4 měsíce a vlastnosti nově vzniklé kosti závisí na podmínkách, za kterých proces probíhá. V mladším věku probíhá proces kostní remodelace s převahou novotvorby a vytváří se kost o vysoké denzitě. Tento proces trvá přibližně do 30 roku věku, kdy končí budování tzv. vrcholové kostní hmoty. Ve vyšším věku je výrazná tendence ke zpomalení fáze novotvorby kosti, proto je výraznější tendence ke ztrátě kostní denzity, tedy ke vzniku osteoporózy. Remodelace probíhá v kortikální kosti asi z 30 %, v trabekulární (trámčité) kosti asi ze 70 %(1).
Postmenopauzální osteoporóza
Tento typ osteoporózy je nutno očekávat u 33 % žen po přirozené menopauze a až u 50 % žen po menopauze navozené. Postmenopauzální osteoporózou je nejvíce postižena kost trámčitá a typickou frakturou pro tento věk je kompresivní fraktura nejčastěji bederních obratlů. Ve věku nad 70 let se vyvíjí osteoporóza senilní postihující také kost kortikální. Tento typ osteoporózy se vyskytuje u 50 % žen po přirozené menopauze a až u dvou třetin žen po menopauze navozené, postihuje také přibližně čtvrtinu mužů a typickou frakturou je zlomenina krčku kosti stehenní.
Význam základních faktorů podílejících se na výstavbě kostní tkáně a její remodelaci, tedy parathormonu, kalcitoninu, vitaminu D, vápníku a zátěže kosterního systému jsou známy již dlouhou dobu. Za hlavní patogenetický proces vzniku osteoporózy ve vyšším věku je stále považován pokles hladiny kalcia, který vede ke zvýšení produkce parathormonu vyplavujícího vápník z kostí k vyrovnání hladiny. Částečně se však toto doplnění děje na úkor kvality kostní hmoty.
Z dalších faktorů, které ovlivňují novotvorbu kosti, jsou nejmocnějšími ve smyslu pozitivním estrogeny a růstový hormon, ve smyslu negativním glukokortikoidy a velké dávky tyroxinu(2).
Tab. 1. Anamnestické údaje upozorňující na možnost existence osteoporózy 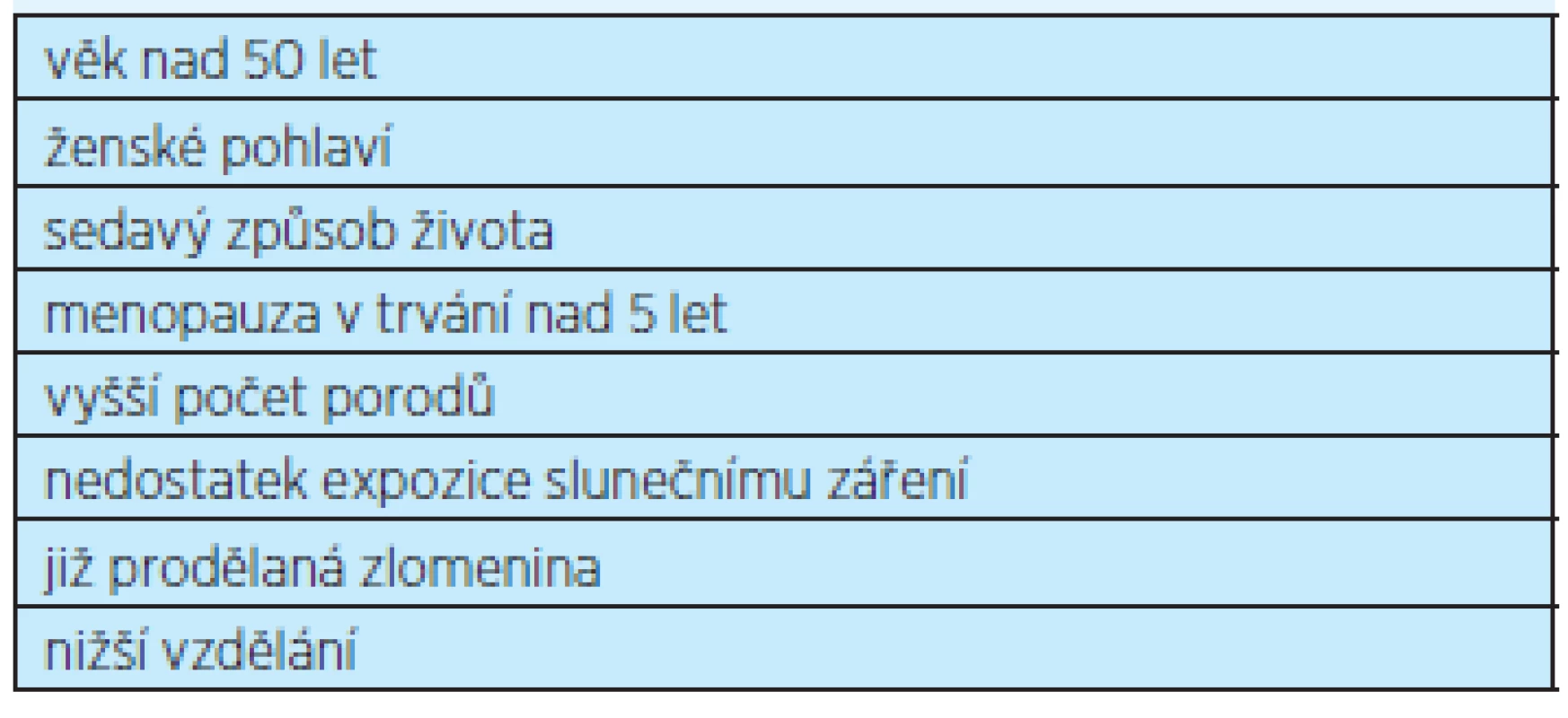
Komplikace osteoporózy
Riziko zlomeniny kyčle zvyšuje nízký příjem kalcia o 50 %, nízká fyzická aktivita o 40 %, hubenost o 100 %, prodělaná zlomenina obratle o 320 %, osteoporotická zlomenina u matky o 50 % a kouření o 30 %(1).
Příznaky subjektivní i objektivní se až do rozvoje komplikací projevují nenápadně a dokonce i zdánlivě nesouvisí s kostním metabolismem. Pořadí kostí, ze kterých kostní hmoty ubývá nejdříve, je: čelist, kosti lebeční, žebra, obratle a dlouhé kosti. Ztráta kostní hmoty čelisti je doprovázena ztrátou opory pro chrup, ztráta v oblasti lebečních kostí a žeber činí své nositele náchylné ke zraněním při případných pádech ve vyšším věku.
Jedním ze zjevných projevů ztráty kostní hmoty v obratlích je ztráta tělesné výšky a narůstání hrudní kyfózy, které vede změnou statiky páteře k chronické bolesti dolní části zad. Komplikace osteoporózy znamenají u žen s postmenopauzálními změnami nejčastěji kompresivní zlomeniny obratlů v bederní oblasti z důvodu výraznějšího postižení trámčité kosti, u seniorů ve věku nad 75 let s vyšším podílem osteoporózy kortikální jsou nejobávanější komplikací zlomeniny proximálního femuru.
Prevence osteoporózy
Z hlediska prevence je nejzásadnější pojem tzv. vrcholová kostní hmota, kterou si každý jedinec vytváří do 30. roku věku a z této zásoby potom čerpá až do konce svého života. Čím menší je vytvořená rezerva, tím dříve se vyvine osteoporóza.
Pro prevenci postmenopauzálních změn skeletu je již dlouho využívána suplementace estrogenů (hormonal replacement therapy – HRT) v časné postmenopauze. Za dobu využívání této nepochybně účinné metody v široké populaci se však nashromáždily i poznatky poněkud zužující dřívější masivní používání. Zvláštní opatrnosti je třeba u žen s pozitivní rodinnou anamnézou tromboembolické nemoci vzhledem k tušenému a postupně odkrývanému výskytu vrozených trombofilií. Tento typ prevence je zcela nevhodný u žen s rizikem či dokonce již anamnézou onkologické malignity. Proto současná doporučení hovoří o kalkulaci rizika vzniku osteoporózy a rizika HRT u konkrétní pacientky a o neprodlužování této terapie na dobu delší než 3–5 let(3) .
Zvláštní skupinu z hlediska rizika rozvoje osteoporózy představují nemocní s intolerancí či malabsorpcí laktózy vzhledem k jejich nízkému příjmu vápníku a vitaminu D. Výskyt těchto poruch v populaci není přesně zmapován – ne každý nemocný s poruchou resorpce laktózy má klinické příznaky a ne každý nemocný s klinickými příznaky intolerance má poruchu absorpce(4).
Náležitou pozornost je nutno věnovat i skupinám nemocných léčených dlouhodobě steroidy pro chronické střevní záněty, chronickou obstrukční plicní nemoc, těžší formy bronchiálního astmatu, systémové choroby pojiva. U těchto skupin nemocných je doporučováno podávat preparáty kalcia a vitaminu D souběžně se steroidní léčbou a pravidelně kontrolovat kostní denzitu(5, 6).
Sarkopenie
Příčně pruhovaný sval člověka se skládá z vláken, která jsou trojího typu. Pomalá vlákna I. typu, zvaná tonická, jsou tenká (50 µm), obsahují pomalou formu myosinu a podílejí se především na udržování svalového tonu, polohy a na svalových činnostech o nízké intenzitě. Jsou vývojově starší. Zajišťují stoj, kontrolu polohy trupu i končetin, držení či pomalou chůzi, podílejí se na vzpřimovacích a posturálních reflexech. Jsou nejpomaleji unavitelná a uvedené bazální svalové činnosti mohou zajišťovat po dlouhou dobu. Fázická rychlá vlákna 2. typu jsou silnější (80–100 µm) a obsahují rychlou izoformu myosinu. Z hlediska funkčního se fázická vlákna rozdělují na červená a bílá lišící se především oxidativní kapacitou, která je u červené formy velmi vysoká, zatímco u bílé nízká. Obě formy se podílí na zajištění rychlých krátkých kontrakcí o velké síle. Fázická vlákna zajišťují rychlé svalové pohyby, jako je rychlá odpověď ve smyslu obranného reflexu na míšní úrovni, úhybu, úderu, běhu(1).
Stárnutí svalu je charakterizováno zmenšením objemu, poklesem síly, výdrže, poddajnosti, a rychlosti kontrakce – to vše významně zvyšuje riziko pádu. Úbytek svaloviny je zčásti kryt zmnožením tukové tkáně. Histologicky je prokazována atrofie myocytů se selektivním úbytkem rychlých vláken 2. typu, zmnožením vaziva a ukládáním lipofuscinu, detailní osvětlení procesů spjatých s tzv. apoptózou myocytu však zatím nemáme(7). Vedou se také diskuse o vzájemných souvislostech dynapenie a sarkopenie – zda prvotní je omezení pohybu s následným postižením svalu, či naopak(8).
Inaktivita a neurogenní postižení
Za rozhodující pro rozvoj změn svalové změny je považována inaktivita a neurogenní postižení. U dlouhodobě imobilizovaných mladých lidí se vyvíjí změny neodlišitelné od starších imobilizovaných. Biopsie prokázala naopak minimální změny u pohybově velmi aktivních mužů na počátku sénia ve srovnání s muži mladými. Po zahájení tréninku se upravoval „involuční“ úbytek motorických jednotek i rychlých vláken, zvyšovala se síla. Nejkonstantnější involuční změnou se zdá být zpomalení rychlosti kontrakce, které pravděpodobně souvisí se zpomalením přenosu na nervosvalové ploténce. Přes zjevný podíl inaktivity a denervačních změn však je involuční úbytek svalové hmoty, označovaný jako sarkopenie, nesporný. V současnosti se považuje za nejpravděpodobnější příčinu působení oxidačního stresu a volných radikálů produkovaných svalovými mitochondriemi(9). Významné pro urychlení involučních svalových změn jsou i deficity mikronutrientů – vitaminů, zvláště vitaminu D a železa. Další vlivy, kterým je přičítána role při vzniku sarkopenie, jsou: zvýšená zánětlivá aktivita, změny v hladinách hormonů a poruchy výživy(10).
Přítomnost sarkopenie znamená pro staršího člověka snížení svalové síly, obratnosti, rychlosti a z toho plynoucí riziko pádů, při současné osteoporóze se násobí riziko vzniku závažných komplikací pádů v podobě zlomenin. Přítomnost sarkopenie znamená dvanáctinásobné zvýšení rizika osteoporózy, dvojnásobné riziko pádu v průběhu jednoho roku a téměř trojnásobné zvýšení rizika vzniku osteoporotické fraktury(11).
Další bludnou spirálou je úbytek svalových vláken čtyřhlavého svalu stehenního, zhoršující extenzi kolenního kloubu, následovanou úbytkem aktivního pohybu seniora pro pocit slabosti dolních končetin. Důsledkem je nárůst tělesné hmotnosti se vznikem abdominální obezity a dalším zhoršením stability(12). Sarkopenie má i významné důsledky metabolické – přiměřená svalová hmota vyvíjející přiměřenou aktivitu je významným regulátorem glykemie.
Do komplexního obrazu seniora v riziku pádů je nutno zakalkulovat i depresi, která se vzájemně oboustranně s rizikem pádů potencuje. Naopak řešení deprese může zlepšit adherenci nemocného k terapii osteoporózy či sarkopenie a preventivním opatřením proti pádům(13).
Průběh již přítomné sarkopenie je možno i ve vysokém věku příznivě ovlivnit dostatečnou dodávkou aminokyselin ve stravě v kombinaci se silovým cvičením, jako zvláště vhodné jsou označovány bílkoviny s vyšším obsahem leucinu(14, 15, 16). Jako účinnější v příznivém ovlivnění sarkopenie se jeví podávání proteinů, aminokyselin a antioxidantů v návaznosti na cvičení(17).
V doporučeních pro léčbu sarkopenie jsou zmiňována i anabolika zvláště pro nemocné s omezenou možností silového cvičení(18), u seniorů je však nutné mít na paměti jejich významné nežádoucí účinky jako je retence tekutin, iontové dysbalance, kolísání krevního tlaku apod.
Je však nutno konstatovat, že byť od zavedení pojmu sarkopenie jako označení změn svalové hmoty ve stáří uplynulo již 20 let, není doposud jednota v kritériích při diagnostice sarkopenie ani v doporučeních její terapie(16).
Prevence u mladých jedinců
Z hlediska celkové péče o stárnoucí populaci je nutno při současném životním stylu mladé a střední generace počítat s obrovským nárůstem projevů osteoporózy a sarkopenie právě v podobě pádů s následnými zlomeninami, ztrátou soběstačnosti a ztrátou schopnosti života ve vlastním prostředí. Běžně se odhaduje 50-100% nárůst ve srovnání s dnešní dobou, kdy do seniorského věku dospívá generace, která v mladším věku měla obecné životní podmínky sice horší, ale pro tvorbu vrcholové kostní hmoty významně lepší.
Pokud máme účinně zasáhnout do tohoto nepříznivého trendu, je třeba masivní informační kampaně oslovující tu část populace, které se bezprostředně týká vytváření vrcholové kostní hmoty, tedy adolescenty a mladé dospělé. Životní styl této části populace je v posledních desetiletích nastaven velmi nepříznivě právě z pohledu vytváření vrcholové kostní hmoty, a to jak z hlediska nízké zátěže kosterního systému, tak i z hlediska nepříznivých stravovacích návyků a nízké dodávky vitaminu D nedostatečným pobytem mimo budovy.
Mladou a střední generaci je nutno motivovat ve smyslu cíleného zvýšení pohybové aktivity, udržování svalové síly a obratnosti, starší střední generaci a mladší seniorskou generaci je potom nutno stimulovat z hlediska příjmu vitaminu D a kalcia jako nenáročné, levné a velmi účinné prevence vzniku osteoporózy, ale i podpory svalové hmoty. Dnes už jsou k dispozici data svědčící pro 75% snížení výskytu osteoporózy u skupiny seniorů, kterým byl po dobu 10 let pravidelně dodáván vitamin D a vápník.
prof. MUDr. Hana Matějovská Kubešová, CSc.
Klinika interní, geriatrie a praktického lékařství LF MU a FN Brno
prof. MUDr. Hana Matějovská Kubešová, CSc.
e-mail: hkubes@fnbrno.cz
Vysokoškolské vzdělání ukončila v roce 1982 na Lékařské fakultě Masarykovy univerzity v Brně, na téže fakultě absolvovala doktorské studium 1993, habilitační řízení 1997 i profesorské řízení 2003. Od roku 1999 je přednostkou Kliniky interní, geriatrie a praktického lékařství LF MU a FN Brno. V roce 2011 byla zvolena předsedkyní České gerontologické a geriatrické společnosti ČLS JEP.
Zdroje
1. Topinková E: Geriatrie pro praxi. Galén 2005.
2. Kalvach Z, Zadák Z, Jirák R et al.: Gerontologie a geriatrie. Grada Avicenum 2005.
3. Gass ML, Heights M, Manson JE et al.: The 2012 hormone therapy position statement of The North American Menopause Society. Menopause 2012; 19(3): 257–71.
4. Suchy FJ, Brannon PM, Carpenter TO et al.: NIH consensus development conference statement: Lactose intolerance and health. NIH Consens State Sci Statements 2010; 27(2): 1–27.
5. Kearney DM, Lockey RF et al.: Osteoporosis and asthma. Ann Allergy Asthma Immunol 2006; 96(6): 769–74.
6. Thanou A, Ali T, Haq O et al.: Utilization of preventive measures for glucocorticoid-induced osteoporosis among veterans with inflammatory bowel disease. ISRN Gastroenterol 2013 : 862312.
7. Marzetti E, Privitera G, Simili V et al.: Multiple pathways to the same end: mechanisms of myonuclear apoptosis in sarcopenia of aging. Scientific World Journal 2010; 19(10): 340–349.
8. Clark BC, Manini TM: Functional consequences of sarcopenia and dynapenia in the elderly. Curr Opin Clin Nutr Metab Care 2010; 13(3): 271–276.
9. Rossi P, Marzani B, Giardina S et al.: Human skeletal muscle aging and the oxidative system: cellular events. Curr Aging Sci 2008; 1(3): 182–91.
10. Jones TE, Stephenson KW, King JG et al.: Sarcopenia-mechanisms and treatments. J Geriatr Phys Ther 2009; 32(2): 39–45.
11. Sjöblom S, Suuronen J, Rikkonen T et al.: Relationship between postmenopausal osteoporosis and the components of clinical sarcopenia. Maturitas 2013; 75(2): 175–80.
12. Ochi M, Tabara Y, Kido T et al.: Quadriceps sarcopenia and visceral obesity are risk factors for postural instability in the middle-aged to elderly population. Geriatr Gerontol Int 2010; 10(3): 233–243.
13. Iaboni A, Flint AJ: The complex interplay of depression and falls in older adults: a clinical review. Am J Geriatr Psychiatry 2013; 21(5): 484–92.
14. Sakuma K, Yamaguchi A: Molecular mechanisms in aging and current strategies to counteract sarcopenia. Curr Aging Sci 2010; 3(2): 90–101.
15. Fujita S, Volpi E: Amino acids and muscle loss with aging. J Nutr 2006; 136, suppl 1 : 277–280.
16. Bautmans I, Van Puyvelde K, Mets T: Sarcopenia and functional decline: pathophysiology, prevention and therapy. Acta Clin Belg 2009; 64(4): 303–16.
17. Kim JS, Wilson JM, Lee SR: Dietary implications on mechanisms of sarcopenia: roles of protein, amino acids and antioxidants. J Nutr Biochem 2010; 21(1): 1–13.
18. Evans WJ: Skeletal muscle loss: cachexia, sarcopenia, and inactivity. Am J Clin Nutr 2010; 91(4): 1123S–1127S.
Štítky
Geriatria a gerontológia Praktické lekárstvo pre dospelých Protetika
Článok vyšiel v časopiseGeriatrie a Gerontologie
Najčítanejšie tento týždeň
2013 Číslo 4- S MUDr. Robertem Šáhó o dnešním pohledu na mukopolysacharidózy: Od fatální prognózy k novým nadějím a možnostem léčby
- Nejnovější pokroky v péči o pacienty s NCL2: Kauzální léčba je v Česku dostupná, klíčem k úspěchu je včasná diagnostika
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
-
Všetky články tohto čísla
- Má dáti – dal
- Alzheimerova demence – epidemie 21. století: můžeme a umíme jí předcházet?
- Genetika v terénní praxi
- Rizikové faktory trombózy
- Profylaxe tromboembolické nemoci
- Profylaxe posttraumatické epilepsie
- Prevence osteoporózya sarkopenie
- Sluneční záření a lidský organismus aneb „kam nechodí slunce, tam chodí lékař“
- Prevence infekcí očkováním jako celoživotní proces
- Diabetes mellitus – existují možnosti prevence?
- Zápis z mimořádného jednání výboru ČGGS ze dne 17. 7. 2013
- Zápis z jednání výboru ČGGS dne 18. 9. 2013
- Geriatrie a Gerontologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Profylaxe tromboembolické nemoci
- Profylaxe posttraumatické epilepsie
- Rizikové faktory trombózy
- Alzheimerova demence – epidemie 21. století: můžeme a umíme jí předcházet?
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy




