-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Studie evaporace vybraných cytostatik a propustnosti ochranných rukavic v rámci výzkumu profesní zátěže zdravotnických pracovníků exponovaných cytotoxickým protinádorovým léčivům (projekt CYTO)
Evaporation of Selected Cytotoxic Drugs and Permeation of Protective Gloves – Research into the Occupational Risks of Health Care Personnel Handling Hazardous Cytotoxic Drugs (CYTO Project)
Backgrounds:
The CYTO project studies an important aspect of healthcare provision -long term occupational exposure, both threshold and below-threshold, to chemical agents with carcinogenic and mutagenic properties, with the major focus on antineoplastic drugs. This contribution presents experimental results from the first stages of the project’s experimental work, i.e. an evaluation of the physico-chemical characteristics of cytostatic agents (evaporation) and an investigation into protective glove permeation. Materials and Methods: In co-operation with IUTA (Institut für Energie - und Umwelttechnik e.V., Duisburg, Germany), the vapour pressure of paclitaxel, doxorubicin and dacarbazine was measured following OECD guideline No. 104: Vapour pressure curve – vapour pressure balance. Furthermore, the evaporation of cytostatic drugs was examined in actual laboratory conditions by monitoring the airborne concentration using the passive sampling technique. Besides the evaporation of selected drugs, the permeation of cisplatin, cyclophosphamide, doxorubicin, 5-fluorouracil and paclitaxel through different types of gloves (vinyl, latex, nitrile) was assessed. Results: Although our experiments showed relatively slow evaporation of the evaluated cytostatic drugs (the highest pressure in paclitaxel was 0.024 Pa), equilibrium concentrations may go up to milligrams per cubic metre. Nevertheless, analytical measurements of airborne contamination did not confirm these concentration levels. The glove permeation experiments with cytostatics showed good resistance of nitrile gloves (which were impermeable to all five drugs). Other materials should be avoided while handling cytostatic agents (e.g. maximum permeation of cyclophosphamide through latex was 19 µg/sqcm/hr). Conclusion: Although the volatility of cytostatic agents is low, it cannot be neglected considering the chronic character of exposure. However, in order to estimate actual occupational exposure, future research should focus on the development of sensitive analytical methods. Nevertheless, dermal uptake is supposed to be the major route of exposure and use of protective gloves is necessary to minimize potential risks. Our simulated time-dependent permeation experiments with cytostatic agents and different glove materials showed that good protection is provided only by nitrile gloves. The results obtained in this study will be used for the modelling of exposure doses and health risk assessment in the subsequent stages of the CYTO research project.Key words:
cytostatics – vaporization – protective gloves – occupational safety
Autoři: L. Doležalová 1; P. Odráška 1,2; L. Gorná 1; M. Prudilová 1; R. Vejpustková 1; L. Bláha 1,2
Působiště autorů: Ústavní lékárna, Masarykův onkologický ústav, Brno 2RECETOX, Přírodovědecká fakulta MU, Brno 1
Vyšlo v časopise: Klin Onkol 2009; 22(5): 218-222
Kategorie: Původní práce
Souhrn
Východiska:
Projekt CYTO studuje významný aspekt poskytování zdravotní péče, kterým je profesní zátěž pracovníků dlouhodobě nakládajících látkami s rizikem karcinogenity a mutagenity v prahových a podprahových expozicích s hlavním akcentem na často používaná protinádorová léčiva. V tomto příspěvku jsou představeny výsledky prvních fází experimentální práce projektu, tj. studie fyzikálně chemických charakteristik cytostatik (evaporační charakteristiky) a propustnosti ochranných rukavic. Materiál a metody: Ve spolupráci s výzkumným ústavem IUTA (Institut für Energie - und Umwelttechnik e.V., Duisburg, Německo) byla hodnocena tenze par paklitaxelu, doxorubicinu a dakarbazinu. Měření bylo realizováno efuzní metodou pomocí vah pro měření tlaku par. V praxi byl evaporační potenciál cytostatických léčiv ověřen stanovením jejich koncentrací ve vzduchu pracovního prostředí za využití metod pasivního vzorkování. Kromě evaporace vybraných léčiv byla také stanovena prostupnost cisplatiny, cyklofosfamidu, doxorubicinu, fluorouracilu a paklitaxelu přes různé typy rukavic (vinyl, latex a nitril). Výsledky: Realizované experimenty prokázaly relativně pomalou evaporaci studovaných cytostatik (nejvyšší tlak páry stanoven pro paclitaxel: 0,024 Pa), nicméně v případě dosažení rovnovážného stavu mohou koncentrace ve vnitřním prostředí dosáhnout hodnot řádově až několika miligramů/m3. Reálná měření však tyto koncentrace v pracovním ovzduší nepotvrdily. Zkoušky prostupnosti cytostatik přes rukavice prokázali dobrou odolnost nitrilových rukavic (průnik nebyl pozorován ani u jednoho léčiva). Ostatní materiály nelze pro práci s cytostatiky doporučit (např. propustnost latexu pro cyklofosfamid činila až 19 µg/cm2/hod). Závěr: Ačkoli je volatilita cytostatik nízká, vzhledem k chronickému charakteru expozice ji nelze zanedbat. Pro odhad skutečných expozic pracovníků je však třeba zaměřit pozornost na vývoj citlivých analytických metod. Za hlavní cestu příjmu cytostatik je považován přestup přes kůži a používání ochranných rukavic je nutné pro minimalizaci možných rizik. Naše simulované časově závislé experimenty prostupnosti cytostatik různými typy ochranných rukavic ukázaly, že dobrou ochranu zaručují pouze nitrilové rukavice. Získané výsledky budou využity pro modelování expozičních dávek a výpočet rizika v dalších fázích řešení projektu CYTO.Klíčová slova:
cytostatika – odpařování – ochranné rukavice – bezpečnost práceÚvod
Chemoterapeutické látky (CL) vykazují mimo vlastní akutní toxicitu i vážné, dlouhodobé efekty jako karcinogenitu, mutagenitu, teratogenitu, hypersenzitivní reakce, endokrinní a imunní supresivní účinky [1–3]. Přestože naše legislativa ukládá povinnost kontroly kontaminace pracovního prostředí [4] a v literatuře lze nalézt odkazy na metodiky pro měření kontaminace při práci s CL [5], do běžné praxe nebyl doposud systematický monitoring zaveden. Při hodnocení zdravotních rizik vycházíme z obecného konsenzu bezprahového působení CL (dáno mutagennímí a karcinogenními účinky) a základním principem omezení rizik je snaha o snížení expozice na co nejmenší dosažitelnou úroveň [6]. Nejčastější praxí je, že pracovníci jsou odkázáni na dodržování pracovních postupů a jsou školeni pro případy úniku kontaminace a havárie.
V literatuře lze najít informace o expozici cytostatikům u různých zdravotnických pracovníků podílejících se na výrobě, přípravě a aplikaci těchto léčiv [7–10]. Kromě přímých expozic se studují také expozice nepřímé, ke kterým dochází při manipulacích s kontaminovaným materiálem, jako jsou obaly léčiv, ložní prádlo z lůžkových oddělení či odpady vznikající při sanitaci pracovního prostředí a hygienických zařízení [11–12]. I přes některé existující vědecké studie máme v našich podmínkách jen minimum dostupných informací o možných expozicích pracovníků. Na rozdíl např. od práce s ionizujícím zářením neexistují pro CL žádné dozimetry pro kontrolu expozice (kontaminace přijaté pracovníkem), ať už při přípravě CL, manipulaci s lahvičkami CL, připravenými infuzemi, či kontrolu kontaminace pracovního prostředí izolátoru, přípravny CL, skladu CL, aplikačního křesla apod. I přes řadu výzkumných prací není doposud k dispozici jednotná metodika hodnocení rizik a sledování expozice CL. Tato problematika je aktuálním předmětem výzkumu v Evropě [13] i v ČR prostřednictvím projektu CYTO (grant 2B06171 podporovaný MŠMT v rámci Národního programu výzkumu II v letech 2006–2010, http://www.cytostatika.cz).
Významným faktorem, který ovlivňuje zdravotní rizika CL, je vlastní příjem – tedy vstup cytostatik do organizmu. Na biologickém příjmu cytostatik při profesních expozicích se může podílet několik cest [14] – především dermální expozice, inhalace cytostatik ve formě aerosolu nebo par a orální příjem (např. při nedůsledném dodržování hygienických standardů či náhodnou ingescí při mimořádných, havarijních událostech).
Konkrétní dávky CL uvnitř exponovaného organizmu lze obtížně experimentálně stanovit. Pro jejich odhad lze však využít vhodných modelů expozice, které zohledňují (i) koncentrace látek v pracovním prostředí, (ii) parametry osudu látek (např. stabilita, evaporace a mobilita, prostupnost přes epitely, metabolizmus atd.) a (iii) parametry chování exponovaných osob (např. pobyt v kontaminovaném prostředí, četnost a doba kontaktu s kontaminovaným povrchem atd.). Kombinace těchto vstupních údajů ve vhodném modelu pak dovoluje realisticky odhadnout specifickou expoziční dávku, jež je základem výpočtu možného rizika [15].
I přes existenci některých dílčích studií [16–18] chybí doposud detailnější charakterizace fyzikálně chemických vlastností a dalších parametrů, které ovlivňují např. uvolňování cytostatik v pracovním prostředí a jejich vstupy do exponovaných osob. V tomto příspěvku jsou prezentovány výsledky našich experimentálních prací, které se zaměřily na studium evaporace cytostatik (s ohledem na výzkum možné respirační expozice CL), a studie prostupnosti CL přes různé typy ochranných rukavic (pro racionální odhad expozice dermální cestou). Nové výsledky jsou využitelné pro praktický management (nutnost užívání ochranných rukavic ze specifických materiálů a jejich pravidelné výměny), ale spolu s výstupy navazujících výzkumných aktivit (sledování hladin kontaminace CL na konkrétních zdravotnických pracovištích) poslouží také pro racionální výpočty případných zdravotních rizik.
Materiál a metody
Evaporace cytostatik
Důležitým parametrem pro posuzování evaporace chemických látek je tlak nasycených par (TP). Pro naše výzkumy byly vybrány CL z chemicky a strukturně různých skupin (tab. 1). Ve spolupráci s IUTA (Institut für Energie - und Umwelttechnik e.V., Duisburg, Německo) bylo provedeno experimentální stanovení evaporace paklitaxelu, doxorubicinu a dakarbazinu dle normované metodiky podle OECD [19]).
Tab. 1. Evaporační charakteristiky vybraných cytostatik (paklitaxelu, doxorubicinu a dakarbazinu) v porovnání s parametry pro vodu a ethanol. 
1 stanovení pomocí metodiky OECD 104 2 vypočtená koncentrace s využitím naměřených hodnot tlaku par [22] Studie výskytu CL ve vnitřním ovzduší
Návazně na výzkum evaporačních charakteristik byla realizována pilotní studie sledování CL ve vnitřním ovzduší Masarykova onkologického ústavu v Brně, která měla za cíl ověřit možné metody sledování kontaminace vzduchu. Ve spolupráci s výzkumným centrem RECETOX na Přírodovědecké fakultě Masarykovy univerzity v Brně bylo provedeno vzorkování vzduchu za pomoci pasivních vzorkovačů založených na bázi polyuretanových filtrů [20]. Vzorkovače byly instalovány do prostor místností intenzivně využívaných k práci s CL (přípravna a sklad CL ústavní lékárny MOÚ a denní stacionář MOÚ, obr. 1), jako negativní kontrola sloužila místnost s jiným využitím a bez kontaminační zátěže (přednášková místnost centra RECETOX, PřF MU). Filtry vzorkovačů byly exponovány 30 dnů, extrahovány a analyzovány na přítomnost fluorouracilu (UV-fluoroscence), cisplatiny (atomová absorpční spektometrie), doxorubicinu a paklitaxelu (vysokoúčinná kapalinová chromatografie, high performance liquid chromatography – HPLC) na spoluřešitelském pracovišti projektu CYTO (společnost Pliva-Lachema a.s., Brno).
Obr. 1. Aplikace metody pasivního vzorkování vzduchu při sledování přítomnosti cytotoxických léčiv v prostorách Masarykova onkologického ústavu, Brno. A – Umístění pasivních vzorkovačů v přípravně cytostatik, B – Umístění vzorkovačů v denním staci onáři, C – Detailní pohled na pasivní vzorkovač. 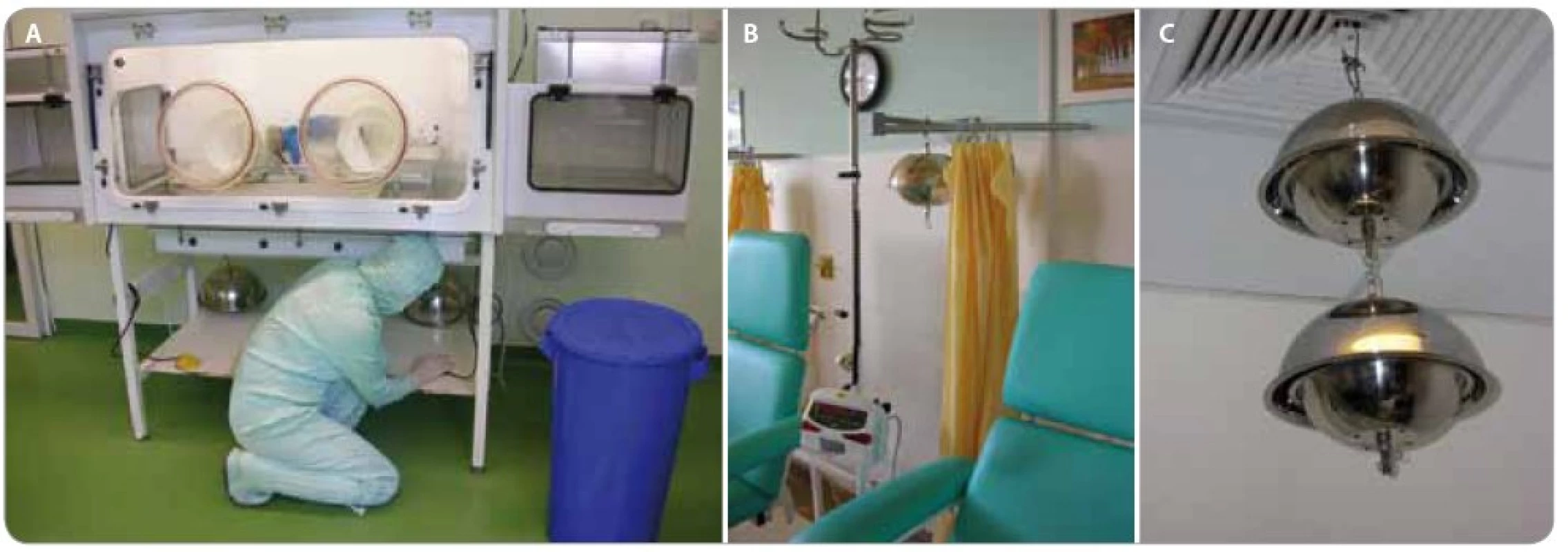
Hodnocení propustnosti rukavic pro CL
Použitá testovací metoda byla založena na měření přestupu studovaných CL z roztoků (připraveny z odpovídajících léčivých přípravků) přes vzorek zkoušených rukavic (vinyl, latex o různé síle, nitril) do receptorového media (pufrovací roztok). Kinetické experimenty byly prováděny po dobu celkem šesti hodin při 30 °C (simulace teploty na povrchu kůže). Detekce a kvantifikace CL v receptorovém mediu byla uskutečněna pomocí vysokoúčinné kapalinové chromatografie na pracovišti MOÚ (Acquity UPLC, Waters). Separace byla provedena na reverzní stacionární fázi (BEH C18 2,1 × 50cm, průměr částic 1,7 µm) metodou využívající gradientu obsahu acetonitrilu v 7mM fosfátovém pufru (pH = 3) jdoucím od 22 do 47%. K detekci a kvantifikaci analytů byly použity chromatografické záznamy pořízené při λ = 195 (cyklofosfamid), 230 (doxorubicin, paklitaxel) a 265 nm (fluorouracil).
Ke stanovení cisplatiny bylo využito atomové absorpční spektrometrie s elektrotermickou atomizací (Perkin Elmer 3030/HGA 500) a bylo realizováno na spoluřešitelském pracovišti (Pliva-Lachema, a.s., Brno).
Výsledky a diskuze
V první fázi projektu byla řešena problematika fyzikálních vlastností vybraných cytostatik, konkrétně evaporace, tedy schopnosti pevných látek se odpařovat [21–22]. Naše studie stanovení tlaku nasycených par (TP) se zaměřila na vybraná strukturně odlišná cytostatika a získané hodnoty TP (tab. 1) se řádově pohybovaly od 10–3 do 10–2 Pa. Předchozí, omezené literární údaje, které popisovaly studie s fluorouracilem, cisplatinou nebo karmustinem [17,22], ukázaly, že TP těchto sloučenin nejsou zcela zanedbatelné, a pokud dojde k jejich vstupu do pracovního prostředí, lze je v určitých koncentracích očekávat také v ovzduší. Získané hodnoty TP cytostatik se v porovnání s vodou a etanolem jeví jako nízké (tab. 1), nicméně i tyto nízké hodnoty indikují potenciál přechodu CL z pevné či kapalné fáze do ovzduší, a tedy možnou kontaminaci vzduchu v pracovním prostředí. Tab. 1 ukazuje také převod hodnot TP na koncentrace, které mohou dosahovat až 7,9mg/m3.
S ohledem na získané výsledky jsme dále realizovali ověřovací pilotní studii sledování CL ve volném pracovním prostředí. Byly využity pasivní vzorkovače na bázi polyuretanových filtrů [20] vyvinuté ve Výzkumném centru RECETOX na Přírodovědecké fakultě Masarykovy univerzity. Princip pasivního vzorkování je založen na utváření a udržování rovnovah mezi plynnou fází a fází sorbovanou na pevnou matrici a je uplatňován např. při dlouhodobém monitoringu prostředí, kdy poskytuje integrující informaci o zátěži a svou podstatou eliminuje jednorázové krátkodobé výkyvy v hladinách sledovaných sloučenin [23]. Analýzy všech sledovaných CL (fluorouracilu, cisplatiny, doxorubicinu a paklitaxelu) byly v této pilotní studii negativní (koncentrace pod limitem detekce použitých metodik). Předchozí literární studie však ukázaly, že s využitím velmi citlivých metod (např. voltametrie nebo hmotnostní spektrometrie [9,22,24–27], které nebyly pro naši práci k dispozici, lze v ovzduší v některých případech prokázat detekovatelná množství například cyklofosfamidu (0,02–13 µg/m3 [22,26–27]) nebo fluorouracilu (0,04–6,3 µg/m3 [9,25]). Problematika vzdušné kontaminace pracovního prostředí z hlediska profesní expozice CL tedy zůstává otevřena a další výzkum v této oblasti by měl směřovat jak k vývoji nových a citlivějších detekčních metod, tak k optimalizaci vzorkovacích a analytických postupů [7].
Vedle potenciálního vstupu CL do organizmu respirací kontaminovaného vzduchu je při profesní expozici další významnou cestou vstupu dermální kontakt a přestup CL přes kůži. Lidské ruce jsou nejvíce exponovanou částí těla nejen při přípravě CL, ale již při příjmu a skladování těchto léčiv, jakož i při aplikaci chemoterapie pacientům, při likvidaci havárií nebo sanitaci či manipulaci s lůžkovinami a exkrety onkologických pacientů [27–29]. Na kvalitu ochranných rukavic by tedy měl být kladen značný důraz a zdravotničtí pracovníci by měli znát vlastnosti a kvalitu jednotlivých typů rukavic.
V rámci námi řešeného projektu bylo provedeno hodnocení propustnosti několika typů ochranných rukavic pro cytostatika. Výsledky prostupnosti pěti nejčastěji používaných CL přes tři typy rukavic, shrnuté v tab. 2, potvrzují, že prostupnost rukavic pro vybraná léčiva závisí jak na konkrétním léčivu, tak na výrobním materiálu a také tloušťce vrstvy tohoto materiálu. Ze zkoušených rukavic byly jako nejúčinnější bariéra pro přestup cytostatik identifikovány rukavice nitrilové, u kterých nebyl pozorován průnik ani jednou z vybraných látek. U vinylových a latexových rukavic byl zjištěn průnik cyklofosfamidu a paklitaxelu. Cisplatina, doxorubicin a fluorouracil nepronikaly ani jedním ze zkoušených materiálů. Pozorované hodnoty prostupnosti (např. první prostupnost cyklofosfamidu přes vinyl po 60 min, celkové množství až 19 µg/cm2) ukazují, že pro zajištění ochrany zdravotnických pracovníků před expozicí CL je nutné využívat jen některé z materiálů (tj. nitrilové rukavice [30]) a také zajistit pravidelnou a častou výměnu ochranných rukavic. Naopak nejméně vhodné pro manipulaci s CL jsou velmi rozšířené a často používané rukavice vinylové. Při edukaci, zaškolování a také kontrole pracovníků různých profesí v lékařských zařízeních je tedy třeba zdůrazňovat používání a časté výměny rukavic nejen při přímé manipulaci s CL, ale i při úklidových a sanitačních činnostech vykonávaných v prostorách s potenciální kontaminací CL (přípravna, aplikační místnost, lůžková oddělení, hygienická zařízení pro onkologické pacienty atd. [7]).
Tab. 2. Čas průniku a permeované (prostoupené) množství vybraných cytostatik přes vinylové, latexové a nitrilové rukavice. Pro každou látku je prezentována dávka, která odpovídá koncentracím po užívaným v aplikačních dávkách sledovaných léčiv. 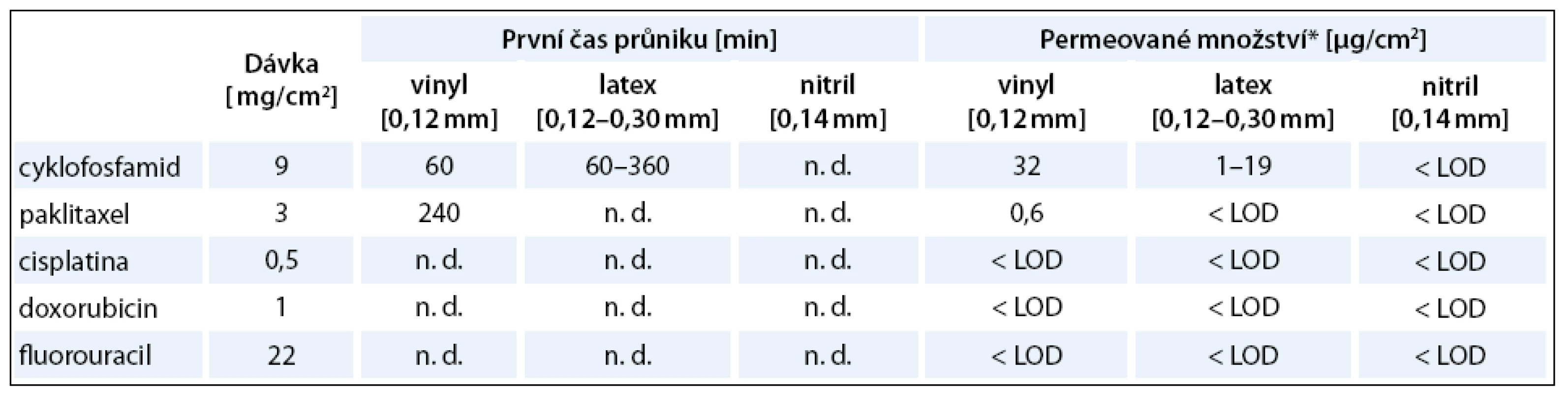
*Celkové množství CL prošlé materi álem za 6 hod, LOD – limit detekce pro jednotlivá léčiva (560 ng/ cm2 cyklofosfamid, 90 ng/cm2 paklitaxel, 90 ng/cm2 cisplatina, 130 ng/cm2 doxorubicin, 80 ng/cm2 fluorouracil), n. d. – nelze definovat (během šestihodinové studi e nebyl pozorován průnik studované látky) Závěr
Projekt CYTO je v ČR první výzkumnou aktivitou, jejímž cílem je prakticky orientovaný výzkum cytotoxických látek s hlavním akcentem na poznání jejich vlastností, hladin a možných zdravotních rizik u profesně exponovaných osob. Naše experimenty přinesly nové informace o hodnotách nasycených tlaků par cytostatik, které indikují malý, ale nezanedbatelný evaporační potenciál cytostatik. Získané hodnoty mohou být dále využity pro odhady hladin CL v pracovním ovzduší konkrétních pracovišť s využitím matematických modelů. Navazující pilotní studie s využitím pasivních vzorkovačů neprokázala významné koncentrace cytostatik v pracovním ovzduší, avšak literární údaje založené na velmi citlivých metodikách stanovení prokazují výskyt CL v ovzduší (např. ve formě aerosolu nebo vázaných na prachové částice [9,24–27]. Experimenty prostupnosti CL přes rukavice ukázaly, že dobrou ochranu zaručují především rukavice nitrilové, jejichž používání a časté výměny je třeba vyžadovat nejen u pracovníků přípravy CL, ale také např. u zdravotních sester, pracovníků sanitace atd. Získané informace budou v dalších fázích projektu kombinovány s výsledky analýz CL na konkrétních zdravotnických pracovištích (stěry z povrchů [31–33]) a dále využity pro výpočty a rovněž management zdravotních rizik profesně exponovaných pracovníků.
Práce byla podpořena grantovým projektem Ministerstva školství, mládeže a tělovýchovy v rámci národního programu výzkumu II (CYTO 2B06171).
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, pruducts, or services used in the study.Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.PharmDr. Lenka Doležalová
Ústavní lékárna
Masarykův onkologický ústav
Žlutý kopec 7
656 53 Brno
e-mail: dolezalova@mou.cz
Zdroje
1. IARC. Some antineoplastic and immunosuppresive agents. Vol. 26. IARC. Lyon, Francie, 1981.
2. IARC. Evaluation of carcinogenic risk to humans: Pharmaceutical drugs. Vol. 50. IARC. Lyon, Francie, 1990.
3. IARC. Some antiviral and antineoplastic drugs, and other pharmaceutical agents. Vol. 76. Lyon, Francie, 1999.
4. §18 nařízení vlády č. 361/2007 Sb., kterým se stanoví podmínky ochrany zdraví při práci.
5. Sessink PJM, Bos RP. Drugs hazardous to healthcare workers. Evaluation of methods for monitoring occupational exposure to cytostatic drugs. Drug Safety 1999; 20(4): 347–359.
6. §7 zákona č. 309/2006 Sb., kterým se upravují další požadavky bezpečnosti a ochrany zdraví při práci v pracovněprávních vztazích a o zajištění bezpečnosti a ochrany zdraví při činnosti nebo poskytování služeb mimo pracovněprávní vztahy (zákon o zajištění dalších podmínek bezpečnosti a ochrany zdraví při práci).
7. Turci R, Sottani C, Ronchi A et al. Biological monitoring of hospital personnel occupationally exposed to antineoplastic agents. Toxicol Lett 2002; 134(1–3): 57–64.
8. Nygren O, Gustavsson B, Ström L et al. Exposure to anti cancer drugs during preparation and administration. Investigations of an open and a closed system. J Environ Monit 2002; 4(5): 739–742.
9. Micoli G, Turci R, Arpellini M et al. Determination of 5-fluorouracil in environmental samples by solid-phase extraction and high performance liquid chromatography with ultraviolet detection. J Chromatogr B Biomed Sci Appl 2001; 750(1): 25–32.
10. Hedmer M, Georgiadi A, Bremberg ER et al. Surface contamination of cyclophosphamide packaging and surface contamination with antineoplastic drugs in a hospital pharmacy in Sweden. Ann Occup Hyg 2005; 49(7): 629–637.
11. Nygren O, Gustavsson B, Ström L et al. Cisplatin contamination observed on the outside of drug vials. Ann Occup Hyg 2002; 46(6): 555–557.
12. Fransman W, Huizer D, Tuerk J et al. Inhalation and dermal exposure to eight antineoplastic drugs in an industrial laundry facility. Int Arch Occup Environ Health 2007; 80(5): 396–403.
13. Blaha L, Dolezalova L, Odraska P. Safe handling of cytotoxic drugs: the need for monitoring and critical risk assessment. Hospital Pharmacy Europe 2008; 40 : 73–75.
14. Opiolka S, Mölter W, Goldschmidt E et al. Verdampfung von Zytostatika aus Sicherheitswerkbänken, Gefahrstoffe-Reinhal. Luft 1998; 58 : 291–295.
15. Poet TS, McDougal JN. Skin absorption and human risk assessment. Chem Biol Interact 2002; 140(1): 19–34.
16. Hirst M, Mills DG, Tse S et al. Occupational exposure to cyclophosphamide. The Lancet 1984; 323(8370): 186–188.
17. Connor T, Shults M, Fraser M. Determination of the vaporization of solutions mutagenic antineoplastic agents at 23 and 37oC using a desiccator technique. Mutation Research 2000; 470 : 85–92.
18. Nygren O, Gustavsson B, Eriksson R. A test method for assessment of spill and leakage from drug preparation systems. Annals of Occupational Hygiene 2005; 49(8): 711–718.
19. Organizace pro ekonomický spolupráci a rozvoj. Guidelines for the testing of chemicals. 104: Vapour pressure curve – vapour presure balance. Paris: OECD 1995.
20. Klánová J, Kohoutek J, Hamplová L et al. Passive air sampler as a tool for long term air pollution monitoring: Part 1. Performance assessment for seasonal and spatial variations. Environ Pollut 2006; 144 (2): 393–405.
21. Opiolka S, Mölter W, Kiffmeyer TK et al. Dampfdürcke von Zytostatika. Gefahrstoffe-Reinhal. Luft 1999; 59 : 443–444.
22. Kiffmeyer T, Kube Ch, Opiolka S et al. Vapour pressures, evaporation behaviour and airborne concentrations of hazardous drugs: Implications for occupational safety. The Pharmaceutical Journal 2002; 268 : 331–337.
23. Klánová J, Čupr P, Kohoutek J et al. Assessing the influence of meteorological parameters on the performance of polyurethane foam based passive air samplers. Environ Sci Technol 2008; 42(2): 550–555.
24. Nygren O, Lundgren C. Determination of platinum in workroom air and in blood and urine from nursing staff attending patients receiving cisplatin chemotherapy. Int A Occup Environ Health 1997; 70(3): 209–214.
25. Bos RP, Weissenberger BFJ, Anzion RBM. Alpha-fluoro beta alanine in urine of workers occupationally exposed to 5-fluorouracil in a 5-fluorouracil-producing factory. Biomarkers 1998; 3(1): 81–87.
26. Minoia C, Turci R, Sottani C et al. Application of high performance liquid chromatography tandem mass spectrometry in the environmental and biological monitoring of health care personnel occupationally exposed to cyclophosphamide and ifosfamide. Rapid Commun Mass Spect 1998; 12(20): 1485–1493.
27. Sessink PJM, Vandekerkhof MCA, Anzion RBM et al. Environmental contamination and assessment of exposure to antineoplastic agents by determination of cyclophosphamide in urine of exposed pharmacy technicians – Is skin absorption an important exposure route? Arch Environ Health 1994; 49(3): 165–169.
28. Fransman W, Vermeulen R, Kromhout H. Dermal exposure to cyclophosphamide in hospitals during preparation, nursing and cleaning activities. Int Arch Occup Environ Health 2005; 78(5): 403–412.
29. Fransman W, Huizer D, Tuerk J et al. Inhalation and dermal exposure to eight antineoplastic drugs in an industrial laundry facility. Int Arch Occup Environ Health 2007; 80(5): 396–403.
30. Gross ER, Groce DF. An evaluation of nitrile gloves as an alternative to natural rubber latex for handling chemotherapeutic agents. J Oncol Pharm Pract 1998; 4(3): 165.
31. Bussieres JF, Theoret Y, Prot-Labarthe S et al. Program to monitor surface contamination by methotrexate in a hematology-oncology satellite pharmacy. Am J Health Syst Pharm 2007; 64(5): 531–535.
32. Kiffmayer T et al. Monitoring-effect study of wipe sampling in pharmacies. International Colloquium: Antineoplastic drug monitoring 30. 4. 2008, Hennef, Germany. [http://www.pharma-monitor.de/objectfiles/3080/Kiffmeyer_Germany_Int_Colloquium_Hennef_30.04.2008.pdf]
33. Odráška P, Doležalová L, Gorná L et al. Protinádorová léčiva v pracovním prostředí člověka – průběžné výsledky projektu CYTO. 12. kongres nemocničních lékárníků 14.–16. 11. 2008, Hradec Králové.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článek Neuroendokrinní nádory rekta
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2009 Číslo 5- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejasný stín na plicích – kazuistika
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Fixní kombinace paracetamol/kodein nabízí synergické analgetické účinky
-
Všetky články tohto čísla
- Neuroendokrinní nádory rekta
- DNA a mikroRNA čipové technologie v diagnostice a predikci u pacientů s renálním karcinomem
- Proteomická analýza nádorových buněk
- Studie evaporace vybraných cytostatik a propustnosti ochranných rukavic v rámci výzkumu profesní zátěže zdravotnických pracovníků exponovaných cytotoxickým protinádorovým léčivům (projekt CYTO)
- Polymorfizmus –2548 G/A v genu pro leptin u pacientek s endometriálním karcinomem
- Profily nízkomolekulárního proteomového spektra získané pomocí hmotnostní spektrometrie SELDI-TOF v sérech pacientů s diseminovaným maligním melanomem: pilotní studie
- Chronická gastrointestinální toxicita po zevní radioterapii karcinomu prostaty
- Úvaha nad vývojem screeningu kolorektálního karcinomu
- Pohled na vývoj onkologie ve 3. tisíciletí
- Zápis ze schůze výboru České onkologické společnosti dne 8. 9. 2009 v Liberci
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Neuroendokrinní nádory rekta
- Chronická gastrointestinální toxicita po zevní radioterapii karcinomu prostaty
- Studie evaporace vybraných cytostatik a propustnosti ochranných rukavic v rámci výzkumu profesní zátěže zdravotnických pracovníků exponovaných cytotoxickým protinádorovým léčivům (projekt CYTO)
- Proteomická analýza nádorových buněk
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



