-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Porovnanie celotelovej scintigrafie skeletu so sérovou koncentráciou ľudského epididymálneho proteínu 4 u pacientov s malígnym melanómom
Comparison of whole body bone scintigraphy with levels of the serum concentration of human epididymal protein 4 in patients with malignant melanoma
Introduction:
Melanoma is the most dangerous type of skin cancer and it is the leading cause of death from skin disease. The annual incidence has increased dramatically over the past few decades. The aim of this study was to correlate serum levels of the tumour marker human epididymal protein 4 (HE4) with the presence of bone metastases detected by whole-body bone scintigraphy in patients with malignant melanoma and to evaluate the importance of HE4 in the malignant melanoma diagnostics.Material and methods:
We determined HE4 in serum from blood sample in 14 patients (4 men, 10 women) with malignant melanoma. The blood sample was took before radioactive tracer application in whole-body bone scintigraphy examination by using hybrid gamma camera SPECT/CT (single photon emission computed tomography/computed tomography). We compared the results with 10 individuals without malignant disease – control group.Results:
Bone metastases using whole-body bone scintigraphy were detected in 5 cases (35.71 %), probably in 3 cases (21.43 %) and 6 patients (42.86 %) were without bone metastases. The concentration of HE4 was significantly higher in patients than in individuals of control group. Serum concentration of HE4 was higher above reference range only in one patient with melanoma. The concentrations of HE4 in patients were not different and dependent on grade of bone metastases.Conclusion:
We observed that serum concentration of HE4 in patients with malignant melanoma was higher comparing to individuals of control group. The serum concentrations of HE4 were not correlated with finding on whole-body bone scintigraphy.Key words:
melanoma, human epididymal protein 4, bone scintigraphy
Autoři: Jaroslav Weissensteiner 1; Eva Babušíková 2
Působiště autorů: Oddelenie nukleárnej medicíny, Nemocnica Poprad, a. s., SR 1; Ústav lekárskej biochémie, Jesseniova lekárska fakulta v Martine, Univerzita Komenského v Bratislave, SR 2
Vyšlo v časopise: NuklMed 2015;4:8-12
Kategorie: Původní práce
Souhrn
Úvod:
Melanóm je jedným z najmalígnejších nádorov kože a je najčastejšou príčinou úmrtia u kožných ochorení. V ostatných desaťročiach sa jeho výskyt výrazne zvýšil. Cieľom našej práce bolo porovnať hladinu onkomarkera ľudský epididymálny proteín 4 (HE4) v korelácii s nálezom kostných metastáz zistených pri celotelovej scintigrafii skeletu u pacientov s malígnym melanómom a posúdiť jeho význam v diagnostike malígneho melanómu.Materiál a metódy:
U 14 pacientov (4 muži, 10 žien) s malígnym melanómom sme stanovili hladinu HE4 v sére z krvnej vzorky odobratej pred aplikáciou rádiofarmaka v rámci vyšetrenia celotelovej scintigrafie skeletu za použitia hybridnej gamakamery SPECT/CT (single photon emission computed tomography/computed tomography, jednofotónová emisná počítačová tomografia/počítačová tomografia). Výsledky sme porovnali s hodnotami 10 ľudí bez prítomného nádorového ochorenia, ktorí tvorili kontrolnú skupinu.Výsledky:
Kostné metastázy zistené pri celotelovej scintigrafii skeletu boli prítomné v 5 prípadoch (35,71 %), pravdepodobné v 3 prípadoch (21,43 %) a 6 pacienti (42,86 %) boli bez nálezu kostných metastáz. Koncentrácia HE4 bola u pacientov signifikantne vyššia ako u kontrolnej skupiny. Nad rozsah referenčných hodnôt bola koncentrácia HE4 zvýšená len u jedného pacienta s melanómom. Koncentrácie HE4 sa u pacientov nelíšili v závislosti od kostných metastáz.Záver:
V našej pilotnej štúdii sme u pacientov s malígnym melanómom pozorovali vyššie koncentrácie HE4 v porovnaní s kontrolnou skupinou. Sérové hladiny HE4 nekorelovali s nálezom pri celotelovej scintigrafii skeletu.Kľúčové slová:
melanóm, ľudský epididymálny proteín 4, scintigrafia skeletuÚvod
Malígny melanóm (MM, melanoma malignum) je najzhubnejší nádor kože a vo všeobecnosti patrí k najmalígnejším nádorom vôbec. Podkladom vzniku malígneho melanómu je malígna transformácia melanocytov, neuroektodermálnych buniek produkujúcich melanín. 1, 2 Najčastejšie sa vyskytuje v koži, oku, zriedkavejšie na slizniciach ústnej a nosovej dutiny, pažeráka, konečníka, penisu, vulvy, vagíny a očných spojoviek. 3 Toto nádorové ochorenie postihuje obe pohlavia (u žienje častejší v pomere 3 : 2) a prevažujúce lokalizácie sú u mužov trup (61 %) a u žien dolné končatiny (37,7 %). Incidencia v Slovenskej republike je 12,7 prípadov u mužov a 11,7 prípadov ochorenia u žien na 100 000 obyvateľov. 4
Melanóm sa môže šíriť krvnou alebo lymfatickou cestou, pozdĺž lymfatických a krvných ciev, nervových štruktúr alebo priamo lokálnou inváziou. 5 Najčastejšie metastázuje do oblasti kože, podkožných tkanív, spádových lymfatických uzlín, do pľúc, pečene, mozgu, menej do kostí a tenkého čreva. 6,7
Kostné metastázy vznikajú pri malígnom melanóme v kostnej dreni. 8 Metastázy v kostnej dreni sú pri malígnom melanóme zriedkavé a vyskytujú sa u 5–7 % pacientov s diseminovaným ochorením, ale pri zameraní sa na vyšetrenie kostnej drene sa ich výskyt zistil až v 45 % prípadov. 9 Kostné metastázy sa vo všeobecnosti vyskytujú u pacientov s pokročilým metastatickým ochorením. Častejšie sa vyskytujú v axiálnom skelete ako v apendikulárnom a hlavne v stavcoch chrbtice. Typické kostné metastázy pri MM sú osteolytické s pôvodom v kostnej dreni. Lézie svojím rastom zapríčiňujú eróziu a deštrukciu kostného tkaniva so vznikom patologických fraktúr. Atypické kostné metastázy sa prejavujú ako osteolyticko-osteoblastické alebo zriedkavo ako kompletne osteoblastické. 10 Na vylúčenie mikrometastáz v regionálnych lymfatických uzlinách sa využíva detekcia a extirpácia sentinelovej, tzv. strážnej lymfatickej uzliny (SLU). Primárne ložisko malígneho melanómu a jeho metastázy sa vyznačujú vysokým metabolizmom glukózy, čo má za následok vysokú akumuláciu 2-[18F]-fluoro-2-deoxy-D-glukózy (18F-FDG) a možnosť celotelového vyšetrenia pozitrónovou emisnou tomografiou/počítačovou tomografiou (positron emission tomography/computed tomography, PET/CT). 11,12,13 Celotelová pozitrónová emisná tomografia/magnetická rezonancia (positron emission tomography/magnetic resonance, PET/MR) je metabolicko-anatomická zobrazovacia metóda, ktorá umožňuje detekciu podkožných metastáz, metastáz v kostnej dreni, v pečeni a v mozgu u pacientov s malígnym melanómom v rámci jedného vyšetrenia. 14 Pri podozrení na kostné metastázy u pacientov s malígnym melanómom sa môže využiť celotelová scintigrafia skeletu a pre upresnenie nálezu aj hybridné SPECT/CT vyšetrenie.
Ľudský epididymálny proteín 4 (HE4, human epididymal protein 4) je kódovaný génom srvátková kyslá 4-disulfidová jadrová doména 2 (WFDC2, whey acidic 4-disulfide core domain 2), ktorý sa nachádza na chromozóme 20q12-13.1. Tento gén je členom rodiny bielkovín, ktoré obsahujú srvátkovú kyslú bielkovinovú doménu (WAP, whey acidic protein). Srvátkové kyslé bielkoviny boli identifikované ako hlavné zložky mlieka hlodavcov i cicavcov, dôležité regulátory v proliferácii cicavčích epiteliálnych buniek a proteázové inhibítory. Ľudský epididymálny proteín 4 je glykozylovaná bielkovina (veľkosť 20–25 kDa) s podobnou štruktúrou, ako majú proteinázové inhibítory, pričom jej funkcia nie je presne známa. Predpokladá sa, že inhibuje trypsín a mohla by participovať na dozrievaní spermií. Táto bielkovina je produkovaná tkanivom nadsemenníkov. Prvýkrát HE4 identifikoval a popísal Kirchhoff a kol. 15,16,17 Zvýšená hladina HE4 bola pozorovaná v sére u karcinómov vaječníkov a má u tohto ochorenia senzitivitu 67–76 % a špecificitu 95–96 %, preto sa predpokladá, že HE4 by mohol hrať úlohu v karcinogenéze a progresii nádoru. 18,19,20,21
Stanovenie hodnôt onkomarkera HE4 možno využiť na sledovanie priebehu ochorenia, hodnotenie progresie a sledovanie účinnosti liečby u pacientok s epiteliálnym karcinómom ovária a na diferenciálnu diagnostiku tumoru ovária (suspektná malignita). Navyše jeho stanovenie je vhodné aj pri sledovaní pacientok s karcinómom endometria. V poslednom období sa ukazuje, že stanovenie koncentrácie HE4 by mohlo mať význam aj u pacientov s inými malígnymi nádorovými ochoreniami.
Naším cieľom bolo porovnať sérovú koncentráciu ľudského epididymálneho proteínu 4 v korelácii s nálezom zisteným pri celotelovej scintigrafii skeletu u pacientov s malígnym melanómom a posúdiť jeho význam v diagnostike malígneho melanómu.
Materiál a metódy
U 14 pacientov (4 muži, 10 žien, vekový priemer 60, rozsah 41–79 rokov) s malígnym melanómom sme stanovili koncentráciu HE4 v sére z krvnej vzorky odobratej pred aplikáciou rádiofarmaka 99mTc-metyléndifosfonát (99mTc-MDP) o aktivite 500–700 MBq v rámci vyšetrenia celotelovej scintigrafie skeletu ako celotelový záznam v prednej a zadnej projekcii za použitia hybridnej gamakamery SPECT/CT typu BrightView XCT, Philips. Vyšetrenie celotelovej scintigrafie skeletu sa realizovalo v rozmedzí 2–4 hodín od aplikácie rádiofarmaka posunom vyšetrovacieho lôžka s pacientom medzi dvoma stacionárnymi detektormi uloženými nad a pod pacientom s rýchlosťou posunu lôžka 10–12 cm za minútu s použitím nízkoenergetických kolimátorov s paralelnými otvormi typu LEGP (low energy general purpose). Pri presnejšej lokalizácii ložiska alebo jeho odlíšení od iného ochorenia podobajúceho sa nálezom na kostnú metastázu sme realizovali hybridné SPECT/CT vyšetrenie. Výsledky sme porovnali s hodnotami 10 ľudí bez prítomného nádorového ochorenia – kontrolná skupina (2 muži, 8 žien, vekový priemer 52,3, rozsah 34–67 rokov), u ktorých sa realizovalo vyšetrenie celotelovej scintigrafie skeletu z iných dôvodov (nejasné bolesti chrbtice, nejasné bolesti kĺbov). Odobratú krv v sterilnej skúmavke o objeme 5–6 ml sme centrifugovali v odstredivke pri otáčkach 4000 za minútu v trvaní 5 minút. Po centrifugácii sme získané sérum uskladnili pri teplote – 20 °C, neskôr pri teplote – 50 a – 70 °C. Po skompletizovaní sme vzorky séra vyšetrili na oddelení klinickej biochémie elektrochemiluminiscenčnou imunoanalýzou (ECLIA) na imunoanalyzátore typu Cobas e 411 (ROCHE Diagnostics).
Výsledky
Kostné metastázy (mts) zistené pri celotelovej scintigrafii skeletu boli prítomné v 5 prípadoch (35,71 %), pravdepodobné v 3 prípadoch (21,43 %) a 6 pacienti (42,86 %) boli bez nálezu kostných metastáz. (Tab. 1) Pravdepodobné mts sú charakterizované ako lézie, ktoré sú podozrivé z kostných metastáz a nepravdepodobné pre iné lézie. Pacientov sme rozdelili aj podľa veku v závislosti od nálezu pri celotelovej scintigrafii skeletu. (Tab. 2) V čase vyšetrenia celotelovou scintigrafiou skeletu boli 4 pacienti po liečbe a u jedného pacienta nebola ešte v čase vyšetrenia liečba chemoterapiou ukončená. Zo 4 pacientov po liečbe dostávali 2 pacienti interferón, jeden pacient bol po rádioterapii a jeden po rádioterapii aj chemoterapii. U 8 pacientov bolo v minulosti realizované aj scintigrafické vyšetrenie a peroperačná detekcia SLU. (Tab. 3) Pozitívna SLU bola u 4 pacientov, pričom u 3 týchto pacientov sa rozvinuli aj mts. V jednom prípade sa u pacienta s negatívnou SLU (Clark II-III, Breslow 6 mm) objavili mts v skelete do 3,5 roka.
Tab. 1. Nález celotelovej scintigrafie skeletu u pacientov s malígnym melanómom (mts – kostné metastázy, n – počet pacientov). 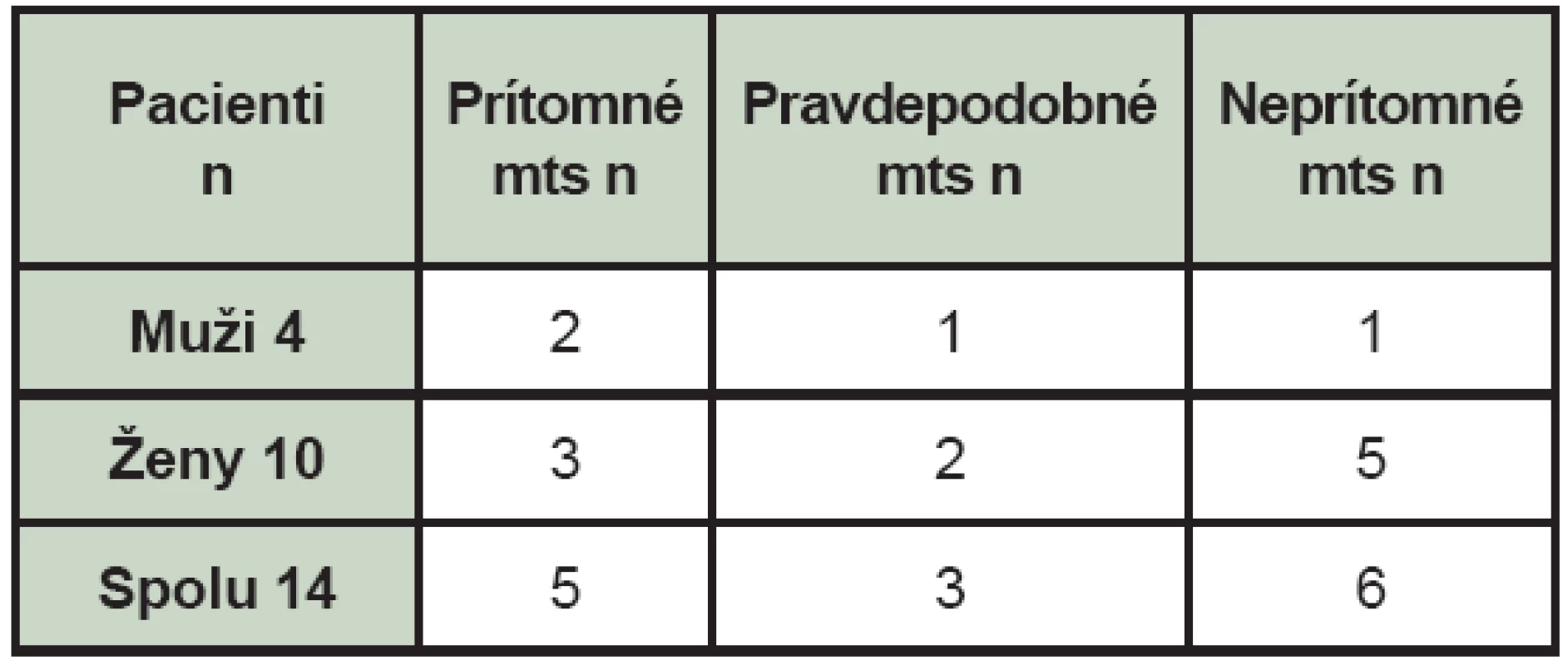
Tab. 2. Nález celotelovej scintigrafie skeletu u pacientov s malígnym melanómom – rozdelenie podľa veku (mts – kostné metastázy, n – počet pacientov). 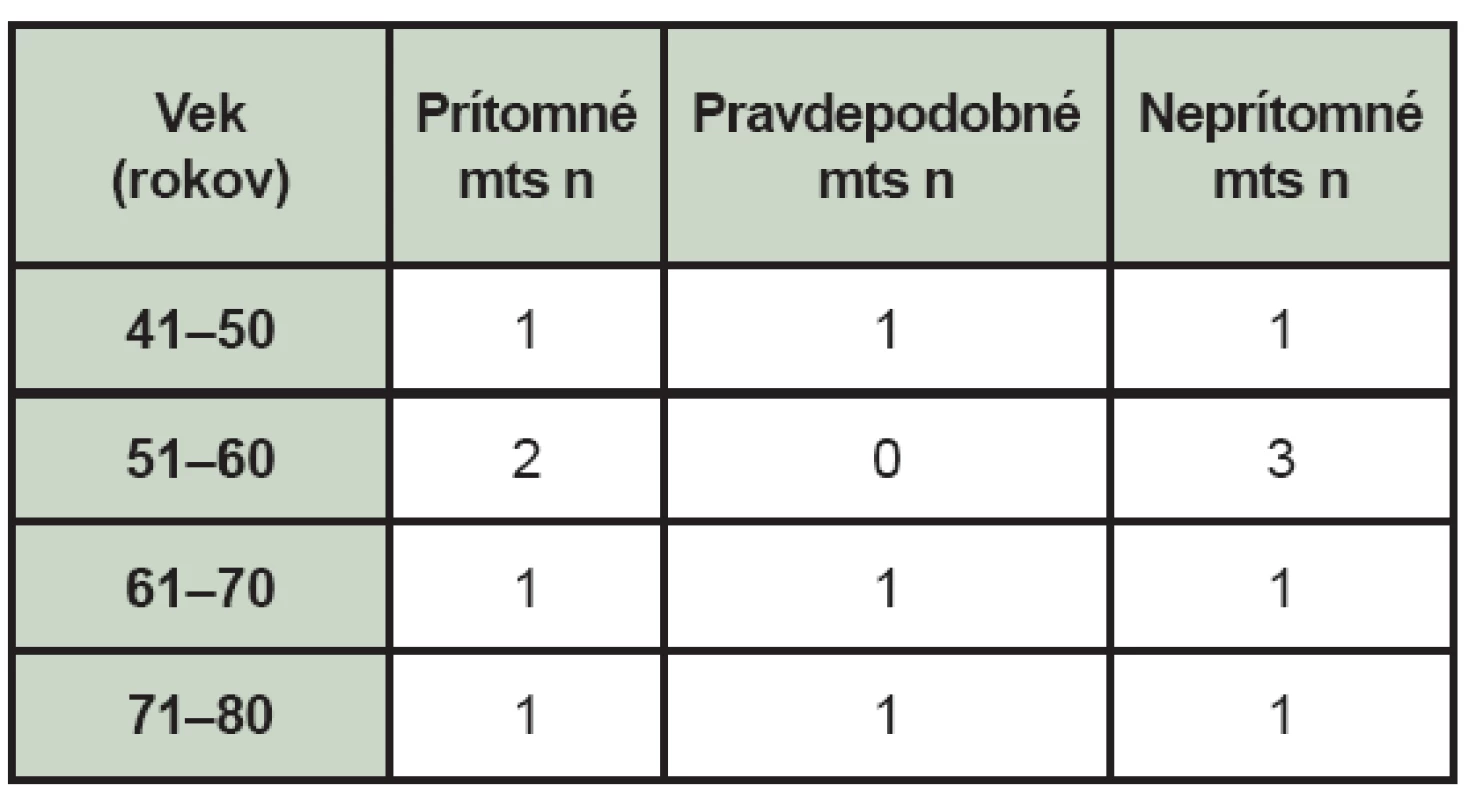
Tab. 3. Nález celotelovej scintigrafie skeletu, SLU, využitie hybridného vyšetrenia SPECT/CT v rámci celotelotelovej scintigrafie skeletu (mts – kostné metastázy, n – počet pacientov, SLU – sentinelová lymfatická uzlina, SPECT/CT – jednofotónová emisná počítačová tomografia/počítačová tomografia). 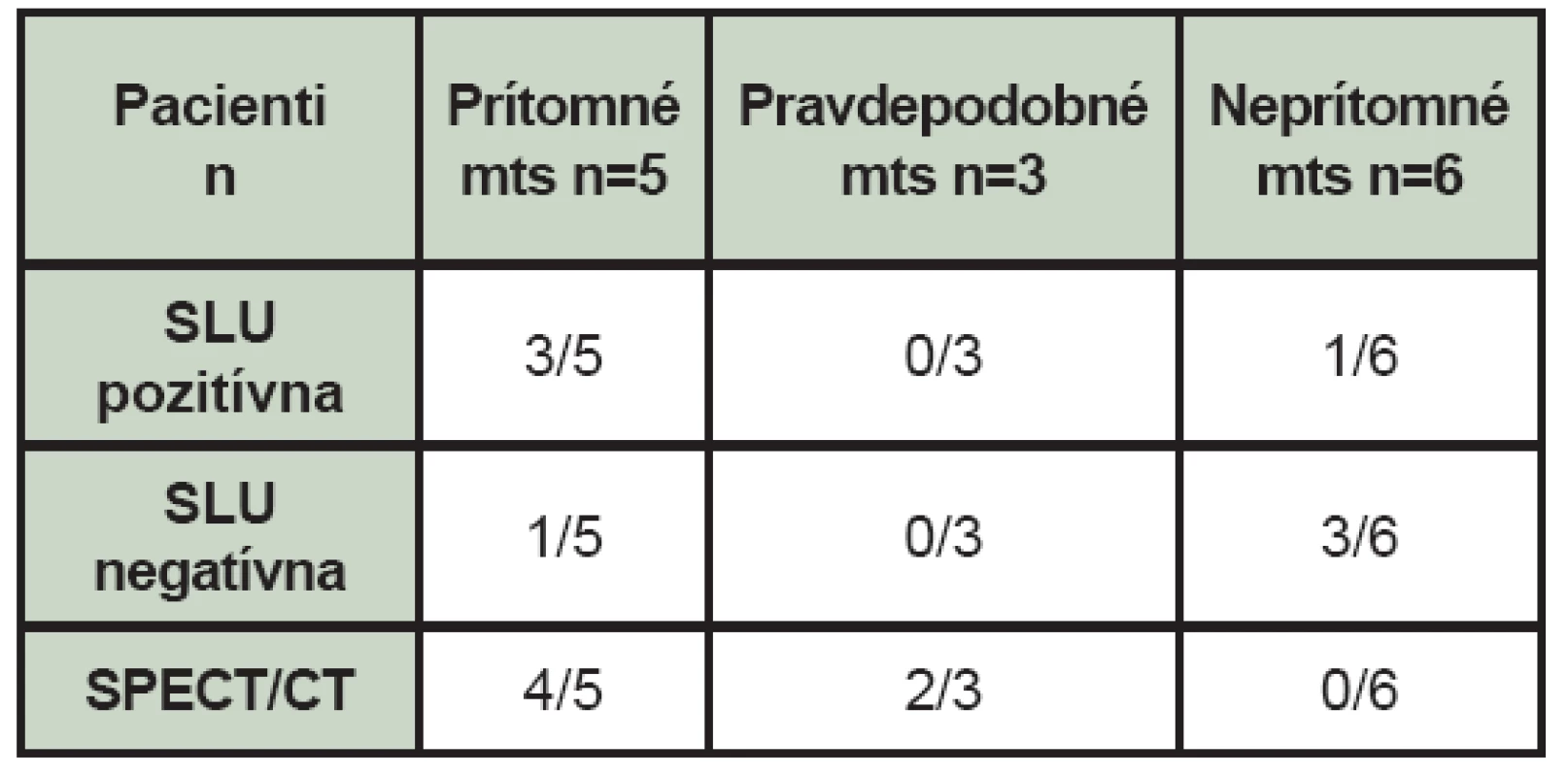
Hybridné SPECT/CT vyšetrenie v rámci celotelovej scintigrafie skeletu sme zo 14 pacientov s melanómom použili v 6 prípadoch a to v 4 prípadoch u pacientov s nálezom kostných metastáz, (Tab. 3) čím sa upresnila diagnostika kostných metastáz. V 2 prípadoch pravdepodobných kostných metastáz však použitie SPECT/CT neprinieslo očakávané upresnenie nálezu.
Malígny melanóm bol lokalizovaný v 3 prípadoch v oblasti chrbta, v 4 prípadoch na ramene, v 3 prípadoch na hlave, v jednom na predlaktí, päte, v oku a v jednom prípade nebola lokalizácia malígneho melanómu známa. (Tab. 4) Najčastejšie boli lokalizované kostné metastázy v oblasti stavcov chrbtice, v panvových kostiach a menej často v stehenných kostiach, v rebrách a v ramenných kostiach. (Tab. 5)
Tab. 4. Nález celotelovej scintigrafie skeletu pri jednotlivých lokalizáciách melanómu (mts – kostné metastázy, n – počet pacientov). 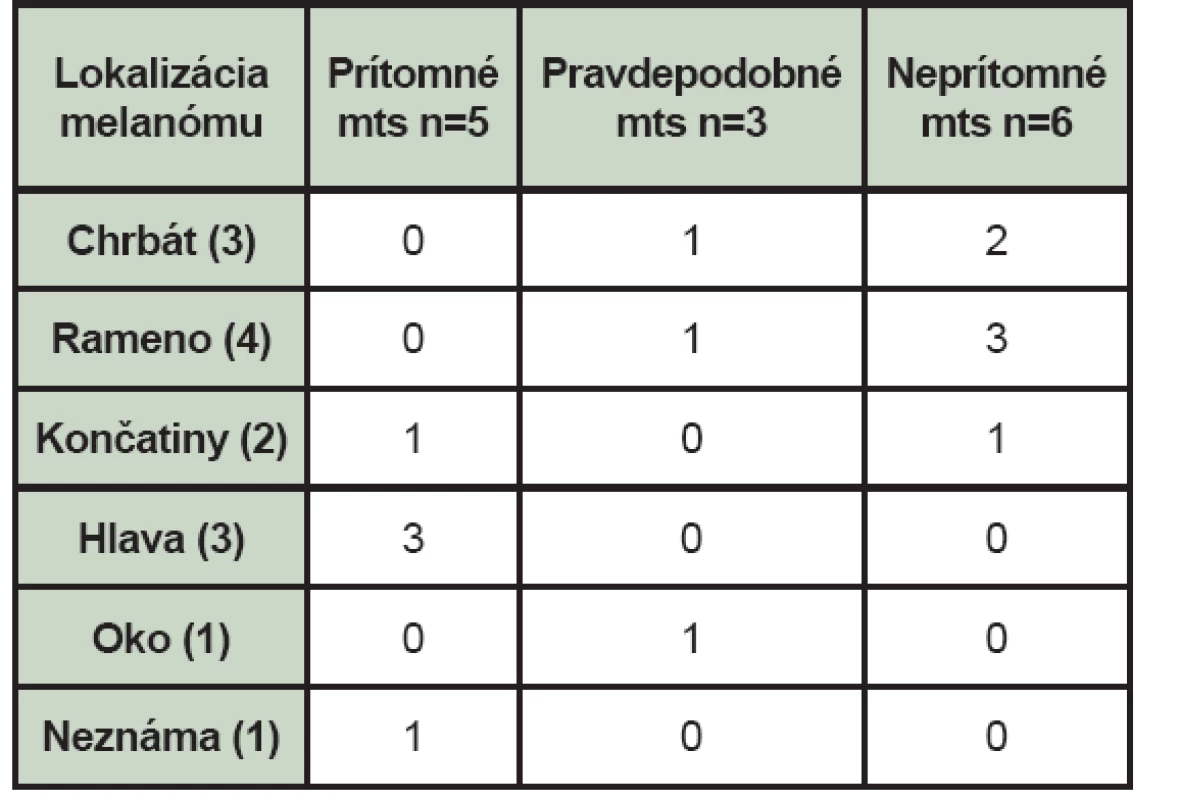
Tab. 5. Lokalizácia kostných metastáz u pacientov s malígnym melanómom na základe nálezu zistenom pri celotelovej scintigrafii skeletu (mts – kostné metastázy, n – počet pacientov s daným nálezom lokalizácie kostnej metastázy). 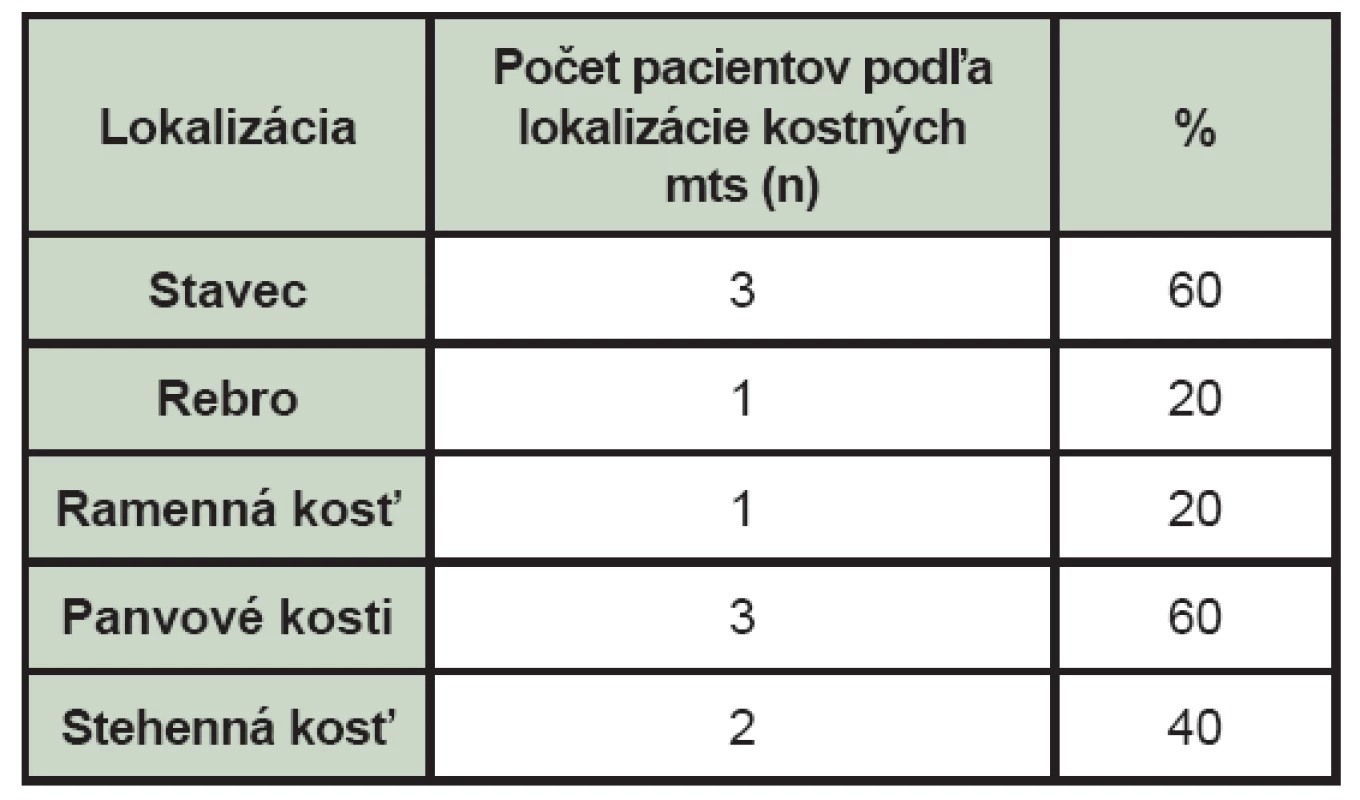
U pacientov s malígnym melanómom a u kontrolnej skupiny sme stanovili koncentrácie HE4 v sére (Graf 1) a následne sme výsledky porovnali s nálezom pri celotelovej scintigrafii skeletu. (Graf 2)
Graf 1. Porovnanie sérovej koncentrácie HE4 (priemerná hodnota) u jedincov bez prítomného malígneho ochorenia a u pacientov s malígnym melanómom (HE4 – ľudský epididymálny proteín 4, KS – kontrolná skupina, M – pacienti s malígnym melanómom); referenčné hodnoty HE4: ≤ 140 pmol/l). 
Graf 2. Priemerná hodnota HE4 v sére u jedincov bez prítomného nádorového ochorenia a u pacientov s malígnym melanómom s nálezom prítomných, pravdepodobných a neprítomných kostných metastáz na celotelovej scintigrafii skeletu (HE4 – ľudský epididymálny proteín 4, KS – kontrolná skupina, PM – prítomné kostné metastázy, PrM – pravdepodobné kostné metastázy, N – neprítomné kostné metastázy). 
Koncentrácia HE4 bola u pacientov s malígnym melanómom signifikantne vyššia (43,6 %) ako u kontrolnej skupiny. Nad rozsah referenčných hodnôt bola koncentrácia HE4 v sére zvýšená len u jedného pacienta s melanómom s nálezom pravdepodobných kostných metastáz na celotelovej scintigrafii skeletu. V kontrolnej skupine boli koncentrácie HE4 v rozsahu referenčných hodnôt. Koncentrácie HE4 sa u pacientov s mts nelíšili od koncentrácie HE4 u pacientov bez mts.
Diskusia
V našej pilotnej štúdii sme u 14 pacientov s malígnym melanómom detekovali kostné metastázy a stanovovali koncentráciu HE4. Kostné metastázy sme zistili u 5 pacientov, u ďalších troch sme pozorovali pravdepodobné metastázy. U týchto troch pacientov bude vhodné zopakovať vyšetrenie celotelovej scintigrafie o 4–5 mesiacov. Vyšetrenie sentinelovej lymfatickej uzliny sa realizovalo u 8 pacientov. U 3 pacientov s pozitívnou SLU boli neskôr na celotelovej scintigrafii skeletu prítomné aj kostné metastázy, v jednom prípade aj pri negatívnej SLU u pacienta s malígnym melanómom (Clark II–III, Breslow 6 mm) sa do 3,5 roka objavili mts. Pozitivita SLU alebo neskoršie stanovenie diagnózy malígneho melanómu a tým jeho neskoršej liečby môže mať za následok zvýšené riziko vzniku metastáz v kostiach.
V tkanive kože zdravých jedincov s neprítomným nádorovým ochorením sa expresia HE4 nezistila. Galgano a kol. nezistili prítomnosť expresie HE4 v karcinómoch z bazálnych buniek kože. 22 Zvýšená expresia HE4 bola nájdená v bunkách označovaných ako MALME-3M. Bunky MALME-3M sú fibroblasty získané z metastáz malígneho melanómu lokalizovaných v pľúcach. 23 Predpokladáme, že zvýšená expresia HE4 v bunkách MALME-3M z metastáz malígneho melanómu v pľúcach môže byť dôsledok obranných mechanizmov a reakcie tkaniva respiračného systému na prítomnosť metastáz malígneho melanómu v pľúcach. Produkcia HE4 by mohla zároveň odzrkadľovať progresiu nádorového ochorenia v pľúcnom tkanive. Iná lokalizácia metastáz mimo kostných tkanív sa tým môže tiež podieľať na zvyšovaní koncentrácie HE4. V našej skupine 14 pacientov s malígnym melanómom bola zvýšená hladina HE4 nad rozsah referenčných hodnôt v jednom prípade s nálezom pravdepodobných kostných mts na celotelovej scintigrafii skeletu. Zmeny sérovej koncentrácie HE4 sme u pacientov s kostnými metastázami prítomnými pri celotelovej scintigrafii skeletu nezistili, hoci koncentrácie HE4 boli vyššie u pacientov ako v kontrolnej skupine. Escudero a kol. vo svojej práci udávajú zvýšenú hodnotu HE4 v sére v jednom prípade v skupine 9 pacientov s malígnym melanómom. 24 Ľudský epididymálny proteín 4 sa v súčasnosti používa ako nádorový marker pri karcinóme ovária, kde má význam pri stanovení diagnózy, prognózy, sledovanie pacientky po operácii a v rámci diferenciálnej diagnostiky u pacientky s tumoróznou masou v oblasti panvy. V ostatnom období nadobúda HE4 ako nádorový marker význam aj pri karcinóme endometria a neustále sa objavujú nové poznatky o jeho expresii aj pri iných druhoch nádorových ochorení. 25,26 Ukazuje sa, že HE4 by mohol byť špecifickým markerom pre viaceré nádorové ochorenia, ale sú potrebné ďalšie štúdie a najmä rozšíriť súbor vyšetrovaných pacientov. Na presnejšie hodnotenie významu tohto onkomarkera by bolo potrebné vyšetriť väčší počet pacientov.
Záver
U pacientov s malígnym melanómom sme pozorovali vyššie koncentrácie ľudského epididymálneho proteínu 4 v porovnaní s kontrolnou skupinou. Sérové hladiny ľudského epididymálneho proteínu 4 nekorelovali s nálezom zisteným pri celotelovej scintigrafii skeletu. Na presnejšie posúdenie sérových koncentrácií ľudského epididymálneho proteínu 4 u pacientov s malígnym melanómom by však bolo vhodné porovnať väčší súbor pacientov a prípadne porovnať koncentrácie aj s nálezom zisteným pri celotelovom PET/CT eventuálne PET/MR vyšetrení s 18F-FDG so zameraním sa aj na metastázy v kostnej dreni.
Jaroslav Weissensteiner 1, Eva Babušíková 2
1 Oddelenie nukleárnej medicíny, Nemocnica Poprad, a.s., SR
2 Ústav lekárskej biochémie, Jesseniova lekárska fakulta v Martine, Univerzita Komenského v Bratislave, SR
jaroslav.weissensteiner@gmail.com
Zdroje
1. Bayraktutan U, Kantarci M, Pirimoglu B et al. Utility of diffusion-weighted imaging in the diagnosis of inguinal lymph node metastasis with malignant melanoma. World J Clin Cases 2014;2 : 42-44
2. Maire C, Vercambre-Darras S, Desmedt E. Diagnosis of melanoma. Rev Prat 2014;64 : 61-68
3. Bandarchii B, Jabbari CA, Vedadi A et al. Molecular biology of normal melanocytes and melanoma cells. J Clin Pathol 2013;66 : 644-648
4. Diba CS, Pleško I, Hlava P. Incidencia zhubných nádorov v Slovenskej republike 2007. Bratislava, NCZI, 2012, 135 s
5. Aladovicz E, Ferro L, Vitali GC et al. Molecular networks in melanoma invasion and metastasis. Future Oncol 2013;9 : 713-726
6. Zbytek B, Carlson JA, Granese J et al. Current concepts of metastasis in melanoma. Expert Rev Dermatol 2008;3 : 569-585
7. Bobrovská M, Minariková E, Plank L. Diagnostika malígneho melanómu. Onkológia 2009;4 : 144-148
8. Jain D, Singh T, Kumar N et al. Metastatic malignant melanoma in bone marrow with occult primary site – a case report with review of literature. Diagnostic Pathology 2007;2 : 38-41
9. Serrier C, Lesesve JF. Metastatic malignant melanoma in the bone marrow. Blood 2013;121 : 721
10. Potepan P, Spagnoli I, Danesini GM et al. The radiodiagnosis of bone metastases from melanoma. Radiol Med 1994;87 : 741-746
11. Votrubová J. Melanom. In: Votrubová J et al. Klinické PET a PET/CT. Praha, Galén, 2009; 159-162
12. Bastiaannet E, Wobbes T, Hoekstra OS et al. Prospective comparison of [18F] fluorodeoxyglucose positron emission tomography and computed tomography in patients with melanoma with palpable lymph node metastases: diagnostic accuracy and impact on treatment. J Clin Oncol 2009;27 : 4774-4780
13. Barsky M, Cherkassky L, Vezederis M et al. The role of preoperative positron emission tomography/computed tomography (PET/CT) in patients with high-risk melanoma. J Surg Oncol 2014;109 : 726-729
14. Buchbender C, Heusner TA, Lauenstein TC et al. Oncologic PET/MRI, part 2: bone tumors, soft-tissue tumors, melanoma, and lymphoma. J Nucl Med 2012;53 : 1244-1252
15. Kirchhoff C, Habben I, Ivell R et al. A major human epididymis-specific cDNA encodes a protein with sequence homology to extracellular proteinase inhibitors. Biol Reprod 1991;45 : 350-357
16. Kirchhoff C. Molecular characterization of epididymal proteins. Rev Reprod 1998;3 : 86-95
17. Bingle L, Cross SS, High AS et al. WFDC2 (HE4): a potential role in the innate imunity of the oral cavity and respiratory tract and the development of adenocarcinomas of the lung. Respir Res 2006;7 : 61-70
18. Clauss A, Lilja H, Lundwall A. A locus on human chromosome 20 contains several genes expressing protease inhibitor domains with homology to whey acidic protein. Biochem J 2002;368 : 233-242
19. Hellström I, Raycraft J, Hayden-Ledbetter M et al. The HE4 (WFDC2) protein is a biomarker for ovarian carcinoma. Cancer Res 2003;63 : 3695-3700
20. Li J, Dowdy S, Tipton T et al. HE4 as a biomarker for ovarian and endometrial cancer management. Expert Rev Mol Diagn 2009;9 : 555-566
21. Moore RG, Hill EK, Horan T et al. HE4 (WFDC2) gene overexpression promotes ovarian tumor growth. Sci Rep 2014;4 : 3574-3580
22. Galgano MT, Hampton GM, Frierson HF Jr. Comprehensive analysis of HE4 expression in normal and malignant human tissues. Mod. Pathol 2006;19 : 847-853
23. Speeckaert MM, Speeckaert R, Delanghe JR. Human epididymis protein 4 in cancer diagnostics: a promising and reliable tumor marker. Adv Clin Chem 2013;59 : 1-21
24. Escudero JM, Auge JM, Filella X et al. Comparison of serum human epididymis protein 4 with cancer antigen 125 as a tumor marker in patients with malignant and nonmalignant diseases. Clin Chem 2011;57 : 1534-1544
25. Li J, Chen H, Mariani A et al. HE4 (WFDC2) Promotes Tumor Growth in Endometrial Cancer Cell Lines. Int J Mol Sci 2013;14 : 6026-6043
26. Karlsen NS, Karlsen MA, Hogdall CK et al. HE4 tissue expression and serum HE4 levels in healthy individuals and patients with benign or malignant tumours – a systematic review. Cancer Epidemiol Biomarkers Prev 2014;23 : 2285-2295
Štítky
Nukleárna medicína Rádiodiagnostika Rádioterapia
Článok vyšiel v časopiseNukleární medicína

2015 Číslo 1-
Všetky články tohto čísla
- Interní a externí klinický audit v nukleární medicíně
- Co je na obrázku?
- Význam sentinelové uzliny u karcinomu prsu
- Indikace axilární disekce uzlin při nálezu mikrometastatického postižení sentinelové uzliny u karcinomu prsu
- Porovnanie celotelovej scintigrafie skeletu so sérovou koncentráciou ľudského epididymálneho proteínu 4 u pacientov s malígnym melanómom
- Nukleární medicína
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Indikace axilární disekce uzlin při nálezu mikrometastatického postižení sentinelové uzliny u karcinomu prsu
- Význam sentinelové uzliny u karcinomu prsu
- Interní a externí klinický audit v nukleární medicíně
- Porovnanie celotelovej scintigrafie skeletu so sérovou koncentráciou ľudského epididymálneho proteínu 4 u pacientov s malígnym melanómom
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



