-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Role 18F-FDG PET/CT při stážování a hodnocení léčebné odpovědi u agresivních forem maligních lymfomů
Role of 18F-FDG PET/CT for staging and assessment of therapy response in aggressive forms of malignant lymphomas
The treatment regimen in patients with lymphoma is selected based on the staging of the disease and prognostic factors, hence imaging methods play a central role in this process. They also have a key role in response assessment. The approach to reading and reporting positron emission tomography (PET) combined with computed tomography (PET/CT) in patients with lymphoma should be revised considering advances in recent knowledge about the disease biology and new methods of treatment. The International Harmonization Project (IHP) first published guidelines about the application of PET using 18F-fluorodeoxyglucose (18F-FDG) in lymphoma in 2007. At a conference in Lugano, the panel of experts proposed new recommendations based on the latest findings in 2013. PET/CT is included into staging of patients with 18F-FDG-avid lymphomas according to these recommendations. Biopsy can be omitted in patients with Hodgkin lymphoma and diffuse large B-cell lymphoma by evaluating bone marrow involvement using PET/CT. The Deauville 5-point scale is recommended in response assessment. The standardization of PET/CT methods is mandatory for quantitative analysis and desirable for interpretation in the context of trials.
Key Words:
18F-FDG PET/CT, lymphomas, staging, therapy response, Lugano classification
Autoři: Lenka Henzlová 1; Pavel Koranda 1; Tomáš Papajík 2
Působiště autorů: Klinika nukleární medicíny, LF UP a FN Olomouc 1; Hemato-onkologická klinika, LF UP a FN Olomouc 2
Vyšlo v časopise: NuklMed 2016;5:55-61
Kategorie: Přehledová práce
Souhrn
Volba léčebného postupu u pacientů s maligním lymfomem závisí ve značné míře na určení stádia onemocnění a zhodnocení prognostických faktorů. Zobrazovací metody hrají proto v tomto rozhodování nezastupitelnou roli. Svou významnou úlohu mají také v hodnocení léčebné odpovědi. S rozvojem znalostí o biologické povaze onemocnění a s vývojem nových metod léčby je třeba průběžně revidovat i přístup k vyhodnocování a interpretaci nálezů pozitronové emisní tomografie (PET) kombinované s výpočetní tomografií (PET/CT). Původní doporučení pro použití PET s použitím 18F-fluorodeoxyglukózy (18F-FDG) u pacientů s maligními lymfomy byla publikována mezinárodní pracovní skupinou (IHP) v roce 2007. Na základě řady nových dat a výsledků klinických studií byla v roce 2013 panelem expertů na konferenci v Luganu vydána doporučení nová, zahrnující PET/CT vyšetření do standardního stážování pacientů s 18F-FDG avidními lymfomy. U pacientů s Hodgkinovým lymfomem a s difuzním B-velkobuněčným lymfomem je pomocí PET/CT možno zhodnotit i postižení kostní dřeně a vyhnout se tak její biopsii. Při hodnocení léčebné odpovědi pomocí PET/CT je doporučeno použití tzv. Deauvilleské 5bodové škály. Cílem nových doporučení je zlepšení a sjednocení hodnocení PET/CT nálezů u pacientů s lymfomy na jednotlivých pracovištích provádějících toto vyšetření.
Klíčová slova:
18F-FDG PET/CT, lymfomy, stážování, léčebná odpověď, Luganská klasifikaceÚvod
Typy maligních lymfomů, které vykazují vysokou a stabilní 18F-FDG aviditu jsou úzce spjaty s vývojem PET již od jejího zavedení do běžné klinické praxe. Stážovací systémy i kritéria hodnocení léčebné odpovědi vyvinuté v minulosti jsou vlivem pokroku v zobrazovacích metodách, užití prognostických indexů a molekulární diagnostice postupně upravovány tak, aby dokázaly lépe charakterizovat onemocnění pacienta a jeho prognózu na začátku onemocnění i v průběhu léčby. První doporučení pro použití PET s 18F-FDG u pacientů s lymfomem byla publikována v roce 2007 1 a PET byla zahrnuta do revidovaných kritérií léčebné odpovědi. 2 V průběhu času byly přinášeny další důkazy o významu a úloze PET a později PET/CT ve stážování a hodnocení léčebné odpovědi u Hodgkinova lymfomu (HL) a vybraných typů ne-hodgkinských lymfomů (NHL).
Pokroky v zobrazování vedly ke snaze prokázat přínos úpravy léčebného režimu individuálně, na základě časného zobrazení léčebné odpovědi. Klinické studie zabývající se tímto tématem si vyžádaly standardizaci hodnocení PET/CT nálezů k dosažení co nejvyšší shody mezi hodnotiteli, a tak byla navržena 5bodová škála, tzv. Deauvilleská kritéria. 3 Tato škála byla původně určena k hodnocení v průběhu terapie, později byla navržena jako vhodný nástroj i k hodnocení po ukončení léčby. Zároveň byly také testovány nové způsoby kvantitativního hodnocení PET/CT s vyjádřením intenzity akumulace 18F-FDG pomocí standardized uptake value (SUV), celkového objemu nádorové tkáně (metabolic tumor volume – MTV), případně kombinací obou těchto parametrů (total lesion glycolysis – TLG).
Na základě workshopu v rámci 11th International Conference on Malignant Lymphoma (ICML) v Luganu v červnu 2011, jehož se účastnili přední hematologové, onkologové, radiační onkologové, patologové, radiologové a specialisté nukleární medicíny, a na základě dalších setkání v rámci Fourth International Workshop on PET in Lymphoma v Mentonu v roce 2012 a 12th ICML v Luganu 2013 byla vydána aktualizovaná doporučení ke stážování a hodnocení léčebné odpovědi pro HL a NHL, tzv. Luganská klasifikace. 4,5 Cílem tohoto článku je shrnout hlavní body těchto doporučení především z hlediska úlohy PET/CT v jejich rámci.
Interpretace PET/CT
Nejčastějším způsobem hodnocení PET/CT v každodenní praxi je vizuální hodnocení, nejlépe ve standardní barevné škále a s normováním k určité hodnotě SUV. Fúzované obrazy PET/CT umožňují identifikovat lokality se zvýšenou akumulací 18F-FDG a odlišit postižení lymfomem od tkání s fyziologicky vysokou konsumpcí glukózy a od zánětlivých lézí.
Fokální akumulace 18F-FDG v kostech nebo kostní dřeni představuje s vysokou senzitivitou její postižení lymfomem u HL a agresivních typů NHL. Podle práce dánských autorů na souboru pacientů s HL nedošlo u žádného z pacientů ke změně léčebného přístupu, pokud by byla kostní dřeň hodnocena pouze pomocí 18F-FDG PET/CT s vynecháním biopsie kostní dřeně. 6 U difuzního B-velkobuněčného lymfomu (DLBCL) prameny rovněž uvádějí, že u pacientů bez známek akumulace 18F-FDG v kostní dřeni a pacientů s fokální akumulací 18F-FDG v lokalitách vzdálených od lopaty kosti kyčelní je malá šance prokázat rutinní biopsií postižení kostní dřeně. 7 Otázka, zda pozitivní nález při biopsii kostní dřeně identifikuje jedince s horší prognózou ve srovnání s pacienty klasifikovanými jako vysoce rizikoví pouze podle neinvazivního stážování, vyžaduje další zkoumání. Prozatím však autoři navrhují upuštění od rutinního provádění biopsie u pacientů s DLBCL a HL v případě průkazu ložiskového procesu v kostní dřeni.
Obtížnější je hodnocení difuzního zvýšení akumulace radiofarmaka v kostní dřeni, které může signalizovat pouze její reaktivní hyperplazii. Proto by tento nález měl být vždy ověřen biopticky, zvláště pokud nejsou u pacienta přítomny jiné rizikové faktory. Nižší stupeň infiltrace kostní dřeně nádorovými buňkami (pod 20 %) či koexistence indolentního lymfomu a DLBCL nemusí být pomocí PET/CT diagnostikována. Podobně difuzní postižení mening nemůže být v důsledku fyziologicky vysokého vychytávání FDG v mozku při 18F-FDG PET/CT zjištěno; zde je metodou volby magnetická rezonance (MR).
Při hodnocení léčebné odpovědi je klíčový pokles akumulace 18F-FDG v patologických lézích, je tedy optimální, pokud je provedeno i vstupní vyšetření před započetím léčby. Starší IHP kritéria 1, která definovala nález jako pozitivní/negativní na základě srovnání s mediastinálním krevním poolem u lézí větších než 2 cm a s okolním pozadím u lézí menších než 2 cm, měla prokázaný prognostický význam při hodnocení po ukončení léčby, méně však v jejím průběhu. 8 Hodnocení odpovědi na léčbu, jako víceméně kontinuálního procesu, v jejím průběhu vyžaduje jemnější než dichotomické rozdělení, a proto byla navržena vizuální 5bodová škála (5-PS). Ta srovnává akumulaci radiofarmaka v patologických lézích s mediastinálním krevním poolem a s akumulací radiofarmaka v játrech. 9 Tato škála byla doporučena panelem expertů na 1. mezinárodním workshopu zabývajícím se PET u lymfomu, který se konal v Deauville ve Francii 3, a je proto někdy nazývána Deauvilleskými kritérii. Její výhodnost byla později potvrzena několika mezinárodními studiemi jak pro použití u časného PET/CT, tak i PET/CT po ukončení chemoterapie. 3,10
Deauvilleská kritéria hodnotí lokalitu s nejvyšší intenzitou akumulace 18F-FDG následovně: (Obr. 1)
Obr. 1. (vpravo) A - Deauvilleské skóre 1, B - Deauvilleské skóre 2, C - Deauvilleské skóre 3, D - Deauvilleské skóre 4, E - Deauvilleské skóre 5, F - Deauvilleské skóre X – duktální karcinom prsu. 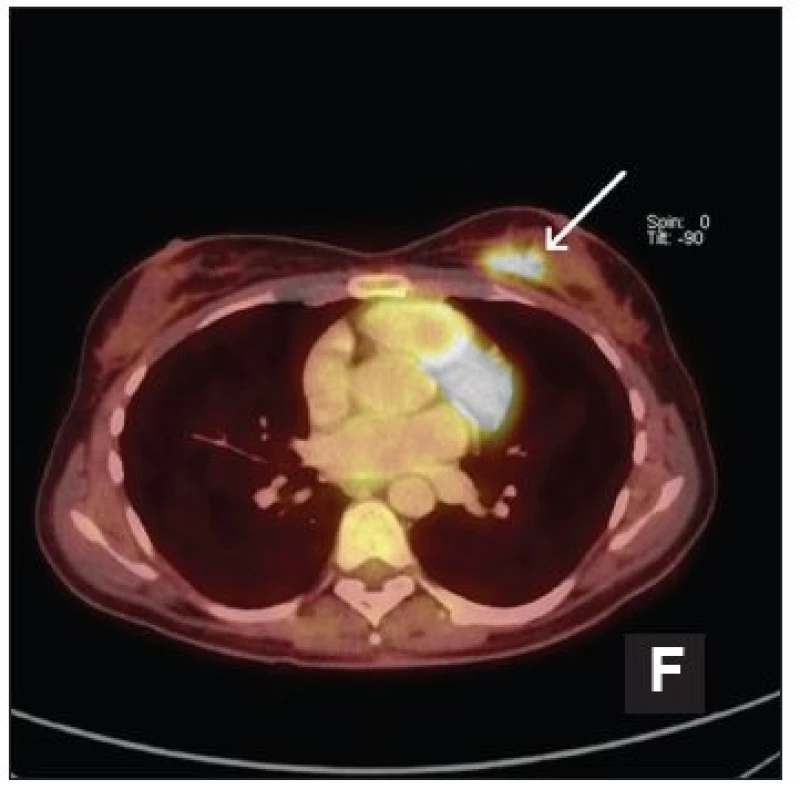
- žádná akumulace
- kumulace ≤ krevní pool mediastina
- akumulace > krevní pool mediastina, ale ≤ v játrech
- akumulace mírně vyšší ve srovnání s játry
- akumulace výrazně vyšší ve srovnání s játry
X. nové léze, které pravděpodobně nesouvisí s lymfomem
Výhodou Deauvilleské škály je flexibilita rozlišení mezi tzv. pozitivním a negativním výsledkem. Většinou je za negativní považováno skóre 1–3. Stupeň 3 lze však považovat za pozitivní výsledek ve vědeckých studiích zaměřených na eskalaci léčby, kde je třeba vysoká pozitivní prediktivní hodnota. Rozlišení stupně 4 a 5 je podle autorů navrženo tak, že skóre 5 reprezentuje léze s akumulací vyšší než dvoj - až trojnásobek SUVmax velké oblasti zájmu vyznačené ve zdravém jaterním parenchymu. 5 Podle těchto doporučení pak skóre 1 a 2 znamená kompletní metabolickou odpověď (CMR), skóre 3 u pacientů léčených standardními léčebnými režimy také pravděpodobně znamená CMR. Skóre 4 a 5, pokud dojde k redukci akumulace 18F-FDG při srovnání se vstupním vyšetřením, představují parciální metabolickou odpověď, zároveň však znamenají reziduální onemocnění. Zvýšení akumulace 18F-FDG na skóre 5, skóre 5 bez poklesu akumulace 18F-FDG a průkaz nové léze vychytávající glukózu způsobené lymfomem představují selhání léčby a/nebo progresi.
Kvantitativní hodnocení poklesu akumulace 18F-FDG v nádorové tkáni pomocí procentuálního poklesu SUVmax (ΔSUVmax) vykazuje vysokou reprodukovatelnost mezi různými hodnotiteli a může snižovat podíl falešně pozitivních výsledků. 11 Nevýhodou je nutnost přesně dodržet standardní akviziční protokol u všech prováděných vyšetření a správná kalibrace přístroje. Navíc hodnoty cut-off ΔSUVmax rozlišující pacienty s příznivou a nepříznivou prognózou se logicky liší u různých histologických typů lymfomů, u vyšetření prováděných v různých fázích léčby i u jednotlivých terapeutických režimů. 12
Úloha PET/CT při určení stádia maligního lymfomu
PET/CT by v běžné klinické praxi i v klinických studiích mělo být upřednostněno před samotným CT při stážování těch typů lymfomů, které obvykle vykazují 18F-FDG aviditu. Součástí prognostických indexů, které jsou používány ke stratifikaci pacientů dle rizika a k rozhodnutí o léčebném režimu, je stanovení přesného stádia onemocnění většinou jedním ze základních bodů, zobrazovací metody mají tedy v tomto procesu nezastupitelný význam. Přidanou hodnotou může být určení nejvýhodnějšího místa pro biopsii nádorové masy. Pro lymfomy s nízkou akumulací 18F-FDG (například SLL) zůstává nezastupitelné hodnocení pomocí CT.
Přínosem využití intravenózně podané jodové kontrastní látky (KL) při PET/CT je zpřesnění hodnocení nálezu v oblasti břicha a pánve, zpřesnění měření velikosti uzlinového postižení a zhodnocení komprese velkých cév nádorovými masami. Může odhalit život ohrožující stavy jako hlubokou žilní trombózu nebo embolizaci do a. pulmonalis, potřebné je i k plánování zevního ozáření. Má však také svá rizika, především vyvolání alergické reakce nebo vznik kontrastové nefropatie. Použití KL může vést k malým odchylkám v měření SUV vlivem na korekci zeslabení záření, jejich klinický význam však není velký. O použití KL při opakovaných vyšetřeních (např. časný PET) by měl rozhodnout typ a lokalizace nádorového postižení při vstupním PET/CT. Pokud při vstupním vyšetření není prokázáno ložiskové postižení parenchymových orgánů, pak při časném PET/CT vyšetření není třeba intravenózní KL podávat. 13
Úloha časného PET/CT
Časný PET/CT nebo též interim PET/CT (prováděný po 2 až 3 cyklech chemoterapie) zatím není sice doporučen pro běžnou klinickou praxi, ale je často prováděn v rámci kontrolovaných klinických hodnocení. Cílem hodnocení časné léčebné odpovědi je především identifikovat pacienty nedostatečně citlivé na podávanou terapii a dle výsledku eventuálně časně eskalovat následnou terapii a zlepšit celkové přežití těchto nemocných. Druhým důvodem pak může být identifikace primárně prognosticky nepříznivých nemocných s generalizovanou chorobou, kteří však na podanou léčbu velmi dobře reagují a její další eskalace nebo plánovaná konsolidace vysoce dávkovanou terapií u nich nepřináší zlepšení léčebného výsledku, ale naopak může zvýšit riziko nežádoucích účinků pro nemocné. Tyto dva cíle jsou testovány v řadě klinických studií.
Většina publikovaných dat uvádí dobrou prediktivní hodnotu časného PET/CT ve srovnání s CT, neboť metabolická odpověď předchází anatomickou změnu. 14 Novější práce však připouštějí nižší prediktivní hodnotu časného PET/CT při použití imunochemoterapie vlivem vyššího počtu falešně pozitivních výsledků (patrně vlivem zánětlivých změn probíhajících v nádorových ložiscích po podání rituximabu) a uvádějí vyšetření na konci terapie jako lepší prediktor. 15
Snahy o lepší standardizaci při hodnocení časného PET/CT v rámci klinických hodnocení vedly ke zkoumání kvantitativních metod interpretace nálezů. Hodnocení pomocí ΔSUVmax je použito ve studii PETAL (Positron Emission Tomography Guided Therapy of Aggressive Non-Hodgkin Lymphomas). 16 Dalšími navrženými parametry jsou metabolický objem nádorové tkáně – „metabolic tumor volume“ (MTV) a celková úroveň glykolýzy patologických lézí – „total lesion glycolysis“ (TLG) vypočtená jako MTV x SUVmean. Předběžné výsledky hodnotící tato měření jsou rozporuplné. 17,18
Úloha PET/CT po ukončení terapie
PET/CT po ukončení terapie je u 18F-FDG avidních typů lymfomů standardem, protože je prokázána jeho vysoká negativní prediktivní hodnota (NPV) (80–100 %), i když výsledky pozitivní prediktivní hodnoty (PPV) jsou poněkud variabilnější (50–100 %). 19 Pokud je na finálním PET/CT přítomna metabolicky aktivní reziduální masa a zvažuje se podání záchranné („salvage“) terapie, je doporučeno bioptické ověření nálezu. Pokud je přítomnost reziduální viabilní nádorové tkáně málo klinicky pravděpodobná, je možno zopakovat vyšetření s časovým odstupem. U pacientů s pokročilými stádii HL, u kterých je dosaženo PET negativity, tedy i u pacientů s přítomností metabolicky neaktivní reziduální masy, není potřebná radioterapie. 20 Kritéria hodnocení finálního PET/CT z roku 2007 1 doporučovala vizuální hodnocení a srovnání s krevním poolem mediastina. Nejnovější doporučení je používat k hodnocení závěrečného PET/CT u HL, DLBCL a folikulárního lymfomu (FL) Deauvilleskou škálu, kde skóre 4 a 5 značí selhání léčby. Pro hodnocení léčebné odpovědi u histologických typů s nízkou nebo variabilní 18F-FDG aviditou je doporučeno CT. (Tab. 1)
Tab. 1. Použité zkratky: PET – pozitronová emisní tomografie, CT – výpočetní tomografie, MR – magnetická rezonance, <sup>18</sup>F-FDG – <sup>18</sup>F-fluorodeoxyglukóza, SPD – součet součinů dvou největších rozměrů u 6 největších uzlin nebo uzlinových mas, PPD – součin nejdelšího rozměru a druhého rozměru na nejdelší rozměr kolmého 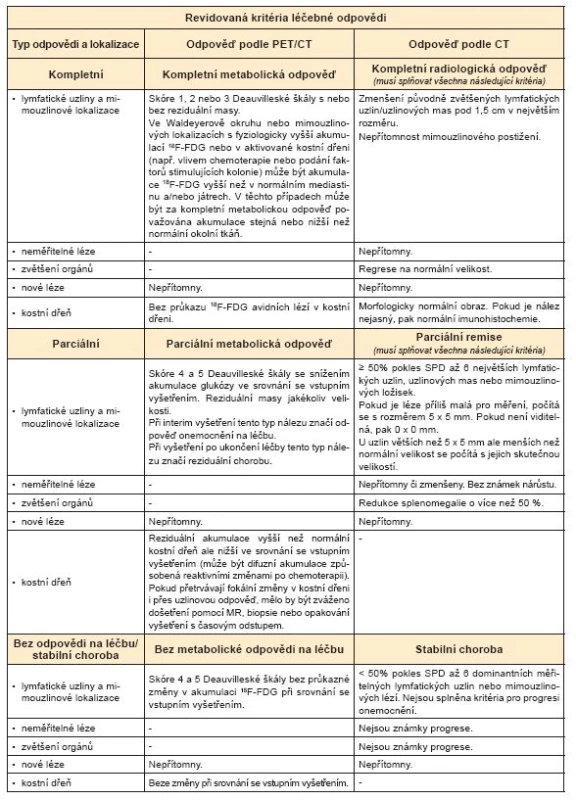

Vysvětlivky: Měření lymfatických uzlin – až 6 nejvýraznějších lymfatických uzlin, uzlinových mas a/nebo extranodálních lézí, které jsou jednoznačně měřitelné ve dvou rozměrech. Uzliny by měly být z odlišných regionů a pokud je to možné, mělo by být zahrnuto mediastinum a retroperitoneum. Extranodální léze zahrnují léze v parenchymových orgánech (např. játra, slezina, ledviny, plíce), gastrointestinální trakt, kožní léze nebo léze zjištěné při palpaci. Neměřitelné léze – jakékoliv onemocnění, které nesplňuje podmínky měřitelnosti a prokazatelně souvisí s lymfomem by mělo být považováno za neměřitelné léze; jde např. o plicní výpotky, ascites, kostní léze, postižení mozkových plen, břišní masy a další. Úloha PET/CT v následné péči
Základem dlouhodobého sledování pacientů po ukončení léčby je pečlivé fyzikální a laboratorní vyšetření, znalost pacientovy anamnézy a klinická zkušenost (různé typy lymfomů mají největší riziko relapsu v různém časovém odstupu po skončení léčby). Rutinní sledování pomocí PET/CT není doporučeno vzhledem k poměrně vysokému počtu falešně pozitivních výsledků (až 20 %), které vedou k dalšímu vyšetřování, radiační zátěži a psychické zátěži pacienta. 21,22
18F-FDG PET/CT by však mělo být provedeno vždy při klinickém podezření na recidivu onemocnění.
Závěr
Pečlivé vyhodnocení všech vstupních vyšetření pacienta i nálezů hodnotících léčebnou odpověď jsou klíčem k určení optimálního léčebného postupu u pacientů s lymfomy.
S přibývajícími znalostmi o povaze onemocnění, novými pronostickými faktory a novými způsoby léčby je třeba měnit i způsob hodnocení zobrazovacích metod. Nejnovější doporučení panelu expertů z ICML se soustředí převážně na hodnocení PET/CT při stážování a hodnocení léčebné odpovědi u HL, DLBCL a FL za použití 5-PS. Posunem je zahrnutí PET/CT u 18F-FDG avidních lymfomů do stážování, protože je senzitivnější než samotné CT. Provedení vstupního PET/CT vyšetření také zpřesňuje hodnocení léčebné odpovědi. Pacienti s HL a DLBCL mohou být díky vstupnímu PET/CT vyšetření ušetřeni biopsie kostní dřeně. Při hodnocení léčebné odpovědi u FDG avidních lymfomů jsou v sou časné době k popisu PET/CT doporučena Deauvilleská kritéria. Pro lymfomy s nízkou akumulací 18F-FDG zůstává nezastupitelné hodnocení pomocí CT.
Současná doporučení by měla sjednotit interpretaci prováděných vyšetření tak, aby bylo možno srovnávat data v rámci klinické praxe i klinických studií a dále zlepšit léčbu pacientů s lymfomy a individualizovat přístup k nim. Využití PET/CT v průběhu léčby, event. v následném sledování zůstává stále poněkud kontroverzní, otevřená je i otázka úpravy terapie na základě časného PET/CT. Pozornost je také nutno věnovat kvantitativním způsobům hodnocení PET/CT pomocí stanovení objemu nádorové masy a intenzity akumulace 18F-FDG v ní. Jejich předpokladem je však jednotná metodologie prováděných vyšetření.
Tato práce byla podpořena vnitřním grantem IGA _LF_2015_006 Univerzity Palackého v Olomouci.
lenka.henzlova@fnol.cz
Zdroje
1. Juweid ME, Stroobants S, Hoekstra OS et al. Use of positron emission tomography for response assessment of lymphoma: Consensus of the Imaging Subcommittee of International Harmonization Project in Lymphoma. J Clin Oncol 2007;25 : 571-578
2. Cheson BD, Pfistner B, Juweid ME et al. Revised response criteria for malignant lymphoma. J Clin Oncol 2007;25 : 579-586
3. Meignan M, Gallamini A, Haioun C. Report on the First International Workshop on Interim-PET-Scan in Lymphoma. Leuk Lymphoma 2009;50 : 1257-1260
4. Cheson BD, Fisher RI, Barrington SF et al. Recommendations for initial evaluation, staging, and response assessment of Hodgkin and non-Hodgkin lymphoma: the Lugano classification. J Clin Oncol 2014;32 : 3059-3068
5. Barrington SF, Mikhaeel NG, Kostakoglu L et al. Role of imaging in the staging and response assessment of lymphoma: consensus of the International Conference on Malignant Lymphomas Imaging Working Group. J Clin Oncol 2014;32 : 3048-3058
6. El-Galaly TC, d’Amore F, Mylam KJ et al. Routine bone marrow biopsy has little or no therapeutic consequence for positron emission tomography/computed tomography–staged treatment-naive patients with Hodgkin lymphoma. J Clin Oncol 2012;30 : 4508-4514
7. Khan AB, Barrington SF, Mikhaeel NG et al. PET-CT staging of DLBCL accurately identifies and provides new insight into the clinical significance of bone marrow involvement. Blood 2013;122 : 61-67
8. Cashen AF, Dehdashti F, Luo J et al. (18)FDG PET/CT for early response assessment in diffuse large B-cell lymphoma: Poor predictive value of International Harmonization Project interpretation. J Nucl Med 2011;52 : 386-392
9. Barrington SF, Qian W, Somer EJ et al. Concordance between four European centres of PET reporting criteria designed for use in multicentre trials in Hodgkin lymphoma. Eur J Nucl Med Mol Imaging 2010;37 : 1824-1833
10. Barrington SF, Fosse P, Withofs et al. Recommendations to stage and assess the response to therapy of lymphomas with [18F]FDG-PET-CT. Médecine Nucléaire 2016;40 : 55-64
11. Lin C, Itti E, Haioun C et al. Early 18F-FDG PET for prediction of prognosis in patients with diffuse large B-cell lymphoma: SUV-based assessment versus visual analysis. J Nucl Med. 2007;48 : 1626–1632
12. Casasnovas RO, Meignan M, Berriolo-Riedinger A et al. SUVmax reduction improves early prognosis value of interim positron emission tomography scans in diffuse large B-cell lymphoma. Blood 2011;118 : 37-43
13. Henzlová L, Kapitáňová Z, Buriánková E et al. Použití intravenózní kontrastní látky při interim 18F-FDG PET/CT u pacientů s non-hodgkinskými lymfomy – je nutné u všech pacientů? NuklMed 2012;1(S1):6
14. Haioun C, Itti E, Rahmouni A et al. F-18 fluoro-2-deoxy-D-glucose positron emission tomography (FDG-PET) in aggressive lymphoma: An early prognostic tool for predicting patient outcome. Blood 2005;106 : 1376-1381
15. Pregno P, Chiappella A, Bello M et al. Interim 18-FDG-PET/CT failed to predict the outcome in diffuse large B-cell lymphoma patients treated at the diagnosis with rituximab-CHOP. Blood 2012;119 : 2066-2073
16. Dührsen U, Hüttmann A, Jöckel KH et al. Positron emission tomography guided therapy of aggressive non-Hodgkin lymphomas: The PETAL trial. Leuk Lymphoma 2009;50 : 1757-1760
17. Mikhaeel NG, Smith D, Dunn JT et al. Combination of baseline metabolic tumor volume and early response on PET/CT improves progression-free survival prediction in DLBCL. Eur J Nucl Med Mol Imaging 2016;43 : 1209-1219
18. Gallicchio R, Mansueto G, Simeon V et al. F-18 FDG PET/CT quantization parameters as predictors of outcome in patients with diffuse large B-cell lymphoma. Eur J Haematol. 2014;92 : 382-389
19. Zijlstra JM, Lindauer-van der Werf G, Hoekstra OS et al. F-18-fluoro-deoxyglucose positron emission tomography for post-treatment evaluation of malignant lymphoma: A systematic review. Haematologica 2006;91 : 522-529
20. Engert A, Haverkamp H, Kobe C et al. Reduced-intensity chemotherapy and PET-guided radiotherapy in patients with advanced stage Hodgkin’s lymphoma (HD15 trial): a randomised, open-label, phase 3 non-inferiority trial. Lancet 2012;379 : 1791-1799
21. Jerusalem G, Beguin Y, Fassotte MF et al. Early detection of relapse by whole-body positron emission tomography in the follow-up of patients with Hodgkin’s disease. Ann Oncol 2003;14 : 123-130
22. Zinzani PL, Stefoni V, Tani M et al. Role of [18F]fluorodeoxyglucose positron emission tomography scan in the follow-up of lymphoma. J Clin Oncol 2009;27 : 1781-1787
Štítky
Nukleárna medicína Rádiodiagnostika Rádioterapia
Článok vyšiel v časopiseNukleární medicína

2016 Číslo 3-
Všetky články tohto čísla
- História slovenskej nukleárnej medicíny
- Vybraná abstrakta 53. Dnů nukleární medicíny Luhačovice 21. – 23. 9. 2016
- Komentář k článku „Artefakty u perfuzní scintigrafie myokardu“
-
Artefakty u perfuzní scintigrafie myokardu
1. část - Role 18F-FDG PET/CT při stážování a hodnocení léčebné odpovědi u agresivních forem maligních lymfomů
- Nukleární medicína
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- História slovenskej nukleárnej medicíny
-
Artefakty u perfuzní scintigrafie myokardu
1. část - Role 18F-FDG PET/CT při stážování a hodnocení léčebné odpovědi u agresivních forem maligních lymfomů
- Komentář k článku „Artefakty u perfuzní scintigrafie myokardu“
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy








