-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Retroperitoneoskopická adrenalektomie dorzálním přístupem
Retroperitoneoscopic adrenalectomy with dorsal approach
Introdustion:
Various surgical mininvasive approaches for adrenalectomy have been established over the last two decades. We are evaluating the retroperitoneoscopic adrenalectomy with dorsal approach.Material and methods:
The prospective open clinical trial was carried out to evaluate intra-operative (operations time, intraoperative complications, blood loss, conversion rate) and peri-operative parameters (morbidity, mortality, hospital stay). Patients who underwent retroperitoneoscopic adrenalectomy with dorsal approach were included in the trial. A tumor size above 12 cm or BMI higher than 35kg/m2 were considered asexclusion criteria. All the patients were perioperatively managed by a multidisciplinary team.Results:
A total of 81 patients were assessed (average age: 45.7 yrs, 37 males, 44 females, BMI 27.8 kg/m2). The average operating time was 61 minutes. The intraoperative blood loss was below 20 ml. The mean hospital stay was 2.1 days. Morbidity was 2.7% and mortality 0%.Conclusion:
Retroperitoneoscopic adrenalectomy with dorsal approach is considered a method of choice in our hospital. The use of this approach is safe, efficient, with excellent reproducible operative results and impressive patient recovery.Key words:
adrenalectomy – retroperitoneoscopic – dorsal
Autoři: P. Zonca 1,2; M. Cambal 1,2; P. Labaš 2; C. A. Jacobi 1
Působiště autorů: Zentrum für Viszeral und Minimal Invasive Chirurgie, Wesseling, Köln am Rhein, Německo, přednosta: Prof. Dr. med. C. A. Jacobi, Ph. D. 1; 1. Chirurgická klinika, Bratislava, přednosta: Prof. MUDr. Peter Labaš, CSc. 2
Vyšlo v časopise: Rozhl. Chir., 2012, roč. 91, č. 4, s. 235-240.
Kategorie: Původní práce
Souhrn
Úvod:
Během posledních dvou dekád se objevily různé miniinvazivní přístupy k adrenalektomii. Zde hodnotíme retroperitoneoskopickou adrenalektomii dorzálním přístupem.Materiál a metodika:
V prospektivní otevřené klinické studii hodnotíme operační (operační čas, intraoperační komplikace, ztráta krve, konverze) a perioperační parametry (30denní morbidita a mortalita, délka hospitalizace). Vstupním kritériem do studie byla adrenalektomie provedená dorzálním retroperitoneoskopickým přístupem. Za exkluzivní kritéria byly považovány tumory větší než 12 cm nebo BMI pacienta vyšší než 35 kg/m2. Diagnostika, příprava k operaci a pooperační péče byly výsledkem interdisciplinární spolupráce.Výsledky:
Bylo zhodnoceno celkem 81 pacientů s průměrným věkem 45,7 roku. Celkem bylo 37 mužů a 44 žen s BMI 27,8 kg/m2. Průměrný operační čas byl 61 minut. Provedli jsme jednu konverzi. Intraoperační ztráty krve byly ve všech případech pod 20 ml. Průměrná délka hospitalizace byla 2,1 dne. Pooperační 30denní morbidita byla 3,7 % a perioperační mortalita byla 0 %.Závěr:
V současné době preferujeme v případě možnosti miniinvazivní operace jednoznačně dorzální retroperitoneoskopickou adrenalektomii a považujeme ji za metodu volby. Tato je operace je bezpečná, efektivní a má dobré výsledky včetně extrémně rychlé rekonvalescence.Klíčová slova:
adrenalektomie – retroperitoneoskopická – dorzálníÚvod
Adrenalektomie otevřenou cestou vyžaduje rozsáhlý přístup k hluboce uloženému, relativně malému orgánu. Miniinvazivní přístup při adrenalektomii představuje zásadní benefit pro pacienta. Dovoluje lepší vizualizaci operačního pole ve srovnání s otevřenou chirurgií. Miniinvazivní adrenalektomii je možné provést laparoskopicky nebo retroperitoneoskopicky. Technika laparoskopická adrenalektomie byla popsána už v roce 1991 Snowem [1] a následně v roce 1992 Gagnerem [2, 3], který ji dále rozpracoval. Standardně se označuje laparoskopický přístup jako Gagnerův přístup. V českém písemnictví se rovněž objevuje řada studií zabývajících se laparoskopickou adrenalektomii [4, 5, 6]. Jak uvádí Frillingová, již v roce 1993 popsal italský urolog Mandressi adrenalektomii retroperitoneoskopickou cestou [7]. První soubor jedenácti pacientů s retroperitoneoskopickou adrenalektomii pak prezentoval Mercan v roce 1995 [8]. Retroperitoneoskopický přístup nabízí oproti laparoskopickému transperitoneálnímu přístupu další výhody. Je možné zvolit laterální nebo dorzální retroperitoneoskopický přístup. K zásadnímu rozšíření dorzálního retroperitoneoskopického přístupu jak v Evropě, tak v USA přispěl Dr. Walz z Essenu, který jej poprvé publikoval stejně jako Mercan již v roce 1995 [9]. V naší práci představujeme techniku retroperitoneoskopické adrenalektomie dorzálním přístupem u vlastního souboru pacientů s rozborem výsledků.
Cílem naší prospektivní otevřené klinické studie je zhodnocení operačních (operační čas, intraoperační komplikace, ztráta krve, konverze) a perioperačních parametrů (30denní morbidita a mortalita, délka hospitalizace). Vstupním kritériem do studie byla adrenalektomie provedená dorzálním retroperitoneoskopickým přístupem. Za exkluzivní kritéria byly považovány tumory větší než 12 cm nebo BMI pacienta vyšší než 35 kg/m2.
Diagnostika, příprava k operaci a pooperační péče jsou úkolem centra s funkční interdisciplinární spoluprací. Operační indikace vychází z doporučení Německé endokrinologické společnosti a v souvislosti s velikostí incidentalomů jsou dále zmíněny v diskuzi.
Operační technika
Použili jsme techniku rozvinutou Dr. Walzem [10, 11]. Pacient je při této technice v pronační „jack-knife“ pozici (Obr. 1).
Obr. 1a: Schéma operační polohy Fig. 1a: Operation position 
Obr. 1b: Pozice trokarů Fig. 1b: Positioning of trocars 
Důležité je získání co největšího prostoru mezi lopatou kosti kyčelní a žeberním obloukem v dorzální oblasti a relativně volně ležícího břicha. Tím je zajištěn dostatečný prostor pro manipulaci s nástroji dorzálně a zároveň dosahujeme minimálního tlaku intraabdominálních orgánů z přední strany na retroperitoneum. Používáme lehce modifikovanou pozici jednoho 12mm, jednoho 10mm a jednoho 5mm trokaru (Obr. 2).
Obr. 1. Identifikace nadledviny - levá strana Fig. 2: Identification of suprarenal gland – the left side 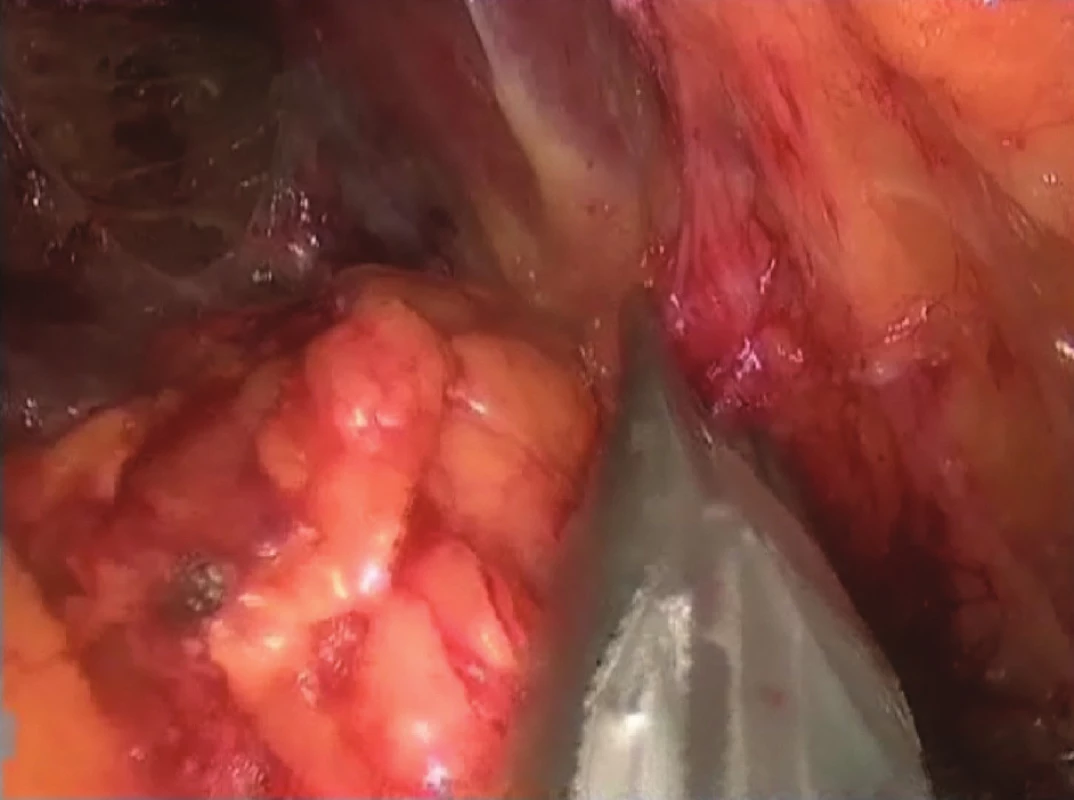
Za sterilních kautel vedeme nejprve příčně orientovanou incizi kraniálně od lopaty kosti kyčelní přibližně ve skapulární linii. Ostře pronikáme svalovou vrstvou do retroperitoneálního prostoru. Následně digitálně vytváříme v retroperitoneu prostor. Nepoužíváme spacer. Zavádíme 10mm trokar pro kameru. Používáme retrokapnoperitoneum ve výši 18 mm Hg, eventuálně u obézních pacientů až do výše 24 mm Hg. Následuje zavedení 12mm trokaru z laterální strany a 5mm trokaru paravertebrálně. Oba trokary směřují kraniálně směrem k poloze nadledviny. Používáme standardní 30stupňovou optiku, kterou zavádíme 10mm trokarem. Pro další preparaci nadledviny je potřebné vytvořit dostatečně velký prostor ve fossa pararenalis posterior až k bránici. Pokračujeme v preparaci prostoru, který byl na začátku vytvořen digitálně. Z mediální strany je hranicí paraspinální muskulatura. Nahoře je možné přes peritoneum identifikovat zadní stranu jater nebo sleziny dle operované strany. Perinefritický tuk musí zůstat s výjimkou horního pólu ledviny intaktní. Identifikujeme nadledvinu (Obr. 3). Oddělíme nadledvinu od horního pólu ledviny. Zajišťujeme přímý přístup k hilárním cévám nadledviny. Výhodou je to, že není nutné retrahovat přilehlé orgány jako u transabdominálního přístupu a zároveň v tomto okamžiku nemusíme manipulovat s fragilní tkání nadledviny. Identifikujeme vena suprarenalis a po naložení klipů ji centrálně přerušujeme (Obr. 4). Je nutné myslet na anatomickou diferenci pravé a levé strany vzhledem ke vztahu vena suprarenalis k vena cava inferior. Následuje kompletní mobilizace nadledviny harmonickým ACE (Ethicon Endosurgery) z laterální, diafragmatické a ventrální strany včetně přerušení arteriálního zásobení bez nutnosti naložení dalších klipů. Po kompletní mobilizaci nadledviny ji vkládáme do endobagu a po rozšíření incize kamerového trokaru ji extrahujeme z retroperitonea. Je vhodné postupné snižování retrokapnoperitonea za vizuální kontroly k identifikaci eventuálního venózního krvácení, které se při přetlaku intraoperačně neprojeví. Nepoužíváme drenáž. Odstraňujeme trokary a uzavíráme rány. S výjimkou operace feochromocytomu, kdy anesteziolog zajišťuje arteriální přístup, je použit standardní periferní venózní přístup. Standardně trvá hospitalizace 1–3 dny. Delší hospitalizace je nutná u některých hormonálně aktivních tumorů včetně feochromocytomu ke korekci eventuálních dysbalancí. Tuto operaci je možno provést i v rámci jednodenní chirurgie, kdy pacient po krátkém pobytu na dospávacím pokoji odchází domů.
Obr. 2. Přerušení v. suprarenalis po naložení klipů centrálně Fig. 3: Dissection of vena suprarenalis after the central clips placement 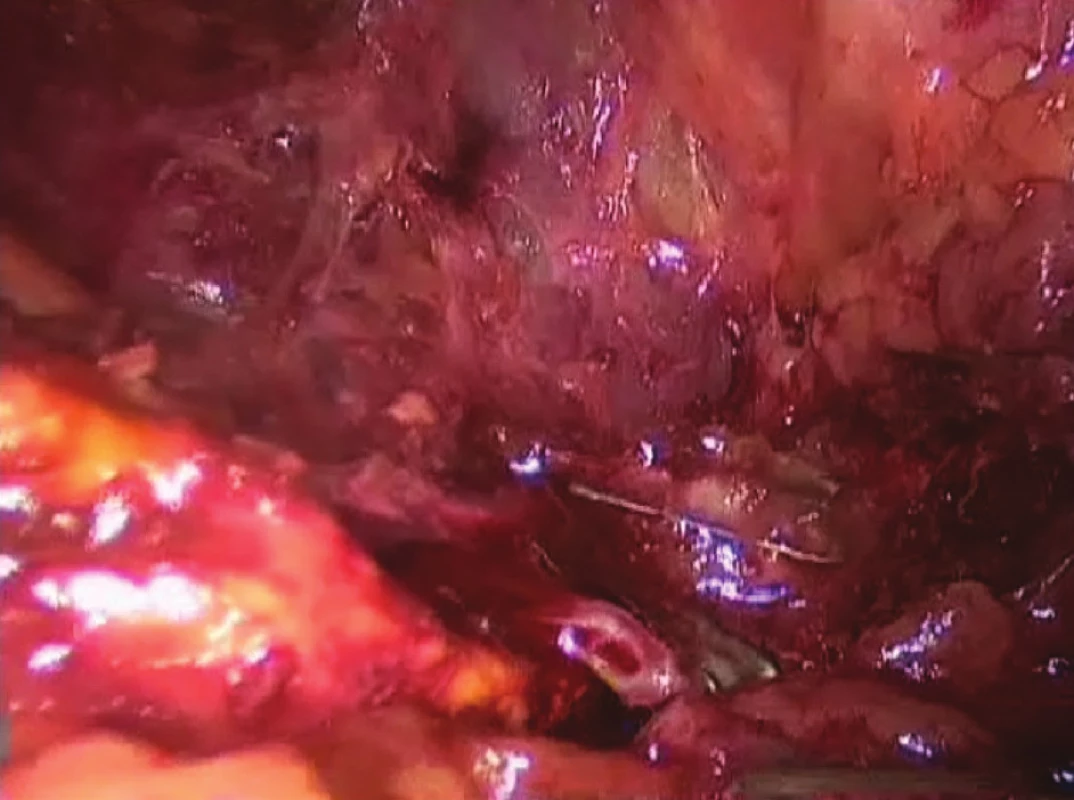
Materiál a metodika
Na našem pracovišti ve Wesselingu jsme operovali od srpna 2007 do listopadu 2011 celkem 81 pacientů s průměrným věkem 45,7 roku. Celkem bylo 37 mužů a 44 žen s BMI 27,8 kg/m2. Levostranná operace byla provedena celkem 44krát a pravostranná celkem 39krát. Průměrná velikost tumoru byla 3,7 cm. Parametry jsou přehledně shrnuty v Tab. 1. Indikace k operaci jsou přehledně shrnuty v Tab. 2. Průměrný operační čas byl 61 minut. Provedli jsme jednu konverzi z důvodu nepřehledných anatomických poměrů při fibróze po anamnesticky předchozí proběhlé pankreatitidě. Vyskytly se následující intraoperační komplikace: poranění v. hepatica posterior (miniinvazivní ošetření defektu) a poranění peritonea (miniinvazivní ošetření defektu). Intraoperační ztráty krve byly ve všech případech pod 20 ml. Pooperačně se u 3 pacientů vyskytla atelektáza nebo pneumonie. Průměrná délka hospitalizace byla 2,1 dne. Tyto parametry jsou přehledně shrnuty v Tab. 3.
Tab. 1. Základní údaje pacientů a tumoru Tab. 1: Basic data on the patients and tumors 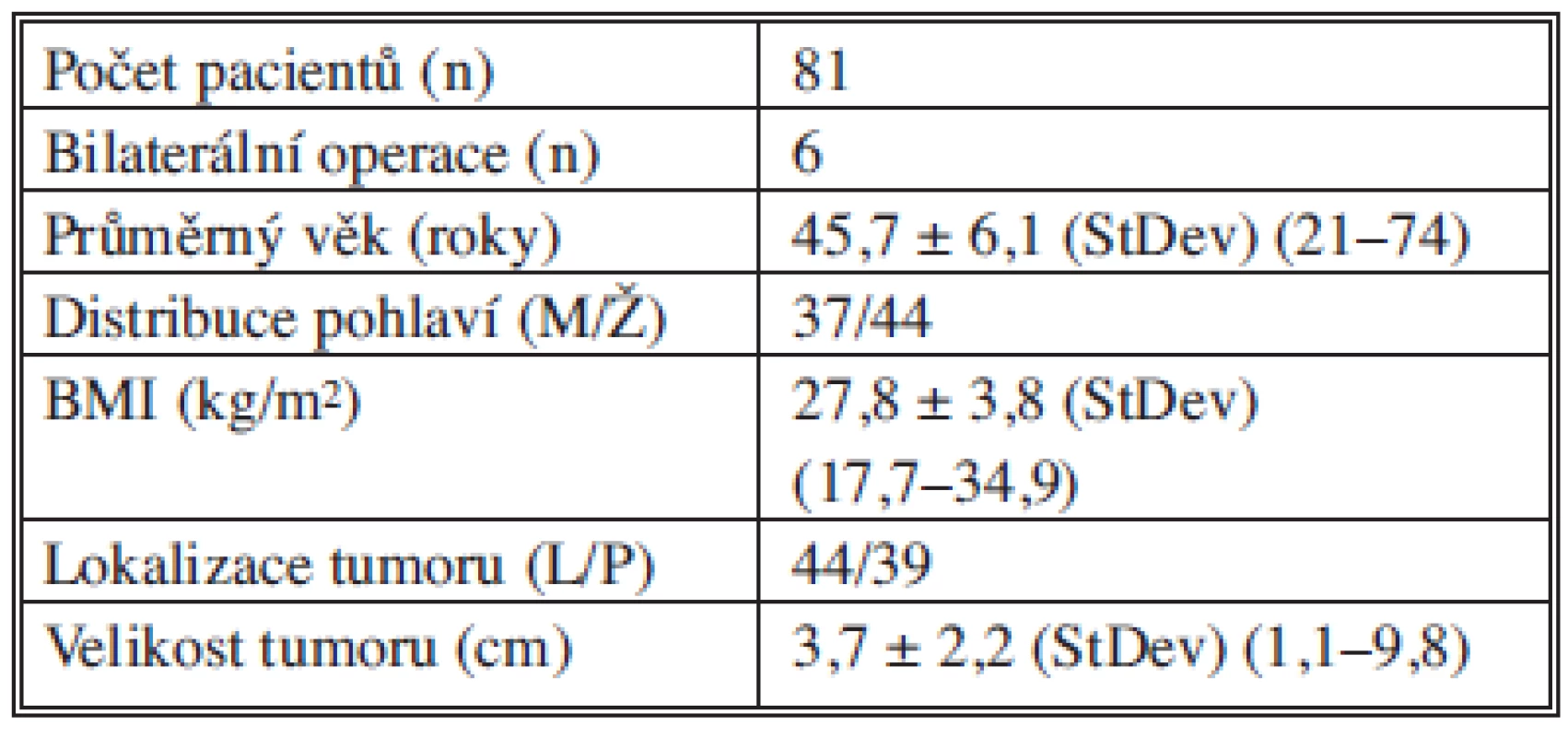
Tab. 2. Spektrum indikací Tab. 2: Indication spectrum 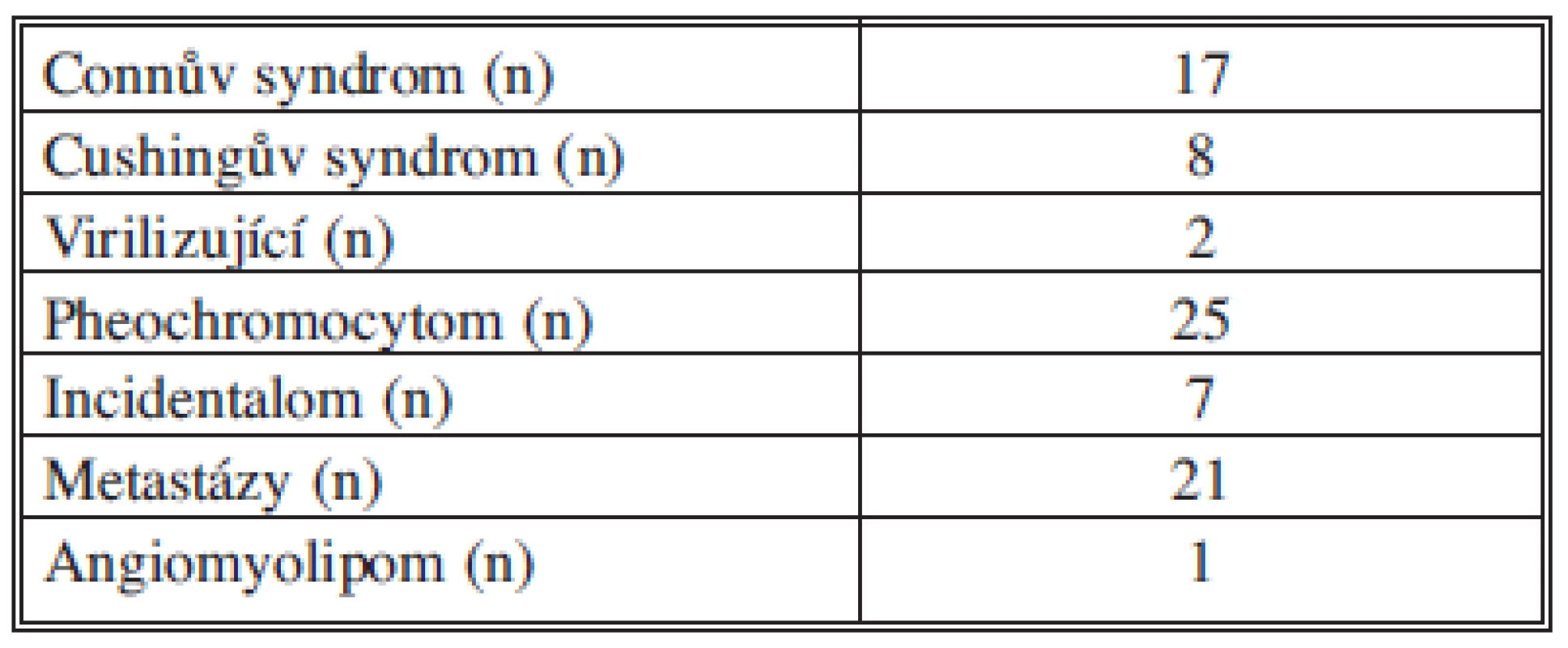
Tab. 3. Vybrané operační a perioperační parametry Tab. 3: Selected operative and peri-operative parameters 
Diskuze
Základní parametry našeho souboru daného věkovým spektrem pacientů, distribucí pohlaví, BMI, stranovou orientací tumoru odpovídají běžnému rozložení v populaci a dalším studiím zabývajícím se podobnou problematikou.
Výsledky kontrolovaných studií z konce 90. let ukazují jednoznačnou výhodu laparoskopické nad otevřenou adrenalektomií, pokud jde o intraoperační morbiditu, mortalitu a délku hospitalizace [12, 13]. Mininvazivní laparoskopická adrenalektomie se stala zlatým standardem [14]. Studií zabývajících se srovnáním laparoskopického a retroperitoneoskopického přístupu, ať již laterálním nebo dorzálním přístupem, je již méně. Jedná se však většinou o studie, které mají malé soubory pacientů. Jedna z prvních studií je Takedova studie z roku 1997, která však měla pouze 11 pacientů ve větvi s retroperitoneoskopickým přístupem. Průměrný operační čas byl 248,3 minuty, krevní ztráta 151,4 ml. Takeda uzavřel, že není rozdíl mezi laparoskopickým a retroperitoneoskopickým přístupem, pokud jde o operační čas, krevní ztrátu nebo o délku rekonvalescence [15]. Dalším autorem srovnávajícím retroperitoneoskopický a laparoskopický přístup byl Naya. V rameni s retroperitoneoskopickým přistupem bylo 22 pacientů. Průměrný čas u laparoskopické adrenalektomie byl 202 minut a u retroperitoneoskopické adrenalektomie byl 221 minut. Ztráty krve byly 113 a 192 ml u jednotlivých skupin. Čas zahájení perorálního příjmu a délka hospitalizace se signifikantně nelišily [16]. Dickson z Houstonu prezentoval své zkušenosti se 118 adrenalektomiemi operovanými retroperitoneoskopicky a srovnal je s předchozími zkušenostmi. Nenalezl signifikantní rozdíly v operačním čase (110 versus 118 min) a BMI (29,63 versus 29,93). Rovněž nebyl nalezen statisticky signifikantní rozdíl v morbiditě a mortalitě u obou skupin. Dokonce 48 % pacientů mělo BMI vyšší než 30 kg/m2 [17]. Další autoři, kteří srovnali dorzální a laterální retroperitoneoskopický přístup, uvádějí, že laterální přístup umožňuje snazší operaci u obézních pacientů [18]. V našem souboru bylo vylučovacím kritériem BMI vyšší než 35 kg/m2, nicméně jsme měli 24 % pacientů s BMI vyšším než 30 kg/m2. Aktuálně nepovažujeme BMI vyšší než 35 kg/m2 za kontraindikaci retroperitoneoskopického přístupu. Jednou z hlavních překážek rozvoje retroperitoneoskopické adrenalektomie byla obtížná orientace v retroperitoneu. Orientace v retroperitoneu dorzálním přístupem vyžaduje určitou zkušenost, protože zde chybějí rutinní orientační body typické pro laparoskopický přístup, na který je chirurg z každodenní praxe zvyklý. Nicméně po překonání úvodních potíží s anatomickou orientací zjistíme, že tento přístup je jednodušší. Nejtěžší je identifikace nadledviny v tukové tkáni po vytvoření dostatečného prostoru v retroperitoneu. Praktickým důvodem horší orientace v retroperitoneu bylo dřívější použití retrokapnoperitonea nižšího než 15 mm Hg z důvodu obavy z hemodynamických konsekvencí. Tím bylo zabráněno vytvoření dostatečného přehledu v retroperitoneu. Giebler prokázal, že použití vyšších tlaků v retroperitoneu je bezpečné. Ačkoliv to bylo doprovázeno signifikantním zvýšením centrálního venózního tlaku o 37 %, zvýšení preloadu vedlo k vyšším plnicím tlakům. Srdeční frekvence, systémová vaskulární rezistence a pulmonární vaskulární rezistence neukázaly zásadní změny. Později Giebler potvrdil hypotézu, že intraperitoneální a retroperitoneální CO2 způsobují jiné kardiovaskulární změny díky rozdílu tlakového gradientu mezi vena cava inferior a superior v závislosti na kompartmentu [19]. Walz z Essenu používá tlaky 20–24 mm Hg k dostatečné expanzi retroperitonálního prostoru. Tyto tlaky rovněž umožňují prakticky bezkrevnou preparaci v retroperitoneu. V našem souboru standardně používáme tlak 18 mm Hg. Tento tlak považujeme za dostatečný k vytvoření dobrého přehledu v operačním poli. Vyšší tlaky používáme pouze u obézních pacientů. Výsledky 30denní morbidity jsou v souladu s ostatními autory minimální. Intraoperační komplikace poranění vena hepatica posterior vyplývá z anatomické variace vyústění vena suprarenalis do této vény asi u 20 % pacientů, jak uvádí Dr. Frillingová ze skupiny Dr. Walze, který má v současné době zkušenosti ze souboru asi 800 pacientů s dorzální retroperitoneoskopickou adrenalektomií [20]. Perioperační mortalita byla v našem souboru nulová. Operační čas u retroperitoneoskopické adrenalektomie má tendenci být kratší než transabdominální laparoskopický přístup. Např. Karabulut z Clevelandu uvádí čas 159 minut ve srovnání s našimi 61 minutami. Operační časy německých studií nebo z pracovišť používajících stejnou techniku jako v Essenu jsou podstatně kratší. Operační časy vybraných studií jsou uvedeny v Tab. 4. Stejný autor právě tak jako řada jiných autorů uvádí možnost robotické laparoskopické adrenalektomie, kterou však nepovažujeme za přínosnou [21]. Samozřejmá je možnost použití jednoho přístupu, kterou v současnosti rovněž zavádíme [22]. Kosmetický přínos single-access u dorzální retroperitoneoskopie však považujeme za minimální. Indikace k adrenalektomii je otázkou multidisciplinárního týmu. Indikace u hormonálně aktivních či neaktivních benigních lézí a u metastáz jsou prakticky jednoznačné. Sporná je pouze indikace vycházející z velikosti léze. Musíme přihlédnout k faktu, že čím je tumor menší, tím je podhodnocení velikosti při CT zobrazení signifikantnější. 30–40 % tumorů menších než 3–5 cm je podhodnoceno oproti reálné velikosti preparátu. Je to dáno vejčitým tvarem a orientací tumoru. Právě tak bývá podhodnocen objem tumoru. Při hodnocení objemu tumoru vycházejícího ze vzorce: π/6 (X*Y*Z) je třeba si uvědomit, že 25 % zvětšení průměru představuje zdvojnásobení objemu tumoru (univerzitní přednáška Quan Yang, 2010, Los Angeles). Tento fakt se nám potvrdil při operačních indikacích u hormonálně neaktivních incidentalomů, kdy velikost preparátu měla tendenci být větší než rozměr v CT zobrazení. Incidentalomy větší než 6 cm indikujeme k operaci. Tumory menší než 4 cm mají být v odstupu 6 měsíců kontrolovány. U incidentalomů velikosti 4–6 cm se vyhodnotí CT a ev. MRT známky malignity. Bereme v úvahu rovněž pacientovo přání. Při 4 cm velikosti tumoru je 2% pravděpodobnost, že se jedná o malignitu, a při 6 cm velikosti tumoru stoupá pravděpodobnost, že se jedná o malignitu, již na 25 % [23, 24]. V současnosti zvažujeme k operaci na základě výše uvedeného již incidentalomy velikosti 3–5 cm. Další indikace k operaci u incidentalomů v závislosti na hormonální aktivitě jsou v souladu s doporučeními Německé endokrinologické společnosti. Debata kolem možností miniinvazivního přístupu adrenalektomie u adrenokortikálního karcinomu probíhá. Stávající guideliny ji nedoporučují. Již však od prvního sympozia zabývajícího se karcinomem nadledviny v Ann Arboru (International Adrenal Cancer Symposium) v roce 2003 proběhlo několik studií zabývajících se možností miniinvazivního přístupu u adrenokortikálního karcinomu. Řada kontroverzních otázek byla zmíněna rovněž během tohoto třetího sympozia ve Würzburgu v roce 2011. Indikace zvolené operační techniky se řídí zkušenostmi daného pracoviště. Dorzální retroperitoneoskopická adrenalektomie je nespornou výhodou u oboustranných operací a u pacientů s předchozí intraabdominální operací. Na rozdíl od dřívějších limitací je možné ji aplikovat u obézních pacientů. Obecnou limitaci miniinvazivního přístupu představují extrémně velké léze.
Tab. 4. Operační časy ve vybraných studiích (chronologicky) Tab. 4: Operative times in selected studies (in a chronological order) 
Závěr
V našem operačním portfoliu disponujeme vedle otevřené adrenalektomie jak laparoskopickou, tak retroperitoneoskopickou adrenalektomií. V současné době preferujeme v případě možnosti miniinvazivního přístupu jednoznačné dorzální retroperitoneoskopickou adrenalektomii a považujeme ji za metodu volby. Tato operace je bezpečná, efektivní a má dobré výsledky včetně extrémně rychlé rekonvalescence.
Doc. MUDr. Pavel Zonča, PhD. FRCS
Siegfried-Leopold Str. 51
532 25 Bonn
e-mail: pavel.zonca@hotmail.co.uk
Zdroje
1. Snow LL. Endoscopic general surgery: an uptodate, Laser Highlights 1991;2 : 1–3.
2. Gagner M, Lacroix A, Bolte E. Laparoscopic adrenalectomy in Cushingęs syndrome and pheochromocytom. N Engl J Med 1992;327 : 1033.
3. Gagner M, Lacroix A, Prinz RA, Bolte E, Albala D, Polvin C. Early experience with laparoscopic approach for adrenalectomy. Surgery 1993;114 : 1120–1125.
4. Kasalický M, Krsek M, Zelinka T, Hána V, Widimský J. 120 laparoscopic adrenalectomies with a harmonic scalpel. Rozhl Chir 2009;88 : 439–443.
5. Stránský P, Hora M, Eret V, Klecka J, Urge T, Grégrová H, Dvoráková E, Hes O, Chudácek Z, Kreuzberg B. Laparoscopic adrenalectomy. Rozhl Chir 2009;88 : 514–520.
6. Safarík L, Vraný M, Widimský J, Dvorácek J, Novák K, Dusková J. Laparoscopic transperitoneal adrenalectomy in hormonally-active adrenal tumors. Rozhl Chir 2002;81(3):127–132.
7. Mandressi A, Buizza C, Antonelli D, Chisena S, Servadio G. Retroperitoneoscopy. Ann Urol (Paris) 1995;29 : 91–96.
8. Mercan S, Seven R, Ozarmagan S. Endoscopic retroperitoneal adrenalectomy. Surgery 1995;118 : 1071–1075.
9. Walz MK, Peitgen K, Krause U, Eigler FW. Die dorsale Adrenalektomie – eine operative Technik, Zentralbl Chir 1995 : 53–58.
10. Walz MK, Peitgen K, Walz MV, Hoermann R, Saller B, Gibler RM, Jockenhövel F, Philipp T, Broelsch CE, Eigler FW, Mann K. Posterior retroperitoneoscopic adrenalectomy: lessons learned within five years. World J Surg 2001;25 : 728–734.
11. Perrier ND, Kennamer DL, Bao R, Jimenez C, Grubbs EG, Lee JE, Evans DB. Posterior retroperitoneoscopic adrenalectomy: preferred technique for removal of benign tumors and isolated metastases. Ann Surg 2008;248 : 666–674.
12. Thomson GB, Grant CS. Van Heerden JA, Schlinkert RT, Young WF, Farley DR, Ilstrup DM. Laparoscopic versus open posterior adrenalectomy: a case-control study of 100 patients. Surgery 1997;122 : 1132–1136.
13. Imai T, Kikumori T, Ohiwa M, Mase T, Funahashi H. A case-controlled study of laparoscopic compared with open lateral adrenalectomy. M J Surg 1999;178 : 50–53.
14. Smith CD, Weber CJ, Amerson JR. Laparoscopic adrenlectomy: new gold standard. World J Surg 1999;23 : 389–396.
15. Takeda M, Go H, Watanabe R, Kurumada S, Obara K, Takahashi E, Komeyama T, Imai T, Takahashi K. Retroperitoneal laparoscopic adrenalectomy for functioning adrenal tumors: comparison with conventional transperitoneal laparoscopic adrenalectomy. J Urol 1997;157 : 19–23.
16. Naya Y, Nagata M, Ichikawa T, Amakasu M, Omura M, Nishikawa T, Yamaguchi K, Ito H. Laparoscopic adrenalectomy: comparison of transperitoneal and retroperitoneal approaches. BJU Int 2002;90 : 199–204.
17. Dickson PV, Jimenez C, Chisholm GB, Kennamer DL, Ng C, Grubbs EG, Evans DB, Lee JE, Perrier ND. Posterior retroperitoneoscopic adrenalectomy: a contemporary American experience. J Am Coll Surg 2011;212(4):659–65, discussion 665–7.
18. Agha A, von Breitenbuch P, Gahli N, Piso P, Schlitt HJ. Retroperitoneoscopic Adrenalectomy: Lateral versus dorsal Approach, JSO 2008;97 : 90–93.
19. Giebler RM, Walz MK, Peitgen K, Scherer RU. Hemodynamic changes after retroperitoneal CO2 insufflation for posterior retroperitoneoscopic adrenalectomy. Anest Analg 1996;82 : 827–831.
20. Walz MK, Alesina PF, Wenger FA, Deligiannis A, Szuczik E, Petersenn S, Ommer A, Groeben H, Peitgen K, Janssen OE, Philipp T, Neumann HP, Schmid KW, Mann K. Posterior retroperitoneoscopic adrenalectomy-results of 560 procedures in 520 patients. Surgery 2006;140(6):943–8;discussion 948–50.
21. Karabulut K, Agcaoglu O, Aliyev S, Siperstein A, Berber E. Comparison of intraoperative time use and perioperative outcomes for robotic versus laparoscopic adrenalectomy. Surgery 2011 Dec 3. [Epub ahead of print].
22. Walz MK, Groeben H, Alesina PF. Single-access retroperitoneoscopic adrenalectomy (SARA) versus conventional retroperitoneoscopic adrenalectomy (CORA): a case-control study. World J Surg 2010;34(6):1386–90.
23. Sturgeon C, Kebebew E. Laparoscopic adrenalectomy for malignancy. Surg Clin North Am 2004;84(3):755–774.
24. Kebebew E, et al. Results of laparoscopic adrenalectomy for suspected and unsuspected malignit adrenal neoplasms. Arch Surg 2002;137(8):948–951;discussion 952–953.
25. Lezoche E, Guerrieri M, Crosta F, et al. Perioperative results of 214laparoscopic adrenalectomies by anterior transperitoneal approach.Surg Endosc 2008;22 : 522–526.
26. Henry JF, Defechereux T, Raffaelli M, et al. Complications of laparoscopic adrenalectomy: results of 169consecutive procedures. World J Surg 2000;24 : 1342–1346.
27. Zhang X, Fu B, Lang B, et al. Technique of anatomical retroperitoneoscopic adrenalectomy with report of 800cases. J Urol 2007;177 : 1254–1257.
Štítky
Chirurgia všeobecná Ortopédia Urgentná medicína
Článok vyšiel v časopiseRozhledy v chirurgii
Najčítanejšie tento týždeň
2012 Číslo 4- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
-
Všetky články tohto čísla
- Budoucnost úrazové chirurgie u nás
- GIST: Novodobé poznatky a léčebné modality
- Kvalita života je důležitým faktorem indikační rozvahy u nemocných s pokročilým karcinomem pankreatu – multicentrická prospektivní studie
- Biomarkery detekce minimální systémové diseminace u nemocných s karcinomem plic
- Prevence parastomální hernie primoimplantací síťky laparoskopicky – první zkušenosti
- Klinické prognostické faktory kolorektálního karcinomu po jeho radikální léčbě
- Laparoskopická adrenalektomie – indikace a selekční kritéria
- Retroperitoneoskopická adrenalektomie dorzálním přístupem
- Překlad knihy Schein´s Common Sense Emergency Abdominal Surgery – Urgentní břišní chirurgie
- Extragastrointestinální stromální tumor (EGIST)
- McKittrick-Wheelockov syndróm: Komplikácia mucinózneho adenómu rekta
- Gastrointestinal Cancers Symposium
- XXI. Jarní setkání Loket – pokroky v léčbě nemocných s karcinomem pankreatu
- Rozhledy v chirurgii
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- GIST: Novodobé poznatky a léčebné modality
- Laparoskopická adrenalektomie – indikace a selekční kritéria
- Prevence parastomální hernie primoimplantací síťky laparoskopicky – první zkušenosti
- Extragastrointestinální stromální tumor (EGIST)
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



