-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Endoskopická léčba motilitních onemocnění trávicího traktu
Endoscopic management of gastrointestinal motility disorders
Gastrointestinal motility disorders include several heterogeneous units affecting the esophagus, stomach, small or large intestine and the rectum. These are namely Zenker’s diverticulum, esophageal achalasia, gastroesophageal reflux disease, gastroparesis, constipation, Ogilvie’s syndrome and post-fundoplication dysphagia. Given the progressive development of endoscopic techniques, patients with most of the above mentioned diseases can be offered a solution consisting of a mini-invasive endoscopic procedure which has already become a first-choice treatment for some of the disorders. This article summarizes the current role of endoscopy in the treatment of the most important gastrointestinal motility disorders.
Keywords:
achalasia – Gastrointestinal motility disorders – endoscopic treatment – gastroparesis – Zenker´s diverticulum
Autori: J. Martínek 1; K. Hugová 1; D. Lovecká 2; R. Husťak 2
Pôsobisko autorov: Klinika hepatogastroenterologie, Institut klinické a experimentální medicíny, Praha 1; Interná klinika, Fakultná nemocnica Trnava 2
Vyšlo v časopise: Rozhl. Chir., 2022, roč. 101, č. 1, s. 4-13.
Kategória: Souhrnné sdělení
doi: https://doi.org/10.33699/PIS.2022.101.1.4–13Súhrn
Mezi motilitní onemocnění gastrointestinálního traktu (GIT) řadíme několik různorodých jednotek postihujících jícen, žaludek, tenké nebo tlusté střevo a konečník. Jde o Zenkerův divertikl, achalázii jícnu, refluxní chorobu jícnu, gastroparézu, zácpu, Ogilvieho syndrom a postfundoplikační dysfagii. Díky progresivnímu rozvoji endoskopických technik lze u většiny z nich nabídnout pacientům řešení v podobě miniinvazivního endoskopického zákroku, který u některých onemocnění již představuje léčebnou metodu první volby. Následující článek shrnuje současné postavení endoskopie v léčbě nejvýznamnějších motilitních poruch gastrointestinálního traktu.
Klíčová slova:
Zenkerův divertikl – endoskopická léčba – achalázie – motilitní poruchy gastrointestinálního traktu – gastroparéza
ÚVOD
Mezi tzv. motilitní onemocnění gastrointestinálního traktu (GIT), kde endoskopie nabízí účinné metody léčby, řadíme Zenkerův divertikl, achalázii jícnu, refluxní chorobu jícnu, gastroparézu, refrakterní zácpu, Ogilvieho syndrom a postfundoplikační dysfagii (Tab. 1). Výhodou endoskopických metod je jejich miniinvazivita, přesto se v mnohých případech jedná o metody, které již svým charakterem představují spíše metody chirurgické, přičemž u mnohých zákroků se uplatňuje nový a revoluční princip submukózní endoskopie. Při submukózní endoskopii se s endoskopem pracuje ve stěně dutého orgánu. Účinnost těchto metod je často srovnatelná s klasickými chirurgickými postupy. V následujícím souhrnném sdělení popíšeme možnosti endoskopické léčby u každé z výše zmíněných jednotek.
Tab. 1. Přehled motilitních onemocnění GIT a možnosti endoskopické a chirurgické léčby
Tab. 1: Overview of gastrointestinal motility disorders and possibilities of endoscopic and surgical treatment
Vysvětlivky: POEM − perorální endoskopická myotomie, G-POEM − gastrická perorální endoskopická pyloromyotomie, Z-POEM − perorální endoskopická myotomie Zenkerova divertiklu, ODS − obstrukční defekační syndrom, ARMS − antirefluxní endoskopická resekce, TIF − transoral incisionless fundoplication, MUSE − medigus ultrasonic surgical endostapler, DJS − dolní svěrač jícnu; *metoda ve stadiu ověřování, **metody bez jednoznačně prokázané účinnosti, viz text.
Legend: POEM – peroral endoscopic myotomy; G-POEM − gastric peroral endoscopic pyloromyotomy; Z-POEM – peroral endoscopic myotomy for Zenker’s diverticulum; ODS – obstructed defecation syndrome; ARMS – antireflux mucosectomy; TIF – transoral incisionless fundoplication; MUSE − medigus ultrasonic surgical endostapler; DJS – lower esophageal sphincter; *method in the stage of evaluation; **methods without clearly demonstrated efficacy, see the text.1. Zenkerův divertikl
Zenkerův divertikl je pulzním nepravým divertiklem (neobsahuje m. propria) tvořícím se na zadní stěně jícnu v místě oslabené stěny zvaném Kiliánův trojúhelník nad m. cricopharyngeus. Jde o nepříliš časté onemocnění s celkovou prevalencí 0,01−0,11 % a nejčastěji se vyskytuje u osob starších 70 let [1]. Klinicky se manifestuje dysfagií a regurgitací. Diagnostikuje se endoskopicky (v případě neopatrného zavádění endoskopu lze takový divertikl perforovat) a zejména radiologicky, jeho velikost je různá a kolísá od několika milimetrů až po několik centimetrů. Při endoskopii je patrná dutina divertiklu, septum tvořené m. cricopharyngeus a lumen jícnu (Obr. 1). V současnosti existují tři možné způsoby léčby Zenkerova divertiklu:
Obr. 1. Zenkerův divertikl – endoskopický obraz
Fig. 1: Zenker´s diverticulum – endoscopic view
a. metody flexibilní endoskopie (septotomie, Z-POEM),
b. metody s použitím rigidního endoskopu (CO2 laser, přetětí zadní stěny staplerem),
c. klasická otevřená chirurgie (transcervikální divertikulektomie, divertikulopexe s myotomií m. cricopharyngeus nebo inverze divertiklu s myotomií).
Cílem léčby je zmenšit velikost či odstranit divertikl a ulehčit postup sousta do jícnu. V současnosti jsou metody flexibilní endoskopie považovány za léčbu první volby díky jejich vysoké účinnosti, miniinvazivitě a bezpečnosti [2].
Princip tradiční endoskopické léčby spočívá v myotomii m. cricopharyngeus, který tvoří septum divertiklu (Obr. 2). Existuje několik modifikací endoskopické septotomie, nejčastěji se provádí endoskopickým nožem, dříve se prováděla argon-plasma koagulací. Myotomie má být co nejúplnější, tj. téměř ke spodině divertiklu, a většina endoskopistů místo septotomie na konci výkonu jistí klipem. Někteří endoskopisté používají divertikuloskop, který vylepší přehlednost, jiní endoskopisté (včetně autorů) používají pouze plastový nástavec na endoskopu. Divertikuloskop (zvláštní typ overtubu) není totiž jednoduché správně nasadit zvláště u menších divertiklů a jeho nasazení může být komplikováno perforací divertiklu. Někteří endoskopisté provádějí dvojitou myotomii (dva řezy) s následnou resekcí septa mezi oběma řezy, septotomie je tak širší.
Obr. 2. Zenkerův divertikl – septotomie
Fig. 2: Zenker´s diverticulum – septotomy
Novou endoskopickou metodou je Z-POEM, kdy se na rozdíl od tradiční septotomie zachovává nad svalem intaktní sliznice. Tato metoda vychází z principu submukózní endoskopie a perorální endoskopické myotomie (POEM – viz dále). Po naříznutí sliznice se tímto otvorem vytvoří dva submukózní tunely – jeden na straně divertiklu, druhý na straně jícnu –, a posléze je provedena kompletní myotomie (Obr. 3). Výhodou tohoto dnes velmi populárního přístupu je možnost kompletní myotomie, což u tradičního přístupu není vždy možné z důvodu bezpečnosti (perforace). Díky tomu lze předpokládat nižší procento recidiv. Další eventuální výhodou Z-POEM je možnost řešení divertiklů menších než 2 cm, které jsou klasickou septotomií obtížně řešitelné. Prospektivní srovnání Z-POEM s tradiční septotomií právě probíhá v randomizované studii.
Obr. 3. Zenkerův divertikl – Z-POEM
A) slizniční incize B) submukózní tunelizace C) myotomie, D) uzávěr sliznice klipy
Fig. 3: Zenker´s diverticulum – Z-POEM
A) mucosal incision, B) submucosal tunneling, C) myotomy, D) mucosal closure with clips
K dispozici nejsou žádné prospektivní studie srovnávající chirurgické a endoskopické přístupy, navíc většina starších publikací srovnávajících retrospektivně endoskopické a chirurgické přístupy se věnovala technikám rigidní, ne flexibilní endoskopie [3]. Velmi kvalitní metaanalýza hodnotí výsledky endoskopické septotomie u 813 pacientů je její účinnost 91 % s výskytem komplikací 11 % a s rekurencí u 11 % pacientů [4].
Flexibilní přístup je upřednostňován nejenom díky výtečným výsledkům a skvělému bezpečnostnímu profilu, ale i díky častým problémům starších pacientů s pohyblivostí krční páteře, což mnohdy neumožňuje bezpečné provedení metody na bázi rigidní endoskopie [2]. Endoskopickou septotomii lze v případě rekurence s úspěchem opakovat.
Endoskopická léčba Zenkerova divertiklu by měla být soustředěna do center zabývajících se terapeutickou endoskopií. Dostupnost tradiční flexibilní septotomie je široká, výkon v ČR provádí řada endoskopických center, Z-POEM se u nás provádí pouze na endoskopických pracovištích v IKEM a ve Fakultní nemocnici v Hradci Králové. Oba typy výkonů se provádějí většinou v celkové anestezii, rutinní podání antibiotik není nutné. Pacienti jsou většinou propuštěni do domácího ošetřování druhý den po výkonu.
2. Achalázie jícnu
Achalázie jícnu je onemocněním ne zcela jasné etiologie, jejíž kauzální léčba není k dispozici a všechny způsoby léčby cílí na uvolnění obvykle zvýšeného tonu dolního svěrače jícnu (DJS). Endoskopie nabízí tři metody léčby tohoto onemocnění:
a) intrasfinkterickou injekci botulotoxinu,
b) tradiční pneumatickou dilataci,
c) perorální endoskopickou myotomii – POEM – tato nejnovější metoda je v současnosti řazena mezi standardní metody léčby achalázie.
Každý pacient s achalázií má tedy na výběr z několika různých metod léčby zahrnujících i laparoskopickou myotomii a lékaři by měli každého pacienta s achalázií podrobně informovat o všech dostupných metodách (Tab. 2). Informovaný pacient by si pak měl za pomoci lékaře vybrat metodu, která mu nejvíce vyhovuje, a tato léčba by samozřejmě měla respektovat i manometrický typ onemocnění (I–III), celkový stav pacienta včetně komorbidit a další faktory.
Tab. 2. Metody léčby achalázie a jejich výhody a nevýhody
Tab. 2: Achalasia treatment methods, their advantages and disadvantages
a) injekce botulotoxinu
Jedná se o jednoduchou metodu, kdy se během endoskopie injektorem aplikuje 100 IU botulotoxinu (Botox) do oblasti DJS. Injekce vede ke krátkodobému zlepšení příznaku u většiny nemocných, efekt je však krátkodobý (měsíce) a většina pacientů vyžaduje opakování injekce nebo jinou léčbu [5]. Další nevýhodou je vznik fibrózy v oblasti DJS, která může ztížit ev. laparoskopickou nebo endoskopickou myotomii. Tato léčba by měla být rezervována jen pro pacienty, kteří si jinou léčbu nepřejí nebo nejsou vhodnými kandidáty jiné léčby. Aplikuje se 100 jednotek do oblasti DJS, není doporučeno aplikovat botulotoxin do oblasti těla jícnu – to je možné u vybraných pacientů s onemocněními typu hyperkontraktilního jícnu nebo distálního jícnového spazmu, kde se mimo DJS botulotoxin aplikuje i do oblasti distálního jícnu.
Injekce botulotoxinu je vcelku bezpečná, měli bychom se vyvarovat hlubokého vpichu, neboť byly popsány případy fatální mediastinitidy [6].
b) pneumatická dilatace
Jedná se o tradiční metodu, dříve prováděnou spíše radiology, v současnosti se provádí dilatace pod endoskopickou a/nebo radiologickou kontrolou balony velikosti 30−35−40 mm. Evropská společnost pro gastrointestinální endoskopii doporučuje jako standardní provedení dvou dilatací, nejprve balonem 30 mm následovanou za 2−4 týdny druhou etapou dilatace balonem velikosti 35 mm a v případě neúplné účinnosti lze ještě provést třetí dilataci balonem 40 mm velkým [7]. Není doporučeno provádět jen jednu etapu dilatace (malá účinnost) ani začít balonem větším, tj. 35 mm (větší riziko perforace). Takto provedená dilatace je stejně účinná jako laparoskopická Hellerova myotomie (LHM) s tím, že až třetina pacientů vyžaduje opakování dilatací. Rizikem výkonu je perforace (1−3 %), jejíž řešení může být jak endoskopické, tak chirurgické. Pneumatická dilatace není vhodnou metodou u pacientů s achalázií typu III.
c) POEM
Jedná se o endoskopické provedení myotomie s využitím submukózního tunelu, jedinou „jizvou“ po výkonu je malá slizniční incize, kterou se endoskop dostává do submukózy a která je na konci výkonu uzavřena nejčastěji klipy (Obr. 4). POEM byla uznána jako standardní léčba achalázie jícnu v ČR již v r. 2016 a tento výkon v současnosti provádějí dvě česká endoskopická centra (IKEM a Hradec Králové). Výhodou POEM, která má srovnatelnou účinnost s LHM (léčebný úspěch nad 90 % po 3 měsících a cca 80 % po 2 letech), je její miniinvazivita a menší mortalita oproti LHM (0,4 % vs. 0,04 %) [8,9]. Nevýhodou je vyšší frekvence léčbu vyžadujícího gastroezofageálního refluxu. Po LHM (s parciální fundoplikací) je 2 roky po zákroku léčeno inhibitory žaludeční sekrece 30 % pacientů, zatímco po POEM 50 % pacientů [10]. V České republice se POEM provádí od r. 2012 a v obou centrech bylo již provedeno více než 500 výkonů, centrum v IKEM publikovalo nejenom střednědobé výsledky [11], ale bylo i důležitou součástí (spolu s chirurgy III. chirurgické kliniky FN Motol) velké mezinárodní studie srovnávající POEM s LHM [10].
Obr. 4. POEM u pacienta s achalázií
A) slizniční incize, B) tvorba submukózního tunelu, C) vhled do submukózního tunelu, D) provedení myotomie, E) kompletní myotomie s viditelnou adventicií, F) kompletní uzávěr místa vstupu klipy
Fig. 4: POEM in a patient with achalasia
A) mucosal incision, B) submucosal tunneling, C) submucosal tunnel view, D) myotomy, E) complete myotomy with visible adventitia, F) complete mucosal closure with clips
3. Refluxní choroba jícnu (RCHJ)
Refluxní choroba jícnu je častým onemocněním postihujícím 10−25 % evropské populace. Tíže onemocnění zahrnuje celé spektrum fenotypů počínaje RCHJ bez ezofagitidy a komplikovanými formami (těžká ezofagitida, Barrettův jícen, adenokarcinom jícnu) konče. Mezi dvě nejvíce využívané, účinné a bezpečné léčebné metody patří laparoskopická fundoplikace a většinou dlouhotrvající podávání inhibitorů protonové pumpy. Laparoskopická operace je však pro některé pacienty příliš invazivní a je též zatížena určitým rizikem komplikací, jako je např. postfundoplikační dysfagie [12], stejně tak je dlouhodobá léčba inhibitory žaludeční sekrece dnes mnohými (ne zcela správně) považována za rizikovou v důsledku nežádoucích účinků této léčby.
I proto se zkoumá celá řada dalších více či méně účinných alternativ, které lze pacientovi s RCHJ nabídnout. Jedná se o metody chirurgické (laparoskopická implantace magnetického náramku − LINX; elektrostimulace DJS), fyzioterapeutické (nácvik diafragmatického dýchání a další fyzioterapeutické postupy), farmakoterapeutické (prokinetika a jiné léky) a samozřejmě i endoskopické. Je pravdou, že v ČR se mnohé z těchto metod nepoužívají či jen velmi málo a je spíše filozofickou otázkou, zda je to dobře, nebo ne. Většina z alternativních chirurgických nebo endoskopických metod však nepatří mezi metody standardní se zaručenou účinností a prokázanou bezpečností, český pacient proto o mnoho nepřichází při prozatímní nedostupnosti těchto metod.
Mezi endoskopické metody léčby RCHJ řadíme:
a) transorální fundpolikaci (= transoral incisionless fundoplication – TIF; antirefluxní bariéra se tvoří se pomocí speciálního endoskopického suturního systému).
b) endoskopickou „fundoplikaci“ s použitím endostapleru s ultrazvukovou kontrolou (= medigus ultrasonic surgical endostapler – MUSE; systém integruje flexibilní endoskopii s ultrazvukovým detektorem a chirurgickým staplerem, antirefluxní bariéra se tvoří pod ultrazvukovou a endoskopickou kontrolou).
c) aplikaci radiofrekvenční energie do oblasti DJS (Stretta) – metoda je nově dostupná v ČR na pracovištích v Ústřední vojenské nemocnici a FN Plzeň, není však hrazena z veřejného pojištění.
d) antirefluxní endoskopickou resekci (= antireflux mucosectomy – ARMS; provede se cirkumferenční piecemeal endoskopická resekce sliznice kardie a díky jizvení se vytvoří antirefluxní bariéra).
Podle ESGE není žádná z výše uvedených metod prokazatelně účinná a bezpečná a tyto metody se mají provádět jen u vybraných pacientů (např. alergie na léky, bez preference tradičního chirurgického řešení aj.) nejlépe v rámci klinických studií [2]. Randomizované studie prokázaly horší výsledky TIF vs. tradiční fundoplikace a u žádné metody nejsou k dispozici dlouhodobé výsledky [13].
Jedinou výjimku představuje metoda Stretta, která je dostupná již řadu let, i když přesný mechanismus účinku není zcela objasněn a její vliv na snížení patologického refluxu je doposud sporný. K metodě lze indikovat vybrané pacienty s RCHJ bez ezofagitidy a bez (velké) hiatové hernie, cílem léčby je zejména dlouhodobá symptomatická úleva. Vhodnými kandidáti jsou např. pacienti, kteří nechtějí dlouhodobě brát inhibitory sekrece a nesouhlasí s provedením tradiční fundoplikace [14].
4. Gastroparéza
Gastroparéza je definována jako syndrom s patologicky zpomalenou evakuací žaludku při absenci organické obstrukce. Nejčastějšími příznaky jsou nauzea, zvracení a nepříjemný, někdy až nesnesitelný pocit plnosti po jídle, což u mnohých pacientů znemožňuje normální příjem stravy. Gastroparéza může být velmi těžkým onemocněním zvyšujícím riziko předčasného úmrtí. Nejčastějšími příčinami jsou diabetes, zvláště 1. typu, operace v oblasti jícnu a žaludku a u třetiny pacientů se jedná o idiopatické onemocnění [15]. Patofyziologie, na rozdíl např. od achalázie, je komplexní a zahrnuje hypomotilitu žaludku nejenom v důsledku poruchy inervace občas atrofické hladké svaloviny žaludku i poruchy na úrovni žaludečního pacemakeru (Cajalovy buňky). Dalším pro endoskopii důležitým faktorem je pylorospasmus, byť v současnosti nevíme, jakou roli pylorospasmus má, u kolika procent pacientů s gastroparézou je přítomný, jak mnoho (či málo) se podílí na příznacích, a též nevíme, jak jej diagnostikovat. Nicméně je známo, že u části pacientů uvolnění pylorospasmu pomáhá.
Diagnostika gastroparézy spočívá v měření evakuace žaludku (scintigrafie nebo dechový test), avšak tyto metody nám nic neříkají o funkci pyloru. Endoskopické vyšetření je v posouzení pylorospasmu zcela neužitečné, neboť jde o hodnocení subjektivní. Dnes již existuje možnost vyšetření pomocí impedanční planimetrie (EndoFLIP, v ČR dostupné jen v IKEM, Obr. 5), které má potenciál pylorospasmus diagnostikovat, avšak vyšetření není standardizované a nejsou známy ani normální hodnoty pylorického tonu u zdravých lidí.
Obr. 5. Měření distenzibility pyloru – EndoFLIP
Fig. 5: Measurement of pyloric distensibility – EndoFLIP
Všechny tyto důvody vysvětlují, proč (např. na rozdíl od achalázie) všechny léčebné metody vedoucí k uvolnění předpokládaného pylorospasmu nejsou považovány za standardní, a tudíž zavedené a většina z nich stále patří do spektra metod ve stadiu klinického výzkumu.
Chirurgické metody léčby gastroparézy zahrnují jednak laparoskopickou pyloroplastiku (podle Heineke - -Mikulicze), jejíž účinnost není prokázaná a může být podobná jako u endoskopické pyloromyotomie (G-POEM), dále pak elektrostimulaci žaludku, jejíž účinnost je též nejednoznačná.
Endoskopické nebo chirurgické metody jsou indikovány až v případě selhání dalších léčebných postupů (dietní opatření, prokinetika, psychologická podpora, nutriční podpora, kompenzace základního onemocnění atd.), tyto metody tudíž nabízíme pacientům trpícím refrakterní gastroparézou.
Všechny endoskopické metody jsou cílené na pylorus a zahrnují
a) injekci botulotoxinu do pylorického svalu,
b) balonovou dilataci pyloru,
c) zavedení metalického stentu do pyloru,
d) endoskopickou pyloromyotomii (G-POEM).
Injekce botulotoxinu není doporučovanou strategií, dvě randomizované studie prokázaly, že tato injekce je stejně účinná jako placebo [16,17]. Injekce botulotoxinu není proto ani doporučována jako screeningový test před eventuální pyloromyotomií [7]. V případě balonové dilatace se nejedná o rutinní a standardní metodu – chybějí jakákoliv prospektivní data s delší dobou sledování, dilataci (ať již hydraulickou s balony 2 cm, nebo pneumatickou s balonem 3 cm velkým) lze zvážit u vybraných pacientů zvláště s postchirurgickou gastroparézou [7]. Není ani známo, zda je výhodnější provádět hydraulickou, nebo pneumatickou dilataci a jaká je ideální velikost balonů [7]. Zavedení stentu skrze pylorus není doporučenou metodou léčby gastroparézy (riziko migrace, přechodný efekt, nezbytnost odstranění stentu, absence relevantních vědeckých dat) [7].
Nejnadějnější z endoskopických metod je endoskopická pyloromyotomie (G-POEM, Obr. 6). Prvně byla provedena v r. 2015, v ČR byla prvně provedena v r. 2017 (jednalo se o sedmnáctý výkon tohoto typu na světě), na pracovišti IKEM byly úspěšně provedeny v rámci jednoho zákroku POEM a G-POEM u pacientky trpící souběžnou achalázií i závažnou gastroparézou [18].
Obr. 6. G-POEM
A) ústí pylorického kanálu s pylorospasmem, B) transverzální mukozotomie, C) submukózní tunelizace, D) identifikace pylorického svěrače, E-F) pyloromyotomie G) uzávěr mukozotomie suturním systémem (OverStitch), H) kompletní uzávěr mukozotomie
Fig. 6: G-POEM
A) pyloric orifice with pylorospasm, B) transverse mucosotomy, C) submucosal tunneling, D) identification of the pyloric sphincter, E-F) pyloromyotomy, G) mucosotomy closure with a suturing system (OverStitch), H) complete mucosotomy closure with anchoring
V současné době jsou známy výsledky několika retrospektivních i prospektivních studií se spíše kratším follow-up. Úspěch léčby (který ne vždy koreluje se zlepšením vyprazdňování žaludku) se pohybuje od 56 % do 75 %. Dlouhodobé výsledky jsou známy jen částečně a nepřesahují 12 měsíců, přičemž některá data ukazují, že rekurence po úspěšné léčbě přicházejí ve frekvenci 12 %/rok, jiná data ukazují, že po úvodním zlepšení jsou rekurence méně časté [19,20,21].
Problémem je absence kontrolované studie (s jinou léčbou nebo „sham-placebem“), neboť u gastroparézy více než kde jinde lze předpokládat významnou placebo odpověď v důsledku nezanedbatelného vlivu psychologických faktorů. Taková studie právě skončila v IKEM a její výsledky budou publikovány v roce 2022 (Clin. Trials. Gov. Id. NCT03356067).
G-POEM je tedy nezbytné považovat za metodu ve stadiu vyšetřování, která by se zatím měla provádět pouze v rámci klinických studií. V ČR ji nabízí endoskopické centrum v pražském IKEM.
5. Refrakterní zácpa
Zácpa je příznakem, který může být způsoben základním onemocněním (tzv. sekundární zácpa), nebo je způsobena funkčními nebo anatomickými abnormalitami v oblasti konečníku (obstrukční defekační syndrom nebo dyssynergie pánevního dna) nebo patologickou hypomotilitou tračníku (syndrom líného střeva).
Léčba zácpy je komplexní a zahrnuje mimo jiné dietní opatření (vláknina), režimová opatření (dostatek tekutin, fyzická námaha), farmakoterapii (prokinetika, laxativa), fyzioterapii (biofeedback, fyziologická poloha při defekaci). Pokud tato opatření nejsou účinná, je namístě zvážení chirurgických alternativ (např. korekce abnormalit typu rektokély či intususcepce aj. při obstrukčním defekačním syndromu nebo kolektomie – nejlépe subtotální – v případě refrakterního syndromu líného střeva).
Možným způsobem ovlivnění refrakterní zácpy je cékostomie, kterou lze zavést čistě endoskopicky (nabízí se srovnání s perkutánní endoskopickou gastrostomií) nebo v kombinaci s laparoskopickým přístupem (tzv. LAPEC = laparoskopicky asistovaná endoskopická cékostomie). Na rozdíl od žaludku je implantace katétru do céka spojena s vyšším rizikem komplikací, zejména infekčních. Nejčastější indikací cékostomie je uvolnění částečné obstrukce tračníku a zejména možnost podávání antegrádních klyzmat, např. s polyethylenglykolem.
Endoskopická cékostomie (nebo LAPEC, Obr. 7) je indikována pouze v případě selhání jiných metod léčby včetně retrográdních klyzmat. Před výkonem je nutná střevní příprava (týden bezezbytková dieta, den dva před výkonem jen tekutiny, příprava 4 l, ev. více s polyethylenglykolem). Výkon samotný se provádí pod clonou antibiotik (před zákrokem a 3 dny po zákroku) a je vždy doporučena fixace céka na třech místech ke stěně břišní (endoskopicky pomocí speciálních T-kotviček nebo laparoskopicky) [2]. Tato fixace prevenuje únik střevního obsahu do peritoneální dutiny. Užívají se dva hlavní způsoby zavedení:
Obr. 7. LAPEC – schéma výkonu
Fig. 7: LAPEC – scheme of the procedure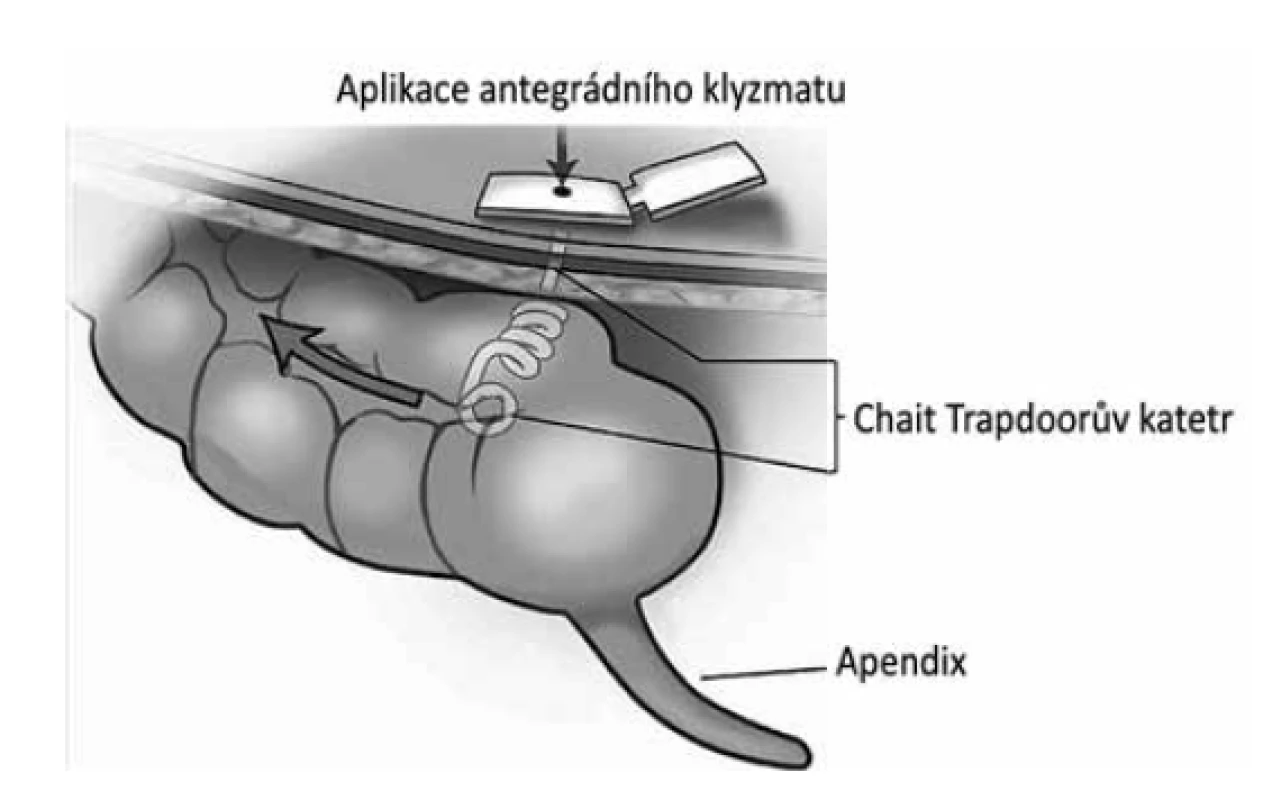
- Pull-through metoda (podobně jako žaludeční PEG), kdy se po fixaci céka zavádí Seldingerova jehla (12−18G), tou se zavede zavaděč, který se vytáhne navenek z rekta, přifixuje se cékostomický katétr (12G u dětí, 14&20G u dospělých) a zavaděč se vtáhne do střeva a vytáhne spolu s katétrem skrze kůži navenek, kde se zafixuje.
- Druhým způsobem je přímé zavedení Chait Trapdoorova katétru (= vypadá jako četné katétry typu pigtail, Obr. 8) do céka po jeho předchozí fixaci skrze kůži, jedná se o mnohými upřednostňovaný způsob, nedochází např. k tzv. burried bumper syndromu a katétry jsou lehce měnitelné.
Obr. 8. Chait Trapdoorův katétr používaný k endoskopické cékostomii nebo LAPEC
Fig. 8: Chait Trapdoor catheter used for endoscopic cecostomy or LAPEC
V případě laparoskopické asistence je možné laparoskopicky provést nejenom fixaci střeva, ale i zavedení cékostomického katétru.
Čistě endoskopický přístup je doporučen zejména u kriticky nemocných pacientů, zatímco LAPEC se doporučuje jako standardní přístup cékostomie u pacientů v jinak dobrém stavu [2]. Zdůraznit je vhodné, že byť katétr lze umístit i jinam než do céka (např. po hemikolektomii), nejedná se v takovém případě o standardní postup, neboť je technicky mnohem komplikovanější a rizikovější.
Jak dlouho ponecháváme cékostomický katétr? Jde o individuální rozhodnutí, katétry měníme podobně jako u žaludečního PEG v případě potřeby (jejich opotřebení, zn. infekce v okolí apod.) a katétry ponecháváme tak dlouho, jak je to možné, i v řádu let, pokud jsou samozřejmě účinné. U mnohých pacientů se jedná o poslední léčebnou možnost před „mutilujícím“ resekčním zákrokem.
6. Ogilvieho syndrom
Tento syndrom je charakterizován akutní pseudoobstrukcí tračníku, kdy je tračník patologicky dilatován bez přítomné organické obstrukce. Většinou se vyskytuje u pacientů v těžkém celkovém stavu s přítomnými komorbiditami. U všech pacientů s podezřením na tento syndrom je nejprve nutné provedení CT vyšetření, aby se vyloučila mechanická příčina obstrukce. Samozřejmostí je i stanovení základních biochemických a endokrinologických parametrů (ionty, renální funkce, hormony štítné žlázy), jejichž korekcí lze patologickou hypomotilitu tračníku upravit.
Léčba Ogilvieho syndromu spočívá v úpravě vnitřního prostředí, léčbě základního onemocnění (např. infekce), přerušení léčby s opioidy, anticholinergiky a jinými predisponujícími léky, parenterální výživě, časté změně polohy pacienta a zavedení rektální rourky. Pokud tato opatření nepřinesou efekt, je namístě zvážit buď endoskopickou dekompresi, nebo i.v. podání neostigminu. Účinnost endoskopické dekomprese se pohybuje mezi 36−88 % a podle některých studií je účinnější než podání neostigminu [22,23].
Promptní endoskopická dekomprese střeva je indikována v případě dilatace céka nad 12 cm, pokud syndrom trvá více než 4−6 dní. V případě rekurence (až 40 %) je opakování endoskopické dekomprese též účinné [2].
K provedení střevní dekomprese (zavedení koloskopu a odsání obsahu) patří další doporučení – jednak se před dekompresí neprovádí střevní příprava (riziko zhoršení stavu), po úspěšné dekompresi je vhodné zavést dekompresní kanylu do c. transversum (a ponechat ji několik dní, lze přišít např. ke kůži v oblasti hýžďového svalu). Po úspěšné dekompresi je vhodné podat 1−3 l roztoku polyethylenglykolu (per os nebo sondou), což prokazatelně snižuje riziko rekurence [24]. V případě refrakterního syndromu je indikována endoskopická (lépe než jiná) perkutánní céko nebo kolostomie.
7. Postfundoplikační dysfagie
Nejedná se o vlastní onemocnění v pravém smyslu slova, ale o stav či lépe komplikaci po provedení fundoplikace, který často představuje složitý problém. Dysfagii po fundoplikaci udává 10−30 % operovaných, u většiny z nich však dojde ke spontánní úpravě během 6 měsíců. Až u 10 % operovaných jde však o dlouhodobý a nezřídka refrakterní problém. Pokud neřešeno, může se vyvinout až obraz pseudoachalázie se stagnací obsahu v jícnu a jeho následnou dilatací.
Mimo reoperace (např. převedení 360stupňové fundoplikace na 270stupňovou) byla standardním postupem pneumatická dilatace 30−35−40mm balony, byť účinnost tohoto postupu nebyla zásadní [25]. Nedávno byla publikována randomizovaná, placebem („sham“) kontrolovaná studie, ve které byla účinnost dilatace (pouhých 40 %) stejná jako účinnost „sham“ procedury, tj. placebo dilatace [26]. Ač jiné většinou retrospektivní studie ukazovaly určitý benefit pneumatické dilatace, je nezbytné vzít výsledky této prospektivní studie vážně a nejspíše tak již nelze považovat pneumatickou dilataci za vhodné řešení tohoto problému.
Na základě aktuálních údajů je tedy jediným účinným řešením pouze reoperace, což zdůrazňuje nezbytnost důkladného zvážení správnosti indikace fundoplikace u všech pacientů, kteří ji podstupují. Je tedy nezbytné tyto pacienty podrobně vyšetřit (podrobná anamnéza, objektivní vyšetření, endoskopie, rentgen, pH metrie a manometrie jícnu) a je nezbytné vyloučit, mimo jiné, i funkční složku obtíží. Ta se totiž po fundoplikaci spíše zhorší (např. nadýmání aj.). Podrobná anamnéza a objektivní vyšetření jsou tudíž zásadní a bohužel nezřídka se setkáváme s pacienty, u nichž nebyla indikace fundoplikace správná nebo byla přinejmenším sporná. Fundoplikaci lze považovat za nejvhodnější v těchto případech:
- pacient má typické refluxní příznaky (pyróza a regurgitace) +,
- pacient odpoví dobře na podání inhibitorů protonové pumpy +,
- reflux je potvrzen pH metrií.
Sporné jsou indikace u pacientů s atypickými příznaky či s typickými příznaky kombinujícími se s příznaky dyspeptickými (nadýmání aj.), dále při neadekvátní reakci na inhibitory protonové pumpy a tato operace by neměla být prováděna ani u pacientů s negativní pH metrií, zvláště pak bez ezofagitidy. Samozřejmostí je kontraindikace tohoto výkonu u pacientů s primárním motilitním onemocněním jícnu. Výše popsané samozřejmě nevylučuje přísně individuální posouzení každého jednotlivého případu v mezioborovém týmu (gastroenterolog, chirurg).
Určitou naději přinesla pilotní studie, která prokázala krátkodobou účinnost POEM u (pouhých) osmi pacientů trpících postfundoplikační dysfagií [27]. Jedná se tedy o studii předběžnou, jejíž výsledky musejí být potvrzeny dalšími, nejlépe prospektivními a kontrolovanými studiemi. V současnosti nelze POEM v této indikaci považovat za ověřenou metodu, a lze ji tedy provádět jen v rámci studií.
Práce byla finančně podpořena z grantu 17-28797A od grantové agentury Ministerstva zdravotnictví ČR.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
prof. MUDr. Jan Martínek, Ph.D., AGAF
Klinika hepatogastroenterologie IKEM
Vídeňská 1958/9
140 21 Praha 4
e-mail: jan.martinek@ikem.cz
Zdroje
1. Bizzotto A, Iacopini F, Landi R, et al. Zenker‘ s diverticulum: exploring treatment options. Acta Otorhinolaryngol Ital. 2013;33(4):219–29.
2. Weusten BLAM, Barret M, Bredenoord AJ, et al. Endoscopic management of gastrointestinal motility disorders – part 2: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy 2020;52(7):600−614. doi:10.1055/a-1171-3174.
3. Howell RJ, Giliberto JP, Harmon J, et al. Open versus endoscopic surgery of Zenker‘s diverticula: A systematic review and meta-analysis. Dysphagia 2019;34(6):930–938. doi:10.1007/s00455 - 019-09994-9.
4. Ishaq S, Hassan C, Antonello A, et al. Flexible endoscopic treatment for Zenker’s diverticulum: A systematic review and meta-analysis. Gastrointest Endosc. 2016;83 : 1076–89.e5. doi:10.1016/j. gie.2016.01.039.
5. Martínek J, Siroký M, Plottová Z, et al. Treatment of patients with achalasia with botulinum toxin: a multicenter prospective cohort study. Dis Esophagus 2003;16(3):204–209. doi:10.1046/j.1442 - 2050.2003.00329.x.
6. van Hoeij FB, Tack JF, Pandolfino JE, et al. Complications of botulinum toxin injections for treatment of esophageal motility disorders. Dis Esophagus 2017;30(3):1 – 5. doi:10.1111/dote.12491.
7. Weusten BLAM, Barret M, Bredenoord AJ, et al. Endoscopic management of gastrointestinal motility disorders − part 1: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy 2020;52(6):498–515. doi:10.1055/a-1160-5549.
8. Ross SW, Oommen B, Wormer BA, et al. National outcomes of laparoscopic Heller myotomy: operative complications and risk factors for adverse events. Surg Endosc. 2015;29(11):3097–105. doi:10.1007/s00464-014-4054-0.
9. Nabi Z, Reddy DN, Ramchandani M. Adverse events during and after per-oral endoscopic myotomy: prevention, diagnosis, and management. Gastrointest Endosc. 2018;87(1):4–17. doi:10.1016/j. gie.2017.09.029.
10. Werner YB, Hakanson B, Martinek J, Repici A, et al. Endoscopic or surgical myotomy in patients with idiopathic achalasia. N Engl J Med. 2019;381(23):2219–2229. doi:10.1056/NEJMoa1905380.
11. Martinek J, Svecova H, Vackova Z, et al. Per-oral endoscopic myotomy (POEM): mid-term efficacy and safety. Surg Endosc. 2018;32(3):1293–302. doi:10.1007/ s00464-017-5807-3.
12. Yadlapati R, Hungness ES, Pandolfino JE. Complications of antireflux surgery. Am J Gastroenterol. 2018 Aug;113(8):1137 – 1147. doi:10.1038/s41395-018-0115-7.
13. Richter JE, Kumar A, Lipka S, et al. Efficacy of laparoscopic Nissen fundoplication vs transoral incisionless fundoplication or proton pump inhibitors in patients with gastroesophageal reflux disease: A systematic review and network meta-analysis. Gastroenterology 2018;154(5):1298−1308.e7. doi:10.1053/j. gastro.2017.12.021.
14. Aziz AM, El-Khayat HR, Sadek A, et al. A prospective randomized trial of sham, single-dose Stretta, and double-dose Stretta for the treatment of gastroesophageal reflux disease. Surg Endosc. 2010;24(4):818–825. doi:10.1007/s00464 - 009-0671-4.
15. Ye Y, Jiang B, Manne S, et al. Epidemiology and outcomes of gastroparesis, as documented in general practice records, in the United Kingdom. Gut 2021;70(4):644 – 653. doi:10.1136/gutjnl-2020-321277.
16. Friedenberg FK, Palit A, Parkman HP, et al. Botulinum toxin A for the treatment of delayed gastric emptying. Am J Gastroenterol. 2008;103(2):416–423. doi:10.1111/j.1572-0241.2007.01676.x.
17. Arts J, Holvoet L, Caenepeel P, et al. Clinical trial: a randomized-controlled crossover study of intrapyloric injection of botulinum toxin in gastroparesis. Aliment Pharmacol Ther. 2007;26(9):1251–1258. doi:10.1111/j.1365-2036.2007.03467.x.
18. Erhartova D, Vackova Z, Hustak R, et al. Peroral endoscopic myotomy and peroral endoscopic pyloromyotomy as a single procedure for concomitant achalasia and gastroparesis. Endoscopy 2018;50(12):E336−E337. doi:10.1055/a-0658-5691.
19. Vosoughi K, Ichkhanian Y, Benias P, et al. Gastric per-oral endoscopic myotomy (G-POEM) for refractory gastroparesis: results from an international prospective trial. Gut 2022 Jan;71(1):25–33. doi: 10.1136/gutjnl-2020-322756
20. Khashab MA, Stein E, Clarke JO, et al. Gastric peroral endoscopic myotomy for refractory gastroparesis: first human endoscopic pyloromyotomy (with video). Gastrointest Endosc. 2013;78(5):764−768. doi: 10.1016/j.gie.2013.07.019.
21. Husťak R, Vacková Z, Krajciova J, et al. Peroral endoscopic pyloromyotomy (g-poem) for the treatment of gastroparesis − a pilot single-centre study with mid-term follow-up. Rozhl Chir. 2020;99(3):116–23. doi:10.33699/PIS.2020.99.3.116-123.
22. Tsirline VB, Zemlyak AY, Avery MJ, et al. Colonoscopy is superior to neostigmine in the treatment of Ogilvie‘s syndrome. Am J Surg. 2012;204(6):849–855; discussion 855. doi:10.1016/j.amjsurg. 2012.05.006.
23. Peker KD, Cikot M, Bozkurt MA, et al. Colonoscopic decompression should be used before neostigmine in the treatment of Ogilvie‘s syndrome. Eur J Trauma Emerg Surg. 2017;43(4):557−566. doi:10.1007/ s00068-016-0709-y.
24. Sgouros SN, Vlachogiannakos J, Vassiliadis K, et al. Effect of polyethylene glycol electrolyte balanced solution on patients with acute colonic pseudo obstruction after resolution of colonic dilation: a prospective, randomised, placebo controlled trial. Gut 2006;55(5):638−642. doi:10.1136/gut.2005.082099.
25. Hui J. Esophageal pneumatic dilation for postfundoplication dysphagia: safety, efficacy, and predictors of outcome. Am J Gastroenterol. 2002;97(12):2986–991. doi:10.1016/S0002-9270(02)05532-6.
26. Schuitenmaker JM, van Hoeij FB, Schijven MP, et al. Pneumatic dilation for persistent dysphagia after antireflux surgery, a multicentre single-blind randomised sham-controlled clinical trial. Gut 2022 Jan;71(1):10−15. doi: 10.1136/ gutjnl-2020-322355.
27. Gonzalez JM, Monino L, Ah-Soune P, et al. Peroral endoscopic myotomy (POEM) for dysphagia and esophageal motor disorder after antireflux fundoplication. Endoscopy 2020;52(7):583–588. doi:10.1055/a-1147−1348.
Štítky
Chirurgia všeobecná Ortopédia Urgentná medicína
Článok vyšiel v časopiseRozhledy v chirurgii
Najčítanejšie tento týždeň
2022 Číslo 1- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
-
Všetky články tohto čísla
- Endoskopie a chirurgie
- Endoskopická léčba motilitních onemocnění trávicího traktu
- Hledání ztraceného ráje – alternativní místa pro transplantaci izolovaných Langerhansových ostrůvků
- Laparoskopicky asistovaná perkutánna endoskopická cekostomia (LAPEC) v liečbe ťažkej zápchy u dospelých – vlastné skúsenosti
- Anorektální manometrie s vysokým rozlišením u pacientů s anorektální dysfunkcí a terapeutické konsekvence
- Úspěšná opakovaná endoskopická pyloromyotomie (re-G-POEM) v léčbě postchirurgické gastroparézy
- Laparoscopic management of cholecysto-duodenal fistula after spontaneous resolution of intestinal obstruction component of gallstone Ileus − case report and literature review
- Inkarcerovaná levostranná paraduodenální kýla − kazuistika a přehled literatury
- Komentář k původní práci Akutní apendicitida v době jarní pandemie covid-19 v roce 2020 – srovnávací retrospektivní studie
- Rozhledy v chirurgii
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Anorektální manometrie s vysokým rozlišením u pacientů s anorektální dysfunkcí a terapeutické konsekvence
- Endoskopická léčba motilitních onemocnění trávicího traktu
- Inkarcerovaná levostranná paraduodenální kýla − kazuistika a přehled literatury
- Úspěšná opakovaná endoskopická pyloromyotomie (re-G-POEM) v léčbě postchirurgické gastroparézy
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



